Documente Academic
Documente Profesional
Documente Cultură
Laboratorio 8 Organica
Încărcat de
cesarinarragaDescriere originală:
Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Laboratorio 8 Organica
Încărcat de
cesarinarragaDrepturi de autor:
Formate disponibile
NDICE
Pg. 1. OBJETIVOS 2. FUNDAMENTO TERICO 3. DATOS Y RESULTADOS 4 DIAGRAMAS DE FLUJO Diagrama de flujo de la preparacin del dimero de isobutileno 5. MECANISMO DE REACCION 6. OBSERVACIONES 7. CONCLUSIONES 8. ANEXO 9. BIBLIOGRAFA 1 1 3 6
6 7 9 10 11 12
Facultad de Ingeniera Qumica y Textil
QU325
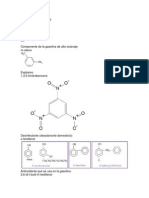
ALQUENOS
1. 2. OBJETIVOS. Entrenar en tcnicas de preparacin, separacin e identificacin de alquenos a nivel de laboratorio. Aprender a realizar la preparacin del dmero isobutileno. Demostrar y reconocer las propiedades qumicas de los alquenos. FUNDAMENTO TERICO. 2.1 Dimerizacion de Alquenos: Es la adicin de alquenos un ejemplo de ello es la dimerizacin del isobutileno que en condiciones apropiadas, el isobutileno es convertido por el cido sulfrico o fosfrico en una mezcla de dos alquenos de frmula molecular C8H16. La hidrogenacin de cualquiera de estos alquenos produce el mismo alcano 2,2,4trimetilpentano .Por tanto, ambos alquenos son ismeros que slo difieren en la posicin del doble enlace. Puesto que los alquenos producidos tienen exactamente el doble de tomos de carbono e hidrgeno que el isobutileno original, se conocen como dmeros del isobutileno, y la reaccin se denomina dimerizacin. Otros alquenos sufren dimerizaciones similares.
2.2 Reacciones de Alquenos: a)Adicin electroflica: La adicin del reactivo cido, HZ, procede en dos pasos:
El paso (1) implica la tranferencia del in hidrgeno de :Z al alqueno para formar un carbocatin: la transferencia de un protn de una base a otra.
-1-
Facultad de Ingeniera Qumica y Textil
QU325
El paso (1) es la etapa difcil y su velocidad controla en gran medida o enteramente la velocidad total de la adicin. Este paso implica un ataque por medio de un reactivo cido buscador de electrones es decir, un reactivo electroflico-, por lo que el proceso se denomina adicin electroflica. El electrfilo, , puede ser, casi cualquier tipo de molcula deficiente en electrones (cidos de Lewis). b) Anlisis de alquenos: El grupo funcional de un alqueno es el doble enlace carbono-carbono. Por consiguiente, para caracterizar un compuesto desconocido como alqueno, debemos demostrar que sufre las reacciones tpicas de ese doble enlace. Se selecciona los mejores ensayos para la caracterizacin de alquenos.
Supongamos que agregamos bromo en tetracloruro de carbono a un compuesto orgnico desconocido y desaparece el color rojo. Qu indica? Slo nos dice que nuestra sustancia desconocida reacciona con el bromo; puede ser un alqueno. Pero no es suficiente saber que un tipo particular de compuestos se combina con un reactivo determinado: tambin debemos conocer las otras clases de sustacnais que tienen el mismo comportamiento. En este caso, nuestra incgnita puede ser un alquino. (Tambin puede ser uno cualquiera de una serie de compuestos que sufren sustitucin por bromo; sin embargo, en tal caso se generara bromuro de hidrgeno, que podra reconocerse por la nube que forma al echar el aliento sobre el tubo de ensayo.) De forma anloga, la decoloracin del permanganato no prueba que un compuesto sea un alqueno, solamente que contiene algn grupo funcional oxidable por el permanganato. El compuesto puede ser un alqueno, pero tambin podra ser un alquino, un aldehdo o cualquier otra sustancia fcilmente oxidable. Incluso puede ser un compuesto contaminado con una impureza oxidable: los alcoholes, por ejemplo, no se oxidan en las condiciones de este ensayo, pero a menudo contienen impurezas que s lo hacen. Generalmente podemos detectar esta posibilidad asegurndonos que se decoloren ms de una o dos gotas de reactivo. De este modo, las pruebas del bromo y del permanganato seran suficientes para diferenciar un alqueno de un alcano, un alqueno de un halogenuro de alquilo o un alqueno de un alcohol.
-2-
Facultad de Ingeniera Qumica y Textil
QU325
c)Adicin de alcanos. Alquilacin: Veamos ahora el mtodo industrial que se emplea actualmente para producir grandes cantidades de 2,2,4-trimetilpentano (isooctano), consumidas en forma de gasolina de alto octanaje. Cuando se hacen reaccionar isobutileno e isobutano en presencia de un catalizador cido, forman directamente 2,2,4-trimetilpentano.
3.
DATOS Y RESULTADOS. 3.1 DATOS REGISTRADOS 3.1.1 Preparacin del dimero de Isobutileno: TABLA N1: Datos registrados SUSTANCIA Agua cido sulfrico concentrado Alcohol Terc-Butilico Dimero obtenido Volumen 20,0ml 20,0ml 19,0ml 7,0 ml
3.1.2 Propiedades qumicas de los alquenos: TABLA N2: Reaccion
Adicion de Acido sulfurico
Reactivo 1
1,0 ml Dimero 1,0 ml Dimero 1,0 ml Br(CCl4) 1,0 ml Br(CCl4)
Reactivo 2
10 gotas H2SO4 10 gotas H2SO4 1,0 ml n-Hexano Cubrir con papel negro 1,0 ml n-Hexano Descubierto 1,0 ml dimero 1,0 ml dimero 5 gotas de KMnO4 al 10 % 5 gotas de Na2CO3 al 10 % Y 5 gotas de KMnO4 al 10 %
Color
Amarillo claro Incoloro Naranja
Bromacion
Naranja claro Incoloro Incoloro, aceitoso Rojizo oscuro marron
Formacion de Halohidrinas
1,0 ml Br(CCl4) 1,5 ml Br(ac) 1,0 ml dimero
Oxidacion 1,0 ml dimero
-3-
Facultad de Ingeniera Qumica y Textil
QU325
3.2
PROPIEDADES FISICOQUIMICAS Y PELIGROSIDAD DE LAS SUSTANCIAS
Peligros y propiedades del cido sulfrico (H2SO4 (conc))
Formula Semidesarrollada: Nombre Sistemtico IUPAC: Aspecto y color: Densidad: Punto de fusin: Punto de Ebullicin: Masa molecular: H2SO4 tetraoxosulfato (VI) de hidrogeno liquido aceitoso incoloro 1800kg/m3 o 1.8g/cm3 283K (10C) 610K (337C) 98.08 g/mol
PELIGROSIDAD Por combustin, formacin de humos txicos de xidos de azufre. La sustancia es un oxidante fuerte y reacciona violentamente con materiales combustibles y reductores. La sustancia es un cido fuerte, reacciona violentamente con bases y es corrosiva para la mayora de metales ms comunes, originando hidrgeno (gas inflamable y explosivo). Reacciona violentamente con agua y compuestos orgnicos con desprendimiento de calor. Al calentar se forman humos (o gases) irritantes y txicos (xido de azufre).
Peligros y propiedades del alcohol Terc-butilico
Nombre Sistemtico Olor: Aspecto y color: Densidad: Punto de fusin: Punto de Ebullicin: Solubilidad: Masa molecular:
2-Metil-2-propanol; ter-butanol resina de madera liquido incoloro 0.78 g/ml a 26C 26C 82C miscible en agua 74,12 g/mol
PELIGROSIDAD: Sus vapores y lquidos inflamables, daino si es ingerido o inhalado afectando el sistema nervioso central. Causa irritacin en piel, ojos y tracto respiratorio.
-4-
Facultad de Ingeniera Qumica y Textil
QU325
Peligros y propiedades del n-hexano
Formula global: Aspecto y color: Olor Punto de fusin: Punto de ebullicin: Solubilidad en agua C6H14 Liquido incoloro suave similar a un hidrocarburo -95.6 o C 69 o C insoluble
Peligros y propiedades del Bromo en agua
Aspecto y color: liquido marrn de olor penetrante Densidad: 1g/cm3 a 20C Punto de Ebullicin: <100C Solubilidad: soluble en cido actico PELIGROSIDAD:
- En la piel: Irrita la piel y las mucosas.. - Ingestin: Puede ser nocivo por ingestin. - Inhalacin: Es extremadamente destructivo para los tejidos de las membranas mucosas y las vas respiratorias superiores.
Peligros y propiedades del Tetracloruro de carbono CCl4
Aspecto y color: Presin de vapor: Punto de fusin: Punto de Ebullicin: Lquido incoloro 12.2 kPa a 20C
-23C 76.5C
0.1 g/ 100 ml a 20C Solubilidad: Masa molecular: 153.8 g/mol PELIGROSIDAD: En contacto con superficies calientes o con llamas esta sustancia se descompone formando humos txicos y corrosivos
-5-
Facultad de Ingeniera Qumica y Textil
QU325
-6-
Facultad de Ingeniera Qumica y Textil
QU325
5.
MECANISMO DE REACCION DIMERIZACIN DE ISOBUTILENO Formacin del carbocatin
Alcohol terc-butilico
Formacin del isobutileno
Formacin del dmero
2,4,4-trimetil-2-penteno (19%)
2,4,4-trimetil-1-penteno (81%)
-7-
Facultad de Ingeniera Qumica y Textil
QU325
PROPIEDADES QUMICAS Adicin de acido sulfrico:
Bromacion:
Con n-Hexano
CCl4
C5H11 C-H + Br2
Formacin de halohidrinas:
C5 H11-C-Br + HBr
-8-
Facultad de Ingeniera Qumica y Textil
QU325
Oxidacin :
6. OBSERVACIONES. 5.1 Preparacin del dimero de Isobutileno: Se realiza un bao de agua helada, debido a que la reaccin de agua con acido sulfrico concentrado es exotrmica, pero debemos mantener la temperatura mayor a 30C, ya que inmediatamente se agregara acohol terc.butilico cuya temperatura de fusin es de 26C. Al calentar se debe realizar con la llama azul y de baja intensidad, ya que no se debe formar vapores en la parte superior del sistema El color de la mezcla al inicio es incoloro, mientras se calienta la mezcla se pone turbia, despus de los 30 minutos notamos que la mezcla es blanquecina, se apaga el mechero. Esperamos que el sistema se enfre y observamos la formacin de dos fases, en la parte inferior esta la fase acuosa acida y en la parte superior la fase orgnica. Usamos la pera de decantacin para obtener la fase orgnica, que es el dimero, se transvasa al erlenmeyer y medimos lo obtenido en una probeta que fue de 7,0 ml. 5.2 Propiedades qumicas de los alquenos: Al anadir las gotas de H2SO4(conc) al tubo con dmero se observo dos fases una de color amarillo claro y otra transparente; pero al agregar H2SO4(conc) al n-hexano se forman dos fases pero ambas transparentes. Para la bromacion, trabajar con cuidado ya que el bromo en agua o en CCl4 es toxico. Tenemos dos tubos cada uno con n-hexano, la diferencia es que esta uno descubierto y el otro cubierto de papel negro, a cada uno se agrega 1ml de bromo en CCl4( color naranja ).
-9-
Facultad de Ingeniera Qumica y Textil
QU325
Se agitando y deja en reposo luego se observa que en el tubo con papel oscuro es color naranja intenso mientras que el descubierto es naranja Al tercer tubo, 1ml de bromo en CCl4, de color amarillento claro cuando se agrega 1ml del dmero, el color desaparece al instante quedando transparente. Para la oxidacin aadir 1ml de dmero y 5 gotas KMnO4 al 10 %(color violeta), desaparece del color violeta y observamos precipitado color rojizo y la solucin transparente. Al aadir al ltimo tubo 1ml de dmero mas 5 gotas de Na2CO3 y calentar suavemente para finalmente agregar 5 gotas de KMnO4 al 10 %(color violeta), se observa la formacin de tres fases, un precipitado marrn oscuro, una fase liquida amarillenta y otra fase liquida transparente. 7. CONCLUSIONES. 7.1 Preparacin del dimero de Isobutileno: Al realizar la hidrogenacin al dimero del isobutileno (C4H8) produce isooctano, que es importante para la determinacin del octanaje de las gasolinas. La dimerizacin de alquenos se realiza por adicin electrofilica como se ve en el mecanismo de reaccin se forma el carbonacin y luego se produce la eliminacin E1, obtenindose dos ismeros por teora sabemos que el de mayor porcentajes es 2,4,4-trimetil-1-penteno.
7.2 Propiedades qumicas de los alquenos:
La bromacion en tetracloruro de carbono, el n-hexano con Br/CCl4 cubierto con papel negro, no se realiza, ya que el halgeno no puede disociarse en ausencia de luz, por ello, la mezcla sigue siendo bsica. Pero el n-hexano con Br/CCl4 descubierto es decir con presencia de luz, se decolora al Br en CCl4 lentamente. La prueba de Baeyer para el dimero fue positiva, ya que se observ la formacin de precipitado oscuro en una solucin incolora, lo que nos indica que el doble enlace se rompi permitiendo la reaccin de oxidacin. La oxidacin con KMnO4, es una forma de detectar la presencia de alquenos en este caso del dmero, pues al adicionar permanganato de potasio la disolucin se decolora formndose un precipitado marrn de MnO2. Si se hubiera probado el n-hexano con KMnO4(prueba de Baeyer) el resultado hubiera sido negativo ya que los alcanos nunca dan positivo la prueba de Baeyer, debido a que no estn conformados por enlaces dobles o triples que se puedan romper. Para formacin de halohidrinas a partir del agua de bromo y el dmero, primero se forma el ion halonio intermediario, luego se realiza el un ataque nucleofilico y tenemos una reaccin competitiva producindose una mezcla de dihalogenuros vecinales y la halohidrina (bromohidrina) se obtiene como producto principal la Halohidrina.
- 10 -
Facultad de Ingeniera Qumica y Textil
QU325
8.
ANEXO. Produccion del Isobutileno
POLIISOBUTILENO El poliisobutileno (en forma de succinimida de poliisobutileno, PIBSI) tiene propiedades interesantes cuando se usa como aditivo en lubricantes y carburantes. El poliisobutileno aadido en pequeas cantidades a los aceites lubricantes usados en labores de mecanizado resulta en una reduccin significativa en la generacin de vapor de aceite y, por lo tanto, reduce la inhalacin por parte del operador de sustancias nocivas. Tambin se utiliza para limpiar el agua en los derrames de petrleo como parte del producto comercial Elastol. Cuando se agrega al petrleo crudo, este aumenta su viscoelasticidad, haciendo que el petrleo permanezca aglomerado cuando es aspirado de la superficie del agua. Como aditivo para el combustible, el poliisobutileno tiene propiedades de detergente. Cuando se agrega al combustible diesel, evita la contaminacin de los inyectores de combustible, dando lugar a la reduccin de emisiones de hidrocarburos y partculas. Mezclado con otros detergentes y aditivos se aade a la gasolina y al combustible diesel para evitar la acumulacin de depsitos en el motor.
- 11 -
Facultad de Ingeniera Qumica y Textil
QU325
Entre otras aplicaciones destaca: En equipos deprtivos Reparacin de techos Mascaras de gas y proteccin de agentes qumicos Goma de mascar El poliisobutileno es utilizado como aglomerante (2.1%) en explosivos plstico, como por ejemplo el C4, El C4 es uno de los explosivos despus del TNT con ms fuerza de los conocidos hasta el momento. El caucho butilo halogenado (bromobutil y clorobutil) son empleados en la industria farmacutica para la elaboracin de tapones para frascos de antibiticos inyectables. Fuente: Consultado 6 de junio de 2012 http://catarina.udlap.mx/u_dl_a/tales/documentos/leip/rojas_t_jl/capitulo4.pdf
9.
BIBLIOGRAFIA. Libro de Consulta L.G.WADE,Jr, Quimica Organica. Segunda edicin.Editorial Prentice-Hall hisnoamericana.Impreso en Mexico.Paginas:311-345. http://organica1.org/qo1/Mo-cap8.htm#_Toc484419730 Consultado el 4 de junio de 2012, Hojas de seguridad de los reactivos http://www.cisproquim.org.co/HOJAS_SEGURIDAD/Acido_sulfurico.p df http://ssfe.itorizaba.edu.mx/webtec/webext/secure/hoja/FAGALAB_COMPLETO/MSDS%20ALCOHOL%20TERBUTILICO%20FA GA-LAB.pdf Consultado el 2 de Junio de 2012 R. KEESE, R. K. MULLER, T. P. TOUBP, 1991, Mtodos de Laboratorio para Qumica Orgnica; Editorial: Addison Wesley Iberoamericano 1ra Edicin; Pginas: 30- 41.
- 12 -
S-ar putea să vă placă și
- Quimica Organica Informe 10Document10 paginiQuimica Organica Informe 10Anne NikolÎncă nu există evaluări
- Manual de Mantenimiento y Reparación de OleoductosDocument117 paginiManual de Mantenimiento y Reparación de OleoductoscesarinarragaÎncă nu există evaluări
- Funciones Quimicas InorganicasDocument8 paginiFunciones Quimicas InorganicasErick BarrientosÎncă nu există evaluări
- Gavión Caja G1-P 10x12 2.4 LDocument1 paginăGavión Caja G1-P 10x12 2.4 LEdwinSanchezVillanuevaÎncă nu există evaluări
- Informe Obtencion e Identificacion de Alquinos Quimica OrganicaDocument10 paginiInforme Obtencion e Identificacion de Alquinos Quimica OrganicaPamela Lissette100% (1)
- 072estrategias Desarrollar Tipos de ResistenciaDocument15 pagini072estrategias Desarrollar Tipos de ResistenciaAldo FloresÎncă nu există evaluări
- Ciclohexanol 3Document5 paginiCiclohexanol 3orale57Încă nu există evaluări
- Guía de Laboratorio 6 Química OrgánicaDocument14 paginiGuía de Laboratorio 6 Química OrgánicaJanice RomeroÎncă nu există evaluări
- Alquinos y Analisis Cualitativo de Elementos OrgánicosDocument13 paginiAlquinos y Analisis Cualitativo de Elementos OrgánicosRicardo Romero0% (1)
- HidrocarburosDocument19 paginiHidrocarburosJefferson Josue Escobedo Flores100% (1)
- OXIDACIÓN DE n-BUTANOL A n-BUTIRALDEHIDODocument12 paginiOXIDACIÓN DE n-BUTANOL A n-BUTIRALDEHIDOKaz MeloÎncă nu există evaluări
- Práctica 1 Química Orgánica 2semestreDocument5 paginiPráctica 1 Química Orgánica 2semestreDiana Katherine0% (1)
- ALQUENOSDocument11 paginiALQUENOSceps10Încă nu există evaluări
- Síntesis Ciclohexanona Grupo ADocument6 paginiSíntesis Ciclohexanona Grupo AmartinÎncă nu există evaluări
- Práctica 6. Identificación de Grupos Funcionales.Document8 paginiPráctica 6. Identificación de Grupos Funcionales.j4malandr0 janoÎncă nu există evaluări
- Practica #4 Hidrocarburos Saturados Alcanos y AlquiloDocument10 paginiPractica #4 Hidrocarburos Saturados Alcanos y AlquiloFranck PhoccoÎncă nu există evaluări
- Práctica 3Document9 paginiPráctica 3Juan Pablo GómezÎncă nu există evaluări
- Reacciones de HidrocarburosDocument11 paginiReacciones de HidrocarburosAnyela Campos TarrilloÎncă nu există evaluări
- Laboratorio 6 - Grupo 1Document19 paginiLaboratorio 6 - Grupo 1MARIANO ENRIQUE VARA ALMANZAÎncă nu există evaluări
- Laboratorio Quimica OrganicaDocument43 paginiLaboratorio Quimica OrganicaRyo Poma100% (1)
- PRACTICA #04hidrocarburos Práctica de Química OrgánicaDocument7 paginiPRACTICA #04hidrocarburos Práctica de Química OrgánicaJIM MAICOL LUDEÑA PAÑAOÎncă nu există evaluări
- Alcoholes 123Document10 paginiAlcoholes 123Joy Way Quispe QuintanaÎncă nu există evaluări
- Pruebas de Caracterización de HidrocarburosDocument12 paginiPruebas de Caracterización de HidrocarburosDiana Mayerly SánchezÎncă nu există evaluări
- Práctica #VIII y IX Reacciones de Sustitución y Eliminación en Haluros de Alquilo y Síntesis de MentonaDocument13 paginiPráctica #VIII y IX Reacciones de Sustitución y Eliminación en Haluros de Alquilo y Síntesis de MentonaIrving JiménezÎncă nu există evaluări
- Obtención de Un Alqueno A Partir de La Deshidratación de Un Alcohol y Reacciones de HidrocarburosDocument11 paginiObtención de Un Alqueno A Partir de La Deshidratación de Un Alcohol y Reacciones de HidrocarburosMichelle Granados JohansenÎncă nu există evaluări
- AlquenosDocument17 paginiAlquenosDiego Velasco CastilloÎncă nu există evaluări
- Informe N°8Document16 paginiInforme N°8FABIAN DIAZ DIAZÎncă nu există evaluări
- OrganicaII-6. Reacciones de Oxidación de AlcoholesDocument6 paginiOrganicaII-6. Reacciones de Oxidación de AlcoholesToño AvilezÎncă nu există evaluări
- Reacciones de HidrocarburosDocument26 paginiReacciones de HidrocarburosAndry BassaÎncă nu există evaluări
- Compuestos Carbonílicos. Haluros de Alquilo.Document17 paginiCompuestos Carbonílicos. Haluros de Alquilo.SARA CHACPI ALFARO100% (1)
- Practica 4 Q-III Reacciones Orgánicas (Eteno)Document11 paginiPractica 4 Q-III Reacciones Orgánicas (Eteno)Jonathan AgueroÎncă nu există evaluări
- PolarimetriaDocument8 paginiPolarimetriaMadelyn Garrido VillarrealÎncă nu există evaluări
- Acido MaleicoDocument15 paginiAcido MaleicoHermes Ricardo Huaman HuamanÎncă nu există evaluări
- Determinación Del Elemento Carbono 1118557525 PDFDocument9 paginiDeterminación Del Elemento Carbono 1118557525 PDFAlexander Araque DiazÎncă nu există evaluări
- Corregido Prueba de Caracterizacion de HidrocarburosDocument7 paginiCorregido Prueba de Caracterizacion de HidrocarburosAnonymous nLd7l02Y50% (2)
- Practica 2 Quimica Organica I REACTIVIDAD Y CARACTERIZACIÓN DE HIDROCARBUROSDocument5 paginiPractica 2 Quimica Organica I REACTIVIDAD Y CARACTERIZACIÓN DE HIDROCARBUROSJeison ArguelloÎncă nu există evaluări
- Propiedades Quimicas de Los AlcoholesDocument13 paginiPropiedades Quimicas de Los AlcoholesDaniela LibrerosÎncă nu există evaluări
- Practica 6Document12 paginiPractica 6Luis Charbel Guzman AguilarÎncă nu există evaluări
- Obtención Del Butiraldehido Por Oxidación Del ButanolDocument15 paginiObtención Del Butiraldehido Por Oxidación Del ButanolFrancisca Poblano MÎncă nu există evaluări
- Informe Quimica Organica 8Document4 paginiInforme Quimica Organica 8Sheyla EspinozaÎncă nu există evaluări
- Ismael Garza - Trabajo Integrador Etapa 4 PDFDocument7 paginiIsmael Garza - Trabajo Integrador Etapa 4 PDFAbraham Samael Lopez MedellinÎncă nu există evaluări
- Ácido Fenoxiacético PrevioDocument12 paginiÁcido Fenoxiacético PrevioAlejandra Mendoza100% (1)
- Informe 9 y 10 Quimica OrganicaDocument16 paginiInforme 9 y 10 Quimica OrganicajotaÎncă nu există evaluări
- Informe Semana 7Document8 paginiInforme Semana 7Karla HuamancajaÎncă nu există evaluări
- Informe de Quimica N°1 PRUEBA DE LLAMADocument9 paginiInforme de Quimica N°1 PRUEBA DE LLAMArosmery.valverde17Încă nu există evaluări
- Lab Organica 8Document15 paginiLab Organica 8Jorge Chávez BarbozaÎncă nu există evaluări
- Práctica 5 - Los Hidrocarburos (Autoguardado)Document12 paginiPráctica 5 - Los Hidrocarburos (Autoguardado)Yude Katia Paucarhuanca Yarihuaman100% (2)
- Cuaderno de Prã-Ctica Qu - 241Document18 paginiCuaderno de Prã-Ctica Qu - 241CN Kenyu AlexÎncă nu există evaluări
- Documento Sin TítuloDocument8 paginiDocumento Sin TítuloCristian PatiñoÎncă nu există evaluări
- Informe de Laboratoria de Química Orgánica GeneralDocument8 paginiInforme de Laboratoria de Química Orgánica Generaling. BRANDON ALBAN BERNALÎncă nu există evaluări
- Laboratorio BencidrolDocument15 paginiLaboratorio BencidrolCarlos Mario Torres ArboledaÎncă nu există evaluări
- Reporte de Práctica 2 Química Orgánica 2Document7 paginiReporte de Práctica 2 Química Orgánica 2Miriam Yaneth Aangeles QuiiterioÎncă nu există evaluări
- TEMA 3 Parte III 2016 PDFDocument30 paginiTEMA 3 Parte III 2016 PDFLeandro PelletànÎncă nu există evaluări
- 2 Informe S2 - G3Document17 pagini2 Informe S2 - G3Ruth Benavidez CarbajalÎncă nu există evaluări
- Practica 3 1Document5 paginiPractica 3 1Diego PaúlÎncă nu există evaluări
- Reacciones Decaracterizacion de Alcanos 7Document7 paginiReacciones Decaracterizacion de Alcanos 7MARIBEL SOLEDAD ALVAREZ CABANAÎncă nu există evaluări
- Práctica #3-Reacciones de Aldehidos, Cetonas y CarbohidratosDocument5 paginiPráctica #3-Reacciones de Aldehidos, Cetonas y CarbohidratosChris HaldenÎncă nu există evaluări
- Sintesis de Un EterDocument6 paginiSintesis de Un EterCami ChavezÎncă nu există evaluări
- INFORME-HIDROCARBUROS-N2Document15 paginiINFORME-HIDROCARBUROS-N2AbelÎncă nu există evaluări
- Informe 14 QuimicaDocument5 paginiInforme 14 QuimicaZHANELA ROSALINDA ALONSO TORIBIO0% (1)
- Seminario Practica 8Document23 paginiSeminario Practica 8Denisse MotaÎncă nu există evaluări
- Informe de Alquinos PDFDocument7 paginiInforme de Alquinos PDFJunnior Alejandro AcostaÎncă nu există evaluări
- Propiedades de Los Alcoholes - InformeDocument11 paginiPropiedades de Los Alcoholes - InformeJavier Alfonso Perez NavarroÎncă nu există evaluări
- Control de Maquinas y Procesos IndustrialesDocument12 paginiControl de Maquinas y Procesos IndustrialescesarinarragaÎncă nu există evaluări
- Poder CalorificoDocument8 paginiPoder CalorificocesarinarragaÎncă nu există evaluări
- Simulación de ProcesosDocument21 paginiSimulación de ProcesoscesarinarragaÎncă nu există evaluări
- FORO - Petroquímica en El PerúDocument124 paginiFORO - Petroquímica en El PerúcesarinarragaÎncă nu există evaluări
- 054 - Balance de Materia en Columnas de Destilación de CrudoDocument10 pagini054 - Balance de Materia en Columnas de Destilación de CrudocesarinarragaÎncă nu există evaluări
- Electrónica de PotenciaDocument88 paginiElectrónica de Potenciacesarinarraga100% (1)
- Clase SoldaduraDocument30 paginiClase SoldaduracesarinarragaÎncă nu există evaluări
- Teoria de Reemplazo de EquiposDocument11 paginiTeoria de Reemplazo de EquiposcesarinarragaÎncă nu există evaluări
- Pepe SilicónDocument3 paginiPepe SilicónRodolfo HuitronÎncă nu există evaluări
- Celdas Electroquimicas DefinitivaDocument4 paginiCeldas Electroquimicas DefinitivaANDERSON RUBIO CLEVESÎncă nu există evaluări
- Formato en El ExelDocument4 paginiFormato en El Exelcarlos canoÎncă nu există evaluări
- Cromatografía de Capa FinaDocument17 paginiCromatografía de Capa FinaMartin Osvaldo Castillo RamosÎncă nu există evaluări
- Laboratorio Fisica IIDocument6 paginiLaboratorio Fisica IIjonathan AmadoÎncă nu există evaluări
- OtroDocument1 paginăOtroDaniela LópezÎncă nu există evaluări
- Bacilos GramnegativosDocument20 paginiBacilos GramnegativosAbii De OsorioÎncă nu există evaluări
- Guía Completo Sobre La Identificación de Los Plásticos y Sus Principales Usos ComercialesDocument4 paginiGuía Completo Sobre La Identificación de Los Plásticos y Sus Principales Usos ComercialesLusmila FloresÎncă nu există evaluări
- Captura 2023-01-15 A Las 21.24.44Document36 paginiCaptura 2023-01-15 A Las 21.24.44Cristina RodrigueGutierrezÎncă nu există evaluări
- Neumatica Final 1 DiapDocument59 paginiNeumatica Final 1 DiapWinfried Kelvin LHuarsayaÎncă nu există evaluări
- Casos de Estudio1Document2 paginiCasos de Estudio1jsaulorbegoso5772Încă nu există evaluări
- 1.mega Pack de Planchas de ConfoDocument137 pagini1.mega Pack de Planchas de ConfoMauricio Chuls LandcasterÎncă nu există evaluări
- Preguntas Cursos ITPEDocument26 paginiPreguntas Cursos ITPECarlosÎncă nu există evaluări
- Bolas Contra Las PolillasDocument7 paginiBolas Contra Las PolillasvictormmcÎncă nu există evaluări
- 4.5 Plan de Seguridad y Prevencion de SiniestrosDocument15 pagini4.5 Plan de Seguridad y Prevencion de SiniestrosRennéMamanniÎncă nu există evaluări
- Hornos para Obtención de AceroDocument53 paginiHornos para Obtención de AceroAIUA92Încă nu există evaluări
- Impercomex Reforzado 5Document4 paginiImpercomex Reforzado 5Jesus Sail Gutierrez MÎncă nu există evaluări
- Glucólisis y Gluconeogénesis 2a ZenodoDocument2 paginiGlucólisis y Gluconeogénesis 2a ZenodoTareas ExpressÎncă nu există evaluări
- CARBOHIDRATOSDocument1 paginăCARBOHIDRATOSalex moraÎncă nu există evaluări
- Proceso de RefinaciónDocument5 paginiProceso de RefinaciónGilberto GuerraÎncă nu există evaluări
- Capítulo VII. Mecánica de FluidosDocument18 paginiCapítulo VII. Mecánica de FluidosDoloritasÎncă nu există evaluări
- Programa 005 BLOQUEO Y ETIQUETADODocument38 paginiPrograma 005 BLOQUEO Y ETIQUETADOVeronica Rojas PlazasÎncă nu există evaluări
- Actividad Big Bang1Document5 paginiActividad Big Bang1Andrea Paola Chaparro100% (1)
- IntroduccionDocument12 paginiIntroduccionMariana LacoaÎncă nu există evaluări
- Sociedad Minera El BrocalDocument5 paginiSociedad Minera El BrocalKevin EduardoÎncă nu există evaluări
- Solucionario Ensayo 8° J.E.G. - Química 2021Document47 paginiSolucionario Ensayo 8° J.E.G. - Química 2021ximenaÎncă nu există evaluări