Documente Academic
Documente Profesional
Documente Cultură
Bio Chim
Încărcat de
Eu VictorDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Bio Chim
Încărcat de
Eu VictorDrepturi de autor:
Formate disponibile
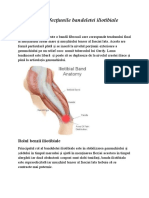
Organizarea structurala a muschiului striat Musculatura scheletica striata sau somatica reprezinta componenta activa a aparatului locomotor; asigura
a tonusul muscular, postura, ehcilibru, mimica, vorbirea si toate miscarile voluntare precise fine si involuntare automate. muschiul striat este constituit din fibre musculare lungi de 1-4 mm; cu diametrul de 10100 micrometri. miocitul (fibra musculara) est o celula polinucleata cu miofibrile (alcatuite din filamente groase si subtiri) asamblate in formatiuni fine (formatiunile lui Leydig) si separate prin sarcoplasma. membrana celulara sau sarcolema prezinta din loc in loc vezicule si alveole cu rol in fenomenele de transport plasmatic. dintre organitele celulare, mitocondriile (sarcozomii Retzius, 1890) variaza ca numar si dispunere spatiala in functie de tipul de muschi (in muschii activi, mitocondriile sunt numeroase si dispuse de-a lungul miofibrilelor, iar in cazul celor mai putini activi, sunt rare si disribuite neregulat).
Mitocondria = sediul metabolismului energetic fibra musculara se asociaza cu un sistem de membrane interne alcatuit din doua formatiuni fundamentale: reticulul sarcoplasmatic si sistemul transversal T. reticulul sarcoplasmatic corespunde reticulului endoplasmatic din celelalte celule, iar sistemul transversal deriva din sarcolema si prezinta tubuli orientati longitudinal sau transversal in profunzimea fibrelor. legatura dintre reticul si sistemul T se realizeaza prin triade si diade. Formatiunile sunt alcatuite din element sarcolemic (tubul) si comunica cu sacii sau cisternele reticulului sarcoplasmatic. sistemul T este responsabil de formarea veziculelor ce alcatuiesc factorul de relaxare prin a carui inhibitie activeaa contractia. unda de depolarizare este raspandita prin intermediul triadelor transversale. Depolarizarea elementului central al triadei pune in libertate ionii de calciu care vor activa miozin-ATPaza, enzima implicata in scindarea energetica a ATP-ului. o miofibrila prezinta o succesiune de benzi sau discuri clare si benzi sau discuri intunecate. zonele A intunecate (anizotrope) prezinta in partea centrala o banda transversala H care la randul sau este strabatut de o linie fina transversala, membrana sau discul M. zonele I luminoase (izotrope) sunt divizate de un sept transversal membrana sau discul Z. Fiecare jumatate a benzii I este subimpartita in doua, de discul N. unitatea morfo-functionala a muschiului este sarcomerul si se intinde intre doua discuri Z consecutive pe o lungime de aproximativ 2 . Fiecare miofibrila prezinta in structura sute de sarcomeri. Un sarcomer cuprinde urmatoarele structuri consecutive:
o semibanda I subdivizata in doua parti prin discul auxiliar N o banda A cu zonele H impartite in doua prin membrana M o a doua semibanda I in discurile sau benzile intunecate se gasesc filamente groase de miozina si zone mici ale filamentelor subtiri de actina. in discurile sau benzile clare se gasesc numai filamente subtiri de actina In repaus, filamentele de actina patrund doar putin intre filamentele de miozina. In contractie, filamentele de actina culiseaza rintre filamentele de miozina, membranele z se aproprie iar muschiul se scurteaza. Un sarcomer are in conditii normale lungimea de aproximativ 2 microni. La lungimi mai mari sarcomerul depaseste lungimea de 2 microni si in contractie nu se mai poate realiza alunecarea lor. Daca sarcomerul este mai mic de 2 microni membranele z ar atinge extremitatile filamentelor miozina, iar contractia nu se mai realizeaza. Filamentul de miozina este alcatuit din aproximativ 200 molecule de proteina contractila, grupate in 6 lanturi de miozina: o 2 lanturi de miozina grea (MH), rasucite in spirala ce alcatuiesc coada; o 4 lanturi de miozina usoara, formeaza capul miozinei (ML). Miozina usoara actioneaza ca o enzima ce scindeaza ATP-ul in adenozin difosforic (ADP), fosfat macroergic si energie. Filamentul de actina este alcatuit din 3 componente proteic: actina, tropomiozina si troponina. Filamentul de actina prezinta un ax central reprezentat de actina fibrilara si globulara (F si G) Pe axul central al actinei se gasesc niste zone numite situsuri. Acestea in repaus sunt inhibate fiind acoperite de catre troponina si tropomiozina impiedicand atractia dintre actina si miozina care ar declansa contractia. Filamentele de actina sunt ferm inserate in benzile Z, iar capetele lor libere patrund in ambele sensuri printre filamente de miozina ale sarcomerelor adiacente. Asocierea fenomenelor chimice cu cele mecanice in contractia musculara se explica prin doua teorii fundamentale: teoria modificarilor conformationale si teoria alunecarii. Prima teorie se bazeaza pe modelul lui Morales, conform caruia proteinele contractile sar comporta ca resorturi cu grade variate de contractie si relaxare. Dupa Astbury, contractia musculara este posibila datorita transformarii structurilor foaie pliata in -helix si invers. (fenomen descoperit la flagelul mobil al bacteriilor si, experiment in vitro prin tratarea actomiozinei cu agenti fizici si chimici). Transformarea conformationala nu a fost decelata la organismul uman, iar absenta modificarii din timpul contractiei musculare constituie un argument ferm in sustinerea teoriei alunecarii.
Glisarea (alunecare) filamentelor de actina de-a lungul celor de miozina explica, conform teoriei alunecarii sau glisarii a lui Hanson-Huxley, scurtarea muschiului in contractie. Teoria nu este unanim recunoscuta, dar reprezinta singurul argument admis pana in prezent. Prin alunecare, discurile Z se apropie scurtand lungimea sarcomerului cu 2/3 din lungimea pe care o are in stare de relaxare. Viteza de scurtare a unui muschi antreneaza 30-100 de punti actina-miozina/secunda. O punte eliberata din miozina se fixeaza pe situsul activ al actinei, apoi se retrage deplasand filamentul de actina spre centrul sarcomerului. Miscare devine repetitiva la nivelul situsurilor urmatoare. Aceasta forma de deplasare se numeste mecanism cu clichet si poate fi descris in sase timpi: 1. impulsul nervos determina schimbarea poterntialului de actiune la nivelul sarcolemei; depolarizarea este transmisa prin sistemul T in membranele reticulului endoplasmatic a caror permeabilitate se modifica; 2. ionii de calciu eliberati din reticul in sarcoplasma miofibrilelor declanseaza interactiunea dintre ATP si filamentele groase si subtiri; 3. ionii de calciu interactioneaza cu sistemul de proteine reglatoare, legandu-se de troponina si schimband conformatia tropomiozinei si a complexului troponinic; 4. modificarile de structura deblocheaza interactiunea miozina-actina, provocand fixarea capului de miozina de actina; 5. actina stimuleaza activitatea miozin-ATP-aza cu hidrolizarea unei molecule de ATP; in acelasi timp, are loc modificarea conformationala a capului de miozina; 6. schimbarea spatiala a structurii provoaca deplasarea puntii, conditionand desfasurarea mecanismului cu clihet ce va deplasa actina.
Remodelarea morfo-functionala a muschiului Se produc modificari ale diametrului, lungimii si fortei, ale retelei vasculare si, intr-o masura mai mica a tipului de fibre structurale. Procesul se desfasoara rapid si poate dura cateva saptamani. Experimental s-a demonstrat o resinteza a proteinelor contractile la fiecare doua saptamani. Cresterea masei totale a unui muschi (hipertrofie) sau scaderea acesteia (atrofie musculara) fac parte din procesul remodelarii in mod frecvent. Orice hipertrofie musculara reprezinta cresterea masei individuale a fiecarei fibra (hipertrofia fibrei). Acesta se produce ca raspuns la o contractie musculara cu forta maximala sau submaximala.
Hipertrofia se produce intr-un grad si mai avansat, daca simultan contractiei, muschiul este intins (tensionat). Mecanismul prin care se ajunge la hipertrofie musculara nu este cunoscut. In timpul producerii hipertrofiei, ritmul sintezei proteinelor contractile este mult mai mare decat ritmul degradarii lor, ceea ce duce la o crestere a numarului de filamente de miozina si actina din miofibrile (miofibrilele fiecarei fibre se divid pentru a forma noi miofibrile). Hipertrofia muschiului poate fi consecinta cresterii numarului de miofibrile (hipertrofie miofibrilara) sau a maririi ansei (masei) sarcoplasmatice (hipetrofie sarcoplasmatica). In paralel cu multiplicarea numarului de miofibrile, are loc o crestere a tuturor sistemelor enzimatice energoformatoare (in special, cele glicolitice anaerobe care furnizeaza energia necesara contractiilor musculare maximale si de scurta durata). Incetarea ativitatii unui muschi pentru o perioada lunga de timp scade ritmul anabolismului proteic si a numarului de miofibrile cu o viteza mai mare decat refacerea acestora, instaland atrofia musculara. Un muschi lipsit de inervatie nu mai receptioneaza semnalele contractile necesare mentinerii dimensiunilor sale normale. In acest caz, aproape imediate se instaleaza atrofia musculara, iar la 2 luni apar procesele degenerative. Reinervarea muschiului in primele 3 luni duce la revenirea functionala aproape completa. Depasirea acestui termen, scade sansa recuperarii, cu pierderea completa in 1-2 ani. In stadiul final al atrofiei, majoritatea fibrelor musculare sunt complet distruse si inlocuite cu tesut fibros si adipos. Distrofiile musculare progresive sunt considerate afectiuni genetice, a caror bazza moleculara ramane o necunoscuta. Aspectele dismetabolice (in cazul, distrofiei maligne Duchenne) cu transmisie X recesiva nu pot sistematiza, intr-o conceptie patogena, fenomenul molecular. Atrofia musculara difuza se coreleaza cu trecerea in sange a unor enzime sarcoplasmatice (fructoza-1.6-difosfat-aldolaza, lactat-dehidrogenaza, fosfocreatinkinaza). Se presupune ca are loc decompensarea energogenezei celulare si utilizarea ineficienta a gruparilor fosfat macroergice pentru mentinerea mecanismelor endergonice de control asupra permeabilitatii selective a sarcolemei.
Endorgonic intra, exorgonic iese In stadii mai avansate, glicoliza scade cu 25%, iar creatina trece, in cantitate mare, in urina. Acest fenomen este consecinta dezechilibrului metabolismului muscular. Miotonia (rar intalnita) se caracterizeaza rin rigiditate musculara cu instalarea lenta a relaxarii, dupa o contractie voluntara. Tulburarea fundamentala consta in alterarea capacitatii sarcolemei de a intrerupe eficient influxul ionilor de sodiu, in timpul procesului de excitatie.
Prin miastenie, musculatura scheletica are tendinta de a obosi pana la epuizare. Cauzele acestui fenomen sunt discutabile: o scade eliberarea de acetilcolina la nivelul terminatiei nervoase fie prin deficit al etapelor sintezei, fie prin inhibarea acestui proces; o accelerarea descompunerii acetilcolinei prin stimularea activitatii colinesterazei; o scaderea sensibilitatii placii terminale fata de acetilcolina (efect de tipul celui produs de curara). Paralizia paroxistica hipokalemica (=concentratie mica de potasiu) (afectiune genetica rara) se caracterizeaza prin stari de paralizie flasca, cu predispozitie la nivelul musculaturii extremitatilor. Forme de miopatii innascute sau dobandite:
Miopatia Sindromul Mc Ardle Miopatii cu depozitare de lipide
Caracteristici lipsa fosforilazei (extrem de rara) nivel cu 20% mai scazut de carnitina (tulburarea biosintezei sau inhibarea preluarii la nivel muscular) Miopatii secundare glicogenozelor tip II, III, tulburari in metabolismul glicogenului VII, VIII Miopatia Larsen secventa hipoglicolitica Boala Addison schimbarea compozitiei minerale la nivelul sanguin induce modificari ale metabolismului muscular (scad ionii de Na si Cl, cresc cei de K) Acidoza diabetica carenta de K cu fenomene de insuficienta musculara Metabolismul = totalitatea transformarilor de materie (substanta), de energie si informatie care au loc in organism dar si intre organism si mediul inconjurator. Prin anabolism includem toate reactiile de sinteza, de constructie care se desfasoara cu consum de energie. Prin catabolism se intelege totalitatea ractiilor de degradare, de descompunere care au loc cu eliberare de energie. Metabolism intermediar Metabolism energetic Exista 2 metode de investigare: - metoda calorimetriei (directa indirecta (=foloseste coeficientul respirator)) Glucoza: C6H12O6 + 6O2 => dioxid de carbon (6CO2) + apa (6H2O) Coeficientul respirator pentru glucide este 1. Lipide mai putin, proteine si mai putin.
GLUCIDE Glucide zaharuri, nitrati, etc. Formula empirica: C:H:O=1:2:1 Glucidele sau zaharurile sunt compusi polihidroxicarbonilici si derivati ai acestora. Numele de hidrati de carbon, care se mai In organism, glucidele indeplinesc urmatoarele functii: surse imediate de refacere a ATP-ului (glucoza) substante de rezerva energetica (amidonul, glicogenul hepatic si muscular) substante structurale si de sustinere (polizaharidele matricei osoase) substante cu functii specifice (mucopolizaharidele structurilor unor factori imunitari)
Zaharurile se clasifica, dupa natura produsilor rezultati, in urma reactiei hidrolitice. Conform acestui criteriu, hidratii de carbon pot fi: oze si ozide. Ozele (sau monozaharidele) contin o singura unitate polihidroxicarbonilica, fiind nehidrolizabile. Monozaharidele reprezinta unitatea structurala de baza a glucidelor. Monozaharidelor se clasifica dupa numarul atomilor de carbon. 3-trioze, 4-tetroze, 5-pentoze, 6hexoze, 7-heptoze, 8-octoze. Cele mai importante si abundente sunt hexozele (glucoza, fructoza si galactoza) si pentozele (riboza). Glucoza reprezinta sursa majora de refacere a ATP-ului, ceea ce ii confera indispensabilitate vietii. In regnul vegetal, se sintetizeaza prin fotosinteza: h 6CO2+6H2O C6H12O6+6O2 pigmenti clorofilieni glucoza Sub forma libera, se gaseste in fructe si in nectarul florilor. Sta la baza formarii a numeroase oligozaharide (zaharoza, maltoza, lactoza) si polizaharide (amidon, celuloza, glicogen). In organismul animal, glucoza se gaseste libera in tesuturi si organe. In sange, concentratia fiziologica variaza intre 80-120mg%. Fructoza sau levuloza este localizata, sub forma libera, in fructe si miere. Se polimerizeaza formand zaharoza si derivati esterici ai acidului fosforic; participa, ca substrat energetic, indirect, in catabolismul glucidic. Ozidele contin un anumit numar de unitati monozaharidice. Astfel: cele cu 2-10 unitati se numesc oligozide sau oligozaharide (zaharoza, maltoza, lactoza) cele cu peste 10 unitati, poliozide sau polizaharide (amidon, celuloza, glicogen). Legaturile chimice stabilite intre unitatile constitutive, sunt de tip covalent glicozidic.
Zaharoza = glucoza + fructoza Maltoza = 2*glucoza Lactoza = galactoza+glucoza Polizaharidele sau glicanii sunt constituite din lanturi liniare sua ramificate de monozaharide, ce pot fi, de asemenea, eliberate prin hidroliza. Polizaharidele, celuloza este constituita din glucoza numai in regnul vegetal, organismul uman nu o poate digera. Amidonul format numai din glucoza, se gaseste in regnul vegetal si poate fi degradat in tubul digestiv. Glicogenul format numai din glucoza, se gaseste numai in regnul animal. Omogen amidonului. Inulina este constituit numai din fructoza. Are valoare de diagnostic. Dextrana numai din glucoza si cateodata inlocuieste plasma Glicemia Ca valoare in sange 80-110 mg/100ml sange. Valorile au fost urcate pana la 120 ca o valoare nonpatologica in conditiile in care este criteriul varstei. +40 ani sunt probleme, -40 ani si 120 este considerata o valoare normala. Hipoglicemie = coma; hiperglicemie Glicemia este controlata prin factori endocrini (hormonii panreasului) si prin factorii metabolici (reactati (ce intra in reactie se gaseste in partea stanga a sagetii/egalului) si produsi de reactie (se gaseste in partea dreapta ceea ce rezulta din reactie)). Daca valoarea glicemiei este peste normal se mareste procesul de anabolizare. Hiperglicemie Hipoglicemie glicogenoliza Trecerea glucozei in urina poate sa instaleze o stare care se numeste glucozurie. La hiperglicemie glucoza trece in sange deoarece rinichiul este adaptat pentru reabsorbtia totala a glucozei. Starea de start 160 mg determinata de declasarea adrenalinei. Nu se administreaza cu mai putin de 4 ore inainte de efort glucoza. Se recomanda administrarea de fructoza, galactoza, riboza, etc. deoarece sunt preluate de metabolismul celular si transformate in glucoza. ENZIMELE SUNT PROTEINE! Lipidele
sunt substante naturale, constituiente ale organismelor vii, plante sau animale, insolubile in apa dar solubile in solventi organici: cloroform, benzen principalele functii biologice ale lipidelor sunt urmatoarele: o componente structurale ale membranelor celulare si subcelulare; o forme de depozit ale energiei (1g de lipide elibereaza 9.3 kcal); o combustiili metabolici, avand rolul de sursa imeiata de energie; o componente protective termic, electric ale peretelui celular pentru anumite celule animale, vegetale sau microorganisme; o substante biologic active (unele vitamie sau hormoni) au rol functional deosebit. se gasesc raspandite, atat in regnul vegetal, ca substante de rezerva (samburi, seminte, fructe oleaginoase), cat si in cel animal, unde detin rol plastic si energetic. Clasificare alipidelor se poate face dupa: o gradul de hidrolizare lipide saponifiabile (solubile) si nesaponifiabile (insolubile); o componenta la nivel celular
Tipuri de lipide Acilglicerlii sau gliceridele sunt cele mai abundente lipide naturale; componente principale ale grasimilor de rezerva, din tesuturi. Proprietatile lor depinde de natura si cantitatea acizilor grasi constituienti. Sunt insolubili in apa si greu solubili in solventi organici. Gliceridele realizeaza cu apa, dispersii coloidale sau emulsii, stabilizabile sub actiunea substantelor tensioactive. Reactiile formative constau in esterificarea glicerolului cu acizii grasi. Dupa numarul gruparilor esterificate, aciglicerolii pot fi mono-, di- si triacilgliceroli. Grasimile de rezerva din adipocite sunt alcatuite aproape exclusiv din trigliceride cuprinde urmatorii acizi grasi: acid oleic (45%), acid linoleic (8%), acid palmitoleic (7%), acid stearic (7%), alti acizi (8%). Trigliceridele au densitati mai mici decat apa (0.96g/cm), caracter hidrofob foarte pronuntat si nu se dizolva in apa. In prezenta luminii, a aerului sau a factorilor generatori de radicali liberi, grasimile nesaturate sufera un proces peroxidare (autooxidare) care le altereaza gustul si mirosul (rancezire). Acizii grasi liberi (AGL) reprezinta elementul structural comun tuturor grasimilor, asigurand pana la 40% din necesarul energetic al unui adult, cu o alimentatie normala si completa. Muschiul cardiac foloseste cea mai mare cantitate de energie, obtinuta prin degradarea oxidativa a AGL. Animalele care hiberneaza sau pasarile migratoare, au ca sursa unica de energie tot acizii grasi liberi. Au fost izolate cateva zeci de tipuri de acizi grasi cu structuri si formule chimice variate, dar care prezinta urmatoarele caracteristici comune:
o minimum 8 atomi de carbon o intotdeauna un numar par de atomi de carbon o contin o grupare carboxil (-COOH) terminala. Eliberarea, transportul si metabolizarea acizilor grasi necesita control hormonal, nutritional si nervos In plasma, acizii grasi sunt legati de serumalbumina, proteina capabila sa fixeze 7 molecule de acid gras in situsuri diferite. Valorile fiziologice serice ale AGL pentru adulti sunt cuprinse intre 0.35-1.2 mEq/l. Depasirea limitelor superioare intensifica cetogeneza si secundar, determina hipercetonemie si cetonurie. Acizii grasi liberi sunt descarcati in plasma majoritar din tesutul adipos, depinzand de echilibrul dintre lipoliza si lipogeneza. AGL sunt utilizati in scop energogen de catre variate tesuturi si celule, cu exceptia creierului si hematiilor. Cresterea nivelului plasmatic a AGL depaseste capacitatea de metabolizare a tesuturilor extrahepatice, astfel incat ficatul va prelua o mare parte din acizi si ii va converti in trigliceride. Eforturile de anduranta (probleme de fond si mare fond din atletism, patinaj fond, schi fond, ciclism de sosea) intensifica activitatea sistemelor enzimatice implicate in degradarile aerobe energoformatoare. In acest context, acizii grasi liberi (AGL) sunt mobilizati in cantitate mai mare, depasinnd posibilitatile de utilizare ale organelor. S-a constatat ca l-carnitina favorizeaza mobilizarea AGL in timpul efortului aerob, facilitand intrarea acestora in mitocondrie si initierea -oxidarii, cu obtinerea de energie Celulele musculare utilizeaza in timpul eforturilor de rezistenta mai mult energia provenita prin degradarea aeroba a AGL, realizand o economie de glucide, indispensabila mentinerii functiilor cerebrale. Cercetari recente au evidentiat la sportivii bine antrenati, comparativ cu cei neantrenati, usoare cresteri ale concentratiei de AGL, in fara de revenire. Aceasta demonstreaza existenta unei stari metabolice bune, cu rezerve energetice mai mari. Colesterolul este component esential al structurilor membranare, alb, solid, insolubil in apa; are caracter hidrofob pronuntat si este precursorul tuturor compusilor steroidici (printre care si vitamina D3) In organism, se gaseste sub forma libera (alcool) sau esterificata (in combinatie cu acizii grasi: acil-colesterol). Colesterolul indeplineste urmatoarele functii: o element structural al membranelor celulare si al lipoproteinelor plasmatice, sub forma libera sau esterificata; regleaza fluiditatea membranelor o substanta alba a structurilor nervoase cuprinde cantitati mari de colesterol liber )mai ales, in perioada de mielinizare, dupa care ramane constant pe tot restul vietii) o precursor al hormonilor steroidici-corticosuprarenali, sexuali si al acizilor biliari o constituent al calciferolului (vitamina D3)
Prezenta colesterolului in sange impune limite cantitative care vor scadea riscul accidentelor vasculare cerebrale si al infarctului miocardic. Astfel: o nivelul sanguin de colesterol adecvat 200 mg/dl o nivelul sanguin de colesterol la limita intre 200 si 239 mg/dl o nivelul sanguin de colesterol crescut peste 239 mg/dl Lipoproteinele cu densitate foarte mica (VLDL) sunt sintetizate in ficat si contin intre 8994% lipide si anume: trigliceride (55-6%), fosfolipide (12-18%), esteri ai colesterolului (12-14%), clesterol liber (6-8%). VLDL asigura transportul trigliceridelor sintetizate in ficat catre tesuturile extrahepatice. Ingerarea unor ratii bogate in glucide va duce la conversia acestora in trigliceride, transportate numai sub forma de VLDL. Sangele unui subiect sanatos recoltat dupa un post de 8-16 ore este lipsit de VLDL. Lipoproteinele cu densitate mica (LDL). Valori optime: o optim <100 mg/dl o aproape optim la valori cuprinse intre 100-129 mg/dl o la limita pentru valori intre 130-159 mg/dl o ridicat pentru valori cuprinse intre 160-189 mg/dl o foarte ridicat la valori >180 mg/dl Asocierea nivelului sanguin ridicat al LDL cu fractiunea trigliceridica (TG) favorizeaza aparitia unui IMA. De aceea, pentru trigliceride sanguine se considera: o nivel optim (la limita) valori de 150-199 mg/dl o nivel ridicat intre 200-500 mg/dl o nivel foarte ridicat (de risc) peste 500 mg/dl
Enzimele Sunt proteine cu rol catalitic a caror clasificare este extrem de complicata datorita structurii. Majoritatea lor se denumesc cu sufixul -aza. Prezinta: specificitate pentru substrat, tip de reactie, tip de legatura sau grupare functionala: pentru reactiile de hidroliza enzimele se numesc hidrolaze, pentru reactiile de deshidrogenare dehidrogenaza Proprietati: sunt sensibile la variatia de temperatura peste 80 grade isi distrug structura ireversibil; sub 0 grade isi distrug structura reversibil sensibilitatea fata de pH (echilibru acido-bazic) Enzimele doar maresc viteza de reactie, nu intra in reactie, nu se consuma. Metabolism
Metabolismul este definit ca totalitatea transformarilor de substanta, energie si informatie, care se desfasoara intr-un organism, dar si intre organism si mediul exterior. D.p.d.v. al studiului, metabolismul se imparte in metabolism intermediar si metabolism energetic. Cel intermediar cuprinde secvente biochimice, care se refera la transformarile de substanta, in cadrul unui organism sau intre acesta si mediul inconjurator. Reinnoirea continua a materiei vii si asigurarea energiei necesare activitatii vitale sunt favorizate de echilibrul permanent, de independenta si interdependenta dintre anabolism si catabolism. Prin catabolism se pun la dispozitia organismului produsii intermediari utilizati in anabolism, se asigura energia necesara functiilor vitale, care este apoi, stocata in structura compusului macroergic ATP (acid adenozin trifosforic). Deoarece procesele catabolice (de dezasimilatie) se petrec cu eliberare de energie, ele se mai numesc procese exotermice sau exergonice. Anabolismul reuneste transformarile chimice, care se refera la fenomene de sinteza (de constructie). Procesele anabolice (de asimilatie) se desfasoara cu consum de energie furnizata de ATP, ele fiind definite si ca procese endotermice sau endergonice. Deci, in timp ce reactiile anabolice reinnoiesc permanent structurile celulare uzate, sintetizeaza substante active (enzime, hormoni), asigura cresterea si inmultirea celulelor cu consum energetic, reactiile catabolice genereaza energia prin procese de oxidoreducere, de ardere a constituentilor in prezenta oxigenului. Metabolismul energetic se refera la totalitatea modificarilor de energie care insotesc reactiile metabolismului intermediar. Degajarea de energie la nivel celular nu are loc brusc, ci in mode treptat, prin lanturi lungi de reactii biochimice. In functie de cheltuielile energetice ale organismului, in stare de repaus sau in timpul unor activitati, se poate institui o ratie alimentara. Energia transformata in fibrele musculare, nu poate fi masurata direct. ATP-ul este cel mai raspandit compus macroenergetic in lumea animala, resintetizat numai prin intermediul energiei rezultate din catabolismul glucidelor, lipidelor si, uneori, proteinelor. Reactiile biochimice de sinteza si hidroliza ale ATP se supun legilor termodinamice, conform carora: in orice proces energia totala a sistemului si a mediului inconjurator ramane constanta: energia nu este creata sau distrusa, dar poate trece dintr-o forma in alta; in toate procesele entropia sistemului si a mediului (entropia universului), creste pana la o valoare maxima, cand se atinge un echilibru. Structura acestui compus macroergic cuprinde o molecula de adenina (baza azotata) legata de o molecula de riboza (monozaharid), ce formeaza adenozina si trei grupari de fosfat anorganic (Pi).
Sub actiunea ATP-azei (enzima specifica), ultima grupare de fosfat se desface eliberand rapid o mare cantitate de energie (aprox. 7.3 Kcal/mol). Prin aceasta ATP-ul se reduce la ADP (acid adenozin difosforic) si radical fosfat (Pi). Continuarea degradarii va genera o noua cantitate de energie (aprox. 7.3 kcal/mol) si un mol de AMP (acid adenozin monofosforic). Aceasta reactie se desfasoara numai in anumite conditii, cand sistemul biologic este privat de surse primare de energie. Reactia inversa de formare a moleculei ATP, proces numit fosforilare, va consuma o cantitate de energie egala cu 7.3 kcal. Caracteristica ATP-ului, care-l face sa fie atat de larg folosit ca sursa de energie, este cantitatea mare de energie libera (7.3 kcal/mol in conditii standard sau 12 kcal/mol in conditii fiziologice) stocata in cele doua legaturi macroergice ale sale. Cantitatea de energie din fiecare legatura, eliberata prin hidroliza unei molecule de ATP, este suficienta pentru a determina desfasurarea oricarei etape a lantului biochimic din organism, printr-un transfer energetic corespunzator. Unele reactii, insa, folosesc doar cateva sute de claorii din totalul disponibil, iar restul se pierde sub forma de caldura. Datorita proprietatilor si rolului sau in energetica celulara, ATP-ul ocupa o pozitie centrala intre compusii macroergici. In timpul contractiei musculare, se consuma 10 moli ATP/g tesut/min. Reactia este reversibila cu procesul regenerarii, desfasurat prin intermediul sistemelor: ATP-CP glicolitic oxidativ SISTEMUL ATP-CP Sistemul ATP-CP este cel maisimplu si rapid sistem energetic. In formarea de ATP, celulele utilizeaza un alt compus macroergic care paote stoca circa 10.3 kcal. Aceasta molecula se numeste creatinfosfat (CP) sau fosfocreatina (PC). Fosfocreatina contine, in conditii fiziologice (37 C si continut scazut de reactanti) 13 kcal/mol. Spre deosebire de ATP, acest compus nu actioneaza ca agent de legatura pentru transferul energiei intre principiile alimentare si sistemele functionale celulare. Energia eliberata prin descompunerea CP nu este folosita direct pentru activitatea celulara, ci pentru refacerea ATP-ului, mentinand la o valoare maxima rezerva energetica a organismului. Din acest motiv, fosfocreatina poate fi denumita ca o componenta tampon.
Prin acest sistem, celulele pot stopa depletia ATP-ului prin reducerea de CP, furnizand energia necesara formarii unei cantitati mari de ATP. Procesul este rapid s ipaote fi realizat fara interventia oxigenului si a unor structuri subcelulare specializate. In acest caz, sistemul ATP-CP poate fi considerat un sistem anaerob. CP + ADP -><- ATP + C In primele secunde ale unei activitati musculare intense, cum ar fi proba de viteza, ATP-ul este mentinut relativ constant pe baza descompunerii CP-ului, aflat intr-o continua scadere cantitativa. Capacitatea de mentinere a nivelului ATP, pe baza descompunerii de CP, este limitata. Energia depozitata in ATP si CP poate sustine un efort de intensitate mare timp de 3-15 secunde. Dincolo de acest punct, muschiul trebuie sa apeleze la alte surse formatoare de ATP. SISTEMUL GLICOLITIC O alta metoda de refacere a ATP-ului implica energia eliberata prin descompunerea glucozei. Sistemul se numeste glicolitic, deoarece se refera la procesul anaerob de catabolizare a unui mol de glucoza, cu participarea unor enzime specifice. Produsul final al glicolizei este acidul lactic. Glicoliza este mult mai complexa decat sistemul ATP-CP si include reactii catalizate de enzime specifice, care opereaza in citoplasma celulara. Bilantul energetic net al degradarii anaerobe este de 3 moli ATP pentru fiecare mol de glicogen descompus si de 2 moli ATP pentru fiecare mol de glucoza catabolizata (1 mol ATP este folosit la conversia glucozei in glucoza 6 fosfat). Acest sistem energetic nu produce o mare cantitate de ATP. In ciuda acestui fapt, prin combinarea actiunii sistemelor ATP-CP si a celui glicolitic, muschiul isi poate permite efectuarea unui lucru mecanic, desi rezerva de oxigen este extrem de mica. Sistemele energogenetice anaerobe predomina in primele 1-2 minute ale unui efort de mare intensitate. Acumularea de acid lactic la nivel sanguin si muscular, limiteaza activitatea sistemului glicolitic. Astfel, la sfarsitul unui sprint de 1-2 minute, necesitatile, iar nivelul acidului lactic poate ajunge de la 1 mmol/kg, in repaus, pana la 25 mmol/kg. Aceasta acidifiere la nivelul fibrelor musculare inhiba degradarea unor noi molecule de glicogen, deoarece scade activitatea enzimelor glicolitice. In plus, un pH scazut conduce la pierderea calciului muscular impiedicand, astfel, contractia. Sistemul oxidativ
Sistemul oxidativ reprezinta ultima rezerva energetica a celulei si foloseste ca substrat metabolic, biomoleculele de combustie pe care le degradeaza in prezenta O2. Sistemul oxidativ este, asadar, un proces aerob cunoscut si sub denumirea de respiratie celulara. Productia oxidativa de ATP se desfasoara la nivelul mitocondriilor (organism celular comun) citoplasmatice. In muschi, acestea sunt invecinate miofibrilelor si raspandite prin toata sarcoplasma. Spre deosebire de productia anaeroba de ATP, sistemul oxidativ genereaza o cantitate enroma de energie devenind important in activitati de anduranta. In aceasta situatie, apar cerinte considerabile de oxigen pentru activitatea musculara. Prin catabolizarea aeroba a glicogenului se produc 39 ATP/mol de glicogen, in timp ce degradarea acizilor grasi regenereaza o cantitate de 3 ori mai mare (de exemplu, arderea acidului palmitic cu 16 atomi de carbon duce la regenerarea a 129 moli de ATP, H2O si CO2) Glicoliza = degradare anaeroba. Nu exista asociere glicoliza anaeroba - glocliza aeroba. Un mol glucoza = 2 moli acid lactic. Aceasta descompunere are loc in 11 reactii succesive. Este conversia si transformarea substratului a.i. sa fie posibila formarea unui compus. In timpul acestor reactii exista riscul eliberarii ionilor de hidrogen (H+). Aparitia in cantitate mare a ionilor de H in sange modifica balanta acido-bazica cu pericolul instalarii comei si decesului. Exista 2 sisteme oxidoreducatoare care preiau hidrogenii limitand patrunderea lor in mediul intern. Hidrogenul, eliberat pe parcursul tuturor reactiilor catabolice, este preluat de coenzimele: NAD+ (nicotinamid dinucleotid) si FAD (favinadenin dinucleotid), sisteme oxireducatoare care isi pot modifica starea de oxidare. In reactia nr. 5 din glicoliza, o molecula de NAD va prelua hidrogenul (pentru protectie) si din lipsa oxigenului va ceda hidrogenul acidului piruvic (care se va obtine in reactia 10 a glicolizei). CH3 | CH3 |
C=O + 2 NADH --> HC-OH + 2NAD | COOH | COOH
acid piruvic
acid lactic
CICLUL CORIN - Acidul lactic, in conditiile unei adaptari metabolice foarte bune, pleaca. 20% este degradat in CO2+H2O+E (energie) si 80% duce la formarea de glucoza pe baza eergiei obtinuta din cele 20% Bilantul net energetic al degradarii anaerobe este de 3 moli ATP pentru fiecare mol de glicogen descompus si de 2 moli ATP pentru fiecare mol de glucoza catabolizata (1 mol ATP este folosit la conversia glucozei in glucoza 6 fosfat). Transformarea glucozei in doua molecule de acid lactic favorizeaza eliberarea a 47 kcal/mol energie. Daca unei legaturi de fosfat macroergic din ATP, ii corespunde o energie chimica de ~ 7.3 kcal, atunci in structura chimica a 2 moli ATP, sunt sotcate numai 14.6 kcal din cele 47 kcal eliberate in cursul glicolizei. Restul reprezinta energie calorica, electrica, osmotic etc. Randamentul glicolizei este de ~ 31%. Degradarea aeroba a glucozei In conditii aerobe, glucoza se degradeaza obtinandu-se o cantitate de energie de 20 ori mai mare. Ea parcurge in transformare mai multe etape: o molecula de glucoza => 2 molecule de acid purivic 2 molecule de acid piruvic => dioxid de carbon + apa + energie = aproximativ 688 kcal In aceste reactii oxidative (aerobe) enzimele sunt insotite in anumite puncte de NAD si FAD care pentru a proteja mediul intern de prezenta ionului de hidrogen in cantitate mare preiau hidrogenul pe care il vor elibera si acesta impreuna cu oxigenul formeaza apa Combinarea dintre hidrogen si oxigen, este o reactie eliberatoare de energie. Potentialul energetic este diferit in functie de substratul (NAD/FAD) care preia hidrogenul astfel: daca e de la NAD, energia este echivalenta cu 3 moli ATP daca e de la FAD, energia este echivalenta cu 2 moli ATP In conditii aerobe, reactia este urmatoarea: C6H12O6 + 6O2 --> 6CO2 + 6H2O + E (E=688 kcal) Randamentul de transformare a energiei potentiale din structura glucozei in legaturi macroergice ATP, este de aproximativ 40%. Aceasta valoare depaseste cu mult randamentul celor mai perfectionate motoare termice. Restul energiei (60%) este convertita, fie in energie calorica, necesara mentinerii temperaturii constante a corpului, fie in energia electrica sau osmotica. Bilantul energetic (exprimat in moli de ATP): glicoliza
Glucoza --> 2 moli acid lactic + 2 moli ATP degradare aeroba Glucoza --> 6 moli CO2 + 6 moli H2O + 28 moli ATP. Sistemul oxidativ de sustinere a unui efort de intensitate medie pe o durata mai mare de 5-6 minute se bazeaza pe degradarea oxidativa a acizilor grasi, degradare care poarta numele de betaoxidare. Fiecare acid gras este preluat din citoplasma si trecut in mitocondrie pentru degradare de catre un transportor specific din membrana mitocondriei care se numeste lcarnitina. BC 9 sau s 2 Sis glicolitic o alta metoda de refacere a atp-ului implica energia eliberata prin descompunerea glucozei. Sistemul se numeste glicolitic, deoarece se refera la procesul anaerob de catabolizare a unui mol de glucoza, cu participarea unor enzime specifice. Produsul final al glucozei este acidul lactic. Glicoliza este mult mai complexa decat sis atp- cp si include reactii catalizate de enzime specifice, care opereaza in citoplasma celulara. Bilantul energetic net al degradarii anaerobe este de 3 moli de atp pentru fiecare mol de glicogen descompus si de 2 moli atp pentru fiecare mol de glucoza catabolizata (1mol atp este folosit la conversia glucozei in glucoza 6 fosfat) Acest sistem energetic nu produce o mare cantitate de ATP. In ciuda acestui fapt, prin combinarea actiunii sistemelor ATP- CP si a celul glicolitic, muschiul isi poate permite efectuarea unui lucru mecanic, desi rezerva de oxigen este extrem de mica. Sistemele energogenetice anaerobe predomina in primele 1-2 minute ale unui efort de mare intensitate. Acumulare de acid lactic la nivelul sanguin si muscular, limiteaza activarea sistemului glicolitic. Astfel, la sfarsitul unui sprint de 1-2 minute, necesitatile sistemului anaerob sunt foarte mari, iar nivelul acidului lactic poate ajunge de la 1mmol\kg, in repaus, pana la 25 mmol\kg. Aceasta acidifiere la nivelul fibrelor musculare inhiba degradarea unor noi molecule de glicogen , deoarece scadde activitatea enzimelor glicolitice. In plus un pH scazut conduce la pierderea calciului muscular impiedicand, astfel, contractia SISTEMUL OXIDATIV
Reprezinta ultima rezerva energetica a celulei si foloseste ca substrat metabolic, biomoleculele de combustie pe care le degradeaza in prezenta 02. Sistemul oxidativ este, asadar, un proces aerob cunoscut si sub denumirea de reparatie celulara. Productia oxidativa de ATP se desfasoara la nivelul mitocondriilor citoplasmatice. In muschi, acestea sunt invecinate miofibrilelor si raspandite prin toata sarcoplasma Spre deosebire de productia anaeroba de ATP, sistemul oxidativ genereaza o cantitate enorma de energie devenind important in activitati de anduranta. In aceasta situatie apar cerinte considerabile de oxigen pentru activitatea msculara. Prin catabolizarea eroba a glicogenului se produc 39 moli ATP/MOL de glicogen, in timm ce degradarea acizilor grasi genereaza o cantitatea de 3 ori mai mare ( de ex, arderea acidului palmitic cu 16atomi de carbon duce la regenerarea a 129 moli de ATP, H2O si CO2)
glicoliza=degradarea anaeroba nu exista asocierea glicolizei anaerobe glicoliza artoba 1 mol glucoza= 2 moli acid lactic, are loc in 11 reactii succesive. Este conversia si transformarea substratului a.i sa fie posibila formarea unui compus In timpul acestor reactii exista riscul eliberarii ionilor de hidrogen. Aparitia in cantiate mare a ionilor de h in sange modifica balanta acido-bazica cu pericoloul instalarii comei si decesului Exista 2 sisteme oxido reducatoare care preiau hidrogenii limitand patrunderea lor in mediul intern. Hidrogenul eliberat pe parcursul tuturor reactiiilor catabolice, este preluat de coenzimele : NAD ( nicotinamid dinucleotid) si FAD ( flavin adenin dinucleotid), sistemele oxidoreducatoare care isi pot modifica starea de oxidare. In a 5-a reactie din glicoliza o molecula de NAD va prelua hidrogenul pentru protectie sidin lipsa oxigenului va ceda hidrogenul acidului piruvic(care se va obtine in reactia a 10 a glicolizei) Acidul lactic in conditiile unei adaptari metabolice foarte bune pleaca 20% este degradata in CO2+H2O+E(energie) si 80% duce la formarea de glucoza pe baza energiei obtinuta din cele 20% Bilantul net energetic al degradarii anaerobe este de 3 moli de atb pentru fiecare mol de glicogen descompus si de 2 moli de ATP pentru fiecare mold de glucoza catabolizata (1 mol ATP este folosit la conversia glucozei in glucoza 6 fosfat) Transformarea glucozei in doua molecule de acid lactic favorizeaza eliberarea a 47 Kcal/mol energie
Daca unei legaturi fosfat macroergic de ATP, ii corespunde o energie chimica ~ 7,3 kcal, atunci in structura chimica a 2 moli ATP, sunt stocate numai 14,6 Kcal din cele 47 kcal eliberate in cursul glicolizei. Restul reprezeinta energie calorica, electrica, osmotica etc. Randamentul glicolizei este de ~ 31% DEGRADAREA AEROBA A GLUCOZEI in conditii aerobe, glucoza se degradeaza obtinandu-se o cantitate de enrergie de 20 ori mai mare, ea parcurge in transformare mai multe etape o molecula de glucoza da 2 de acid piruvic 2 molecule de acid piruvic => CO2 si H2O = energie 668 kcal
In aceste reactii oxidative, enzimele sunt insotite in anumimte puncte de NAD si FAD care pt a proteja mediul intern de prezenta ionului de hidrogen in cantitate mare preiau hidrogenul pe care il vor elibera si acesta impreuna cu O2 formeaza H2O Combinarea dintre hidrogen si oxigen este o reactie eliberatoare de energie. Potentialul energetic este diferit in functie de substratul NAD sau FAC care preia hidrogenul. Daca e de la NAD energia este echivalenta cu 3 moli de ATP; Daca e de la FAD energia este echivalenta cu 2 moli de ATP. In conditii aerobe reactia este urmatoarea C6H12O6+6O2 --->6CO2+6H2O+e Randamentul de transformare a energiei potentiale din structura glucozei in legaturi macroenergice ATP, este de aprox 40%. Aceasta valoare depaseste cu mult randamentul celor mai perfectionate motoare termice. Restul energiei (60%) este convertita, fie in energie calorica, necesara mentinerii temperaturii constante a corpului, fie in energie electrica sau osmotica. Bilantul energetic exprimat in moli de ATP al glicolizei cu cel al degradarii oxidative a glucozei, se constata o eliberare de energie de 19 ori mai mare in cel de-al 2lea proces. Glicoliza GLUCOZA degradare aeroba Glucoza 6 moli CO2+ 6 moli H2O + 38 moli ATP 2 moli acid lactic + 2 moli ATP
Sistemul oxidativ deci sustinerea de efort de intensitate medie pe o durata mai mare de 5-6 min se bazeaza pe degradarea oxidativa a acizilor grasi, degradare care poarta numele de betaoxidare
Fiecare acid gras este preluat din citoplasama si trecut in mitocondrie pt degradare de catre un transportor specific din membrana mitocondriei care se numeste l-carnitina Metabolismul proteinelor Proteinele alimentare (exogene) sunt supuse proceselor de digestie si absorbtie, in diferite nivele ale tractului gastrointestinal, sub actiunea enzimelor proteolitice. In stomac, moleculele proteice sunt scindate in prezenta pepsinei, care, este secretata sub forma inactiva pepsinogen devine optima, in mediul acid al cavitatii gastrice Polipeptidele cu cate 7 resturi de aminoacizi continua degradarea enzimatica, in intestin . Enzimele implicate (tripsina, chimotripsina si carboxipeptidaza) sunt, mai intai, secretate, sub forma inactiva in sucul pancreatic, iar dipeptidazele in cel intestinal. Catabolismul aminoacizilor Procesele de degradare si sinteza a proteinelor se desfasoara, in organism, pe masura necesitatilor. Proteinele nu se depoziteaza intr-un organ sau tesut specializat. Intotdeauna aprotul sporit de proteine este urmat de o intensificare a proceselor de degradare, iar reducerea ingestiei alimentare, mareste viteza reactiilor de sinteza. Organismul are capacitatea de a mentine un echilibru permanent intre aportul si eliminarea de proteine. Stabilirea echilibrului azotat depinde de ingestia exogena de aminoacizi, in conditiile in care importanta este, nu numai masa proteica, ci si calitatea (continutul in aminoacizi esentiali). Principalele mecanisme generale de degradare a aminoacizilor sunt: Dezaminarea oxidativa care consta in eliminarea unei molecule de amoniac (NH3), din cadrul structurii unui aminoacid, cu formare de cetoacid. H2N CH COOH + 1/2 O2 -> R C COOH + NH3 | aminoacid || cetoacid
Reactiile de acest tip se desfasoara cu participarea unor enzime, avand in structura lor NAD+ (forma oxidata). Acesta preia hidrogenul si-l transfera latului respirator. Transaminarea se refera la transferul unei grupari amino (NH2) de la un aminoacid la un cetoacid, in prezenta aminotransferazelor. Enzimele prezinta in structura, un derivat de la vitamina B6 (piridoxal fosfat).
In urma degradarii, se vor forma aminoacizi si cetoacizi noi, care intra in ciclul Krebs sau in alte serii metabolice. Reactia reprezinta o cale de formare a aminoacizilor neesentiali. R1 CH COOH + R2 C COOH | NH2 aminoacid || O cetoacid
R1 C COOH + R2 CH COOH || O cetoacid | NH2 aminoacid
Decarboxilarea este un proces de eliberare a unei molecule de CO2, cu formare de amine biogene R CH -COOH -> R CH2 NH2 + CO2 | NH2 aminoacid amina
Mecanismul acestei reactii se desfasoara sub actiunea unei enzime, care are in componenta piridoxal fosfatul derivat de la vitamina B6. Detoxifierea amoniacului Amoniacul (NH3) este produsul final al catabolismului proteic, la nivel celular. Se formeaza continuu si in cantitati relativ mari, prin dezaminarea aminoacizilor sau degradarea bazelor azotate si a altor compusi cu azot. Cu toate acestea, concentratia amoniacului in sange, oscileaza intre 0.1 0.2 mg% Pentru mentinerea acestor limite, inofensive organismului, au loc procese de detoxifiere, extrem de eficiente. Acestea sunt reprezentate de ureogeneza ( formarea ureei) si biosinteza glutaminei (fixarea temporara si reversibila a amoniacului pe molecula acidului glutamic).
Ureogeneza este un proces consumator de energie si impiedica acumularea de amoniac liber, in concentratii prea mari. Energia necesara desfasurarii ciclului ureogenetic este furnizata de compusii macroergici specifici. Ureea se sintetizeaza, exclusiv, in ficat si are, ca limite normale sanguine, valori de 20-40 mg%. EXAMEN Fiziologie - in principal subiecte gen eseu. Modificari de adaptare in efort pentru sistemul cardiovascular, sistemul respirator, sistemul muscular. / Adaptarea organismului la nivelul sistemului muscular, cardiovascular, respirator la efort fizic. Biochimie glucide, lipide, proteine. Generalitati proteine, definitie, in ce se gasesc, din ce sunt formate, clasificare, metabolism. Glucide: definitie, clasificare, unde se gasesc, degradare. Lipide: ce sunt, unde se gasesc, rolul, clasificare (nu e exacta ca au o structura...). Digestie, punctul de emulsionare (degradarea fizica). Degradarea acizilor grasi. In cadrul sistemului oxidativ de refacere a ATP-ului, oxidarea acizilor grasi reprezinta o etapa importanta in sustinerea energetica a miscarii. Astfel, grasimile suporta in tubul digestiv transformari fizice si chimice. Transformarile fizice emulsionarea sub actiunea componentelor bilei care au proprietati tensioactive facand accesibila actiunea enzimelor din pancreas Transformarile chimice se refera la degradarea specifica a grasimilor sub actiunea lipazei pancreatice. In urma procesului de digestie, din structura grasimilor se desprind formatiunile de baza. Acizii grasi vor fi supusi procesului de oxidare printr-un mecanism care se numeste betaoxidare (se actioneaza la nivelul atomului de carbon beta). Procesul are loc in mitocondrie, iar trecerea din citosoli in mitocondrie se face prin intermediul L-carnitinei. Acest compus are rol de transportor in sensul ca preia molecula de acid gras si o activeaza transferand-o in mitocondrie pentru betaoxidare. Fenomenul este consumator de energie echivalenta cu 2 moli de ATP. Acidul gras odata ajuns in mitocondrie trece printr-un circuit oxidativ sub actiunea sistemelor enzimatice de scindare succesiva a cate unui fragment cu 2 atomi de carbon. Fiecare fragment este convertit in acetilcoenzima A care va initia cate un ciclu Krebs (in acest ciclu se elibereaza 12 moli ATP). Deci, in fiecare circuit Krebs sews elibereaza o energie care va fi depozitata in 12 moli ATP. Ex. acid palmitic => C16 C16 = C14 + C2 -> Ciclu Krebs => 12 ATP
-> C12 + C2 -> C10 + C2 -> C8 + C2 -> C6 + C2 -> C4 + C2 -> C2 + C2 => 8C2 = 96 ATP Fiecare etapa prin care se desprinde cate un fragment de C2 (acetilcoenzima) reprezinta o succesiune de alte 4 reactii biochimice in care intervin cele 2 sisteme oxidoreducatoare (NAD si FAD) care preiau hidrogenul si in prezenta oxigenului formeaza molecula de apa si elibereaza energie. 7NAD -> 7*3 => 21 ATP. 7FAD -> 7*2 => 14 ATP C16 => 96+21+14 = 131 ATP 2 ATP (activare cu L-carnitina) => 129 ATP (energie stocata ~ lucru mecanic) TEMA: Bilantul energetic net pentru acidul stearic C18. In conditiile unui efort de anduranta acizii grasi pot sa sustina de la 10 minute pana la cateva ore de efort.
S-ar putea să vă placă și
- Dobre Amelia KINETOTERAPIA DEFICIENTELOR FIZICE SI SENZORIALEDocument4 paginiDobre Amelia KINETOTERAPIA DEFICIENTELOR FIZICE SI SENZORIALEAmelia F. DobreÎncă nu există evaluări
- Ioana Pearsica - Relatia Actor-Spectator La GrotowskiDocument8 paginiIoana Pearsica - Relatia Actor-Spectator La GrotowskiAntonia IordacheÎncă nu există evaluări
- C 1 Sistemul NeuromuscularDocument22 paginiC 1 Sistemul NeuromuscularDaniela Acceleanu100% (1)
- DVMDocument30 paginiDVMValentin Bogdan VfbÎncă nu există evaluări
- Chirped LessDocument158 paginiChirped LessLemmyÎncă nu există evaluări
- Sindroamele Si Afectiunile ExtrapiramidaleDocument39 paginiSindroamele Si Afectiunile ExtrapiramidaleanaebritÎncă nu există evaluări
- Exercitiul Fizic În Profilaxia Si Tratamentul Procesului de ImbatranireDocument6 paginiExercitiul Fizic În Profilaxia Si Tratamentul Procesului de ImbatranireVas Raul-MihaiÎncă nu există evaluări
- SUBIECTE Recuperare NeurologieDocument3 paginiSUBIECTE Recuperare NeurologieTurta AdyÎncă nu există evaluări
- AruncariDocument38 paginiAruncaricriminalistÎncă nu există evaluări
- DefinitieDocument1 paginăDefinitieMaria AdÎncă nu există evaluări
- NociceptiaDocument17 paginiNociceptiaVica LazariÎncă nu există evaluări
- Leziuni Musculare de SuprasolicitareDocument16 paginiLeziuni Musculare de SuprasolicitareValentin Bogdan VfbÎncă nu există evaluări
- Fortele Interioare Ale LocomotieiDocument8 paginiFortele Interioare Ale LocomotieiStefan ToaderÎncă nu există evaluări
- Miologie CursDocument18 paginiMiologie Cursblizzard90Încă nu există evaluări
- Referat Mortean VladimirDocument17 paginiReferat Mortean VladimirVladimir MorteanÎncă nu există evaluări
- Anatomie Si Biomecanica UmarDocument28 paginiAnatomie Si Biomecanica UmarHristodoulakis Stefanos0% (1)
- KinesiologieDocument7 paginiKinesiologieValeria StillÎncă nu există evaluări
- Mușchi Origine Insertie Actiune InervatieDocument6 paginiMușchi Origine Insertie Actiune InervatieFlorinel OpreaÎncă nu există evaluări
- Afectiunile BandeleteiDocument16 paginiAfectiunile BandeleteiAlexandra CroitoruÎncă nu există evaluări
- Refacerea Dupa Efort ArticolDocument2 paginiRefacerea Dupa Efort Articolkarl_bluewishÎncă nu există evaluări
- Fiziopatologia AntrenamentuluiDocument11 paginiFiziopatologia AntrenamentuluiGeanina ButunoiÎncă nu există evaluări
- RECEPTORIIDocument3 paginiRECEPTORIIAlexe DianaÎncă nu există evaluări
- Asistenta Psihologica in KinetoterapieDocument4 paginiAsistenta Psihologica in KinetoterapieFlorin DinuÎncă nu există evaluări
- Clavicula Si OmoplatulDocument10 paginiClavicula Si OmoplatulAlina CamerzanÎncă nu există evaluări
- Contractia Musculaturii Muschiului CardiacDocument4 paginiContractia Musculaturii Muschiului CardiacMitrache AureliaÎncă nu există evaluări
- Sistem MuschiDocument19 paginiSistem MuschiDan MassonÎncă nu există evaluări
- Neuro BunDocument41 paginiNeuro Bunpunktuletzz100% (1)
- Nervii SpinaliDocument3 paginiNervii SpinaliDanutz MariusÎncă nu există evaluări
- FiziopatologiaDocument9 paginiFiziopatologiachivumihaelaÎncă nu există evaluări
- KinetologieDocument15 paginiKinetologiejulie77eÎncă nu există evaluări
- Luxatia Congenitala de SoldDocument11 paginiLuxatia Congenitala de SoldPintilie AlexandraÎncă nu există evaluări
- Dorina Flora Tehnici de Baza in Kinetoterapie PDFDocument327 paginiDorina Flora Tehnici de Baza in Kinetoterapie PDFIsabela IacobÎncă nu există evaluări
- Muschiul StriatDocument7 paginiMuschiul StriatDima SilviuÎncă nu există evaluări
- Profesia de KinetoterapeutDocument2 paginiProfesia de KinetoterapeutMihai AcăeiÎncă nu există evaluări
- Subiecte KinesiologieDocument6 paginiSubiecte KinesiologieDaniel Nitescu100% (1)
- Caile Sensibilitatii La Cap Si La Gat CURS 4Document4 paginiCaile Sensibilitatii La Cap Si La Gat CURS 4Alin PacurarÎncă nu există evaluări
- Coada de CalDocument4 paginiCoada de CalAdi RughiÎncă nu există evaluări
- RELAXAREADocument34 paginiRELAXAREAAdrian VladÎncă nu există evaluări
- AlpinismulDocument56 paginiAlpinismulElena TonuÎncă nu există evaluări
- 8 Circuite Neuronale 2Document1 pagină8 Circuite Neuronale 2Alex Cu TridentÎncă nu există evaluări
- Traumatismele Maduvei SpinariiDocument27 paginiTraumatismele Maduvei SpinariiIonut Si Madalina PatrascuÎncă nu există evaluări
- Functia de Conducere A Trunchiului CerebralDocument19 paginiFunctia de Conducere A Trunchiului Cerebral12345Încă nu există evaluări
- Curs 3 - Generalitati Despre Muschi PDFDocument60 paginiCurs 3 - Generalitati Despre Muschi PDFFlorinela PopaÎncă nu există evaluări
- HemodinamicaDocument28 paginiHemodinamicazxcvnbvnÎncă nu există evaluări
- Sindromul ExtrapiramidalDocument27 paginiSindromul ExtrapiramidalFlorentina Kociopolos CiobanuÎncă nu există evaluări
- Universitatea Spiru Haret Olga DjamoDocument30 paginiUniversitatea Spiru Haret Olga Djamocosmin_mirelÎncă nu există evaluări
- Educatie Fizica Sport Si KinetoterapieDocument200 paginiEducatie Fizica Sport Si KinetoterapieMironescu LaviniaÎncă nu există evaluări
- Fiziologie TotDocument34 paginiFiziologie TotbamsweÎncă nu există evaluări
- TMK Curs ViiiDocument10 paginiTMK Curs ViiiviorelÎncă nu există evaluări
- Curs 5Document14 paginiCurs 5sham harbaÎncă nu există evaluări
- FiziologieDocument47 paginiFiziologieGeorgian SerafimÎncă nu există evaluări
- Anatomia Si Fiziologia Sistemului MuscularDocument36 paginiAnatomia Si Fiziologia Sistemului MuscularGligan MihaiÎncă nu există evaluări
- Îfiziologia Sist MuscDocument11 paginiÎfiziologia Sist MuscmalexandraÎncă nu există evaluări
- Tema 1 BGKDocument10 paginiTema 1 BGKDorian T FlorinÎncă nu există evaluări
- MuscularDocument46 paginiMuscularCatalin CusnirÎncă nu există evaluări
- Fiziologia MuschilorDocument24 paginiFiziologia Muschilorlena red100% (1)
- CURS MUSCHI FIZIO PPTDocument46 paginiCURS MUSCHI FIZIO PPTIrina MureșanÎncă nu există evaluări
- Sistemului NeuromuscularDocument54 paginiSistemului NeuromuscularStefi MaryÎncă nu există evaluări
- Referat Anatomie 3Document6 paginiReferat Anatomie 3Mihnea BucurÎncă nu există evaluări
- Sistemul MuscularDocument9 paginiSistemul MuscularDiana AndreeaÎncă nu există evaluări
- Institutii Ale Uniunii EuropeneDocument11 paginiInstitutii Ale Uniunii EuropeneEu VictorÎncă nu există evaluări
- Anexa 1 - Asamblari DemontabileDocument1 paginăAnexa 1 - Asamblari DemontabileEu VictorÎncă nu există evaluări
- Curs 13 - 13 LPDocument20 paginiCurs 13 - 13 LPSimionHessÎncă nu există evaluări
- Coroziunea GalvanicaDocument2 paginiCoroziunea GalvanicaCatalin DumitruÎncă nu există evaluări
- AnoziDocument3 paginiAnoziFlorin MuşatÎncă nu există evaluări
- Peda GogiePeda GogiePeda GogiePeda GogiePeda GogiePeda GogieDocument2 paginiPeda GogiePeda GogiePeda GogiePeda GogiePeda GogiePeda GogieEu VictorÎncă nu există evaluări
- Principiul Minimului de Energie Si Maximul de EntropieDocument9 paginiPrincipiul Minimului de Energie Si Maximul de EntropieCristina MoldoveanuÎncă nu există evaluări
- Conductia Extrinseca A SemiconductorilorDocument1 paginăConductia Extrinseca A SemiconductorilorEu VictorÎncă nu există evaluări
- Bioingineria CDocument1 paginăBioingineria CEu VictorÎncă nu există evaluări
- Copiute MEEDocument3 paginiCopiute MEEEu VictorÎncă nu există evaluări
- Lista Lucrarilor Practice de LaboratorDocument1 paginăLista Lucrarilor Practice de LaboratorEu VictorÎncă nu există evaluări
- SUBIECTE Chimie 2011 ELTHDocument11 paginiSUBIECTE Chimie 2011 ELTHRaduCiciuÎncă nu există evaluări
- 3 Calculul Parametrilor InfasurariiDocument13 pagini3 Calculul Parametrilor InfasurariiMihai ConstantinescuÎncă nu există evaluări
- Proiect MP 93Document6 paginiProiect MP 93Eu VictorÎncă nu există evaluări
- Chimie Grafic Duritatea ApeiDocument2 paginiChimie Grafic Duritatea ApeiEu VictorÎncă nu există evaluări
- Caracteristici ExterneDocument3 paginiCaracteristici ExterneEu VictorÎncă nu există evaluări
- T1 - Transformator Monofazat PDFDocument2 paginiT1 - Transformator Monofazat PDFNicu IlieÎncă nu există evaluări
- Proiect MPDocument14 paginiProiect MPEu VictorÎncă nu există evaluări
- Radarul IstoricDocument2 paginiRadarul IstoricEu VictorÎncă nu există evaluări
- Probleme TDEE 2015Document8 paginiProbleme TDEE 2015Eu VictorÎncă nu există evaluări
- Principiul Minimului de Energie Si Maximul de EntropieDocument9 paginiPrincipiul Minimului de Energie Si Maximul de EntropieCristina MoldoveanuÎncă nu există evaluări
- Introducere Curenti TurbionariDocument3 paginiIntroducere Curenti TurbionariEu VictorÎncă nu există evaluări
- Determinarea Rezistivitatiii de VolumDocument4 paginiDeterminarea Rezistivitatiii de VolumDan Petre100% (1)
- Radar ComponenteDocument2 paginiRadar ComponenteEu VictorÎncă nu există evaluări
- Determinarea Rezistivitatiii de VolumDocument4 paginiDeterminarea Rezistivitatiii de VolumDan Petre100% (1)
- Linii Electrice SubteraneDocument5 paginiLinii Electrice SubteraneEu VictorÎncă nu există evaluări
- Linii Electrice SubteraneDocument5 paginiLinii Electrice SubteraneEu VictorÎncă nu există evaluări
- Fiziopatologia InfectieiDocument6 paginiFiziopatologia InfectieiRoxanaktÎncă nu există evaluări
- Catabolismul AminoacizilorDocument2 paginiCatabolismul AminoacizilorEu VictorÎncă nu există evaluări