Documente Academic
Documente Profesional
Documente Cultură
Fiziopatologie
Încărcat de
Cella DaniDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Fiziopatologie
Încărcat de
Cella DaniDrepturi de autor:
Formate disponibile
Fiziopatologie Curs XVIII 02.04.
2014
Fiziopatologia insuficientei
respiratorii de origine pulmonara
Partea III
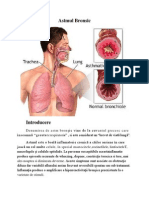
Fiziopatologia astmului bronsic
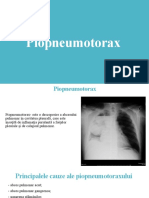
Astmul bronsic reprezinta o dezordine inflamatorie crunta si difuza a cailor aerifere
intrapulmonare care, la persoanele cu o anumita predispozitie genetica, determina
simptome asociate cu obstructia difuza, generalizata si variabila a acestor cai
aerifere, obstructie care este, spre deosebire de alte afectiuni pulmonare,
reversibila, fie spontan fie sub tratament. De asemenea, fenomenele inflamatorii
cronice si difuze cresc reactivitatea bronsica si bronhiolara la diferiti stimuli.
Mecanismele obstructiei bronho-bronhiolare in astmul bronsic sunt urmatoarele
(sunt similare cu cele din BPOC, dar sunt difuze si in mare parte reversibile):
Bronhospasmul Este produs atat pe cale umorala (prin diferiti mediatori
proinflamatori) cat si pe cale nervoasa (reflexa pornind de la acei receptori
de iritatie care devin mult mai sensibili in conditiile proceselor inflamatorii
pulmonare cronice).
Edemul inflamator al mucoasei bronsice si bronhiolare
Hipersecretia de mucus Are loc de asemenea sub influenta unor mediatori
proinflamatori.
Compresiunea multor bronhiole terminale de catre alveole vecine hiperinflate
Ingustarea intrinseca a lumenului bronsic si bronhiolar datorita ingrosarii
peretilor acestor cai Aceasta ingrosare se datoreaza pe o parte fibrozarii
interstitiale a peretilor bronsici si bronhiolari sub actiunea cantitatilor mari de
FGF eliberate in timp de catre macrofagele activate in cursul proceselor
inflamatorii, iar pe de alta parte hipertrofiei tunicii musculare bronsice si
bronhiolare, indusa de asemenea de un factor de crestere, anume TGF,
eliberat de asemenea in special de catre macrofagele participante la
raspunsul inflamator. Aceste doua modificari structurale apar in formele vechi
de astm (la indivizii care au multe crize de astm in antecedente, astfel incat
acesti doi factori de crestere au avut ocazia sa induca ingrosarea peretilor).
Tipurile de astm bronsic
Din punct de vedere etiopatogenic, acestea sunt in numar de doua:
Astmul bronsic alergic sau extrinsec
Astmul bronsic nealergic sau intrinsec
Fiziopatologie Curs XVIII 02.04.2014
Indiferent de etiopatogenie, in fiziopatologia starilor de astm bronsic intervin doua
tipuri de anomalii:
Anomalii imunologice si de descarcare a unor mediatori proinflamatori
Intervin in primul rand in astmul bronsic alergic.
Anomalii de inervatie vegetativa a arborelui bronsic si/sau un raspuns
inflamator exagerat al organismului la diferiti factori cu impact pulmonar
bronho-bronhiolar.
Astmul bronsic alergic (extrinsec)
Este forma cea mai frecvent intalnita. In cazul sau, intervin in principal anomaliile
imunologice si de descarcare a unor mediatori proinflamator. Este declansat de
inhalarea unor alergeni, precum praf, polen, par de animale etc. In general, alergenii
sunt antigene comune, banale, foarte slab imunogene, care la persoanele fara nicio
anomalie imunologica nu produc niciun fel de reactie. In general in alergii, si in
particular in cazul astmului bronsic, primul contact cu un alergen nu produce nicio
simptomatologie (se numeste contactul sensibilizant), pentru ca, la aceste persoane
predispuse, primul contact induce formarea in cantitate crescuta a unor anticorpi
dintr-o clasa neobisnuita (IgE). IgE sunt puternic citofile (se fixeaza, prin capatul lor
FC, pe mastocitele si bazofilele din intregul organism, aceste doua tipuri celulare
avand pe membrana lor receptori de tip F CR). La urmatoarele contacte cu acelasi
alergen, inhalat in cazul astmului bronsic, alergenul se ataseaza in mod specific de
IgE fixate in prealabil la suprafata mastocitelor, anume cele de la nivelul mucoasei
bronsice si bronhiolare. Desi IgE se depun pe toate mastocitele din organism,
conflictul antigen-anticorp are loc numai la nivelul portii de intrare. Exista de fapt
doua straturi de mastocite la nivelul mucoasei bronsice si bronhiolare:
Strat superficial Sunt intercalate cu celulele epiteliale si vin in contact cu
lumenul bronsic si bronhiolar.
Strat profund Sunt situate sub membrana bazala a epiteliului bronsic si
bronhiolar.
Conflictul antigen-anticorp din stratul superficial determina, prin modificari ale
receptorului si semnale transmise intracelulare, degranularea si activarea
metabolica a acestor mastocite, avand drept consecinta eliberarea unor cantitati
mari de mediatori de tip proinflamator. Din aceste mastocite de suprafata se
elibereaza inclusiv un factor proteic care deschide jonctiunile interepiteliale,
permitand alergenului sa ajunga la mastocitele mai profunde, degranulandu-le si pe
acestea.
Se elibereaza doua categorii de mediatori:
Mediatori preformati histamine, hidrolaze acide, enzime proteolitice, factori
chemotactici
Fiziopatologie Curs XVIII 02.04.2014
Mediatori neoformati Acestia se sintetizeaza in exces odata cu activarea
metabolica a mastocitelor. Exemple sunt prostaglandinele, leucotrienele, PAF
si TXA2.
In functie de proprietatile lor, acesti mediatori pot fi impartiti in doua categorii:
Mediatori cu proprietati bronhoconstrictorii Sunt reprezentati de histamina,
SRS-A, PAF, PGD2, PGF2, TXA2 etc. Toti acesti mediatori au receptori specifici
la nivelul fibrelor musculare netede bronsice si bronhiolare, dar actioneaza
printr-un sistem de mesageri secundari comun (sistemul guanilat ciclaza
GMPc).
Mediatori cu proprietati chemotactice Printre cei mai importanti se afla ECFA
(eosinophilic chemotactic factor of anaphylaxis). Acesta atrage in peretii
bronsici si bronhiolari eozinofile pe care le si activeaza metabolic, din acestea
descarcandu-se radicali liberi de oxigen, hidrolaze acide, enzime proteolitice
etc., precum si proteina bazica majora (PBM), care are proprietatea de a opri
miscarile cililor bronsici si bronhiolari, favorizand acumularea de mucus si
obstructia cailor aerifere respective. In acelasi timp, aceasta proteina are un
efect lezional asupra celulelor epiteliale bronsice si bronhiolare, favorizand
descuamarea acestora. Prin aceasta descuamare, sunt favorizate fenomenel
obstructive, mai ales in caile aeriene mici. De asemenea, din punct de vedere
morfopatologic, astmul bronsic are, spre deosebire de alte afectiuni
inflamatorii pulmonare (ex.: BPOC), se caracterizeaza prin invadarea peretilor
bronsici si bronhiolari de catre eozinofile, prin descuamari epiteliale si printr-o
foarte puternica activare a mastocitelor. Un alt factor chemotactic este NCFA
(neutrophilic chemotactic factor of anaphylaxis), care atrage si activeaza
neutrofilele, aparand deci o noua sursa de factori proinflamatori. In plus,
neutrofilele si monocitele sunt puternic atrase si de catre LTB4 eliberata din
mastocite. Alti factori chemotactici, cu pondere mai mica, sunt reprezentati
de histamina, PGA, PGE si PAF. Desi este un factor chemotactic relativ slab,
PAF stimuleaza foarte puternic toate cele trei functii ale celulelor profesionale
proinflamatorii (chemotactismul, citotoxicitatea oxigen-dependenta si
capacitatea de fagocitoza).
In plus, in formele mai vechi de astm bronsic, prin descarcarile repetate de TGF si
FGF, se ajunge la o ingrosarea a peretilor bronsici si bronhiolari si implicit o ingustare
a lumenului. Aceasta modificare anatomica face ca, in formele vechi de astm, in
perioadele dintre crize, obstructia sa nu mai fie complet reversibila (lumenul este
ingustat din punct de vedere structural).
Persoanele predispuse la a face astm bronsic alergic sunt cele cu anumite
modificari:
Numar prea mare de LTh2 subtipul Acestea interactioneaza cu LB subtipul
, stimuland productia de IgE.
3
Fiziopatologie Curs XVIII 02.04.2014
Numar prea mare de LB subtipul
Numar prea mic de LTs care controleaza cooperarea anterior mentionata
Prezenta pe CPA, in special pe macrofage, a unor molecule MHC-II particulare
Acestea, in complex cu alergenul, stimuleaza anormal de puternic LT h2
subtipul , chiar daca acestea sunt prezente in numar normal, iar in acelasi
timp nu stimuleaza LTs.
Astmul bronsic nealergic (intrinsec)
Poate fi declansat, de asemenea la persoane predispuse genetic, de inhalarea unor
iritanti (praf, gaze industriale, pulberi industriale, fum, aer prea rece/uscat), de efort
fizic, de emotii puternice, de administrarea unor medicamente (in special blocante), precum si de o serie de infectii bronhopulmonare (asa-numitul astm
infectios). In toate aceste cazuri, cu exceptia ultimului, in producerea astmului
intervin cu precadere anomalii de inervatie vegetativa a arborelui bronsic. In cazul
astmului infectios intervine, tot din motive genetice, un raspuns inflamator exagerat
al organismului, cu formarea si descarcarea exagerat de mare a unor mediatori de
tip proinflamator, care produc bronhoconstrictie.
Anomaliile de inervatie vegetativa a arborelui bronsic pot fi:
Predominanta inervatiei colinergice (parasimpatice), in detrimentul celei
adrenergice Aceasta duce la o crestere a sensibilitatii receptorilor de iritatie,
care sunt inervati parasimpatic. Astfel, la inhalarea unei cantitati foarte mici
de iritanti produce bronhoconstrictie reflexa.
Un numar mai mare de receptori -adrenergici (prin a caror stimulare se
produce bronhoconstrictie) si/sau un numar prea mic de receptori adrenergici (prin a caror stimulare se produce bronhodilatatie) Astfel, in
conditiile descarcarii unor cantitati mari de catecolamine, acestea vor actiona
la nivel pulmonar predominant pe receptori , producand bronhoconstrictie.
Un dezechilibru in ceea ce priveste sistemul NANC (non-adrenergic noncolinergic) Caile aerifere, in special cele mici, au si filete nervoase NANC, din
terminatiile carora se elibereaza atat neurotransmitatori de tip
bronhodilatator (ex.: VIP) cat si neurotransmitatori de tip bronhoconstrictor
(tahikinine ex.: substanta P, calcitonina, neurokininele A si B). Un
dezechilibru ereditar in favoarea tahikininelor predispune la bronhoconstrictie.
Acest tahikinine cresc si secretia de mucus si permeabilitatea capilara,
favorizand edemul mucoase bronsice si bronhiolare.
Din punct de vedere al mecanismelor generatoare de insuficienta pulmonara, in
astmul bronsic de inceput, principalul mecanism este inegalitatea rapoartelor V/Q
(obstructia este difuza, dar nu este omogena la inceput). In astmul bronsic vechi,
cand apar acele modificari structurale ale bronhiilor si bronhiolelor, cu ingustarea
ireversibila a lumenelor, obstructia se uniformizeaza. Chiar mai mult, cu cat
conflictele imunologice se repeta, din cauza LT cu memorie, intensitatea
raspunsurilor imune creste, deci si inflamatia si bronhoconstrictia vor fi mai
4
Fiziopatologie Curs XVIII 02.04.2014
puternice, astfel incat in aceste stadii tardive, principalul mecanism devine
hipoventilatia alveolara generalizata. Astfel, in perioada crizei, pe langa hipoxemie
va exista si hipercapnie. De asemenea, intervine scaderea difuziunii oxigenului prin
MAC (membrana alveolo-capilara), in mod indirect:
Scaderea suprafetei alveolare totale, din cauza componentei emfizematoase
Inegalitatea rapoartelor V/Q
Ruperea capilarelor pulmonar, tot din cauza componentei emfizematoase,
scade dimensiunea total a patului capilar pulmonar, deci creste viteza de
circulatie a sangelui si scade timpul de contact cu alveolele
Suntul vascular intrapulmonar Unitatile V/Q=0 echivaleaza cu un sunt, dar
exista si sunt real. Faptul ca numarul capilarelor pulmonare scade, iar VD
(ventriculul drept) trimite in plamani o cantitate normala de sange, face sa
creasca atat de mult presiunea in sistemul arteriolar pulmonar incat sa
forteze deschiderea anastomozelor arteriolovenulare.
Fiziopatologia edemului pulmonar acut cardiogen
Este o complicatie grava a unei insuficiente cardiace stangi severe sau a unei
stenoze mitrale stranse. Din punct de vedere fiziopatologic, edemul pulmonar acut
(EPA) se caracterizeaza printr-o extravazare hidrica masiva din capilarele pulmonare,
la inceput in interstitiul pulmonar, iar cand acesta se satureaza, apare si inundarea
alveolara. Bolnavul poate muri sufocat de propriul sau lichid de edem. Principalul
mecanism fiziopatologic implicat in constituirea EPA cardiogen este cresterea foarte
mare a presiunii hidrostatice in capilarele pumonare. Aceasta se datoreaza in primul
rand stazei venoase pulmonare retrograde in amontele unui baraj reprezentat fie de
un VS insuficient care nu mai este capabil sa preia din circulatia venoasa pulmonara
o cantitate suficienta de sange, fie stenoza mitrala stransa. Staza venoasa
retrograda, cu cresterea presiunii hidrostatice, se rasfrange pana la nivelul
capilarelor pulmonare, si prin aceasta cresterea presionala este favorizata
extravazarea lichidului. In insuficienta cardiaca stanga, staza pulmonara creste
suplimentar din cauza unei hipervolemii determinata de o retentie renala hidrosalina
mare, deoarece in insuficienta ventriculara stanga, exista un nivel mare de
aldosteron si ADH.
Un alt mecanism, de data aceasta auxiliar, implicat in constituirea EPA cardiogen,
este scaderea presiunii coloid-osmotice a plasmei, din cauza unei scaderi relative a
concentratiei de proteine plasmatice, din cauza hipervolemiei, consecinta a retentei
renale hidrosaline.
Un al treilea mecanism, tot auxiliar, este scaderea drenajului limfatic pulmonar, mai
exact al apei interstitiale. Acesta este un mecanism care este implicat in agravarea
EPA si nu in generarea acestuia si care se datoreaza scaderii intensitatii fenomenului
de pompa respiratorie. Drenajul limfatic al plamanului este foarte mult asistat
mecanic de miscarile ciclice de expansiune si contractie pulmonara in timpul ciclului
5
Fiziopatologie Curs XVIII 02.04.2014
respirator, aceste miscari succesive actionand ca o pompa mecanica ce ajuta
drenajul limfatic interstitial pulmonar. Faptul ca interstitiul pulmonar contine mult
lichid face ca plamanul sa devina foarte rigid. Atunci, amplitudinea miscarilor
plamanilor este mult mai mica decat in mod normal, lucru care va stanjeni drenajul
limfatic pulmonar.
Din punct de vedere al insuficientei pulmonare, si in EPA cardiogen intervin toate
cele patru mecanisme. Initial, pe primul plan se afla inegalitatea rapoartelor V/Q.
Initial sunt inundate, din cauza gravitatiei, teritorii alveolare de la bazele plamanilor.
Edemul intersitial are un efect compresiv asupra capilarelor pulmonare, in special in
teritoriile bazale.
Ulterior insa, pe masura ce sunt invadate tot mai multe alveole, mergandu-se pana
la apex (hipoventilatie pulmonara totala apare si hipercapnia), intervin si celelalte
doua mecanisme, de data aceasta nu doar cu rol auxiliar. De exemplu, scaderea
difuziunii oxigenului prin MAC apar in mod direct prin ingrosarea MAC, prin edemul
interstitial. Apare in proportie mare si efectul de sunt. Presiunea creste de multe ori
atat de tare incat se forteaza deschiderea de anastomoze arteriolovenulare.
Fiziopatologia sindromului de detresa respiratorie a adultului
Este un sindrom care imbraca forma unui edem pulmonar necardiogen. In cele mai
multe situatii, acest sindrom de detresa respiratorie a adultului apare in stadiile
avansate ale starilor de soc, indiferent de natura socului. Cand apar acele tulburari
grave la nivelul microcirculatiei, cu sechestrari sangvine importante, hipoxie grava si
acidoza, inclusiv la nivel pulmonar, multi dintre mediatorii eliberati cresc foarte mult
permeabilitatea capilara, cu extravazare lichidiana si edem pulmonar masiv.
De asemenea, acest sindrom poate sa apara in conditiilor inhalarii unor conditii
semnificative de gaze toxice, care produc in mod direct leziuni alveolare, cu reactie
inflamatorie consecutiva grava, aseptica dar cu eliberarea de mediatori care produc
edem.
Se poate ajunge la astfel de leziuni cu reactie inflamatorie puternica si in cazul unor
radioterapii pulmonare prelungite cu doze mari sau in cazul CID (coagulare
intravasculara diseminata).
S-ar putea să vă placă și
- Examen MorfpatDocument61 paginiExamen MorfpatGuțaÎncă nu există evaluări
- Subiecte Morfopat An III Sem IDocument61 paginiSubiecte Morfopat An III Sem IElena-Dana Oprea100% (1)
- MorfopatologieDocument15 paginiMorfopatologieAndra PintilieÎncă nu există evaluări
- Teste - Rezidenti Ati Cu RaspunsuriDocument150 paginiTeste - Rezidenti Ati Cu RaspunsuriPopescu VioricaÎncă nu există evaluări
- Fiziologie SubiecteDocument22 paginiFiziologie SubiecteMareș Ion-AlexandruÎncă nu există evaluări
- PiopneumotoraxDocument17 paginiPiopneumotoraxArtiom MinzateanÎncă nu există evaluări
- Hemostaza Secundara - CoagulareaDocument6 paginiHemostaza Secundara - CoagulareaBogdan NiculaeÎncă nu există evaluări
- Curs 7 FiziopatologieDocument4 paginiCurs 7 FiziopatologieRamonaÎncă nu există evaluări
- ȘoculDocument94 paginiȘoculMihai DumbravanÎncă nu există evaluări
- Hipersensibilitatea Tip IDocument40 paginiHipersensibilitatea Tip IAlina GeanaliuÎncă nu există evaluări
- Fiziopatologia Reactiei Sitemice Postagresive Si A Starilor de SocDocument10 paginiFiziopatologia Reactiei Sitemice Postagresive Si A Starilor de Sockiller9666Încă nu există evaluări
- Chirurgie SemiologieDocument64 paginiChirurgie SemiologieAnna EnachiÎncă nu există evaluări
- 2 Curs Organe HematopoieticeDocument20 pagini2 Curs Organe HematopoieticeBrigitte Si AlinÎncă nu există evaluări
- Colocviu NeuroDocument36 paginiColocviu NeuroMariaBoicuÎncă nu există evaluări
- Virusuri OncogeneDocument37 paginiVirusuri OncogeneNona SimonyanÎncă nu există evaluări
- Familia TogaviridaeDocument3 paginiFamilia TogaviridaeAriela SăvuţÎncă nu există evaluări
- Metabolismul GlucidicDocument48 paginiMetabolismul GlucidicBrinza Olga100% (1)
- Chirurgie - ApendicitaDocument5 paginiChirurgie - ApendicitaTina AcridahÎncă nu există evaluări
- Radiatii CursDocument25 paginiRadiatii CursAndreea BorislavschiÎncă nu există evaluări
- Bun-Curs Si LP3-MG Serie Alba Si TrombocitaraDocument76 paginiBun-Curs Si LP3-MG Serie Alba Si TrombocitaraIonut AftÎncă nu există evaluări
- Indicatii Total.3 FarmaDocument1 paginăIndicatii Total.3 FarmaCristian SîrbuÎncă nu există evaluări
- Insuficienta Hepatica 2015Document119 paginiInsuficienta Hepatica 2015Andra-Elena ObrejaÎncă nu există evaluări
- Sinteza AGDocument71 paginiSinteza AGConstantin UntilaÎncă nu există evaluări
- Preparate AntituberculoaseDocument30 paginiPreparate AntituberculoaseMihaela Procop100% (1)
- Curs 4 ColinolitDocument52 paginiCurs 4 ColinolitRaluca IoanaÎncă nu există evaluări
- Sub Farmaco Sem1 1Document11 paginiSub Farmaco Sem1 1Simona NeculaÎncă nu există evaluări
- Raspunsurile La Farma ClinicaDocument33 paginiRaspunsurile La Farma ClinicaPasha StupelimanÎncă nu există evaluări
- Intrebări Atestarea II Medicina 1Document20 paginiIntrebări Atestarea II Medicina 1M SÎncă nu există evaluări
- Peritonita DifuzaDocument15 paginiPeritonita DifuzaUffie-Isabela Ghe100% (1)
- Afecțiunile Organelor Genitale Feminine - Patologia Sarcinii Şi LăuzieiDocument43 paginiAfecțiunile Organelor Genitale Feminine - Patologia Sarcinii Şi LăuzieiTanyaDonciuÎncă nu există evaluări
- Apendicita Acuta Si CronicaDocument63 paginiApendicita Acuta Si CronicaAndrei LereniuÎncă nu există evaluări
- Aorta Abdominal ADocument1 paginăAorta Abdominal ASavin RamonaÎncă nu există evaluări
- Cardiotonice Chisinau Craiova 2017 Stratu FinalDocument60 paginiCardiotonice Chisinau Craiova 2017 Stratu FinalАня ПрикопÎncă nu există evaluări
- Subiecte Rezolvate Morfopatologie CantacuzinoDocument14 paginiSubiecte Rezolvate Morfopatologie CantacuzinoLuiza BezneaÎncă nu există evaluări
- Celulele PurkinjeDocument2 paginiCelulele PurkinjeAly AlynaÎncă nu există evaluări
- Curs 3 Trunchiul CerebralDocument68 paginiCurs 3 Trunchiul CerebralPetrica Taranu100% (2)
- Leziuni CelulareDocument16 paginiLeziuni CelulareIon TudorÎncă nu există evaluări
- LeucemiaDocument14 paginiLeucemiadan9372100% (1)
- Substante Anestezice Utilizate in Anestezia Loco-RegionalaDocument79 paginiSubstante Anestezice Utilizate in Anestezia Loco-RegionalaLoredana Barbaneagra100% (1)
- 1526279167172322Document60 pagini1526279167172322Razaria DailyneÎncă nu există evaluări
- Sindromul Cavitar - Medicina Interna, Usmf-MdDocument51 paginiSindromul Cavitar - Medicina Interna, Usmf-Mddr_vcÎncă nu există evaluări
- Caragat Supurative-5583Document57 paginiCaragat Supurative-5583AnnitaCristalÎncă nu există evaluări
- Reglarea CardiacDocument70 paginiReglarea CardiacDoina IațîșinÎncă nu există evaluări
- Curs FiziopatDocument85 paginiCurs FiziopatMihai MyoÎncă nu există evaluări
- Anemia FierodeficitaraDocument49 paginiAnemia FierodeficitaraCracea Alexandru100% (1)
- EpinefrinaDocument12 paginiEpinefrinaNadia BadacăÎncă nu există evaluări
- Insuficiența Pulmonară Fiziopatologia Astmului BronșicDocument5 paginiInsuficiența Pulmonară Fiziopatologia Astmului BronșicDamian CojocaruÎncă nu există evaluări
- Astmul Bron?icDocument7 paginiAstmul Bron?icCristian NedÎncă nu există evaluări
- CURS - 03 - 2022 - Fiziopatologia APARATULUI RESPIRATOR - (I) - TXTDocument14 paginiCURS - 03 - 2022 - Fiziopatologia APARATULUI RESPIRATOR - (I) - TXTCosmin PaunÎncă nu există evaluări
- BPOCDocument31 paginiBPOCsilvia_buru50% (2)
- Bronsita AstmDocument29 paginiBronsita AstmCristina DincaÎncă nu există evaluări
- Examenul Terapia TotulDocument25 paginiExamenul Terapia TotulObada AnaÎncă nu există evaluări
- Astmul BRDocument5 paginiAstmul BRGheorghe IstrateÎncă nu există evaluări
- Bronsita AcutaDocument4 paginiBronsita AcutaKamy Roxy0% (1)
- Astm BronsicDocument10 paginiAstm BronsicBianca Loredana Marinescu100% (2)
- Fiziopatologie Curs 6 PDFDocument4 paginiFiziopatologie Curs 6 PDFCosmin BurleanuÎncă nu există evaluări
- Astmul BronsicDocument26 paginiAstmul BronsicAlina Lupsa100% (1)
- DvoDocument9 paginiDvoBabolea Oana BiancaÎncă nu există evaluări
- Astmul BronsicDocument11 paginiAstmul Bronsicmarian_pintilei100% (3)
- AstmDocument15 paginiAstmazerty112001Încă nu există evaluări