Documente Academic
Documente Profesional
Documente Cultură
CursoDra Caturla
Încărcat de
sudaquitaTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
CursoDra Caturla
Încărcat de
sudaquitaDrepturi de autor:
Formate disponibile
OBJETIVO
Capacitar a los asistentes para la aplicacin de las Buenas Prcticas de Laboratorio en los distintos aspectos en los que afecta a la investigacin farmacutica: Desarrollo de proyectos de I+D, estudios preclnicos: farmacolgicos y toxicolgicos, estudios bioanalticos, funcionamiento de una Unidad de Garanta de Calidad, etc
interpretativas de la OCDE. Explicacin de los 10 apartados del Real Decreto de BPL.
de tener presentes el director de estudio y tcnicos. Las Buenas Prcticas de Laboratorio y los sistemas informatizados. Comentario e interpretacin de la monografa 10 de la OCDE sobre el tema.
DIRIGIDO A
Este curso va dirigido a licenciados y profesionales del rea de salud, cuya actividad est o pueda estar sujeta al cumplimiento de las Buenas Prcticas de Laboratorio (BPL).
Auditora de estudios preclnicos, de procesos y de instalaciones. Responsabilidades del personal de garanta de calidad. Fases de una auditora. Auditora de un estudio. Auditora de un informe final. Auditora de procesos. Las Buenas Prcticas de Laboratorio y el cuidado y estabulacin de los animales de experimentacin. El comit tico de experimentacin animal. Marco tico/legal. Aspectos sanitarios. Aspectos derivados del procedimiento experimental. Relacin: personal de animalario-director del estudio-unidad de garanta de calidad. Las Buenas Prcticas de Laboratorio en los estudios de Toxicologa. Tipos de estudios toxicolgicos. Instalaciones. Estabulario. Organizacin y desarrollo de un estudio toxicolgico. Puntos crticos de los procesos que han de tener presentes el director de estudio y tcnicos. Las Buenas Prcticas de Laboratorio en el bioanlisis y la farmacocintica. Tipos de estudios de farmacocintica. Fases de un estudio bioanaltico: desarrollo del mtodo analtico, validacin del mismo y anlisis de muestras. Documentacin: protocolos, informes, registro y archivo de datos originales. Instrumentacin analtica, reactivos, patrones y muestras a analizar. Las Buenas Prcticas de Laboratorio en farmacologa de seguridad. Tipos de estudios de farmacologa de seguridad. ICH S7A sobre safety pharmacology studies for human pharmaceuticals. Organizacin y desarrollo de un estudio de farmacologa. Puntos crticos de los procesos que han
PROFESORADO
M Cruz Caturla Gmez Javier Guillen Jos Luis Montero Llus Guzmn Xavier Sol Carmen Lpez Calull David Lpez Francisca
FORMULARIO DE INSCRIPCIN
Apellidos: Nombre: NIF: . Departamento: Universidad/Centro de trabajo: Puesto de trabajo que ocupa: Direccin: Ciudad: Cdigo Postal: Telfono: . Correo electrnico: DATOS PROFESIONALES: Empresa:
PROGRAMA DEFINITIVO
Las Buenas Prcticas de Laboratorio en la industria farmacutica Actividades de un proyecto de I+D y las normas BPL, NCF y BPC. Evolucin del registro de un nuevo medicamento. Fases en el desarrollo de un medicamento. Tendencias en la I+D farmacutica. Organizacin de I+D; gestin por proyectos, desarrollo biolgico o seguridad preclnica, desarrollo qumico, desarrollo galnico, desarrollo clnico, asuntos regulatorios, garanta de calidad, las normas BPL, NCF, BPC. Historia de las Buenas Prcticas de Laboratorio. Organizacin y desarrollo de un estudio. Origen y desarrollo de las BPL. Normativas existentes. Guas
NIF: Direccin: Cdigo Postal: Telfono: . Es miembro de la SEF? Si/No Para formalizar la matrcula enviar el formulario de inscripcin del curso, debidamente cumplimentada, a la Sociedad Espaola de Farmacologa ANTES DEL 23 DE ABRIL DE 2004. Emitir factura a nombre de: Particular Empresa Transferencia bancaria a: Banco Popular Espaol: c/c: 0075-0227-720600420927.
Web: www.socesfar.com
Horario: hs y
de 10:00 hs a 13.00 de 15.00 hs a 18.00 hs
Con el patrocinio: Lugar:
Auditorio Novartis
C/ Marina 206 Barcelona
Con la colaboracin de:
PRECIO
No socios SEF: 500 Euros Socios SEF: 100 Euros
COORDINADORES DEL CURSO
M Cruz Caturla Xavier Sol
Sociedad Espaola de Farmacologa C/ Arag 312, 4, 5 08009 - Barcelona Tel./Fax: 034-93-4874115 E-mail: socesfar@socesfar.com
ORGANIZACIN
Sociedad Espaola de Farmacologa
Fechas: 3 a 6 de Mayo 2004
Curso buenas prcticas de laboratorio en la industria farmacutica
Barcelona 3-6 de Mayo 2004
S-ar putea să vă placă și
- Material para El Docente. Matematica. Quinto GradoDocument95 paginiMaterial para El Docente. Matematica. Quinto GradoMica Sp100% (1)
- 1 2... ¿Posible?: Segui Los PasosDocument2 pagini1 2... ¿Posible?: Segui Los PasossudaquitaÎncă nu există evaluări
- Hacer Carteles y Títulos: Fácil, Rápido y Bonito. Tutorial Picmonkey - Creative MindlyDocument3 paginiHacer Carteles y Títulos: Fácil, Rápido y Bonito. Tutorial Picmonkey - Creative MindlysudaquitaÎncă nu există evaluări
- Septiembre09 Aguilar Amat Fernandez Margarita3Document10 paginiSeptiembre09 Aguilar Amat Fernandez Margarita3asadasasadasÎncă nu există evaluări
- Reglamento Juego de MenteDocument4 paginiReglamento Juego de Mentesudaquita50% (2)
- Las Matematicas de Tu AlrededorDocument6 paginiLas Matematicas de Tu AlrededorsudaquitaÎncă nu există evaluări
- La Pila Documento en Mac OS X Snow Leopard (Por Apple)Document1 paginăLa Pila Documento en Mac OS X Snow Leopard (Por Apple)Luis Miguel CaballeroÎncă nu există evaluări
- 18 Trucos para Dominar A Tu CuerpoDocument4 pagini18 Trucos para Dominar A Tu CuerposudaquitaÎncă nu există evaluări
- Las 25 reglas de la desinformación políticaDocument7 paginiLas 25 reglas de la desinformación políticasudaquitaÎncă nu există evaluări
- Colecciones Simpsons JACKDocument13 paginiColecciones Simpsons JACKsudaquitaÎncă nu există evaluări
- Lemon pie receta 40cDocument8 paginiLemon pie receta 40csudaquitaÎncă nu există evaluări
- Chistes KDocument26 paginiChistes KsudaquitaÎncă nu există evaluări
- Historia SudafricaDocument15 paginiHistoria SudafricasudaquitaÎncă nu există evaluări
- 10 Mejores PizzasDocument5 pagini10 Mejores PizzassudaquitaÎncă nu există evaluări
- Pequeño Diccionario Burrero IlustradoDocument5 paginiPequeño Diccionario Burrero IlustradosudaquitaÎncă nu există evaluări
- FOT - Aprende A Hacer Mejores Fotos en 31 Días - DZoomDocument209 paginiFOT - Aprende A Hacer Mejores Fotos en 31 Días - DZoomJotape_PhotosÎncă nu există evaluări
- Recetas Con Galletitas LincolnDocument3 paginiRecetas Con Galletitas Lincolnsudaquita100% (1)
- Diccionario FutbolisticoDocument12 paginiDiccionario FutbolisticosudaquitaÎncă nu există evaluări
- 1 Manu GinobiliDocument7 pagini1 Manu GinobilimpetraÎncă nu există evaluări
- 10 Tips para Tomar Un Buen CaféDocument10 pagini10 Tips para Tomar Un Buen CafésudaquitaÎncă nu există evaluări
- La PesteK y La Década de Las Promesas IncumplidasDocument5 paginiLa PesteK y La Década de Las Promesas IncumplidassudaquitaÎncă nu există evaluări
- 09 2014 Servicio para Transmision en Venezuela Programa de ZurdaDocument5 pagini09 2014 Servicio para Transmision en Venezuela Programa de ZurdasudaquitaÎncă nu există evaluări
- Ácidos NucleicosDocument7 paginiÁcidos NucleicossudaquitaÎncă nu există evaluări
- Manual Basico de FotografiaDocument25 paginiManual Basico de FotografiagianpaÎncă nu există evaluări
- Salsas HeladosDocument4 paginiSalsas HeladossudaquitaÎncă nu există evaluări
- Espacios UrbanosDocument3 paginiEspacios UrbanossudaquitaÎncă nu există evaluări
- Las Milanesas PDFDocument7 paginiLas Milanesas PDFsudaquitaÎncă nu există evaluări
- Curso de Cozinha AfrodisiacaDocument84 paginiCurso de Cozinha Afrodisiacajoseolim6536Încă nu există evaluări
- Masa de Hojaldre PDFDocument2 paginiMasa de Hojaldre PDFsudaquitaÎncă nu există evaluări
- Juegos Matemáticos en La EnseñanzaDocument66 paginiJuegos Matemáticos en La EnseñanzasudaquitaÎncă nu există evaluări
- Educación Sexual Integral y Embarazo AdolescenteDocument21 paginiEducación Sexual Integral y Embarazo AdolescentehablasintemorÎncă nu există evaluări
- Matemática Sesion 7 - UNIDAD 1Document6 paginiMatemática Sesion 7 - UNIDAD 1Bruno BeltranÎncă nu există evaluări
- Psicofarmacologia AntidepresivosDocument12 paginiPsicofarmacologia Antidepresivossfdgfhg100% (1)
- Introduccion A La Higiene y Seguridad IndustrialDocument10 paginiIntroduccion A La Higiene y Seguridad IndustrialDaisy AguilarÎncă nu există evaluări
- Farmacología Del Sistema Digestivo 1 - Modulos de FarmaciaDocument12 paginiFarmacología Del Sistema Digestivo 1 - Modulos de FarmaciaMiguel Machaca Flores (QuimioFarma)100% (2)
- Qué Son Las EmocionesDocument7 paginiQué Son Las EmocionesPrevencion Poliestudios100% (3)
- Den - 04B - Sala de Comando Imágenes Dental BDocument2 paginiDen - 04B - Sala de Comando Imágenes Dental BVanessa MorenoÎncă nu există evaluări
- Síntesis de Glucógeno J Grasas y Proteínas J Metabolismo J Calor y Vitaminas HidrosolublesDocument12 paginiSíntesis de Glucógeno J Grasas y Proteínas J Metabolismo J Calor y Vitaminas HidrosolublesHaide BlancoÎncă nu există evaluări
- BTC U2 Atr DiraDocument2 paginiBTC U2 Atr DiradianaÎncă nu există evaluări
- Expectoracion y VomicaDocument4 paginiExpectoracion y Vomicaangelax1.10% (1)
- Historia ClinicaDocument9 paginiHistoria ClinicaShelly Catalina AlmendaresÎncă nu există evaluări
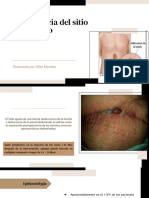
- Dehiscencia Del Sitio QuirurgicoDocument15 paginiDehiscencia Del Sitio QuirurgicoelbamendezÎncă nu există evaluări
- Que Es RadionicaDocument13 paginiQue Es RadionicaJaimeÎncă nu există evaluări
- Documento 1Document2 paginiDocumento 1FRANCK DENIS DELGADO TAFURÎncă nu există evaluări
- Maybe Now (Colleen Hoover)Document362 paginiMaybe Now (Colleen Hoover)Laura Macias63% (8)
- Ensayo Del Tratamiento de AsmaDocument9 paginiEnsayo Del Tratamiento de AsmaCarlos J Estrella CanulÎncă nu există evaluări
- Triptico Endo ColoscopíaDocument2 paginiTriptico Endo Coloscopíajavieratricot0% (1)
- Harina Zootécnica de MaízDocument4 paginiHarina Zootécnica de MaízJordano MoisesÎncă nu există evaluări
- Informacion Complementaria de FloralesDocument84 paginiInformacion Complementaria de Floralesolgaelenacamacho100% (8)
- Simulacro18 2021Document30 paginiSimulacro18 2021Anais SnchzÎncă nu există evaluări
- Guia Practica 02Document8 paginiGuia Practica 02BRISA MARICIELO CONTRERAS COLLAZOSÎncă nu există evaluări
- Google Drive Las Aves Purifican El Aire 1Document10 paginiGoogle Drive Las Aves Purifican El Aire 1api-263248243Încă nu există evaluări
- Estudio CRASH analiza efecto de esteroides en TECDocument2 paginiEstudio CRASH analiza efecto de esteroides en TECmedico1982Încă nu există evaluări
- Recoleccion de Muestras: Heces FecalesDocument16 paginiRecoleccion de Muestras: Heces FecalesLixi Madelin Fernandez RomeroÎncă nu există evaluări
- Enloqueciendo A KurtDocument536 paginiEnloqueciendo A KurtIxia HidalgoÎncă nu există evaluări
- Taller Unidad 1Document3 paginiTaller Unidad 1Ana Maria HernandezÎncă nu există evaluări
- MD-SSIG-001 Equipo de Protección Personal Ed3Document14 paginiMD-SSIG-001 Equipo de Protección Personal Ed3Renzo MaldonadoÎncă nu există evaluări
- Capacidad Operativa - SociocomunitarioDocument2 paginiCapacidad Operativa - SociocomunitarioLuis ManriqueÎncă nu există evaluări
- Salud mental de hombres mayores en Chile: una realidad por priorizarDocument5 paginiSalud mental de hombres mayores en Chile: una realidad por priorizarDaniela Campos HerreraÎncă nu există evaluări
- RCP 150118114939 Conversion Gate02Document39 paginiRCP 150118114939 Conversion Gate02Karem VelezÎncă nu există evaluări