Documente Academic
Documente Profesional
Documente Cultură
04 PH Tau Correction
Încărcat de
Chartier JulienTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
04 PH Tau Correction
Încărcat de
Chartier JulienDrepturi de autor:
Formate disponibile
TS – TP Chimie n°4 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.
org
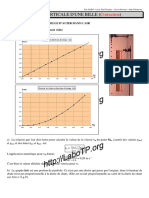
ÉTUDE pH-METRIQUE DU TAUX D'AVANCEMENT FINAL D'UNE REACTION
CORRECTION
I. PREPARATION DE SOLUTIONS ACIDES
1) Equation de la réaction entre l'acide éthanoïque et l'eau: CH3COOH (aq) + H2O (l) = CH3COO- (q) + H3O+ (aq)
Les couples (acide / base) mis en jeu sont:
(CH3COOH (aq) / CH3COO- (aq))
(H3O+(aq) / H2O (l))
2) Mode opératoire pour obtenir, à partir de la solution mère S1 de concentration apportée C1 = 5,0.10-2 mol.L-1, un volume
V2 = 100,0 mL d'une solution fille S2 de concentration apportée C2 = 5,0.10-3 mol.L-1:
• Lors d'une dilution la quantité de matière se conserve: la quantité d'acide éthanoïque dans la solution mère notée n1 est égale à la
quantité d'acide éthanoïque dans la solution fille notée n2:
n1 = n2 ⇔ C1.V1 = C2.V2
donc:
C .V 5,0.10−3 × 100
V1 = 2 2 = = 10 mL
C1 5,0.10−2
• Le matériel à utiliser pour réaliser cette dilution est une pipette jaugée de 10,0 mL munie d'une propipette, une fiole jaugé de
100,0 mL et un bécher pour le prélèvement de la solution mère:
propipette
Eau distillée
Fiole jaugée
Pipette jaugée de volume V2
Volume V1 de la
solution mère
Solution mère: C1, V1 Solution fille: C2, V2
• Protocole expérimental:
- On verse un volume de solution mère S1 (supérieur à V1) dans un bécher de prélèvement.
- On prélève le volume V1 avec la pipette jaugée de 10,0 mL munie de la propipette.
- On place V1 dans une fiole jaugée de volume V2 = 100,0 mL
-On complète la fiole avec de l'eau distillée jusqu'au trait et on agite pour homogénéiser la solution.
II. MESURES DE pH
Solution S2: Solution S1:
C2 = 5,0.10-3 mol.L-1 C1 = 5,0.10-2 mol.L-1
pH lu = 3,24 pH lu = 2,87
pH retenu = 3,2 pH retenu = 2,9
TS – TP Chimie n°4 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.org
Solutions S2 S1
C (mol.L-1) 5,0.10-3 5,0.10-2
pH 3,2 2,9
- logC 2,3 1,3
1) En commençant par la solution la plus concentrée en acide éthanoïque, on limite les erreurs dues à un mauvais rinçage de l'électrode
ayant plongée dans une solution plus concentrée que celle étudiée.
2) On constate que pH est différent de – logC. Le tableau montre que pH > – logC pour les deux solutions.
III. TRANSFORMATION TOTALE ?
1) La transformation est supposée totale:
• On considère un volume VS de la solution S1 de concentration apportée C1. La quantité d'acide apportée est: n1 = C1.VS.
CH3COOH (aq) + H 2O = CH3COO -
(aq) + H3O+ (aq)
EI n1 = C1 × VS excès 0 0
En cours n1 - x excès x x
EF n1 - xmax excès xmax xmax
2) Le réactif limitant est CH COOH car l'eau est le solvant donc:
3 xmax = n1 = C1 × VS
Or on a aussi: xmax = nmax(H3O+) = [H3O+] .VS
En égalant les deux expressions de xmax il vient: C1 ⋅ VS = [H3O+] .VS Finalement: C1 = [H3O+]
3) On a: C1 = [H3O+] ⇔ log C1 = log [H3O+] ⇔ - log C1 = - log[H3O+]
Finalement: pH = - log C1
4) Expérimentalement nous avons obtenu: pH > -log C1 (soit C1 > [H3O+] ) .
On en conclut que la réaction entre l'acide éthanoïque et l'eau est une transformation non totale soit limitée.
IV. TAUX D'AVANCEMENT FINAL τ
1) Influence de la concentration apportée en acide éthanoïque
a) Pour VS = 100 mL des 2 solutions, la valeur de xmax en mmol est: xmax,i = nmax,i(H3O+) = Ci × VS
Pour S1: xmax = 5,0.10–2 × 100,0.10-3 = 5,0.10-3 mol = 5,0 mmol
Pour S2: xmax = 5,0.10–3 × 100,0.10-3 = 5,0.10-4 mol = 0,50 mmol
b) La transformation étant limitée, dans l'état final x = xf:
CH3COOH (aq) + H 2O = CH3COO -
(aq) + H3O+ (aq)
EI ni = Ci.VS excès 0 0
En cours ni - x excès x x
EF ni - xf excès xf xf
Avec i =1,2.
La réaction étant limitée dans le sens direct on a: xf,i < xmax,i
c) On a: x = n (H3O+) = [H3O+]i ⋅ Vi = 10 ⋅ Vi
f,i f,i
– pHi
Pour S1: xf = 10 – 2,9 × 100,0.10-3 = 1,3.10 mol = 1,3.10-1 mmol
-4
Pour S2: xf = 10 – 3,2
× 100,0.10 = 6,3.10 mol = 6,3.10-2 mmol
-3 -5
TS – TP Chimie n°4 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.org
Solutions S2 S1
C (mol.L-1) 5,0.10-3 5,0.10-2
xmax (mmol) 5,0.10-1 5,0
xf (mmol) 6,3.10-2 1,3.10-1
τ (%) 13 2,6
xf
d) Le taux d'avancement final τ est: τ =
x max
Pour S1: τ = 1,3.10-1 / 5,0 = 0,026 = 2,6 %
Pour S2: τ = 6,3.10-2 / 5,0.10-1 = 0,13 = 13 %
e) On constate que pour C1 > C2 on a: τ1 < τ2.
Plus la concentration apportée de la solution est grande plus le taux d'avancement est petit.
Ainsi la dilution d'une solution d'acide éthanoïque favorise la dissociation de l'acide.
Lors de la dilution, on ajoute de l'eau: le système réagit en éliminant le réactif que l'on ajoute. L'équilibre est alors déplacé dans le sens
direct.
2) Influence de la nature de l'acide
• On dispose:
- d'une solution S2 d'acide éthanoïque CH3COOH de concentration apportée: C2 = 5,0 × 10-3 mol.L-1
- d'une solution S4 d'acide méthanoïque HCOOH de concentration apportée: C4 = 5,0 × 10-3 mol.L-1
- d'une solution S5 de chlorure d'ammonium (NH4+, Cl- ) de concentration apportée: C5 = 5,0 × 10-3 mol.L-1.
Solution S2: Solution S4: Solution S5:
C2 = 5,0.10-3 mol.L-1 C4 = 5,0.10-3 mol.L-1 C5 = 5,0.10-3 mol.L-1
pH lu = 3,24 pH lu = 2,94 pH lu = 5,32
pH retenu = 3,2 pH retenu = 2,9 pH retenu = 5,3
Solutions S2 S4 S5
C (mol.L-1) 5,0.10-3 5,0.10-3 5,0.10-3
pH 3,2 2,9 5,3
xmax (mmol) 5,0.10-1 5,0.10-1 5,0.10-1
xf (mmol) 6,3.10-2 1,3.10-2 5,0.10-4
τ (%) 13 26 0,10
a) Equations des réactions des acides avec l'eau:
HCOOH (aq) + H2O = HCOO- (aq) + H3O+ (aq)
Couples: (HCOOH (aq) / HCOO- (aq) )
(H3O+ (aq) / H2O)
NH4+ (aq) + H2O = NH3 (aq) + H3O+ (aq)
Couples: (NH4+ (aq) / NH3 (aq))
(H3O+ (aq) / H2O)
TS – TP Chimie n°4 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.org
b) Taux d'avancement final pour VS = 100 mL de solution:
On a: xf,i = nf,i(H3O+) = [H3O+]i × VS = 10 – pHi × VS
Pour S2 xf = 10 – 3,2 × 100,0.10-3 = 6,3.10-5 mol = 6,3.10-2 mmol
Pour S4: xf = 10 – 2,9 × 100,0 × 10-3 = 1,3.10 mol = 1,3.10-2 mmol
-4
× 100,0 × 10 = 5,0.10 mol = 5,0.10 mmol
– 5,3 -3 -7 -4
Pour S5: xf = 10
Pour S2: τ2 = 6,3.10-2 / 5,0.10-1 = 0,13 = 13 %
Pour S4: τ4 = 1,3.10-1 / 5,0.10-1 = 0,50 = 26 %
Pour S5: τ5 = 5,0.10 / 5,0.10-1 = 0,001 = 0,10 %
-4
c) Le taux d'avancement final dépend donc de la nature de l'acide.
d) A concentration apportée égale, l'acide le plus dissocié dans l'eau est l'acide méthanoïque.
S-ar putea să vă placă și
- Résumé - La Puissance de Votre SubconscientDocument7 paginiRésumé - La Puissance de Votre SubconscientBoussad Nait MessaoudÎncă nu există evaluări
- 07 - Titrage Colorimetrique Deboucheur CorDocument2 pagini07 - Titrage Colorimetrique Deboucheur CorChartier JulienÎncă nu există evaluări
- 04 Charge Condensateur CorrectionDocument4 pagini04 Charge Condensateur CorrectionChartier Julien100% (1)
- 07 - Titrage PH VinaigreDocument3 pagini07 - Titrage PH VinaigreChartier Julien50% (2)
- 08 Loi Newton CorrectionDocument4 pagini08 Loi Newton CorrectionChartier JulienÎncă nu există evaluări
- Titrage ConductimétriqueDocument3 paginiTitrage Conductimétriquekarimzid100% (1)
- 11 Pendule Simple CorrectionDocument2 pagini11 Pendule Simple CorrectionChartier Julien87% (23)
- 12 Pendule Elastique CorrectionDocument2 pagini12 Pendule Elastique CorrectionChartier Julien90% (10)
- ch13 Separation Extraction BenzocaineDocument3 paginich13 Separation Extraction Benzocaineالغزيزال الحسن EL GHZIZAL HassaneÎncă nu există evaluări
- 11 Ester CorrectionDocument7 pagini11 Ester CorrectionChartier Julien100% (2)
- 07 RLC CorrectionDocument5 pagini07 RLC CorrectionChartier JulienÎncă nu există evaluări
- TP2 de ChimieDocument2 paginiTP2 de Chimiemohammed el amineÎncă nu există evaluări
- 09 Chute CorrectionDocument3 pagini09 Chute CorrectionChartier Julien100% (3)
- DS 1 CorrigéDocument3 paginiDS 1 CorrigéFethi BorsaliÎncă nu există evaluări
- Applications de la spectrophotomérie en phytochimie: sciencesDe la EverandApplications de la spectrophotomérie en phytochimie: sciencesÎncă nu există evaluări
- 01 Transf Dos CorDocument5 pagini01 Transf Dos CorChartier JulienÎncă nu există evaluări
- 06 BBT CorrectionDocument4 pagini06 BBT CorrectionChartier JulienÎncă nu există evaluări
- 03 Suivi Spectro CorDocument5 pagini03 Suivi Spectro CorChartier JulienÎncă nu există evaluări
- Chimie-TP6 Dosage D'un Produit CommercialDocument3 paginiChimie-TP6 Dosage D'un Produit CommercialChartier JulienÎncă nu există evaluări
- 05 ConductDocument3 pagini05 ConductChartier JulienÎncă nu există evaluări
- Dosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)Document4 paginiDosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)theobromine100% (5)
- Chimie-TP4 Determination de Qr-CorrDocument3 paginiChimie-TP4 Determination de Qr-CorrChartier Julien100% (1)
- Chapitre 1,2,3,4,5,6,7,8,9,....Document37 paginiChapitre 1,2,3,4,5,6,7,8,9,....Arfa BouchtaÎncă nu există evaluări
- TP ch4 Titrage PhmetriqueDocument2 paginiTP ch4 Titrage PhmetriquebounegabÎncă nu există evaluări
- P2016 CM11 TP FasciculeDocument44 paginiP2016 CM11 TP FasciculeRochdi BAATIÎncă nu există evaluări
- Des Définitions: TP N1: Préparation D'une Solution D'acide Faible, L'acide OxaliqueDocument3 paginiDes Définitions: TP N1: Préparation D'une Solution D'acide Faible, L'acide Oxaliquesidi mohamed el amine nekkalÎncă nu există evaluări
- Chimie B Chap8 Titrage AcidobasiqueDocument6 paginiChimie B Chap8 Titrage AcidobasiqueSamantha Farah100% (1)
- 1059 TP Doser Par ConductimetrieDocument3 pagini1059 TP Doser Par ConductimetrieAli TrikiÎncă nu există evaluări
- Titrage AbDocument3 paginiTitrage AbLahcen N'ait AliÎncă nu există evaluări
- TP Chimie Analytique Et Instrumentale Manip1 FinalDocument16 paginiTP Chimie Analytique Et Instrumentale Manip1 FinalHamed AbbassiÎncă nu există evaluări
- Bilan TPO - 02Document12 paginiBilan TPO - 02Simona StefanÎncă nu există evaluări
- Lec 15 Les PHDocument12 paginiLec 15 Les PHPierreEustacheÎncă nu există evaluări
- TP Chimie n1Document2 paginiTP Chimie n1Oussoufi Mze Kaanbi100% (2)
- Chimie-TP1 Facteurs CinetiquesDocument1 paginăChimie-TP1 Facteurs CinetiquesChartier JulienÎncă nu există evaluări
- Correction de La Chimie Du Bac Blan PC & SMDocument5 paginiCorrection de La Chimie Du Bac Blan PC & SMMouhibi AbdellahÎncă nu există evaluări
- Devoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Document3 paginiDevoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Moufida ZouaghiÎncă nu există evaluări
- 5 - Chap5-Dosages Et Calcul D'incertitude - Mode de Compatibilité PDFDocument63 pagini5 - Chap5-Dosages Et Calcul D'incertitude - Mode de Compatibilité PDFoulaiÎncă nu există evaluări
- PS CMM b3 TP Dosage Du Diiode Dans La BetadineDocument7 paginiPS CMM b3 TP Dosage Du Diiode Dans La BetadinemranonimosÎncă nu există evaluări
- Eau - Oxygenee. .Copie 1Document1 paginăEau - Oxygenee. .Copie 1fatimazahraÎncă nu există evaluări
- TP-PH-métrie ElectrochimieDocument14 paginiTP-PH-métrie ElectrochimieAya DgmÎncă nu există evaluări
- Cinetique 01Document3 paginiCinetique 01badreÎncă nu există evaluări
- TP .Avancement .4sc - Exp.2022Document6 paginiTP .Avancement .4sc - Exp.2022Med Brini100% (1)
- Cinétique ChimiqueDocument10 paginiCinétique Chimiquearfpower100% (2)
- Compte Rendu 1Document11 paginiCompte Rendu 1hadil100% (1)
- Methode de MohrDocument9 paginiMethode de MohrMoed MoedÎncă nu există evaluări
- TP N 3 Chimie Sem1 2022 Sujet IodometrieDocument4 paginiTP N 3 Chimie Sem1 2022 Sujet IodometrieRaouf RamoulÎncă nu există evaluări
- C03 Cinetique ReactionDocument2 paginiC03 Cinetique ReactionmohÎncă nu există evaluări
- TP SM24 2011-2012Document35 paginiTP SM24 2011-2012HichamLahbilÎncă nu există evaluări
- TP ÉlectroDocument18 paginiTP ÉlectroBichou HomÎncă nu există evaluări
- 2008 TP EXAO BacPro Dosage VinaigreDocument5 pagini2008 TP EXAO BacPro Dosage VinaigremohÎncă nu există evaluări
- Corrige TPchim8 Titrage Indirect 2009Document3 paginiCorrige TPchim8 Titrage Indirect 2009Kouki RkaÎncă nu există evaluări
- Chimie TP2 Dosage CorrDocument3 paginiChimie TP2 Dosage CorrChartier JulienÎncă nu există evaluări
- Ch06 SolutionsDocument46 paginiCh06 SolutionsMateus SantosÎncă nu există evaluări
- TP2 PH Métrie 2022-2023Document6 paginiTP2 PH Métrie 2022-2023abderrahmane lalaouiÎncă nu există evaluări
- TP 05 Determination Du Degre Chlorometrique (Oxydo-Réduction)Document6 paginiTP 05 Determination Du Degre Chlorometrique (Oxydo-Réduction)Moume AmiraÎncă nu există evaluări
- Correction To CinetiqueDocument5 paginiCorrection To CinetiquejaywalkÎncă nu există evaluări
- Conductim PDFDocument4 paginiConductim PDFMokhtarBensaidÎncă nu există evaluări
- TP PH Metre ATHIR - New1Document8 paginiTP PH Metre ATHIR - New1samibenhabileÎncă nu există evaluări
- TitrageDocument3 paginiTitrageelhijaziyoussefÎncă nu există evaluări
- Chap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFDocument2 paginiChap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFYouSsef EchafaiÎncă nu există evaluări
- TPchim3 Cinetique SaponificationDocument3 paginiTPchim3 Cinetique SaponificationKESSAB MOHAMEDÎncă nu există evaluări
- Site TS C 12 CatalyseDocument3 paginiSite TS C 12 CatalysePecorellaÎncă nu există evaluări
- PS CMM b1 TP Dosage Du Diiode Dans La Betadine Version Sans DilutionDocument7 paginiPS CMM b1 TP Dosage Du Diiode Dans La Betadine Version Sans DilutionmranonimosÎncă nu există evaluări
- Manipulation 355Document7 paginiManipulation 355oulahnoud boubakerÎncă nu există evaluări
- 2008 Polynesie Exo1 Correction Acides 7ptsDocument3 pagini2008 Polynesie Exo1 Correction Acides 7ptsla physique selon le programme FrançaisÎncă nu există evaluări
- C3Chim - Transformations - Limitees - Exercices - Sabatier PDFDocument5 paginiC3Chim - Transformations - Limitees - Exercices - Sabatier PDFAzizElheni0% (1)
- QCM - Medecine ChimieMr SABOUR 2023Document9 paginiQCM - Medecine ChimieMr SABOUR 2023SABOUR MOHAMMEDÎncă nu există evaluări
- Chimie-TP4 Determination de Qr-CorrDocument3 paginiChimie-TP4 Determination de Qr-CorrChartier Julien100% (1)
- 11 Pendule SimpleDocument2 pagini11 Pendule SimpleChartier Julien100% (5)
- Chimie-TP6 Dosage D'un Produit CommercialDocument3 paginiChimie-TP6 Dosage D'un Produit CommercialChartier JulienÎncă nu există evaluări
- Chimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeDocument2 paginiChimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeChartier Julien100% (1)
- 10 Euler CorrectionDocument5 pagini10 Euler CorrectionChartier JulienÎncă nu există evaluări
- 14 RadioactivitéDocument2 pagini14 RadioactivitéChartier Julien100% (1)
- Chimie-TP3 Mesure Du PH de SolutionsDocument2 paginiChimie-TP3 Mesure Du PH de SolutionsChartier JulienÎncă nu există evaluări
- Chimie-TP4 Determination de QRDocument2 paginiChimie-TP4 Determination de QRChartier JulienÎncă nu există evaluări
- Chimie-TP3 Mesure Du PH de Solutions-CorrDocument2 paginiChimie-TP3 Mesure Du PH de Solutions-CorrChartier JulienÎncă nu există evaluări
- 13 Etude Dynamique Energetique Ressort CorDocument7 pagini13 Etude Dynamique Energetique Ressort CorChartier JulienÎncă nu există evaluări
- Chimie TP1 Facteurs Cinetiques CorrDocument1 paginăChimie TP1 Facteurs Cinetiques CorrChartier Julien100% (1)
- 10 EulerDocument3 pagini10 EulerChartier JulienÎncă nu există evaluări
- Chimie TP2 Dosage CorrDocument3 paginiChimie TP2 Dosage CorrChartier JulienÎncă nu există evaluări
- Chimie-TP1 Facteurs CinetiquesDocument1 paginăChimie-TP1 Facteurs CinetiquesChartier JulienÎncă nu există evaluări
- 12 Pendule ElastiqueDocument2 pagini12 Pendule ElastiqueChartier JulienÎncă nu există evaluări
- 08 Loi NewtonDocument4 pagini08 Loi NewtonChartier JulienÎncă nu există evaluări
- 07 RLCDocument5 pagini07 RLCChartier JulienÎncă nu există evaluări
- 09 ChuteDocument4 pagini09 ChuteChartier Julien100% (2)
- 06 RL CorrectionDocument6 pagini06 RL CorrectionChartier JulienÎncă nu există evaluări
- 05 RC CorrectionDocument5 pagini05 RC CorrectionChartier JulienÎncă nu există evaluări
- 06 RLDocument4 pagini06 RLChartier JulienÎncă nu există evaluări
- 04 Charge CondensateurDocument4 pagini04 Charge CondensateurChartier JulienÎncă nu există evaluări
- 04 Charge CondensateurDocument4 pagini04 Charge CondensateurChartier JulienÎncă nu există evaluări
- 03 Ondes Lunmineuses CorrectionDocument2 pagini03 Ondes Lunmineuses CorrectionChartier JulienÎncă nu există evaluări
- Fy23 Electromenager Hfb07 r2 118-BdDocument59 paginiFy23 Electromenager Hfb07 r2 118-Bds.alahcen76Încă nu există evaluări
- Fiche Installer Une PDocument9 paginiFiche Installer Une PBelez LezbeÎncă nu există evaluări
- Bellissant CV CS 2015Document61 paginiBellissant CV CS 2015Zoubir DerbouzÎncă nu există evaluări
- CORRECTIONS-3 DS Environnement D'un Objet Technique 2018 - 19-794796Document2 paginiCORRECTIONS-3 DS Environnement D'un Objet Technique 2018 - 19-794796Cyprien BrabantÎncă nu există evaluări
- Dossier Informatique CommercialeDocument13 paginiDossier Informatique CommercialeAdn NiivÎncă nu există evaluări
- Exercices Pratiques de PrononciationDocument3 paginiExercices Pratiques de PrononciationFranc AntoineÎncă nu există evaluări
- Document Technique D'application 5.2/17-2581 - V1: Sika Protection Fondation Et DrainageDocument16 paginiDocument Technique D'application 5.2/17-2581 - V1: Sika Protection Fondation Et DrainageLuis DuarteÎncă nu există evaluări
- Pnds Epilepies Neonatales Texte IntegralDocument51 paginiPnds Epilepies Neonatales Texte IntegralHAKIMOPÎncă nu există evaluări
- (1904) Petit Dictionnaire Annamite - Français - P. VallotDocument296 pagini(1904) Petit Dictionnaire Annamite - Français - P. Vallotnvh92Încă nu există evaluări
- Semaine Menu 2604Document21 paginiSemaine Menu 2604Coste AngelaÎncă nu există evaluări
- Leçon Vocabulaire 12 - Fiche ÉlèveDocument4 paginiLeçon Vocabulaire 12 - Fiche ÉlèveMaynardÎncă nu există evaluări
- CoursDocument16 paginiCoursrchid100% (1)
- DUT Chapitre VI Tri PPDocument17 paginiDUT Chapitre VI Tri PPFall DjibrilÎncă nu există evaluări
- EL ALLAM Ayad TCSDocument70 paginiEL ALLAM Ayad TCSKhalid OualiÎncă nu există evaluări
- Cofrastra 40Document16 paginiCofrastra 40Eduar BrionesÎncă nu există evaluări
- Td5 Lois Statistique Loi BinomialeDocument12 paginiTd5 Lois Statistique Loi BinomialeAyoub HwitéÎncă nu există evaluări
- Regime Neutre PresDocument61 paginiRegime Neutre PresHadja Savané100% (1)
- Sujet Sciences Brevet Pro 2018Document7 paginiSujet Sciences Brevet Pro 2018Petits talents symphoniques du Nord PTSNÎncă nu există evaluări
- 17 - Part-2 Chapitre-5 Lecon-2 Quelle Sont Les Processus Qui Conduisent A La DevianceDocument5 pagini17 - Part-2 Chapitre-5 Lecon-2 Quelle Sont Les Processus Qui Conduisent A La DevianceIsrael DjegueÎncă nu există evaluări
- 014 Ex 009 Certificat MedicauxDocument6 pagini014 Ex 009 Certificat MedicauxbrgÎncă nu există evaluări
- Mots Et Phrases Pour Voyageurs en SwahiliDocument6 paginiMots Et Phrases Pour Voyageurs en Swahilibruno stephanÎncă nu există evaluări
- Brvet 2021 AnnaleDocument6 paginiBrvet 2021 AnnaleYacine MessaouiÎncă nu există evaluări
- Le Fait SocialDocument4 paginiLe Fait Socialhayatmahi42Încă nu există evaluări
- PEMEDCI COMOE 2. Note de Synth Se VDEFDocument69 paginiPEMEDCI COMOE 2. Note de Synth Se VDEFKouadjoÎncă nu există evaluări
- Chap 1Document15 paginiChap 1Anonymous f5yW3N0jSÎncă nu există evaluări
- PRC5333ADocument2 paginiPRC5333AChaimaeÎncă nu există evaluări
- Catalogue Des FormationsDocument11 paginiCatalogue Des FormationsStro Maé0% (1)
- KPMG Guide AssurancesDocument140 paginiKPMG Guide AssurancesaissanisÎncă nu există evaluări
- Study On Palm Oil Production: The Genus TeneraDocument96 paginiStudy On Palm Oil Production: The Genus TeneraFerdinand NoukweÎncă nu există evaluări