Documente Academic
Documente Profesional
Documente Cultură
Alcani - Exercitii Rezolvate
Încărcat de
Stefan SerbTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Alcani - Exercitii Rezolvate
Încărcat de
Stefan SerbDrepturi de autor:
Formate disponibile
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
EXERCIII I PROBLEME
*****************************************************************************
*****************************************************************************
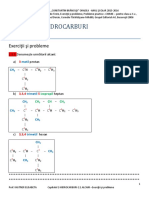
2.1.1.Denumete urmtorii alcani:
a) 3 metil pentan
CH3 C3H C4H2 C5H3
C2H2
C1H3
b) 3,3,4 trimetil 5 izopropil heptan
CH3
CH3 CH CH3
CH3
C H C H C6H2 C7H3
c)
C H2
CH3
1
C H3
3,3,4 trimetil hexan
CH3
C H2 C H
6
C H3
CH3
C3
CH3
C H2
C1H3
1
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
*****************************************************************************
*****************************************************************************
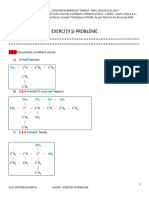
2.1.2. Se dau urmtorii izoalcani:
a) 3 -metil pentan
CH3 C3H C4H2 C5H3
C2H2
C1H3
b) 2,2-dimetil propan
CH3
C H3
C2
C3H3
CH3
c) 2-metil butan
C3H2 C2H C1H3
C H3
CH3
d) 2-metil pentan
C5H3 C4H2 C3H2 C2H C1H3
CH3
2
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
e) 2,3- dimetil butan
C1H3 C2H C3H C4H3
CH3
CH3
Denumete cei 5 izoalcani i precizeaz care sunt izomeri i care sunt omologi.
Izomeri: a, d i e.
Izomeri: b i c.
Omologi: c i d.
*****************************************************************************
*****************************************************************************
2.1.3.Scrie formulele de structur i denumete conform IUPAC urmtorii izoalcani:
a) 2 etil butan;
C1H3 C2H C3H2 C4H3
CH2
CH3
Denumire incorect. Nu s-a numerotat catena cea mai lung.
Rezolvare:
a) 3 -metil pentan (denumirea conform IUPAC)
3
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
CH3 C3H C4H2 C5H3
C H2
C1H3
============================================================================
b) 1,2,2 trimetil propan;
CH3
C H2
C2
CH3
CH3
C3H3
Denumire incorect. Nu s-a numerotat catena cea mai lung.
Rezolvare:
b) 2,2 -dimetil butan (denumirea conform IUPAC)
CH3
C H2
C H3
C2
C1H3
CH3
===========================================================================
c) 2,3-dietil-4-metil pentan;
4
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
C1H3 C2H C3H C4H C5H3
CH2
CH3
CH2
CH3
CH3
Denumire incorect. Nu s-a numerotat catena cea mai lung.
Rezolvare:
c) 2,4 dimetil- 3-etil hexan (denumirea conform IUPAC)
CH3 C4H C3H C2H C1H3
C5H2
C6H3
CH2
CH3
CH3
============================================================================
d) 3-izopropil pentan.
C5H3 C4H2 C3H C2H2 C1H3
CH3
CH
CH3
Rezolvare:
d) 2 metil- 3-etil pentan (denumirea conform IUPAC)
5
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
CH3 CH2 C3H C4H2 C5H3
CH3 C H
1
C H3
*****************************************************************************
*****************************************************************************
2.1.4. Se supun clorurrii fotochimice 6 moli de metan. tiind c n amestecul final de reacie
se afl monoclormetan, diclormetan i triclormetan n raport molar de 2 : 2 : 1, iar cu acidul
clorhidric obinut se pot prepara 9 l soluie de HCl de concentraie 1M, se cere:
a) scrie ecuaiile reaciilor chimice care au loc;
b) calculeaz procentul de metan rmas nereacionat;
c) calculeaz masa de monoclormetan obinut.
Rezolvare:
CH3Cl : CH2Cl2 : CHCl3 = 2 : 2 : 1 raport molar
CH3Cl : CH2Cl2 : CHCl3 = 2x : 2x : x raport molar
2x moli
CH4
2x moli
metan
1 mol
Cl2
clor
2x moli
CH4
metan
1 mol
2Cl2
clor
CH3Cl
2x moli
HCl
monoclormetan
1 mol
acid clorhidric
1 mol
2x moli
4x moli
CH2Cl2
diclormetan
1 mol
2HCl
acid clorhidric
2 mol
6
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
x moli
CH4
x moli
metan
1 mol
3Cl2
CHCl3
clor
3x moli
3HCl
diclormetan
1 mol
acid clorhidric
3 mol
(6-5x) moli
(6-5x) moli
CH4
metan
1 mol
CH4
metan nereacionat
1 mol
9 l soluie de HCl de concentraie 1M conin 9 moli de HCl.
2x +4x + 3x = 9
x = 1 mol
CH4 nereacionat este 6- 5x = 1 mol CH4
6 moli CH4 ..1 mol CH4 nereacionat
100 moli CH4 .% CH4 nereacionat
% CH4 nereacionat = (100*1)/6 = 16,66 % CH4 nereacionat
MCH3Cl = 12+3+35,5 = 50,5 g /mol
1 mol CH3Cl..50,5 g
2 moli CH3Clm g
m = (2*60,5)/1 = 101 g CH3Cl.
*******************************************************************
*******************************************************************
2.1.5. n urma bromurrii fotochimice a etanului se obine un compus care conine 85,1 % Br.
Determin formula molecular a compusului bromurat obinut i scrie formulele de structur
ale substanelor izomere care au formula molecular determinat.
7
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Rezolvare:
C2H6
etan
xBr2
C2H6-xBrx
brom
xHBr
acid bromhidric
MC2H6-xBrx = 2*12 +(6 x) + x*80 = (30 + 79x) g /mol
(30 + 79x) g compus bromurat..80x g Br
100 g compus bromurat85,1 % Br
80x*100 = (30 + 79x)*85,1
8000x = 30*85,1 + 79x*85,1
x(8000 - 6723) =2553
1277x = 2553
x=2
Formula molecular: C2H6-xBrx unde l nlocuim pe x i obinem
C2H4Br2
Izomeri:
1,2-dibromoetan
C1H2 C2H2
Br
Br
1,1-dibromoetan
Br
C2H3 C1H
8
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Br
*****************************************************************************
*****************************************************************************
2.1.6. Un amestec de monoclorometan i diclorometan conine 76,344 % Cl. Determin
raportul molar n care se gsesc cei doi derivai clorurai n amestec.
Rezolvare:
CH3Cl : CH2Cl2 = x : 1
raport molar
Calculm masa amestecului:
MCH3Cl = 12+ 3 + 35,5 = 50,5 g /mol;
MCH2Cl2 = 12 + 2 + 71 = 85 g / mol;
masa amestecului = (50,5x + 85) g amestec
(50,5x + 85) g amestec..(35,5x +71) g Cl
100 g amestec.76,344 g Cl
(50,5x + 85)*76,344 = 100*(35,5x + 71)
50,5x*76,344 -100*35,5x = 100*71 85*76,344
3855x -3550x = 7100 6489
305x = 611
x=2
CH3Cl : CH2Cl2 = x : 1
raport molar
CH3Cl : CH2Cl2 = 2 : 1
raport molar
9
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
*****************************************************************************
*****************************************************************************
2.1.7. Se ard 4 moli de propan. Se cere:
a) Scrie ecuaia reaciei chimice de ardere a propanului;
b) Calculeaz volumul de aer, msurat n condiii normale, necesar arderii;
c) Calculeaz masa de CO2 degajat din reacie.
Rezolvare:
4 moli
C3H8
xl
propan
1 mol
5O2
oxigen
5*22,4 l
yg
3CO2
dioxid de carbon
3*44 g
4H2O
ap
x = (4*5*22,4) / 1 = 448 l O2
Calculm volumul de aer cu 20 % O2 :
100 l aer..20 l O280 l N2
Vaer ..448 l O2(Vaer 448) l N2
Vaer = (448*100) / 20 =2240 l aer 20 % O2
MCO2 = 12 + 16*2 = 44 g / mol;
y = (4*3*44) / 1 = 528 g CO2.
*****************************************************************************
*****************************************************************************
2.1.8. 9,2 kg amestec echimolecular de metan i etan este supus arderii cu o cantitate
stoechiometric de oxigen. Calculeaz volumul de oxigen msurat la 25 0C, necesar arderii
amestecului. Care este compoziia procentual, n procente molare i n procente masice, a
amestecului supus arderii?
10
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Rezolvare:
Calculm numrul de moli de metan, respectiv etan din amestecul dat:
x = nr. de moli de CH4;
x = nr. de moli de C2H6.
MCH4 = 12 + 4 = 16 g / mol;
MC2H6 = 2*12 + 6 = 30 g / mol.
9,2 kg amestec = 9200 g amestec
16x + 30x = 9200
46x = 9200
x = 200 moli de CH4
x = 200 moli de C2H6.
200 moli
CH4
xl
2O2
metan
1 mol
oxigen
2*22,4 l
200 moli
yl
C2H6
etan
1 mol
7/2O2
oxigen
(7/2)*22,4 l
CO2
dioxid de carbon
2CO2
dioxid de carbon
2H2O
ap
3H2O
ap
x = (200*2*22,4) /1 = 8960 l O2;
y = (200*3,5*22,4) /1 = 15680 l O2;
11
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
V0 = 8960 + 15680 = 24640 l O2;
0
T = t + 273
unde t = 25 C.
V0 / T0 = V / T
unde T0 = 273 0K iar T = 25 + 273 = 298 0K.
V = (24640*298)/273 = 26896 l O2.
400 moli amestec.200 moli metan..200 moli etan
100 moli amestec% moli metan% moli etan
% moli metan = 50 %;
% moli etan = 50 %.
9200 g amestec.200*16 g metan..200*30 g etan
100 g amestec % masic metan.% masic etan
% masic metan = (100*3200)/9200 = 34,78 %
% masic etan = (100*6000)/9200 = 65,22 %.
*****************************************************************************
*****************************************************************************
2.1.9. Prin arderea 1 g de alcan necunoscut se degaj n condiii normale, 1,568 l CO2.
Determin formula molecular a alcanului necunoscut i scrie formulele de structur pentru
toi izomerii alcanului determinat.
Rezolvare:
1g
CnH2n+2
1.568 l
alcan
(14n+2) g
(3n+1)/2O2
oxigen
nCO2
dioxid de carbon
n*22.4 l
(n+1)H2O
ap
12
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
MCnH2n+2 = n*12 + 2n +2 = (14n +2) g / mol.
22,4n = (14n+2)*1.568
22,4n = 14n*1.568 + 2*1.568
22,4n 21.952n = 3,136
0,448n = 3,136
n=7
deci C7H16
heptan
H3C1 C2H2-C3H2-C4H2-C5H2-C6H2-C7H3
n heptan
3 metil hexan
C1H3 C2H2 C3H C4H2 C5H2
C6H3
CH3
2 metil hexan
C1H3 C2H
C3H2 C4H2 C5H2 C6H3
CH3
CH3
C H3 C2
C3H2 C4H2 C5H3
CH3
2,2 dimetil pentan
13
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
C1H3 C2H C3H
CH3
CH3
C4H2 C5H3
2,3 dimetil pentan
C1H3 C2H C3H2 C4H
CH3
CH3
C5H3
2,4 dimetil pentan
CH3
C H3 C H2 C3
C4H2 C5H3
CH3
3,3 dimetil pentan
C1H3 C2H2 C3H C4H2 C5H3
CH2
CH3
3 etil pentan
14
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
CH3
C1H3 C2
C3H C4H3
CH3
CH3
2,2,3 trimetil butan
************************************************************
************************************************************
2.1.10. Un alcan A, are densitatea n raport cu aerul egal cu 2.01. Determin alcanul A,
denumete izomerii acestuia i scrie formulele de structur pentru toi derivaii diclorurai
care se pot obine din alcanul A.
MCnH2n+2 = n*12 + 2n +2 = (14n +2) g / mol.
daer =
MCnH2n+2
/Maer
Maer = 28,9 g/mol
14n + 2 = 28,9*2,01
14n + 2 = 58
14n = 56
n = 4 deci
C4H10 butan
C1H3 C2H2 C3H2 C4H3
n butan
15
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
C1H3 C2H
C3H3
CH3
2 metil propan sau izobutan
Cl
C1H
C2H2 C3H2 C4H3
Cl
1,1 diclor butan
Cl
2
C H3 C
1
C3H2 C4H3
Cl
2,2 diclor butan
2
C1H2 C H
Cl
Cl
C3H2 C4H3
1,2 diclor butan
2
3
C1H2 C H2 C H
Cl
Cl
C4H3
1,3 diclor butan
16
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
2
3
4
C1H2 C H2 C H2 C H3
Cl
Cl
1,4 diclor butan
2
C1H3 C H
C3H
Cl
Cl
C4H3
2,3 diclor butan
C1H2 C2H C3H2
Cl
CH3
Cl
1,3 diclor 2 metil propan
Cl
C1H
C2H C3H3
Cl
CH3
1,1 diclor 2 metil propan
17
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Cl
Cl
C H2 C2
C3H3
CH3
1,2 diclor 2 metil propan
*****************************************************************************
*****************************************************************************
2.1.11. 200 g amestec de etan, propan i butan se supun arderii cu exces de aer. tiind c cei
trei alcani se gsesc n amestec n raport masic de 1: 2: 1 iar, aerul este 100% n exces se cere:
a)
b)
c)
d)
calculeaz compoziia amestecului de alcani;
scrie ecuaiile reaciilor chimice de ardere ale celor trei alcani;
calculeaz volumul de aer (c.n.) folosit;
calculeaz compoziia n procente volumetrice, a amestecului gazos obinut n final.( apa
se consider n stare de vapori).
Rezolvare :
metan = x
metan + mpropan + mbutan = 200 g
metan : mpropan : mbutan = 1 : 2 : 1
raport masic
metan : mpropan : mbutan = x : 2x : x
raport masic
mproan = 2x
mbutan = x
x + 2x + x = 200
4x = 200
x = 50 g etan;
2x = 100 g propan ; x = 50 g butan
18
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
50 g
C2H6
a1 l
7/2O2
a2 l
2CO2
a3 l
3H2O
etan
30 g
oxigen
7/2*22,4 l
dioxid de carbon
2*22,4 l
ap
3*22,4 l
100 g
b1 l
b2 l
b3 l
C3H8
5O2
3CO2
4H2O
propan
44 g
oxigen
5*22,4 l
dioxid de carbon
3*22,4 l
ap
4*22,4 l
50 g
c1 l
c2 l
c3 l
C4H10
butan
58 g
13/2O2
oxigen
13/2*22,4 l
4CO2
dioxid de carbon
4*22,4 l
5H2O
ap
5*22,4 l
MC2H6 = 12*2 + 6 = 30 g/mol
MC3H8 = 12*3 + 8 = 44 g/mol
MC4H10 = 12*4 + 10 = 58 g/mol
a1 = 50*3,5*22,4/30 = 130.7 l O2
b1 = 100*5*22,4/44 = 254.5 l O2
c1 = 50*6,5*22,4/58 = 125.5 l O2
VO2 = a1 + b1 + c1 = 510.7 l O2 consumat la ardere
VN2 = 4VO2 = 2042.92 l N2
Vaer = VO2 + VN2 = 2553.65 l aer
19
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Vaer folosit = 2Vaer = 5107.29 l aer
adic dublu (100% exces)
5107,29 l aer = 510,7 l O2 consumat + 510,7 l O2 rmas + 2042,92 l N2 rmas + 2042,92 l N2 rmas
a2 = 50*2*22,4/30 = 74.67 l CO2
b2 = 100*3*22,4/44 = 152.7 l CO2
c2 = 50*4*22,4/58 = 77.24 l CO2
VCO2 = a2 + b2 + c2 = 304.6 l CO2
a3 = 50*3*22.4/30 = 112 l H2O
b3 = 100*4*22.4/44 = 203,63 l H2O
c3 = 50*5*22.4/58 = 96,55 l H2O
VH2O = a3 + b3 + c3 = 412,18 l H2O
Amestecul final conine:
O2 oxigen
VO2 = 510,7 l O2
510,7 l O2 se consum la ardere
N2 azot
: 2VN2 = 2*2042.92 = 4085,83 l N2
CO2 dioxid de carbon : VCO2 = 304,6 l CO2
H20 vapori de ap
VH2O = 412,18 l H2O
Vamestec final = 510,7 + 4085,83 + 304,6 + 412,18 = 5313,31 litri
20
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
5313,31 l amestec.510,7 l O2...4085,83 l N2 ...304,6 l CO2..412,18 l H2O
100 l amestec.....% O2....% N2...% CO2....% H2O
% O2 = 100*510,7/5313,31 = 9,61 % O2
% N2 = 100*4085,83/5313,31 = 76,89 % N2
% CO2 = 100*304,6/5313,31 = 5,73 % CO2
% H2O = 100*412,18/5313,31 = 7,75 % H2O
************************************************************************
************************************************************************
2.1.12. Se supun arderii cu aer 0,896 l amestec de etan i propan. n urma arderii se obine un
amestec gazos care trecu printr-o soluie de KOH i scade volumul cu 2.24 l. Se cere :
a) calculeaz compoziia, n procente de volum, a amestecului de hidrocarburi supus
arderii;
b) calculeaz volumul de gaze obinut n urma arderii. Apa este considerat n stare
de vapori.
Rezolvare:
xl
C2H6
3,5x l
7/2O2
2x l
2CO2
3x l
3H2O
etan
22,4 l
oxigen
(7/2)*22,4 l
dioxid de carbon
2*22,4 l
ap
3*22,4 l
yl
5y l
3y l
4y l
C3H8
propan
22,4 l
5O2
oxigen
5*22,4 l
3CO2
dioxid de carbon
3*22,4 l
4H2O
ap
4*22,4 l
x + y = 0,896
2x + 3y = 2,24
21
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
2(x + y) + y = 2,24
2*0,896 + y = 2,24
y = 2,24 1,792
C3H8
x = 0,448 l etan C2H6
y = 0,448 l propan
0,896 l amestec0,448 l etan..0,448 l propan
100 l amestec..% etan% propan
% etan = 100*0,448/0,896 = 50 % etan
% propan = 100*0,448/0,896 = 50 % propan
Amestecul final conine:
N2, CO2 i H2O
Calculm volumul de O2 consumat:
VO2 = 3,5x + 5y = 3,5*0,448 + 5*0,448 = 8,5*0,448 = 3,808 l O2 consumat
VN2 = 4VO2 = 4*3,808 = 15,23 l N2
VCO2 = 2x + 3y = 2*0,448 + 3*0,448 = 5*0,448 = 2,24 l CO2
VH2O = 3x + 4y = 3*0,448 + 4*0,448 = 7*0,448 = 3,136 l H2O
V amestec final = 15,23 + 2,24 + 3,136 = 20,60 l amestec final
20,60 l amestec....15,23 l N2 ...2,24 l CO2...3,136 l H2O
100 l amestec....% N2.....% CO2......% H2O
% N2 = 100*15,23/20,60 = 73,93 % N2
% CO2 = 100*2,24/20,60 = 10,87 % CO2
% H2O = 100*3,136/20,60 = 15,22 % H2O
22
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
*****************************************************************************
*****************************************************************************
2.1.13. ntr-un rezervor cu volumul de 6 m3 se introduc 2 kmoli de etan i 29 kg dintr-un alt
alcan gazos. Amestecul gazos exercit la temperatura de 150C o presiune de 9.84 atm.
Determin alcanul necunoscut i denumete izomerul acestuia cu cel mai sczut punct de
fierbere.
PV = nRT unde n este numrul total de moli iar R = 0,082 l*atm/mol*grad
sau R = 0,082 m3*atm/kmol*grad;
T = 273 + 15 = 288 0K ; P = 9,84 atm ; V = 6 m3.
6*9,84 = n*0,082*288
n = (6*9,84)/(0,082*288) = 2,5 kmoli (din care 2 kmoli de etan i 0,5 kmoli alcan necunoscut)
MCnH2n+2 = 12n + 2n +2 = (14n +2) kg/kmoli
1 kmol alcan necunoscut..(14n +2) kg alcan necunoscut
0,5 kmol alcan necunoscut29 kg alcan necunoscut
14n + 2 = 29/0,5
14n + 2 = 58
14n = 56
n=4
deci
C4H10 butan;
C1H3 C2H2 C3H2 C4H3
n butan
23
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
C1H3 C2H
C3H3
CH3
2 metil propan sau izobutan
Izomerul cu punctul de fierbere cel mai sczut este 2 metil propan sau izobutan.
2.1.14. Se supune arderii cu oxigen un amestec echimolecular format din doi alcani omologi. n
urma arderii se degaj 6,72 l CO2 i 9 g H2O. Determin cei 2 alcani. Scrie ecuaiile reaciilor
chimice de ardere ale celor doi alcani i calculeaz volumul de oxigen, msurat n condiii
normale, tiind c s-a introdus n procesul de ardere un exces de 10 % O2.
Rezolvare:
x moli
CnH2n+2
a1 l
(3n+1)/2O2
alcan
1 mol
alcan
1 mol
oxigen
22,4*(3n+1)/2
x moli
Cn+1H2(n+1)+2 +
b1 l
nCO2
oxigen
22,4*(3n+4)/2
dioxid de carbon
n*22.4 l
a2 l
(3n+4)/2O2
c1 g
ap
(n+1)*18 g
b2 l
(n+1)CO2
dioxid de carbon
(n+1)*22.4 l
(n+1)H2O
c2 g
(n+2)H2O
ap
(n+2)*18 g
MH2O = 2 + 16 = 18 g/mol;
b1 +b2 = 6,72 l CO2
c1 +c2 = 9 g H2O
nx*22,4 + (n+1)x*22,4 = 6,72
(n+1)x*18 + (n+2)x*18 = 9
24
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
nx + nx + x = 0,3
(n+1)x + (n +2)x = 0,5
(2n+1)x = 0,3
(2n+3)x = 0,5
(2n+1)x = 0,3
(2n+1)x +2x = 0,5
(2n+1)x = 0,3
0,3 + 2x = 0,5
(2n+1)x = 0,3
2x = 0,2
(2n+1)x = 0,3
x = 0,1
(2n+1)*0,1 = 0,3
x = 0,1
2n +1 = 3
x = 0,1
n=1
x = 0,1
Cei doi alcani sunt
CH4 i C2H6 .
Avem 0,1 moli de CH4 metan i 0,1 moli C2H6 etan.
25
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
0,1 moli
CH4
a1 l
2O2
metan
1 mol
oxigen
2*22,4 l
0,1 moli
a2 l
C2H6
etan
1 mol
7/2O2
CO2
dioxid de carbon
oxigen
3,5*22,4 l
2CO2
dioxid de carbon
2H2O
ap
3H2O
ap
a1 = 0,1*2*22,4 = 4,48 l O2;
a2 = 0,1*3,5*22,4 = 7,84 l O2;
VO2 = 4,48 + 7,84 = 12,32 l O2;
Excesul de oxigen este 12,32*10/100 = 1,232 l O2;
Oxigenul introdus: 12,32 + 1,232 = 13,55 l O2.
*******************************************************************
*******************************************************************
2.1.15. 5 moli pentan se supun cracrii. Amestecul gazos format conine n
procente de volum 20% metan, 15% etan i 15% propan. Se cere:
a) scrie ecuaiile reaciilor chimice care au loc la cracarea pentanului;
b) calculeaz volumul total de gaze care se degaj la cracarea celor 5 moli de
pentan;
c) determin procentul de pentan transformat n metan.
Rezolvare:
26
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
20 l
20%
H3C -CH2-CH2-CH2- CH3
n-pentan
CH4
metan
20%
H2C = CH-CH2-CH3
1-buten
22,4 l
22,4 l
22,4 l
15 l
15%
15%
H3C -CH2-CH2-CH2- CH3
n-pentan
22,4 l
H3C-CH3
etan
H2C = CH-CH3
propen
22,4 l
15 l
22,4 l
15%
H3C -CH2-CH2-CH2- CH3
n-pentan
22,4 l
H3C-CH2-CH3
propan
22,4 l
15%
H2C = CH2
eten
22,4 l
Vpentan = 20 + 15 + 15 = 50 l
50 l pentan..20 l pentanmetan..15 l pentanetan..15 l pentanpropan
5*22,4 l pentan.x1....x2....x3
x1 = 5*22,4*20/50 = 44,8 l pentanmetan;
x2 = 5*22,4*15/50 = 33,6 l pentanetan;
x1 = 5*22,4*15/50 = 33,6 l pentanpropan;
50 l pentan..20 l pentanmetan..15 l pentanetan..15 l pentanpropan
100 l pentan.% pentanmetan .% pentanetan % pentanpropan
27
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
% pentanmetan = 100*20/50 = 40%
% pentanetan = 100*15/50 = 30%
pentanmetan
pentanetan
% pentanpropan = 100*15/50 = 30%
pentanpropan
44,8 l
44,8 l
H3C -CH2-CH2-CH2- CH3
n-pentan
CH4
metan
44,8 l
H2C = CH-CH2-CH3
1-buten
22,4 l
22,4 l
22,4 l
33,6 l
33,6 l
33,6 l
H3C -CH2-CH2-CH2- CH3
n-pentan
22,4 l
H2C = CH-CH3
propen
22,4 l
33,6 l
22,4 l
33,6 l
H3C -CH2-CH2-CH2- CH3
n-pentan
22,4 l
H3C-CH3
etan
H3C-CH2-CH3
propan
22,4 l
33,6 l
H2C = CH2
eten
22,4 l
Volumul total de gaze rezultat = 2*44,8 + 4*33,6 = 224 l.
*****************************************************************************
*****************************************************************************
2.1.16. ntr-un recipient nchis etan, se gsete propan la presiunea de 1 atm. Considernd c
propanul sufer o reacie de dehidrogenare n proporie de 30% i c temperatura n recipient
se menine constant, calculeaz presiunea din recipient la finalul procesului.
Rezolvare:
28
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
30 moli
30 moli
H3C -CH2- CH3
propan
1 mol
30 moli
H2C = CH-CH3
propen
H2
hidrogen
1 mol
70 moli
1 mol
70 moli
H3C -CH2- CH3
propan
1 mol
H3C -CH2- CH3
propan
1 mol
P1Vr = n1RT
unde n1 = 100 moli iar Vr = volumul recipientului
P2Vr = n2RT
unde n2 = 130 moli iar Vr = volumul recipientului
P1 = 1 atm
P1 /P2 = n1/n2
P2 = P1*n2/n1
P2 = 130/100 = 1,3 atm
*******************************************************************
*******************************************************************
2.1.17. Una din cile de chimizare a metanului este oxidarea cu vapori de ap pe un catalizator
de nichel. n urma oxidrii a x moli de metan se obine, cu un randament de 70% un volum de
125,44 l gaz de ap (c.n.). Determin valoarea lui x i calculeaz densitatea n raport cu aerul a
gazului de ap.
29
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Rezolvare:
a moli
CH4
a moli
metan
1 mol
3a moli
H2O
CO
ap
Ni
monoxid de carbon
1 mol
b moli
3H2
hidrogen
3 moli
b moli
CH4
metan
1 mol
CH4
metan
1 mol
= 100a/(a +b) = 70%
x =a+b
Gazul de ap :
(a + 3a)*22,4 = 125,44
a = 125,44/89,6
a = 1,4 moli
(a +b) = 1,4*100/70 = 2 moli
x = 2 moli CH4
Mgaz de ap = (MCO + 3MH2)/4 = (28 + 3*2)/4 = 34/4 = 8,5 g/mol
Maer = 28,9 g/mol
daer = 8,5/28,9 = 0,2941.
************************************************************
************************************************************
30
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
2.1.18. 200 m (c.n.) de CH4 de puritate 89,6% se supun oxidrii n prezena oxizilor de azot
la 600 0C, cu un randament de 80%. Aldehida formic obinut se dizolv n ap cu formarea
unei soluii de concentraie 40%, numit formol, folosit la conservarea preparatelor
anatomice. Calculeaz masa de formol obinut.
Rezolvare:
Calculm volumul de metan pur:
3
100 m de metan impur..89,6 m metan pur..10,4 m impuriti
3
200 m de metan impur..x
m3 metan pury m3 impuriti
x = 200*89,6/100 = 178,4 m metan pur
= 100a/(a +b) = 80%
x =a+b
3
a = (a + b)*80/100 = 178,4*80/100 = 142,72 m metanaldehid formic
MCH2O = 12 + 2 +16 = 30 kg/kmol
a m3
CH4
metan
22,4 m
O2
oxigen
oxizi de azot
md
H2C=O
aldehid formic
30 kg
b m3
H2O
ap
b m3
CH4
metan
22,4 m
CH4
metan
22,4 m
31
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
md = 142,72*30/22,4 = 191,14 kg aldehid formic
cp
= 40%
100 g formol .cp
ms....md
ms = 100*191,14/40 = 477,85 kg formol.
*****************************************************************************
*****************************************************************************
2.1.19. n urma amonoxidrii metanului se obin 200 kg acid cianhidric de puritate 81%, cu un
randament de 80%. Calculeaz volumul de metan de puritate 98%, msurat la 250C, supus
oxidrii i volumele de hidrogen i azot, msurate n condiii normale, necesare preparrii
amoniacului introdus n procesul de amonoxidare.
Rezolvare:
100 kg HCN impur.81 kg HCN pur..19 kg impuriti
200 kg HCN impurmHCN kg purmimpuriti
mHCN
= 200*81/100 = 162 kg HCN pur
= 100a/(a +b) = 80%
MHCN = 1 + 12 + 14 = 27 kg/mol
a m3
x m3
CH4
metan
22,4 m
3/2O2
oxigen
mHCN kg
NH3
amoniac
22,4 m
H-CN
acid cianhidric
27 kg
3H2O
ap
32
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
b m3
b m3
CH4
CH4
metan
22,4 m
metan
22,4 m
y m3
y m3
NH3
NH3
amoniac
22,4 m
amoniac
22,4 m
= 100x/(x +y) = 80%
3
a = 162*22,4/27 = 134,4 m CH4
3
x = 162*22,4/27 = 134,4 m NH3
(a + b) = 134,4*100/80 = 168 m3 CH4 pur.
(x + y) = 134,4*100/80 = 168 m3 NH3 .
100 m3 de metan impur.98 m3 metan pur..2 m3 impuriti
V0 m3 de metan impur168 m3 metan purz m3 impuriti
V0 m3 de metan impur = 168*100/98 = 171,42 m3 de metan 98% puritate la 00C.
V0/T0 = V1/T1
0
unde T0 = 273 K i T1 = 273 + 25 = 298 K
V1 = 171,42*298/273 = 187,11 m3 de metan 98% puritate la 250C.
33
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
VN2
N2
azot
22,4 m
168 m
VH2
3H2
hidrogen
3
3*22,4 m
2NH3
amoniac
2*22,4 m
VN2 = (22,4*168)/(2*22,4) = 84 m3 N2
VH2 = (3*22,4*168)/(2*22,4) = 252 m3 H2
*********************************************
*********************************************
34
Prof. KASTNER ELISABETA
ALCANI EXERCIII I PROBLEME
S-ar putea să vă placă și
- Alcani Exercitii Si ProbDocument34 paginiAlcani Exercitii Si ProbSorina Bob100% (1)
- Probleme Chimie Clasa X RezolvateDocument6 paginiProbleme Chimie Clasa X RezolvateFayerah100% (3)
- Probleme RezolvateDocument34 paginiProbleme RezolvateAnonymous TNyPmi7sÎncă nu există evaluări
- Capitolul 2 - HIDROCARBURI 2.4.ALCADIENEDocument14 paginiCapitolul 2 - HIDROCARBURI 2.4.ALCADIENERadu SlatinaÎncă nu există evaluări
- Probleme Chimie RezolvateDocument17 paginiProbleme Chimie Rezolvatedeniel2u71% (7)
- Alchine-Exercitii Si Probleme PDFDocument36 paginiAlchine-Exercitii Si Probleme PDFVlad IonutÎncă nu există evaluări
- Din CulegereDocument42 paginiDin CulegereHortMihaiÎncă nu există evaluări
- Probleme Rezolvate Chimie OrganicaDocument30 paginiProbleme Rezolvate Chimie OrganicaBurtan Diana82% (11)
- Chimie Organică - AlcaniiDocument41 paginiChimie Organică - AlcaniiBianca Voisa90% (39)
- Exercitii AreneDocument1 paginăExercitii ArenestedanaÎncă nu există evaluări
- Probleme La ChmieDocument10 paginiProbleme La ChmiePricope Cosmin100% (1)
- Exercitii HidrocarburiDocument65 paginiExercitii HidrocarburiAlex BabeuÎncă nu există evaluări
- ALCHENEDocument5 paginiALCHENENicholas Owens100% (7)
- AlcaniDocument3 paginiAlcanimelamel2100% (3)
- Test Alcani Cl. 10Document1 paginăTest Alcani Cl. 10Lavinia Misaila0% (1)
- Test AlcaniDocument3 paginiTest AlcaniOlimpia AlexandruÎncă nu există evaluări
- Teste - Alchine - Clasa A X-ADocument2 paginiTeste - Alchine - Clasa A X-AAdriana Boca100% (5)
- Test XI Izomerie OpticaDocument1 paginăTest XI Izomerie OpticaLauren EllisonÎncă nu există evaluări
- Alchene (Teste)Document20 paginiAlchene (Teste)Cristian Mosnegutu60% (5)
- Test - Alcani Si AlcheneDocument7 paginiTest - Alcani Si AlcheneEmilia CiocanÎncă nu există evaluări
- Complement GrupatDocument124 paginiComplement GrupatMihai Danu100% (1)
- Subiecte Rezolvate Chimie OrganicaDocument0 paginiSubiecte Rezolvate Chimie OrganicaIoana Georgiana82% (11)
- Chimie - Clasa 10 - Exercitii Si ProblemeDocument10 paginiChimie - Clasa 10 - Exercitii Si ProblemeCazacu Mihaela Elena0% (2)
- Test AlcheneDocument2 paginiTest AlcheneAnonymous JRXMkbzvaP100% (4)
- 1760 Intrebari 1760 Raspunsuri de Chimie OrganicaDocument141 pagini1760 Intrebari 1760 Raspunsuri de Chimie OrganicaLoredana Grigorie100% (1)
- Alchene Probleme RezolvateDocument6 paginiAlchene Probleme RezolvateOlga Popescu50% (2)
- Acetilena Obtinuta Din Reactia Cu Apa A 24g Carbid ImpurDocument2 paginiAcetilena Obtinuta Din Reactia Cu Apa A 24g Carbid ImpurUN OARECARE100% (4)
- Test2 2 1Document9 paginiTest2 2 1Scoala GârbăuÎncă nu există evaluări
- Test IX Acizi Si BazeDocument2 paginiTest IX Acizi Si BazeAndreea Andreea S100% (3)
- Curs-Alchine 1Document5 paginiCurs-Alchine 1Lucian Vinteler100% (1)
- Test Alcani 2Document6 paginiTest Alcani 2Nicoleta CosteaÎncă nu există evaluări
- Analiza Elementara CalitativaDocument4 paginiAnaliza Elementara CalitativaEne Vlad0% (1)
- Clasificarea Compușilor OrganiciDocument45 paginiClasificarea Compușilor OrganiciEugeniuÎncă nu există evaluări
- Teste de Chimie Organica CL 11 1-1Document252 paginiTeste de Chimie Organica CL 11 1-1Anonymous 9i0oA5Ya100% (4)
- Test AlcaniDocument4 paginiTest AlcaniAnca Lungu67% (6)
- Un Test Pentru Capitolul Arene La Chimie, Clasa AxaDocument2 paginiUn Test Pentru Capitolul Arene La Chimie, Clasa AxaAdriana Boca100% (7)
- UuDocument8 paginiUuScoala GârbăuÎncă nu există evaluări
- Ep2 5Document37 paginiEp2 5Ela ElaÎncă nu există evaluări
- Exercitii Si ProblemeDocument34 paginiExercitii Si ProblemeLorena IlincaÎncă nu există evaluări
- 4 CH Probl Alcani RezolvateDocument3 pagini4 CH Probl Alcani RezolvategcimpanÎncă nu există evaluări
- Modelarea Proceselor de Epurare Cu Namol ActivDocument99 paginiModelarea Proceselor de Epurare Cu Namol Activdadu2k40% (1)
- Clasa A Xi - Hid. NesaturateDocument4 paginiClasa A Xi - Hid. Nesaturategeorgianaeleve1Încă nu există evaluări
- Arderea Catalitica A Amestecurilor GazoaseDocument22 paginiArderea Catalitica A Amestecurilor GazoasedantopanÎncă nu există evaluări
- CORNELIU OBRASCU A Bolnavilor Cardiovasculari Prin Exercitii FiziceDocument182 paginiCORNELIU OBRASCU A Bolnavilor Cardiovasculari Prin Exercitii FiziceDanaSirb100% (1)
- CURS Tolerante Masuratori Si Control DimensionalDocument194 paginiCURS Tolerante Masuratori Si Control DimensionalTiberiu Giurgiu100% (1)
- XI - Fizica (In Limba Rusa) PDFDocument256 paginiXI - Fizica (In Limba Rusa) PDFAnonymous 48142keÎncă nu există evaluări
- 2 Fisa de LucruDocument5 pagini2 Fisa de LucruAliona AliÎncă nu există evaluări
- Poluarea Atmosferei AutostraziDocument71 paginiPoluarea Atmosferei AutostraziIonutÎncă nu există evaluări
- Caiet LaboratorDocument101 paginiCaiet LaboratorIonutz IonutzÎncă nu există evaluări
- 2010 Chimie Alte Concursuri Barem Clasa A XI-A 1Document2 pagini2010 Chimie Alte Concursuri Barem Clasa A XI-A 1amadeus_amadeus36Încă nu există evaluări
- Cartea Tamplarului Universal - Cu OCRDocument392 paginiCartea Tamplarului Universal - Cu OCRzorghi1100% (4)
- LungeanuDocument597 paginiLungeanutvrossy100% (5)
- Chimie UMFCV 2021Document164 paginiChimie UMFCV 2021Ioana Petrescu100% (1)
- E F Chimie Organica I Niv I Niv II Siii 098Document1 paginăE F Chimie Organica I Niv I Niv II Siii 098Andrei SavinÎncă nu există evaluări
- Andrei Radulescu - ElectroterapiaDocument359 paginiAndrei Radulescu - Electroterapiasmara_nda100% (3)
- Test AlcadieneDocument7 paginiTest AlcadieneAndreaÎncă nu există evaluări
- T 2 ADocument5 paginiT 2 AVIerme VRm ZOr0% (1)
- CursDED v20140822Document136 paginiCursDED v20140822adinabÎncă nu există evaluări
- Test AreneDocument14 paginiTest AreneAndrea100% (1)
- RezumatDocument36 paginiRezumatTatiana ScutelnicÎncă nu există evaluări
- Vrabiuta Si CocostarculDocument1 paginăVrabiuta Si CocostarculAdiÎncă nu există evaluări
- În Vreme de RăzboiDocument9 paginiÎn Vreme de RăzboiStefan SerbÎncă nu există evaluări
- Manual FizicaDocument161 paginiManual Fizicaraulstoin100% (2)
- Alexandru Lapuseneanu de C NegruzziDocument32 paginiAlexandru Lapuseneanu de C NegruzziNicu IlieÎncă nu există evaluări
- Divide Et Impera - InformaticaDocument2 paginiDivide Et Impera - InformaticaStefan SerbÎncă nu există evaluări
- ProbabilitatiDocument6 paginiProbabilitatiStefan SerbÎncă nu există evaluări
- 01.procesare DistribuitaDocument15 pagini01.procesare DistribuitaivandankoÎncă nu există evaluări
- Probleme SubprogramareDocument2 paginiProbleme SubprogramareStefan SerbÎncă nu există evaluări
- Prefixoide Sufixoide BacDocument27 paginiPrefixoide Sufixoide BacFinchi PaulÎncă nu există evaluări
- Mesaj Catre Toti RomaniiDocument2 paginiMesaj Catre Toti RomaniiStefan SerbÎncă nu există evaluări
- Cine Este DumnezeuDocument2 paginiCine Este DumnezeuStefan SerbÎncă nu există evaluări