Documente Academic
Documente Profesional
Documente Cultură
00 885
Încărcat de
hizballah27Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
00 885
Încărcat de
hizballah27Drepturi de autor:
Formate disponibile
Neurologie
A 49
Syndrome myogène
Orientation diagnostique
DR Dominique CAPARROS-LEFÈBVRE
Service de neurologie, CHU de la Guadeloupe, 97159 Pointe-à-Pitre.
Points Forts à comprendre la petite enfance pour la maladie de Duchenne, à l’ado-
lescence pour d’autres dystrophies musculaires, après
50 ans pour les myopathies oculo-pharyngées et les
• Le syndrome myogène, dénominateur commun myosites à inclusion), l’évolution rapide (pathologies
d’un groupe très hétérogène d’affections, ne inflammatoires) ou lentement progressive (maladies à
comporte aucun signe qui soit individuellement déterminisme génétique).
spécifique de pathologie musculaire. • Syndrome douloureux : la topographie et le type des
• Le diagnostic étiologique repose douleurs, leur majoration éventuelle lors de l’effort au
sur l’interrogatoire (antécédents familiaux, cours des myopathies métaboliques, leur déclenchement
évolution), sur l’examen général à la recherche par la pression des masses musculaires peuvent apporter
d’une pathologie multiviscérale, la biologie et des arguments confirmant le syndrome myogène. La
l’électromyogramme qui montrent des signes prédominance des douleurs sur le déficit est en faveur
myogènes assez spécifiques, sur la biopsie d’une myosite.
musculaire et surtout sur la génétique qui a • Antécédents familiaux : dans la majorité des cas, il
bouleversé la classification des dystrophies est nécessaire de réaliser un arbre généalogique afin de
musculaires. définir le caractère autosomique récessif (glycogénoses
• En dépit des progrès de la génétique, et myopathies métaboliques) ou dominant (myopathie
la thérapie génique n’a pas apporté de résultat oculo-pharyngée) ou récessif lié au chromosome X,
significatif à ce jour. affectant exclusivement ou majoritairement les individus
• Plusieurs myopathies métaboliques justifient de sexe masculin (dystrophies musculaires).
un traitement. Il faut aussi reconnaître
les myopathies inflammatoires, endocriniennes
ou toxiques qui sont curables. Examen clinique
• Examen neurologique : à l’inspection, il existe le plus
souvent une amyotrophie globale ou sélective (dystro-
Le syndrome myogène correspond à un dysfonction- phies), habituellement symétrique. L’amyotrophie de la
nement primitif localisé ou diffus des muscles squelet- ceinture scapulaire entraîne un décollement caractéris-
tiques qui est responsable d’un déficit moteur, et de tique des omoplates (scapulæ alatæ). Une hypertrophie du
modifications du volume des masses musculaires triceps sural ou une pseudo-hypertrophie, liée à l’involu-
(amyotrophie ou hypertrophie) en l’absence de lésions tion fibreuse du muscle, précède l’atrophie, en particulier
du système nerveux central (SNC) ou périphérique. dans certaines dystrophies musculaires. Le déficit a le
plus souvent une distribution symétrique et sa prédomi-
Diagnostic clinique nance aux racines des membres [ceinture pelvienne et
(ou) scapulaire] constitue un argument en faveur d’une
Classiquement, le syndrome myogène est constitué par maladie musculaire, donnant à la marche une allure par-
l’association de 4 symptômes cardinaux : déficit moteur ticulière : marche dandinante ou marche en canard. La
global ou focal, amyotrophie, douleurs, disparition du localisation du déficit détermine le handicap fonctionnel :
réflexe idiomusculaire. Cependant, l’absence du réflexe difficulté pour s’accroupir, se lever d’une chaise, courir,
idiomusculaire peut être difficile à démontrer, et les monter les escaliers, lever les bras. Dans les myopathies
autres symptômes constituant le syndrome myogène ne oculo-pharyngées, le ptosis bilatéral et la dysphagie sont
sont pas spécifiques car ils peuvent aussi être produits les signes principaux.
par des neuropathies périphériques ou des lésions de la Le testing musculaire offre une évaluation quantitative
corne antérieure de la moelle épinière. du déficit moteur segmentaire. Ils permet de mesurer
avec plus de précision la rapidité d’évolution ou encore
Interrogatoire l’efficacité d’une thérapeutique immuno-suppressive
dans les myosites. En cours d’évolution, des rétractions
• Histoire de la maladie : il faut obtenir le mode d’instal- tendineuses et des déformations osseuses aggravent
lation des troubles : début proximal (cas le plus fréquent) le handicap. Le déficit peut évoluer vers une perte d’au-
ou distal (myosite à inclusion), l’âge d’apparition (dans tonomie.
LA REVUE DU PRATICIEN 2000, 50 885
SYNDROME MYOGÈNE
Certains symptômes ne font pas partie du syndrome pathies précoces. Le diagnostic repose alors sur l’élec-
myogène : incontinence urinaire ou anale, déficit sensitif tromyogramme, la biopsie musculaire et la génétique.
ou dysesthésies. Leur présence témoigne d’une atteinte • Myasthénie : cette pathologie de la plaque motrice se
neurogène associée, ou d’une pathologie métabolique manifeste par un déficit moteur symétrique et une
complexe comme dans les myopathies mitochondriales. fatigabilité. La prédominance des troubles au niveau de
Les réflexes ostéo-tendineux sont habituellement présents la musculature faciale et la variabilité du déficit dans le
mais peuvent être abolis dans les dystrophies musculaires temps, prédominant le soir ou après un effort est plus en
à un stade avancé ou dans les myosites à inclusion. faveur d’une myasthénie, qui sera confirmée par l’élec-
Le suivi évolutif comporte un bilan fonctionnel régulier, tromyogramme, révélant un décrément des potentiels
avec une évaluation des complications orthopédiques : moteurs lors d’une stimulation itérative.
rétractions tendineuses (surtout du tendon d’Achille),
scoliose, évaluation de l’atteinte myocardique et du Examens paracliniques contributifs
risque de survenue d’une insuffisance respiratoire liée
au déficit des muscles ventilatoires et aux déformations
au diagnostic
secondaires de la cage thoracique. La kinésithérapie • Examens biologiques standards : on procède au
peut prévenir les rétractions. Les indications chirur- dosage des enzymes musculaires – créatine phosphokinase
gicales correctrices des déformations osseuses sont (CPK) surtout, mais aussi lactate deshydrogénase
discutées en fonction du bénéfice fonctionnel attendu. (LDH), – l’aldolase est un bon marqueur de la cytolyse
• Recherche de signes associés : en fonction de l’étio- musculaire. Les créatines phosphokinases sont très
logie (génétique, métabolique ou inflammatoire) des augmentées dans les dystrophinopathies (myopathies de
signes évocateurs d’une pathologie multiviscérale sont Duchenne, et de Becker), moins dans les dystrophies
recherchés. Le myocarde, muscle strié, peut être atteint musculaires des ceintures. Elles sont inconstamment
dans certaines dystrophies musculaires ou au cours des élevées dans les autres dystrophies. Au cours des myo-
polymyosites, alors que les muscles lisses le sont plus sites infectieuses aiguës (virales ou parasitaires) et des
rarement. Une défaillance myocardique existe dans la myosites inflammatoires (polymyosites, dermatomyo-
maladie de Duchenne, dans les glycogénoses et cer- sites), les créatines phosphokinases sont souvent très
taines myopathies mitochondriales. Elle évolue parallè- élevées. En revanche, elles peuvent être normales dans
lement à l’atteinte du muscle. Un Holter rythmique per- les myosites à inclusions.
met de dépister des anomalies paroxystiques de la • L’électromyogramme peut objectiver un syndrome
conduction auriculo-ventriculaire dans la dystrophie myogène électrique, qui est plus spécifique que le syn-
myotonique de Steinert. Une insuffisance respiratoire drome myogène clinique. Le tracé est anormalement
restrictive est une cause fréquente de décès, en particu- riche par rapport à l’effort. Les potentiels d’unité motrice
lier dans la myopathie de Duchenne. sont polyphasiques, d’amplitude et de durée diminuées.
Les pathologies musculaires, en particulier inflamma- Par ailleurs, les vitesses de conduction nerveuse des
toires ou métaboliques, sont aux confins de plusieurs fibres motrices et sensitives sont normales, sauf dans
spécialités, et leur diagnostic est difficile en l’absence certaines maladies métaboliques où il peut exister une
d’une collaboration interdisciplinaire. neuropathie associée.
• L’imagerie par tomodensitométrie ou résonance
Diagnostic différentiel magnétique objective les anomalies musculaires liées à
l’involution et permet d’établir une cartographie des
• Neuropathies : une polyradiculonévrite chronique muscles sélectivement atteints. La spectrométrie par
peut faire évoquer à tort une pathologie musculaire, du résonance magnétique nucléaire du phosphore permet
fait de la symétrie du déficit moteur prédominant à la de mesurer la concentration de phosphocréatine et les
ceinture pelvienne et de la discrétion des troubles sensitifs. variations de pH musculaire à l’effort. Une acidose
La marche a alors une allure pseudomyopathique. marquée à l’effort, ainsi qu’une lente récupération de la
L’électromyogramme (EMG) est indispensable pour phosphocréatine et du pH après l’effort sont des
montrer les signes neurogènes et les anomalies des arguments en faveur d’une myopathie mitochondriale.
vitesses de conduction nerveuse. L’étude du liquide • Biopsie musculaire : elle est l’examen majeur en
céphalo-rachidien recherche une hyperprotéinorachie. pathologie musculaire et est indispensable dans la
• Atteinte de corne antérieure de la moelle épinière : démarche diagnostique de nombreuses maladies neuro-
certaines amyotrophies spinales d’évolution chronique musculaires et d’affections systémiques (maladies de
peuvent avoir un aspect pseudomyopathique, lorsque système, vascularites). L’histopathologie musculaire
l’amyotrophie prédomine aux ceintures et racines des conventionnelle, après inclusion en paraffine et colora-
membres. L’étude génétique permet d’obtenir le dia- tion par l’hématéïne-éosine et le trichrome de Masson,
gnostic dans les formes héréditaires [anomalies du gène permet une description analytique des lésions élémen-
SMN (survival motor neuron) sur le chromosome 5 taires : atrophie et hypertrophie compensatrices des
surtout]. L’amyotrophie spinale aiguë du nourrisson ou fibres musculaires, fréquentes dans les dystrophies
maladie de Werdnig-Hoffmann se manifeste par une musculaires ; nécrose et régénération ; modifications
hypotonie non spécifique, comparable à celle des myo- nucléaires ; vacuoles (glycogénoses, myopathies oculo-
886 LA REVUE DU PRATICIEN 2000, 50
Neurologie
pharyngées, myosites à inclusions) ; anomalies du tissu tendons d’Achille sont les premières complications
interstitiel (involution fibro-adipeuse des dystrophies, orthopédiques. Il existe une hypertrophie des masses
infiltrats inflammatoires de l’endomysium ou du péri- musculaires des mollets. L’enfant marche sur la pointe
mysium des vascularites ou des myosites infectieuses). des pieds et de façon dandinante. De façon lentement
Des techniques récentes (histo-enzymologie, immunocy- progressive, le déficit s’accentue et la marche devient
tochimie, microscopie électronique) permettent un dia- impossible vers l’âge de 10 ans. L’atrophie musculaire
gnostic formel des myopathies congénitales et dystrophi- remplace peu à peu l’hypertrophie. Le décès survient
nopathies. Grâce aux études biochimiques et génétiques, il vers 20 ans, du fait de la défaillance cardiorespiratoire
est possible de caractériser les myopathies métaboliques : ou des complications du décubitus. L’atteinte myocar-
déficits enzymatiques des glycogénoses, déficits sélectifs dique évolue parallèlement à l’atteinte des muscles
des complexes de la chaîne respiratoire mitochondriale. squelettiques et entraîne une insuffisance cardiaque.
• Diagnostic génétique : il s’applique particulièrement La dystrophie musculaire de Becker se distingue clini-
aux dystrophies musculaires. Dans un passé récent, leur quement par un début plus tardif, vers l’âge de 12 ans,
classification reposait sur l’aspect clinique : topographie avec des extrêmes de 2 à 45 ans. Le déficit apparaît à la
de l’atteinte musculaire, évolution et mode de transmission. ceinture pelvienne, puis scapulaire. Les muscles distaux
Depuis la mise en évidence de plusieurs mutations géné- sont préservés. L’hypertrophie des mollets est constante.
tiques responsables de la synthèse de protéines anormales, La marche devient impossible vers l’âge de 30 ans et le
la classification est faite en fonction du type de mutations décès survient vers 40 ans, par défaillance myocardique
et de la protéine anormale. Les principales protéines pour ou insuffisance respiratoire restrictive liée à la paralysie
lesquelles des anomalies ont été identifiées sont la dystro- des muscles respiratoires, qui peut être transitoirement
phine, les dystroglycanes (dont la mérosine) qui lient la améliorée par une ventilation mécanique au masque.
dystrophine aux éléments extracellulaires, les sarco- Dans la dystrophie musculaire de Duchenne et dans
glycanes transmembranaires (voir : Pour approfondir). celle de Becker, les enzymes musculaires, en particulier
les créatines phosphokinases, sont très élevées (10 à
100 fois la normale). Cette élévation apparaît avant le
Étiologie début des signes cliniques et n’est pas corrélée à la
gravité de la maladie. En fin d’évolution, les taux de
Dystrophies musculaires (tableau I) créatines phosphokinases diminuent.
• Dystrophinopathies : dystrophie musculaire de La dystrophie musculaire de Duchenne se caractérise
Duchenne (DMD) et dystrophie de Becker : la dystro- par l’absence de dystrophine, qui est anormale ou en
phie musculaire de Duchenne est la plus fréquente et la quantité réduite dans la dystrophie musculaire de
plus sévère des dystrophies musculaires liées au chro- Becker. Le diagnostic est obtenu par la biopsie médul-
mosome X. Le mode de transmission explique que seuls laire, dont l’étude immunocytochimique, avec des anti-
les enfants de sexe masculin sont atteints, cependant les corps monoclonaux dirigés contre la dystrophine,
femmes qui transmettent le gène peuvent développer un montre l’absence de marquage dans la dystrophie
syndrome myogène d’expression modérée. musculaire de Duchenne, ou une diminution du marquage
La dystrophie musculaire de Duchenne se manifeste dans celle de Becker. Un aspect en mosaïque, avec des
vers l’âge de 3 ans, mais la marche a souvent été acqui- fibres positives et des fibres négatives apparaît chez les
se avec un peu de retard, vers 15 à 18 mois. Une diffi- femmes porteuses. Le diagnostic génétique repose sur la
culté pour courir, sauter, monter les escaliers apparaît, mise en évidence d’une délétion du gène de la dystro-
puis une hyperlordose lombaire et une rétraction des phine, par amplification génique.
TABLEAU I
Dystrophies musculaires
Dénomination Protéine anormale Transmission
Dystrophie de Duchenne dystrophine (Xq21) récessif lié à X
et dystrophie de Becker
Dystrophie d’Emery-Dreifuss émerine récessif lié à X
Dystrophie facio-scapulo-humérale ? AD chr 4
Dystrophie des ceintures ? AR/AD chr 2,5, 15
Dystrophies sévères de l’enfant sarcoglycanes AR chr 4, 13, 17
Myopathie oculo-pharyngée ? AD chr 14
Myopathies distales ? AD/AR localisation ?
Myopathies congénitales mérosine AR chr 6 ou 9
LA REVUE DU PRATICIEN 2000, 50 887
SYNDROME MYOGÈNE
En l’absence de thérapeutique, et sur la base de l’histoire transmission est autosomique, dominant ou récessif.
familiale et de l’étude de la délétion génique, il est La forme de Miyoshi s’observe chez l’adulte jeune
possible de détecter les femmes porteuses afin de leur et s’accompagne d’une augmentation importante des
apporter un conseil génétique et faire un diagnostic créatines phosphokinases.
prénatal. Lorsque la délétion est mise en évidence sur • Maladie de Steinert ou dystrophie myotonique :
la biopsie trophoblastique du fœtus, l’avortement théra- Cette affection de transmission autosomique dominante
peutique est proposé. a une expressivité variable. Un phénomène d’anticipa-
• Dystrophie d’Emery-Dreifuss : dystrophie musculaire tion rend compte de la gravité croissante de la sympto-
liée au chromosome X, elle se caractérise par 3 signes matologie dans les générations successives. L’anomalie
cardinaux : rétractions musculaires précoces, déficit génétique est une amplification anormale d’une séquence
moteur et amyotrophie de topographie huméro-péronière, trinucléotidique sur le bras long du chromosome 19,
troubles de la conduction cardiaque. Le handicap fonc- produisant la myotonine protéine kinase. La symptoma-
tionnel est modéré jusqu’à la cinquantaine, mais le tologie est dominée par une amyotrophie prédominant à
risque de mort subite par bloc auriculo-ventriculaire doit l’extrémité céphalique responsable d’un faciès très
être évalué et prévenu par la pose d’un pacemaker. particulier : ptosis, visage inexpressif et allongé du fait
L’étude génétique met en évidence un gène patholo- de l’atrophie des muscles masticateurs. La voix est
gique responsable de la synthèse d’une protéine, l’émé- nasonnée. Il existe souvent une calvitie. La myotonie se
rine, dont le rôle pathogène n’est pas encore connu. manifeste par une lenteur à la décontraction après un
• Myopathie facio-scapulo-humérale ou myopathie de mouvement volontaire ou après percussion d’un muscle,
Landouzy-Dejerine : de transmission autosomique par exemple l’ouverture de la main après une poignée de
dominante à pénétrance complète, de nombreuses main est lente. La myotonie a une traduction électro-
formes frustes ne sont pas diagnostiquées. L’anomalie myographique spécifique : les averses myotoniques.
génétique qui est une délétion d’un gène siégeant sur le L’atteinte systémique associe une cataracte bilatérale,
chromosome 4, en position 4q35 permet le diagnostic des troubles du rythme et de la conduction cardiaque, et
par biologie moléculaire sur un prélèvement sanguin. des anomalies hormonales.
Elle se manifeste par une atteinte musculaire de topo-
graphie très particulière, volontiers asymétrique : inex- Myopathies congénitales
pressivité faciale, déficit de la ceinture scapulaire avec
décollement des omoplates, atrophie des muscles des Longtemps confondues avec les amyotrophies spinales
bras alors que les muscles des avant-bras sont respectés. type Werdnig-Hoffmann, il est important de les distin-
Diverses formes cliniques ont été identifiées en fonction guer, car le pronostic de certaines formes est bien
de la topographie du déficit. L’atteinte péronière peut meilleur. Elles comportent le plus souvent une hypoto-
être responsable d’un steppage. nie, un déficit modéré et un syndrome dysmorphique :
• Dystrophies musculaires des ceintures : de transmis- thorax en entonnoir, faciès allongé, palais ogival.
sion autosomique récessive, elles constituent un groupe Certaines sont caractérisées par des anomalies morpho-
hétérogène, correspondant à des anomalies génétiques logiques intracellulaires, qui les définissent et leur
diverses. La forme la plus fréquente survient chez ont donné leur nom : myopathie à « centralcore », à
l’adolescent ou l’adulte jeune. Elles furent initialement bâtonnets, à « multicores »…
individualisées dans des pays à fort taux de consan-
guinité. Ce groupe comporte aussi des myopathies plus Myopathies métaboliques
graves atteignant l’enfant, initialement observées en
Tunisie, dénommées SCARMD (severe childhood auto- • Glycogénoses musculaires : ces maladies de surcharge
somic recessive muscular dystrophy). Elles sont liées à sont secondaires à un déficit congénital d’une des
une anomalie d’une des unités des sarcoglycanes : enzymes du métabolisme du glycogène. Elles sont habi-
α, β, δ, γ, mais aussi à d’autres protéines identifiées très tuellement de transmission autosomique récessive. Une
récemment (calpaïne 3, dysferline). atteinte multiviscérale est fréquente, affectant le myo-
• Myopathies oculo-pharyngées : d’hérédité autoso- carde, le foie (hépatomégalie, cirrhose), parfois le système
mique dominante, elles surviennent toujours après nerveux central. La maladie de Mac Ardle se traduit par
50 ans, le plus souvent entre 60 et 80 ans. Elles associent une intolérance musculaire à l’effort et parfois une myo-
un ptosis bilatéral, parfois asymétrique et une dysphagie. globinurie d’effort. La biopsie médullaire apporte le
Le ptosis peut conduire à une occlusion palpébrale diagnostic en montrant une accumulation de vacuoles
complète. Elles peuvent être confondues avec une myas- riches en glycogène, marquées par la coloration PAS (perio-
thénie, mais le déficit permanent, l’absence de réponse dic acid schiff). L’analyse biochimique du muscle permet
aux anticholinestérasiques et la biopsie musculaire per- d’identifier le déficit enzymatique qui les caractérise.
mettent de rectifier le diagnostic. L’anomalie génique se • Myopathies mitochondriales. Les mitochondries
situe sur le chromosome 14. fournissent l’énergie aux cellules en fabriquant de l’adé-
• Myopathies distales : elles affectent initialement les nosine triphosphate (ATP) par le cycle de Krebs. Elles
muscles de la jambe. L’âge de début est variable. sont donc très abondantes dans les tissus consommant
Certaines sont proches des myopathies à inclusion, du beaucoup d’énergie, comme les muscles. La synthèse
fait de la constatation de vacuoles bordées. Le mode de protéique mitochondriale dépend à la fois de l’ADN
888 LA REVUE DU PRATICIEN 2000, 50
Neurologie
TABLEAU II chondrial myopathy encephalopathy lactic acidosis and
stroke like episodes) est une vasculopathie cérébrale
Glycogénoses et déficits mitochondriale, débutant dans l’enfance par un retard de
enzymatiques associés croissance, des crises convulsives, des céphalées vascu-
laires, puis vers l’âge de 40 ans apparaissent des acci-
dents vasculaires ischémiques à répétition. Le déficit
Glycogénose Enzyme déficiente
porte sur le complexe I de la chaîne respiratoire.
Le diagnostic de ces mitochondriopathies repose sur
❑ Type II α-glycosidase acide l’association d’une acidose lactique surtout à l’effort,
dont maladie de Pompe d’un taux diminué des complexes de la chaîne respira-
❑ Type III ou maladie 1,6 glucosidase toire dans le muscle et sur la mise en évidence de l’alté-
de Forbe
ration de l’acide désoxyribonucléique mitochondrial ou
❑ Type IV ou maladie enzyme ramifiante nucléaire. Ces techniques n’ont pas encore une grande
d’Andersen (synthèse glycogène)
diffusion. Sur le plan clinique, une association sympto-
❑ Type V ou maladie phosporylase musculaire
de Mac Ardle matique multiviscérale doit inciter à évoquer le diagnos-
tic de pathologie mitochondriale devant l’association
❑ Type VII ou maladie phosphofructokinase
de Tarui d’une encéphalopathie, avec surdité acquise, et atteinte
❑ Type VIII phosphorylase kinase musculaire ou neurogène périphérique.
• Hyperthermie maligne : la rigidité musculaire induite
❑ Type IX phosphoglycérate kinase
par les anesthésiques provoque une contracture généralisée,
❑ Type X phosphoglycérate mutase
une rhabdomyolyse avec hyperthermie pouvant dépasser
❑ Type XI lactate deshydrogénase 41 ˚C, et souvent mortelle. Elle est produite par une
anomalie des canaux calciques musculaires. Plusieurs
événements métaboliques se succèdent : production
d’énergie excessive, d’où acidose, puis rigidité musculaire.
nucléaire, mais aussi de l’ADN mitochondrial intracyto-
Cette affection est génétique (anomalie du gène codant
plasmique (transmis uniquement par la mère). Les mala-
pour le récepteur ryanodine, sur le chromosome 19).
dies mitochondriales se divisent donc en 2 groupes :
Elle s’associe souvent à la myopathie à « centralcore ».
celles liées à une altération de l’acide désoxyribonu-
cléique (DNA) nucléaire et celles liées à une délétion ou
une mutation de l’acide désoxyribonucléique mitochon- Myosites inflammatoires
drial. Les déficits en complexes I, II, III, IV ou V de la • Dermatomyosites : elles sont la conséquence d’un
chaîne respiratoire, d’origine nucléaire, sont respon- processus dysimmunitaire responsable d’une vascularite
sables d’une encéphalomyopathie de gravité variable, en distale avec dépôts de complexes immuns circulants sur
fonction de l’intensité du déficit enzymatique. Le déficit l’endothélium des capillaires, qui se thrombosent et se
en carnitine ou carnitine-palmityl-transférase produit nécrosent, provoquant une ischémie musculaire. Dans
une insuffisance de transport des acides gras à longue 25 % des cas, elles sont associées à un cancer qu’il fau-
chaîne vers les mitochondries. Le déficit en carnitine est dra systématiquement rechercher dans le cadre d’un
important à reconnaître car l’apport de L-carnitine per- syndrome paranéoplasique.
met de corriger l’atteinte musculaire. Les altérations de Les dermatomyosites sont des affections aiguës dont les
l’ADN mitochondrial sont responsables de syndromes lésions cutanées caractéristiques sont un œdème et un
cliniques plus spécifiques, décrits depuis une vingtaine érythème prédominant sur les zones découvertes : visa-
d’années. L’expression clinique est très diverse, en fonc- ge, décolleté. L’atteinte musculaire, d’intensité variable,
tion du complexe (de la chaîne respiratoire) prédomine aux ceintures. Des myalgies sont fréquentes,
déficitaire. Les myopathies oculaires, responsables de même que des arthralgies, une altération de l’état
d’une ophtalmoplégie progressive avec ptosis sont sou- général et un syndrome inflammatoire biologique. Les
vent liées à un déficit de la cytochrome oxydase (com- localisations systémiques peuvent être myocardiques
plexe IV ou Cox). La biopsie médullaire met en éviden- (voire péricardiques), gastro-intestinales, rénales, et pul-
ce des fibres musculaires anormales : fibres rouges monaires. En l’absence de traitement immunosuppres-
déchiquetées (ragged red fibers, RRF) par la coloration seur, l’affection est mortelle dans 70 % des cas. La cor-
du trichrome de Gomori et des fibres Cox-négatives. Le ticothérapie permet d’obtenir souvent une guérison mais
syndrome de Kearns et Sayre associe une ophtalmoplé- des rechutes sont fréquentes. D’autres traitements
gie progressive, une rétinite pigmentaire, un syndrome immunosuppresseurs peuvent être nécessaires.
cérébelleux, une surdité et une détérioration intellectuel- • Polymyosites : elles se distinguent des dermatomyo-
le progressive. La biopsie médullaire montre aussi des sites par leur physiopathologie, et par l’association,
RRF. Le syndrome MERRF (myoclonus epilepsy asso- beaucoup plus rare, à un cancer, mais fréquente (20 %) à
ciated with ragged red fibers) comporte un tremble- une autre pathologie auto-immune (lupus, myasthénie,
ment, une spasticité, une neuropathie périphérique et sclérodermie). Elles résultent d’une dysimmunité cellu-
une démence. La biopsie médullaire montre des RRF et laire dirigée contre les cellules musculaires, respon-
des fibres Cox-négatives. Le syndrome MELAS (mito- sables de phénomènes de nécrose et de régénération, et
LA REVUE DU PRATICIEN 2000, 50 889
SYNDROME MYOGÈNE
sont habituellement sensibles à la corticothérapie. l’héroïne. Cette liste n’est pas exhaustive. Les corti-
Certaines ont une étiologie spécifique : sarcoïdose (sou- coïdes (fluorés surtout) provoquent des myopathies
vent en association avec une atteinte du système ner- chroniques. Une ascension des créatines phosphoki-
veux central ou périphérique), ou syndrome hyperéosi- nases et des douleurs musculaires sous hypolipémiants
nophilique, affection hématologique grave. constituent une des myopathies médicamenteuses les
• Myosites à inclusions : survenant plus souvent après plus fréquentes. ■
50 ans, plus fréquente chez l’homme, elle comporte un
déficit et une amyotrophie distale, orientant à tort vers POUR APPROFONDIR
un processus neurogène, progressant vers les ceintures,
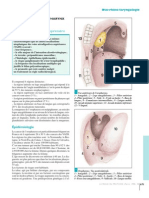
affectant surtout les muscles de la face antérieure des Organisation des protéines contractuelles et des
membres, parfois le sterno-cléido-mastoïdien. Elles protéines membranaires de la cellule musculaire
comportent des lésions morphologiques à type de
vacuoles bordées en microscopie optique et des inclu- Représentation schématique du complexe multiprotéique reliant à tra-
sions filamenteuses caractéristiques en microscopie élec- vers le sarcolemme les protéines contractiles intracytoplasmiques liées
tronique. Les lésions inflammatoires sont inconstantes. à l’actine et la matrice extracellulaire de la lame basale. Ce complexe
comporte : la dystrophine, les différentes unités constituant les sarcogly-
canes (dont l’adhaline), les dystroglycanes α et β et la mérosine (d’après
Myosites infectieuses Desnuelle et coll., 1996.
Les plus fréquentes sont les myosites parasitaires.
• La trichinose, dont le parasite adulte infeste le tube POUR EN SAVOIR PLUS
digestif, pond des larves qui, par dissémination lympha-
tique, produisent un syndrome inflammatoire sévère, Desnuelle C, Butori C, Paquis V. Autres dystrophies muscu-
avec myalgies, et atteinte du système nerveux central. laires. Encycl Med Chir Neurologie. Paris : Elsevier 1996 ; 17-
179-A-30.
• La cysticercose, première cause d’épilepsie dans le
Leroy-Willig A, Carlier P, Morvan D, Duboc D, Fardeau M.
monde du fait de sa grande fréquence dans les pays L’imagerie fonctionnelle du muscle humain. Rev Neurol 1998 ;
tropicaux (sauf dans les Antilles françaises), est liée à 154 : 379-88.
l’ingestion de larves de tænia solium. Le diagnostic Pelissier JF, Figarella-Branger D, Coquet M. Biopsie mpusculaire.
repose sur la mise en évidence des larves calcifiées Encyclopédie médico-chirurgicale. Neurologie. Paris : Éditions
ayant un aspect en grains de riz, sur les radiographies de Techniques, 1995 ; 17030 G10.
parties molles (mollets, bras). La migration et l’enkyste- Serratrice G, Desnuelle C. Les encéphalomyopathies mitochon-
ment des larves dans le parenchyme cérébral se manifes- driales. Presse Med 1990 ; 19 : 645-7.
tent par une encéphalite qui peut guérir spontanément, Serratrice G, Pelissier JF, Desnuelle C, Pouget J. Myopathies
mais les larves calcifiées sont responsables d’une épi- mitochondriales et myopathies oculaires. Rev Neurol 1991 ;
147 : 474-5.
lepsie séquellaire.
• D’autres parasitoses peuvent produire une myosite Serratrice G, Pellissier JF, Pouget J. Les maladies neuromuscu-
plus ou moins symptomatique : toxoplasmose, échino-
coccose, trypanosomiase, toxocarose…
• L’infection par le virus de l’immunodéficience Points Forts à comprendre
humaine (VIH) peut engendrer une myosite, parfois
favorisée par les traitements antiviraux. • Un syndrome myogène est commun
• Le myxovirus, le virus coxsackie (et bien d’autres à des affections diverses classées en 4 groupes :
virus) peuvent être à l’origine de myosites, avec prépon- – 1 : dystrophies musculaires liées à une mutation
dérance des myalgies. du gène codant les protéines des cellules
musculaires ;
Myopathies endocriniennes et toxiques – 2 : maladies musculaires métaboliques :
glycogénoses et itochondriales ;
L’hyperthyroïdie peut induire une myopathie des cein- – 3 : myosites ;
tures chronique, et une myopathie oculaire basedowienne – 4 : myopathies endocriniennes et toxiques.
ou exophtalmie maligne. Une myopathie est classique Le pronostic et les traitements de ces affections
au cours de l’hypothyroïdie avec des taux élevés de dépendent donc de l’étiologie.
créatines phosphokinases. Une myopathie peut compli- • Une élévation des créatines phosphokinases,
quer une hyperparathyroïdie, une acromégalie, un syn- des anomalies à l’électromyogramme
drome de Cushing ou une maladie d’Addison. Il est caractéristiques contribuent au diagnostic de
important de détecter l’endocrinopathie, car ces myopa- syndrome myogène.
thies sont curables. Les myopathies toxiques peuvent • Des affections neurogènes : polyradiculo-
être dues à : une intoxication alcoolique massive (par- névrites, maladies du motoneurone peuvent
fois avec une rhabdomyolyse), la D-pénicillamine, mimer un syndrome myogène, de même
l’AZT (azidothymidine), l’amphotéricine B, le disulfirame, que la myasthénie.
les psychotropes, la méthadone, les amphétamines et
890 LA REVUE DU PRATICIEN 2000, 50
S-ar putea să vă placă și
- Tout Ce Qu Il Voudra 1 Sara FawkesDocument22 paginiTout Ce Qu Il Voudra 1 Sara Fawkesjajazza83% (6)
- QCM Tête Et Cou NCDocument9 paginiQCM Tête Et Cou NCŽĭņëb Bėñ100% (2)
- Maladies Metaboliques Hereditaires Par (WWW - Heights Book - Blogspot.com)Document309 paginiMaladies Metaboliques Hereditaires Par (WWW - Heights Book - Blogspot.com)pepeÎncă nu există evaluări
- L'héminégligence: Prise en Charge KinésithérapiqueDocument42 paginiL'héminégligence: Prise en Charge KinésithérapiqueAymen DabboussiÎncă nu există evaluări
- Myopathies CongénitalesDocument3 paginiMyopathies Congénitalesimma_drÎncă nu există evaluări
- MyopathiesDocument5 paginiMyopathiesMehdi BayanaÎncă nu există evaluări
- La Polyneuropathie Du Syndrome POEMS: Mise Au PointDocument7 paginiLa Polyneuropathie Du Syndrome POEMS: Mise Au Pointsara laadamiÎncă nu există evaluări
- Polynevrite Pathologie Musculaire PRN - IFSIDocument48 paginiPolynevrite Pathologie Musculaire PRN - IFSIMouad AbritÎncă nu există evaluări
- Alzheimer : fatalité ou espoir ?: Une étude pour mieux appréhender la maladieDe la EverandAlzheimer : fatalité ou espoir ?: Une étude pour mieux appréhender la maladieÎncă nu există evaluări
- Les coliques du cheval : diagnostic et traitementDe la EverandLes coliques du cheval : diagnostic et traitementÎncă nu există evaluări
- Endocrino PDFDocument311 paginiEndocrino PDFتقوى اللهÎncă nu există evaluări
- Pediatrie DP1Document26 paginiPediatrie DP1Lina NouriÎncă nu există evaluări
- Les Fondamentaux de La Pathologie Neurologique 2023Document638 paginiLes Fondamentaux de La Pathologie Neurologique 2023Doc Lotfi OmriÎncă nu există evaluări
- Anatomie-Physiologie Du Systeme Nerveux 2013041712271888Document38 paginiAnatomie-Physiologie Du Systeme Nerveux 2013041712271888Jo HannaÎncă nu există evaluări
- Bilan Et Prise en Charge Des Maladies NeuromusculairesDocument11 paginiBilan Et Prise en Charge Des Maladies NeuromusculairesEddy BOUABIDAÎncă nu există evaluări
- Neuro Anatomie SemioDocument58 paginiNeuro Anatomie SemiodorinatcaciÎncă nu există evaluări
- 24-Diarrhées Chroniques Chez L'enfant Fevrier 2023.ppsxDocument47 pagini24-Diarrhées Chroniques Chez L'enfant Fevrier 2023.ppsxmonsif el ansariÎncă nu există evaluări
- PORPHYRINESDocument4 paginiPORPHYRINESFranck BitaÎncă nu există evaluări
- Cours de Neurologie FinDocument130 paginiCours de Neurologie FinWillson Peter Dungu businessÎncă nu există evaluări
- TP N - 2 - Examen Clinique InteractifDocument20 paginiTP N - 2 - Examen Clinique Interactifanis anisÎncă nu există evaluări
- 19.04.diarrhée ChroniqueDocument11 pagini19.04.diarrhée ChroniqueAna ManaÎncă nu există evaluări
- Neuro Bruce L LoseDocument13 paginiNeuro Bruce L LoseaissaÎncă nu există evaluări
- Syndrome Pyramidal-1Document23 paginiSyndrome Pyramidal-1Stesy NancyÎncă nu există evaluări
- 1.syndromes TopographiquesDocument45 pagini1.syndromes Topographiquessally croweÎncă nu există evaluări
- Coma de L'enfantDocument23 paginiComa de L'enfantIdiAmadouÎncă nu există evaluări
- Syndrome VestibulaireDocument2 paginiSyndrome VestibulaireSouheil MansouriÎncă nu există evaluări
- Rappel Anatomo Physiologique Du Système NerveuxDocument58 paginiRappel Anatomo Physiologique Du Système Nerveuxlina mezianÎncă nu există evaluări
- Drepanocytose Cas Clinique PediatrieDocument16 paginiDrepanocytose Cas Clinique PediatrieEya EL KAMELÎncă nu există evaluări
- Pediatrie CompleteDocument67 paginiPediatrie Completerabe deimonoÎncă nu există evaluări
- IMC Et Syndrome de LittleDocument17 paginiIMC Et Syndrome de LittleAchwak AliÎncă nu există evaluări
- Prise en Charge Des Vertiges en UrgenceDocument30 paginiPrise en Charge Des Vertiges en UrgenceAbdelmoumen DjazairiÎncă nu există evaluări
- SD CerebDocument22 paginiSD Cereb31243564Încă nu există evaluări
- Immunoglobuline Monoclonale Et Orientation DiagnostiqueDocument7 paginiImmunoglobuline Monoclonale Et Orientation DiagnostiqueabdellahÎncă nu există evaluări
- Pathologies Pédiatriques Aigues PDFDocument47 paginiPathologies Pédiatriques Aigues PDFMahefa Serge RakotozafyÎncă nu există evaluări
- Urgences Chirurgicales NéonatalesDocument18 paginiUrgences Chirurgicales Néonataleskajol14100% (3)
- Neuro Pathologie Poly PS 2000 PDFDocument83 paginiNeuro Pathologie Poly PS 2000 PDFJi JaneÎncă nu există evaluări
- LVR EndocrinorpDocument69 paginiLVR EndocrinorpFlamant RoseÎncă nu există evaluări
- Chaine RespiratoireDocument1 paginăChaine RespiratoireayoubborombaÎncă nu există evaluări
- 241 284 Neuroradiologie PDFDocument44 pagini241 284 Neuroradiologie PDFEliza CrăciunÎncă nu există evaluări
- Math3as Resume Hamada-Handasa Fada2iaDocument5 paginiMath3as Resume Hamada-Handasa Fada2iachaimabnzÎncă nu există evaluări
- Urgences-Respiratoires SommaireDocument16 paginiUrgences-Respiratoires SommaireFaycal TabetÎncă nu există evaluări
- Guide Complet V2021.07.16Document244 paginiGuide Complet V2021.07.16BecausegrÎncă nu există evaluări
- Myosites À InclusionsDocument10 paginiMyosites À InclusionsAbdou RahmouniÎncă nu există evaluări
- La Drépanocytose en PédiatrieDocument28 paginiLa Drépanocytose en PédiatriepepeÎncă nu există evaluări
- 3.Sd Myogène, Neurogène Périphérique - Pyramidal 2018Document57 pagini3.Sd Myogène, Neurogène Périphérique - Pyramidal 2018soualhi1819Încă nu există evaluări
- Tumeurs Du SNPDocument11 paginiTumeurs Du SNPyaalaÎncă nu există evaluări
- 2 - HAS - Accident Vasculaire Cerebral Prise en Charge Precoce PDFDocument21 pagini2 - HAS - Accident Vasculaire Cerebral Prise en Charge Precoce PDFSonia MarchÎncă nu există evaluări
- Manifestations Neurologiques Centrales Du SAPLDocument9 paginiManifestations Neurologiques Centrales Du SAPLAmine DounaneÎncă nu există evaluări
- Rachitisme CarencielDocument9 paginiRachitisme CarencielJude EmmanuelÎncă nu există evaluări
- Elevation Des CPK - Orientation DiagnostiqueDocument4 paginiElevation Des CPK - Orientation DiagnostiqueMedox007Încă nu există evaluări
- Syndrome CerebelleuxDocument7 paginiSyndrome CerebelleuxJosselin CrosatoÎncă nu există evaluări
- Les Accidents Vasulaires Cerebraux IschemiquesDocument58 paginiLes Accidents Vasulaires Cerebraux IschemiquesHASNA BENBARKAÎncă nu există evaluări
- Dossier Diagnostic Clinique de La Maladie D'Alzheimer 12-2021Document19 paginiDossier Diagnostic Clinique de La Maladie D'Alzheimer 12-2021mohamaed abbasÎncă nu există evaluări
- Table Ronde TANGER PDF Cas Cliniques 25 Janvier 2023 Clinique internationalePDFDocument88 paginiTable Ronde TANGER PDF Cas Cliniques 25 Janvier 2023 Clinique internationalePDFRoyd Jesse Kwibisa JrÎncă nu există evaluări
- BIO111 ChapitreI Suite 01Document5 paginiBIO111 ChapitreI Suite 01Berthe Aristide Ngue Nkongo100% (1)
- Hasboun Ens Master2007Document93 paginiHasboun Ens Master2007acbernevigÎncă nu există evaluări
- Sérologie de L'auto-ImmunitéDocument18 paginiSérologie de L'auto-Immunitéasmahane mohammediÎncă nu există evaluări
- Atlas Des Déformations Et Fractures VertébralesDocument355 paginiAtlas Des Déformations Et Fractures VertébralesMahamadou Amadou IdiÎncă nu există evaluări
- Syndrome MéningéDocument7 paginiSyndrome MéningéEbe100% (1)
- Lymphomes Intracraniens Du Sujet ImmunocompétentsDocument14 paginiLymphomes Intracraniens Du Sujet ImmunocompétentsyaalaÎncă nu există evaluări
- NeurolipidosesDocument11 paginiNeurolipidosesImene DerbalÎncă nu există evaluări
- 3 - Œdème Cérébral Nouvelles Pistes ThérapeutiquesDocument8 pagini3 - Œdème Cérébral Nouvelles Pistes ThérapeutiquesyaalaÎncă nu există evaluări
- 98 999Document4 pagini98 999hizballah27Încă nu există evaluări
- 98 805Document5 pagini98 805hizballah27Încă nu există evaluări
- 98 1011Document7 pagini98 1011hizballah27100% (1)
- 98 1003Document7 pagini98 1003hizballah27Încă nu există evaluări
- 98 802Document3 pagini98 802hizballah27Încă nu există evaluări
- 98 899Document6 pagini98 899hizballah27Încă nu există evaluări
- 98 919Document5 pagini98 919hizballah27Încă nu există evaluări
- 98 991Document7 pagini98 991hizballah27Încă nu există evaluări
- 98 987Document3 pagini98 987hizballah27Încă nu există evaluări
- Antagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À ProtonsDocument6 paginiAntagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À Protonshizballah27Încă nu există evaluări
- 98 909Document3 pagini98 909hizballah27Încă nu există evaluări
- 98 797Document5 pagini98 797hizballah27Încă nu există evaluări
- 98 913Document6 pagini98 913hizballah27Încă nu există evaluări
- 98 905Document4 pagini98 905hizballah27Încă nu există evaluări
- 98 887Document5 pagini98 887hizballah27100% (1)
- 98 881Document5 pagini98 881hizballah27Încă nu există evaluări
- 98 765Document5 pagini98 765hizballah27Încă nu există evaluări
- 98 875Document5 pagini98 875hizballah27Încă nu există evaluări
- 98 685Document3 pagini98 685hizballah27Încă nu există evaluări
- 98 689Document5 pagini98 689hizballah27Încă nu există evaluări
- 98 781Document5 pagini98 781hizballah27Încă nu există evaluări
- 98 787Document10 pagini98 787hizballah27Încă nu există evaluări
- 98 771Document6 pagini98 771hizballah27100% (1)
- 98 679Document6 pagini98 679hizballah27Încă nu există evaluări
- 98 671Document4 pagini98 671hizballah27Încă nu există evaluări
- Lipothymie, Syncope Et Perte de Connaissance Brève: Orientation DiagnostiqueDocument4 paginiLipothymie, Syncope Et Perte de Connaissance Brève: Orientation Diagnostiquehizballah27100% (1)
- 98 667Document4 pagini98 667hizballah27Încă nu există evaluări
- 98 657Document3 pagini98 657hizballah27Încă nu există evaluări
- 98 661Document6 pagini98 661hizballah27Încă nu există evaluări
- 98 653Document4 pagini98 653hizballah27Încă nu există evaluări
- Le Robot Qui RevaitDocument5 paginiLe Robot Qui Revaitdostoevsky.is.godÎncă nu există evaluări
- Bases de La Biologie Végétale Physiologie Et Méristèmes de Croissance 02Document66 paginiBases de La Biologie Végétale Physiologie Et Méristèmes de Croissance 02ali100% (2)
- Sujets de Revision Bepc 2022Document14 paginiSujets de Revision Bepc 2022Daniel KATCHOBI100% (2)
- Le Potentiel Des Peptides Antimicrobiens Comme BiocidesDocument24 paginiLe Potentiel Des Peptides Antimicrobiens Comme BiocidesbenoitdriencourtÎncă nu există evaluări
- TD5 Appareil de Golgi & Lysosomes 2021-2022Document3 paginiTD5 Appareil de Golgi & Lysosomes 2021-2022Ita ChiÎncă nu există evaluări
- Modes Ventilatoiresv 01Document63 paginiModes Ventilatoiresv 01Iria SoteloÎncă nu există evaluări
- Questions Sur Les 1er SecoursDocument3 paginiQuestions Sur Les 1er SecoursChloé FésignyÎncă nu există evaluări
- CE_Exercice-2_CorrigéDocument3 paginiCE_Exercice-2_CorrigéNhatran93Încă nu există evaluări
- AnatomieDocument33 paginiAnatomiedjuissi doriane100% (1)
- Rehabilitation Dun Edentement Unitaire Anterieur Par Prothese Implanto PorteeDocument207 paginiRehabilitation Dun Edentement Unitaire Anterieur Par Prothese Implanto PorteeMedecine DentaireÎncă nu există evaluări
- Métabolisme Des Acides Aminés Cours de Biochimie 2eme Année Pharmacie DR CHERIETDocument15 paginiMétabolisme Des Acides Aminés Cours de Biochimie 2eme Année Pharmacie DR CHERIETHea FÎncă nu există evaluări
- Partie3 PDFDocument192 paginiPartie3 PDFMich RAÎncă nu există evaluări
- Électrophysiologie Des MembranesDocument4 paginiÉlectrophysiologie Des Membranesyenom4bagÎncă nu există evaluări
- BIO111 ChapitreI Suite 01Document5 paginiBIO111 ChapitreI Suite 01Berthe Aristide Ngue Nkongo100% (1)
- Anatomie Obstétricale Du Pelvis Et de La TêteDocument27 paginiAnatomie Obstétricale Du Pelvis Et de La TêteIdiAmadouÎncă nu există evaluări
- Praticien en Ayurveda Module 13Document40 paginiPraticien en Ayurveda Module 13amandineÎncă nu există evaluări
- La Vascularisation de L EstomacDocument4 paginiLa Vascularisation de L EstomacHamza KarmouchiÎncă nu există evaluări
- Heart RapportDocument4 paginiHeart RapportMimikoÎncă nu există evaluări
- GoitreDocument5 paginiGoitreDoaa RialiÎncă nu există evaluări
- 2022 QR34 Systemes PortesDocument2 pagini2022 QR34 Systemes PortesGhislain AssogbaÎncă nu există evaluări
- SV-A-1 Vache - Nutri - Planches - SDDocument76 paginiSV-A-1 Vache - Nutri - Planches - SDmamywane9Încă nu există evaluări
- Drainage Manuel PDFDocument7 paginiDrainage Manuel PDFAlice Bchn100% (1)
- Choc HemorragiqueDocument2 paginiChoc HemorragiqueDembouz FÎncă nu există evaluări
- Expose-Croissance Des VegetauxDocument5 paginiExpose-Croissance Des VegetauxjamalÎncă nu există evaluări
- ALT GPT BR FR Rev. 02Document2 paginiALT GPT BR FR Rev. 02MOHAMEDÎncă nu există evaluări
- Le Recepteur T de L'Antigene: I-Introduction Ii - Structure Iii - GenetiqueDocument5 paginiLe Recepteur T de L'Antigene: I-Introduction Ii - Structure Iii - Genetiqueimane yakhlefÎncă nu există evaluări
- Burkina 2016 SVT Series C 1er Tour S1Document3 paginiBurkina 2016 SVT Series C 1er Tour S1narutoÎncă nu există evaluări
- SUJET BAC Blanc SERIE D SVT (Odienne 2023)Document4 paginiSUJET BAC Blanc SERIE D SVT (Odienne 2023)arsene BATAWUILAÎncă nu există evaluări