Documente Academic
Documente Profesional
Documente Cultură
Ejercicios Resueltos Sistema Hierro
Încărcat de
Edggar GarrafaDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Ejercicios Resueltos Sistema Hierro
Încărcat de
Edggar GarrafaDrepturi de autor:
Formate disponibile
EJERCICIOS RESUELTOS SISTEMA HIERRO-
CARBONO
30. Una pieza de acero de 50 Kg contiene 800 g de carbono. Se pide:
a) De que tipo de aleacin se trata?.
b) Cules son sus constituyentes y su estructura a temperatura ambiente?
c) Cul es su densidad a temperatura ambiente, sabiendo que la densidad del
hierro es de 7,87 g/cm
3
y la de la cementita Fe
3
C de 7,54 g/cm
3
?.
a) Calculamos en primer lugar el porcentaje de carbono que posee:
% 6 , 1 100
000 . 50
800
% = = C Por tanto se trata de un acero hipoeutectoide.
b) A partir del diagrama calculamos los constituyentes y su composicin o
estructura:
) % 33 , 93 , % 67 , 6 %( 24 %
) % 100 , % 0 ( % 76 100
67 , 6
6 , 1 67 , 6
%
Fe C Cementita
Fe C Ferrita
=
=
=
c) Finalmente la densidad () ser:
3
3
79 , 7 24 , 0 54 , 7 76 , 0 87 , 7 ) ( ) (
cm
g
C Fe = + = + = o
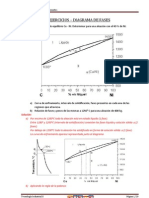
31. Un acero hipoeutectoide (0,4%C) se enfra lentamente desde 970 C hasta la
temperatura ambiente. Calcula a partir del diagrama Hierro-Carbono simplificado:
a) Las fracciones de Austenita () y Ferrita () proeutectoide que contendr
dicho acero cuando se halle a una temperatura justo por encima de la
eutectoiude (723+T).
b) Las fracciones de Ferrita () y Cementita (Fe
3
C) que contendr el acero
cuando se halle a una temperatura justo por debajo de la eutectoiude (723-T).
c) Las cantidad de ferrita eutectoide (secundaria) que contendr la perlita a una
temperatura justo por debajo de la eutectoiude (723-T).
a)
Fe y C con Austenita
Fe y C con
e oeutectoid Ferrita
% 1 , 99 % 89 , 0 % 44 %
% 98 , 99 % 02 , 0
) (Pr % 56 100
02 , 0 89 , 0
4 , 0 89 , 0
%
=
=
=
b)
c) Teniendo en cuenta que la austenita se transforma en perlita y que la
cantidad total de ferrita es del 94%, la cantidad de ferrita eutectoide que
contiene la perlita la obtenemos restando el 94% total menos el 56% de ferrita
proeutectoide (primaria):38%.
32. Un acero hipereutectoide (1,2%C) se enfra lentamente desde 970 C hasta la
temperatura ambiente. Calcula:
a) Las fracciones de Austenita () y Cementita (Fe
3
C) proeutectoide que
contendr dicho acero cuando se halle a una temperatura justo por encima de
la eutectoiude(723+T).
b) Las fracciones de Ferrita () y Cementita (Fe
3
C) que contendr el acero
cuando se halle a una temperatura justo por debajo de la eutectoiude (723-T).
c) La cantidad de cementita eutectoide que contendr la perlita a una
temperatura justo por debajo de la eutectoiude (723-T).
a)
Fe y C con con Cementita
Fe y C con
total Ferrita
% 33 , 93 % 67 , 6 % 6 %
% 98 , 99 % 02 , 0
) ( % 94 100
02 , 0 67 , 6
4 , 0 67 , 6
%
=
=
=
% 64 , 94 %
% 36 , 5 100
89 , 0 67 , 6
89 , 0 2 , 1
%
=
=
=
Austenita
Cementita
NOTA: la austenita () posteriormente se transforma en Perlita
(ferrita+cementita).
b)
c) Teniendo en cuenta que la cantidad total de cementita es del 17,75% y que la
cantiadad de cementita proeutectoide es del 5,36%, la cantidad de cementita
eutectoide que contiene la perlita ser ser por tanto del 12,39%; es decir:
Fe
3
C(eutectoide)= Fe
3
C(total)- Fe
3
C(proeutectoide)=17,75-5,36=12,39%
33. Una fundicin de composicin eutctica (4 %C) se enfra lentamente desde
1200 C hasta la temperatura ambiente. Calcula:
a) Las fracciones de Austenita () y Cementita (Fe
3
C) que contendr la aleacin
cuando se halle a una temperatura justo por debajo de la eutctica (1130-T).
b) Las cantidades relativas de Austenita () y las distintas clases de Cementita
(Fe
3
C) que contendr la fundicin a una temperatura justo por encima de la
eutectoiude (723+T).
c) Las cantidades relativas de todos los microconstituyentes cuando la fundicin
se halle a una temperatura justo por debajo de la eutectoiude (723-T).
a) A la temperatura por debajo de la eutctica la fundicin se encuentra en un
campo bifsico Austenita y Cementita de composicin:
) ( % 75 , 17 %
) ( % 25 , 82 100
02 , 0 67 , 6
2 , 1 67 , 6
%
total Cementita
total Ferrita
=
=
=
% 5 , 41 %
% 5 , 58 100
11 , 2 67 , 6
4 67 , 6
%
=
=
=
eutectica Cementita
Austenita
Ambas no aparecen de forma aislada sino formando un compuesto eutctico
denominado ledeburita
b) A una temperatura justo por encima de la eutectoide la aleacin
permanece en el mismo campo bifsico de composicin:
% 8 , 53 %
% 2 , 46 100
89 , 0 67 , 6
4 67 , 6
%
=
=
=
total Cementita
Austenita
Se observa que la cementita aparece de dos formas: como cementita eutctica
(41,5%) y como cementita proeutectoide (12,3%), que ser la diferencia entre
la cementita total (53,8%) y la eutctica (41,5%)
c) A una temperatura por debajo de la eutectoide tendremos dos fases,
ferrita y cementita de composicin:
% 85 , 59 %
% 15 , 40 100
02 , 0 67 , 6
4 67 , 6
%
=
=
=
Cementita
Ferrita
Se observa por tanto que ha ido aumentando la cantidad de cementita ya que
ahora se ha creado la cementita eutectoide asociada a la ferrita (perlita):
% 05 , 6 % 5 , 41 % 3 , 12 % 8 , 59
) ( ) ( ) ( ) (
3 3 3 3
= =
= eutctica C Fe ide proeutecto C Fe total C Fe eutectoide C Fe
34. Explica en que consiste el tratamiento trmico del temple, cuales son los factores
que influyen en l y que tipos de temple existen fundamentalmente.
Consiste en calentar el acero hasta una temperatura superior a la de austenizacin
(50C por encima de la temperatura Ac
1
y Ac
3
) al objeto de transformar toda la
masa en austenita (-FCC), seguido de un enfriamiento rpido (con velocidad
superior a la crtica) lo que permite que toda la austenita se transforme en
martensita e impidiendo de este modo la formacin de perlita y/o ferrita que son
ms blandos. Esta temperatura es mayor para los aceros hipoeutectoides que para
los hipereutectoides y con este tratamiento se consigue mejorar la dureza,
resistencia mecnica, elasticidad (disminuye), magnetismo, resistencia elctrica,
etc. Ejemplos: herramientas de corte, brocas, sierras, cuhillos, etc.
La velocidad crtica de temple se define como la velocidad de enfriamiento mnima
para que toda la masa de austenita se transforme en martensita (oscila entre 200-
600 C/seg). La velocidad de enfriamiento tambin influye en el tamao medio del
grano, siendo ste tanto menor cuanto mayor haya sido la velocidad.
Los factores que influyen en el temple son los siguientes:
- Composicin del acero: a mayor contenido de carbono o de otros elementos
si se trata de aceros aleados (Mo, Al, Si, W y V), menor velocidad de
enfriamiento se necesita y mayor dureza y profundidad de temple se
consigue.
- Temperatura de temple: los aceros hipoeutectoides ser necesario
calentarlos por encima de Ac3+50 C ya que el producto preutectoide es
ms blando (ferrita), mientras que los aceros hipereutectoides bastar con
hacerlo por encina de Ac1+50 C ya que la cementita en este caso es mas
dura.
- Tiempo de calentamiento: depende del tamao de la muestra ya que si el
tiempo es corto no se produce la austenizacin completa de la pieza, y si es
excesivo, se puede producir un grano grueso que empobrece el temple.
- Velocidad de enfriamiento: debe ser superior a la crtica para impedir que
se produzcan otras transformaciones indeseables de la austenita y
conseguir as la mxima dureza. Por su parte, la velocidad de enfriamiento
depende a su vez de la temperatura de temple, del medio refrigerante y de
las dimensiones de la pieza. As mientras el calentamiento se hace en hornos
especiales, el enfriamiento se puede hacer empleando: agua, aceite mineral,
baos de sales, aire, etc.
Existen varios tipos de temple entre los que podemos destacar (ver figura
siguiente):
- Temple continuo de austenizacin completa: se aplica en aceros
hipoeutectoides, calentando el material (ferrita+perlita) hasta
Ac3+50 C, seguido de un enfriamiento rpido hasta conseguir un
nico constituyente: la martensita.
- Temple continuo de austenizacin incompleta: se aplica en aceros
hipereutectoides, calentando el material (perlita+cementita) hasta
Ac1+50 C, por lo que ferrita de la perlita se transforma en
austenita, quedando intacta la cementita. Enfriando a la velocidad
adecuada obtenemos martensita+cementita.
- Temple escalonado martenstico: consiste en calentar la pieza de
acero hasta la austenizacin completa y enfriarla rpidamente en un
bao de sales hasta una temperatura prxima a 200-300 C, donde
se mantiene un tiempo para evitar as que la austenita sufra otro tipo
de transformacin. Una vez que la pieza ha adquirido esa
temperatura, se saca del bao y se enfra rpidamente hasta la
temperatura ambiente.
- Temple superficial: consiste en aplicar un temple superficial (entre 1
y 3 mm) a la pieza en cuestin, enfrindola de forma rpida. El
calentamiento se puede hacer por medio de soplete o por induccin
elctrica.
35. Explica en que consisten los tratamientos trmicos del recocido, normalizado y
revenido y sus principales caractersticas.
- Recocido: significa ablandamiento por calor y consiste en calentar el acero
entre 15 y 45 C por encima de Ac3 para los aceros hipoeutectoides y de
Ac1 para los hipereutectoides, seguido de un enfriamiento muy lento (por lo
general se apaga el horno y se deja que el material enfre en su interior). De
esta forma la velocidad de enfriamiento no es muy elevada como para
formar martensita, y lo que se obtiene es perlita+ ferrita de grano grueso
en el caso de los aceros hipoeutectoides o perlita+cementita de grano
grueso en el caso de los hipereutectoides.El recocido se aplica al acero para
ablandarlo y proporcionarle la ductilidad y maleabilidad suficientes para
conformarlo plsticamente o darle su forma final por mecanizado. Los
factores de que depende el recocido son bsicamente tres: temperatura de
calentamiento, tiempo de calentamiento y velocidad de enfriamiento. Se
aplica para eliminar los defectos del conformado en fro; es decir, para
ablandar y ductilizar un material agrio, como por ejemplo en la fabricacin
de alambre o en el estampado del latn.
- Normalizado: consiste en calentar el acero entre 55 y 85 C por encima de
la temperatura crtica superior (Ac3 para los aceros hipoeutectoides y de
Ac1 para los hipereutectoides), seguido de un enfriamiento al aire. De esta
forma la velocidad de enfriamiento no es muy elevada como para formar
martensita, y lo que se obtiene es perlita+ ferrita de grano fino en el caso
de los aceros hipoeutectoides o perlita+cementita de grano fino en el caso
de los hipereutectoides.
El objetivo que se pretende con este tratamiento es volver al acero a su
estado normal, y se suele aplicar a los aceros que se han deformado
plsticamente por laminacin o forja (tienen una microestructura perltica
de grano fino) con el fin de afinar el tamao del grano y eliminar tensiones
internas.
C
Austenizacin Calentamiento Enfriamiento
Ac3
tiempo
Recocido
Normalizado
Temple
- Revenido: es un tratamiento que se suele aplicar a los aceros despus de
ser templados para reducir la fragilidad y las tensiones internas e
incrementar la ductilidad. Consiste en calentar las piezas despus de
templadas hasta una temperatura inferior al punto crtico (Ac1), seguido de
un enfriamiento ms bien lento con el fin de que la martensita del temple se
transforme en una estructura ms estable (BCC).
Su efecto depende de la temperatura de calentamiento, del tiempo de
permanencia en ella y de la estructura de la pieza (generalmente
martensita). Con este tratamiento conseguimos disminuir la dureza (ya que
se destruye parte del temple) y la resistencia mecnica y por el contrario
aumentar la tenacidad y la plasticidad de la pieza (martensita revenida).
36. Explica en que consisten los tratamientos termoqumicos y enumera los principales
tipos.
Son operaciones de calentamiento y enfriamiento de los aceros, durante los cuales
se modifica la composicin qumica del material, adicionando al mismo tiempo otros
elementos para mejorar sus propiedades superficiales tales como la dureza, la
resistencia a la corrosin, al desgaste y a los esfuerzos de fatiga. Los principales
son:
- Cementacin con carbono: Se aplica en piezas de acero con un bajo
contenido en carbono (<0,3%), aleados o no, sometidas a desgaste y a
golpes, es decir que poseen dureza superficial y resiliencia. Consiste en
aumentar la cantidad de carbono de la capa superficial, calentndola hasta
la temperatura de austenizacin en presencia de un medio cementante
(atmsfera donde existe carbono y oxgeno en estado atmico).
De esta forma el carbono se difunde por la superficie y en funcin del
tiempo de exposicin y de la temperatura vara el espesor (entre 0,5 y 1,5
mm) a conseguir.
- Nitruracin: es igualmente un tratamiento de endurecimiento superficial
aplicado a ciertos aceros y fundiciones, que se efecta en hornos especiales
exponiendo las piezas a una corriente de amoniaco (2NH
3
) a una
temperatura de 500 a 525 C. Los aceros nitrurados son ms duros y
resistentes a la corrosin y se utilizan para endurecer camisas de cilindros,
herramientas de corte, brocas, rboles de levas, etc.
- Cianuracin: se trata un mezcla de los dos anteriores ya que consiste en
endurecer la superficie de las piezas de acero a travs de una capa
superficial rica en carbono (cementacin) y en nitrgeno (nitruracin). Las
piezas a tratar se introducen en un bao lquido (mezcla de cloruro de
cianuro y carbonato sdico) a una temperatura entre 800-900 C y en
presencia de oxgeno del aire. Una vez que se consigue la capa adecuada en
funcin del tiempo de exposicin es conveniente darle un temple superficial
para aumentar su dureza.
- Sulfinizacin: permite incorporar una capa superficial de carbono, nitrgeno
y en especial azufre, a los aceros, a las aleaciones frricas y al cobre. Se
consigue introduciendo las piezas en un bao de sales a 565 C, aumentando
as la resistencia al desgaste y disminuyendo el coeficiente de rozamiento,
favoreciendo al mimo tiempo la lubricacin. Se utiliza en herramientas de
corte para mecanizado de torno y fresa por ejemplo.
37. Explica en que consisten los tratamientos mecnicos de los materiales y enumera
los principales tipos.
Son operaciones de deformacin del material, que permiten mediante esfuerzos
mecnicos, mejorar su estructura interna al eliminar fisuras (cavidades) y
tensiones internas. Estos tratamientos pueden ser:
- En fro: permiten deformar el material a temperatura ambiente por golpes o
laminacin (estampacin, trefilado, laminacin, y estirado)
- En caliente: una vez calentado permite deformar el material generalmente
por golpes (laminacin, inyeccin, extrusin y forja)
38. Explica en que consisten los tratamientos superficiales de los materiales e indica
cuales son los ms comunes.
Permiten mejorar la superficie del material sin alterar su composicin qumica.
Cualquier tratamiento de este tipo requiere que la superficie a tratar se someta
previamente a un proceso de pulido, desengrasado y decapado. Los ms comunes
son:
- Cromado: se deposita cromo sobre la superficie del material a proteger con
el fin de aumentar adems de su dureza superficial, su resistencia al
desgaste, al rayado y a la corrosin.
- Metalizacin: se proyecta con una pistola sobre la superficie en cuestin,
metal fundido pulverizado (oxgeno+acetileno+polvo metlico)
- Recubrimientos por inmersin: la pieza se somete en un bao de metal
fundido durante un tiempo, hablando entonces de galvanizado (cinc) y
estaado (estao). Los recubrimientos tambin se pueden hacer con
productos orgnicos (pinturas y lacas) o con inorgnicos como el vidrio
fundido.
- Electrolisis: controlando el tiempo de inmersin y la intensidad de corriente
(I), se puede controlar la cantidad de metal depositado. En este caso, el
metal protector (Zn) se utiliza como nodo y el metal a proteger como
ctodo, empleando como electrolito una solucin del metal que se ha de
depositar en forma de sulfatos (en este caso sulfato de cinc). Por este
procedimiento se realiza el cobreado, niquelado, cincado, etc. Ver figura.
Pila
+
-
I
R
nodo
(Metal protector-Zn)
Ctodo
(Metal a proteger)
Zn
2+
39. Explica en que consiste el fenmeno de la corrosin y cuales son los
principales tipos.
Se puede definir como el deterioro lento de un material por la accin de un agente
exterior, en un ambiente hmedo y debido principalmente a reacciones de tipo
electroqumico. Por su parte, las reacciones electroqumicas, son reacciones de
oxidacin-reduccin, que tienen lugar cuando dos elementos distintos se ponen en
contacto a travs de un electrolito. As un metal M puede pasar de su estado
elemental a formar iones positivos por la prdida de n electrones, es lo que se
conoce como reaccin de oxidacin o reaccin andica:
+
+ ne M M
n
Para el caso del hierro (Fe) y el aluminio (Al) tenemos:
+
+
+
+
e Al Al
e Fe Fe
3
2
3
2
La reaccin inversa a la oxidacin es la reaccin de reduccin o reaccin catdica y
es la que toma los electrones de la oxidacin:
M ne M
n
+
+
Podemos decir por tanto que, la corrosin electroqumica se origina debido a la
formacin de pilas electroqumicas, en las que un metal determinado acta como
nodo y por tanto se disuelve. Este tipo de corrosin exige la presencia de
ambientes acuosos (hmedos) y en general con medios de conductividad
electroltica.
Los principales tipos de corrosin son:
- Corrosin uniforme: acta sobre toda la superficie del material expuesta a
la corrosin, disminuyendo su seccin de forma gradual. Se puede controlar
por medio recubrimientos.
- Corrosin galvnica: tiene lugar cuando dos metales con potenciales
distintos, que estn en contacto con un electrolito (agua, aire hmedo, etc.)
se ponen a su vez en contacto entre si. En este caso, los materiales que
tienen potenciales ms electronegativos, tendrn mayor facilidad a la
corrosin, por lo que no se deben juntar metales que estn muy separados en
la serie galvnica como por ejemplo Litio y Plata, procurando al mismo tiempo
que la superficie andica sea muy grande con respecto a la catdica. Para
evitar este problema, se recomienda recubrir previamente (pintura, plstico)
estos metales antes de juntarlos.
- Corrosin por grietas: se suele dar en grietas y rendijas en las que penetra
la suciedad y la humedad, con lo que las zonas exteriores estarn ms
aireadas y las interiores quedarn ms empobrecidas de oxgeno al gastarse
en la oxidacin y no poder ser renovado. Es frecuente en uniones remachadas
y atornilladas, as como en juntas por lo que la soldadura puede ser una buena
solucin.
- Corrosin intergranular: afecta a la unin de los granos de los
constituyentes de los metales, debilitando la resistencia del conjunto. Se da
cuando en los bornes del grano ha precipitado una
segunda fase (por ejemplo ferrita+cementita),
con lo cual se crea una celda galvnica en la cual la
ferrita es andica con respecto a la cementita. Se
produce por tanto una circulacin de electrones,
quedando libres los iones Fe
2+
de la ferrita, que se
combinan con los grupos hidrxido (OH
-
) del aire.
Finalmente lo que se forma es una capa de xido
Ferrita
Ferrita
Cementita
Fe
2+
Fe
2+
e
-
e
-
Fe(OH)
2
de hierro Fe(OH)
2
pegada a la cementita.
- Corrosin selectiva: el caso ms comn es el de la corrosin del cinc en el
latn (Cu-Zn), de tal forma que en la zona descincada slo queda cobre
poroso de color rojizo, pues el Zn es andico con respecto al Cu.
- Corrosin por erosin: se produce en las superficies que se encuentran en
contacto con un lquido que circula a gran velocidad (tubos, vlvulas, bombas,
etc.), que debido a la accin mecnica (desgaste) del fluido, va eliminando la
capa protectora de xido que se forma en los metales. Para corregirlo, es
necesario evitar turbulencias y burbujas as como elementos en suspensin.
40. Explica en que consiste el fenmeno de la oxidacin.
Cuando un metal se combina con el oxgeno del aire, transformndose en xidos
ms o menos complejos, se dice que experimenta una reaccin de oxidacin
(corrosin seca):
Material + Oxgeno xido de material Energa liberada en el proceso
El signo + o indica que en la reaccin se desprende o se absorbe energa, en cuyo
caso el material ser de difcil o fcil oxidacin. Considerando un metal divalente
(de valencia 2 como el Fe) y cuya oxidacin se verifica segn la reaccin:
FeO O Fe E MO O M + +
2 2
2
1
;
2
1
En este caso, se pueden producir dos tipos de reacciones:
- Reaccin endotrmica: hay aporte de energa y por tanto favorece la
oxidacin. Este es el caso por ejemplo, de cuando una pieza de acero se
somete a vapor de agua.
MO E O M + +
2
2
1
- Reaccin exotrmica: hay desprendimiento de energa, por ejemplo cuando
dos elementos de distinto nivel energtico tienden a juntarse, ambos
reaccionan y esa diferencia de energa la liberan en forma de calor (Na-O
2
),
por lo que el de menor nivel energtico se oxida rpidamente.
Recordar que cuando un metal se encuentra en una atmsfera oxidante, su
superficie se oxida ms o menos rpidamente en funcin de la energa liberada en
el proceso de oxidacin, y el xido que se forma en la parte exterior recubre el
metal. Una vez que se ha formado la primera capa de xido, para que el proceso
contine es necesario que el anin O
2-
atraviese por difusin la capa de xido, la
cual se opone al movimiento de stos y acta a su vez de capa protectora.
41. Explica cuando se forma una pila de corrosin electroqumica y cuales son sus
partes.
Una pila electroqumica se forma cuando dos piezas de metal se ponen en contacto
a travs de un lquido conductor o electroltico. Los componentes de una pila
electroqumica son:
- nodo: cede electrones por el circuito exterior al ctodo (reaccin de
oxidacin)
- Ctodo: recibe los electrones cedidos por el nodo (reaccin de reduccin),
mientras que los iones encargados de restablecer la neutralidad elctrica
circulan en sentido contrario a travs del tabique poroso o membrana
(permite la transferencia de carga pero no la mezcla de electrolitos).
- Electrolito: lquido que est en contacto con el nodo y el ctodo y
proporciona el medio a travs del cual los iones metlicos abandonan la
superficie del nodo y llegan al ctodo.
Ctodo
nodo
E
e
-
e
-
Electrolito
Iones
Debido a los dos tipos de reacciones (andica y catdica) que se producen en la
pila, los iones metlicos, tanto los aadidos al electrolito como los formados en
la reaccin del nodo, se combinan con los electrones del ctodo y como
consecuencia de ello el metal (ctodo) recubre su superficie.
Para determinar la tendencia a la corrosin (ceder electrones) de un
determinado elemento, se mide la diferencia de potencial entre el metal
(nodo) y un electrodo normal de hidrgeno (ctodo) tomado como referencia,
al que se le asigna un potencial arbitrario de 0V, sumergidos en una disolucin
de iones H
+
de concentracin 1M. Recuerda que la concentracin molar de una
disolucin es el nmero de moles de soluto contenidos en un litro de disolucin.
Finalmente la ecuacin de Nerst permite calcular el potencial de un metal
para una concentracin del electrolito distinta a 1M:
ion
C
n
E E log
0592 , 0
0
+ =
donde: E
0
es el potencial electrdico normal; n es la valencia del ion
metlico; C
ion
es la concentracin del electrolito.
42. Una pila electroqumica est formada por un electrodo de Zn sumergida en una
disolucin 1M de sulfato de cinc (ZnSO
4
) y por otro electrodo de Ni sumergido en otra
disolucin 1M de sulfato de nquel (NiSO
4
). Calcula:
a) La fuerza electromotriz (f.e.m.) de la pila (E) al conectar los dos electrodos.
b) Si las concentraciones son ahora de 0,05M (ZnSO
4
) y de 0,1M (NiSO
4
), cual
ser la nueva f.e.m.
E
e
-
e
-
Zn (nodo)
Ni (niquel)
Zn
2+
Ni
2+
+
a) Si la concentracin es la misma en los dos electrodos (1M) las reacciones
que se producen sern:
V E Ni Zn Ni Zn
Ni e Zn e Ni Zn Global R
Ni e Ni Catdica R
e Zn Zn Andica R
51 , 0 25 , 0 76 , 0
76 , 0 2 25 , 0 2 : .
25 , 0 2 : .
76 , 0 2 : .
2 2
2 2
2
2
= + + +
+ + + +
+
+
+ +
+ +
+
+
b) Suponiendo que el sentido de la reaccin sigue siendo el mismo, aplicando la
Ley de Nernst tenemos:
V ctodo E
V nodo E
2796 , 0 1 , 0 log
2
0592 , 0
25 , 0 ) (
8015 , 0 05 , 0 log
2
0592 , 0
76 , 0 ) (
= + =
= + =
Por tanto la nuevas reacciones sern:
V E Ni Zn Ni Zn
Ni e Zn e Ni Zn Global R
Ni e Ni Catdica R
e Zn Zn Andica R
5219 , 0 2796 , 0 8015 , 0
8015 , 0 2 2796 , 0 2 : .
2796 , 0 2 : .
8015 , 0 2 : .
2 2
2 2
2
2
= + + +
+ + + +
+
+
+ +
+ +
+
+
43. Explica como afecta la corrosin a los materiales en general
Se puede definir como el deterioro lento de un material por la accin de un
agente exterior, en un ambiente hmedo y debido principalmente a reacciones de
tipo electroqumico.. El trmino corrosin se aplica a la accin gradual de agentes
naturales, como el aire hmedo o el agua sobre los metales.
El ejemplo ms comn de corrosin es la oxidacin del hierro, que consiste en una
compleja reaccin qumica en la que el hierro se combina con oxgeno y agua para
formar xido de hierro hidratado. El xido es un slido que mantiene la misma
forma general que el metal del que se ha formado, pero con un aspecto poroso y
relativamente dbil y quebradizo.
Hay tres mtodos para evitar la oxidacin del hierro:
a) Mediante aleaciones del hierro que lo convierten en qumicamente
resistente a la corrosin. Un buen ejemplo de ello es el acero inoxidable,
una aleacin de hierro con cromo y nquel. El mtodo de la aleacin es el
ms satisfactorio pero tambin el ms caro.
b) Impregnndolo con materiales que reaccionen a las sustancias corrosivas
ms fcilmente que el hierro, quedando ste protegido al consumirse
aqullas. El ejemplo ms frecuente es el hierro galvanizado que consiste
en hierro cubierto con cinc. En presencia de soluciones corrosivas se
establece un potencial elctrico entre el hierro y el cinc, que disuelve
ste y protege al hierro mientras dure el cinc.
c) Recubrindolo con una capa impermeable que impida el contacto con el aire
y el agua. En este caso, la proteccin de la superficie con una capa
impermeable, es el ms barato y por ello el ms comn. Este mtodo es
vlido mientras no aparezcan grietas en la capa exterior, en cuyo caso la
oxidacin se produce como si no existiera dicha capa. Si la capa
protectora es un metal inactivo, como el cromo o el estao, se establece
un potencial elctrico que protege la capa, pero que provoca la oxidacin
acelerada del hierro. Los recubrimientos ms apreciados son los esmaltes
horneados, y los menos costosos son las pinturas de minio de plomo.
Algunos metales como el aluminio, aunque son muy activos qumicamente, no
suelen sufrir corrosin en condiciones atmosfricas normales. Generalmente el
aluminio se corroe con facilidad, formando en la superficie del metal una fina
capa continua y transparente que lo protege de una corrosin acelerada. El plomo
y el cinc, aunque son menos activos que el aluminio, estn protegidos por una
pelcula semejante de xido. El cobre, comparativamente inactivo, se corroe
lentamente con el agua y el aire en presencia de cidos dbiles como la disolucin
de dixido de carbono en agua (que posee propiedades cidas), produciendo
carbonato de cobre bsico, verde y poroso. Los productos de corrosin verdes,
conocidos como cardenillo o ptina, aparecen en aleaciones de cobre como el
bronce y el latn, o en el cobre puro, y se aprecian con frecuencia en estatuas y
techos ornamentales.
Los metales llamados nobles son tan inactivos qumicamente que no sufren
corrosin atmosfrica. Entre ellos se encuentran el oro, la plata y el platino. La
combinacin de agua, aire y sulfuro de hidrgeno afecta a la plata, pero la cantidad
de sulfuro de hidrgeno normalmente presente en la atmsfera es tan escasa que
el grado de corrosin es insignificante, apareciendo nicamente un ennegrecimiento
causado por la formacin de sulfuro de plata. Este fenmeno puede apreciarse en
las joyas antiguas y en las cuberteras de plata.
S-ar putea să vă placă și
- Tratamientos TermicosResuletoDocument10 paginiTratamientos TermicosResuletoChus AsekasÎncă nu există evaluări
- Ejercicios Resueltos Sistema Hierro CarbonoDocument14 paginiEjercicios Resueltos Sistema Hierro CarbonoByron Jose Galeano Manzanares0% (1)
- Ejercicios Resueltos TTTDocument15 paginiEjercicios Resueltos TTTxerrox267Încă nu există evaluări
- Resueltos Fe-Fe3CDocument19 paginiResueltos Fe-Fe3CIsi CastilloÎncă nu există evaluări
- Capìtulo 9 Schey Procesos de Deformaciòn VolumètricaDocument55 paginiCapìtulo 9 Schey Procesos de Deformaciòn VolumètricaMiguel Angel López Navarrete100% (1)
- Ejercicio Práctico Diagrama Hierro CarbonoDocument4 paginiEjercicio Práctico Diagrama Hierro CarbonoVictor SalayaÎncă nu există evaluări
- Problemas Resueltos Diagramas TTTDocument22 paginiProblemas Resueltos Diagramas TTTMargarita Yaneth Cabrera Medrano100% (3)
- Fundicion Clases 2013 - 12 RiserDocument73 paginiFundicion Clases 2013 - 12 Risertaccama100% (2)
- Diagrama Fe Fe3CDocument37 paginiDiagrama Fe Fe3Calex roÎncă nu există evaluări
- Ejercicios Diagrama Fe-C - METALÚRGIA FÍSICA II - 2020 PDFDocument6 paginiEjercicios Diagrama Fe-C - METALÚRGIA FÍSICA II - 2020 PDFEmerson SivinchaÎncă nu există evaluări
- Ii Laboratorio de Metalurgia Física IiDocument17 paginiIi Laboratorio de Metalurgia Física IiAnonymous 4KiEElYÎncă nu există evaluări
- Diagrama Hierro CarbonoDocument14 paginiDiagrama Hierro CarbonoAnibal Vp100% (1)
- Metalografia Acero 4140 VespertinoDocument10 paginiMetalografia Acero 4140 VespertinoGabrielÎncă nu există evaluări
- Ejercicios Resueltos Diagrama de Fases - Daniel Gomariz - Ingeniería IndustrialDocument20 paginiEjercicios Resueltos Diagrama de Fases - Daniel Gomariz - Ingeniería IndustrialDaniel Gomariz63% (8)
- Diagramas TTT - Ejemplos y EjerciciosDocument5 paginiDiagramas TTT - Ejemplos y EjerciciosJuan Carlos Niño VargasÎncă nu există evaluări
- Cuestionario DurezaDocument6 paginiCuestionario DurezaAngelÎncă nu există evaluări
- Preguntas FundiciónDocument5 paginiPreguntas FundiciónRashOteroM100% (1)
- Enunciado Ejercicios Ensayo Jominy-LamontDocument7 paginiEnunciado Ejercicios Ensayo Jominy-LamontHolver Sivincha100% (2)
- Ejercicios de Tratamientos Termicos ResueltosDocument10 paginiEjercicios de Tratamientos Termicos ResueltosErik Yantas25% (4)
- Diagrama Hierro CarbonoDocument28 paginiDiagrama Hierro CarbonoDiego MirandaÎncă nu există evaluări
- Preguntas para El ExamenDocument12 paginiPreguntas para El ExamenEccRodoÎncă nu există evaluări
- Corrosion A Altas TemperaturasDocument10 paginiCorrosion A Altas Temperaturaskratox01Încă nu există evaluări
- M3 07 02 Sesión 2.-Fractografía PDFDocument97 paginiM3 07 02 Sesión 2.-Fractografía PDFBRUNO ADRIEL ZAMORA FERNÁNDEZÎncă nu există evaluări
- Informe de MetalografiaDocument54 paginiInforme de MetalografiaMaycol FernandoÎncă nu există evaluări
- Examen 02 Tratamientos TermicosDocument2 paginiExamen 02 Tratamientos TermicosGustavo Castro100% (1)
- Informe 5 Tratamientos TermicosDocument14 paginiInforme 5 Tratamientos TermicosCarbajal JavierÎncă nu există evaluări
- Cementado, Templado y Revenido AISI 1018Document31 paginiCementado, Templado y Revenido AISI 1018Ronaldo100% (1)
- Aleaciones FerrosasDocument69 paginiAleaciones FerrosasGabriel Ch100% (3)
- Examen de Metalurgia Fisica IIDocument4 paginiExamen de Metalurgia Fisica IIGamarra OrlandoÎncă nu există evaluări
- IV. - Metalurgia de La SoldaduraDocument31 paginiIV. - Metalurgia de La SoldaduraparedessegurÎncă nu există evaluări
- Microestructuras de Los AcerosDocument18 paginiMicroestructuras de Los AcerosCrystal Wood71% (14)
- Prob. de Tratamientos TermicosDocument58 paginiProb. de Tratamientos TermicosPaola Moya75% (4)
- Practica Cementación de AcerosDocument7 paginiPractica Cementación de AcerosStalyn LemaÎncă nu există evaluări
- Informe de Práctica de Fundicion en Molde de Arena Con AlmaDocument6 paginiInforme de Práctica de Fundicion en Molde de Arena Con AlmaHugo FaguaÎncă nu există evaluări
- CurvasTTT - Problemasresueltos A ColoresDocument74 paginiCurvasTTT - Problemasresueltos A ColoresJoseluis Campean Sedano50% (2)
- Problemas de Proceso de FundicionDocument20 paginiProblemas de Proceso de Fundiciongabriel castroÎncă nu există evaluări
- Ejercicios Resueltos Diagrama Hierro-Cab PDFDocument411 paginiEjercicios Resueltos Diagrama Hierro-Cab PDFJLVriverÎncă nu există evaluări
- Informe Ensayo JominyDocument8 paginiInforme Ensayo JominyLogan Sct0% (1)
- Libro - Procesos de Manufactura - 2ra Parte OkDocument71 paginiLibro - Procesos de Manufactura - 2ra Parte Okronald0% (1)
- PREGUNTAS Tercer Parcial TT 1Document28 paginiPREGUNTAS Tercer Parcial TT 1Arnold NiñoÎncă nu există evaluări
- Tipos de Hornos MetalurgicosDocument34 paginiTipos de Hornos MetalurgicosRocael Scmr80% (5)
- Sol-Ejercicios de Diagramas Fe-C-2021-1Document23 paginiSol-Ejercicios de Diagramas Fe-C-2021-1Andy Josue Rivera0% (1)
- ProblemasDocument8 paginiProblemasMiguel Buendia QuilicheÎncă nu există evaluări
- Ejercicios Resueltos Sistema HierroDocument13 paginiEjercicios Resueltos Sistema HierroMaykol Villanueva Tolentino100% (2)
- Ejercicios Resueltos Sistema Hierro - CarDocument14 paginiEjercicios Resueltos Sistema Hierro - CarBrandon ArceÎncă nu există evaluări
- Ventura - Fernando - Deber5Document4 paginiVentura - Fernando - Deber5JOSEPH FRANCISCO ALMACHI PALADINESÎncă nu există evaluări
- 02 - Tratamientos Térmicos en AcerosDocument17 pagini02 - Tratamientos Térmicos en AcerosCarlos BeltranÎncă nu există evaluări
- Taller 3Document4 paginiTaller 3elias muñoz100% (2)
- Tema 2.3 - Ejercicios ExtraDocument5 paginiTema 2.3 - Ejercicios ExtraGerard CerezoÎncă nu există evaluări
- TemperaturasDocument56 paginiTemperaturasJoel Mamani BordaÎncă nu există evaluări
- CAPII Tratamientos-Termicos FINALDocument59 paginiCAPII Tratamientos-Termicos FINALnelsonÎncă nu există evaluări
- PC4 Materiales PosibleDocument7 paginiPC4 Materiales PosibleSUSAN50% (2)
- EFIM2023IISEC2Document7 paginiEFIM2023IISEC2Carlos ArbaizaÎncă nu există evaluări
- 12 Tratamientos TermicosDocument50 pagini12 Tratamientos TermicosLuis ApoyalaÎncă nu există evaluări
- Tratam Term AcerosDocument73 paginiTratam Term AcerosCesar PiñeroÎncă nu există evaluări
- Clase 12 Materiales de Ingeniería II.Document6 paginiClase 12 Materiales de Ingeniería II.Luis Daniel Guzman CruzÎncă nu există evaluări
- Unidad 4 Ing de MaterialesDocument25 paginiUnidad 4 Ing de MaterialesIvan ReyesÎncă nu există evaluări
- Ejercicios TT Paolo LavadoDocument44 paginiEjercicios TT Paolo LavadoPAOLO MIGUEL LAVADO ESCALANTEÎncă nu există evaluări
- 05 T.T Temple Diagrama TTTDocument38 pagini05 T.T Temple Diagrama TTTJaime Alfonso Gonzalez Vivas100% (1)
- León y El HombreDocument7 paginiLeón y El HombreRoy Tristan SilvaÎncă nu există evaluări
- León y El HombreDocument7 paginiLeón y El HombreRoy Tristan SilvaÎncă nu există evaluări
- Baloncesto Kevin 777Document2 paginiBaloncesto Kevin 777Roy Tristan SilvaÎncă nu există evaluări
- GeologíaDocument18 paginiGeologíaRoy Tristan SilvaÎncă nu există evaluări
- HidrometalurgiaDocument183 paginiHidrometalurgiapablo reyes95% (19)
- Te Ama en Secreto Ese Soy YoDocument1 paginăTe Ama en Secreto Ese Soy YoRoy Tristan SilvaÎncă nu există evaluări
- Oficio Anco LimaDocument6 paginiOficio Anco LimaRoy Tristan SilvaÎncă nu există evaluări
- Tranf. Masa, EvaporacionDocument30 paginiTranf. Masa, EvaporacionRoy Tristan Silva0% (1)
- Tarea2 CQ LDCLDocument33 paginiTarea2 CQ LDCLdavidÎncă nu există evaluări
- IntroDocument16 paginiIntromileidisÎncă nu există evaluări
- La Producción y Exportación de Petróleo - Jose Vladislav Cedeño Rodriguez2Document3 paginiLa Producción y Exportación de Petróleo - Jose Vladislav Cedeño Rodriguez2Juniver GomezÎncă nu există evaluări
- Simbologia y Diagrama de FlujoDocument44 paginiSimbologia y Diagrama de FlujoMorocha BellaÎncă nu există evaluări
- Los Estándares de Calidad AmbientalDocument4 paginiLos Estándares de Calidad AmbientalKeeninBryanLeonZevallosÎncă nu există evaluări
- Chimeneas y RampasDocument11 paginiChimeneas y RampasvidaluncÎncă nu există evaluări
- Practica de Pipe FloDocument10 paginiPractica de Pipe FloJuanjo Sejas Salinas100% (1)
- UPS-GT002558-tesis de GradoDocument133 paginiUPS-GT002558-tesis de GradoWILSON MIGUEL QUISPE HERHUAYÎncă nu există evaluări
- Informe Final Rsu - Bambú Como Material de Construcción Grupo 3Document16 paginiInforme Final Rsu - Bambú Como Material de Construcción Grupo 3xiomara saldañaÎncă nu există evaluări
- Silabo UndacDocument9 paginiSilabo Undaceduardomayorca2012Încă nu există evaluări
- Pautas de Cableado y Conexión A Tierra para Variadores de CA Con Modulación de Ancho de Pulsos (PWM) (Drives-In001 - Es-P)Document110 paginiPautas de Cableado y Conexión A Tierra para Variadores de CA Con Modulación de Ancho de Pulsos (PWM) (Drives-In001 - Es-P)AlbinNavaÎncă nu există evaluări
- Copia de TEORIAS DEL ORIGEN DE LA TIERRADocument8 paginiCopia de TEORIAS DEL ORIGEN DE LA TIERRAByron ArguetaÎncă nu există evaluări
- Cables OLFLEX Areas Riesgo de ExplosiónDocument8 paginiCables OLFLEX Areas Riesgo de ExplosiónLapp Latinamerica Support Corp.100% (1)
- Presentacion,¿Qué Es La Sener?Document8 paginiPresentacion,¿Qué Es La Sener?Jesus WillmerÎncă nu există evaluări
- Prueba 4Document24 paginiPrueba 4Fernando OrdoñezÎncă nu există evaluări
- Turbina de GasDocument10 paginiTurbina de GasLuis Fernando DavilaÎncă nu există evaluări
- Catalogo Solartronic PDFDocument34 paginiCatalogo Solartronic PDFhannibal2004685Încă nu există evaluări
- Sistema GABIDocument89 paginiSistema GABIFabricio MarañonÎncă nu există evaluări
- Aporte Ejercicio 6 - EletricaDocument3 paginiAporte Ejercicio 6 - Eletricafelipe castroÎncă nu există evaluări
- NTC4579Document48 paginiNTC4579jhonja751Încă nu există evaluări
- Electricidad 1 2Document3 paginiElectricidad 1 2trinidad viturro diestesÎncă nu există evaluări
- Consulta Historia de La Ceramica en EcuadorDocument3 paginiConsulta Historia de La Ceramica en EcuadorSelena Jimenez RamirezÎncă nu există evaluări
- Bladders de AcumuladoresDocument48 paginiBladders de Acumuladoresjorvasqu100% (1)
- Trabajo y Potencia InformeDocument13 paginiTrabajo y Potencia InformeAna Martinez100% (2)
- Altos Explosivos - Agentes de VoladuraDocument49 paginiAltos Explosivos - Agentes de VoladuramarcoÎncă nu există evaluări
- Que Impacto Tiene La Clorofila Sobre El PlanetaDocument3 paginiQue Impacto Tiene La Clorofila Sobre El PlanetaRAUL NAVARRO SALGADO0% (2)
- Evaporacion HidrologiaDocument7 paginiEvaporacion HidrologiaRoberth VillafuerteÎncă nu există evaluări
- Transistor de Inducción EstáticaDocument12 paginiTransistor de Inducción EstáticaAlxNelSonCarrascoArauco100% (2)
- Ge - Proyecto Módulo Gerencia Estratégica Ent2Document39 paginiGe - Proyecto Módulo Gerencia Estratégica Ent2Estevan DávilaÎncă nu există evaluări
- ACTIVIDADn 3Document5 paginiACTIVIDADn 3Jösüe Dävïd LïzäräzöÎncă nu există evaluări