Documente Academic
Documente Profesional
Documente Cultură
Ejercitario Primera Ley-Amb.
Încărcat de
Gema RodriguezDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Ejercitario Primera Ley-Amb.
Încărcat de
Gema RodriguezDrepturi de autor:
Formate disponibile
FACULTAD DE CIENCIAS AGRARIAS - UNA FISICA APLICADA - EJERCITARIO III Carrera: Ing. Ambiental Secciones: Primera Segunda Prof.
. Lic. Laura Snchez/Lic. Ruth Meaurio Auxiliar: Lic. Cristina Vega
TERMODINMICA Primea Ley Recordemos ciertos conceptos y ecuaciones a utilizar en la resolucin de los problemas. W>0 Trabajo realizado por el sistema contra el entorno. Ejemplo: un gas en expansin. W<0 Trabajo realizado por el entorno contra el sistema. Ejemplo: compresin de un gas. (Primera Ley de la Termodinmica) (Trabajo efectuado en un cambio de volumen a presin constante) Q y W dependen de la trayectoria U no depende de la trayectoria, slo de los estados inicial y final Proceso cclico El sistema vuelve a su estado inicial por lo tanto , lo que resulta que Sistema aislado El sistema no realiza trabajo sobre su entorno ni intercambia calor con l. Es decir, , resultando que La energa interna de un sistema aislado es constante. Tipos de procesos termodinmicos. 1) Proceso adiabtico: no entra ni sale calor del sistema. y Cuando un sistema se expande adiabticamente, W>0, U<0 Cuando un sistema se comprime adiabticamente, W<0, U>0 Especficamente para un gas ideal se tiene que: , por lo tanto 2) Proceso isocrico: se efecta a volumen constante. W=0, por lo tanto U=Q Si se agrega energa mediante calor a un sistema que se mantiene a volumen constante, toda la energa transferida permanece en el sistema como un aumento en su energa interna. 3) Proceso isobrico: se efecta a presin constante.
Se puede calcular el trabajo por medio de la ecuacin:
FACULTAD DE CIENCIAS AGRARIAS - UNA FISICA APLICADA - EJERCITARIO III Carrera: Ing. Ambiental Secciones: Primera Segunda Prof. Lic. Laura Snchez/Lic. Ruth Meaurio Auxiliar: Lic. Cristina Vega
4) Proceso isotrmico: se efecta a temperatura constante. Para un gas ideal se tiene que U=0, por lo tanto Toda la energa que entre en el sistema como calor deber salir como trabajo efectuado por el sistema. Capacidad calorfica del gas ideal La capacidad calorfica molar a volumen constante se denota por CV. La capacidad calorfica molar a presin constante se denota por CP
Siendo R la constante de los gases. Razn de capacidades calorficas
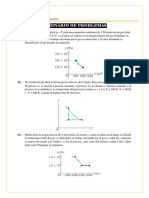
Calor especfico molar de un gas ideal (para un volumen constante) (para una presin constante) Resuelve los siguientes ejercicios 1) Un sistema se lleva por el ciclo de la figura, del estado a al estado b y de regreso al a. El valor absoluto de la transferencia de calor durante un ciclo es de 7200 J. a) El sistema absorbe o desprende calor cuando recorre el ciclo en la direccin indicada en la figura? b) Qu trabajo efecta el sistema en un ciclo? c) Si el sistema recorre el ciclo en direccin antihoraria, absorbe o desprende calor en un ciclo? Qu magnitud tiene el calor absorbido o desprendido en un ciclo antihorario? (Rta.: absorbe calor, 7200 J, 7200J) 2) Cuando una cantidad de gas ideal monoatmico se expande a presin constante de 4x104 Pa, el volumen del gas aumenta de 2x10-3 m3 a 8x10-3 m3. Cunto cambia la energa interna del gas? (Rta.: 3690J) 3) Se aumenta la temperatura de 5 moles de gas, de -10C a 20C. Calcule el calor que se deber transferir al gas, si ste es: a) He a presin constante de 1,5 atm; b) Ar a volumen constante de 8,2 m3; c) CO2 a presin constante de 20.000 Pa. (Rta.: 3120 J, 1870 J, 5540 J) 4) Un gas ideal se encierra en un cilindro con un pistn mvil encima de l. El pistn tiene una masa de 8000 g y un rea de 5 cm2 y tiene libertad de deslizarse hacia arriba y hacia abajo, lo que mantiene constante la presin del gas. Cunto trabajo se consume en el gas a medida que la temperatura de 0,2 moles del gas se elevan de 20C a 300C? (Rta.: 466J)
FACULTAD DE CIENCIAS AGRARIAS - UNA FISICA APLICADA - EJERCITARIO III Carrera: Ing. Ambiental Secciones: Primera Segunda Prof. Lic. Laura Snchez/Lic. Ruth Meaurio Auxiliar: Lic. Cristina Vega
5) Un gas se lleva a travs del proceso cclico descrito en la figura. a) Encuentre la energa neta transferida al sistema por calor durante un ciclo completo. b) Si el ciclo se invierte (esto es, el proceso sigue la trayectoria ACBA), Cul es la entrada de energa neta por cada ciclo por calor?
6) Una muestra de un gas ideal pasa por el proceso que se muestra en la figura. De A a B, el proceso es adiabtico, de B a C es isobrico con 100kJ de energa que entran al sistema por calor. De C a D el proceso es isotrmico, de D a A es isobrico con 150kJ de energa que salen del sistema por calor. Determine la diferencia de energa interna UB UA.
7) Un bloque de aluminio de 1 kg se calienta a presin atmosfrica de modo que su temperatura aumenta de 22C a 40C. Encuentre, a) el trabajo consumido en el aluminio, b) la energa agregada a l por calor, c) el cambio en su energa interna. 8) Una muestra de 2 moles de gas Helio, inicialmente a 300 K y 0,4 atm, se comprime isotrmicamente a 1,2 atm. Si nota que el Helio se comporta como gas ideal, encuentra a) el volumen final del gas, b) el trabajo consumido en el gas, c) la energa transferida por calor. (Rta.: a) 0,0041 m3, b) 5,48 kJ, c) 5,48 kJ) 9) Un gas ideal monoatmico (CV=3R/2) se expande a la presin constante desde un estado inicial a temperatura T1 a otro final a T2. El proceso se realiza aportando una cantidad de calor Q, lentamente y se determina de forma experimental la variacin de volumen, V. En funcin de T1, T2, Q y V, calcular: a) el nmero de moles, b) la presin, c) el volumen inicial. (Rta.: a) ; b) ; c) 10) Un mol de oxgeno gaseoso que ocupa inicialmente un volumen V=20 L a una presin p1=1,5.105 Pa, se expande muy lentamente hasta duplicar su volumen. Determinar la presin y temperatura del gas si el proceso seguido ha sido: a) isotrmico, b) isobrico, c) adiabtico. (Rta.: a) 361 K y 0,74 atm; b) 722 K y 1,48 atm; c) 273 K y 0,56 atm)
S-ar putea să vă placă și
- Ejercitario Leyes Termodinamica AgronomíaDocument5 paginiEjercitario Leyes Termodinamica AgronomíaRuth MeaurioÎncă nu există evaluări
- Ejercicios Recomendados-Termodinamica 1leyDocument3 paginiEjercicios Recomendados-Termodinamica 1leyLily Margareth ArrietaÎncă nu există evaluări
- S Sem14 Ses2 PPRIMERA LEYDocument2 paginiS Sem14 Ses2 PPRIMERA LEYBrandon TamaraÎncă nu există evaluări
- Ley de La TermoDocument27 paginiLey de La TermoNathaly AlvaradoÎncă nu există evaluări
- Taller Primer Quiz FISICA ONDASDocument3 paginiTaller Primer Quiz FISICA ONDASJuan Carlos Riveros MedinaÎncă nu există evaluări
- S14.s3+ +materialDocument9 paginiS14.s3+ +materialEmi GarciaÎncă nu există evaluări
- Problemas TermodinamicaDocument7 paginiProblemas TermodinamicaNey Smith Mijahuanca ChuquillanqueÎncă nu există evaluări
- Guia Termodinamica2Document4 paginiGuia Termodinamica2Daniel Cristóbal MéndezÎncă nu există evaluări
- 2016 0 NFG Semana 6Document92 pagini2016 0 NFG Semana 6Victor Nëkito Bostwick0% (1)
- 21 EcuascionesDocument4 pagini21 EcuascionesCarlos Herrera Delgado0% (1)
- Tarea Cap19 fs200Document2 paginiTarea Cap19 fs200el Catracho 504Încă nu există evaluări
- Termodinámica Ejercitación 1Document2 paginiTermodinámica Ejercitación 1Luis ContrerasÎncă nu există evaluări
- CAP - 4 1era Ley de La TermodinamicaDocument4 paginiCAP - 4 1era Ley de La TermodinamicaSteven B-Roen100% (1)
- Seminario 1 Ley TermodinámicaDocument2 paginiSeminario 1 Ley TermodinámicaDiego MillaÎncă nu există evaluări
- Semana 14 - TermodinámicaDocument48 paginiSemana 14 - TermodinámicaLeonel Agsgdf100% (1)
- Trabajo - Termodinamica PDFDocument2 paginiTrabajo - Termodinamica PDFExamenesPorWhatsappÎncă nu există evaluări
- Practica N°06 - Manrique Acuña KevinDocument9 paginiPractica N°06 - Manrique Acuña KevinKevin Keith Manrique Acuña100% (2)
- Taller Numero 3Document4 paginiTaller Numero 3Daniel DBÎncă nu există evaluări
- Primera Ley de TermodinamicaDocument3 paginiPrimera Ley de TermodinamicaCristian Andres Vargas GuerreroÎncă nu există evaluări
- 4 - Primera Ley de La TermodinamicaDocument17 pagini4 - Primera Ley de La TermodinamicaAMOGUSÎncă nu există evaluări
- Guia Cap19 y 20Document5 paginiGuia Cap19 y 20victrexÎncă nu există evaluări
- Principios de La TermodinamicaDocument3 paginiPrincipios de La Termodinamica1991aolÎncă nu există evaluări
- Ejercicios Termodinamica - Primera LeyDocument3 paginiEjercicios Termodinamica - Primera LeyMaria Teresa Gavalo VergaraÎncă nu există evaluări
- S05. s1 - Separata de Ejercicios para Clase (Termodinamica)Document19 paginiS05. s1 - Separata de Ejercicios para Clase (Termodinamica)AaronÎncă nu există evaluări
- Taller de Termodinamica Samuel Ortega y Gabriel MirandaDocument16 paginiTaller de Termodinamica Samuel Ortega y Gabriel MirandaGabriel MirandaÎncă nu există evaluări
- Clase 10. Primera Ley de La TermodinamicaDocument8 paginiClase 10. Primera Ley de La TermodinamicaAndres LeonÎncă nu există evaluări
- Termo Completoo!!Document25 paginiTermo Completoo!!drg88100% (4)
- Guía 1 PDFDocument3 paginiGuía 1 PDFDaniel Andres Roa UmañaÎncă nu există evaluări
- Procesos TermodinámicosDocument4 paginiProcesos TermodinámicosFernandoÎncă nu există evaluări
- Ilide - Info Problemas Semana 14 Sesion 1 Primera Ley de Termodinamica PRDocument2 paginiIlide - Info Problemas Semana 14 Sesion 1 Primera Ley de Termodinamica PRAkkiÎncă nu există evaluări
- Termoquímica IDocument24 paginiTermoquímica IALI EDSON MARTINEZ ZEGARRAÎncă nu există evaluări
- TallORI S07 08 OyC 2020 1Document4 paginiTallORI S07 08 OyC 2020 1jcaceresaleÎncă nu există evaluări
- Guia Leyes TermodinamicaDocument6 paginiGuia Leyes TermodinamicaPollito ValorantÎncă nu există evaluări
- Term Odin A MicaDocument23 paginiTerm Odin A MicaDiego NavarroÎncă nu există evaluări
- Tarea 3Document7 paginiTarea 3Felipe SanhuezaÎncă nu există evaluări
- Problemas Propuestos Primera LeyDocument3 paginiProblemas Propuestos Primera LeyJunior PeñaÎncă nu există evaluări
- 07-1 - Práctica Primer PpioDocument3 pagini07-1 - Práctica Primer PpioEmilia TamantiniÎncă nu există evaluări
- Guía5 Ejerc Termodinamica 4os DifDocument4 paginiGuía5 Ejerc Termodinamica 4os DifalxcalixÎncă nu există evaluări
- Hoja de Problemas #04Document4 paginiHoja de Problemas #04Paul Quiroz AliagaÎncă nu există evaluări
- Taller 2 FisicoquímicaDocument12 paginiTaller 2 FisicoquímicaRAFAEL ENRIQUE ESQUIVEL MERCADOÎncă nu există evaluări
- Fisica 2 Semana 4Document24 paginiFisica 2 Semana 4Aldo EspinozaÎncă nu există evaluări
- TERMODINAMICADocument2 paginiTERMODINAMICARosanaEstela0% (1)
- Solucion Tarea1 TermodinamicaDocument3 paginiSolucion Tarea1 TermodinamicaJMGHÎncă nu există evaluări
- 1er Taller de Ejercicios - TermodinámicaDocument8 pagini1er Taller de Ejercicios - Termodinámicacamilo cifuentesÎncă nu există evaluări
- Serie de Primera Ley 20-IiDocument3 paginiSerie de Primera Ley 20-IiKarina Fernanda0% (1)
- La Termodinamica Ejercicios ResueltosDocument120 paginiLa Termodinamica Ejercicios ResueltosLuis Anara Ticona78% (9)
- TermoQca Taller No. 4 2018-1Document1 paginăTermoQca Taller No. 4 2018-1Mauricio Taborda MontañoÎncă nu există evaluări
- Guia de TermodinamiaDocument8 paginiGuia de TermodinamiaByDiego :3Încă nu există evaluări
- Programa INAP Mujeres Intensivo Reformulado para Enviar A NachaDocument2 paginiPrograma INAP Mujeres Intensivo Reformulado para Enviar A NachaChristianAprosoffÎncă nu există evaluări
- 1° ParcialDocument8 pagini1° ParcialManuel SolisÎncă nu există evaluări
- Biofisica Del Transporte Corte 2Document2 paginiBiofisica Del Transporte Corte 2Nataly BonillaÎncă nu există evaluări
- B TermodinamicaDocument2 paginiB TermodinamicaOscar OcsaÎncă nu există evaluări
- Ejercitario Leyes TermodinamicaDocument3 paginiEjercitario Leyes TermodinamicaPEDRO REYESÎncă nu există evaluări
- Práctica 06Document3 paginiPráctica 06TadeoÎncă nu există evaluări
- 9 TermodinamicaDocument14 pagini9 TermodinamicaStephy ValenciaÎncă nu există evaluări
- Quimica FDocument3 paginiQuimica FDaniela ObregónÎncă nu există evaluări
- Taller de TermodinamicaDocument8 paginiTaller de TermodinamicaFabián SawÎncă nu există evaluări
- Ciclo Del AzufreDocument12 paginiCiclo Del AzufremaiÎncă nu există evaluări
- 2 Concreto PreesforzadoDocument12 pagini2 Concreto PreesforzadoJuan Pablo Muñoz RomeroÎncă nu există evaluări
- Diagramas de Transformación Isotérmica Gerardo HuertaDocument7 paginiDiagramas de Transformación Isotérmica Gerardo HuertaGerardo HuertaÎncă nu există evaluări
- TEMA3-Reología de Las RocasDocument20 paginiTEMA3-Reología de Las Rocasmarcos_ayala_12Încă nu există evaluări
- ManualDocument10 paginiManualJosé A. GilÎncă nu există evaluări
- Proyecto de Curso IC-0801 II-22Document5 paginiProyecto de Curso IC-0801 II-22Daniel Ovares ArroyoÎncă nu există evaluări
- Detector de Hall de Conductividad Electrolítica Análisis InstrumentalDocument13 paginiDetector de Hall de Conductividad Electrolítica Análisis InstrumentalNadiaLizbethFlores100% (1)
- Informe Viaje CollpaDocument9 paginiInforme Viaje Collpamelina aguilar chiraÎncă nu există evaluări
- Reporte #4 Preparacion Sistemas ColoidalesDocument7 paginiReporte #4 Preparacion Sistemas ColoidalesJorge RenánÎncă nu există evaluări
- Laboratorio #4: Reacciones Orgánicas: Asignatura Química OrgánicaDocument6 paginiLaboratorio #4: Reacciones Orgánicas: Asignatura Química OrgánicaJhojan JairoÎncă nu există evaluări
- UNIDAD II. Teoria Atomica y FormulasDocument96 paginiUNIDAD II. Teoria Atomica y FormulasCorronchaÎncă nu există evaluări
- Fertilizantes de Ultima GeneracionDocument6 paginiFertilizantes de Ultima GeneracionAtaulfo RomeroÎncă nu există evaluări
- IE - MD y MC - MSC - 12.01.2022 - 13.15PMDocument16 paginiIE - MD y MC - MSC - 12.01.2022 - 13.15PMfernandoÎncă nu există evaluări
- PTQ 2018-I Guía PrácticasDocument62 paginiPTQ 2018-I Guía PrácticasErick AlorÎncă nu există evaluări
- Elementos de Sostenimiento-Mecanica de RocasDocument41 paginiElementos de Sostenimiento-Mecanica de RocasFernando Medina100% (1)
- Cuestionario Elaboración de PapelDocument5 paginiCuestionario Elaboración de PapelDayana B. Villena100% (2)
- Origen Del PetroleoDocument24 paginiOrigen Del PetroleoAnonymous 64HDY7IiN0Încă nu există evaluări
- Enunciado GeocienciasDocument12 paginiEnunciado Geocienciasnicolas sebastian garcia pradaÎncă nu există evaluări
- Practica 7Document12 paginiPractica 7karla Yessenia Gomez SantiagoÎncă nu există evaluări
- Agua y ElectrolitosDocument23 paginiAgua y ElectrolitosRoxy LuceroÎncă nu există evaluări
- Cinetica de La CorrosionDocument13 paginiCinetica de La CorrosionAris Cardenas Huaman100% (1)
- Lavadoras ExtractorasDocument82 paginiLavadoras ExtractorasFernando TovarÎncă nu există evaluări
- Ensayo DesengrasanteDocument8 paginiEnsayo DesengrasanteCesar SalazarÎncă nu există evaluări
- Lista de Precios Labperu 2016Document1 paginăLista de Precios Labperu 2016Hugo Leonidas Acosta GrandezÎncă nu există evaluări
- Mecanizado Sin Arranque de Viruta PDFDocument47 paginiMecanizado Sin Arranque de Viruta PDFMaxter DragonÎncă nu există evaluări
- SAL Ganazufre-3-14Document1 paginăSAL Ganazufre-3-14Rafael ArdilaÎncă nu există evaluări
- Práctica 9 - Titulaciones ComplejométricasDocument7 paginiPráctica 9 - Titulaciones ComplejométricasBrandon obando chavarriaÎncă nu există evaluări
- Trabajo de DurezasDocument8 paginiTrabajo de DurezasLayonel Arencibia LuzardoÎncă nu există evaluări
- PRACTICA 07 ElectrolisisDocument6 paginiPRACTICA 07 ElectrolisisDiego SkateÎncă nu există evaluări
- Guía 5 Verificacion de Pie de Rey - Garcia - EspinozaDocument24 paginiGuía 5 Verificacion de Pie de Rey - Garcia - EspinozaChristianGarcía100% (1)