Documente Academic
Documente Profesional
Documente Cultură
Acetato Metilo
Încărcat de
Gus Ortega PedrazaTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Acetato Metilo
Încărcat de
Gus Ortega PedrazaDrepturi de autor:
Formate disponibile
PRODUCCI N DE ACETATO DE METI LO
Descripcin del proceso
Los reactivos son almacenados en un tanque diferente cada uno a una temperatura de 25C, es
importante saber que ambos, metanol y cido actico, estan concentrados para escoger el material
de los tanques, de dichos tanques cada reactivo es subido por una tubera de 1.5 plg tamao
nominal por medio de dos bombas, una para cada uno, para ser introducidos a los respectivos
interacambiadores de calor para su acondicionamiento antes de ingresar al reactor. La entrada de
alimentacin a dicho reactor est a la altura de la salida de los intercambiadores. Dichos
intercambiadores trabajan con vapor de agua obtenido en una caldera (vvc) y en ellos se calientan
los reactivos hasta la temperatura de reaccin (328K). Toda la tubera utilizada es de acero de 1.5
plg tamao nominal.
Como el reactor trabaja isotrmicamente la corriente de salida contiene los dos reactivos y adems
acetato de metilo y agua, se encuentra a 328K, y de all es conducida a una bomba que la eleva
hasta una altura necesaria para alcanzar la etapa de alimentacin de la torre de destilacin I cuyo
producto de cabeza es una mezcla de metanol con acetato a la composicin azeotropica a 1.2 bar y
Temperatura azeotrpica, mientras el producto de cola es una mezcla de methanol, agua y cido
actico.
Posteriormente este producto de cola es llevado a la torre de destilacin III donde se separa la
mayor parte del methanol de la mezcla como producto de cabeza (con algo de agua y cido
actico) y teniendo como producto de cola cido actico diluido. Como en las dems torres de
destilacin es necesaria una bomba para llevar la corriente hasta la etapa de alimentacin.
El producto de cabeza es llevado a la torre I I donde se baja la presin drsticamente, empleando
una bomba de vaco, hasta 0.3 bar para desplazar el azeotropo acetato de metilo-metanol de
manera que el producto de cabeza pueda tener una alta composicin de acetato muy cercana a la
azeotropica. En cuanto al producto de cola de dicha torre es methanol y acetato en pequea
cantidad y con una composicin mayor de methanol.
Produccin Mundial:
El Acetato de metilo es producido en Venezuela, Estados Unidos y Alemania.
Produccin Colombiana:
En Colombia no se produce, por esta razn es importado de los pases productores.
Utilizacin o aplicabilidad del Acetato de Metilo:
El Acetato de Metilo de alta pureza es usado, en grandes cantidades, como intermediario en la
manufactura de gran variedad de poliesteres, como base para pelculas fotogrficas, como materia
prima para Acetato de Celulosa, plsticos de celulosa, filtros de cigarrillo y, principalmente, en la
produccin de solventes, colorantes y otros productos anlogos.
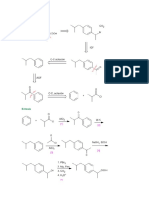
Mtodos de sntesis y cual es el mas usado:
Proceso para la produccin de Metil Acetato a partir de Metanol y Monxido de
Carbono utilizando un nuevo catalizador:
Resumen:
El metil acetato es preparado en buena produccin por reaccin de metanol con monxido de
carbono en presencia de un catalizador de composicin homognea que comprende un compuesto
que contiene rutenio, un compuesto que contiene cobalto y una base o sal cuaternaria de onium, y
calentando la mezcla resultante en una temperatura y presin elevada por suficiente tiempo para
producir el metil acetato deseado, y luego recuperar el mismo e la mezcla de reaccin.
Lo que se pretende es:
1. Un proceso para preparacin de metil acetato por metanol y monxido de carbono el cual
comprende el contacto de una mezcla de metanol y monxido con una cantidad cataltica
de un sistema catalizador de Yodo libre el cual comprende un compuesto que contiene
rutenio, un compuesto que contiene cobalto y una base o sal cuaternaria de onium,
calentando la mezcla resultante en una temperatura arriba de los 100 C y una presin
sobre atmosfrica por suficiente tiempo para producir el metil acetato deseado, y luego
recuperar el mismo de la mezcla en reaccin.
2. Un proceso como en 1 donde la mezcla en reaccin dicha es calentada en una temperatura
entre 150 C a 350C.
3. Un proceso como en 1 donde el proceso es conducido en una presin entre 1000 psi y
7560 psi.
4. Un proceso como en 1 donde el compuesto que contiene rutenio es un miembro del grupo
que consiste de xidos de rutenio, acetilacetonato de rutenio, y carbonil y
hidrocarboniliutenio.
5. Un proceso como en 1 donde el compuesto que contiene rutenio es un miembro del grupo
que consiste de dixido de rutenio anhidro 4, dixido de rutenio 4 hidratado, tetroxido de
rutenio 8, acetato de rutenio, propionato de rutenio, acetilacetonao de rutenio 3 y
dodecarbonil trirutenio.
6. Un proceso como en 1 donde el compuesto que contiene cobalto es un miembro del grupo
que consiste de carbonilos de cobalto y derivados de ellos obtenidos por reaccin del
carbonilo con un donante del grupo 5.
7. Un proceso como en 1 donde la base o sal cuaternaria de onium es una sal cuaternaria de
fosfonium.
8. Un proceso como en 1 donde la base o sal cuaternaria de onium es una sal cuaternaria de
amonio.
9. Un proceso como en 1 donde la base o sal cuaternaria de onium es una sal cuaternaria de
tetrahidrocarbilfosfonium.
10. Un proceso como en 1 donde la base o sal cuaternaria de onium es una sal cuaternaria de
tetralkilfosfonium.
Fondo de la invencin:
1. Campo de invencin:
Esta invencin relaciona nuevos procesos para preparar metil acetato. Mas particularmente,
la invencin relaciona un proceso desarrollado para preparar metil acetato desde metanol y
monxido de carbono utilizando un sistema de catlisis nuevo.
Especficamente, la invencin, provee un sistema nuevo y desarrollado para preparacin de
metil acetato.
2. Arte previo:
El metil acetato es un qumico el cual ha encontrado un amplio uso en la industria. El es
usado, por ejemplo, en la produccin de cido Actico anhidro, cido Actico y Etil Acetato,
y como un solvente o disolvente o diluente.
Varios mtodos han sido utilizados en el pasado para la produccin de acetato de metilo.
Este ester puede ser producido por ejemplo por la reaccin de alcohol metilico con cido
actico, el cual a la vez es obtenido por carbonilacion usando un promotor Yodo y Rhodio.
Una sntesis directa de alcohol metilico podra ser mas econmica y altamente deseable.
Ha sido propuesto preparar el acetato de metilo por carbonilacion directa de metanol, pero
estos mtodos no han sido enteramente satisfactorios porque ellos dan bajas producciones
del ester deseado o usan un catalizador costoso que es difcil de utilizar a gran escala.
Destilacin reactiva.
La destilacin reactiva es un proceso combinado, utilizado principalmente para aquellas reacciones
qumicas en las que el equilibrio de reaccin limita la conversin, en un reactor de lecho fijo, de un
nivel bajo a moderado. La separacin continua de uno de los productos, permite que la reaccin
proceda, a mucho mas alto nivel de conversin, en sentido directo.
Este es el procedimiento mas usado actualmente ya que sus caractersticas presentan ciertas
ventajas siendo una de las mas importante la disminucin en el consumo de energa y la reduccin
del costo de mantenimiento de los equipos. Por llevarse a cabo la reaccin qumica y la destilacin
en un mismo equipo, un paso del proceso es eliminado, en asocio con las bombas, vlvulas e
instrumentacin.
La destilacin reactiva se lleva a cabo en una columna de reaccin a contracorriente. La reaccin
ocurre en la zona media de la columna o seccin de reaccin, en una serie de etapas de
evaporacin a contracorriente. En la seccin superior, el agua es extrada con cido actico en la
zona de destilacin extractiva en la que se ubica la alimentacin de cido actico. El cido actico y
el acetato de metilo son separados por encima de la alimentacin de cido actico, en la seccin de
rectificacin. En la seccin mas baja de la columna, el metanol es despojado del agua. Por tanto, el
acetato de metilo refinado es el producto de la cabeza de la columna de destilacin reactiva, y el
agua es el producto de fondo.
Para hacer practico el concepto, debe seleccionarse un catalizador apropiado, y las impurezas de
punto intermedio de ebullicin, deben ser removidas mediante una corriente lateral en un punto
apropiado de la columna reactiva.
Produccin de mtil acetato en un reactor de esterificacin
El objeto de esta invencin es proporcionar un proceso para la produccin de metil acetato. Es un
proceso integrado que consiste de alimentacin continua de metanol y cido actico a un reactor
de esterificacin. Dicho reactor conteniendo inicialmente un solvente que forma un azeotropo de
punto e ebullicin mnimo y es insoluble en agua, luego ingresan el cido actico, el metanol y el
catalizador para la esterificacin, para producir un producto que contiene principalmente metil
acetato, metanol sin reaccionar, solvente y agua.
Destilando el producto en una torre de destilacin, obteniendo en los productos de cabeza una
corriente que contiene principalmente metil acetato, condensndolo, regresando una porcin a la
columna como reflujo y pasando el que permanece, con o sin purificacin posterior, a la siguiente
operacin, removiendo de un punto intermedio en la columna una fraccin de lquido lateral que
contiene agua, metil acetato y solvente con algo de metanol, enfriando esta faccin, separando la
fraccin por decantacin dentro de una fase orgnica superior que contiene principalmente solvente
y algo de metil acetato, y una fase acuosa inferior que comprende principalmente agua y algo de
metil acetato y metanol, retornando la fase orgnica separada a la columna en un punto ms bajo
de donde fue removida la fraccin y pasando la fase acuosa separada a una columna de stripping
donde una fase de base acuosa es separada de una fraccin de cabeza, la base acuosa es retirada
del proceso y la fraccin de cola recirculada al reactor de esterificacin y/o a la columna de
destilacin.
El solvente puede ser adicionado al reactor o en un punto apropiado de la columna de destilacin;
puede ser cualquier hidrocarburo, eter, ester o cetona, algunos ejemplos apropiados son: Tolueno,
di-isobutil eter, normal e isobutil acetato, metil isobutil cetona.
El catalizador apropiado puede ser un cido mineral como el sulfrico o uno orgnico como el
metanosulfnico, el cul es preferido aqu. El catalizador puede estar presente en cantidades de 0.1
al 10%, preferiblemente del 2 al 6% en peso total de masa reaccionante
Origen y accesibilidad de la materia prima:
cido Actico:
El cido Actico es de fcil adquisicin en nuestro pas. La empresa Sucromiles en Palmira, esa la
principal productora a nivel mundial de este compuesto (40000 lb/da), va biotecnolgica. Tambin
se importa de Estados Unidos. El cido actico es de fcil manipulacin y almacenamiento.
Metanol:
En Colombia no existe ninguna empresa manufacturera de metanol, sin embargo, ENKA de
Colombia lo tiene como subproducto, por lo que puede considerarse de fcil consecucin. En su
gran mayora se importa de Venezuela y Estados Unidos. El metanol es un compuesto de fcil
manipulacin.
Tipos de reactores que se utilizan
De acuerdo a lo investigado y resumido en las patentes anteriores los reactores que ms se
emplean en este tipo de reacciones (esterificacin), son los reactores de tanque agitado del tipo de
operacin continua y del tipo semibatch. La seleccin del reactor depende del tipo operacin de
separacin que se vaya a realizar, es decir, si se va a hacer una destilacin diferencial o una
continua.
Exigencias
Las siguientes especificaciones, aplicaciones, propiedades, almacenamiento y empacado del
producto fueron proporcionadas por la empresa ERKOL S.A. (USA)
Referencia: MM-80
Pureza: 79.5% en peso min.
Densidad a 20C: 0.902 0.003g/cm
3
Acidez: 0.05% en peso mx.
Contenido de agua: 0.05% en peso mx.
Aplicaciones: preparacin de solventes para lacas y una amplia variedad de resinas. Solvente
general para limpiar y remover pinturas y barnices con base de nitrocelulosa.
Empacado: contenedores de 20 a 25 TM de capacidad mx.
Almacenamiento: el MM-80 debe ser almacenado en reas ventiladas lejos de fuentes de ignicin y
sustancias oxidables incompatibles. Es estable a temperatura ambiente y bajo condiciones normales
de uso.
Seguridad I ndustrial
N I dentificacin de riesgos.
Peligro, lquido y vapor extremadamente flamable. El vapor puede causar una llamarada.
Causa irritacin en la piel, ojos y el tracto respiratorio, es fatal si se ingiere. Afecta el
sistema nervioso central.
Ratings:
Sanidad: 1-ligero.
Flamabilidad: 3-severo.
Reactividad: 1-ligero.
Equipo proteccin: gafas, delantal de laboratorio, ventilacin, guantes, extinguidor clase B.
Color de almacenamiento: Rojo (flamable).
Efectos en la salud
Inhalacin: la inhalacin de vapores causa irritacin de los ojos, nariz y tracto respiratorio;
los vapores tienen un efecto narctico, produciendo sntomas de disnesia, depresin,
desaliento y arritmia. Altas concentraciones pueden causar depresin CNS caracterizada por
la inflamacin de los ojos, irritacin neural, dolor de cabeza, disnesia, conjuntivitis y
somnolencia.
I ngestin: puede producir dolor abdominal, nauseas. La aspiracin en los pulmones
produce daos severos.
Contacto con la piel: causa prdida de aceites naturales e irritacin de la piel.
Contacto con los ojos: los vapores pueden causar irritacin con enrojecimiento, lloriqueo y
dolor.
h Primeros auxilios
Inhalacin: llevar aire fresco, si no responde dar respiracin artificial, si la respiracin es
difcil dar oxgeno. Dar atencin mdica
Ingestin: si lo ingiri, el vmito ocurre espontneamente, no inducir. Si vomita, colocar la
cabeza abajo para prevenir la aspiracin en los pulmones. Nunca d nada oral a una
persona inconsciente.
Contacto con la piel: lavar inmediatamente la piel con abundante agua durante 15 min.
Remueva la ropa y los zapatos contaminados.
Contacto con los ojos: lavar inmediatamente los ojos con abundante agua durante 15 min.
M Medidas de Fuego
Flash Point: -10C (14F)
Temperatura de autoignicin: 454C (849F)
Lmites Flamables en % de aire por volumen: lel: 3.1; vel: 16.
Explosin: Arriba del flash point las mezclas vapor aire son explosivas cerca de los lmites
notados arriba. Los contenedores sellados pueden romperse cuando son calentados.
Sensible a descargas estticas.
Medios para extinguir: qumicos secos, alcohol en espuma o dixido de carbono, el agua no
puede ser efectiva.
~ Medidas en caso de accidente
Ventilar el rea de escape o derrame. Remueva todas las superficies de ignicin. Aisl el
rea. Recoja el lquido e un contenedor o absorbedor apropiado con un material inerte
(verniculita, arena seca o tierra seca) y colquelo en un contenedor de desechos qumicos.
No use materiales combustibles. No inunde para desechar. Si la fuga o derrame no se ha
encendido, use spray de agua para dispersar los vapores.
> Manejo y almacenamiento
Proteja contra daos fsicos. Almacene en lugar fresco y seco, lejos de un rea donde haya
peligro de fuego. Se aconseja almacenamiento externo o por separado. Los contenedores
deben ser aislados y colocados en tierra para evitar descargas elctricas. En el rea de
almacenamiento no se debe fumar. Utilice herramientas antiestticas. Aslelo de sustancias
incompatibles.
Controles de exposicin y proteccin del personal.
Lmites de concentracin en el aire
- OSHA: Lmite permitido de exposicin (PEL): 200 ppm (TWA).
- ACGI H: Treshold limit value (TLV): 200 ppm (TWA) 250 ppm (STEL).
Sistema de ventilacin: Se recomienda un sistema local o general de escape. Generalmente
se usa el sistema local porque puede controlar las emisiones en la misma fuente de
contaminante, previniendo la dispersin en el aire total de trabajo.
Proteccin para la piel: ropa impermeable, botas, guantes, delantal de laboratorio.
Proteccin para los ojos: gafas qumicas de seguridad o una mscara.
> Estabilidad y reactividad
Estabilidad: estable a temperatura ambiente en contenedores sellados
Peligro por productos de descomposicin: se puede formar CO
2
y CO cuanta se calienta
para descomponer.
Peligro por Polimerizacin: no ocurre
Incompatibilidades: Nitratos, oxidantes fuertes, lcalis y cidos; reacciona lentamente con
el agua.
Condiciones a prevenir: Calor, llama, fuentes de ignicin e incompatibles.
N I nformacin Toxicolgica.
Oral R LD50>5g/kg; Piel R. LD50>50g/kg
Datos de irritacin: Piel R. 500mg/24h, suave, leve
Ojos R: 100mg/24h, moderado.
Propiedades del cido Actico.
Propiedades fsicas.
Densidad (g/cm
3
) 1.0492
ndice de refraccin 1.3716
Punto de fusin (c) 16.6
Punto de ebullicin (c) 117.9
Punto de flash (c) 39
Tensin superficial (dinas/cm
3)
a = 29.58 b = 0.0094
Constante dielctrica 6.15
Momento dipolar (debyes) 1.76
Masa molecular (g/gmol) 60.052
Viscosidad (N*s/m
2
) 1.232
Presin de vapor (mm Hg.) A = 16.8080 B = 3405.57 C = -56.340
Propiedades criticas.
T
c
(k) 594.4
P
c
(atm) 57.1
V
c
(cm
3
/gmol) 171.3
Z
c
0.2005
0.4477
Propiedades termodinmicas.
H
f
(kJ /mol) -484.4
G
f
(kJ /mol) -390.2
S
f
(J /c*mol) 159.9
C
p
(kJ /kmol*k)
v Gas ideal A + BT + CT
2
+ DT
3
+ ET
4
A = 6.89949 B = 257.0680*10
-3
E = -12.31750*10
-12
C = -191.771*10
-6
D = 75.7676*10
-9
v Liquido A + BT + CT
2
+ DT
3
A = 1.7791 B = 13.456*10
-4
C = -13.378*10
-7
D = 10.368*10
-10
Nota: Todas las propiedades a 20 C
La ecuacin para la tensin superficial es: = a b T (C)
La ecuacin para la presin de vapor es: ln P
v
= A B / (T + C), T en K
Propiedades del Metanol
Propiedades fsicas.
Densidad (g/cm
3
) 0.7913
ndice de refraccin 1.3284
Punto de fusin (c) -97.7
Punto de ebullicin (c) 64.7
Punto de flash (c) 12.0
Tensin superficial (dinas/cm
3)
a = 24.0 b = 0.0773
Constante dielctrica 33.62
Momento dipolar (debyes) 1.69
Masa molecular (g/gmol) 32.042
Viscosidad (N*s/m
2
) 0.544
Presin de vapor (mm Hg.) A = 18.5875 B = 3626.550 C = -34.290
Propiedades criticas.
T
c
(k) 512.6
P
c
(atm) 79.9
V
c
(cm
3
/gmol) 118.0
Z
c
0.2241
0.5553
Propiedades termodinmicas.
H
f
(kJ /mol) -239.30
G
f
(kJ /mol) -166.80
S
f
(J /c*mol) 127.20
C
p
(kJ /kmol*k)
v Gas ideal A + BT + CT
2
+ DT
3
+ ET
4
A = 34.49250 B = -29.18870*10
-3
C = 286.8440*10
-6
D = -312.5010*10
-9
E = 109.8330*10
-12
v Liquido A + BT + CT
2
+ DT
3
A = 1.82964*10 B = 4.72118*10
-1
C =-1.33878*10
-3
D = 1.31424*10
-6
Mezclas azeotrpicas binarias
Acetato de metilo Metanol
v Punto de ebullicin (c) 53.5
v Composicin (% peso )
Metanol 19.0
Acetato de metilo 81.0
Nota: Todas las propiedades a 20 C
La ecuacin para la tensin superficial es: = a b T (C)
La ecuacin para la presin de vapor es: ln P
v
= A B / (T + C), T en K
Propiedades del Acetato de Metilo.
Propiedades fsicas.
Densidad (g/cm
3
) 0.9342
ndice de refraccin 1.3619
Punto de fusin (c) -98
Punto de ebullicin (c) 57
Punto de flash (c) -10
Tensin superficial (dinas/cm
3)
a = 27.95 b = 0.1289
Constante dielctrica 7.03
Momento dipolar (debyes) 1.70
Masa molecular (g/gmol) 74.080
Viscosidad (N*s/m
2
) 0.388
Presin de vapor (mm Hg.) A = 16.7222 B = 2917.7017 C = -41.3724
Propiedades criticas.
T
c
(k) 506.8
P
c
(atm) 46.3
V
c
(cm
3
/gmol) 228.0
Z
c
0.2538
0.3206
Propiedades termodinmicas.
H
f
(kJ /mol) -445.8
G
f
(kJ /mol) ______
S
f
(J /c*mol) ______
C
p
(kJ /kmol*k)
v Gas ideal A + BT + CT
2
+ DT
3
+ ET
4
A = 48.02070 B = 112.2610*10
-3
C = 266.8210*10
-6
D = -403.3800*10
-9
E = 161.4930*10
-12
v Liquido A + BT + CT
2
+ DT
3
A = 1.9287 B = 29.090*10
-4
C = -113.01*10
-7
D = 168.380*10
-10
Mezclas azeotrpicas binarias
Acetato de metilo Metanol
v Punto de ebullicin (c) 53.5
v Composicin (% peso )
Metanol 19.0
Acetato de metilo 81.0
Acetato de metilo Agua
v Punto de ebullicin (c) 56.1
v Composicin (% peso )
Agua 5.0
Acetato de metilo 95.0
Nota: Todas las propiedades a 20 C
La ecuacin para la tensin superficial es: = a b T (C)
La ecuacin para la presin de vapor es: ln P
v
= A B / (T + C), T en K
Propiedades del Agua.
Propiedades fsicas.
Densidad (g/cm
3
) 0.99997
ndice de refraccin 1.333
Punto de fusin (c) 0.0
Punto de ebullicin (c) 100.0
Punto de flash (c) ------
Tensin superficial (dinas/cm
3) ---------
Constante dielctrica ------
Momento dipolar (debyes) ------
Masa molecular (g/gmol) 18.015
Viscosidad (N*s/m
2
) ------
Presin de vapor (mm Hg.) A = 18.3036 B = 3816.440 C = -46.130
Propiedades criticas.
T
c
(k) 647.3
P
c
(atm) 217.6
V
c
(cm
3
/gmol) 56.0
Z
c
0.2294
0.3206
Propiedades termodinmicas.
H
f
(kJ /mol) -285.83
G
f
(kJ /mol) -237.129
S
f
(J /c*mol) ---------
C
p
(kJ /kmol*k)
v Gas ideal A + BT + CT
2
+ DT
3
+ ET
4
A = 34.04710 B = -9.65064*10
-3
C = 32.9983*10
-6
D = -20.4467*10
-9
E = 4.30228*10
-12
v Liquido A + BT + CT
2
+ DT
3
A = 1.82964*10 B = 4.72118*10
-1
C =-1.33878*10
-3
D = 1.31424*10
-6
Nota: Todas las propiedades a 20 C
La ecuacin para la tensin superficial es: = a b T (C)
La ecuacin para la presin de vapor es: ln P
v
= A B / (T + C), T en K
Cintica Qumica
Para la reaccin reversible en fase lquida:
O H COOCH CH OH CH COOH CH
2 3 3 3 3
+ +
Tomando:
A: CH
3
COOH C: CH
3
COOCH
3
B: CH
3
OH D: H
2
O
La reaccin queda:
D C B A + +
La ecuacin de velocidad de reaccin para el reactivo A es:
-r
A
= K
1
C
A
C
B
K
2
C
D
C
C
Si K
e
es la constante de equilibrio y:
2
1
K
K
K
e
La ecuacin de velocidad queda:
1
]
1
e
D
b A A
K
CcC
C C K r
1
De acuerdo a lo presentado en la tesis Modelamiento matemtico y simulacin de una columna
para la obtencin de acetato de mtilo por destilacin reactiva, la ecuacin para K
1
es:
K
1
= K
3
.X
cat
+K
4
.X
cat
Donde :
X
cat
: composicin msica de catalizador
Las correspondientes ecuaciones para K
3
y K
4
son:
1
]
1
RT
Ea
K exp 485 . 0
3
Ea = 41800 J /mol
1
]
1
RT
Ea
K exp 123 . 0
4
Termodinmica, equilibrio qumico y de fases.
Para nuestro caso como no se dispona de datos bibliogrficos acerca de la conversin alcanzada en
esta reaccin, nos propusimos calcularla por medio de la Termodinmica y el equilibrio qumico.
A continuacin se presenta un algoritmo de clculo detallado.
Nuestra reaccin es:
D C B A
Cat
+ +
Debemos entrar los valores de calores de formacin ?H
f
0
y las energas libres de formacin
?G
f
0
de cada una de las sustancias a 298K.
Calculamos el cambio en la entalpa estndar y la energa de gibas estndar ? H
0
0
y ?G
0
0
respectivamente, a 298K
H
i
i
0
0
o
fi
H
G
i
i
0
0
o
fi
G
Donde s
i
es el coeficiente estequiomtrico de cada una de las sustancias presentes en la
reaccin, referido al reactivo lmite, en nuestro caso todos los coeficientes estequiomtricos
valen 1.
Asumimos una temperatura de reaccin para calcular el calor de reaccin o entalpa de
reaccin ? H
r
a esta Temperatura.
+
T
r
CpdT H H
15 . 298
0
0
?Cp= ?A+?BT+?CT
2
+?DT
3
i
i i
A A
i
i i
B B
i
i i
C C
i
i i
D D
Determinamos la constante de equilibrio a 298K por medio de ? G
0
0
:
RT
G
K
0
0
298
ln
Determinamos la constante de equilibrio a la Temperatura asumida por medio de la
ecuacin:
1
]
1
15 . 298
1 1
ln
0
298
T R
H
K
K
r
Ahora con la K calculada a la Temperatura supuesta determinamos el valor de ? G
0
por
medio de la ecuacin:
RT
G
K
0
ln
Como se puede apreciar en este clculo obtuvimos para un determinado valor de la
Temperatura un valor de la constante de equilibrio y de ? G
0
necesarios para determinar el
equilibrio qumico. Por medio de un programa se pueden obtener valores de ? G
0
y K en
funcin de T, se construyen graficas de K vs. T y ? G
0
vs. T. A partir de estas graficas
establecemos la Temperatura ptima de reaccin.
Una vez definida la Temperatura de reaccin se define la correspondiente constante de
equilibrio y con ella la conversin en el equilibrio e.
.
0
+
+
n
n
n
n
X
i io i
i
i
i
Donde:
X
i
: composicin molar de la sustancia i. n
i
: moles de la sustancia i.
n
io
: moles iniciales de la sustancia i. n: moles totales.
n
o
: moles totales iniciales. s: coeficiente estequiomtrico total.
De esta manera para el metil acetato:
agua Ac met
X X
+
2 0 2
.
Para el cido actico:
ol me Hac
X X
tan
2
1
En el equilibrio:
( )
2
2
tan
.
1 .
.
ol me Hac
agua Ac met
X X
X X
K
Realizando una primera aproximacin, en esta ecuacin se calcula el valor de e a partir del
valor de K hallado, despus se calculan los valores de las composiciones en el equilibrio de
cada una de las sustancias.
Con estas composiciones conocidas se calculan los coeficientes de actividad de las
sustancias a la Temperatura ptima de reaccin para emplearlos en la ecuacin:
( )
2
2
tan
. .
1
. . .
. . .
agua ol me Hac Hac
agua agua Ac met Ac met
X X
X X
K
Por medio de una serie de iteraciones se halla el valor real de e y de las composiciones en
el equilibrio.
Muestra de clculo
Sustancia ? H
f
0
(kJ / kmol) ? G
f
0
(kJ / kmol)
Acetato de Metilo -442874.704 318280.00
Agua -285830.000 237129.00
cido actico -484500.000 -389900.00
Metanol -238660.000 -166270.00
A partir de las ecuaciones:
H
i
i
0
0
o
fi
H = -5549.7040 kJ /kmol
G
i
i
0
0
o
fi
G = 761 kJ /kmol
Asumiendo que la reaccin se lleva a cabo a 40C = 313.15K
RT
G
K
0
0
298
ln
K
298
= 0.8541
Ahora procedemos a hallar ? H
r
:
Para cada sustancia: Cp= A + BT + CT
2
+DT
3
(kJ /kmol) T en K.
Sustancia A B C D
Acetato de Metilo 3.92701*10 7.96701*10
-1
-2.47205*10
-3
3.23124*10
-6
Agua 1.82964*10 4.72118*10
-1
-1.33878*10
-3
1.31424*10
-6
cido actico -3.60814*10 6.04681*10
-1
-3.93957*10
-4
-5.61602*10
-7
Metanol -2.58250*10
2
3.35820*10
0
-1.16388*10
-2
1.40516*10
-5
?A= 351.8979 ?B=-2.6491
?C= 8.22*10
-3
?D=-8.9413*10
-6
Reemplazando:
15 . 313
15 . 298
/ 7225 . 618 kmol kJ Cpdt
?H
r
= -5549.7040kJ /kmol +618.7225kJ /kmol = -4930.9815 kJ /kmol
A partir de:
1
]
1
15 . 298
1 1
ln
0
298
T R
H
K
K
r
K
313.15
= 0.9404
RT
G
K
0
ln
?G
0
=159.9868 kJ /kmol
Para construir las grficas K vs. T y ?G
0
vs. T, se suponen otros valores de Temperatura. Las
grficas obtenidas son las que se muestran en las Fig. 1 y Fig. 2.
Analizando la grfica K vs. T se ve que a partir de T= 328K la pendiente de esta curva no cambia
mucho con el incremento de la temperatura, por lo cual elegimos esta como la T ptima de
reaccin, dado que un incremento en la temperatura no se justifica pues el valor de K no va a
cambiar mucho. Adems realizando un anlisis similar a la grfica ? G
0
vs. T, y teniendo en cuenta
que un sistema est en equilibrio para cambios negativos de ? G
0
y cuanto ms pequeos sean
estos cambios mejor, se llega a la misma conclusin.
De la grfica K vs. T para T= 328K, K= 1.0164
Reemplazando valores y a partir de:
( )
2
2
tan
.
1 .
.
ol me Hac
agua Ac met
X X
X X
K
e= 0.5020
Con este valor inicial de e, se pueden calcular las composiciones de las sustancias:
agua Ac met
X X
+
2 0 2
.
= 0.251
ol me Hac
X X
tan
2
1
= 0.2489
Con estos valores y el valor de la T de reaccin se calculan los coeficientes de actividad por medio
del programa Destilacin :
1
tan
1
1
1
.
10 * 0727 . 3
10 * 3523 . 7
10 * 5495 . 8
10 * 7801 . 7
ol me
Hac
agua
ac metil
Despus de realizar varias iteraciones se encuentran los valores reales:
e= 0.3181
1
tan
1
1
.
10 * 2927 . 3
10 * 55 . 5
3345 . 1
10 * 398 . 6
ol me
Hac
agua
ac metil
agua Ac met
X X
+
2 0 2
.
= 0.1591
ol me Hac
X X
tan
2
1
= 0.3410
Condiciones ptimas de Proceso
En los intercambiadores de calor se trabaja con agua como fluido de servicio. En el punto anterior
se hallo la temperatura a la cual va a operar el reactor. Para determinar la presin de operacin
calculamos la presin de vapor del acetato de metilo, que es la sustancia ms voltil, a la
temperatura de reaccin. Para las condiciones de operacin en la torre de destilacin I evaluamos
el equilibrio lquido vapor del sistema a al presin de operacin del reactor, a partir de este
equilibrio decidimos trabajar la Torre a esta presin y a una T
mx
= T
azeotropo
= 331.4716K. Para la
torre I I evaluamos el EVL del sistema metanol-metil acetato. Al analizar este sistema a diferentes
presiones, notamos que la composicin del azeotropo para el metil acetato aumenta a medida que
disminuye la presin de operacin, es por esto que decidimos trabajar a una presin baja (0.3
bar).Las condiciones de operacin de la torre III no se especifican por cuanto se trabaja con un
sistema terciario y nuestros conocimientos no abarcan an esa clase de separacin.
Unidad P
operacin
(bar) T
operacin
(K)
I ntercambiador I 1.0 -
Intercambiador II 1.0 -
Reactor 1.2 328
Torre I 1.2 332 mx.
Torre I I 0.3 298 mx.
En el intercambiador el metanol y el cido actico entran a 298K y salen a 328K.
Parmetros de conversin, selectividad y rendimiento.
Ya que no se cont con datos de la literatura para los anteriores parmetros tomamos, de acuerdo
a la conversin de equilibrio hallada en la parte termodinmica, una conversin del 29% previo
acuerdo con el profesor.
SEPARACI N DEL PRODUCTO:
El proceso de la planta que se pretende montar consta de un reactor donde se lleva a cabo la
reaccin isotermicamente y cuya corriente de salida contiene los dos reactivos (metanol cido
actico) y los dos productos (acetato de metilo agua). Para la separacin de dicha mezcla se va a
utilizar un sistema de tres torres de destilacin.
En la primera torre, que recibe la corriente que sale del reactor, se destila el azetropo (metanol -
acetato de metilo) como producto de cabeza en el cual se saca todo el acetato presente en la
mezcla, el producto de cola de dicha torre contiene metanol, agua y cido actico. Esta primera
torre trabaja a 1.2 bar de presin.
El producto de cabeza de la torre 1 es llevado a una segunda torre donde se pretende purificar el
acetato de metilo, dicha torre es trabajada a baja presin (0.3 bar) para desplazar el azetropo a
una composicin mayor de acetato conservando una temperatura de operacin coherente.
El acetato en mayor composicin y algo de metanol es obtenido como producto de cabeza, de esta
misma manera el producto de cola es una mezcla de los dos con metanol en mayor composicin.
El producto de cola de la torre 2 es llevado a una tercera torre donde se busca separar el metanol
casi puro debido a su bajo punto de ebullicin respecto al agua y el cido. En esta torre 3 el
producto de cabeza es metanol con cido y agua en pequeas cantidades y el producto de cola
contiene solo agua y cido actico en cierta proporcin.
Separacin multicomponente
Muchas de las destilaciones en la industria emplean ms de dos components. No obstante que los
principios establecidos para soluciones binarias se aplican generalmente a estas destilaciones, se
introducen nuevos problemas de diseo que requieren consideracin especial.
Un principio importante que debe acentuarse es que un nico fraccionador no puede separar ms
de un componente en forma razonablemente pura a partir de una solucin de varios components,
sino que se requerir un total de n-1 fraccionadores para lograr la separacin compoleta de un
sistema de n components.
Los principios de diseo de los fraccionadores de multicomponentes son los mismos que en muchos
aspectos que aquellos para sistemas binarios, pero la escasez de adecuados datos en el EVL
imponen severas restricciones a su aplicacin. Otro serio problema que an no se resuelve son los
mtodos inadecuados de manejar la eficiencia de los platos en los sistemas multicomponentes.
El procedimiento de diseo de una torre para sistema multicomponente es el de Thiele-Giddes. Este
mtodo supone que para una alimentacin dada, se conocen desde el principio el nmero de
platos, la posicin del plato de alimentacin, la relacin lquido/ vapor y la temperatura en cada
plato; en consecuencia, proceda a calcular el producto destilado y el residuo resultante. Por
supuesto, en la mayora de los casos, al principio de los clculos se desconocen las cantidades
necesarias. En el libro Operaciones de Transferencia de masa de Treybal, se seala un esquema
que empieza por obtener, con un mnimo de pruebas, la informacin necesaria para utilizar el
mtodo Thiele- Giddes as como el desarrollo del mismo para obtener el diseo final.
Conveniencia de un reactor isotrmico o no isotrmico y seleccin del reactor:
La reaccin de cido actico con metanol que se trabaja en el procedimiento descrito es cataltica y
esto hace necesario que se haga un anlisis detallado de todas las condiciones de operacin del
reactor.
Como el catalizador a utilizar es slido se requiere e un sistema de agitacin que lo distribuya por
toda la mezcla para que haya un buen aprovechamiento del mismo. Dicho sistema de agitacin nos
garantiza la uniformidad de todas las propiedades de la mezcla reaccionante al interior del
recipiente. Debido a que la reaccin es reversible, y de acuerdo al anlisis termodinmico ya
realizado a la misma se encontr que existe una temperatura optima de reaccin a la cual se debe
llevar a cabo para garantizar una mxima conversin (conversin de equilibrio). Teniendo en
cuenta que el recipiente es agitado se podra creer que esto es suficiente para conservar la
temperatura de reaccin en todo el recipiente, pero no se puede olvidar que la reaccin es
exotrmica y la liberacin del calor de reaccin representa un inconveniente ya que podra calentar
la mezcla reaccionante y elevar la temperatura perturbando el equilibrio y ocasionando que no se
consiga la mxima conversin . En consecuencia al inconveniente anterior se hace necesario utilizar
un enchaquetado de enfriamiento para retirar el calor de reaccin y garantizar el mantenimiento
de la temperatura optima para que se obtenga la mxima conversin.
Del anlisis anterior se obtiene el perfil del reactor necesario:
Un CSTR (empacado)con catalizador slido e isotrmico con enchaquetado de enfriamiento. Las
caractersticas de dicho reactor se describirn mas a fondo cuando se presente el diseo del mismo.
El comportamiento de la constante de equilibrio para una reaccin exotrmica con la temperatura
es la siguiente:
Como se observa en la grfica un incremento de la temperatura conduce a una menor conversin
de equilibrio. Este es uno de los motivos por los cuales conviene trabajar el reactor isotrmico, de
manera que al retirar el calor de reaccin de la mezcla reaccionante se prevenga un calentamiento
de la misma y una posible disminucin de la conversin del equilibrio.
Otra ventaja de llevar el control de la temperatura es prevenir que se alcancen temperaturas para
las cuales la velocidad de reaccin sea tan lenta que no se aproveche el catalizador en el perodo
de residencia de la mezcla y se obtengan de estas formas conversiones en el equilibrio muy bajas.
Balance molar y msico general.
Reactor
Reaccin:
D C B A
Cat
+ +
Balances estequiomtricos:
F
A
= F
A0
(1-X) F
c
= F
A0
X
F
B
= F
A0
(1-X) F
D
= F
A0
X
Ecuacin de diseo
C
C C
r
F F
W
0
Ecuacin cintica
r
C
=
1
]
1
e
D
b A A
K
CcC
C C K r
1
1
]
1
e
D
b A
C
K
CcC
C C K
F
W
1
W: masa de catalizador
K
1
= K
3
.X
cat
+K
4
.X
cat
X
cat
= 0.08
1
]
1
RT
Ea
K exp 485 . 0
3
=
7
10 * 0693 . 1
328 . . / 314 . 8
/ 41800
exp 485 . 0
1
]
1
k k mol J
mol J
1
]
1
RT
Ea
K exp 123 . 0
4
= 2.7118*10
-8
K
1
= 2.8538 *10
-9
m
6
/Kg.mol.s
Resolviendo los balances estequiomtricos se obtiene:
F
A0
= F
B0
= 147.7624 mol/s
F
C
= F
D
= 42.8511 mol/s
Como la reaccin se lleva a cabo en fase lquida:
v
0A
=
s
lt
Kg
kmol
lt
kg
s kmol
C
F
A
A
4436 . 8
60
1
. 05 . 1
/ 1477624 . 0
0
0
v
0B
=
s
lt
Kg
kmol
lt
kg
s kmol
C
F
B
B
9740 . 5
32
1
. 7915 . 0
/ 1477624 . 0
0
0
v
0T
= v
0A
+ v
0B
= 14.4175 lt/s
B
T
A
A
C
lt
mol
v
F
C 2766 . 7
0
D
T
C
C
C
lt
mol
v
F
C 9722 . 2
0
kg
lt
mol
lt
mol
s mol kg
lt
s
mol
W 1937 . 324
3319 . 1
9722 . 2
2766 . 7
. .
10 * 8538 . 2
8511 . 42
2
2
2
2
2
2
2
3
1
1
1
1
]
1
Torre I
Balance de C:
3
3
2
2
. . F X F X
c c
3
. 652 . 0 / 85 . 42 F s mol
F
3
= 65.7225mol/s
Balance Total:
F
2
= F
A
+ F
B
+ F
C
+ F
D
= F3 + F
4
= 295.5226 mol/s
F
4
= 229.8 mol/s
Balance de B:
4
4
3
3
2
2
. . . F X F X F X
B B B
+
X
B
3
= X
B
azeotropo
= 0.348 X
B
4
= 0.357
Balance de A:
4
4
2
2
. . F X F X
A A
X
A
4
= 0.457
Torre II
Diseo de la Torre II
El flujo de entrada a esta torre tiene la composicin del azeotropo a 1.2 bar y se pretende sacar
como producto de cabeza metil acetato con una alta pureza desplazando el azeotropo reduciendo la
presin del sistema a 0.3 bar, para dicha presin de trabajo la temperatura de burbuja del
azeotropo es de 297.69K y la composicin 0.2 de metanol y 0.8 de metil acetato. Se podra
desplazar el azeotropo para conseguir una mayor pureza pero en este caso no es posible
ya que al disminuir ms la presin, la temperatura de burbuja estara por debajo de la temperatura
de entrada de la alimentacin, lo cual sera ilgico.
Para saber el nmero de platos tericos y reales empleados en la separacin y las cargas trmicas
en el condensador y el rehervidor, se emplea el mtodo de Mc.Cabe-Thiele.
Mtodo Mc. Cabe-Thiele.
En este mtodo se recomienda elegir una composicin de producto de cabeza cercana a la
composicin del azeotropo, pero no igual a ella.
Pasos a seguir:
1. Construir el diagrama de equilibrio Y vs. X.
2. Graficar la lnea auxiliar Y = X.
3. Ubicar el punto Y = X = X
D
= 0.75
4. Ubicar el punto Y = X = X
F
= 0.652.
5. Ubicar el punto Y = X = X
W
= 0.15.
Esta composicin se eligi tomando como gua un ejemplo, segn la literatura debe estar
comprendida entre 0.2 y 0.05.
6. Ubicar la lnea de operacin superior L.O.S.S por medio de la siguiente ecuacin:
1
.
1
1
+
+
+
+
R
X
X
R
R
Y
D
n n
Donde:
R = L/D
R: reflujo del condensador.
Con esta ecuacin se ubica el punto Y cuando X = 0.
Y(0) = 0.53
La LOSS se traza a travs de los puntos Y(0) y X
D
.
7. Ubicar y trazar la lnea de alimentacin. Esta lnea debe pasar a travs del punto X
F
y en
nuestro caso La interseccin de dicha lnea con la curva de equilibrio se denomina punto
P.
8. Trazar la lnea de operacin de la seccin inferior LOSI , la cual debe pasar a travs de los
puntos X
W
y P.
9. Trazar las etapas, la forma como se trazan esta se puede apreciar fcilmente en el
diagrama.
Platos Tericos: 12.012
10. Construir la curva de equilibrio para la eficiencia de Murphree.
Para construir esta curva y ante la carencia de datos acerca de este sistema asumimos una
eficiencia de Murphree de 60% con base en un ejercicio resuelto.
Una descripcin amplia acerca de la construccin de esta curva se muestra en Treybal.
11. Se trazan los platos reales. El trazado se muestra en la grafica.
Como se ve en el grfico el plato de alimentacin puede ser el 7 o el 8, ya que el punto P
esta ubicado al final del plato 7 y al principio del plato 8.
Balance Total :
6 5 3
F F F +
5 6
/ 7225 . 65 F s mol F
Balance de C :
( )
5 5
6
6
5
5
3
3
/ 7225 . 65 . 15 . 0 . 75 . 0 / 8511 . 42
. . .
F s mol F s mol
F X F X F X
C C C
+
+
F
5
= 54.9879 mol/s
F
6
= 10.7346 mol/s
Condensador y rehervidor de la Torre I I
Para calcular las cargas trmicas del rehervidor y condensador de esta torre de destilacin se
emplearn las siguientes ecuaciones del libro de Robert E. Treybal.
LO G
G
H H
H Q
R
1
1
'
(ec. 9.65)
F.H
F
= D.Q+W.Q (ec. 9.77)
D
Q
H Q
W
Q
H Q
C
D
B
W
' '
' '
(ec. 9.70)
Donde:
H
G1
: entalpa de la mezcla en fase vapor que entra al condensador.
H
LO
: entalpa de la mezcla en fase lquida que sale del condensador.
D: flujo molar de destilado.
W: flujo molar de residuo.
Clculo de H
LO
:
+
T
Tref
mezcla LO LO
dT Cp H H
.
0
.
Como en el estado de referencia la entalpa vale cero:
T
Tref
mezcla LO
dT Cp H
.
.
Debido a que no se encontr mtodos de clculo para cp de mezcla en la literatura disponible,
hacemos una aproximacin de este de la siguiente forma.
+
T
Tref
ac met ac Met
T
Tref
ol me ol me LO
dT Cp X dT Cp X H
.
. .
.
tan tan
. . .
+ +
71 . 297
. 293
3 5 2 2 2
.
tan
). * 10 * 40516 . 1 * 10 * 16388 . 1 * 3582 . 3 10 * 5825 . 2 ( . dT T T T dT Cp
T
Tref
ol me
= 378.4425 J /mol
+ +
71 . 297
. 293
3 6 2 3 1 1
.
. .
). * 10 * 2322 . 3 * 10 * 47205 . 2 * 10 * 967 . 7 10 * 927 . 3 ( . dT T T T dT Cp
T
Tref
ac met
= 669.8091 J /mol
Realizando un balance de energa:
F
3
.Cp.?T = ?H
v
.W
?T = T
F
- T
entrada
Donde:
?H
v
: calor latente de vaporizacin.
T
F
: Temperatura real de entrada de la mezcla.
Clculo de ? H
v
:
Mtodo de Riedel (Reid-Prausnitz-Poling).
1
]
1
br
c br
C v
T
P T
T R H
930 . 0
013 . 1 ln .
. . . 093 . 1
Donde:
T
C
: Temperatura crtica de la mezcla.
T
br
: Temperatura de ebullicin reducida de la mezcla.
P
C
: Presin crtica de la mezcla.
Clculo de T
C
de la mezcla:
i
ci i
cj j
j
v y
v y
.
.
(ec. 5-6.1 Reid)
j
Cj j C
T T . (ec. 5-6.2 Reid)
7836 . 0
2164 . 0
. .
ac met
MetOH
T
C
= 507.87K
Clculo de la P
C
de la mezcla:
1
]
1
1
]
1
+ + 1
*
). . 93 . 4 808 . 5 ( 1 . *
T
Tc
w P P
C
(ec. 5-6.22 Reid)
3
1
2
2 2
3
1
1
1 1
2 2 1 1
3
1
*
.
*
.
. .
.
*
*
*
V
T
V
T
P P
V
T
P
C C
C C
+
+
(ec. 5-6.21 Reid)
1
1
]
1
'
+ +
2 1
3
1
2
2
3
1
1
1
3
1
1
12
3
1
2
2 2
3
1
1
1 1
3
1
. .
* * *
* . 2
*
.
*
.
. * *
V
T
V
T
V
T
V
T
V
T
V T
c c c c
(ec. 5-6.18 Reid)
) 2 .( . .
2 1 12 2 1 2 2 1 1
w w w w w w + +
2 1
12
1 1
2
w w
w
+
3
2
2 2
3
2
1 1
3
2
1 1
1
* . * .
* .
V y V y
V y
+
1 2
1
8
) * * (
*
3
3
1
2
3
1
1
12
V V
V
+
*) * * 2 .( . * . * *
2 1 12 2 1 2 2 1 1
V V V y y y V y V V + +
2
3
1
2
1
3
1
1
12
12
* *
* 2
*
c c
T
V
T
V
V
T
+
Datos necesarios:
Tomando
Metil acetato = 1
Metanol = 2
V
1
*
= 0.2262 lt/mol P
C1
= 47.50 bar
V
2
*
= 0.1198 lt/mol P
C2
= 80.97 bar
Reemplazando valores en las ecuaciones anteriores y resolviendo, se obtiene:
P
C
= 59.285 bar
Reemplazando en la ecuacin de Riedel para una mezcla:
1
1
1
1
]
1
K
K
K
K
K
K mol
bar
cm H
v
87 . 507
4716 . 331
930 . 0
013 . 1 285 . 59 ln
.
87 . 507
4716 . 331
* 87 . 507 *
.
14 . 83 * 093 . 1
3
?H
v
= 33337.0551 J /mol
Reemplazando en el balance de energa y despejando T
F
se obtiene:
T
F
= 288.9397K
A esta temperatura se debe calcular H
F
:
+
T
Tref
ac met ac Met
T
Tref
ol me ol me F
dT Cp X dT Cp X H
.
. .
.
tan tan
. . .
H
F
= -486.8916 J /mol
Despejando Q de la ecuacin:
F.H
F
= D.Q+W.Q
Q = -4459.0235
Y de las ecuaciones:
D
Q
H Q
W
Q
H Q
C
D
B
W
' '
' '
Q
B
= 505.9615 W
Q
C
= 91.9488 W
Torre III
Balance de B
7
7
4
4
. . F X F X
B B
Debido a que en esta torre se lleva a cabo una destilacin de tres componentes, a que de los tres
el ms voltil es el metanol y a que la diferencia de temperaturas de ebullicin entre el metanol y
las otras dos sustancias es alta, suponemos que la composicin de metanol en la mezcla de salida
en forma de vapor de la torre es por consiguiente alta y la suponemos X
B
7
=0.95. Consideramos que
la segunda composicin ms alta es la del agua pues es la segunda en la escala de volatilidades y
suponemos X
D
7
= 0.035, por consiguiente X
A
7
=0.015.
F
7
=86.3564 mol/s
Balance Total
s mol F
F F F
/ 4436 . 143
8
8 7 4
+
Balance de A
8
8
7
7
4
4
. . . F X F X F X
A A A
+
X
A
8
=0.7282
Tabla de Resultados
Unidad Flujo de
entrada
(mol/ s)
Flujo de salida
(mol/ s)
X
A
X
B
X
C
X
D
Reactor 295.5248 295.5226 0.500
0.355
0.500
0.355
0.000
0.145
0.000
0.145
Torre I 295.5226 F
3
= 65.7225
F
4
= 229.800
0.00
0.457
0.348
0.357
0.652
0.00
0.000
0.186
Torre I I 65.7225 F
5
= 54.9879
F
6
=10.7346
0.00
0.00
0.348
0.850
0.652
0.150
0.00
0.00
Torre I I I 229.800 F
7
=86.3564
F
8
=143.4436
0.0150
0.7282
0.95
0.00
0.000
0.000
0.0350
0.2718
Balance de energa en el reactor:
Para garantizar la isotermicidad en que es llevada a cabo la reaccin se debe retirar el H
rxn
a la
mezcla. Para este propsito se va a usar un enchaquetado por el cual fluir agua fra. Para el
calculo del calor que debe ser retirado por el fluido en la chaqueta se requiere conocer la
temperatura de pared exterior en el reactor.
Como el reactor esta completamente agitado la temperatura en la pared interior del mismo es la
temperatura de reaccin.
Debido a que en el interior del recipiente no hay gradientes de temperatura este se puede evaluar
en dos partes: la tapa inferior, que posee una curvatura despreciable, como una pared plana y las
paredes como un cilindro.
r
r
Q
Q Q
r
r r r r
+
+
* |
Sale Entra + Acumula = Genera
V
T
Q
Q Q
H
r
r r r r r
+
+
* | |
con:
r
T
S K Q
r r
* *
L r S
r
* * * 2
r L r V * * * * 2
r = R1 = 0.865 m T = Ti = 328 K
r = R2 = 0.875 m T = Tw
H
= H
rxn
*mol que reacciona de A / volumen de mezcla
H
= 4930.9815 J /mol *42.8511 mol/seg. / 3.9552 m
3
H
= 53422.8261 W/m
3
K : conductividad trmica del material de construccin (Acero estructural)
K = 44.9991W/(m*K)
Resolviendo la ecuacin diferencial resultante del balance se llega a:
) 1 ( * )
* 4
*
(
2
2
2
1
2
2
R
R
K
R
Tw Ti
H
Reemplazando los valores en la anterior ecuacin se obtiene:
Tw = 322.8357 K
Calculo del coeficiente de transferencia de calor del fluido de la chaqueta.
m
w
p b a t
K
C
N D
a
K
D h
) ( * )
*
( * )
* *
( *
*
3
1 2
ec. 3.11-1 Geankoplis
Para un agitador con deflectores:
a = 0.74 b =2/3 m = 0.14 Geankoplis. Pag 241
h: coeficiente convectivo de transferencia de calor del fluido de la chaqueta.
D
t
: dimetro del reactor. : viscosidad de la mezcla
K: conductividad trmica de la mezcla. C
p
: capacidad calorfica de la mezcla.
D
a
: dimetro del agitador.
w
: viscosidad de la mezcla a T de pared.
N: revoluciones por segundo del agitador. : densidad de la mezcla.
Todas las propiedades de la mezcla excepto
w
medidas a la temperatura de reacciona.
D
t
= 1.73 m
D
a
= 0.52 m
N = 120 rev / s = 2 rev / s
Calculo de la viscosidad de la mezcla liquida: Mtodo de NI SSAN ( Reid )
+
ij j i
j i
i i m
G x x Ln x Ln * *
Para mezcla binaria:
12 2 1 2 2 1 1
* * * * G x x Ln x Ln x Ln
m
+ +
x
i
= fraccin molar del compuesto i
Se asume que la mezcla solo tiene cido actico y metanol en cantidad equimolar puesto que ellos
dos se encuentran en mayor cantidad. Ya que el mtodo del cual se dispone para calcular
w
solo
es valido para mezcla binaria debido a que solamente se tiene la ecuacin de G
12
.
Metanol: 1
cido Actico: 2
1
= 0.5 cp
2
= 0.8 cp
T
rxn
= 328 K
T
w
= 315.3563 K
Desarrollando el mtodo se obtiene:
m
(328 K) = 8.331*10
-4
kg 7/ (m*s)
w
(322.8357 K) = 8.338*10
-4
kg / (m*s)
Clculo de la conductividad trmica de la mezcla liquida: Mtodo Li. ( Reid Pg. 565 )
ij j i
n
j
n
i
m
* *
1 1
ec. 10-12.7
1
1 1
) ( * 2
+
j i ij
j j
n
j
i i
i
V x
V x
*
*
1
m
= K
m
= conductividad trmica de la mezcla.
i
= conductividad trmica del compuesto i.
j
= conductividad trmica del compuesto j.
x
i
= fraccin molar del componente i.
V
i
= volumen molar critico del componente i.
Para cuatro componentes:
cido Actico: 1
Metanol: 2
Acetato de metilo: 3
Agua: 4
Componente X
i
V
i
(cm
3
/ mol)
I
(W / m*K)
1 0.3550 179.7 5.7201*10
-2
2 0.3550 118 6.5868*10
-2
3 0.1450 228 5.0268*10
-2
4 0.1450 55.9 0.2201
Resolviendo el mtodo para los cuatro componentes se tiene:
m
= K
m
= 0.0619 W / (m*K).
Reemplazando en la ecuacin para el coeficiente convectivo se obtiene:
h = 609.5514 W / (m
2
*K)
Carga trmica de la chaqueta:
Fluido de servicio: agua t1 = t
entrada
= 18 C
t2 = t
salida
= 25 C
MLDT
T A h Q * *
1 2
2 1
) 1 2 ( 2 1
t T
t T
Ln
t T t T
T
MLDT
T1 = T2 = Tw = 322.8357
2
2 2
* * * * 2 R L R A +
Q: carga trmica en la chaqueta.
A: rea total exterior del reactor.
T
MLDT
: diferencia media logartmica de temperaturas.
Tw: temperatura de pared exterior de pared del reactor.
h: coeficiente convectivo de transferencia de calor del fluido de la chaqueta.
Reemplazando los valores respectivos en cada ecuacin se tiene:
T
MLDT
= 28.0462 K
A = 12.9061 m
2
Q = 220582.2576 W
Calculo del flujo msico de agua necesaria en la chaqueta:
T C
Q
m
P
agua
*
m
agua
: flujo msico de agua en la chaqueta.
Q: carga trmica en la chaqueta.
C
p
: capacidad calorfica del agua.
T: diferencia de temperatura entre el agua de entrada y el agua de salida.
Resolviendo la ecuacin anterior con:
C
p
= 4186.8 J / (kg*K)
Se tiene:
m
agua
= 7.5265 Kg/ s
Como ya se conocen tanto el flujo masico de agua como sus temperaturas en el enchaquetado se
puede fijar el espesor que se desee, en nuestro caso se escogi un espesor de 2 cm entre el
reactor y la chaqueta.
En cuanto al material de la chaqueta puede ser acero inoxidable corriente, ya que ella maneja
temperaturas muy bajas.
Coeficiente Total de Diseo U
MLDT
T A U Q * *
1 2
2 1
) 1 2 ( 2 1
t T
t T
Ln
t T t T
T
MLDT
T1 = T2 = Trxn = 328K
Reemplazando los valores y despejando U se obtiene:
U = 514.3773 W/m
2
.K
Espesor de pared del reactor y seleccin del material apropiado:
Para el calculo del espesor de pared de un recipiente, en nuestro caso el reactor, se utiliza le
ecuacin para el esfuerzo de costilla:
t
r p *
1
1
: esfuerzo de costilla.
P: presin manomtrica.
r: radio interior del reactor.
t: espesor de la pared del reactor.
El material elegido para la construccin del reactor es Acero AI SI 302 inoxidable recocido, este
material tiene una resistencia de 655 Mpa, aunque esto no sea de gran importancia pues la presin
de operacin es de apenas 1.2 bar. En cuanto a la corrosin la mezcla reaccionante no representa
gran peligro, pues el cido Actico que es el compuesto mas agresivo de la mezcla se ve diluido por
los otros tres componentes, por esta razn el Acero Estructural no presenta inconvenientes para la
construccin del reactor. Es importante que sea inoxidable debido a que en la reaccin se obtiene
como subproducto agua.
En el apndice B. Propiedades tpicas de materiales seleccionados usados en ingeniera.
Del libro MECANICA DE MATERIALES. Segunda edicin. Ferdinand P Beer.
Se lee el
1
de la columna Resistencia Ultima (Tensin. Mpa) para el material en cuestin:
1
= 655 Mpa.
Despejando el espesor de pared d la ecuacin anterior se tiene:
1
*
r p
t
Con p = 0.4201 bar = 0.042 Mpa r = 0.865 m
Resolviendo para el espesor de pared :
t = 0.055mm
Como se puede ver debido a las bajas condiciones de presin que se trabaja el valor obtenido es
ilgico, por esta razn el valor utilizado para la construccin del reactor es asumido como:
t = 1 cm
Especificacin de dimensiones de acuerdo al volumen o tiempo de residencia segn el
aparato:
Calculo del volumen del reactor:
Conociendo la masa del reactor
M
cat
= 324.1937 Kg. de amberlitz.
Y tomando informacin de una de las patentes cuyo reactor se asemeja bastante al propuesto por
nosotros, la cual aconseja que el porcentaje en peso de catalizador en el reactor este entre 6 10
%, elegimos un porcentaje de 8 % el cual nos permite por una simple regla de tres conocer la
masa total de mezcla reaccionante que debe permanecer en el interior del reactor.
M
mezcla
= 4052.4213 Kg.
Una buena aproximacin del tiempo de residencia de la mezcla en el reactor se puede obtener a
partir del flujo msico total de salida del reactor y la masa libre de catalizador que debe
permanecer en el mismo.
M
lbre de cat.
= M
mezcla
- M
cat
= 3728.2276 Kg.
El flujo msico total de salida es la suma de los flujos msicos de cada uno de los componentes de
la mezcla, los cuales se obtienen multiplicando cada flujo molar por su respectivo peso molecular.
W
A
= 6294.684 g/s
W
B
= 3357.1648 g/s
W
C
= 3170.9814 g/s
W
D
= 771.3198 g/s
W
total
= 13.5942 kg/s
Como ya conocemos la masa de mezcla sin catalizador que fluye por el reactor en un segundo,
podemos calcular el tiempo necesario para que fluya M
lbre de cat.
por el mismo por una simple regla
de tres.
= 274.2524 s
De la ecuacin:
0
V
V
V = volumen del reactor.
V
0
= flujo volumtrico
Despejando V se tiene:
0
*V V
Con V
0
= 1.4418*10
-2
m
3
/ s
V = 3.9552 m
3
En realidad el anterior volumen no es el volumen del reactor sino de la mezcla reaccionante, pues
el reactor debe ser un poco mas grande para poder introducir un gas inerte que nos permita
alcanzar la presin de operacin.
El volumen escogido para nuestro reactor es:
V
reactor
= 4.5 m
3
Calculo detallado del sistema de agitacin:
Para el sistema de agitacin que requiere el reactor se eligi un agitador de hlice, pues este
debido a las condiciones del proceso presenta ciertas ventajas sobre los otros tipos de agitadores.
El agitador de hlice es una buena opcin cuando se requiere mantener slidos suspendidos ya que
proporciona fuertes corrientes verticales, adems trabaja a altas velocidades.
Los factores de forma que limitan el diseo de un sistema de agitacin son los siguientes:
S1 = Da/Dt S2 = E/Da S3 = L/Da
S4 = W/Da S5 = J /Dt S6 = H/Dt
En la figura 9.14 de Mc Cabe, se muestra una grfica de Nmero de potencia frente a Nmero de
Reinolds para rodetes de tres palas. En dicha grfica la curva A representa un agitador de tres
palas en un tanque con cuatro placas deflectoras que se adapta perfectamente a nuestras
necesidades, adems proporciona el paso y los factores de forma S1, S2, S5 y S6.
Diseo:
Volumen del reactor = 4.5 m
3
S6 = H/Dt = 1.0 S2 = E/Da = 1.0
S5 = J /Dt = 0.1 S1 = Da/Dt = 0.3
H: altura del liquido + slido
Dt: dimetro del tanque
Da: dimetro del agitador
J : ancho de la placa deflectora
E: altura desde el fondo del tanque hasta la hlice
L: altura real del tanque
Como S6 = 1 entonces H = Dt
Volumen de liquido + slido = 0.25**Dt
2
*H = 0.25** H
3
= 4.05 m
3
Despejando H se tiene:
H = Dt = 1.73 m
Longitud real del tanque:
Volumen del tanque = 0.25**Dt
2
*L = 4.5 m
3
Despejando L se tiene:
L = 1.91 m
3
De S5, S2, y S1 se tiene :
J = 0.173 m
E = 0.52 m
Da = 0.52 m
Potencia del agitador
c
g
Da n Np
P
. . .
5 3
Donde:
P: Potencia suministrada (ft.lbf/s) Da: dimetro del agitador = 1.71ft
Np: nmero de potencia ?: densidad de la mezcla (lb/ft
3
)
n: velocidad del agitador = 2 rps g
c
= 32.174 ft/s
2
En la figura 9.14 de Mc. Cabe se presenta una curva de Np vs. Re, por lo que es necesario calcular
Re para conocer Np:
. .
Re
2
n Da
: viscosidad de la mezcla (lb/ft.s)
Clculo de ?
mezcla
:
?
mezcla
=
3 3
5979 . 1000
05 . 4
4213 . 4052
m
kg
m
kg
al Volumentot
masatotal
2192 . 652521
10 * 5984 . 5
4653 . 62 . 2 . 71 . 1
Re
4
2
En la curva referenciada anteriormente para Re>10
5
Np = 1.0
W
s
lbf ft
P 8972 . 307
.
0933 . 227
174 . 32
4653 . 62 . 75 . 1 . 2 . 1
5 3
Diseo de Bomba para el cido actico
A partir de la ecuacin:
P
B
= m.W
p
Donde:
m: flujo msico de metanol
W
p
:
A partir de la ecuacin de Bernoulli:
f
c
b
c
b b
c
a
c
a a
h
g
V
g
z g P
Wp
g
V
g
z g P
+ + + + + +
. 2
.
.
. 2
.
2 2
Datos:
Q = 8.4436*10
-3
m
3
/s Z
b
=1m P
b
= 101.325 kPa DET= 4.26 cm
? = 1.05*10
3
kg/m
3
P
a
= 77.99 kPa DIT=4.089 cm ? = 0.7
Tipo tuberia : 1.5 plg Tamao nominal schedule 40.
En el apndice 6 del Mc. Cabe para una tubera de 1,5 plg schedule 40 la capacidad para la
velocidad de 1m/s en lt/min es 78.79 lt/min = 1.3132 lt/s.
V
b
= 8.4436*10
-3
/ 1.3132*10
-3
= 6.4298 m/s
Reemplazando en la ecuacin de Bernoulli y depreciando las prdidas:
W
p
= 42.8916 m
2
/s
2
m = Q. ? = 8.4436*10
-3
m
3
/s*1.05 kg/m
3
= 8.8657 kg/s
P
B
= 380.2659 W
Diseo de Bomba para el Metanol
A partir de la ecuacin:
P
B
= m.W
p
Donde:
m: flujo msico de metanol
W
p
:
A partir de la ecuacin de Bernoulli:
f
c
b
c
b b
c
a
c
a a
h
g
V
g
z g P
Wp
g
V
g
z g P
+ + + + + +
. 2
.
.
. 2
.
2 2
Datos:
Q = 5.974 lt/s Z
b
=1m P
b
= 101.325 kPa DET= 4.26 cm
1? = 0.7915 kg/lt P
a
= 77.99 kPa DIT=4.089 cm ? = 0.7
Tipo tuberia : 1.5 plg Tamao nominal schedule 40.
En el apndice 6 del Mc. Cabe para una tubera de 1,5 plg schedule 40 la capacidad para la
velocidad de 1m/s en lt/min es 78.79 lt/min = 1.3132 lt/s.
V
b
= 5.974/ 1.3132 = 4.4953 m/s
Reemplazando en la ecuacin de Bernoulli y depreciando las prdidas:
W
p
= 61.8636 m
2
/s
2
m = Q. ? = 5.974 lt/s*0.7915 kg/lt = 4.7284 kg/s
P
B
= 292.5173 W
Conclusiones
Al inicio de los clculos del presente proyecto, notamos la importancia y necesidad de la resolucin
del reactor, y no slo su resolucin, sino resolverlo bien, pues una vez hecho esto, se conocan las
dems corrientes de salida del reactor para disear las dems etapas. El acoplamiento del reactor
con las respectivas operaciones de acondicionamiento de reactivos y separacin de productos es la
clave de todo el proceso, la cual le da validez y mide la viabilidad del mismo.
En la realizacin de este proyecto, utilizamos al mximo nuestras capacidades y tambin
aprendimos cosas nuevas, as como tambin camos en cuenta de muchos vacos que tenemos,
como por ejemplo una destilacin multicomponentes, pero en general se aplicaron de manera
integral la gran mayora de conocimientos adquiridos en el curso y durante la carrera. Es as como
tuvimos que aplicar conceptos cinticos, Termodinmicos, de transferencia de calor y masa,
mecnica de fluidos, etc.
En cuanto a la formacin del estudiante , la realizacin del trabajo es una experiencia muy
enriquecedora, ya que adems de evaluar de forma indirecta lo aprendido, le da una oportunidad
de desempearse como profesional, adquiriendo cierto nivel de madurez al enfrentarse a
situaciones que sern muy cotidianas en su trabajo a nivel de industria.
La importancia del trabajo radica en que nos obliga a pensar, discutir e ingeniar para encontrar la
solucin a los posibles problemas que se nos puedan presentar en la industria. Adems nos
proporciona una nueva visin acerca de los conceptos aprehendidos durante el curso y durante la
carrera, pues a lo largo de esta, todo ha sido terico y, aunque as ocurre en este proyecto, se vi
la necesidad de tener una realidad fsica para proporcionar una verdadera solucin a un problema
determinado. I gualmente nos sirvi para cuestionarnos, pues durante el desarrollo de ste
surgieron muchas dudas que nunca fueron formuladas en una clase, o ni siquiera se nos haban
ocurrido.
La aplicacin de este proceso a nivel industrial tiene que ser totalmente descartada, puesto que
debida a la carencia de conocimientos que se adquieren en semestres superiores como por ejemplo
la destilacin multicomponente, hubo que hacer muchas suposiciones. Adems de lo expuesto ya
existen procesos para la produccin de acetato de metilo correctamente evaluados y patentados.
En cuanto al reactor que se dise, se puede decir que es un aparato confiable en cuanto a peligro
por explosin, tambin posee un buen desempeo en cuanto a agitacin, pues se dise con
dimensiones recomendadas o las ms empleadas en las industrias para el tipo de proceso que se
necesita; con este diseo se asegura que las partculas de catalizador permanecen suspendidas en
el volumen de mezcla reaccionante y no se depositan en el fondo del tanque.
I gualmente es eficiente en cuanto al manejo de la isotermicidad, pues el flujo de agua de
enfriamiento necesario, nos parece pequeo al compararlo con flujos empleados en otros procesos.
Recomendaciones:
Reactor:
Proporcionar una mayor potencia para incrementar la turbulencia y favorecer la
transferencia de calor y masa.
Dotar de un sistema de termocuplas para controlar la temperatura interior.
Ubicar vlvulas antes y despus para manejar diferentes niveles de produccin.
Etapas:
Falt realizar una separacin despus de la torre III, se recomienda realizar una extraccin
lquida para los productos de cabeza, seguida de otra destilacin; para los productos de
cola se recomienda realizar destilacin azeotrpica seguida de una decantacin y una de las
corrientes (la que contiene altas cantidades de cido actico) recircularla al reactor.
Falt hacer recirculacin a las torres I y II.
Falt ubicar una bomba a la salida del reactor para que llevara las sustancias al plato de
alimentacin de las Torres I y II.
La construccin de planos en los cuales se especifican correctamente todas las dimensiones de los
equipos es imprescindible para el montaje de una planta ya que un error por parte del constructor
podra alterar drsticamente el desarrollo de las operaciones o procesos de acuerdo al equipo y
generar desestabilizaciones en todo el proceso y derivar en una tragedia.
Bibliografa
Procesos de Transporte y Operaciones Unitarias. Geankoplis.
Operaciones de Transferencia de Masa. Robert E. Treybal.
The Properties of gases and liquids. Reid-Praunitz-Poling.
Operaciones Unitarias en I ngeniera Qumica. Mc. Cabe. Warren L.
Elements of chemical reaction engineering. Scott Fogler.
Procesos de Transferencia de Calor. Donald Q. Kern.
Modelamiento matemtico y simulacin de una columna para la obtencin de
acetato de metilo por destilacin reactiva. Gutierrez Luis F. Martinez Adriana.
Enciclopedy of chemical process. Ullman.
Chemical Engineering Science. Vol 52 No 19.
www.uspto.gov
www.es.espacenet.com
www.alche.com
www.elsevier.com
www.chemweb.com
www.dechema.com
www.siri.org
www.erkol.com
S-ar putea să vă placă și
- Metodo Wagner Nelson Clase 2011Document13 paginiMetodo Wagner Nelson Clase 2011Gus Ortega PedrazaÎncă nu există evaluări
- Guias PDFDocument1 paginăGuias PDFGus Ortega PedrazaÎncă nu există evaluări
- HPLC - Practicas de Laboratorio y Cuestiones Teorico-Practicos Cuarta ParteDocument11 paginiHPLC - Practicas de Laboratorio y Cuestiones Teorico-Practicos Cuarta ParteGiancarlo DlcÎncă nu există evaluări
- 5 Anexo 5 Del Informe 34 EstabilidadDocument18 pagini5 Anexo 5 Del Informe 34 EstabilidadJean RomeroÎncă nu există evaluări
- Interacciones 1CDocument52 paginiInteracciones 1CGus Ortega PedrazaÎncă nu există evaluări
- 6 - Esther - Consejos para El Mantenimiento de Su Equipo de HPLCDocument60 pagini6 - Esther - Consejos para El Mantenimiento de Su Equipo de HPLCGus Ortega Pedraza100% (1)
- Determinación de Arsénico en Agua Por Espectrometría de Absorción AtómicaDocument4 paginiDeterminación de Arsénico en Agua Por Espectrometría de Absorción AtómicaDany Daniel Oblitas SoteloÎncă nu există evaluări
- Tesis PilasDocument57 paginiTesis PilasGus Ortega PedrazaÎncă nu există evaluări
- Perfumes y SaborizantesDocument13 paginiPerfumes y SaborizantesGus Ortega PedrazaÎncă nu există evaluări
- Nomenclatura OrganicaDocument32 paginiNomenclatura OrganicaPablina Rosa Guiñez EspinozaÎncă nu există evaluări
- Expo BienDocument17 paginiExpo BienGus Ortega PedrazaÎncă nu există evaluări
- Sintesis de Farmacos AnaestesicosDocument36 paginiSintesis de Farmacos AnaestesicosGus Ortega Pedraza100% (1)
- Articulo TraducidoDocument4 paginiArticulo TraducidoGus Ortega PedrazaÎncă nu există evaluări
- Pruebas Mecánicas A Películas de ResinaDocument60 paginiPruebas Mecánicas A Películas de ResinaAngélica SixtosÎncă nu există evaluări
- Reacciones QuímicasDocument22 paginiReacciones QuímicasCarlo Bastidas JaimesÎncă nu există evaluări
- 19-CPR-004 - GRUPO VTEK SAS - BOG (Equipo Eléctrico)Document10 pagini19-CPR-004 - GRUPO VTEK SAS - BOG (Equipo Eléctrico)juandagomezÎncă nu există evaluări
- Técnico de Proyectos en Instalaciones de Gas NaturalDocument14 paginiTécnico de Proyectos en Instalaciones de Gas NaturalesterÎncă nu există evaluări
- Las 4 Fuerzas FundamentalesDocument11 paginiLas 4 Fuerzas FundamentalesPedro PeñasÎncă nu există evaluări
- Al4 Descripción Evs PDFDocument5 paginiAl4 Descripción Evs PDFEduardo AponteÎncă nu există evaluări
- Informe N 6 ElectromagnetismoDocument17 paginiInforme N 6 ElectromagnetismoVictorÎncă nu există evaluări
- Tesis Beneficios de La Construccion Modular en La Industria ForestalDocument63 paginiTesis Beneficios de La Construccion Modular en La Industria ForestalPauli FigueroaÎncă nu există evaluări
- Motores Taller 3Document4 paginiMotores Taller 3Into The MazeÎncă nu există evaluări
- Control ACDocument5 paginiControl ACChristian SaraguroÎncă nu există evaluări
- 01 Ecuaciones de EstadoDocument2 pagini01 Ecuaciones de EstadoCeballos AsociadosÎncă nu există evaluări
- 09balance de EnergiaDocument46 pagini09balance de EnergiaFabiola Del Pilar CuroÎncă nu există evaluări
- Proyecto PintucoDocument79 paginiProyecto PintucoDanny Camilo Jimenez Enciso50% (2)
- Andres Felipe Pachon Flechas: Pregunta Sin Contestar Puntúa Como 10,00Document6 paginiAndres Felipe Pachon Flechas: Pregunta Sin Contestar Puntúa Como 10,00Felipe PachonÎncă nu există evaluări
- Combustion A Volumen ConstanteDocument10 paginiCombustion A Volumen ConstanteLuis CarlosÎncă nu există evaluări
- Idepot Catalogo May 2014.Pdf1605189764Document29 paginiIdepot Catalogo May 2014.Pdf1605189764katjhoÎncă nu există evaluări
- Primer Parcial de Operaciones UnitariasDocument30 paginiPrimer Parcial de Operaciones UnitariasMaria Belen Ocampo FloresÎncă nu există evaluări
- TFM-G 105 PDFDocument89 paginiTFM-G 105 PDFBryan GrifterÎncă nu există evaluări
- Formularios de Mecanica de Los MaterialesDocument23 paginiFormularios de Mecanica de Los MaterialesimeldoÎncă nu există evaluări
- Registro de Uso y Manejo de ExtintoresDocument2 paginiRegistro de Uso y Manejo de ExtintoresNicolasMuñozVillalobosÎncă nu există evaluări
- Informe n03 Lab. de ConcretoDocument21 paginiInforme n03 Lab. de Concretoalex huayllaÎncă nu există evaluări
- PRACTICA 4 de Maquinas Eléctricas IDocument5 paginiPRACTICA 4 de Maquinas Eléctricas ILuis Benjamin Mendoza BallinesÎncă nu există evaluări
- Problemas de Termo Cap 3 (36, 43, 114, 121)Document4 paginiProblemas de Termo Cap 3 (36, 43, 114, 121)María Serrano100% (2)
- Las PresasDocument27 paginiLas PresasMichael Reyes100% (1)
- O.C. 3280Document4 paginiO.C. 3280drive jujspaÎncă nu există evaluări
- Tension Superficial y CapilaridadDocument4 paginiTension Superficial y Capilaridadyohn genryÎncă nu există evaluări
- Santisteban Ag PDFDocument383 paginiSantisteban Ag PDFMiguel PinchiÎncă nu există evaluări
- Caza FallasDocument16 paginiCaza FallasDiego CarreñoÎncă nu există evaluări
- Ast PitagoraDocument2 paginiAst Pitagoraivis molina tapiaÎncă nu există evaluări
- INOCUIDAD de BebidasDocument11 paginiINOCUIDAD de BebidasRosa Terrones Muñoz0% (1)