Documente Academic
Documente Profesional
Documente Cultură
Efecto Joule
Încărcat de
Juan Carlos Escobar ArosDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Efecto Joule
Încărcat de
Juan Carlos Escobar ArosDrepturi de autor:
Formate disponibile
EFECTO JOULE
INTEGRANTES:
Juan Carlos Escobar Aros 1227002
Juan Felipe Moreno 1228265
Christian Camilo Aragn 1429189
GRUPO 5
Resumen
Se determin el equivalente mecnico del calor (J) por medio de un calormetro y
diferentes masas de agua, el agua, que se encontraba en el calormetro se le aumento la
temperatura por medio de una resistencia por la cual recorra una corriente I de (20.1) A,
el incremento en la temperatura se registraba constantemente con un termmetro durante
un tiempo determinado con el fin de observar la relacin entre el incremento de la
temperatura y el tiempo para poder obtener un valor de J para cada experimento y probar
la valides de la Ley de Joule.
Mtodo experimental:
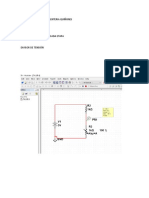
I. Inicialmente se procedi a
construir el circuito (Figura 1) que se
utilizara como montaje experimental y
posteriormente se ajust la fuente de
tal forma que circulara una corriente
de 2 A. El circuito se dej
desconectado del borne positivo de la
fuente mientras se empezaba a
realizar el experimento.
Figura 1. Circuito Elctrico para el
estudio del Efecto Joule [1]
II. Despus de tener el circuito
armado y ajusto, se procedi a pesar
el vaso pequeo del calormetro
(vaco y sin el anillo de caucho que lo
rodea).
III. Posteriormente se verti en el
vaso pequeo del calormetro una
cierta cantidad de agua y se pes
nuevamente, que por diferencia se
hall la cantidad de agua aadida
(alrededor de 200g).
IV. Con la masa del agua y del vaso
pequeo del calormetro ya obtenidas,
se procedi a colocar el vaso pequeo
del calormetro con agua dentro del
recipiente mayor del mismo y
seguidamente ambos se sellaron con
la parte final de este, que es el que
contiene la resistencia que debi
quedar inmersa en el agua del vaso
pequeo y que sera la encargada de
transforma aquella energa elctrica
que pasa por ella en energa calrica
que se disipara por el agua y por el
calormetro.
V. Con el calormetro ya cuadrado,
se introdujo un termmetro para medir
los cambios de temperatura e
inicialmente se tom la temperatura
inicial (T
i
) de agua, en el instante
anterior a conectar el circuito a la
fuente
VI. Ya con todo listo, se conect el
borne positivo de la fuente al circuito e
inmediatamente se empezaron a
tomar los valores de incremento de
temperatura hasta tener una
elevacin de la temperatura el minuto
10C. A medida que pasaba el tiempo;
el agua se estuvo agitando para
obtener una distribucin equilibrada
de la temperatura en el agua en
dentro del vaso. Estos datos
obtenidos se fueron registrando en la
tabla1A y finalmente despus
terminado el proceso de tomar los
diez datos se desconect el circuito
de la fuente
El procedimiento llevado a cabo desde el
paso III hasta el paso VI, se repiti para
una cantidad de agua alrededor de los
245,71g y para una de alrededor de
295,92g; los datos de temperaturas,
masa del agua y del calormetro, los
tiempos, la corriente y la diferencia de
potencial se observan en la Tabla 1B y
1C respectivamente.
Anlisis experimental:
Tabla 1.
Experimento 1
Masa del calormetro
54,33g
0,01g
Masa de Agua
200,11g
0,01g
Masa del calormetro mas
el agua
254,44g
0,01g
Calor especifico del
calormetro
0,21
Calor especifico del agua 1,00
Temperatura Inicial (T
i
) 26C 0,1C
t[s]
0,01s
T[C]
0,1C
t[s]
0,01s
T[C]
0,1C
0
85
155
220
280
26
27
28
29
30
340
396
440
463
494
31
32
33
34
35
V=6,67v0,
1v
I=2A0,1
A
VI=13,34w0,1
w
Experimento 2
Masa del calormetro
54,33g
0,01g
Masa de Agua
245,71g
0,01g
Masa del calormetro mas
el agua
300,04g
0,01g
Calor especifico del
calormetro
0,21
Calor especifico del agua 1,00
Temperatura Inicial (T
i
) 27C 0,1C
t[s]
0,01s
T[C]
0,1C
t[s]
0,01s
T[C]
0,1C
0
50
110
175
217
27
28
29
30
31
256
330
385
458
530
32
33
34
35
36
V=6,54v0,
1v
I=2A00,
1A
VI=13,08w0,1
w
Experimento 3
Masa del calormetro 54,33g
0,01g
Masa de Agua
295,92g
0,01g
Masa del calormetro mas
el agua
350,25g
0,1g
Calor especifico del
calormetro
0,22
Calor especifico del agua 1,00
Temperatura Inicial (T
i
) 27C 0,1C
t[s]
0,01s
T[C]
0,1C
t[s]
0,01s
T[C]
0,1C
0
60
105
206
283
27
28
29
30
31
405
460
546
632
750
32
32
34
35
36
V=6,56v0,
1v
I=2A0,1
A
VI=13,12w0,1
0w
Tabla 1. Datos obtenidos
experimentalmente para cada masa de
agua.
A partir de los datos obtenidos en el
primer procedimiento, en donde la masa
del agua fue Magua= 200,11 0,01g
dispuso a calcular
Mc=Magua*Cagua + Mcal*Ccal
De la cual ya conocemos todos los
datos, as que:
Mc
1
= 200,11*1 + 54,33*0,21= 211,52
Y de la misma forma calculamos Mc para
los 2 procedimientos restantes, en donde
la unica variacion era Magua:
Mc
2
= 245,71*1 + 54,33*0,21= 257,12
Mc
3
= 295,92*1 + 54,33*0,21= 306,41
Luego, con estos datos de potencia, la
desviacin estndar con ayuda de la
siguiente frmula:
Ec.1
S= watts
Como paso a seguir graficamos la
Temperatura en funcin del tiempo, una
sola grafica para los tres procedimientos
a partir de los datos consignados en las
tablas No1, 2 y 3, presentada a
continuacin:
Figura No.2 Grafica de Temperatura en
funcin del tiempo, de los tres casos del
experimento.
A partir de sta grafica, encontramos la
pendiente m, el intercepto b y el
coeficiente de correlacin r, para cada
una de las curvas descritas.
Para el caso 1(masa1):
m= 0,0177 0,001
b= 25,41 0,01
r= 0,988
Para el caso 2 (masa 2):
m= 0,017 0,001
b= 27,16 0,01
r= 0,997
Para el caso 3 (masa3):
m= 0,0118 0,001
b= 27,42 0,01
r= 0,996
Analizando la Figura No. 2 podemos
apreciar que las 3 relaciones de
Temperatura vs Tiempo parecen
describir un comportamiento lineal
esperado, ya que el aumento de la
temperatura en el agua es proporcional
al tiempo en el que la resistencia,
cargada con voltaje, est sumergida en
ella.
Con los datos calculados anteriormente
de Mc y VI, nos disponemos a calcular la
constante de Joule experimental para
cada caso usando la siguiente relacin:
Ec.2
= 3,563 0,622 j / cal
= 2,99 1,194 j / cal
= 3,628 0,55 j / cal
Ya con estos valores de J
experimentales encontramos el valor de
Error porcentual de cada una de ellas
respecto a la J terica que es J=4,186
j/cal, con ayuda de la ecuacin:
Error %=
* 100% Ec.3
Hallando as:
Error 1= 14,88%
Error 2= 28,57%
Error 3= 13.33%
A partir de los resultados obtenidos,
podemos decir que en comparacin con
el valor terico de J= 4,186 j / cal,
nuestros J experimentales son muy
cercanos a ese valor, a excepcin de
muestro J experimental del caso 2 que
muestra una gran diferencia, tambin
puede estar tal vez relacionada con que
el valor de temperatura inicial que para
este caso fue de 26C a diferencia de
los dos casos siguientes para los cuales
la temperatura inicial fue de 27C. Y las
pequeas diferencias de los J exp de los
casos 2 y 3 respecto a la J terica se
deben tal vez a los clculos hechos con
las pendientes, debido a que puede ser
que al usarlas con sus incertidumbres el
valor cambie lo necesario para llegar a
un valor ms cercano a 4,186 j / cal.
Ahora, habiendo hallado lo valores de las
pendientes para cada caso y teniendo
los valores de masa de agua usados en
cada uno, graficamos la relacin de
pendiente inversa en funcin de la masa
de agua, en la siguiente figura:
Figura No.3 Grafica de la relacin de
pendiente inversa en funcin de la masa
de agua, desarrollada a partir de la
ecuacin 6.
De la grafica anterior y con ayuda del
programa usado para hacerla,
encontramos la pendiente y el intercepto
que tendra al ser linealizada, lo obtenido
es:
m=0,2746 0,001
b=-0,449 0,001
Para esta grafica, la pendiente
representa el valor proporcional de la
capacidad calorfica del agua. Para
nuestro caso el resultado es m=0,2746 ,
pero el esperado es 0,2 idealizando el
valor de J=4,186 y promediando el valor
de VI=13,18 watts. A pesar de todo, la
diferencia entre los dos valores no es
grande y podemos decir que el resultado
es el esperado, tomando en cuenta los
diferentes variables que intervinieron en
el experimento y pudieron interferir en
este resultado.
CONCLUSIONES
Se observ que la energa
potencial elctrica proveniente de
una fuente, sufre una
transformacin a energa calrica
confirmando el principio de la
conservacin de la energa.
Apreciamos el cumplimiento de la
Ley de joule ya que los
equivalentes de J experimentales
hallados en cada caso fueron
muy cercanos al valor terico de
esta J=4,186 J/cal.
Pudimos observar el
cumplimiento del principio de
conservacin de energa al ver
que la energa de potencial
elctrico aplicado en la
resistencia se transformaba en
energa calrica al estar en
contacto con el agua.
REFERENCIAS
[1] Gua de Practicas Laboratorio de
Electromagnetismo, Universidad del
Valle, Facultad de Ciencias,
Departamento de Fsica.
[2] El Efecto Joule y los Artefactos que
trabajan con este efecto. Universidad
Central de Venezuela. Facultad de
Ciencias. Caracas 2011.
[3] SEARS. Fsica Universitaria. Volumen
2. Onceava edicin. Mxico: Cengage
Learning 2009
S-ar putea să vă placă și
- 6th Central Pay Commission Salary CalculatorDocument15 pagini6th Central Pay Commission Salary Calculatorrakhonde100% (436)
- Interpretacion de Fallas en Motores ElectricosDocument59 paginiInterpretacion de Fallas en Motores ElectricosJaime Martin Torres HuamaniÎncă nu există evaluări
- 2017 - Proyecto Aula 9o.Document10 pagini2017 - Proyecto Aula 9o.Juan Carlos Escobar ArosÎncă nu există evaluări
- Copia de Presupuesto - IntinerarioDocument11 paginiCopia de Presupuesto - IntinerarioJuan Carlos Escobar ArosÎncă nu există evaluări
- Scient DirectDocument13 paginiScient DirectJuan Carlos Escobar ArosÎncă nu există evaluări
- P.II 9o. C.SocialesDocument7 paginiP.II 9o. C.SocialesJuan Carlos Escobar ArosÎncă nu există evaluări
- Taller 4Document8 paginiTaller 4Juan Carlos Escobar ArosÎncă nu există evaluări
- Conexión paralela generadoresDocument4 paginiConexión paralela generadoresJuan Carlos Escobar ArosÎncă nu există evaluări
- PC Valor Del Dinero EqFDocument1 paginăPC Valor Del Dinero EqFJuan Carlos Escobar ArosÎncă nu există evaluări
- Vibraciones MecanicasDocument35 paginiVibraciones Mecanicaskiefer_hardÎncă nu există evaluări
- Analisis de Las VibracionesDocument27 paginiAnalisis de Las VibracionesSamuel M Sarmiento MorenoÎncă nu există evaluări
- 12 TurbinasgasPROBLEMAS PDFDocument20 pagini12 TurbinasgasPROBLEMAS PDFJuan Carlos Escobar ArosÎncă nu există evaluări
- TransforDocument26 paginiTransforJuan Carlos Escobar ArosÎncă nu există evaluări
- 12 TurbinasgasPROBLEMAS PDFDocument20 pagini12 TurbinasgasPROBLEMAS PDFJuan Carlos Escobar ArosÎncă nu există evaluări
- Requerimiento TécnicoDocument2 paginiRequerimiento TécnicoJuan Carlos Escobar ArosÎncă nu există evaluări
- Antep Roy EctoDocument18 paginiAntep Roy EctoJuan Carlos Escobar ArosÎncă nu există evaluări
- IcfesDocument2 paginiIcfesJuan Carlos Escobar ArosÎncă nu există evaluări
- File View Design 4046 Report PDFDocument5 paginiFile View Design 4046 Report PDFJuan Carlos Escobar ArosÎncă nu există evaluări
- Proyecto Electro 1Document16 paginiProyecto Electro 1Juan Carlos Escobar ArosÎncă nu există evaluări
- Lab 1Document19 paginiLab 1Juan Carlos Escobar ArosÎncă nu există evaluări
- Proyecto FinalDocument15 paginiProyecto FinalJuan Carlos Escobar ArosÎncă nu există evaluări
- Pendulo SimpleDocument4 paginiPendulo SimpleJuan Carlos Escobar ArosÎncă nu există evaluări
- Energías alternativas ColombiaDocument2 paginiEnergías alternativas ColombiaJuan Carlos Escobar Aros75% (4)
- ElectronicaDocument4 paginiElectronicaJuan Carlos Escobar ArosÎncă nu există evaluări
- Campos Magnéticos en Las Proximidades de Conductores Con CorrientesDocument4 paginiCampos Magnéticos en Las Proximidades de Conductores Con CorrientesJuan Carlos Escobar ArosÎncă nu există evaluări
- Actividad Central Act 1Document9 paginiActividad Central Act 1Juan Carlos Escobar ArosÎncă nu există evaluări
- Prueba Recursos NaturalesDocument11 paginiPrueba Recursos NaturalesCristobal EnriquezÎncă nu există evaluări
- Tema V Difusión de SólidosDocument52 paginiTema V Difusión de SólidosGisel Viviana Molina MoreÎncă nu există evaluări
- Informe de FisicaDocument7 paginiInforme de FisicaJOSEPH ENRIQUE BUGARIN QUISPEÎncă nu există evaluări
- Laboratorio 05 - Grupo de ConexiónDocument12 paginiLaboratorio 05 - Grupo de ConexiónMario Brevis Castillo0% (1)
- Ireca - Armonización Centros de EnergíaDocument1 paginăIreca - Armonización Centros de Energíalaleydelaatraccion100% (7)
- Estrategia Regulacion Nacional H2Document199 paginiEstrategia Regulacion Nacional H2Jose Maria Jara Vilugron100% (1)
- (Clase 5) Conservación de La Energía (Ejercicios)Document9 pagini(Clase 5) Conservación de La Energía (Ejercicios)Daniel Rios PrietoÎncă nu există evaluări
- Partes de Un Generador SincronoDocument3 paginiPartes de Un Generador SincronoJonathan Hernandez GuijosaÎncă nu există evaluări
- Informe N°9 Transformadores de Medida, Transformadores de TensiónDocument10 paginiInforme N°9 Transformadores de Medida, Transformadores de TensiónEnrique Rivera SantosÎncă nu există evaluări
- Prueba1 2d BimestreDocument2 paginiPrueba1 2d BimestreDarwin MoranÎncă nu există evaluări
- Conexión RED eléctricaDocument12 paginiConexión RED eléctricaJose Maria Castillo HernandezÎncă nu există evaluări
- Tintes ecológicosDocument5 paginiTintes ecológicosterryhch20Încă nu există evaluări
- Termodinamica Unidad 1Document60 paginiTermodinamica Unidad 1Jesus Perez PerezÎncă nu există evaluări
- Qué Es El Motor de CondensadorDocument11 paginiQué Es El Motor de CondensadorHector GonzalezÎncă nu există evaluări
- Conservación de La Energía MecánicaDocument2 paginiConservación de La Energía MecánicaleslyÎncă nu există evaluări
- Ciencia y Tecnología Pilar Guzmán: Valores Y Actitudes Recursos Y MaterialesDocument7 paginiCiencia y Tecnología Pilar Guzmán: Valores Y Actitudes Recursos Y MaterialesAnto PMontoyaÎncă nu există evaluări
- Ciclo CombinadoDocument31 paginiCiclo CombinadoLuis Antonio Soto100% (1)
- Control de RegistrosDocument11 paginiControl de RegistrosisaiasÎncă nu există evaluări
- Pintarás Los Soles de Su CaminoDocument204 paginiPintarás Los Soles de Su Caminopapclise100% (2)
- Aislamiento de energíasDocument11 paginiAislamiento de energíasfrancisco florsÎncă nu există evaluări
- Cuestionario FinalDocument37 paginiCuestionario FinalJaviv Fernando AmayaÎncă nu există evaluări
- Inprosa Informe Anual 2022Document3 paginiInprosa Informe Anual 2022Joel CarrielÎncă nu există evaluări
- Grandes Misterios de Catedrales y El AltarDocument12 paginiGrandes Misterios de Catedrales y El Altarcarolina_sorrenti100% (1)
- Instalaciones eléctricas distribución cablesDocument63 paginiInstalaciones eléctricas distribución cablesLauro Landazuri Montenegro100% (1)
- EspanholDocument2 paginiEspanholElio Vila100% (2)
- InvestigaciónDocument10 paginiInvestigaciónKevin RodriguezÎncă nu există evaluări
- Manual Ingenieria Tigre-ADS - Cap 3 HidraulicaDocument16 paginiManual Ingenieria Tigre-ADS - Cap 3 HidraulicaemiliolgÎncă nu există evaluări
- Alternador y SopladorDocument17 paginiAlternador y SopladorEnny Pizarro CortésÎncă nu există evaluări
- Qué Es Una Reacción ExotérmicaDocument1 paginăQué Es Una Reacción ExotérmicaAlan Sebastian MontoyaÎncă nu există evaluări
- Listado Preliminar 07-2023Document36 paginiListado Preliminar 07-2023crife.1994.2014Încă nu există evaluări