Documente Academic
Documente Profesional
Documente Cultură
Química Experimental I Relatorio Jakeline
Încărcat de
Jakeline de Souza Bastos100%(3)100% au considerat acest document util (3 voturi)
682 vizualizări23 paginiDrepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
100%(3)100% au considerat acest document util (3 voturi)
682 vizualizări23 paginiQuímica Experimental I Relatorio Jakeline
Încărcat de
Jakeline de Souza BastosDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 23
FUNDAO UNIVERSIDADE FEDERAL DO TOCANTINS
CURSO DE LICENCIATURA EM QUMICA
DISCIPLINA: QUMICA EXPERIMENTAL I
Sntese Do Cloreto De Hexaaminoclorocobalto(III) - [CO(NH
3
)
6
]CL
3
Sntese Do Cloreto De Pentaaminoclorocobalto(III) - [CO(NH
3
)
5
CL ]CL
2
Sntese Do Cloreto De Pentaamino(Nitro)Cobalto(III)-[CO(NH
3
)
5
NO
2
]CL
2
Sntese Do Cloreto De Pentaamino(Nitrito)Cobalto(III)-[CO(NH
3
)
5
ONO]CL
2
ACADMICOS (A): JAKELINE DE SOUZA BASTOS
PROFESSOR: DR. JOS EXPEDITO
ARAGUANA, 20 DE AGOSTO DE 2013.
INTRODUO
Os complexos so espcies formadas pela interao de ons ou molculas neutras
(bases de Lewis) com um tomo metlico central neutro ou ction (cido de Lewis), de
tal modo que o nmero de tomos diretamente ligados a esse tomo central superior
valncia normal (estado de oxidao formal) deste tomo. Os complexos podem ser
aninicos, neutros ou catinicos e apresentam uma variedade de geometrias, sendo as
mais comuns a octadrica, no caso de complexos hexa-coordenados e a plano-quadrado
ou a tetradrica, no de complexos tetra-coordenados (RIVER, 2003).
Os complexos de Co(III) contendo o ligante amina foram extensivamente
investigados por Werner. Os complexos de Co
2+
so bastante lbeis, isto sofrem fcil
reao de substituio dos seus ligantes, enquanto os de Co
3+
so inertes. Por esta razo,
normalmente os complexos de Co
3+
so produzidos a partir de [Co(OH
2
)
6
]
2+
na presena
de NH
4
X (X = Cl, Br, etc), NH
3
e de um agente oxidante. Dependendo das condies da
reao, formam-se [Co(NH
3
)
6
]3
+
, [Co(NH
3
)
5
X]
2+
ou [Co(NH
3
)
4
X
2
]
+
. O complexo
[Co(NH
3
)
6
]
3+
pode ser isolado, por exemplo na forma do cloreto, [Co(NH
3
)
6
]Cl
3.
(MAGALHES, 2013).
Segundo a Teoria do Campo Cristalino (TCC), o ligante amino (ou amin)
mais forte que o ligante aquo (ou aqua) e este ltimo, mais forte que o ligante
cloro. Assim, considerando-se apenas a fora dos ligantes, pode-se supor que os
complexos de cobalto com amnia so mais estveis que os complexos de cobalto com
nions cloreto na esfera de coordenao. Isso pode ser verificado experimentalmente
para os compostos: [Co(NH
3
)
6
]Cl
3
e [CoCl(NH
3
)
5
]Cl
2
. Enquanto o primeiro bastante
estvel em solues aquosas, o segundo reage com gua produzindo [Co(NH
3
)
5
H
2
O]Cl
3
(OLIVEIRA, 2010).
Werner deduziu que no CoCl
3
.6NH
3
os trs cloros atuam como tendo valncias
primrias e as seis molculas de amnia com valncia secundria. Em termos atuais, os
trs cloros so inicos, ou seja, ons cloretos, por isso precipitam como AgCl; os seis
ligantes NH3 formam ligaes coordenadas com o on Co
+3
, originando o on complexo
[Co(NH
3
)
6
]
+3
. Werner verificou que o CoCl
3
.5NH
3
poderia ser obtido do CoCl
3
.6NH
3
por perda de uma molcula de amnia, com a simultnea transformao de um cloro de
valncia primria para um cloro de valncia secundria. Assim somente dois Cl
-
so
inicos e podem precipitar com o AgNO
3
na forma de AgCl, portanto, cinco molculas
de amnia e um on cloreto formam valncias secundrias (ligaes coordenadas) a um
on Co
+3
, formando o on complexos [Co(NH
3
)
5
Cl]
+2
. (MENDES, 2013)
Quando temos um ligante ambidentado, como, por exemplo o SCN
-
e o on
nitrito NO
2
-
, a ligao com o metal pode ser pelo enxofre ou nitrognio no on
tiocianato e pelo nitrognio ou oxignio no on nitrito, os dois ismeros formados
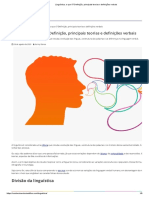
constituem ento de uma isomeria de ligao (COELHO, 2010).
Figura1. Rota de obteno de dois ismeros de ligao de um complexo de Co(III).
(Fonte: http://pt.scribd.com/document_downloads/direct/44483242.)
OBJETIVO
Experimento I: Preparar o complexo de hexaaminocobalto(III) a partir de cloreto de
cobalto (II) hexa-hidratado.
Experimento II: Preparar o cloreto de pentaaminoclorocobalto(III) a partir de cloreto de
cobalto (II) hexa-hidratado.
Experimento III: Sintetizar o cloreto de pentaamino(nitro)cobalto(III) e o cloreto de
pentaamino(nitrito)cobalto(III) a partir do o cloreto de pentaaminoclorocobalto(III) .
MATERIAIS E MTODOS
Materiais Utilizados
- Bquer
- Erlernmeyer
- Balana analtica
- Chapa de aquecimento
- Basto de vidro
- Pipeta volumtrica
- Pisseta
- Termmetro
- Geladeira
- Funil de Buncher
- Micro filtro fibra
- Papel de tornasso
- Kitassato
- Aste Universal e Garra
- Vidro de relgio
- Bquer
- Bomba de vcuo
- Funil
- Papel de filtro
- Espatula.
Reagentes:
- Cloreto de amnia
- Cloreto hexaquacobalto II
- Carvo ativo
- Hidrxido de amnia concentrado
- cido clordrico concentrado
- Perxido de hidrognio a 30 % m/m
- gua destilada
- lcool etlico (Etanol Absoluto)
- ter etlico
- gua destilada
- Soluo de 6 mol/L de cido
clordrico
-Soluo de cido clordrico 0,17
mol/L
- Nitrato de sdio
- Pentaminclorocobalto III
EXPERIMENTO I
Sntese Do Cloreto De Hexaaminoclorocobalto(III) - [CO(NH
3
)
6
]Cl
3
Deixou-se na geladeira uma pisseta contendo H2O gua destilada para ser
utilizada posteriormente durante a realizao da sntese. Inicialmente foram pesados
2,0056g de NH
4
Cl em um bquer de 50 mL e 3,0000g de CoCl
2
.6H
2
O em um bquer de
50 mL.
Em um bquer com o NH
4
Cl adicionou 10 mL de gua destilada foi levado para
a chapa aquecedora a soluo de NH
4
Cl em um erlenmeyer de 250 mL e submetido ao
aquecimento chegando quase a entra em ebulio com temperatura prximo 100 C.
Quando a soluo comeou a entra em ebulio foram adicionados 3,0000g de
CoCl
2
.6H
2
O, e ainda com a soluo aquecida foi adicionado 0,2g de carvo ativado. Ao
terminar esse procedimento o bquer de 250 mL foi resfriado em gua corrente (gua de
torneira), afim que atingisse a temperatura ambiente.
Na capela adicionou 8 mL de hidrxido de Amnia e colocou a soluo em
banho de gelo ate que a soluo atingisse uma temperatura prxima de 10 C. Em
seguida adicionou 6 mL de perxido de hidrognio H
2
O
2
a 30% m/m, em seis pores
de um mL e levou para aquecimento de 5 minutos agitando-o, aps decorrido as 5
minutos levou a soluo para resfriar em gua corrente, e depois colocou em banho de
gelo. Para acelerar o processo de resfriamento colocamos a soluo no congelador e
verificamos a temperatura a cada 2 minutos.
1 Verificao: 18 C
2 Verificao: 8 C
3 Verificao: 4 C
4 Verificao: 3 C
5 Verificao: 0 C
Depois de a soluo atingir 0 C, filtrou-se a mistura a quente, sob presso
reduzida. O filtrado foi colocado em um erlenmeyer e adicionou-se 2 mL de cido
clordrico (HCl) concentrado para poder formar o complexo, sendo que o cloro age
como conta on para formao no complexo.
A soluo foi resfriada em banho de gelo com agitao contnua manual. Foi
filtrado o precipitado obtido em funil de vidro com placa filtrao sob presso reduzida.
Lavou-se o slido obtido com duas pores de 5 mL de lcool etlico absoluto e, em
seguida, com duas pores de 5 mL de ter etlico. Foi deixado o slido secar ao ar,
posteriormente colocado no dissecador para ser pesado na aula seguinte.
EXPERIMENTO II
Sntese Do Cloreto De Pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
Procedimento
Deixou-se na geladeira uma pisseta contendo H2O gua destilada para ser
utilizada posteriormente durante a realizao da sntese. Inicialmente foram pesados
1,2626 g de NH
4
Cl em um bquer de 50 mL e 2,5792 g de CoCl
2
.6H
2
O em um bquer
de 50 mL.
Primeiramente diluiu-se o NH
4
Cl em um Becker com 8 mL de uma soluo
concentrada de hidrxido de Amnio, logo aps transferiu-se a soluo para um
erlenmeyer de 150 mL homogeneizando-a, sob agitao adicionou-se o CoCl
2
.6H
2
O. Na
capela adicionou-se 6 mL de H
2
O
2
a 30% em seis pores de um mL e 8 mL de cido
clordrico levando-o a soluo para aquecer em torno de 20 min a 90 C (neste
momento observa-se que a colorao da soluo apresenta um cor semelhante ao azul
marinho).
Quando a soluo foi aquecida (estava liquida), depois de passado os 20 min
com a soluo na chapa de aquecimento, aps o aquecimento percebe-se que a soluo
formou um precipitado (azul marinho solido), a soluo foi retirada e levada com gua
corrente at atingir a temperatura ambiente para depois levar para o banho de gelo para
atingir uma temperatura prxima zero, onde ir solidificar a soluo quando a soluo
atingiu zero grau a colorao muda de azul marinho para violeta.
Depois de solidificado levou a soluo contendo o complexo para filtrao a
vcuo utilizando o micro filtro fibra, a soluo foi ento lavada com 16 mL de gua
destilada em quatro pores de 4 mL, 5 mL de lcool etlico (absoluto) em duas pores
de 2,5 mL e com uma poro de 1,25 mL de ter de petrleo, depois desta etapa de
filtrao transferiu-se os cristais para o dissecador , para em seguida calcular a sua
massa e fazer os clculos de rendimento.
EXPERIMENTO III
Sntese Do Cloreto De Pentaamino(Nitro)Cobalto(III)-[Co(NH
3
)
5
NO
2
]Cl
2
Sntese Do Cloreto De Pentaamino(Nitrito)Cobalto(III)-[Co(NH
3
)
5
ONO]Cl
2
Sntese Do Cloreto De Pentaamino(Nitro)Cobalto(III)-[Co(NH
3
)
5
NO
2
]Cl
2
Em um becker foi pesado 1,00g do complexo [Co(NH
3
)
5
Cl]Cl
2
, em seguida o
complexo [Co(NH
3
)
5
Cl]Cl
2
foi diludo em uma soluo contendo 12,5mL de gua
destilada e 1mL de amnia concentrada, aps feita a diluio do complexo o mesmo foi
levado para uma chapa de aquecimento at atingir aproximadamente 60C. A soluo
foi filtrada a quente no sistema a vcuo trapo. Aps a filtragem a soluo que estava
levemente aquecida, foi deixada na bancada para que atingisse a temperatura ambiente.
Quando a soluo atingiu a temperatura ambiente, neutralizamos com a soluo
de cido clordrico diludo com o auxilio do papel de tornassol (papel indicador
universal) para que a soluo ficasse neutra pH = 7.. Depois de neutralizada a soluo
foram adicionados 1, 55 g de nitrito de sdio NaNO
2
e a soluo foi levada novamente
para a chapa de aquecimento at atingir a temperatura de 60 C, at que todo o
precipitado avermelhado tenha se dissolvido, para poder retirar a soluo da chapa de
aquecimento e esperar que a mesma atingisse a temperatura ambiente.
Esperou-se soluo resfriar a temperatura ambiente e adicionou-se 17, 5 mL de
cido clordrico concentrado a principio ir colocado a soluo cuidadosamente para que
em seguida pudesse colocar o restante da soluo de cido. A soluo foi ento levada
para banho de gelo, at que se perceba a formao dos cristais para poder realizar a
filtrao. Separaram-se os cristais por filtrao a vcuo, lavando-os em seguida com
pequenas pores de gua gelada, lcool etlico e ter. A lavagem segue essa ordem,
pois a gua primeiramente retira as impurezas j que o complexo formado insolvel
em gua, o lcool tambm atua retirando as impurezas e o ter vai agir retirando o total
de gua presente. Os cristais obtidos foram levados ao dissecador para posteriormente
serem pesados e ser realizado o calculo do rendimento.
Sntese Do Cloreto De Pentaamino(Nitrito)Cobalto(III)-[Co(NH
3
)
5
ONO]Cl
2
Primeiramente em um bquer foi pesado 0,5245 g de pentaminclorocobalto III e
adicionados 10 mL de gua destilada e na capela adicionados 2,5 mL de hidrxido de
amnia e depois levou a soluo para a chapa de aquecimento para aquecer em ~ 20 min
at que a temperatura atingisse aproximadamente 60 C, a soluo foi ento filtrada
utilizando um suporte, funil de vidro e papel filtro.
depois de filtrado, transferiu a soluo para um erlenmeyer, e deixada em
repouso at que atingisse a temperatura ambiente e neutralizou a mesma com 0,75 mL +
2 gotas de uma soluo de 6 mol/L de cido clordrico com o auxilio do papel de
tornassol (papel indicador universal), para que a soluo ficasse neutra pH = 7.
Realizada a neutraliza a soluo foi adicionada a soluo 0,7519 g de nitrato de
sdio e mais 0,75 mL de uma soluo de 6 mol/L de cido clordrico, posteriormente o
experimento foi levado para o banho de gelo, para que a formaes ocorresse com mais
eficincia a soluo foi deixada em repouso no congelador a soluo para formar os
cristais, aps realizado o banho de gelo (resfriamento da soluo), percebe-se que h a
formao de cristais.
Depois de formado os cristais, levaram-o para fazer a filtragem a vcuo, para
retirar o excesso de reagente. No filtro colocou 5mL de gua destilada, em seguida
adicionou 5 mL de lcool etlico e 5 mL de ter de petrleo,.A lavagem segue essa
ordem, pois a gua primeiramente retira as impurezas j que o complexo formado
insolvel em gua, o lcool tambm atua retirando as impurezas e o ter vai agir
retirando o total de gua presente. Depois de filtrado deixou o composto em repouso
para secar e fazer a pesagem de qual a massa produzida e posteriormente fazer os
clculos de rendimento.
RESULTADOS
Para a sntese do cloreto de Hexaaminoclorocobalto(III) - [CO(NH
3
)
6
]Cl
3
(experimento I), a reao para a formao do complexo ocorre entre o cloreto de cobalto
(II) hexa-hidratado ([Co(H
2
O)
6
]
2+
com o cloreto de amnio NH
4
Cl primeiramente,
posteriormente com amnia e catalisada com o oxignio liberado na reao da
decomposio do pexorido de hidrognio produzindo um complexo de colorao
laranja. Para a preparao do composto utilizamos 3,00 g de ([Co(H
2
O)
6
]
2
reagiu com
2,0056g de NH
4
Cl produzindo 0,4206 g de (Hexaaminocobalto (III)).
Para a sntese do cloreto de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
(experimento II), cloreto de cobalto (II) hexa-hidratado ([Co(H
2
O)
6
]
2+
vai reagir com o
NH
4
Cl primeiramente, posteriormente com amnia e catalisada com o oxignio liberado
na reao da decomposio do pexorido de hidrognio, a reao de substituio dos
ligantes do Cobalto, os ligantes que podem substituir a gua neste caso so (NH
3
) e (Cl
-
), onde os seis ligantes do cobalto sero substitudos por 5 (NH
3
) e 1 (Cl
-
) formando
assim o cloreto de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
]Cl
2
de colorao roxa.
Para a preparao do cloreto de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
]Cl
2,
foram
utilizados 2, 5792 g de ([Co(H
2
O)
6
]
2+
que reagiram com 1.2628g de NH
4
Cl produzindo
0,0343 g de cloreto de pentaaminoclorocobalto(III). Percebe-se que ouve um formao
muito pequena do complexo, que resultar consequentemente em rendimento muito
baixo, isso pode ter sido ocasionado tanto por erros dos participantes na realizao do
experimento, como por erros de equipamentos ou mesmo as solues no estarem com
a concentrao ideal para a realizao deste experimento.
O experimento III consistiu na realizao de duas snteses: a sntese do cloreto
de pentaamino(nitro)cobalto(III)-[Co(NH
3
)
5
NO
2
]Cl
2
e a sntese do cloreto de
pentaamino(nitrito)cobalto(III)-[Co(NH
3
)
5
ONO]Cl
2
. Para a realizao da sntese dos
dois complexo partimos do complexo de cloreto de pentaaminoclorocobalto(III) -
[CO(NH
3
)
5
Cl]Cl
2
sintetizado em aulas anteriores, o que vai diferir uma sntese da outra
a quantidade de cloreto de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
que ser
utilizado para a formao desses novos complexos e a quantidade de nitrito de sdio
NaNO
2
tambm utilizado.
Para a sntese do a sntese do cloreto de pentaamino(nitro)cobalto(III)-
[Co(NH
3
)
5
NO
2
]Cl
2 ,
utilizamos 1,0 g do complexo de cloreto de
pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
e 1,55 g de NaNO
2
que produziu 0,510
g de cloreto de pentaamino(nitro)cobalto(III)-[Co(NH
3
)
5
NO
2
]Cl
2.
Para a sntese do
sntese do cloreto de pentaamino(nitrito)cobalto(III)-[Co(NH
3
)
5
ONO]Cl
2
utilizamos
0,5245 do complexo de cloreto de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
e
0,7519g de NaNO
2
que produziu 0,277 g de cloreto de pentaamino(nitro)cobalto(III)-
[Co(NH
3
)
5
NO
2
]Cl
2
CONCLUSO
As snteses dos complexos do Co
3+
, so tcnicas fceis de serem trabalhadas em
sala de aula, o Co
3+
tem o numero de coordenao 6, ou seja, possui seis ligantes ao seu
redor formando uma estrutura octaedrica. Para que as snteses dos complexos do Co
3+
sejam formados, primeiramente o cobalto (II) ser oxidado a cobalto (III) pela H
2
O
2
,
posteriormente, foi adicionado excesso de HCl para formao da ligao coordenada de
cloro com o cobalto, resultando no complexo octadrico.
A partir dos clculos dos rendimentos (que sero mostrados posteriormente nas
questes no final deste relatrio), pode-se concluir que muitos podem ser os fatores que
alteram no resultado de uma sntese de um complexo. Os rendimentos para os
complexos de cobalto: cloreto de hexaaminoclorocobalto(III) - [CO(NH
3
)
6
]Cl
3
, cloreto
de pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl ]Cl
2
, cloreto de
pentaamino(nitro)cobalto(III)-[Co(NH
3
)
5
NO
2
]Cl
2
e do cloreto de
pentaamino(nitrito)cobalto(III)-[Co(NH
3
)
5
ONO]Cl
2
, foram respectivamente: 12,45 %;
1,3%; 49,08% e 52,81%.
De acordo com esses resultados percebe-se que o cloreto de
pentaaminoclorocobalto(III) - [CO(NH
3
)
5
Cl]Cl
2
foi o que obteve o menor rendimento,
o que pode ter sido ocasionado por falhas na realizao do experimento, j os outros
complexos do cobalto apresentaram um maior rendimento indicando uma melhor
eficincia na realizao dos experimentos.
QUESTIONRIOS
EXPERIMENTO I:
1. Qual a funo de NH
4
Cl nesta sntese?
A funo do cloreto de amnio nesta sntese evitar a formao de complexos
intermedirios e fazer com que todas as molculas de gua que esto ligadas ao cobalto
sejam substitudas pelas do ligante.
2. Escreva a equao da reao entre cloreto de hexaaquocobalto(II) e amnia.
[Co(H
2
O)
6
] Cl
2
+ 6NH
3
[Co(NH
3
)
6
]Cl
2
+ 6H
2
O
3. Veja os potenciais padres de reduo abaixo. A sntese feita nesta prtica seria
vivel utilizando-se O
2
em vez de H
2
O
2
? Por que foi utilizado perxido de
Hidrognio? Explique.
Porque o perxido de hidrognio quando adicionada a soluo
decompe-se em gua (H
2
O) e oxignio (O
2)
sua utilizao nesta reao era
justamente para que O
2
produzido na sua decomposio agisse como agente oxidante a
reao a qual foi intensa e exotrmica. Utilizamos o H
2
O
2
para a sntese desses
complexos porque este um reagente de mais fcil acesso.
4. Por que o composto obtido foi lavado com etanol e ter etlico?
O lcool nesta reao vai retirar as possveis impurezas contidas no complexo e
o ter etlico vai retirar todo o excesso de gua presente no composto.
5. Calcule o rendimento para a obteno de [Co(NH
3
)
6
]Cl
3
.
Para o calculo do rendimento vamos partir da reao que ocorre entre os reagentes para
a obteno do complexo.
4 CoCl
2
.6H
2
O + 4 NH
4
Cl + 20 NH
3
+ O
2
4 [Co(NH
3
)
6
]Cl
3
+ 26 H
2
O
Dados:
MM das Substancias de acordo com a estequiometria da reao:
CoCl
2
.6H
2
O = 956 g/mol
NH
4
Cl = 216 g/mol
NH
3
= 340 g/mol
O
2
= 32g/mol
[Co(NH
3
)
5
]Cl
3
= 1.076 g/mol
H
2
O = 486g/mols
Massa utilizada:
CoCl
2
.6H
2
O = 3,000 g
NH
4
Cl = 2,0056 g
Massa obtida:
[Co(NH
3
)
5
]Cl
3
= 0,4206 g (rendimento real)
Antes de calcular o rendimento terico da formao do complexo, vamos saber quem
o reagente limitante a partir da quantidade de mols de cada substancia, neste casa vamos
analisar a quantidade de mols desses dois compostos CoCl
2
.6H
2
O e NH
4
Cl , a partir
desta formula:
N
mols
= __m(g)__
MM(g/mol)
N
CoCl2.6H2O
= __3,0000g__ = 3,1x10
-3
mols
956 g/mol
N NH
4
Cl = __2,0056__ = 9,23x10
-3
mols
216 g/mol
A partir desses valores conclumos que o reagente limitante desta reao o cloreto de
hexaaminocobalto(III). A partir do reagente limitante podemos calcular qual a massa do
reagente que est em excesso, e calcular o rendimento terico da reao.
Massa do reagente em excesso:
956 g de CoCl
2
.6H
2
O 216 g de NH
4
Cl
3,000 g de CoCl
2
.6H
2
O x
X = 0,677 g de NH
4
Cl
X = 0,677 g de NH
4
Cl que eu preciso para reagir com 3,000 g de CoCl
2
.6H
2
O. Ento a
massa em excesso = (massa que foi utilizada) (massa que realmente precisa)
massa em excesso = 2,0056 0,677 = 1,3276 g de NH
4
Cl em excesso.
Agora partimos a partir do reagente limitante para calcular o rendimento terico do
complexo.
956 g de CoCl
2
.6H
2
O 1.076 g de [Co(NH
3
)
6
]Cl
3
3,000 g de CoCl
2
.6H
2
O x
X= 3,3765 g de [Co(NH
3
)
6
]Cl
3
(rendimento terico)
Calculo do rendimento = __rendimento real__ x 100
Rendimento terico
Calculo do rendimento = 0,4206 g x 100
3,3765 g
Rendimento = 12,45%
6. Desenhe as estruturas dos ons hexaaminocobalto(III) e hexaaminocobalto(II).
EXPERIMENTO II:
1. Quais so as diferenas nos procedimentos experimentais nas snteses de
[CoCl(NH
3
)
5
]Cl
2
e de [Co(NH
3
)
6
]Cl
3
? Justifique.
As diferenas nos procedimentos experimentais dos dois complexos so as
quantidades de reagentes utilizados, para a sntese do [Co(NH
3
)
6
]Cl
3
foram utilizados
3,00 g de ([Co(H
2
O)
6
]
2
reagiu com 2,0056g de NH
4
Cl, neste procedimento foi
adicionado 0,2 g de carvo ativo, e tambm foi realizada uma filtragem a quente. J para
a sntese do [Co(NH
3
)
6
]Cl
3
foram utilizados 2, 5792 g de ([Co(H
2
O
6
]
2+
que reagiram
com 1.2628g de NH
4
Cl, neste experimento no foi adicionado carvo ativo nem feito a
filtragem a quente.
2. Proponha um procedimento para se obter [CoCl
2
(NH
3
)
4
]Cl.
3. Por que se recomenda gua gelada para lavar o produto obtido?
No procedimento para a formao do precipitado submetemos a soluo a uma
temperatura aproximada a 0C, para que no haja nenhuma variao de temperatura
durante o processo de filtrao, a gua gelada para a lavagem do produto obtido.
4. Calcule o rendimento para a obteno de [CoCl(NH
3
)
5
]Cl
2
.
2 CoCl
2
.6H
2
O + 2 NH
4
Cl + 18 NH
3
+ O
2
2 [Co(NH
3
)
5
]Cl
2
+ 14 H
2
O
Dados:
MM das Substancias de acordo com a estequiometria da reao:
CoCl
2
.6H
2
O = 478 g/mol
NH
4
Cl = 108 g/mol
NH
3
= 306 g/mol
O
2
= 32g/mol
[Co(NH
3
)
5
Cl]Cl
2
= 484,5 g/mol
H
2
O = 252g/mols
Massa utilizada:
CoCl
2
.6H
2
O = 2,5792 g
NH
4
Cl = 1,2628 g
Massa obtida:
[Co(NH
3
)
5
]Cl
2
= 0,0343 g (rendimento real)
Antes de calcular o rendimento terico da formao do complexo, vamos saber quem
o reagente limitante a partir da quantidade de mols de cada substancia, neste casa vamos
analisar a quantidade de mols desses dois compostos CoCl
2
.6H
2
O e NH
4
Cl , a partir
desta formula:
N
mols
= __m(g)__
MM(g/mol)
N
CoCl2.6H2O
= 2,5792 g = 5,39x10
-3
mols
478 g/mol
N NH
4
Cl = __1,2628__ = 1,16 x10
-2
mols
108 g/mol
A partir desses valores conclumos que o reagente limitante desta reao o cloreto de
pentaaminoclorocobalto(III). A partir do reagente limitante podemos calcular qual a
massa do reagente que est em excesso, e calcular o rendimento terico da reao.
Massa do reagente em excesso:
478 g de CoCl
2
.6H
2
O 108 g de NH
4
Cl
2,5792 g de CoCl
2
.6H
2
O x
X = 0,582 g de NH
4
Cl
X = 0,582 g de NH
4
Cl que eu preciso para reagir com 3,000 g de CoCl
2
.6H
2
O. Ento a
massa em excesso = (massa que foi utilizada) (massa que realmente precisa)
massa em excesso = 1,2628 0,582 = 0,6808 g de NH
4
Cl em excesso.
Agora partimos a partir do reagente limitante para calcular o rendimento terico do
complexo.
478 g de CoCl
2
.6H
2
O 484,5 g de [Co(NH
3
)
5
Cl]Cl
2
2,5792 g de CoCl
2
.6H
2
O x
X= 2,614 g de [Co(NH
3
)
5
]Cl
3
(rendimento terico)
Calculo do rendimento = __rendimento real__ x 100
Rendimento terico
Calculo do rendimento = 0,0343 g x 100
2,614 g
Rendimento = 1,3%
5. Desenhe as estruturas dos complexos: pentaaminoclorocobalto(III),
tetraaminodiclorocobalto(III) e triaminotriclorocobalto(III). Inclua as
possibilidades de
isomeria.
pentaaminoclorocobalto(III),
tetraaminodiclorocobalto(III)
triaminotriclorocobalto(III).
EXPERIMENTO III:
Experimental III
1.Escrever todas as equaes das reaes:
- Obteno do [Co(NH
3
)
5
Cl]Cl
2
A obteno pode ser feita por diversos processos, partindo, por exemplo, de
CoCl
2
.6H
2
O, ou ento dos complexos de Co
3+
como [Co(NH
3
)
5
CO
3
]NO
3
.
A equao da reao a partir de CoCl
2
.6H
2
O pode ser escrita:
2 CoCl2.6H2O + 2 NH4Cl + 8 NH3 + H2O2 2 [Co(NH3)5Cl]Cl2 + 14 H2O
- Decomposio do [Co(NH
3
)
5
Cl]Cl
2
Embora os complexos de cobalto(III) sejam caracteristicamente inertes,
temperatura elevada (80C), algumas reaes de substituio podem ser razoavelmente
rpidas. As seguintes equaes mostram os passos da substituio envolvidos na
preparao:
- Sintese do Cloreto de PEntaamino(nitro)cobalto(III) e sntese do Cloreto
de Pentaamino(nitrito)cobalto(III).
2. Explore as diferenas estruturais entre Cloreto de Pentaamino(nitro)cobalto(III)
e Cloreto de Pentaamino(nitrito)cobalto(III). Que tcnica voc proporia para
identificar estes compostos.
Os compostos podem ser distinguidos pelas suas cores: o coordenado pelo
oxignio tem cor vermelha, e o coordenado pelo nitrognio tem a cor amarela. A
identificao neste caso pode ser feita, por exemplo, por espectroscopia no
infravermelho. Para o complexo com [Co(ONO)(NH
3
)
5
]Cl
2
, (coordenado pelo O) o
ligante (NO
2
)
-
d duas bandas caractersticas em 1065 e 1470 cm
-1
.
3. Calcule o rendimento para a obteno de [Co(NH
3
)
5
NO
2
]Cl
2
Para o calculo do rendimento vamos partir da reao que ocorre entre os reagentes para
a obteno do complexo.
[Co(NH
3
)
5
]Cl
2
+ NaNO
2
[Co(NH
3
)
5
)NO]Cl
2
+ NaCl
Dados:
MM das Substancias de acordo com a estequiometria da reao:
[Co(NH
3
)
5
]Cl
2
= 252 g/mol
NaNO
2
= 69 g/mol
[Co(NH
3
)
5
NO
2
]Cl
2
= 262 g/mol
NaCl = 40 g/mol
Massa utilizada:
[Co(NH
3
)
5
]Cl
2
= 1,0000 g
NaNO
2
= 1,55 g
Massa obtida:
[Co(NH
3
)
5
NO
2
]Cl
2
= 0,510 g/mol (rendimento real)
Antes de calcular o rendimento terico da formao do complexo, vamos saber quem
o reagente limitante a partir da quantidade de mols de cada substancia, neste casa vamos
analisar a quantidade de mols desses dois compostos [Co(NH
3
)
5
]Cl
2
e NaNO
2
, a partir
desta formula:
N
mols
= __m(g)__
MM(g/mol)
N
[Co(NH3)5]Cl2
= __1,000__ = 3, 96x10
-3
mols
252 g/mol
N
NaNO2
= __1,55__ = 2,24 x10
-2
mols
262 g/mol
A partir desses valores conclumos que o reagente limitante desta reao o cloreto de
pentaaminoclorocobalto(III). A partir do reagente limitante podemos calcular qual a
massa do reagente que est em excesso, e calcular o rendimento terico da reao.
Massa do reagente em excesso:
252 g de [Co(NH
3
)
5
]Cl
2
262g de NaNO
2
1, 0000 g de [Co(NH
3
)
5
]Cl
2
x
X = 0,2738 g de NaNO
2
X = 0,2738 g de NaNO
2
que eu preciso para reagir com 1,000 g de [Co(NH
3
)
5
]Cl
2
.
Ento a massa em excesso = (massa que foi utilizada) (massa que realmente precisa)
massa em excesso = 1,55 0,2738 = 1,27 g de NaNO
2
em excesso.
Agora partimos a partir do reagente limitante para calcular o rendimento terico do
complexo.
252 g de [Co(NH
3
)
5
Cl]Cl
2
262 g de [Co(NH
3
)
5
NO
2
]Cl
2
1,000 g de [Co(NH
3
)
5
Cl]Cl
2
x
X= 1,0396 g de [Co(NH
3
)
5
NO
2
]Cl
2
(rendimento terico)
Calculo do rendimento = __rendimento real__ x 100
Rendimento terico
Calculo do rendimento = 0,510 g x 100
1,0396 g
Rendimento = 49,05%
4. Calcule o rendimento para a obteno de [Co(NH
3
)
5
ONO]Cl
2
.
Para o calculo do rendimento vamos partir da reao que ocorre entre os reagentes para
a obteno do complexo.
[Co(NH
3
)
5
]Cl
2
+ NaNO
2
[Co(NH
3
)
5
)NO]Cl
2
+ NaCl
Dados:
MM das Substancias de acordo com a estequiometria da reao:
[Co(NH
3
)
5
]Cl
2
= 252 g/mol
NaNO
2
= 69 g/mol
[Co(NH
3
)
5
ONO]Cl
2
= 262 g/mol
NaCl = 40 g/mol
Massa utilizada:
[Co(NH
3
)
5
]Cl
2
= 0,5245 g
NaNO
2
= 0,7519 g
Massa obtida:
[Co(NH
3
)
5
ONO]Cl
2
= 0,277 g/mol (rendimento real)
Antes de calcular o rendimento terico da formao do complexo, vamos saber quem
o reagente limitante a partir da quantidade de mols de cada substancia, neste casa vamos
analisar a quantidade de mols desses dois compostos [Co(NH
3
)
5
]Cl
2
e NaNO
2
, a partir
desta formula:
N
mols
= __m(g)__
MM(g/mol)
N
[Co(NH3)5]Cl2
= __0,5245g__ = 2,08x10
-3
mols
252 g/mol
N
NaNO2
= __0,7519g__ = 1,08x10
-2
mols
262 g/mol
A partir desses valores conclumos que o reagente limitante desta reao o cloreto de
pentaaminoclorocobalto(III). A partir do reagente limitante podemos calcular qual a
massa do reagente que est em excesso, e calcular o rendimento terico da reao.
Massa do reagente em excesso:
252 g de [Co(NH
3
)
5
]Cl
2
262g de NaNO
2
0,5245 g de [Co(NH
3
)
5
]Cl
2
x
X = 0,1436g de NaNO
2
X = 0,1436 g de NaNO
2
que eu preciso para reagir com 0,5245 g de [Co(NH
3
)
5
]Cl
2
.
Ento a massa em excesso = (massa que foi utilizada) (massa que realmente precisa)
massa em excesso = 0,7519 0,1236 = 0,5083 g de NaNO
2
em excesso.
Agora partimos a partir do reagente limitante para calcular o rendimento terico do
complexo.
252 g de [Co(NH
3
)
5
Cl]Cl
2
262 g de [Co(NH
3
)
5
ONO]Cl
2
0,5245 g de [Co(NH
3
)
5
Cl]Cl
2
x
X= 0,5453 g de [Co(NH
3
)
5
ONO]Cl
2
(rendimento terico)
Calculo do rendimento = __rendimento real__ x 100
Rendimento terico
Calculo do rendimento = 0,227 g x 100
0,5453 g
Rendimento = 52,81%
REFERENCIAS BIBLIOGRFICA
RIVER, D. F. e ATKINS, P. W. Qumica Inorgnica. 3 ed. Bookman, Porto
Alegre, 2003.
MENDES, A. N. F. Qumica Inorgnica. 2010. Disponvel em <
http://www.ceunes.ufes.br/downloads/2/ananeryfm-Apostila_2012_2_parte_3.pdf>
Acessado em 19 de Agosto de 2013.
MAGALHES, A. Experimento VII. Disponvel em <
http://abragam.iqm.unicamp.br/wordpress/?page_id=449> Acessado em 19 de Agosto
de 2013.
OLIVEIRA, M. R de.; MAIA, J. R. S.; BRAATHEN, P. C. Prticas de Qumica
Inorgnica Viosa, MG : UFV/CEAD, 2010.
S-ar putea să vă placă și
- Potenciometria: aspectos teóricos e práticosDe la EverandPotenciometria: aspectos teóricos e práticosÎncă nu există evaluări
- A Síntese Do Cloreto de PentaminclorocobaltoDocument5 paginiA Síntese Do Cloreto de PentaminclorocobaltogalerosaÎncă nu există evaluări
- Relatório InorgânciaDocument30 paginiRelatório InorgânciaJessica Cristhina100% (1)
- Relatório - Isomeria de LigaçãoDocument15 paginiRelatório - Isomeria de LigaçãoAline ScarduaÎncă nu există evaluări
- Relatório 5 Sínteses de Complexos de CobaltoDocument8 paginiRelatório 5 Sínteses de Complexos de CobaltoHeronildes JúniorÎncă nu există evaluări
- P2 Exp 04 Trans-Co Cl2 en CLDocument6 paginiP2 Exp 04 Trans-Co Cl2 en CLherai03Încă nu există evaluări
- Experimento 1 2 3Document15 paginiExperimento 1 2 3Karollyne Santana PaixãoÎncă nu există evaluări
- Síntese Do Cloreto de Pentaaminclorocobalto (III)Document12 paginiSíntese Do Cloreto de Pentaaminclorocobalto (III)Fabio Aleixo100% (1)
- Relatório 03 - Síntese Cloreto de Hexaminoníquel (II)Document13 paginiRelatório 03 - Síntese Cloreto de Hexaminoníquel (II)Marcos Vinicius MarquesÎncă nu există evaluări
- Isomeria de Ligação em Compostos de Coordenação de Co (III)Document11 paginiIsomeria de Ligação em Compostos de Coordenação de Co (III)Gustavo Henrique OliveiraÎncă nu există evaluări
- Relatório Aula III - Preparação e Propriedades Do Carbonato de Sódie e Do Bicarbonato de SódioDocument9 paginiRelatório Aula III - Preparação e Propriedades Do Carbonato de Sódie e Do Bicarbonato de SódioNick AllenÎncă nu există evaluări
- Isomeria Geométrica em Compostos de CoordenaçãoDocument12 paginiIsomeria Geométrica em Compostos de CoordenaçãoLarissa CristinaÎncă nu există evaluări
- Prática de Química Inorgânica - Grupo 17Document6 paginiPrática de Química Inorgânica - Grupo 17claudiagomessantosÎncă nu există evaluări
- Prática - 06 - QUI137 - Síntese - e - Caracterização - de - (Cu (NH3) 4) SO4.H2ODocument3 paginiPrática - 06 - QUI137 - Síntese - e - Caracterização - de - (Cu (NH3) 4) SO4.H2OajrbaptistaÎncă nu există evaluări
- Relatorio de Sintese Do VanadioDocument10 paginiRelatorio de Sintese Do VanadioThais Luz SouzaÎncă nu există evaluări
- Relatório 02 - InorgânicaDocument7 paginiRelatório 02 - InorgânicaTereza Cristina EvangelistaÎncă nu există evaluări
- Relatório Grupo 15 - Compostos de NitrogênioDocument13 paginiRelatório Grupo 15 - Compostos de NitrogênioDimas BritoÎncă nu există evaluări
- Os Elementos Metais Alcalinos TerrososDocument23 paginiOs Elementos Metais Alcalinos Terrososmarco_santos3079Încă nu există evaluări
- Vichagas-Exercícios ComplexosDocument3 paginiVichagas-Exercícios Complexoscarlos201412Încă nu există evaluări
- Cidos e BasesDocument4 paginiCidos e BasesliviadgpÎncă nu există evaluări
- Relatorio 4 Coordenação FlaviaDocument5 paginiRelatorio 4 Coordenação FlaviaAldair OliveiraÎncă nu există evaluări
- A QUÍMICA DE COMPOSTOS DE COORDENAÇÃO Nanotecnologia - 2 - 2013Document26 paginiA QUÍMICA DE COMPOSTOS DE COORDENAÇÃO Nanotecnologia - 2 - 2013lilian6650% (2)
- SÍNTESE DO SULFATO DE TETRAMINCOBRE (II) MONO HIDRATADO (Cu (NH3) ) SO4 . H2ODocument4 paginiSÍNTESE DO SULFATO DE TETRAMINCOBRE (II) MONO HIDRATADO (Cu (NH3) ) SO4 . H2OPauloVidalÎncă nu există evaluări
- Relatório - Atividade 8 (Equilíbrio Químico - Reações No Equilíbrio Químico e Princípio de Le Chatelier) - Passei DiretoDocument10 paginiRelatório - Atividade 8 (Equilíbrio Químico - Reações No Equilíbrio Químico e Princípio de Le Chatelier) - Passei DiretoAugusto EspagollaÎncă nu există evaluări
- Relatório Do Grupo 15Document6 paginiRelatório Do Grupo 15Aline MaíraÎncă nu există evaluări
- Exp 8 - Viscosidade PVA e BrooksfieldDocument17 paginiExp 8 - Viscosidade PVA e BrooksfieldWalasJoãoÎncă nu există evaluări
- Parte 2 Campo-CristalinoDocument51 paginiParte 2 Campo-CristalinoBruno NunesÎncă nu există evaluări
- Relatório Experimento 4Document5 paginiRelatório Experimento 4Grazi LeiteÎncă nu există evaluări
- Relatório Grupos FuncionaisDocument8 paginiRelatório Grupos FuncionaisAndrezza Geovanna100% (1)
- Pratica 5. Sintese Do (CoCl (NH3) 5) Cl2Document4 paginiPratica 5. Sintese Do (CoCl (NH3) 5) Cl2LuizFelipeCantarino100% (1)
- Relatório 2 - Solubilidade de Compostos OrgânicosDocument9 paginiRelatório 2 - Solubilidade de Compostos OrgânicosLeandronmsmÎncă nu există evaluări
- Experimento 1.1 - Alex GuedesDocument10 paginiExperimento 1.1 - Alex GuedesAlex GuedesÎncă nu există evaluări
- Relatório - Sintese de Complexos de Niquel...Document6 paginiRelatório - Sintese de Complexos de Niquel...Mariana AlmeidaÎncă nu există evaluări
- Aula 7 Volumetria de Complexação 2012.2Document38 paginiAula 7 Volumetria de Complexação 2012.2Robson RaduanÎncă nu există evaluări
- RELATÓRIO 01 - AIQ - DispersõesDocument5 paginiRELATÓRIO 01 - AIQ - DispersõesMel FernandesÎncă nu există evaluări
- Teste de BayerDocument3 paginiTeste de Bayerthullinha67% (3)
- Aula 1 QO II - Sistemas Insaturados ConjugadosDocument69 paginiAula 1 QO II - Sistemas Insaturados ConjugadosPedro Morais100% (1)
- Diagrama de Solubilidade para Um Sistema Ternário de LíquidosDocument24 paginiDiagrama de Solubilidade para Um Sistema Ternário de LíquidosFernanda BonfimÎncă nu există evaluări
- Relatório 3 LabDocument7 paginiRelatório 3 LabFernanda SilvaÎncă nu există evaluări
- Complexos em Solução - Química - UTFPR - 2010Document7 paginiComplexos em Solução - Química - UTFPR - 2010joaomarcoslsÎncă nu există evaluări
- Relatorio Quimica Inorganica Experimental Familia Do CarbonoDocument7 paginiRelatorio Quimica Inorganica Experimental Familia Do CarbonoDaniel MendezÎncă nu există evaluări
- Síntese Do Cloreto de Hexaminíquel II - Química - UTFPR - 2010Document4 paginiSíntese Do Cloreto de Hexaminíquel II - Química - UTFPR - 2010joaomarcosls100% (1)
- Relatório Iodo - Química Geral (UFMG)Document6 paginiRelatório Iodo - Química Geral (UFMG)Júlia SoaresÎncă nu există evaluări
- Síntese Do Ácido BenzoicoDocument8 paginiSíntese Do Ácido BenzoicocaelÎncă nu există evaluări
- Basolo - Livro TraduzidoDocument133 paginiBasolo - Livro TraduzidoEliel MendonçaÎncă nu există evaluări
- Relatorio Química InorgânicaDocument12 paginiRelatorio Química InorgânicaJoão Pedro Martins OliveiraÎncă nu există evaluări
- Equilibrio Quimico Questoes SubbjetivasDocument17 paginiEquilibrio Quimico Questoes Subbjetivasbelzinha567Încă nu există evaluări
- 04 - Relatorio (Chama)Document2 pagini04 - Relatorio (Chama)Vanessa PeçanhaÎncă nu există evaluări
- Cloreto de HexamincobaltoIIIDocument13 paginiCloreto de HexamincobaltoIIIYuri GomesÎncă nu există evaluări
- Síntese Do Cloreto de Pentaminclorocobalto (LLL)Document26 paginiSíntese Do Cloreto de Pentaminclorocobalto (LLL)João Paulo50% (2)
- Química - Relatórios - 4 - Corrosão e Protecção Catódica - 3Document5 paginiQuímica - Relatórios - 4 - Corrosão e Protecção Catódica - 3Jhonatha JsÎncă nu există evaluări
- 8 - Preparação Do Cicloexeno (Reparado)Document4 pagini8 - Preparação Do Cicloexeno (Reparado)Vaghner Silva0% (1)
- 2 Lista de ExercíciosDocument2 pagini2 Lista de ExercíciosDarllen CampeloÎncă nu există evaluări
- Propriedades Oxidantes e Redutoras Do No3 e No2Document5 paginiPropriedades Oxidantes e Redutoras Do No3 e No2PauloVidalÎncă nu există evaluări
- Síntese e Caracterização Do Complexo K3Document7 paginiSíntese e Caracterização Do Complexo K3Laís BarbosaÎncă nu există evaluări
- Complexo de CobaltoDocument16 paginiComplexo de CobaltoCezar ManziniÎncă nu există evaluări
- Prática 3 - PREPARAÇÃO DE CLORETO DE PENTAAMINOCLOROCOBALTO (III)Document4 paginiPrática 3 - PREPARAÇÃO DE CLORETO DE PENTAAMINOCLOROCOBALTO (III)Aline ScarduaÎncă nu există evaluări
- Roteiro Prtico 2Document5 paginiRoteiro Prtico 2Mariana KattahÎncă nu există evaluări
- Síntese Dos Compostos de Cobalto Nitrato de Tetraamimcarbonatocabalto (Iii) e Cloreto de Pentaamimclorocobalto (Iii)Document14 paginiSíntese Dos Compostos de Cobalto Nitrato de Tetraamimcarbonatocabalto (Iii) e Cloreto de Pentaamimclorocobalto (Iii)Luis ManoÎncă nu există evaluări
- (CoCl (NH3) 5) Cl2 - Cloreto de Pentaaminclorocobalto (III)Document11 pagini(CoCl (NH3) 5) Cl2 - Cloreto de Pentaaminclorocobalto (III)lucas roniery0% (1)
- Relatorio AASDocument10 paginiRelatorio AASJakeline de Souza Bastos100% (1)
- Universidade Federal Do TocantinsDocument2 paginiUniversidade Federal Do TocantinsJakeline de Souza BastosÎncă nu există evaluări
- Preparção e Propriedades Dos SabõesDocument13 paginiPreparção e Propriedades Dos SabõesJakeline de Souza BastosÎncă nu există evaluări
- Fundamentos de Química Experimental PDFDocument233 paginiFundamentos de Química Experimental PDFElizael De Jesus GonçalvesÎncă nu există evaluări
- Relatorio CafeinaDocument6 paginiRelatorio CafeinaJakeline de Souza BastosÎncă nu există evaluări
- Relatorio AASDocument10 paginiRelatorio AASJakeline de Souza Bastos100% (1)
- 21 Aula Af 2019 Obsessao AutoobsessaoDocument11 pagini21 Aula Af 2019 Obsessao AutoobsessaoMarcos MarosticaÎncă nu există evaluări
- Atividade de Física - 3° AnoDocument3 paginiAtividade de Física - 3° Anokaique reinaldoÎncă nu există evaluări
- 10 Melhores Casa de Repouso para Idosos em Poços de Caldas Preços - CronoshareDocument1 pagină10 Melhores Casa de Repouso para Idosos em Poços de Caldas Preços - CronoshareJuciene DiasÎncă nu există evaluări
- Dinâmicas de GrupoDocument3 paginiDinâmicas de GrupoTPSaraHÎncă nu există evaluări
- (Aula 02) Citologia No EnemDocument5 pagini(Aula 02) Citologia No EnemPedro SoaresÎncă nu există evaluări
- 9º ANO EF - Ficha de Estudo - AV1 - 3º TRIM - QuímicaDocument7 pagini9º ANO EF - Ficha de Estudo - AV1 - 3º TRIM - QuímicaCarolina TavaresÎncă nu există evaluări
- Curso de Digitação - ApostilaDocument69 paginiCurso de Digitação - ApostilaNélio MeloÎncă nu există evaluări
- Atividades Sobre SubstantivoDocument2 paginiAtividades Sobre SubstantivoChrisRebelo100% (1)
- 2º Ano-Filosofia V.02-EM-EJA-Semana 17Document2 pagini2º Ano-Filosofia V.02-EM-EJA-Semana 17Bruna DPC AbellanedaÎncă nu există evaluări
- Planilha para Cálculo de AgitadoresDocument29 paginiPlanilha para Cálculo de AgitadoresElton Neves da Silva100% (1)
- Abraco RP Pac 002 Rev. 0 Maio 2018 2Document18 paginiAbraco RP Pac 002 Rev. 0 Maio 2018 2PaulaÎncă nu există evaluări
- Bons Sebenta-DIP TeóricaDocument78 paginiBons Sebenta-DIP TeóricaFilipe Rodrigues BandeiraÎncă nu există evaluări
- Linguística - o Que ÉDocument9 paginiLinguística - o Que ÉSILVIO REINOD COSTAÎncă nu există evaluări
- Aula LadderDocument29 paginiAula Ladderwelltonarruda100% (3)
- Rádio Comunitária - ApostilaDocument27 paginiRádio Comunitária - ApostilaLondulade BezerraÎncă nu există evaluări
- LIVRO Comecando A Vida Crista 02Document23 paginiLIVRO Comecando A Vida Crista 02Fabio Costa100% (1)
- Apostila 4 - A Missão de AlmaDocument9 paginiApostila 4 - A Missão de AlmaRodrigo LeiteÎncă nu există evaluări
- Escolha MúltiplaDocument6 paginiEscolha MúltiplaIrina Filipa100% (2)
- Vitaminas HidrossolúveisDocument4 paginiVitaminas HidrossolúveisJoao Vitor Cavalari CoimbraÎncă nu există evaluări
- O Mundo Do Trabalho e o Projeto de Vida: Química AplicadaDocument19 paginiO Mundo Do Trabalho e o Projeto de Vida: Química AplicadaLaura TorresÎncă nu există evaluări
- Folder MeditacaoDocument2 paginiFolder MeditacaoRafael AméricoÎncă nu există evaluări
- Material Complementar Ashtanga Yoga AvancadoDocument12 paginiMaterial Complementar Ashtanga Yoga AvancadoHeitor Medeiros Vieira100% (2)
- Anatomia e Fisiologia Humana FacialDocument20 paginiAnatomia e Fisiologia Humana FacialJakeline Alexandre da Silva100% (1)
- Alienista RoteiroDocument16 paginiAlienista RoteiroJetterson CondeÎncă nu există evaluări
- Prefácio Da Introdução A Critica Da Economia Política, MarxDocument3 paginiPrefácio Da Introdução A Critica Da Economia Política, MarxRoberta SampertÎncă nu există evaluări
- História Da Moeda AngolanaDocument10 paginiHistória Da Moeda AngolanaDomingos Loveres Massissa86% (7)
- CATALOGODocument28 paginiCATALOGOGABRIELÎncă nu există evaluări
- Folha de Respostas Pep-R - Com VocêDocument14 paginiFolha de Respostas Pep-R - Com VocêEstágio EspecíficoÎncă nu există evaluări
- Maçonaria e Clube de ServiçosDocument25 paginiMaçonaria e Clube de ServiçosWagner Cruz da CruzÎncă nu există evaluări
- Check List - Serra de BancadaDocument1 paginăCheck List - Serra de BancadaKarina MeloÎncă nu există evaluări