Documente Academic
Documente Profesional
Documente Cultură
Tema 25
Încărcat de
Eddie Mondragon Gomez0 evaluări0% au considerat acest document util (0 voturi)
44 vizualizări20 paginiEl documento describe las funciones del citoesqueleto en las células eucariotas. El citoesqueleto está formado por tres tipos de filamentos (finos de actina, intermedios y microtúbulos) que cumplen funciones como mantener la forma celular, controlar la posición de los orgánulos, y permitir diferentes tipos de movimiento celular como la locomoción y la migración celular durante el desarrollo embrionario.
Descriere originală:
Titlu original
Tema25
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentEl documento describe las funciones del citoesqueleto en las células eucariotas. El citoesqueleto está formado por tres tipos de filamentos (finos de actina, intermedios y microtúbulos) que cumplen funciones como mantener la forma celular, controlar la posición de los orgánulos, y permitir diferentes tipos de movimiento celular como la locomoción y la migración celular durante el desarrollo embrionario.
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
44 vizualizări20 paginiTema 25
Încărcat de
Eddie Mondragon GomezEl documento describe las funciones del citoesqueleto en las células eucariotas. El citoesqueleto está formado por tres tipos de filamentos (finos de actina, intermedios y microtúbulos) que cumplen funciones como mantener la forma celular, controlar la posición de los orgánulos, y permitir diferentes tipos de movimiento celular como la locomoción y la migración celular durante el desarrollo embrionario.
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 20
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 1 -
TEMA 27
El Citoesqueleto III:
Funciones del citoesqueleto
27.1.- Introduccin al estudio del citoesqueleto.
El citoesqueleto se encuentra solo en clulas eucariotas. Las clulas eucariotas
son clulas complejas que tienen que organizar sus orgnulos, mover vesculas de un
lado a otro del citoplasma, moverse ellas mismas Estas funciones se realizan gracias
al citoesqueleto. El citoesqueleto es como un armazn intramolecular, responsable de:
- Mantenimiento de la forma celular.
- Movimiento de la clula.
- Mantenimiento de la posicin y movimiento, de las estructuras celulares.
Estas diferentes funciones se llevan a cabo mediante 3 tipos de filamentos
proteicos, como son:
- Finos: estn formados bsicamente de actina y son responsables sobre todo del
mantenimiento de la forma y superficie celular, as como de la contraccin
celular y de la locomocin celular (como ocurre en las amebas).
- Microtbulos: son los ms gruesos y se encargan de la organizacin y del
movimiento de las estructuras intracelulares.
- Intermedios: son muy resistentes y se encargan del mantenimiento de la forma
celular y tienen tambin una funcin mecnica que acta tambin como
respuesta al estrs celular.
Cada tipo de filamento se especializa en distintas funciones pero presentan una
serie de caractersticas comunes:
- Son proteicos.
- Se asocian a protenas. Sus funciones dependen no solo de su estructura sino
tambin de las protenas con las que se asocian, las llamadas protenas
asociadas.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 2 -
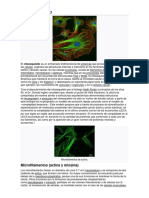
Esta clula pigmentada se encarga de distribuir por la clula los melanosomas, que son acmulos de
melanina, que posteriormente pasar a los queratinocitos. Si aumenta la concentracin de AMPc los
melanosomas se dispersarn gracias al transporte por los microtbulos por todo el citoplasma, hacia la
periferia, mientras que si disminuye la concentracin de AMPc, se acumularn los melanosomas,
prximos al MTOC ya que stos se transportan mediante microtbulos y si desciende la concentracin
de AMPc, se producen fenmenos de polimerizacin. Si aplicamos el funcionamiento de la clula
pigmentada, al experimento de la imagen, nos daremos cuenta que, si cortamos una clula pigmentada,
no solo se redistribuirn los microtbulos alrededor de un nuevo centro organizador de microtbulos
sin centrolos, sino que adems, encontramos de nuevo, siempre y cuando haya una elevada
concentracin de AMPc, a los melanosomas en la periferia.
Todos estos elementos actan coordinadamente en las clulas. Los componentes
del citoesqueleto son estructuras muy dinmicas, es decir, estn en renovacin
constante. Sabemos que son estructuras muy dinmicas, ya que intervienen en el
transporte de estructuras celulares y de las propias clulas, pero en el caso de los
filamentos intermedios no se produce una polimerizacin y despolimerizacin como en
los microtbulos y microfilamentos.
Debido al gran nmero de protenas accesorias de los filamentos del
citoesqueleto que se van descubriendo, el estudio del mismo entraa cierta dificultad.
27.2.- Funciones del citoesqueleto.
Control de la posicin de las estructuras intracelulares:
Los orgnulos no estn libres en el citoplasma, sino que estn unidos a
los filamentos del citoesqueleto, principalmente a los microtbulos y protenas
asociadas, aunque aparecen otros filamentos.
En las clulas animales la configuracin astral de los microtbulos es
muy robusta, con extremos ms muy dinmicos que apuntan hacia la periferia
celular y extremos menos muy estables cerca del ncleo. El sistema de
microtbulos que irradia a partir del centrosoma (tambin llamado MTOC,
Centro Organizador de Microtbulos) acta como un dispositivo que
proporciona supervivencia a las regiones ms alejadas de la clula y que coloca
el centrosoma en su centro. Incluso en un fragmento celular aislado que haya
perdido el centrosoma, los microtbulos dinmicos interactan con los orgnulos
membranosos a travs de las protenas motoras, y dichos filamentos se organizan
adoptando una disposicin astral con los extremos menos dirigidos hacia el
centro. Esta capacidad de los microtbulos del citoesqueleto para encontrar el
centro de la clula establece un sistema general coordinado, que permite
posicionar muchos orgnulos dentro de ella.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 3 -
Control de la forma celular:
En el control de la forma celular van a intervenir los tres tipos de
filamentos del citoesqueleto, pero los filamentos intermedios van a provocar
cierta estabilidad y resistencia mecnica. Estos filamentos son muy importantes,
como vemos en enfermedades como la Epidermlisis Bullosa.
En la mayora de clulas hay una densidad mayor de filamentos de actina
en la periferia celular. Estos filamentos de actina de la capa situada bajo la
membrana plasmtica determinan el denominado crtex celular. Son los
responsables de la forma y el movimiento de la superficie de la clula. As,
dependiendo de su unin entre s y a la membrana plasmtica, las estructuras de
actina pueden formar proyecciones de la superficie de la clula
extraordinariamente variadas. stas incluyen haces puntiagudos como las
microvellosidades o filopodios, velos emergentes y alargados llamados
lamelipodios que ayudan a las clulas a desplazarse sobre sustratos slidos, y las
evaginaciones fagocticas de los macrfagos.
Si las clasificamos segn su dinamismo, podemos decir que unas son
rgidas, como las microvellosidades, y que otras son dinmicas, como los
pseudpodos, filopodios, lamelipodios, fibras de estrs (que a veces tienen
capacidad contrctil), etc.
Control transmembrana de la organizacin intracelular:
Ciertas seales extracelulares pueden unirse a receptores de la membrana
plasmtica y generar en ese punto una seal, que como consecuencia de ella se
produzcan cambios en la organizacin intracelular (variacin de la posicin de
los orgnulos, etc.).
Un ejemplo es la actuacin de clulas inmunitarias como son los
linfocitos T. stos, tienen en su estructura receptores antignicos, es decir,
receptores que mediante identificacin celular, marcar o establecen que
elementos son propios del organismo, y cuales no, y por tanto, cuando
identifique un cuerpo ajeno al cuerpo tratar de eliminarlo. El reconocimiento
inicial comporta la aparicin de seales que causan la polimerizacin de actina
en ambas clulas, en el lugar del contacto. En el linfocito T, las interacciones
entre las zonas de contacto ricas en actina y los microtbulos procedentes del
centrosoma provocan la reorientacin del centrosoma, de forma que el complejo
de Golgi asociado se coloca adyacente a la clula diana. Al modificarse la
posicin del aparato de Golgi, este est ms prximo a la membrana por lo que
podr verter los lisosomas al exterior para poder degradar el elemento extrao.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 4 -
Movimientos celulares:
En el desarrollo de esta funcin vital van a intervenir los tres tipos de
filamentos del citoesqueleto, en mayor o menor medida. Los tipos de
movimientos que la clula desarrolla podemos dividirlos en:
o Movimientos ciliares: este tipo de movimientos estn llevados a cabo por
los microtbulos, ya que son este tipo de filamentos los que componen
las estructuras de los cilios y de los flagelos, que estructuralmente son
iguales, solo que vara la longitud final y el nmero de veces que se
repite la estructura. A su vez, los movimientos ciliares pueden ser:
De cilios propiamente dichos, que son realizados por estructuras
digitiformes, cortas y numerosas y que fundamentalmente se
encargan de mover el lquido extracelular, no la clula en
cuestin. Ej.: epitelio del aparato respiratorio.
De flagelos, que son estructuras menos numerosas, ms largas y
que realizan movimientos de tipo ltigo, con la funcin de mover
la clula en la que se encuentran. Ej.: espermatozoide.
o Movimientos de clulas en cultivo: no solo lo realizan clulas en cultivo
como veremos, pero en ellas se estudia muy bien. Muchas clulas, en
lugar de utilizar cilios y flagelos para nadar, se desplazan arrastrndose
sobre superficies. Las amebas predadoras se arrastran continuamente para
buscar alimento y fcilmente puede observarse en una gota de agua cmo
atacan y devoran a flagelados y ciliados ms pequeos. En el caso de los
animales, la mayor parte de los sistemas de locomocin tambin se
producen arrastrndose, con la excepcin de los espermatozoides.
Durante la embriognesis, la estructura de un animal se genera a
partir de las migraciones de clulas individuales hacia localizaciones diana
especficas y por el movimiento coordinado de capas epiteliales. En los
vertebrados las clulas de la cresta neural recorren largas distancias desde su
lugar de origen en el tubo neural hacia una gran variedad de destinos del
embrin. Estas clulas tienen destinos diversos, convirtindose en clulas
pigmentarias de la piel, neuronas sensoriales o simpticas y clulas gliales
u otros tipos celulares. Este largo recorrido es fundamental para la
construccin del sistema nervioso completo: tambin es de esta forma
como los conos de crecimiento en los frentes de avance, ricos en actina, de
los axones en desarrollo viajan hacia sus futuras dianas sinpticas,
guiados, a lo largo de su recorrido, por una combinacin de seales
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 5 -
La extensin dependiente de la
polimerizacin de actina y la firme
adhesin de un lamelipodio en el
frente de avance de la clula
desplaza el extremo hacia adelante
(flechas verdes delante) y contrae
el crtex de actina. La contraccin
en la parte posterior de la clula
empuja el resto del cuerpo hacia
adelante (flecha verde detrs)
relajando parte de la tensin
generada (traccin). Delante se
forman nuevos contactos focales y los
antiguos se desensamblan en la parte
posterior mientras la clula se
arrastra hacia adelante. Este mismo
ciclo se puede repetir, con lo que la
clula se desplaza hacia adelante.
Alternativamente, todos los pasos
pueden estar ntimamente
coordinados, desplazando
suavemente la clula hacia adelante.
En rojo se muestra la actina
cortical) polimerizada de nuevo.
solubles y de seales asociadas con la superficie celular y con la matriz
extracelular. El animal adulto tambin dispone de clulas que se arrastran.
Los macrfagos y los neutrfilos se dirigen hacia los lugares de infeccin
y engullen los organismos invasores extraos como funcin crtica de la
respuesta inmune. Los osteoclastos (clulas gigantes, con varios ncleos)
del hueso forman canales rellenos de osteoblastos (clulas productoras de
sustancia sea), que los siguen en un proceso continuado de remodelacin
y renovacin del hueso. De forma parecida, los fibroblastos pueden migrar
a travs del tejido conjuntivo, remodelndolo donde sea necesario y
ayudando a la reconstruccin de las estructuras daadas en las heridas. En
un proceso ordenado, las clulas del epitelio que tapiza el intestino viajan
hacia las capas superiores reemplazando las clulas absorbentes que se han
eliminado en los extremos de las vellosidades. Este desplazamiento de
rastreo tambin es muy importante en muchos cnceres, cuando las clulas
de un tumor primario invaden el tejido circundante, se arrastran hacia
los vasos sanguneos y linfticos y son transportadas hacia otros
lugares del organismo donde producen metstasis. Este movimiento es un
proceso complejo altamente integrado, dependiente del crtex de actina
situado bajo la membrana plasmtica. En l estn implicadas tres
actividades distintas: protrusin, mediante la cual las estructuras ricas en
actina son empujadas hacia el frente celular; adhesin, mediante la cual
el citoesqueleto de actina conecta la membrana plasmtica con el sustrato
o con clulas vecinas a travs de protenas transmembrana; y traccin,
mediante la cual la mayor parte del citoplasma es dirigido hacia adelante.
En algunas clulas, como los queratinocitos de la epidermis de los peces,
estas actividades estn muy coordinadas y parece que las clulas se deslicen
casi sin cambiar de forma. En otras clulas como los fibroblastos, estas
actividades son ms independientes y la locomocin es ms irregular.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 6 -
o Movimientos por quimiotaxis: en general, un tactismo es un movimiento
de la clula en respuesta a un excitante anterior. El tactismo es positivo
cuando el movimiento se realiza en direccin al excitante, y negativo en
el caso contrario. Algunos de los tipos de tactismos son, la quimiotaxis,
que es una respuesta a seales qumicas, y la fototaxis una respuesta a la
luz. Por tanto, cuando nos refiramos a quimiotaxis estaremos hablando
de movimientos que realiza la clula, atrada por alguna sustancia
qumica. Ejemplos:
Neuronas, que van estableciendo sinapsis guiadas por diferentes
sustancias.
Clulas sanguneas, como los leucocitos, que se dirigen hacia las
bacterias ya que se ven atrados por algunas de sus protenas. En
el caso concreto de que se produzca el paso de elementos formes
de la sangre (como los leucocitos) a travs de fenestraciones en
los capilares para dirigirse al foco de infeccin sin que se
produzca lesin estructural estamos hablando de diapdesis,
trmino que se refiere al hecho de cruzar el endotelio, no a la
causa, que sera quimiottica (atrado por la inflamacin).
27.3.- Protenas motor.
Las protenas motor son un tipo de protenas que se unen a algn tipo de
filamento polarizado, como son los microfilamentos o los microtbulos y que utilizan la
energa de la hidrlisis de ATP para desplazarse por estos elementos filamentosos, en
ambos sentidos. En las clulas eucariotas encontramos docenas de estas protenas.
Las diferentes protenas motor se diferencian en tres aspectos fundamentales,
como son:
- El tipo de filamento al que se unen (microtbulos)
- La direccin en la que se desplazan a lo largo del filamento.
- El cargamento que llevan consigo (mitocondrias, retculo endoplsmico,
Aparato de Golgi).
Las protenas motoras del citoesqueleto se asocian a sus vas de filamentos
mediante regiones apicales o "cabezas", tambin llamadas dominios motores, que
presentan una estructura globular, capaces de unir ATP e hidrolizarlo. De forma
coordinada con su ciclo de hidrlisis del nucletido y cambio conformacional, la
protena oscila entre estados en los cuales est fuertemente unida al filamento y estados
en los que no est unida. A travs de un ciclo mecnico-qumico de unin al filamento,
cambio conformacional, liberacin del filamento, relajacin conformacional y unin de
nuevo al filamento, la protena motora y su carga asociada se desplazan, paso a paso, a
lo largo del filamento (tpicamente una distancia de unos cuantos nanmetros). La
identificacin de la va (del tipo de filamento) y la direccin del desplazamiento estn
determinadas por el dominio motor, mientras que la identificacin de la carga (y por
tanto, la funcin biolgica de cada protena motora) vienen determinadas por la cola de
la protena motora. La clula puede regular la funcin de las protenas motoras,
permitiendo o cual permite:
- Cambiar la localizacin de los orgnulos y molculas en general, estn o no
rodeados de membrana, ya que en ocasiones, encontramos ARN unido a los
microtbulos.
- Regular todos los movimientos celulares.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 7 -
Protena motor de los microtbulos:
En las clulas en interfase, una funcin importante de los motores del
citoesqueleto es el transporte y posicionamiento de los orgnulos rodeados de
membrana. Inicialmente se identific la quinesina como la protena
responsable del transporte rpido a lo largo de los axones, del desplazamiento
rpido de las mitocondrias, de las vesculas secretoras precursoras y de varios
componentes de las sinapsis a lo largo de las autopistas microtubulares de los
axones hacia las distantes terminales nerviosas. Aunque en general los
orgnulos no han de recorrer distancias tan grandes, es necesario su transporte
polarizado. Un conjunto tpico de microtbulos de una clula en interfase est
orientado con sus extremos menos cerca del centro de la clula, en el
centrmero, y los extremos ms extendidos hacia la periferia. As pues, los
movimientos centrpetos de los orgnulos hacia el centro celular requieren la
accin de las protenas motoras que se dirigen hacia los extremos menos, como
la dinena citoplasmtica, y los movimientos centrfugos, hacia la periferia
celular, requieren motores dirigidos hacia los extremos ms, como las
quinesinas.
Un buen ejemplo del papel de los microtbulos y las protenas
motoras de los microtbulos sobre el comportamiento de las membranas
intracelulares lo constituye la funcin organizadora que tienen en el retculo
endoplasmtico (ER) y en el complejo de Golgi. La red de tbulos
membranosos del ER se alinea con los microtbulos y se extiende casi hasta los
extremos celulares. El complejo de Golgi, por el contrario, est localizado cerca
del centrosoma. Cuando se tratan las clulas con una droga que despolimeriza
los microtbulos, como la colchicina o el nocodazol, el ER se colapsa en el
centro de la clula, mientras que el complejo de Golgi se fragmenta y queda
disperso por el citoplasma. In vitro, las quinesinas pueden aferrar las
membranas derivadas del ER a pistas de microtbulos preformadas y hacerlas
avanzar hacia sus extremos ms, formando protrusiones tubulares y espacios
membranosos muy parecidos a los del ER de las clulas. Asimismo, el
desplazamiento de los tbulos del ER hacia la periferia celular est asociado con
el crecimiento de los microtbulos en las clulas vivas. En cambio, las dinenas
son necesarias para el posicionamiento del complejo de Golgi en el centro de
la clula, desplazando las vesculas a lo largo de los microtbulos hasta el
centrosoma.
o Quinesinas:
La quinesina es una protena motora que se desplaza a lo largo de los
microtbulos. Fue identificada en el axn gigante del calamar, donde
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 8 -
transporta orgnulos rodeados de membrana desde el cuerpo neuronal
hacia el axn terminal, caminando hacia los extremos ms de los
microtbulos. La quinesina es estructuralmente parecida a la miosina II,
ya que cada motor activo tiene dos cadenas pesadas y dos cadenas
ligeras, dos cabezas globulares que actan como dominios motores y un
fragmento helicoidal alargado responsable de la dimerizacin de la
cadena pesada. Como la miosina, la quinesina es miembro de una gran
superfamilia de protenas cuyo nico elemento comn es el dominio
motor. Los humanos tenemos cerca de 40.
En la superfamilia de las quinesinas hay al menos diez familias de
protenas relacionadas con la quinesina o KRE. La mayora tienen el
dominio motor en el extremo N-terminal de la cadena pesada y se dirigen
hacia el extremo ms de los microtbulos.
La mayora de quinesinas tienen un lugar de unin en la cola que
transporta orgnulos rodeados de membrana u otros microtbulos.
Muchos de los miembros de la superfamilia de las quinesinas juegan
papeles especficos en la formacin de los husos mittico y meitico y en
la separacin de los cromosomas en la divisin celular.
o Dinenas:
Las dinenas son una familia de protenas motoras que se dirigen hacia
los extremos menos de los microtbulos, pero que no estn relacionadas
con las quinesinas. Estn formadas por dos o tres cadenas pesadas (que
incluyen un dominio motor) y un nmero grande y variable de cadenas
ligeras asociadas. Tienen dos ramas principales. La ms ancestral
contiene las dinenas citoplasmticas, homodmeros de cadenas pesadas
con dos dominios motores muy grandes como cabeza. Se encuentran en
casi todas las clulas eucariotas y son importantes para el trfico de
vesculas y para la localizacin del complejo de Golgi cerca del centro de
la clula. La otra gran rama son las dinenas axonemales, heterodmeros
o heterotrmeros, con dos o tres dominios motores o cabezas
respectivamente. Estn muy especializadas en el movimiento deslizante
eficiente y rpido de los microtbulos en los cilios y flagelos. Una
tercera rama minoritaria comparte semejanzas de secuencia con las
dinenas citoplasmticas, aunque parece que participa en el movimiento
de cilios y flagelos.
Las dinenas son los motores moleculares conocidos de mayor tamao y
tambin unos de los ms rpidos: in vitro las dinenas axonemales
pueden desplazar los microtbulos a la velocidad de 14 m/seg. Las
quinesinas ms rpidas pueden hacerlo a unos 2-3 m/seg.
LAS PROTENAS MOTORAS PRESENTAN DIFERENTES FORMAS DE UNIN
Los distintos tipos de colas y sus cadenas ligeras asociadas sobre protenas
motoras especficas permiten a estas protenas motoras unirse de forma especfica a los
orgnulos que transportarn. Por ejemplo, existen pruebas para el caso de receptores
motores asociados a membrana, dirigidos especficamente hacia compartimientos
rodeados de membrana, que interactan directa o indirectamente con las colas de
determinados miembros de la familia de las quinesinas.
En el caso de la dinena se sabe que su unin a las membranas est mediada por
un gran ensamblaje macromolecular. La dinena citoplasmtica ya es, por s misma, un
gran complejo proteico y para transportar orgnulos de forma eficiente ha de asociarse a
otro gran complejo, llamado dinactina. Este complejo incluye un corto filamento
parecido a la actina formado por una protena relacionada con la actina, la protena Arp1
(distinta de Arp2 y Arp3, los componentes del complejo ARP implicado en la nucleacin de
los filamentos de actina convencionales). Las membranas del complejo de Golgi estn
recubiertas con las protenas anquirina y espectrina. Se propone que estas protenas se
asocien con el filamento de Arp1 en el complejo de dinactina formando un citoesqueleto
plano parecido al de la membrana de los eritrocitos. Probablemente el conjunto de
espectrina proporciona estabilidad estructural a la membrana del complejo de Golgi y -
a travs del filamento Arp1- puede mediar la unin regulable de la dinena al orgnulo.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 9 -
Protena motor de la actina: Miosina II:
Las protenas motoras juegan tambin un papel significativo en el
transporte de orgnulos a lo largo de los filamentos de actina. La primera
miosina detectada como mediador del desplazamiento de los orgnulos fue la
miosina V, una miosina de doble cabeza que genera un gran desplazamiento en
cada etapa. En los ratones, el transporte de los melanosomas est asociado a
los microfilamentos, mientras que en peces, este tipo de transporte lo llevan a
cabo los microtbulos. Otras miosinas, incluyendo la miosina 1, estn
asociadas a endosomas y a una gran variedad de otros orgnulos.
Una de las actividades que caracteriza a los animales es la capacidad de
movimiento, que se debe a la contraccin muscular, fenmeno que se produce
gracias al deslizamiento de la miosina II a travs de los filamentos de actina.
UNIN: Al iniciarse el ciclo que se muestra en la
figura, una cabeza de miosina, sin ningn nucletido
unido, se une fuertemente a un filamento de actina en una
configuracin de rigor (as llamada porque es la
responsable del rigor mortis, la rigidez de la muerte). En
un msculo en contraccin activa, este estado es de corta
duracin y finaliza rpidamente mediante la unin de
una molcula de ATP.
LIBERACIN: Una molcula de ATP se une en el surco
de la "parte trasera" de la cabeza (es decir, en la parte
ms alejada del filamento de actina) e inmediatamente
provoca un cambio ligero en la conformacin de los
dominios que conforman el lugar de unin a la actina.
Esto reduce la afinidad de la cabeza por la actina y le
permite desplazarse a lo largo del filamento. (El espacio
dibujado aqu entre la cabeza y la actina destaca este
cambio, aunque en realidad probablemente se mantiene
muy cerca de la actina).
MOVIMIENTO: El surco se cierra como la concha de
una almeja sobre la molcula de ATP, induciendo un gran
cambio morfolgico que provoca el desplazamiento de la
cabeza a lo largo del filamento, a una distancia de unos
5 nm. Se produce la hidrlisis del ATP, pero el ADP y el
fosfato inorgnico (Pi) producidos se mantienen
ntimamente unidos a la protena.
GENERACIN DE LA FUERZA: La dbil unin de la
cabeza de la miosina a un nuevo lugar en el filamento
de actina provoca la liberacin del fosfato inorgnico
producido por la hidrlisis del ATP, con lo cual se refuerza
la unin de la cabeza con la actina. Esta liberacin
proporciona el gran golpe de potencia -el cambio de forma
que genera la fuerza, mediante el cual la cabeza recupera
su conformacin original-. Durante este golpe de potencia,
la cabeza pierde el ADP que tena unido y se inicia un
nuevo ciclo.
UNIN: Al final del ciclo, la cabeza de la miosina se
encuentra de nuevo ntimamente unida al filamento de
actina en la configuracin de rigor. Ntese que la cabeza
se ha desplazado hacia una nueva posicin en el
filamento de actina.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 10 -
27.4.- Regulacin de la actividad de los filamentos.
La clula es capaz de regular la longitud y estabilidad de sus filamentos
citoesquelticos, as como su cantidad y disposicin geomtrica; los cambios son
programados. Esto se consigue regulando los contactos que establecen unos con otros y
con distintas estructuras celulares dando lugar a estructuras variadas, complejas y
cambiantes. Los principales mediadores de estos procesos de regulacin son las
protenas accesorias, que van a unirse a:
- Subunidades libres.
- Filamentos polimerizados.
Las protenas accesorias van a intervienen en una serie de procesos que pasamos
a describir:
Nucleacin de los filamentos:
El fenmeno de la nucleacin tiene una gran importancia como principio
organizador general de las clulas.
o Microtbulos: mientras que las tubulinas y son los bloques de
construccin de los microtbulos, otra tubulina, llamada tubulina , juega
un papel mucho ms especializado. Esta protena, presente en mucha
menor cantidad que las otras dos, est implicada en la nucleacin del
crecimiento de los microtbulos en organismos muy diferentes.
Generalmente los microtbulos se nuclean a partir de una localizacin
intracelular llamada Centro Organizador de Microtbulos (MTOC). Los
microtbulos se nuclean por su
extremo menos, de forma que su
extremo ms va creciendo a partir de
cada MTOC generando diferentes
tipos de disposiciones de
microtbulos. Parece ser que la
tubulina , junto con otras protenas
forman un anillo que acta de base
para nuclear un microtbulo de 13
protofilamentos.
o Filamentos de actina: los filamentos de actina se nuclean frecuentemente
cerca de la membrana plasmtica. Por lo tanto, en la mayora de clulas
hay una densidad ms elevada de estos filamentos en la periferia celular.
Estos filamentos de actina de la capa situada bajo la membrana
plasmtica determinan el denominado crtex celular. Son los
responsables de la forma y el movimiento de la superficie de la clula.
As, dependiendo de su unin entre s y a la membrana plasmtica, las
estructuras de actina pueden formar proyecciones de la superficie de la
clula extraordinariamente variadas. La nucleacin de los filamentos de
actina en la membrana plasmtica a menudo est regulada por seales
externas, lo cual permite a las clulas cambiar rpidamente su forma y
rigidez respondiendo a los cambios de su entorno. Esta nucleacin est
catalizada por un complejo de protenas que incluye dos protenas
relacionadas con la actina, o ARP (de actin-related proteins), cada una
de las cuales presenta una homologa del 45% con la actina. El complejo
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 11 -
ARP nuclea el crecimiento de los filamentos de actina a partir del
extremo menos, permitiendo as un alargamiento rpido de los filamentos
por el extremo ms. Sin embargo, el complejo tambin puede unirse
lateralmente a otro filamento de actina y permanecer unido al extremo
menos del filamento que ha nucleado, de forma que se generan
filamentos en forma de rbol. El complejo ARP se localiza en regiones
de rpido crecimiento de los filamentos de actina como los lamelipodios,
y su actividad nucleadora est regulada por molculas sealizadoras
intracelulares y componentes de la cara citoslica de la membrana
plasmtica.
Elongacin de los filamentos:
El alargamiento de los filamentos est modificado por protenas que se
unen a las subunidades libres.
Cuando los filamentos han sido nucleados, generalmente se alargan por
adicin de subunidades solubles. En la mayora de clulas no musculares de los
vertebrados, en torno al 50% de la actina est formando filamentos, mientras que
el 50% restante se encuentra en forma soluble. Pero por qu no polimeriza la
actina soluble formando filamentos? La razn es que este conjunto tan
abundante de subunidades contiene protenas especiales que se unen a los
monmeros de actina e impiden su polimerizacin o la hacen menos favorable.
De estas protenas, la ms abundante es la timosina. Los monmeros de actina
unidos a ella se encuentran en un estado cerrado, en el cual no pueden asociarse
ni al extremo ms ni al extremo menos de los filamentos de actina ni hidrolizar o
cambiar el nucletido que llevan unido. Entonces cmo consiguen las clulas
recolectar estos monmeros de actina de este conjunto secuestrado y usarlos para
polimerizar? Cabra imaginar que la timosina podra estar regulada por vas de
transduccin de seal, aunque no se ha demostrado. Por el contrario, el
reclutamiento depende de otra protena de unin al monmero, la profilina. La
profilina se une al monmero de actina en la cara opuesta al lugar de unin al
ATP, de forma que bloquea el lugar al que se asociara el monmero con el
extremo menos del filamento. Sin embargo, el complejo profilina-actina puede
Modelo de nucleacin de los filamentos de actina por el
complejo ARP Arp2 y Arp3 pueden estar unidas mediante
protenas accesorias manteniendo una orientacin que se
parece a la de los extremos ms de los filamentos de actina.
Entonces, las subunidades de actina pueden ensamblarse en
esta estructura, superando la etapa limitante de la nucleacin
del filamento.
El complejo ARP nuclea filamentos de forma ms eficiente
cuando est unido lateralmente a un filamento preexistente.
El resultado es una rama de filamento que crece en un
ngulo de 70 con respecto al filamento original.
Ramificaciones repetidas permiten la formacin de una red de
actina en forma de rbol.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 12 -
unirse fcilmente al extremo ms libre. Al hacerlo, se induce un cambio
conformacional de la actina, la cual disminuye su afinidad por la profilina, por lo
que sta se disocia, dejando al filamento con una subunidad ms. La profilina
compite con la timosina por la unin a los monmeros de actina, de forma que
una activacin local de molculas de profilina desplaza las subunidades de actina
secuestradas por la timosina a los extremos ms de los filamentos. Existen
diferentes tipos de mecanismos intracelulares que regulan la actividad de la
profilina, como son la fosforilacin de la propia profilina, la unin de la profilina
a lpidos del tipo inositol fosfato, o la unin a otras protenas intracelulares que
presentan dominios ricos en prolina; segn a que componentes se una, se
producir la polimerizacin en un determinado lugar de la clula. En cualquier
caso, si la cantidad de timosina y de profilina est en equilibrio, no se produce
elongacin de los filamentos de actina; pero para regular su longitud basta que la
clula aumente la expresin de los genes de estas protenas.
Como ocurre con los monmeros de actina, dentro de la clula la tubulina
no polimerizada se halla secuestrada, lo cual permite mantener el conjunto de
subunidades libres en unos niveles sensiblemente ms altos que la concentracin
crtica. Una molcula de la pequea protena estatmina se une a dos
heterodmeros de tubulina e impide su unin a los extremos de los microtbulos.
As pues, la estatmina disminuye la concentracin efectiva de las subunidades de
tubulina disponibles para la polimerizacin. Niveles elevados de estatmina en
una clula disminuyen la velocidad de elongacin de los microtbulos. Esta
velocidad lenta de elongacin tiene un segundo efecto remarcable. Dado que, en
un microtbulo que mantiene una inestabilidad dinmica, la transicin desde el
estado en crecimiento al estado de despolimerizacin depende del balance entre
la hidrlisis de GTP y la elongacin del filamento, disminuyendo la velocidad de
elongacin al secuestrar las subunidades de tubulina puede incrementarse la fre-
cuencia de despolimerizacin de los microtbulos. As pues, una protena que
inhibe la polimerizacin de tubulina puede tener el efecto secundario de
incrementar marcadamente el recambio dinmico de los microtbulos dentro de
la clula. La fosforilacin de la estatmina puede inhibir su unin a la tubulina de
forma que las seales que producen esta fosforilacin pueden incrementar la
velocidad de elongacin de los microtbulos y suprimir la inestabilidad
dinmica. Adems de la estatmina, que es una protena sintetizada por las
clulas, podemos nombrar la colchicina que es una droga.
Efectos de la timosina y de la profilina sobre la
polimerizacin de la actina
Efectos de la estatmina sobre la polimerizacin de
los microtbulos
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 13 -
Estabilizacin de los filamentos:
Cuando se ha formado el filamento mediante nucleacin y elongacin
a partir del conjunto de subunidades solubles, su estabilidad y propiedades
dinmicas a menudo se ven modificadas por un conjunto de protenas que
pueden unirse lateralmente al polmero. Diferentes protenas asociadas a los
filamentos utilizan su energa de unin para disminuir o incrementar la energa
libre del polmero, de forma que pueden estabilizarlo o desestabilizarlo,
respectivamente.
Las protenas que se unen lateralmente a los microtbulos se llaman
protenas asociadas a los microtbulos, o MAP. Las MAP pueden estabilizar los
microtbulos evitando su desensamblaje. Un conjunto de MAP puede tambin
mediar la interaccin de los microtbulos con otros componentes celulares,
como en las neuronas, en las que los haces de microtbulos estabilizados
forman el ncleo de los axones y dendritas. Estas MAP tienen como mnimo
un dominio mediante el cual se unen a la superficie de los microtbulos y otro
que se proyecta hacia su exterior. La longitud de este dominio de proyeccin
determina la distancia de empaquetamiento entre distintos microtbulos.
As, las clulas que sobreexpresan MAP2, la cual presenta un dominio de
proyeccin muy largo, forman haces de microtbulos estables muy distantes
los unos de los otros, mientras que las clulas que sobreexpresan tau, una MAP
con un dominio ms corto, forman haces ms cercanos de microtbulos
empaquetados. El dominio de unin a los microtbulos de algunas MAP
incluyendo a tau y a MAP2, contiene varias copias de un dominio de unin a
tubulina, que permite que se produzca aceleracin elevada de la nucleacin, ya
que pueden estabilizar los pequeos oligmeros de tubulina que se forman
inicialmente en el proceso de polimerizacin. Adems, estas MAP son reguladas
mediante fosforilaciones. Tambin podemos nombrar algunas drogas como el
taxol, que se une a la tubulina , y evita la despolimerizacin del microtbulo.
De forma parecida, los filamentos de actina tambin se pueden ver
afectados por la unin lateral de protenas accesorias. En la mayora de clulas
algunos de los filamentos de actina se estabilizan mediante unin a tropomiosina,
una protena alargada que se une simultneamente a siete subunidades de actina
adyacentes en un mismo protofilamento. La unin de tropomiosina a lo largo del
filamento de actina puede impedir a este filamento interactuar con otras
protenas; por esta razn, la regulacin de la unin de la tropomiosina es una etapa
muy importante en la contraccin muscular. Otra importante protena de unin a la
actina, presentes en todas las clulas eucariotas, es la cofilina, que desestabiliza los
filamentos de actina. Tambin denominada factor despolimerizador de actina,
tiene la caracterstica poco comn de unirse tanto a la forma de filamento de
actina como a las subunidades libres. Se une a lo largo de todo el filamento
haciendo que se enrosque un poco ms estrechamente. Este estrs mecnico
debilita los contactos entre las subunidades de actina del filamento, debilitndolo y
favoreciendo su rotura. Adems, tambin facilita la prdida de las subunidades con
ADP del extremo menos. Puesto que normalmente la velocidad de recambio
rotatorio del filamento de actina se ve limitada por una velocidad de disociacin
lenta en el extremo menos, la unin de cofilina aumenta mucho su velocidad de
recambio rotatorio. En definitiva, la cofilina favorece la despolimerizacin de los
filamentos ms antiguos (aquellos que tienen unidos ADP), asegurando un
recambio rpido de todos los filamentos de actina.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 14 -
Organizacin de los haces de microtbulos por las MAP Giro de un filamento de actina inducido por cofilina
Entrecruzamiento de los filamentos:
o Filamentos de actina: en las clulas animales los filamentos de actina
estn organizados en dos tipos de disposiciones: en haces y en redes
parecidas a geles. Por tanto, las protenas de entrecruzamiento de los
filamentos de actina pueden dividirse en dos clases: protenas que
forman haces y protenas que forman geles. Las protenas que forman
haces entrecruzan los filamentos de actina en disposiciones paralelas,
pueden ir paralelas en el mismo sentido, como los filopodios o las
microespculas, o paralelas en sentidos diferentes, como ocurre con los
haces contrctiles de las fibras de estrs. Por el contrario, las que forman
geles mantienen unidos los filamentos de actina en intersecciones en
diagonal dando lugar a redes laxas (crtex celular). Generalmente, ambos
tipos de protenas entrecruzadoras tienen dos lugares de unin al
filamento de actina parecidos entre s, que pueden formar parte de un
monmero (una cadena polipeptdica) o de un dmero (dos cadenas
polipeptdicas juntas). El espaciado y la disposicin de estos dominios de
unin determinan el tipo de estructura de actina que forma una protena
entrecruzadora.
Haces de actina en una clula
Los filamentos de actina
pueden verse en rojo, con
flechas negras que apuntan
hacia los extremos ms. Las
fibras de estrs son contrctiles
y ejercen tensin. Los
filopodios y las proyecciones
espinosas de la membrana
plasmtica permiten a la clula
explorar los alrededores. El
crtex se sita por debajo de la
membrana plasmtica.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 15 -
La fimbrina y la -actinina son protenas formadoras de haces
ampliamente distribuidas. La fimbrina es una protena entrecruzadora
pequea, con dos dominios de unin a la actina ntimamente unidos entre
s formando una cadena polipeptdica sencilla. Se encuentra en grandes
cantidades en los haces paralelos de actina de los filopodios y se supone
que es la responsable de la estrecha asociacin entre estos filamentos de
actina. La -actinina presenta dos dominios de unin a la actina con un
espaciado ms grande; se encuentra en grandes cantidades en las fibras de
estrs, en las que es responsable de la laxitud de los filamentos de actina
entrecruzados que forman estos haces contrctiles. Tambin participa en la
estructura que mantiene los extremos de las fibras de estrs en las uniones
focales de la membrana plasmtica, que son un tipo de unin de anclaje.
Cada tipo de protena empaquetadora determina que molculas diferentes
puedan interactuar con los filamentos de actina. La miosina II es la
protena responsable de que se contraigan las fibras de estrs y otros
conjuntos contrctiles. El empaquetamiento tan elevado provocado por la
fimbrina excluye al parecer a la miosina, por lo que los filopodios no son
contrctiles; en cambio, la laxitud del empaquetamiento provocado por la
-actinina permite la entrada de molculas de miosina, haciendo que las
fibras de estrs sean contrctiles.
La villina es otra protena empaquetadora que presenta dos lugares de
unin al filamento de actina muy cercanos en una misma cadena
polipeptdica. La villina (junto con la fimbrina) ayuda a entrecruzar de 20
a 30 filamentos de actina empaquetndolos muy estrechamente, como los
de las microvellosidades. Por ejemplo cada clula epitelial de absorcin
del intestino delgado humano (enterocito) tiene algunos miles de
microvellosidades en su superficie apical. Cada uno de ellos mide cerca
de 0,08 m de dimetro y 1 m de largo, haciendo que la superficie de
absorcin celular sea 20 veces mayor de lo que sera si no los tuviera.
Cuando se introduce villina en un cultivo de fibroblastos, clulas que
habitualmente no presentan esta protena y slo tienen unas cuantas
microvellosidades, los existentes se alargan y se estabilizan a la vez que se
induce la aparicin de ms. El ncleo de los filamentos de actina de la
microvellosidad se adhiere a la membrana plasmtica de forma lateral con
los brazos de la miosina I, protena que presenta un lugar de unin al
filamento de actina por un lado y un dominio de unin a lpidos por el
otro. Parece que estos dos tipos de entrecruzamientos, uno que une los
filamentos de actina entre s y el otro que los une a la membrana
plasmtica, bastan para formar las microvellosidades celulares.
Las diferentes protenas empaquetadoras que hemos tratado disponen de
conexiones rectas y rgidas entre sus dos dominios de unin a los
filamentos de actina y tienden a alinear los filamentos en haces paralelos.
Por el contrario, las protenas entrecruzadoras que disponen de conexiones
flexibles entre sus dos dominios de unin no forman haces sino geles
laxos de filamentos de actina.
Una protena formadora de geles muy bien estudiada es la espectrina,
identificada en los eritrocitos. Larga y flexible, est formada por cuatro
cadenas polipeptdicas (dos subunidades y dos , dispuestas de forma
que los dos lugares de unin al filamento de actina se hallan a 200 nm
(mucho mayor que la fibrina y la -actinina). En los eritrocitos, la
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 16 -
espectrina slo se encuentra debajo de la membrana plasmtica,
formando un gel bidimensional mantenido por filamentos cortos de
actina; une este gel a la membrana plasmtica puesto que dispone de
sitios de unin independientes para protenas perifricas de membrana,
las cuales son posicionadas cerca de la bicapa lipdica por protenas
integrales de membrana. La red resultante genera un crtex celular
rgido que confiere soporte mecnico a la membrana plasmtica y
permite a los eritrocitos recuperar su forma despus de atravesar los
capilares. En general, cualquier protena entrecruzadora que tenga sus
dos dominios de unin a la actina separados entre s una distancia
suficiente puede formar geles de actina tridimensionales, como es el
caso de la espectrina o de la filamina, que enlaza dos filamentos de
actina en ngulo recto, facilitando la formacin de geles altamente
viscosos y laxos. Los geles de actina formados por filamina son
necesarios para que las clulas extiendan los lamelipodios, que les
permiten extenderse por superficies slidas. La filamina ha
desaparecido en algunas clulas cancerosas, especialmente en los
melanomas malignos (cnceres de las clulas pigmentarias). Estas
clulas no pueden extenderse de forma apropiada y presentan
protrusiones desorganizadas de la membrana. La prdida de filamina es
una mala noticia para la clula de melanoma pero es una buena
noticia para el paciente; puesto que la clula es incapaz de extenderse y
emigrar, las clulas sin filamina son menos invasivas que sus
semejantes que todava expresan la protena, por lo que el cncer
formar metstasis con mayor dificultad.
Estructuras modulares de cuatro protenas que entrecruzan filamentos de actina
Cada una de estas protenas presenta dos lugares de unin a la actina (rojo) de secuencias relacionadas:
- La fimbrina tiene dos lugares de unin a la actina adyacentes, de forma que mantiene muy juntos dos
filamentos de actina (unos 14 nm de distancia), alineados con la misma polaridad.
- En cambio, los dos lugares de unin para la -actinina estn separados cerca de 30 nm, de forma que los
haces de actina que forman estn empaquetados de un modo ms laxo.
- La filamina dispone de dos lugares de unin en forma de V, de manera que entrecruza filamentos de
actina formando una red en la que los filamentos forman ngulos de casi 90 grados unos con otros.
- La espectrina es un tetrmero de dos subunidades y dos subunidades , y el tetrmero tiene dos
lugares de unin de actina espaciados cerca de 200 nm.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 17 -
Una microvellosidad
La parte central de la
microvellosidad est formada
por un haz de filamentos de
actina paralelos, que se
mantienen mediante protenas
formadoras de haces de actina
(villina y fimbrina). Los brazos
laterales (formados por miosina
I y por la protena de unin al
Ca
2+
calmodulina) conectan los
lados del haz de filamentos de
actina a la membrana
plasmtica contigua. Los
extremos ms de los filamentos
de actina se hallan en el
extremo de la estructura, donde
estn inmersos en una sustancia
amorfa, muy electrodensa, de
composicin desconocida.
Formacin de dos tipos de haces de filamentos de actina
La -actinina, que es un homodmero, entrecruza filamentos de
actina en haces laxos que permiten a la protena motora miosina II
(no mostrada) participar en el ensamblaje. La fimbrina entrecruza
los filamentos en haces muy juntos, que excluyen la miosina. La
fimbrina y la -actinina tienden a excluirse una a otra debido a las
diferencias de espaciado que generan entre los haces de
filamentos de actina.
La filamina entrecruza filamentos de actina en una red
tridimensional que tiene propiedades fsicas de gel
Cada homodmero de filamina tiene cerca de 160 nm de longitud
cuando est totalmente extendida y forma un ngulo grande y
flexible entre dos filamentos de actina adyacentes. Un conjunto de
filamentos de actina entrecruzados por filamina forman una red o
gel muy fuerte mecnicamente.
o Filamentos intermedios: Cada filamento intermedio se forma como un
largo paquete de subunidades tetramricas. Adems, muchos se
empaquetan entre s autoasocindose; as, las protenas NF-M y NF-H
de los neurofilamentos presentan un dominio C-terminal que se extiende
desde la superficie de un filamento intermedio ensamblado hacia el
exterior, unindose al filamento vecino. Estos grupos de
neurofilamentos forman hileras paralelas muy robustas que se
mantienen unidas por contactos laterales mltiples, confiriendo
estabilidad y fuerza a las largas expansiones neuronales. Otros tipos de
empaquetamiento de los filamentos intermedios se mantienen unidos por
protenas accesorias, como la filagrina, que en las clulas en
diferenciacin de la epidermis empaqueta los filamentos de queratina. La
plectina, que empaqueta los filamentos de vimentina, es una protena de
entrecruzamiento muy interesante. Adems de empaquetar los
filamentos intermedios, tambin los une a los microtbulos, a los haces
de filamentos de actina y a los filamentos de la protena motora miosina
II, y adems permite la unin de los haces de filamentos intermedios a
las estructuras adhesivas de la membrana plasmtica.
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 18 -
Rotura de los filamentos:
En algunas ocasiones, una clula puede romper un filamento largo ya
existente en muchos filamentos ms cortos. Esto genera una gran cantidad de
extremos nuevos: un filamento largo slo tiene un extremo ms y un extremo
menos, pero al romperse en docenas de filamentos cortos, cada uno de ellos
presentar su propio extremo menos y su propio extremo ms. En ciertas
condiciones intracelulares, estos extremos acabados de formar nuclean la
elongacin de un filamento, acelerndose el ensamblaje de nuevas estructuras
formadas por filamentos mientras que en otras condiciones, la fragmentacin
induce la despolimerizacin de los filamentos viejos. Adems, algunos
filamentos cambian las propiedades fsicas y mecnicas del citoplasma: cuando
los filamentos se fragmentan los haces largos y rgidos y los geles se hacen ms
fluidos.
o Microtbulos: para romper un microtbulo se han de romper trece enlaces
longitudinales, uno por cada protofilamento. La protena catanina realiza
esta funcin. La catanina est formada por dos subunidades, una subunidad
pequea que hidroliza el ATP y que realiza la fragmentacin y una
subunidad mayor que dirige la catanina hacia el centrosoma. La catanina
libera los microtbulos de su unin al centro organizador de microtbulos y
se cree que juega un papel crucial y particularmente importante en la rpida
despolimerizacin observada en los polos del huso mittico durante la
mitosis. Tambin se ha encontrado en la profase de las clulas proliferantes y
en clulas postmitticas como las neuronas, donde puede participar en la
liberacin y despolimerizacin de los microtbulos.
o Filamentos de actina: la mayora de las protenas fragmentadotas de
filamentos de actina forman parte de la superfamilia gelsolina, cuya
actividad fragmentadora se activa por un incremento de los niveles de Ca
+2
citoslico, y no mediante la hidrlisis de ATP como ocurre con la catanina.
La gelsolina presenta subdominios que se unen a dos lugares distintos de la
subunidad de actina, uno expuesto en la superficie del filamento y otro
normalmente escondido en el enlace longitudinal hacia la prxima subunidad
del protofilamento. Segn un modelo de su fragmentacin, se une lateral-
mente a un filamento de actina y espera hasta que se produce una fluctuacin
trmica que genera un pequeo agujero entre dos subunidades vecinas del
protofilamento; entonces, introduce su subdominio en el agujero, rompiendo
el filamento. Cuando la gelsolina ha fragmentado el filamento de actina,
permanece unida al extremo ms.
Unin de los filamentos a la membrana celular:
Una funcin comn de las estructuras citoesquelticas de actina consiste
en endurecer o cambiar la forma de la membrana plasmtica. Hemos descrito al
menos dos ejemplos: la red de espectrina-actina que yace debajo de la membrana
plasmtica de los eritrocitos y los haces de villina-actina de las
microvellosidades que incrementan la superficie de absorcin en las clulas
epiteliales. La efectividad de estas estructuras depende tanto del
empaquetamiento y del entrecruzamiento de los filamentos de actina como de la
unin especfica entre estas estructuras y las protenas o lpidos de la membrana
plasmtica. En la mayora de casos, el ensamblaje del citoesqueleto tambin
conecta la estructura interna de la clula con el medio que la rodea, como otras
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 19 -
clulas y la matriz extracelular. Los filamentos de actina y los intermedios son
cruciales para ello.
Una familia muy extensa e ntimamente relacionada de protenas
intracelulares es la familia ERM (llamada as por sus tres primeros miembros,
ezrina, radixina y moesina), que actan uniendo filamentos de actina a la
membrana plasmtica en muchos tipos celulares. El dominio C-terminal de las
protenas ERM se une directamente a los lados de los filamentos de actina. El
dominio N-terminal se une a la cara citoplasmtica de algunas glucoprotenas
transmembrana, y tambin a algn componente de la matriz extracelular. La
importancia funcional de las protenas ERM viene indicada por las
consecuencias que se derivan de mutaciones que comportan la prdida de uno de
los miembros de la familia, llamado merlina. Esta prdida comporta la aparicin
de una forma de la enfermedad gentica llamada neurofibromatosis, en la cual se
desarrollan mltiples tumores benignos en los nervios auditivos y en otras partes
del sistema nervioso.
Las uniones mediadas por las protenas ERM estn reguladas por seales
tanto intracelulares como extracelulares. Las protenas ERM pueden existir en
dos conformaciones, una conformacin extendida activa que oligomeriza y se
une a la actina y a CD44, y una conformacin plegada inactiva, en la cual los
extremos N- terminal y C-terminal estn empaquetados juntos mediante
interacciones intramoleculares. El paso de una conformacin a otra se puede
producir por fosforilacin o por la unin a Fosfoinositol bifosfato (PIP
2
), y las
dos cosas se pueden producir, por ejemplo, en respuesta a seales extracelulares.
As pues, la fuerza de los contactos mediados por las protenas ERM entre el
citoesqueleto de actina y la matriz extracelular es sensible a una gran variedad de
seales recibidas por la clula.
El desplegamiento de las protenas de la familia ERM inducido por fosforilacin o unin a PIP
2
(Phosphatidylinositol bisphosphate) deja expuestos dos lugares de unin, uno para un filamento de actina
y otro para una protena transmembrana. La activacin de estas protenas puede originar y estabilizar
protrusiones superficiales de la clula que se forman respondiendo a seales extracelulares.
Las uniones focales son unos tipos de adhesin muy especializados entre
los filamentos de actina y la matriz extracelular que permiten a la clula
extenderse sobre el sustrato al cual est unida.
Las fibras de estrs -haces contrctiles de actina y filamentos de miosina
II- finalizan en la membrana plasmtica, donde se localizan grupos de protenas
de adhesin transmembrana, llamadas integrinas. Las integrinas son una gran
familia de protenas heterodimricas que se unen a distintos componentes de la
TEMA 27: El Citoesqueleto III
Carlos Navarro Lpez - 20 -
matriz extracelular y su unin a los haces de filamentos de actina est mediada
por un complejo formado por muchas protenas intracelulares de anclaje.
Adems de realizar una funcin de anclaje para la clula, las uniones focales
tambin pueden transmitir seales desde la matriz extracelular al interior de la
clula.
Adems de formar adhesiones mecnicas fuertes con la matriz
extracelular, los elementos del citoesqueleto unidos a la membrana plasmtica
tambin proporcionan uniones con otras clulas. As, los contactos clula-clula
formados en los epitelios se producen sobre todo por interacciones de protenas
transmembrana tipo cadherina. La cola citoplasmtica de la molcula de
cadherina se une a cateninas, que a su vez se unen a los filamentos de actina.
Grupos de estos contactos clula-clula mediados por cadherina y reforzados por
actina forman las uniones adherentes.
En la unin de los filamentos intermedios a la membrana plasmtica
operan los mismos principios generales que en los contactos focales en las
uniones adherentes, en los cuales haces de filamentos del citoesqueleto estn
unidos, indirectamente a travs de elaborados complejos multiproteicos, a
protenas de adhesin transmembrana. Los filamentos intermedios estn
anclados a la membrana plasmtica a travs de desmosomas (en las uniones
clula-clula) y hemidesmosomas (en las uniones clula-matriz extracelular).
Estas uniones son muy importantes para mantener la fuerza de los tejidos
epiteliales.
Respuesta a seales extracelulares:
Como ya hemos dicho, las protenas accesorias asociadas con los
sistemas de filamentos del citoesqueleto pueden regular la longitud, la
localizacin la organizacin y el comportamiento dinmico del filamento. Las
seales extracelulares pueden alterar su actividad y, as, cambiar el citoesqueleto
y el comportamiento celular.
En el citoesqueleto de actina, las reorganizaciones estructurales globales
en respuesta a seales externas se inducen a travs de receptores diversos de la
superficie celular. Pero, todas estas seales convergen en el interior celular en un
grupo ntimamente relacionado de GTPasas monomricas de la familia de
protenas Rho -Cdc42, Rac y Rho-, las cuales actan como dispositivos
moleculares que controlan procesos celulares y alternan una forma activa unida a
GTP con una forma inactiva unida a GDP. La activacin de unas u otras
protenas har que la actina se empaquete de una manera o de otra, y que se
asocie a unas protenas motor o a otras.
Estas protenas Rho pueden presentarse en una conformacin plegada
inactiva y en una abierta activada.
S-ar putea să vă placă și
- Citoesqueleto PDFDocument20 paginiCitoesqueleto PDFIsidoraÎncă nu există evaluări
- Histología y Embrología del Sitema NerviosoDe la EverandHistología y Embrología del Sitema NerviosoEvaluare: 4 din 5 stele4/5 (4)
- 05 Citoplasma - CitoesqueletoDocument19 pagini05 Citoplasma - CitoesqueletoAlfredo Sam Alvaro HerreraÎncă nu există evaluări
- Anemia Para Todos: Medicina Para TodosDe la EverandAnemia Para Todos: Medicina Para TodosEvaluare: 3 din 5 stele3/5 (1)
- El CitoesqueletoDocument7 paginiEl CitoesqueletoKateryn ÁlvarezÎncă nu există evaluări
- Citoesqueleto: Microfilamentos Filamentos Intermedios MicrotúbulosDocument10 paginiCitoesqueleto: Microfilamentos Filamentos Intermedios MicrotúbulosDian GÎncă nu există evaluări
- La Celula Parte 2Document50 paginiLa Celula Parte 2Ale CaballeroÎncă nu există evaluări
- Movimiento Celular PDFDocument32 paginiMovimiento Celular PDFAnonymous mpkNzlmTf100% (2)
- Biología P19Document15 paginiBiología P19jg2488955Încă nu există evaluări
- Cito EsqueletoDocument4 paginiCito EsqueletoMateo DuraznoÎncă nu există evaluări
- CitoesqueletoDocument11 paginiCitoesqueletoMilagros QuispeÎncă nu există evaluări
- Observación Del Flagelo y Algunas Características de Los Espermatozoides HumanosDocument12 paginiObservación Del Flagelo y Algunas Características de Los Espermatozoides HumanosJose Marco Muñoz Bocanegra100% (1)
- CITOESQUELETO GenomasurDocument32 paginiCITOESQUELETO GenomasurDaiana tabordaÎncă nu există evaluări
- CitoesqueletoDocument21 paginiCitoesqueletoSoraida Sanchez ParraÎncă nu există evaluări
- 8 - Trabajo de Biologia (Word) - El CitoesqueletoDocument3 pagini8 - Trabajo de Biologia (Word) - El CitoesqueletoAndrea Blanco Sánchez100% (1)
- Tarea 8 Biología 3°Document8 paginiTarea 8 Biología 3°Esteban Barrios RodriguezÎncă nu există evaluări
- Citoesqueleto Final IntroDocument6 paginiCitoesqueleto Final IntroBelenMinÎncă nu există evaluări
- Seg Exa BiologiaDocument36 paginiSeg Exa BiologiaBrayan Villavicencio TovarÎncă nu există evaluări
- Citoesqueleto PresentacionDocument13 paginiCitoesqueleto PresentacionRachel CardenasÎncă nu există evaluări
- Transcripcion de CITOESQUELETODocument19 paginiTranscripcion de CITOESQUELETOJonathan GonzalezÎncă nu există evaluări
- LLANQUI CALSIN Luis Pascual (Matriz Citoplasmatica)Document39 paginiLLANQUI CALSIN Luis Pascual (Matriz Citoplasmatica)Gavino José Flores ChipanaÎncă nu există evaluări
- Cito PlasmaDocument21 paginiCito PlasmaBarbara VegaÎncă nu există evaluări
- Que Es El ProtoplasmaDocument13 paginiQue Es El ProtoplasmaDenian CastilloÎncă nu există evaluări
- Citosol, Comunicaciones y CitoesqueletoDocument4 paginiCitosol, Comunicaciones y CitoesqueletoPaulaÎncă nu există evaluări
- UNIDAD 1 CitologiaDocument16 paginiUNIDAD 1 CitologiaLara AgnoluzziÎncă nu există evaluări
- AnlisisDocument4 paginiAnlisisestefania figueroaÎncă nu există evaluări
- ENSAYO Citoesqueleto Karisbel SDocument4 paginiENSAYO Citoesqueleto Karisbel Skarisbel suarezÎncă nu există evaluări
- CITOESKELETODocument14 paginiCITOESKELETOJose Vicente Banda NuñezÎncă nu există evaluări
- Membrana Celular Mapa Conceptual..... Norma 5..Document8 paginiMembrana Celular Mapa Conceptual..... Norma 5..Jamirton Erledy GarciaÎncă nu există evaluări
- CitoesqueletoDocument9 paginiCitoesqueletojennifer arizaÎncă nu există evaluări
- Organelos CelularesDocument12 paginiOrganelos CelularesJulio Rz100% (3)
- CITOESQUELETODocument23 paginiCITOESQUELETOMeritxell Planell CastellsÎncă nu există evaluări
- 4 Citoplasma y Citoesqueleto UBODocument35 pagini4 Citoplasma y Citoesqueleto UBOPerro PeregrinoÎncă nu există evaluări
- CitoesqueletoDocument13 paginiCitoesqueletoBian RamirezÎncă nu există evaluări
- Cómo Es El Tráfico IntracelularDocument9 paginiCómo Es El Tráfico IntracelularJonathan Atlahua MorenoÎncă nu există evaluări
- 6 Ensayo CitoesqueletoDocument6 pagini6 Ensayo CitoesqueletoValeria Fernanda Rocha MerinoÎncă nu există evaluări
- Cuestionario Sobre La CelulaDocument6 paginiCuestionario Sobre La CelulaArco VersoÎncă nu există evaluări
- B2 T4 - CÉLULA EUCARIOTA - Citoplasma ApuntesDocument16 paginiB2 T4 - CÉLULA EUCARIOTA - Citoplasma ApuntesNacho Orio FernándezÎncă nu există evaluări
- 3º Medio - Electivo Biología - Guía 3Document9 pagini3º Medio - Electivo Biología - Guía 3Leslie VillalobosÎncă nu există evaluări
- CélulaDocument18 paginiCélulaABAD TÎncă nu există evaluări
- TALLER # 4 Estructura Celular.Document7 paginiTALLER # 4 Estructura Celular.Camilo MedinaÎncă nu există evaluări
- Celula, Morfologia CelularDocument8 paginiCelula, Morfologia Celularscarletlugo4751Încă nu există evaluări
- Unidad 3 La CelulaDocument8 paginiUnidad 3 La CelulaTania LopezÎncă nu există evaluări
- Copia de Célula Eucariótica. Componentes Estructurales y Funciones. PARED CELULAR, CITOSOL y RIBOSOMASDocument9 paginiCopia de Célula Eucariótica. Componentes Estructurales y Funciones. PARED CELULAR, CITOSOL y RIBOSOMASCristina BlancoÎncă nu există evaluări
- Apuntes GenomasurDocument67 paginiApuntes GenomasurJuan José VasquezÎncă nu există evaluări
- Microtúbulos Del Citoesqueleto de Las CelulasDocument1 paginăMicrotúbulos Del Citoesqueleto de Las Celulaspitu_alÎncă nu există evaluări
- Citoplasma 2 WordDocument11 paginiCitoplasma 2 WordYessenia AlulimaÎncă nu există evaluări
- Informe El CitoesqueletoDocument4 paginiInforme El CitoesqueletoclaudiaÎncă nu există evaluări
- InformeDocument20 paginiInformevicmarcorderoiseaÎncă nu există evaluări
- Guia de Estudio 1biologíaDocument7 paginiGuia de Estudio 1biologíaCristina MoralesÎncă nu există evaluări
- Guia Células Octavo BásicoDocument6 paginiGuia Células Octavo BásicoSscc Primero Medio BÎncă nu există evaluări
- Cuestionario Capítulo 9Document5 paginiCuestionario Capítulo 9Abi Jtl50% (2)
- Cito EsqueletoDocument8 paginiCito EsqueletoJuan OrtízÎncă nu există evaluări
- Sem5 CitoesqueletoDocument13 paginiSem5 CitoesqueletoAna Gabriela PuiconÎncă nu există evaluări
- Que Son Los Microtubulos Filamentos IntermediosDocument6 paginiQue Son Los Microtubulos Filamentos IntermediosMarvinRiveraÎncă nu există evaluări
- 4.4 Transduccion-Citoesqueleto y 4.5 SeñalizacionDocument11 pagini4.4 Transduccion-Citoesqueleto y 4.5 Señalizacion6s5h49v2jrÎncă nu există evaluări
- Vacuola CentralDocument3 paginiVacuola CentralAlexRmzMtz0% (1)
- Movimiento de ProtozoosDocument5 paginiMovimiento de Protozooseduar2626226100% (1)
- Microtubulos y Filamentos IntermediosDocument43 paginiMicrotubulos y Filamentos IntermediosRQ ChristianÎncă nu există evaluări
- Diabetic Ketoacidosis and Hyperosmolar Hyperglycemic State in Adults - Clinical Features, Evaluation, and Diagnosis - UpToDateDocument18 paginiDiabetic Ketoacidosis and Hyperosmolar Hyperglycemic State in Adults - Clinical Features, Evaluation, and Diagnosis - UpToDateEddie Mondragon Gomez100% (1)
- Definición de Asma y Crisis Aguda de Asma BronquialDocument8 paginiDefinición de Asma y Crisis Aguda de Asma BronquialEddie Mondragon GomezÎncă nu există evaluări
- Modulo Medicina InternaDocument41 paginiModulo Medicina InternaEddie Mondragon GomezÎncă nu există evaluări
- Manual de Normas y Procedimientos PAIDocument176 paginiManual de Normas y Procedimientos PAIEddie Mondragon Gomez100% (1)
- Dolor PrecordialDocument11 paginiDolor PrecordialEddie Mondragon Gomez100% (1)
- Angina de PechoDocument11 paginiAngina de PechoEddie Mondragon GomezÎncă nu există evaluări
- Verificacion Negocios Verdes Hidroherbal TotaDocument94 paginiVerificacion Negocios Verdes Hidroherbal TotaSandoval YaisaÎncă nu există evaluări
- Edafologia y NutricionDocument17 paginiEdafologia y NutricionTitoariel FloresÎncă nu există evaluări
- 5 Valeria Souza 03022012Document40 pagini5 Valeria Souza 03022012LUZMAÎncă nu există evaluări
- Intrumentos de BioquimicaDocument6 paginiIntrumentos de Bioquimicaligia05Încă nu există evaluări
- Las Lomas de CarabaylloDocument2 paginiLas Lomas de CarabaylloKathii la HozÎncă nu există evaluări
- GUIA - Personalidad y EmociónDocument25 paginiGUIA - Personalidad y EmociónDiana CabezasÎncă nu există evaluări
- Cuestionario de Ciencias NaturalesDocument3 paginiCuestionario de Ciencias NaturalesAlexandra RoseroÎncă nu există evaluări
- 7 Mejoramiento CacaoDocument13 pagini7 Mejoramiento CacaoAlex Cordova RÎncă nu există evaluări
- Guia 6 Floculación VDRL RPRDocument9 paginiGuia 6 Floculación VDRL RPRAndrews CeballosÎncă nu există evaluări
- Manejo Sostenible Del Cultivo Del TomateDocument60 paginiManejo Sostenible Del Cultivo Del TomateAndrea Nogales OrozcoÎncă nu există evaluări
- Aprovechamiento Del MaizDocument4 paginiAprovechamiento Del MaizIsidro Orozco AlvarezÎncă nu există evaluări
- MoraxellaDocument9 paginiMoraxellaDavid GarciaÎncă nu există evaluări
- Deforestacion Del Guaviare Otros EstudiDocument9 paginiDeforestacion Del Guaviare Otros EstudiEulerFÎncă nu există evaluări
- CuadernoDocument27 paginiCuadernoCristhian SilvaÎncă nu există evaluări
- Orangutanes, Gibon y GorilasDocument7 paginiOrangutanes, Gibon y GorilasErika GarciaÎncă nu există evaluări
- Enfermedad de HartnupDocument5 paginiEnfermedad de HartnupKaty DelgadoÎncă nu există evaluări
- Los Compuestos Flavonoides Comparten Una Estructura Química ComúnDocument4 paginiLos Compuestos Flavonoides Comparten Una Estructura Química ComúnMauricio Martinez100% (1)
- GDG FreeDocument96 paginiGDG FreeAndrés SambóniÎncă nu există evaluări
- Congreso Internacional de Medicina y Cirugía Equina 2010Document355 paginiCongreso Internacional de Medicina y Cirugía Equina 2010Enciaflor100% (2)
- Metodo CientificoDocument2 paginiMetodo CientificoCarlos Miguel Mercado PanduroÎncă nu există evaluări
- Regulación de La Expresión GénicaDocument25 paginiRegulación de La Expresión GénicaWALTER PHILIPPE CESAR LEONCIO SAENZ LOPEZÎncă nu există evaluări
- Jugo de Limón AqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqDocument9 paginiJugo de Limón AqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqqEver Castillo PeñaÎncă nu există evaluări
- FOLLETO Animales en Peligro de ExtinciónDocument17 paginiFOLLETO Animales en Peligro de ExtinciónXimena GarciaÎncă nu există evaluări
- Informe Fincas LecherasDocument18 paginiInforme Fincas LecherasSaray MarmolejoÎncă nu există evaluări
- Imagenologia de ATMDocument104 paginiImagenologia de ATMAlbeiro David Cordoba SolarteÎncă nu există evaluări
- 2000 002 001 PDFDocument156 pagini2000 002 001 PDFCarolina de SevaniÎncă nu există evaluări
- Bitacora Bioquimica Practica 2 SangerDocument4 paginiBitacora Bioquimica Practica 2 SangerDiego AmrÎncă nu există evaluări
- Posturas de Yoga - Grupo 6Document3 paginiPosturas de Yoga - Grupo 6Jason Cerdas AnchiaÎncă nu există evaluări
- Sánchez González, E - Determinación de La Producción Forrajera y La Carga Bovina Ante La Variabilidad...Document28 paginiSánchez González, E - Determinación de La Producción Forrajera y La Carga Bovina Ante La Variabilidad...Ana paola Flores RodriguezÎncă nu există evaluări
- Ficha RespiratorioDocument2 paginiFicha RespiratorioJose Luis Medina LlicanÎncă nu există evaluări