Documente Academic
Documente Profesional
Documente Cultură
Allogreffe de Cellules Souches Hématopoïétiques Réalisation Et Complications 2010 EMC
Încărcat de
Jankis KhanDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Allogreffe de Cellules Souches Hématopoïétiques Réalisation Et Complications 2010 EMC
Încărcat de
Jankis KhanDrepturi de autor:
Formate disponibile
13-061-A-10
Allogreffe de cellules souches
hmatopotiques :
ralisation et complications
N. Dhdin, J.-P. Vernant
Lallogreffe de cellules souches hmatopotiques permet de gurir des hmopathies malignes et des
maladies non malignes de la moelle osseuse ou du systme immunitaire. Elle implique ladministration au
receveur dun conditionnement qui a pour but de dtruire : son systme immunitaire (pour prvenir le
rejet de greffe) et, un degr variable, un clone malin. Le conditionnement est suivi de linjection du
greffon de cellules souches hmatopotiques. Dans ce greffon, les lymphocytes peuvent reconnatre et
dtruire les cellules tumorales rsiduelles du receveur (effet du greffon contre la leucmie). Cette raction
explique lintrt de lallogreffe dans les hmopathies malignes. Paralllement, le systme immunitaire du
greffon peut tre lorigine de ractions dltres vis--vis des organes sains du receveur, cest la raction
du greffon contre lhte. Lallogreffe de cellules souches hmatopotiques saccompagne dune morbidit
et dune mortalit secondaires la toxicit du conditionnement, la raction du greffon contre lhte et
au dficit immunitaire postgreffe. Lincidence et la gravit de ces complications dpendent la fois de
paramtres propres au receveur (ge, statut de lhmopathie) et des modalits de la greffe (type de
conditionnement, compatibilit HLA [human leucocyte antigen] entre le donneur et le receveur,
manipulation ex vivo du greffon, type de greffon). Le dveloppement de nouvelles techniques et modalits
de greffe a permis damliorer la survie des patients greffs et dtendre les indications de greffe. Les
principaux progrs concernent le dveloppement des greffes conditionnement rduit, des greffes de
cellules souches priphriques ou de sang placentaire, lamlioration des techniques de typage HLA dans
les greffes non apparentes.
2010 Elsevier Masson SAS. Tous droits rservs.
Mots cls : Allogreffe de cellules souches hmatopotiques ; Greffe de cellules souches priphriques ;
Raction du greffon contre lhte ; Effet du greffon contre la leucmie ; Greffe de sang placentaire
Introduction
Plan
Introduction
Principes et mthodes
Conditionnement de greffe
Diffrents types de greffons
Choix du donneur
2
2
3
5
Ractions immunologiques lallogreffe de cellules
souches hmatopotiques
Raction du greffon contre lhte (GVHD)
Non-prise et rejet de greffe
Raction du greffon contre la leucmie
Dficit immunitaire
6
6
10
10
11
Autres complications de lallogreffe
Complications prcoces
Complications tardives
13
13
14
Rechutes aprs allogreffe de cellules souches
hmatopotiques pour hmopathies malignes
Facteurs favorisants
Dtection de la rechute
Traitement de la rechute
14
14
14
15
Voies de dveloppement et perspectives davenir
Contrle de la maladie du greffon contre lhte
Amlioration de leffet antitumoral
15
15
16
Lallogreffe de cellules souches hmatopotiques (CSH)
constitue un traitement curatif dans les hmopathies malignes
et dans certaines maladies non malignes de la moelle osseuse ou
du systme immunitaire (aplasies mdullaires, hmoglobinopathies, dficits immunitaires congnitaux). Dans les hmopathies
malignes, lallogreffe a pour but dradiquer une maladie
maligne clonale. Dans les autres cas, il sagit schmatiquement
de remplacer une moelle malade par une moelle fonctionnelle.
La ralisation dune allogreffe implique ladministration au
receveur dun conditionnement qui permet :
limmunosuppression de lhte ncessaire la prise du
greffon et la prvention du rejet de greffe ;
la destruction des cellules hmatopotiques de lhte, visant
supprimer un ventuel clone malin. Ce deuxime objectif
est assur par le conditionnement, de faon variable en
fonction de son intensit.
Cette premire tape est suivie de ladministration du greffon
qui peut provenir de trois sources : moelle osseuse, cellules
souches priphriques (CSP) mobilises par exemple par le
granulocyte-colony stimulating factor (G-CSF) chez le donneur, ou
unit(s) de sang placentaire(s) (USP). Ces greffons peuvent
provenir de donneurs apparents ou non apparents.
La greffe de CSH peut saccompagner de ractions immunologiques dues la disparit dhistocompatibilit entre le
donneur et le receveur : il sagit principalement de la raction
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
du greffon contre lhte (maladie du greffon contre lhte graft
versus host disease [GVHD]) et du rejet de greffe (host versus graft
[HVG]). Dans des conditions habituelles de greffe, la frquence
de la GVHD est bien plus leve que celle de lHVG. La GVHD
est due la reconnaissance dalloantignes (majeurs ou mineurs
dhistocompatibilit) du receveur par les lymphocytes T du
donneur. Si lactivation de ces lymphocytes peut provoquer des
ractions dltres de certains organes cibles du receveur, elle
peut aussi tre responsable de la reconnaissance et de la
destruction des cellules tumorales rsiduelles du receveur (effet
du greffon contre la leucmie graft versus leukemia [GVL]).
Cest cet effet qui justifie la ralisation dallogreffes de CSH dans
les hmopathies malignes.
Le choix des modalits de greffe, cest--dire le type de
conditionnement et de prvention de la GVHD, la source du
greffon et la slection du donneur, dpend de la pathologie du
receveur, de son ge, de ses ventuelles comorbidits et du type
de greffon Lintrt et les limites des diffrentes modalits de
greffe vont tre dvelopps ci-dessous, ainsi que les complications possibles des allogreffes de CSH.
Principes et mthodes
Conditionnement de greffe
Le conditionnement joue un rle essentiel dans lallogreffe de
CSH. Il a pour but dassurer une immunosuppression du
receveur suffisante pour permettre la prise de greffe et prvenir
le rejet de greffe. Il doit aussi, un degr variable, dtruire les
cellules tumorales du receveur. Les premiers conditionnements
utiliss sont actuellement qualifis de myloablatifs, cest--dire
quils sont responsables dune destruction suppose dfinitive
des CSH du receveur. Ce type de conditionnement entrane une
morbidit et une mortalit certaine dont lincidence augmente
avec lge et les comorbidits du receveur. Outre ces greffes
conditionnements myloablatifs sont apparues depuis bientt
15 ans des greffes conditionnements rduits ou greffes
conditionnements non myloablatifs. La notion de conditionnement non myloablatif repose sur les principes suivants :
leffet antitumoral observ aprs lallogreffe est plus en
rapport avec leffet GVL quavec le conditionnement chimiothrapie plus ou moins radiothrapique ;
la destruction de la moelle du receveur par le conditionnement nest pas indispensable la prise de greffe.
La prise de greffe peut tre assure par les lymphocytes
alloractifs du donneur, qui dtruisent progressivement les
cellules du systme immunitaire du receveur et permettent
linstallation progressive de lhmatopose de donneur. Pendant
les premires semaines postgreffe, il existe un tat de chimrisme mixte (coexistence de cellules hmatopotiques du
donneur et du receveur) jusquau remplacement complet de
lhmatopose du receveur par celle du donneur.
Selon ce principe, le conditionnement a pour fonction
principale de prvenir le rejet de greffe en dtruisant le systme
immunitaire du receveur. Ce conditionnement doit, de ce fait,
tre plus immunosuppresseur que mylotoxique. Lallgement du
conditionnement devrait saccompagner dune diminution de la
frquence de la GVHD (cf. sous-chapitre Raction du greffon
contre lhte ). Limmunosuppression postgreffe, utilise pour
prvenir la GVHD peut contribuer prvenir lHVG. Les conditionnements non myloablatifs ont pour avantage une moindre
toxicit extrahmatologique. Ils peuvent, de ce fait, tre proposs
des patients plus gs et des patients fragiles chez lesquels un
conditionnement myloablatif est contre-indiqu [1, 2].
Il est habituellement admis que la limite dge pour la
ralisation dune greffe conditionnement myloablatif est
environ 50 ou 55 ans alors quelle atteint 65 ans et parfois plus
dans les greffes conditionnement rduit. Il existe actuellement
un dveloppement trs important des greffes conditionnement rduit, principalement dans les pathologies des sujets gs
telles que le mylome, les syndromes lymphoprolifratifs de bas
grade de malignit et les syndromes mylodysplasiques. Il est
difficile de comparer les rsultats des greffes conditionnement
myloablatif de celles conditionnement rduit, ces dernires
tant habituellement ralises chez les patients prsentant une
contre-indication la ralisation dune greffe conditionnement myloablatif. Les tudes rtrospectives semblent montrer
que si la toxicit est moins importante dans les greffes
conditionnement rduit, lincidence de rechute est probablement suprieure.
Conditionnement myloablatif
Le conditionnement myloablatif entrane la destruction des
cellules hmatopotiques de lhte et la vacuit mdullaire
hmatologique. Il assure la fois la rduction de la maladie,
maligne ou non, pour laquelle la greffe est ralise, et limmunosuppression de lhte ncessaire la prise du greffon. Ce
conditionnement est ainsi la fois immunosuppresseur et
mylotoxique. La soumission ces impratifs na pas la mme
importance selon les indications de la greffe : titre dexemple,
un conditionnement de greffe pour aplasie mdullaire a pour
principal objectif limmunosuppression du receveur, alors que,
pour une hmopathie maligne, il doit tre la fois antitumoral
et immunosuppresseur.
Techniques
Irradiation corporelle totale. Le choix des paramtres
dirradiation (la dose totale, le nombre de fractions et le dbit
de dose) peut avoir des consquences sur lefficacit de lirradiation corporelle totale (ICT) en termes de rduction tumorale, de
pouvoir immunosuppresseur et daction sur les cellules mdullaires non tumorales. LICT peut tre ralise en dose unique ou
fractionne. Dans le premier cas, la dose totale est en gnral de
10 Gy, dlivre en une seule fois avec un dbit de dose bas. Le
problme pos par lICT en une seule fraction est celui de sa
tolrance immdiate et surtout long terme. Les effets secondaires, survenant dans les semaines, les mois ou les annes qui
suivent la greffe, sont les pneumopathies interstitielles, la
maladie veino-occlusive du foie, la cataracte et les troubles
endocriniens. Le fractionnement de la dose est un moyen
dobtenir une meilleure rparation des lsions subltales dans les
tissus sains, notamment le poumon. Plusieurs schmas sont
utiliss, la dose totale tant gnralement de lordre de 12 Gy,
le plus souvent dlivre en six fractions de 2 Gy sur 3 jours [3,
4]. De nombreux essais non contrls semblent confirmer leffet
bnfique du fractionnement sur le risque de pneumopathie
interstitielle. Le risque de maladie veino-occlusive parat
galement diminu par ce schma dirradiation, de mme que
les effets secondaires moyen ou long terme.
Chimiothrapie. Plusieurs types de chimiothrapie peuvent
tre utiliss dans le conditionnement lallogreffe. La grande
majorit des conditionnements associe un ou plusieurs agents
de chimiothrapie une ICT ou du busulfan. Les deux
conditionnements de greffe les plus classiques associent une ICT
du cyclophosphamide (Endoxan) pour lun et du busulfan
du cyclophosphamide pour lautre. Ces conditionnements
peuvent tre renforcs pour augmenter leffet antitumoral dans
les hmopathies grand risque de rechute (ajout dtoposide
dans les leucmies aigus lymphodes) ou pour diminuer le
risque de non-prise dans les greffes non totalement HLAidentiques (ajout de srum antilymphocytaire).
Indications
Hmopathies malignes. Le conditionnement de rfrence a
longtemps t constitu par lassociation dune ICT dlivre en
dose unique 10 Gy et de cyclophosphamide (60 mg/kg
pendant 2 jours) [5]. De nombreuses modulations sont ensuite
intervenues pour diminuer la toxicit (en particulier pulmonaire
et hpatique) de cette association radiochimiothrapique ou
augmenter son activit antileucmique. Ces deux impratifs
sont souvent contradictoires. En outre, des tentatives intressantes ont t ralises, qui visent substituer le busulfan
forte dose lICT.
2
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
Conditionnement avec irradiation corporelle totale. Outre lassociation classique de lICT et du cyclophosphamide, dautres
schmas sont utiliss :
cytarabine (Ara-C) forte dose plus ICT ;
Ara-C forte dose plus ICT plus melphalan ;
ICT plus toposide ;
ICT plus toposide plus cyclophosphamide ;
ICT plus melphalan.
Les avantages thoriques dun conditionnement avec ICT par
rapport un conditionnement purement chimiothrapique
restent :
la meilleure immunodpression ;
latteinte de toutes les cellules tumorales en phase G0 ;
lradication tumorale des sanctuaires ;
la possibilit de moduler les doses dlivres dans certains
organes que lon souhaite protger (du fait du risque de
toxicit) ou que lon souhaite irradier plus fortes doses (du
fait du risque de rechute).
Conditionnement sans irradiation corporelle totale. La lourdeur,
les contraintes et les complications de lICT ont incit certaines
quipes utiliser des conditionnements sans irradiation. Le
busulfan, la dose habituelle de 16 mg/kg chez ladulte pour la
forme orale et de 12,8 mg/kg pour la forme intraveineuse (i.v.),
est alors, le plus souvent associ au cyclophosphamide la dose
de 120 ou 200 mg/kg [6, 7] . Dans les leucmies mylodes
chroniques, les rsultats sont peu diffrents de ceux rapports
avec une association de cyclophosphamide et dune ICT [8]. En
revanche, plusieurs tudes comparant un conditionnement par
busulfan et cyclophosphamide un conditionnement par
cyclophosphamide et ICT, chez des patients atteints de leucmie
aigu, ont montr une mortalit lie la greffe plus importante
chez les patients conditionns par busulfan [7, 9, 10]. De plus,
une tude a rapport une incidence leve de rejet dans les
greffes non apparentes conditionnes par busulfan.
Outre la chimiothrapie et la radiothrapie, les conditionnements de greffe peuvent aussi comporter des anticorps monoclonaux ou des immunotoxines.
Le choix du conditionnement doit prendre en compte deux
risques : celui de la toxicit (immdiate ou retarde) et celui de
la rechute. Cest en fonction de ltat des malades (ge, tat
gnral, comorbidits) et de lhmopathie elle-mme (haut
risque de rechute ou non) que ce choix est fait. Chez le jeune
enfant, lassociation cyclophosphamide-busulfan parat sduisante, car elle est suppose diminuer les squelles endocriniennes observes aprs ICT.
Aplasies mdullaires svres. Dans les aplasies mdullaires,
le conditionnement a pour objectif limmunosuppression. Chez
les patients non immuniss avant la greffe, ce conditionnement
peut comporter le cyclophosphamide seul (50 mg/kg pendant
4 jours) ou une association de cyclophosphamide et de srum
antilymphocytaire [11]. Ladjonction dune irradiation lymphode totale (TLI) peut se discuter chez les malades haut
risque de non-prise.
Dans le cas particulier de la maladie de Fanconi, compte tenu
de la fragilit chromosomique, les doses de chimiothrapie du
conditionnement doivent tre rduites.
Problmes particuliers : greffes non HLA-identiques et
greffes dpltes en lymphocytes T. Toute greffe non strictement HLA-identique entrane, outre un risque lev de GVHD,
un risque accru de non-prise et de rejet. Le risque de non-prise
et de rejet est galement important aprs les greffes dpltes en
lymphocytes T. Ce risque justifie lutilisation de conditionnements plus myloablatifs et surtout plus immunosuppresseurs
(comportant du srum antilymphocytaire, de la fludarabine ou
des anticorps monoclonaux anti-T).
Conditionnement dintensit rduite
La faisabilit dallogreffes conditionnement dintensit
rduite (CIR) a initialement t dmontre dans des modles
animaux [12]. Des modles murins ont montr lintrt de la
fludarabine dans ce type de conditionnement : cette molcule
Myloablation
Cyclophosphamide / ICT 12Gy
Bu / Cyclophosphamide
Cyclophosphamide / ICT 5Gy
Fluda / Mel
Fluda / Bu
Fluda / Mel / Alemtuzumab
Fluda / Bu / SAL
Fluda / Cyclophosphamide
Fluda / ICT 2Gy
ICT 2Gy
Immunosuppression
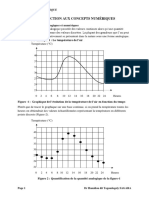
Figure 1. Diffrents types de conditionnements en fonction du degr
dimmunosuppression et de myloablation (daprs [14]) ; Bu : busulfan ;
ICT : irradiation corporelle totale ; Fluda : fludarabine ; Gy : Gray ;
Mel : melphalan ; SAL : srum antilymphocytaire.
est dote dun trs fort potentiel immunosuppresseur avec une
toxicit extrahmatologique rduite [13].
La premire srie de greffes CIR a t rapporte par Slavin
en 1998 [2] ; le conditionnement associait de la fludarabine, du
srum antilymphocytaire et du busulfan dose rduite par
rapport aux conditionnements myloablatifs. Cette premire
srie a montr la faisabilit de ce type dapproche chez
lhomme, en particulier en termes de prise de greffe. Depuis, la
greffe CIR a connu un essor considrable et diffrents types de
conditionnements ont t valus. Certains dentre eux sont
non myloablatifs (ICT 2 Gy + fludarabine), alors que dautres
comportent un certain degr de myloablation (Fig. 1) [2, 14-17].
La plupart de ces conditionnements ont en commun lutilisation dimmunosuppresseurs puissants (la fludarabine, le srum
antilymphocytaire, le mycophnolate moftil) associs des
doses plus ou moins myloablatives de chimiothrapie (busulfan, cytarabine, cyclophosphamide) ou de faibles doses dICT.
ce jour, aucun de ces conditionnements na montr sa supriorit par rapport un autre.
Diffrents types de greffons
Un greffon de CSH allognique peut provenir de trois sources : moelle, sang priphrique ou sang placentaire.
En 2007, 15 % des allogreffes en France ont t ralises
partir de sang placentaire, 33 % partir de moelle osseuse et
52 % de cellules souches priphriques.
Greffon mdullaire
Lors dun prlvement mdullaire, le donneur est ponctionn, sous anesthsie gnrale, dans les crtes iliaques
postrieures et, si besoin, dans les crtes iliaques antrieures et
le sternum. En cours de prlvement, un compte des cellules
nucles sur chantillon permet de calculer un volume
prlever pour assurer un minimum de 3 108 cellules
nucles/kg de poids de receveur.
La moelle est ensuite transfuse au receveur qui a reu le
conditionnement de greffe, si besoin aprs sparation des
hmaties ou dplasmatisation sil existe une compatibilit ABO
entre le donneur et le receveur, ou manipulation immunologique du greffon.
Greffon de cellules souches priphriques
Ds lapparition, au dbut des annes 1990, des facteurs de
croissance hmatopotiques recombinants (G-CSF) permettant
la mobilisation dans le sang des CSH et leur recueil par cytaphrse, cette technique a trs rapidement remplac le prlvement mdullaire pour les autogreffes. En revanche, le recueil de
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
cellules souches priphriques pour la ralisation dallogreffes ne
sest dvelopp que beaucoup plus lentement. Cependant,
depuis les annes 2000, la majorit des allogreffes sont ralises
en France partir de greffons de CSP, et cette source de cellules
souches hmatopotiques est utilise pour environ 80 % des
allogreffes en Amrique du Nord.
Les raisons pour lesquelles lutilisation de greffons de CSP
sest rpandue lentement en situation allognique sont schmatiquement de deux ordres : dune part, ladministration dun
facteur de croissance recombinant un donneur sain posait le
problme dventuelles consquences pour la sant du donneur ; dautre part, les importantes quantits de lymphocytes T
contenues dans les greffons de CSP faisaient craindre un risque
lev de GVHD chez le receveur. Inversement, le prlvement et
ladministration dun nombre de cellules souches plus important que lors dun prlvement mdullaire permettent une
reconstitution hmatopotique plus rapide et une diminution
du risque de non-prise, lment particulirement important
dans les greffes CIR.
Au total, malgr les avantages vidents des greffons de CSP en
termes de facilit de recueil et de raccourcissement de laplasie,
le rapport bnfices-risques de leur emploi a d faire lobjet
dtudes. Ce rapport reste valuer prcisment au cas par cas,
et seul le dveloppement trs rapide des greffes conditionnement non myloablatif a finalement conduit la banalisation
des greffons de CSP dans le contexte de la greffe allognique.
Les techniques utilises pour la constitution dun greffon de
CSP mobilisation des CSH par le G-CSF puis recueil par
cytaphrse expliquent les diffrences quantitatives et qualitatives qui existent entre le contenu cellulaire dun greffon de
moelle et celui dun greffon de CSP. Dune part, le G-CSF
modifie qualitativement certaines cellules de la rponse immunitaire, dautre part, les cytaphrses permettent de recueillir un
plus grand nombre de cellules (cellules souches CD34+, lymphocytes, monocytes) que lors dun prlvement mdullaire. Le
nombre de cellules CD34 + injectes par kg de receveur est
multipli, en moyenne, par un facteur de 3 6 dans un greffon
de CSP par rapport un greffon mdullaire et le nombre de
lymphocytes T par 10 environ. Il existe un intrt certain
lutilisation dun greffon trs riche en cellules souches
CD34+ pour les greffes comportant un risque accru dHVG,
telles que les greffes conditionnements non myloablatifs, les
greffes dpltes en lymphocytes T et les greffes en situation
partiellement HLA-incompatibles.
Allogreffe de cellules souches priphriques
aprs un conditionnement myloablatif
partir de 1995, des tudes pilotes ralises aux tats-Unis et
en Europe ont dmontr la faisabilit des allogreffes de CSP, en
particulier labsence daugmentation majeure de lincidence des
GVHD aigus [18]. Par la suite, dautres tudes ont compar
rtrospectivement, puis prospectivement la moelle et les CSP.
Les questions poses concernaient lintrt des CSP pour la
rapidit de reconstitution hmatopotique, mais surtout
limpact de ce type de greffon sur lincidence de la GVHD aigu
et chronique, la rechute et la survie. Plusieurs tudes prospectives ont randomis lutilisation dun greffon mdullaire ou de
CSP dans des greffes familiales HLA-identiques, aprs un
conditionnement myloablatif [19-22]. Si toutes saccordent pour
conclure une reconstitution hmatopotique plus rapide avec
les CSP, leur impact sur la GVHD aigu ou chronique, la rechute
et la survie est plus difficile dfinir. Schmatiquement, la
majorit de ces tudes ne montre pas daugmentation vidente
de lincidence de la GVHD aigu avec les CSP, mais une tendance une augmentation de la GVHD chronique, mme si les
conclusions sont parfois sujettes caution du fait du nombre
limit de patients inclus [23]. Une mta-analyse portant sur
1 111 patients inclus dans neuf de ces essais prospectifs a permis
de comparer les greffes de CSP et de moelle osseuse dans une
population bien plus large [23]. Cette tude conclut :
labsence de diffrence significative pour lincidence de la
GVHD aigu ;
Incidence de GVHD chronique extensive
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
100
90
80
2 = 27,20
Cellules souches priphriques
p < 0,00001
Moelle
70
60
50,99 %
47,12 %
50
40
30
35,22 %
31,14 %
20
10
0
Annes
Figure 2. Incidence de la maladie du greffon contre lhte (GVHD)
chronique extensive en fonction de la source cellulaire (daprs Stem Cell
Trialists Collaborative Group JCO 2005 [23]).
laugmentation importante de lincidence de la GVHD
chronique extensive avec les CSP, sans impact sur la mortalit
lie la greffe (Fig. 2).
la diminution significative du taux de rechutes aprs greffe
de CSP, particulirement chez les patients greffs un stade
avanc de leur hmopathie.
Au total, le taux de survies sans maladie est suprieur aprs
allogreffe de CSP dans la population des patients haut risque,
mais pas dans celle des patients risque standard. Compte tenu
des consquences de la GVHD chronique sur la qualit de vie,
cette tude inciterait privilgier les greffons mdullaires chez
les patients risque standard et les greffons de CSP chez les
patients haut risque de rechute.
Allogreffe de cellules souches priphriques
aprs des conditionnements dintensit rduite
Depuis la fin des annes 1990, le concept de greffe CIR sest
largement rpandu. Dans ces nouveaux schmas, les cellules
alloractives du greffon (essentiellement des lymphocytes T) se
voient attribuer la fois le rle antitumoral et celui de la
destruction de lhmatopose normale de lhte que jouait
auparavant le conditionnement classique. Le rle propre du
conditionnement est alors rduit au minimum : il sagit seulement dempcher le rejet. Ce type de greffe comporte thoriquement un risque de non-prise suprieur celui des greffes
conditionnement myloablatif. Lusage de greffons de CSP
permet de diminuer ce risque en augmentant la fois le
nombre de lymphocytes T injects (qui jouent ici un rle
essentiel) et le nombre de cellules souches CD34+, ce qui permet
de combattre lHVG. Dans des modles murins, il a en en effet
t tabli depuis longtemps que le nombre de cellules allogniques injectes jouait un rle fondamental pour surmonter le
rejet. Force est de constater que les arguments rationnels pour
utiliser des CSP plutt que de la moelle osseuse pour les greffes
non myloablatives sont apparus aux quipes cliniques concernes suffisamment convaincants pour se dispenser de toute
tude comparative prospective des deux types de greffon.
Impact du contenu cellulaire des greffes de cellules souches
priphriques sur les vnements postgreffe
Une relation entre la quantit de cellules CD34+ injecte et
la dure daplasie granuleuse ou plaquettaire existe sans doute
comme au cours des autogreffes, mais cet effet est de peu
dintrt clinique dans la mesure o les plus petits greffons
contiennent au minimum 4 106 CD34+/kg (quantit gnralement considre comme un objectif minimum atteindre) et
que cette quantit est largement suffisante pour assurer une
sortie daplasie prcoce. Dans ces conditions, le gain dun ou
4
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
deux jours apport par les trs gros greffons (jusqu 20 106
CD34 + /kg), en terme de sortie daplasie granuleuse, est
ngligeable.
La GVHD, survenant aprs greffe de CSP, se distingue de celle
observe aprs greffe de moelle diffrents points de vue :
lincidence de la GVHD aigu nest pas accrue, malgr ladministration de dix fois plus de lymphocytes T, contrairement
celle de la GVHD chronique, souvent extensive et rsistante aux
traitements immunosuppresseurs. Une autre particularit,
actuellement mal explique, est la corrlation tonnante
existant entre lincidence de la GVHD et la dose de cellules
CD34+ injecte, alors que la dose de lymphocytes injecte na
pas dimpact [24-27].
Les explications avances reposent sur lanalyse de leffet du
G-CSF sur les cellules de limmunit : cette molcule entrane la
polarisation des lymphocytes vers un profil de scrtion
cytokinique de type Th-2 (interleuline 4 [IL4] et interleukine 10
[IL10]) [28]. Or, la GVHD aigu est mdie par les lymphocytes
Th-1 (scrtant de lIL2 et de linterfron c), alors que la GVHD
chronique est mdie par les lymphocytes Th-2. Ces travaux
sont conforts par dautres, montrant chez lhomme une
rduction de la prolifration et de la cytotoxicit des lymphocytes T sous leffet du G-CSF. Le G-CSF entrane galement une
diminution de la production de cytokines pro-inflammatoires,
la mobilisation de monocytes suppresseurs de lalloractivit des
lymphocytes T [29], la mobilisation de cellules dendritiques de
type DC-2 qui induisent une rponse T de type Th-2 [30], une
diminution du nombre des progniteurs natural killer (NK)
et de leur cytotoxicit [31]. Ces rsultats permettent de mieux
comprendre les raisons pour lesquelles lutilisation dun greffon
de CSP favorise la survenue dune GVHD chronique plutt
quaigu.
Greffe de sang placentaire
Caractristiques des greffons
Le fondement rationnel des greffes de sang placentaire repose
sur lobservation du fait que les cellules prsentes dans la
circulation du nouveau-n et du placenta sont riches en cellules
souches hmatopotiques. La premire greffe de sang placentaire a t effectue lhpital Saint-Louis Paris en 1988, chez
une enfant atteinte de maladie de Fanconi [32]. Ralise partir
du sang placentaire dune sur HLA-identique prlev la
naissance, elle a dmontr la faisabilit dune telle approche. Il
a t ensuite montr que les cellules contenues dans le sang
placentaire (encore appel sang de cordon par les AngloSaxons) possdent certaines particularits par rapport aux
cellules dun greffon mdullaire. Elles prsentent un plus grand
potentiel de rgnration et une moindre immunoractivit,
permettant de rduire les risques lis lincompatibilit HLA.
Cette seconde caractristique permet la ralisation de greffes de
sang placentaire en situation partiellement HLA-incompatible,
cest--dire permet de greffer des patients qui nont ni donneur
familial ni donneur compatible dans les fichiers de donneurs
non apparents. Il a t ainsi montr quen situation non
apparente, un greffon de sang placentaire HLA-discordant (une
ou deux discordances sur les six antignes HLA-A, -B et -Dr)
tait une source possible de CSH pour une allogreffe chez
lenfant [33-35]. Cependant, la quantit restreinte de cellules
souches contenues dans un greffon de sang placentaire a
initialement limit quasi exclusivement lutilisation de greffon
de sang placentaire aux receveurs pdiatriques.
Depuis une dizaine dannes ont t cres des banques de
sang placentaire pour les greffes non apparentes. Il existait en
2008 environ 350 000 units de sang placentaire congeles dans
le monde, et le nombre de greffes ralises cette date tait
estim plus de 10 000.
Les rsultats des greffes de sang placentaire dpendent de
deux paramtres principaux : la quantit de cellules injectes et
lappariement HLA entre le donneur et le receveur. Ces facteurs
ont un impact majeur sur la prise de greffe et lincidence de la
GVHD [34].
Avantages et inconvnients des greffes dunit de sang
placentaire par rapport aux greffes de donneur
non apparent
Lutilisation dUSP comporte certains avantages :
disponibilit rapide du greffon ;
moindre exigence de compatibilit HLA ;
diminution de lincidence de la GVHD ;
faible risque de transmission dinfections virales ;
risque nul pour le donneur.
En revanche, les inconvnients sont les suivants :
risque accru de non-prise ;
reconstitution hmatopotique plus lente ;
impossibilit dutiliser ultrieurement les cellules du donneur
pour une immunothrapie complmentaire.
Rsultats : comparaison des greffes de sang placentaire
et des greffes de moelle partir de donneurs non apparents
Chez les enfants. Plusieurs tudes ont compar rtrospectivement les greffes de sang placentaire et les greffes de moelle
non apparentes HLA-identiques. Les rsultats de ces tudes
montrent :
une reconstitution hmatopotique plus lente dans les
greffes de sang placentaire ;
une diminution de lincidence de la GVHD ;
des taux de rechutes, de mortalit la greffe et de survie
comparables.
La greffe de sang placentaire apparat comme une alternative
satisfaisante chez les enfants atteints dhmopathies malignes et
qui nont pas de donneurs HLA-identiques [35-37].
Chez les adultes. Trois tudes ont compar, chez ladulte,
lallogreffe de sang placentaire lallogreffe de moelle non
apparente (HLA-compatible ou avec une seule diffrence HLA).
Dans les trois tudes, la reconstitution hmatopotique se
rvle plus lente chez les patients greffs partir dUSP. En
revanche, les donnes sur lincidence de GVHD et la survie sont
discordantes [38-40].
Dans le but damliorer la probabilit de prise du greffon et
de diminuer la dure daplasie et la mortalit prcoce lie la
greffe, des modalits nouvelles de greffe de sang placentaire se
dveloppent : utilisation de deux USP de donneurs diffrents, ou
de conditionnements dintensit rduite [41, 42]. Les rsultats
publis sont encourageants et permettent dtendre largement
les indications de greffe de sang placentaire aux patients
adultes.
Choix du donneur
Si la majorit des allogreffes sont encore ralises partir de
frres ou de surs HLA-identiques, on assiste, depuis le dbut
des annes 1990, une augmentation importante du nombre de
greffes ralises partir dun donneur non apparent ou partir
dUSP. En outre, les techniques de manipulation ex vivo du
greffon permettent denvisager des greffes partir de donneurs
non HLA-identiques.
Frre ou sur gno-identique
Les gnes du systme HLA tant cods par un mme chromosome (le chromosome 6), chaque patient a 25 % de chances
dtre HLA-identique avec un membre de sa fratrie. En labsence
de consanguinit, seuls les frres et surs peuvent tre HLAidentiques entre eux. Lorsquil existe dans la famille du patient
un germain HLA-identique au receveur, ce donneur est choisi en
priorit. Sil existe dans une fratrie plusieurs frres et surs
HLA-identiques avec le patient, le donneur est choisi en
fonction de son statut srologique pour le cytomgalovirus
(CMV) et des facteurs de risque de GVHD chez le receveur (cf.
sous-chapitre consacr la raction du greffon contre lhte).
En France, compte tenu de la taille de la fratrie, 25 % 30 %
seulement des patients justiciables dune allogreffe ont un
donneur HLA-identique dans la fratrie.
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
Donneur non apparent
Pour les patients qui nont pas de donneur familial HLAidentique, une allogreffe peut tre envisage partir dun
donneur non apparent : les fichiers de donneurs volontaires
comptaient, en 2008, environ 13 millions de donneurs. Cependant, les patients originaires de populations peu reprsentes
dans les fichiers ont peu de chance de trouver un donneur. En
2007 en France, environ la moiti des allogreffes ont t
ralises partir dun donneur non apparent.
Le pronostic des patients greffs partir dun donneur non
apparent dpend de la compatibilit HLA entre donneur et
receveur. En raison dune compatibilit moins parfaite quen
situation familiale (gno-identique), les greffes ralises partir
dun donneur non apparent phno-identique comportent
classiquement un risque suprieur de GVHD et dHVG. Cependant, les typages HLA de classe I (HLA-A, -B et -C) et de classe II
(HLA-DR, -DQ, -DP) sont dsormais raliss par des techniques
de biologie molculaire de haute rsolution. La gnralisation de
ces techniques permet un meilleur appariement entre donneur et
receveur et une amlioration du taux de survie des patients [43].
En cas de greffe parfaitement apparie par des techniques de
biologie molculaire de haute rsolution, le taux de survie sans
maladie des patients semble comparable celui observ aprs
greffe gno-identique [44].
la morbidit et la mortalit demeurent leves : la maladie du
greffon contre lhte (GVHD). Les lymphocytes T du donneur
contenus dans le greffon :
jouent un rle important dans la prvention du rejet de
greffe (HVG), en participant la destruction du systme
immunitaire de lhte ;
contribuent de faon significative leffet antitumoral associ
la greffe : leffet du greffon contre la leucmie (GVL).
En outre, le transfert de cellules immunocomptentes du
donneur permet la reconstitution postgreffe dun systme
immunitaire chez le receveur.
Raction du greffon contre lhte (GVHD)
La GVHD est la consquence dinteractions entre des antignes allogniques du receveur, prsents par ses cellules prsentatrices dantignes, et les lymphocytes T matures du greffon.
Cest la complication la plus frquente aprs allogreffe de CSH,
premire cause de mortalit postgreffe. La mortalit lie la
GVHD est non seulement due aux consquences directes de
cette raction, mais surtout aux complications infectieuses
favorises par les traitements immunosuppresseurs ncessaires
pour la traiter. La GVHD est troitement lie la GVL ;
labsence totale de GVHD nest donc pas forcment un objectif
atteindre aprs allogreffe pour hmopathie maligne.
Physiopathologie
Donneur familial non HLA-identique :
HLA-haplo-identique
Quarante pour cent des patients justiciables dune allogreffe
nont ni donneur familial ni apparent HLA-compatible.
Presque tous ont en revanche un donneur potentiel familial
haplo-identique (identique sur un haplotype et diffrent sur
lautre) : parent, enfant, germain. Dans ce type de greffe, il
existe un conflit immunologique majeur entre donneur et
receveur. Ce conflit immunologique existe la fois dans le sens
HVG et dans le sens GVHD. Des travaux exprimentaux, dj
anciens, portant sur des modles murins greffs en situation
haplo-identique, ont tabli que le nombre de CSH injectes tait
le paramtre essentiel de la prise de greffe : plus lincompatibilit HLA est grande, plus la dose injecte doit tre importante [45]. Lutilisation de greffons trs riches en cellules souches
permet maintenant dassurer la prise de la greffe malgr une
T-dpltion majeure ncessaire la prvention de la GVHD. La
pratique de telles greffes sappuie sur trois grands principes [46] :
un conditionnement alourdi et trs fortement immunosuppresseur afin de combattre la raction HVG ;
une prvention de la raction du greffon contre lhte par
une T-dpltion la plus radicale possible du greffon ;
une dose trs leve de cellules CD34 + , provenant dun
greffon de CSP.
Si une telle approche prvient efficacement la GVHD et
lHVG, la dpltion radicale du greffon en lymphocytes T
saccompagne dun profond dficit immunitaire postgreffe et
dun risque de rechute major, surtout dans les situations o le
risque est lev [46, 47]. Cest dans ce type de greffe, partiellement HLA-incompatible, qua t rapport un effet antileucmique d aux cellules NK du donneur (cf. infra).
Ractions immunologiques
lallogreffe de cellules souches
hmatopotiques
Un greffon hmatopotique comprend des cellules souches
capables de reconstituer de faon durable lhmatopose. Il
comprend galement des cellules immunocomptentes susceptibles de reconnatre lhte comme tranger. Cette ractivit
allognique est responsable dune complication importante dont
Trois conditions sont ncessaires au dveloppement dune
GVHD :
le greffon doit contenir des cellules immunocomptentes ;
lhte doit comporter, avec le donneur, des diffrences
dantignes majeurs (antignes HLA) ou mineurs dhistocompatibilit (peptides drivs de protines polymorphiques
codes par des gnes non lis au complexe majeur dhistocompatibilit) capables dtre reconnus comme trangers par
le systme immunitaire du donneur. En dehors de la situation
trs rare de greffes ralises entre vrais jumeaux (greffes
syngniques), il existe toujours des diffrences pour les
antignes mineurs dhistocompatibilit entre le donneur et le
receveur. Cela explique que, mme en situation HLAidentique, il existe un risque de GVHD ;
lhte doit tre suffisamment immunodprim pour tre
incapable de rejeter les cellules du donneur.
La physiopathologie de la GVHD est complexe et encore
imparfaitement connue. Elle fait intervenir limmunit cellulaire
et humorale et des phnomnes inflammatoires, avec de
nombreuses interactions entre ces diffrents types de ractions.
Deux faits sont importants souligner :
la GVHD nest pas une rponse anormale du systme immunitaire. Les lymphocytes du donneur ont un comportement
appropri lenvironnement anormal dans lequel ils se
trouvent ;
les lymphocytes T contenus dans le greffon sont injects dans
un environnement altr par :
C la maladie sous-jacente ;
C les infections ;
C le conditionnement, responsables de phnomnes inflammatoires dans les endothliums et les pithliums.
Les phnomnes infectieux jouent un rle important dans
le dclenchement de la GVHD et expliquent que les
organes cibles de cette raction soient en particulier le tube
digestif et la peau : il existe dans ces cas des endotoxines
ou des bactries responsables de phnomnes inflammatoires qui favorisent le dveloppement de la GVHD.
Physiopathologie de la maladie du greffon
contre lhte aigu
Les cellules du donneur sactivent non seulement vis--vis
dalloantignes du receveur, mais aussi de manire non spcifique. Cela aboutit lactivation et la prolifration de cellules de
linflammation, et laugmentation de lexpression de diffrentes molcules de surface, en particulier de molcules dadhsion,
6
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
I. Conditionnement
Atteinte tissulaire
pithlium et
endothlium
du receveur
IL1
TNF-
CPA
receveur
LPS
Augmentation des
molcules dadhsion
et du CMH
Ly T
Macrophage
TNF-
II. Activation
des lymphocytes T
du donneur
IL1
IL12
Apoptose de
la cellule cible
Th1
CTL
NK
IFN-
IL2
III. Effecteur
Figure 3. Physiopathologie de la maladie du greffon contre lhte
(GVHD) aigu. CPA : cellules prsentatrices dantigne ; CTL : lymphocyte T cytotoxique ; NK : cellules natural killer ; Ly : lymphocyte ;
Th : lymphocyte T helper (auxilliaire) ; LPS : lipopolysaccharide ;
TNF : tumor necrosis factor ; CMH : complexe majeur dhistocompatibilit ; IL : interleukine ; IFN- c : interfron gamma.
de cytokines et de chimiokines [48]. La physiopathologie de la
GVHD aigu peut se dcomposer en trois phases (Fig. 3).
Premire phase : effet du conditionnement. La premire
phase dbute avant la greffe, au moment du conditionnement.
Celui-ci est responsable de lsions tissulaires de lpithlium et
de lendothlium, aboutissant la scrtion, par les cellules de
lhte, de cytokines de linflammation (tumor necrosis factor
alpha [TNF-a] et IL1) et de granulocyte macrophage (GM)-CSF. Les
cytokines entranent une surexpression des molcules dadhsion et des molcules du complexe majeur dhistocompatibilit
(CMH) responsables de la reconnaissance des antignes mineurs
ou majeurs de lhte par les cellules immunitaires du greffon [49]. La translocation des lipopolysaccharides (LPS) travers
la muqueuse intestinale active les cellules du systme immunitaire et favorise la scrtion de cytokines pro-inflammatoires. Le
rle du conditionnement dans linitiation de la GVHD explique
que la frquence de la GVHD augmente avec la lourdeur du
conditionnement et que le risque de GVHD soit moins important aprs un conditionnement non myloablatif ou lorsque les
lymphocytes du donneur sont injects distance du conditionnement (aprs 30 45 jours).
Deuxime phase : activation des lymphocytes T du donneur. Lactivation des lymphocytes T du donneur inclut la
prsentation de lantigne, lactivation propre des lymphocytes,
leur prolifration et leur diffrenciation en cellules effectrices.
Les alloantignes sont prsents par les cellules prsentatrices
dantignes du receveur aux lymphocytes T du donneur. Avec le
premier contact antigne/rcepteur du lymphocyte T, les
molcules de costimulation et dadhsion jouent un rle
important dans le phnomne dactivation lymphocytaire. Ces
phnomnes aboutissent une transcription des gnes de lIL2,
de lIL12, de lIFN-c, et de leurs rcepteurs. Les cytokines
produites en rponse cette stimulation sont principalement de
type Th1 (IFN-c, IL2). Ces cytokines jouent un rle central :
dans lactivation, la prolifration et linduction de la cytotoxicit T du donneur ;
dans la rponse NK du donneur ;
dans lactivation des cellules phagocytaires de lhte et du
donneur, aboutissant la scrtion dIL1 et de TNF-a.
La phase dactivation lymphocytaire T est suivie dune phase
dexpansion et de diffrenciation.
Paralllement, les chimiokines jouent un rle fondamental
dans la GVHD, en induisant la migration des lymphocytes T
vers les organes cibles. Elles interviennent diffrentes tapes.
Lactivation des lymphocytes T du donneur en rponse aux
alloantignes du receveur saccompagne de lexpression leur
surface des rcepteurs de chimiokines et de la scrtion de
cytokines pro-inflammatoires. Ces cytokines vont induire la
production de chimiokines par le foie, la peau, les poumons,
qui sont les organes cibles de la GVHD et secondairement la
migration des lymphocytes T, exprimant leurs rcepteurs depuis
les organes lymphodes vers les organes cibles de la GVHD [50].
Troisime phase : effecteurs de la raction. Il sagit de la
phase la plus complexe et la moins bien connue. Les lymphocytes T cytotoxiques ne sont probablement pas responsables de
la totalit des atteintes tissulaires observes et, dans plusieurs
modles animaux, il a t montr que les cellules NK taient
galement des effecteurs importants de la GVHD. Les lymphocytes T cytotoxiques et les cellules NK induisent lapoptose des
cellules cibles. Les cellules phagocytaires, stimules soit par les
cytokines de type Th1, soit par des LPS, librs par les muqueuses intestinales de lhte lses par le conditionnement, scrtent des cytokines de linflammation (IL1 et TNF-a). Le TNF-a
peut induire directement la ncrose des cellules cibles ou
intervenir dans les phnomnes dapoptose. En outre, le
monoxyde dazote (NO), produit par les macrophages activs,
est galement responsable de lsions des tissus cibles de la
GVHD. La mort des cellules cibles fait intervenir trois mcanismes principaux : la voie granzyme-perforine, la voie Fas et de
son ligand, et la toxicit directe des cytokines.
Physiopathologie de la maladie du greffon contre lhte
chronique
Les mcanismes et la prsentation clinique de la GVHD
chronique se rapprochent de ceux de lauto-immunit. Dans des
modles animaux, il a t montr que, si les lymphocytes T
impliqus dans la GVHD aigu taient spcifiques dalloantignes, ceux impliqus dans la GVHD chronique pouvaient
reconnatre des antignes publics. Ces lymphocytes T produisent des cytokines de type Th2 : IL4 et IL10. Ces cytokines
peuvent entre autres stimuler la production de collagne par les
fibroblastes [51].
Classification
Traditionnellement, la dfinition de la GVHD aigu et
chronique tait fonde sur sa date de dbut : avant 100 jours
postgreffe pour la GVHD aigu et aprs pour la GVHD chronique. Depuis le dveloppement des greffes CIR et des greffes de
CSP, cette dfinition est moins valide : certaines GVHD de dbut
tardif se manifestent comme des GVHD aigus ; linverse,
certains patients prsentent avant j100 des manifestations
voquant une GVHD chronique. Une confrence de consensus
du National Institutes of Health (NIH) amricain a propos une
classification tenant compte la fois des symptmes et de la
date de dbut [52].
Raction aigu du greffon contre lhte :
diagnostic et traitement
Aprs une greffe de moelle conditionnement myloablatif,
la frquence de la GVHD aigu est maximale entre les deuxime
et quatrime semaines postgreffe, mais elle peut se dclarer
pendant les trois premiers mois qui suivent la greffe. Aprs une
greffe de CSP et/ou conditionnement dintensit rduite, des
manifestations de GVHD aigu peuvent survenir aprs
j100 postgreffe.
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
Figure 4. Maladie du greffon contre lhte cutane grade 1 (A), grade 4 (B).
Tableau 1.
Stade de svrit de la maladie du greffon contre lhte (GVHD) aigu par organe (Glucksberg).
Stade
Peau
Foie
Intestin
ruption maculopapuleuse touchant moins de 25 %
de la surface corporelle
Bilirubine 2-3 mg/dl
(34-50 m/l)
Diarrhe > 500 ml/j ou nause, anorexie ou vomissement
avec confirmation dune GVHD dans le tractus
gastro-intestinal haut par biopsie
ruption maculopapuleuse touchant 25 %
50 % de la surface corporelle
Bilirubine 3,1-6 mg/dl
Diarrhe > 1 000 ml/j
ruption maculopapuleuse touchant plus de 50 %
de la surface corporelle
Bilirubine 6,1-15 mg/dl
rythrodermie gnralise avec formation de bulles
et desquamation
Bilirubine >15 mg/dl
Diarrhe > 1 500 ml/j
(> 255 m/l)
+ douleurs abdominales
(51-102 m/l)
Diarrhe > 1 500 ml/j
(103-255 m/l)
ilus
Manifestations cliniques
La peau, le foie et le tube digestif en sont les organes cibles.
Latteinte cutane, en gnral inaugurale, ralise un rythme
morbilliforme parfois prurigineux, prdominant sur le visage, les
faces dextension des membres, le thorax, et surtout les paumes,
les plantes et les rgions rtro-auriculaires. Son volution,
souvent enraye par le traitement, peut se faire vers la diffusion
des lsions qui deviennent confluentes et pourpres. un stade
de plus peuvent apparatre, plus rarement, des dcollements
cutans, dabord localiss et provoqus (signe de Nikolsky), puis
diffus et spontans, ralisant une authentique pidermolyse
(Fig. 4).
Latteinte digestive se manifeste par une diarrhe subaigu,
dintensit variable, parfois dysentriforme, associe ou non
des douleurs abdominales. La surinfection, les hmorragies
associes, la dnutrition peuvent mettre en jeu le pronostic
vital.
Latteinte hpatique, en rgle plus tardive, est surtout
biologique, associant des degrs variables cytolyse et surtout
cholestase, mais en rgle sans insuffisance hpatocellulaire.
La classification de la GVHD aigu est ralise en fonction du
nombre et de la svrit des localisations de la maladie.
Glucksberg, ds 1974, a publi la premire classification, dans
laquelle un score de 1 4 est donn chaque organe en
fonction de la svrit de latteinte (Tableau 1), et le score global
de I IV tient compte de latteinte de lensemble des organes
et de ltat gnral (Tableau 2). Il est classique de sparer les
grades II-IV cliniquement significatifs et ncessitant un traitement, des grades I-II [53]. Plus rcemment, lInternational Bone
Marrow Transplant (IBMTR) a propos une autre classification
galement corrle au pronostic (Tableau 3).
Diagnostic
En fonction de la symptomatologie peuvent se discuter :
les toxidermies ou les ruptions virales pour les atteintes
cutanes ;
les hpatites mdicamenteuses ou virales, la maladie veinoocclusive hpatique, pour les atteintes hpatiques ;
Tableau 2.
Grade de svrit de la maladie du greffon contre lhte (GVHD) aigu
(Glucksberg).
Grade
Atteinte par organe
Peau : 1 2
II
Peau : 1 3
Intestin et/ou foie : 1
Altration modre de ltat gnral
III
Peau : 2 3
Intestin et/ou foie : 2 3
Altration marque de ltat gnral
IV
Peau : 2 4
Intestin et/ou foie : 2 4
Altration majeure de ltat gnral
les diarrhes infectieuses pour les atteintes digestives.
Le diagnostic est orient par lassociation des symptmes et
leur date de survenue.
Au plan histopathologique, les lsions cutanes ne sont
typiques qu partir du 20e jour aprs la greffe. Auparavant, elles
sont difficiles distinguer des lsions toxiques dues au conditionnement ou des lsions infectieuses. partir du 20e jour, les
principales lsions sont composes de foyers de ncrose avec
vacuolisation des cellules basales de lpiderme, ddme et
dun infiltrat inflammatoire lymphocytaire du derme superficiel.
Latteinte hpatique se traduit au dbut par des foyers de
ncrose osinophile, une dgnrescence des canaux biliaires,
une hypertrophie des cellules de Kppfer et des infiltrats
lymphocytaires pribiliaires.
Latteinte digestive se caractrise, sur le plan macroscopique,
par une muqueuse inflammatoire, sige de lsions rosives,
dexsudats tendance hmorragique. Anatomiquement, les
lsions histologiques associent une atrophie villositaire, une
ncrose cellulaire des cryptes, une infiltration lymphocytaire de
8
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
Tableau 3.
Score de svrit de la maladie du greffon contre lhte (GVHD) aigu selon lInternational Bone Marrow Transplant (IBMTR).
Peau
Foie
Intestin
Index
Stade maximal
Surface atteinte
Stade maximal
Bilirubine (mol/l)
Stade maximal
Diarrhe (ml/j)
< 25 %
< 34
< 500
25-50 % ou
1-2
34-102
1-2
550-1 500
> 50 % ou
103 255 ou
> 1 500
Dcollement ou
> 255 ou
Ilus
la lamina propria voluant vers la formation de micro-abcs,
voire dune ncrose complte focale ou diffuse de la couche
muqueuse.
Incidence
Avec les techniques classiques de prvention de la GVHD, et
selon les sries, 25 % 75 % des patients allogreffs partir
dun frre ou dune sur HLA-identique prsentent une GVHD
aigu. Le taux de mortalit des GVHD de grade III ou IV peut
atteindre 90 %. Certains facteurs favorisent la survenue dune
GVHD :
lge lev du receveur ;
les femmes donneuses (surtout en cas de grossesses antrieures et si le receveur est un homme) ;
les greffes ralises en pousse de lhmopathie ;
lutilisation dun conditionnement alourdi ;
les infections aprs la greffe, en particulier les ractivations
de CMV ;
la disparit HLA ;
le type de greffon : les greffes ralises partir de sang
placentaire saccompagnent moins frquemment de GVHD
que les greffes ralises partir de la moelle ou de CSP. Cela
sexplique par la navet du systme immunitaire des greffons
de sang placentaire.
Traitement prventif
La frquence et la gravit de la GVHD aigu imposent un
traitement prventif systmatique, sauf en cas de greffe syngnique (dun donneur jumeau monozygote). Habituellement, le
traitement prventif consiste en lutilisation dun traitement
immunosuppresseur aprs la greffe.
Immunosuppression postgreffe. Lassociation de ciclosporine A et de mthotrexate est, depuis plus de 20 ans, considre
comme la prophylaxie de rfrence [54] dans les greffes
conditionnement myloablatif. Plus rcemment, le tacrolimus
(FK 506) et la rapamycine ont galement t valus, avec des
rsultats intressants [55, 56]. Lintrt du mycophnolate moftil,
en association de la ciclosporine, est actuellement bien
document dans les greffes conditionnement non
myloablatif [16].
Le srum antilymphocytaire utilis dans le conditionnement
pour prvenir le rejet joue galement un rle dans la prvention
de la GVHD en raison de sa dure de vie responsable dune
dpltion T du greffon in vivo.
Alors que la corticothrapie est le traitement curatif de
premire intention dans les GVHD aigus, son intrt pour le
traitement prventif est controvers [57].
Manipulation du greffon avant la greffe. Il a t prouv
que llimination des lymphocytes T du greffon tait un moyen
trs efficace de prvention de la GVHD aigu et chronique [58].
Actuellement, la dpltion en lymphocytes T se fait le plus
souvent par slection positive des cellules CD34+. Cette technique est principalement utilise dans les greffes haut risque de
GVHD.
Lutilisation de techniques de dpltion T prsente trois
inconvnients principaux [59] :
une incidence de rechute plus leve, labolition de la GVHD
saccompagnant dune abolition de leffet GVL ;
une augmentation de non-prise ou de rejet ;
une aggravation du dficit immunitaire postgreffe.
Traitement curatif
Le traitement curatif est indiqu pour les GVHD de grade
suprieur ou gal II. En effet, les GVHD peu svres ne sont
souvent pas traites, pour prserver leffet GVL. Les corticodes
sont initialement employs la dose de 2 mg/kg par jour de
mthylprednisolone. Une rponse complte est obtenue chez
25 % 40 % des patients prsentant une GVHD de grade II
IV. Il nexiste actuellement pas de consensus quant au traitement de seconde ligne proposer en cas dchec de la corticothrapie. Si le taux de rponses compltes alors obtenues parat
assez important (entre 35 % et 70 %), le taux de survie 1 an
est infrieur 30 % dans la plupart des tudes, principalement
en raison des complications infectieuses favorises par les
traitements immunosuppresseurs. Les traitements de seconde
ligne actuellement valus sont : la corticothrapie haute dose
jusqu 10 20 mg/kg/j pendant 2 5 jours, le srum antilymphocytaire, les anticorps monoclonaux antircepteur de lIL2,
les anticorps anti-TNF, le mycophnolate moftil (MMF), la
rapamycine, la photothrapie extracorporelle, linjection de
cellules msenchymateuses allogniques [60-66].
Raction chronique du greffon contre lhte :
diagnostic et traitement
Elle apparat en rgle partir du troisime mois, mais parfois
plus tt, et les formes prcoces, voire subaigus ne sont pas
exceptionnelles.
Description
En raison de la multiplicit des organes cibles possibles, le
tableau clinique est dun grand polymorphisme [67]. La symptomatologie est celle dune maladie auto-immune. Gnralement,
la GVHD chronique est prcde, avec ou sans intervalle libre,
dune GVHD aigu, mais elle peut galement apparatre de
novo.
Latteinte cutane est quasi constante : elle est constitue de
zones dhyper- et/ou dhypopigmentation, le plus souvent
planes (type lichen plan) ou associes des papules plus ou
moins squameuses. Il peut sagir dun rythme diffus associ
une desquamation intense. Le lichen plan peut voluer vers une
forme sclroatrophique, puis vers dauthentiques lsions de
sclrodermie avec atteinte tendineuse et articulaire.
Latteinte des muqueuses, frquente sur la langue, les gencives,
la face interne des joues, comporte des lsions lichniennes
associes un syndrome sec buccal, oculaire et gnital. Une
atteinte sophagienne, sreuse ou articulaire peut y tre
associe.
Latteinte hpatique, au moins au plan biologique, est trs
frquente (95 % des cas). Elle se traduit par une cytolyse
dintensit variable, le plus souvent modre, associe une
importante cholestase responsable ou non dun ictre.
Latteinte bronchique nest pas exceptionnelle, il sagit dune
bronchiolite oblitrante. Elle se manifeste initialement par une
atteinte obstructive des bronches distales, avec, au scanner, des
images de bronchectasies. Latteinte bronchique de la GVHD
chronique est relativement rsistante au traitement et peut
voluer vers une insuffisance respiratoire terminale. La dtection
prcoce de cette complication en amliore peut-tre le pronostic [68].
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
Tableau 4.
Classification de la maladie du greffon contre lhte (GVHD) chronique
(daprs [69]).
Grade
Type datteinte
Limit
Atteinte cutane localise et/ou atteinte hpatique
Extensif
Atteinte cutane gnralise ou
Atteinte cutane localise, ou atteinte hpatique,
plus lune des atteintes suivantes :
histologie hpatique montrant une hpatite
chronique agressive, une ncrose ou une cirrhose ou
atteinte oculaire (Schirmer < 5 mm) ou
atteinte salivaire ou buccale dmontre par biopsie ou
atteinte de tout autre organe
Latteinte des autres organes est variable dans sa frquence et sa
svrit : latteinte digestive, avec malabsorption, est plus rare
que dans la GVHD aigu. La GVHD chronique est souvent
associe des cytopnies.
Le tableau clinique de GVHD chronique est voisin de pathologies auto-immunes dcrites en dehors de la greffe de moelle, tels
que le lupus, le syndrome de Sjgren, la cirrhose biliaire
primitive, la sclrodermie.
Au plan biologique, une hyperosinophilie est frquente.
Plusieurs types danticorps antitissus ont t dcrits : anticorps
antinoyaux, antimuscle lisse, antimitochondries, antithyrodiens. Il existe une hypo- ou une hyperglobulinmie, avec
frquemment un profond et durable dficit en immunoglobulines A (IgA) associ un dficit en IgG2 et IgG4. Limmunopathologie des lsions cutanes ou labiales rvle des dpts dIgM
et de complment le long des membranes basales.
La GVHD chronique est classiquement classe en forme
limite et en forme extensive (Tableau 4), mais une nouvelle
classification rendant compte du nombre et de la svrit des
sites atteints a t propose par le NIH amricain.
Incidence et facteurs favorisants
Pour le mme type de conditionnement, la GVHD chronique
est plus frquente aprs greffe de CSP quaprs greffe de moelle.
Dans une population de greffes familiales HLA-identiques, avec
un conditionnement myloablatif, lincidence de la GVHD
chronique 3 ans a t de 51 % pour la moelle et de 67 % pour
les CSP et respectivement de 31 % et 47 % pour les formes
extensives [23] (Fig. 2). La topographie des lsions parat similaire
dans les deux types de greffe, y compris les manifestations
hpatiques et pulmonaires, avec cependant une tendance
latteinte cutane sclrodermiforme plus tendue, latteinte
oculaire et latteinte vaginale plus frquente pour les CSP.
Lautre caractre spcifique de la GVHD chronique post-CSP
concerne sa rsistance particulire aux traitements habituels.
Limpact de cette maladie rsistante sur la qualit de vie des
patients peut tre illustr par le temps mdian pour obtenir un
index de Karnofsky 90 % aprs GVHD chronique, qui est de
6 mois dans le groupe moelle et de 12 mois dans le groupe
CSP [70, 71].
La GVHD chronique succde souvent une GVHD aigu,
avec ou sans intervalle libre, mais elle peut apparatre de novo
surtout aprs les greffes de CSP. Les facteurs favorisants sont
lge lev, la prexistence dune GVHD aigu et lutilisation de
CSP comme source de CSH.
Prvention et traitement
La meilleure prvention de la GVHD chronique est celle de
la GVHD aigu. Le traitement de rfrence de la GVHD chronique, depuis 20 ans, est en premire intention une association de
ciclosporine A et de corticothrapie [72]. Il nexiste actuellement
pas de standard pour le traitement de seconde ligne. De
nombreux traitements sont utiliss : lazathioprine, la thalidomide, le mycophnolate moftil, la rapamycine [73], le rituximab
(anticorps monoclonal anti-CD20) [74]. En outre, la photothrapie extracorporelle a montr une certaine efficacit principalement dans les formes sclrodermiformes [75]. Malgr cela, 10 %
15 % des malades atteints de GVHD chronique meurent de
complications infectieuses secondaires limmunosuppression
induite par la GVHD chronique elle-mme ou par ses
traitements.
Voies actuelles de dveloppement
dans le traitement de la maladie du greffon
contre lhte
La dpltion ex vivo des lymphocytes T du greffon permet de
diminuer fortement lincidence de la GVHD, mais augmente
lincidence du rejet et aggrave le dficit immunitaire postgreffe
responsable de complications infectieuses. La ralisation de
greffes dpltes spcifiquement en lymphocytes T alloractifs
du greffon devrait permettre de prvenir la GVHD sans entraner de dficit immunitaire svre. Cest dans ce but que
plusieurs quipes ont dvelopp, dabord in vitro et dans des
modles animaux, des stratgies consistant stimuler et
activer spcifiquement ex vivo les lymphocytes T alloractifs du
greffon en les mettant en prsence de cellules mononucles
irradies du receveur. Les lymphocytes alloractifs sont ensuite :
tris et limins [76] ;
dtruits par lutilisation dune immunotoxine dirige contre
le rcepteur de linterleukine 2 [77] ou anergiss par lutilisation de cytotoxic T lymphocyte antigen (CTLA)-4-Ig [78].
Ces techniques permettent de prvenir efficacement la
GVHD, mais leur intrt est encore difficile apprcier en
termes de rapidit et de qualit de reconstitution immunitaire.
Non-prise et rejet de greffe
La non-prise peut tre lie un rejet ou une inhibition
toxique ou virale de lhmatopose.
Le rejet (HVG) est d la persistance, aprs le conditionnement, de lymphocytes T de lhte capables de sactiver et de
rejeter le greffon. Il a t montr quil existe alors, temporairement, un chimrisme mixte, cest--dire la cohabitation de
cellules hmatopotiques de lhte et du donneur.
LHVG est une complication rare (moins de 2 %) aprs greffe
de moelle gno-identique utilisant un conditionnement myloablatif et en labsence de manipulation ex vivo du greffon. En
revanche, elle est favorise par :
la disparit HLA entre donneur et receveur ;
lutilisation dun conditionnement non myloablatif ;
lutilisation dun greffon pauvre en cellules CD34+ comme
dans les greffes de sang placentaire o le risque de non prise
est suprieur celui observ aprs les greffes de CSP ou les
greffes de moelle ;
la dpltion en cellules T du greffon.
Dans les situations haut risque dHVG, diffrentes techniques de prvention sont utilises [79] :
modifications du conditionnement, rendu davantage immunosuppresseur afin de dtruire les lymphocytes T rsiduels de
lhte (utilisation de srum antilymphocytaire, danticorps
monoclonaux anti-T, etc.) ;
augmentation du nombre de cellules souches CD34+ contenues dans le greffon par lutilisation dun greffon de cellules
souches priphriques plus riche en cellules CD34+ quun
greffon mdullaire.
En cas de rejet, des secondes greffes ont t ralises avec
succs. Il parat alors prfrable de choisir un greffon de CSP,
plus riche en CSH, plutt quun greffon mdullaire.
Raction du greffon contre la leucmie
Lide que lalloractivit puisse gnrer un effet antileucmique a t suggre dans un modle murin de leucmie o le
taux de rechutes aprs greffe syngnique est suprieur celui
observ aprs greffe allognique. Chez lhomme, leffet greffon
10
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
contre la leucmie (GVL) est troitement corrl la GVHD : le
taux de rechutes de la leucmie est moindre chez les patients
atteints dune GVHD aigu et/ou chronique [80]. Leffet GVL est
observ mme en labsence de GVHD clinique comme lindique
le taux de rechutes plus lev aprs une greffe allognique
comportant une dpltion des lymphocytes T quaprs une
greffe allognique standard, mme en labsence de GVHD
patente [81].
La physiopathologie de la GVL nest quimparfaitement
connue. Des questions restent poses au sujet des cibles et des
effecteurs exacts de cette raction, et donc de la possibilit de
dissocier la GVL et la GVHD. Il est probable que la rponse
dpende principalement de lantigne cible en cause. Si lantigne impliqu dans leffet GVL est spcifique de la cellule
tumorale ou dexpression restreinte au tissu hmatopotique,
GVL et GVHD sont potentiellement sparables. En revanche, si
lantigne reconnu est un antigne mineur ou majeur dhistocompatibilit, leffet GVL est proportionnel lintensit de la
GVHD. Dans la leucmie mylode chronique (LMC), une cible
vidente pourrait tre la protine de fusion BCR-ABL. Les
lymphocytes T contenus dans le greffon sont probablement les
effecteurs de la GVL, car celle-ci diminue aprs dpltion T du
greffon.
Dans des greffes ralises en situation dhisto-incompatibilit
partielle, les cellules NK du donneur pourraient tre responsables dun effet GVL. En effet, dans ce type de greffe, labsence
dinteraction entre les rcepteurs inhibiteurs des cellules NK du
donneur (KIR) et les molcules HLA de classe I exprimes la
surface des cellules leucmiques du receveur permet la lyse des
cellules leucmiques par les cellules NK du donneur.
Limportance de leffet antitumoral des cellules NK dans ce
type de greffe a t rapporte par lquipe italienne de
Prouse [82], mais na pas t confirme dans notre exprience,
en raison de limmaturit des cellules NK en priode postgreffe
prcoce [47].
Si les cibles et les effecteurs de la GVL ne sont quimparfaitement connus, limportance de ce phnomne est cependant
bien tablie chez lhomme. Elle justifie lutilisation de la greffe
de CSH allognique dans le traitement des hmopathies malignes. Lefficacit clinique de leffet GVL dpend du type
dhmopathie maligne. Il parat trs important dans la LMC :
environ 15 % des patients greffs en phase chronique avec une
moelle non manipule rechutent contre plus de 70 % lorsque
le moelle est T-dplte. Leffet GVL semble moins important
dans les leucmies aigus mylodes et surtout lymphodes.
Lexistence dun effet GVL justifie la mise en uvre de perfusions de lymphocytes du donneur pour traiter les rechutes
postallogreffe (cf. infra).
tumoraux. Durant les premiers mois postgreffe, les lymphocytes T
proviennent en majorit de lexpansion des lymphocytes T
matures du greffon et les phnomnes de diffrenciation/
maturation partir des progniteurs rinjects restent minoritaires. La rapparition dune population nave tmoignant dune
diffrenciation partir des cellules souches survient chez ladulte
au-del d1 an postgreffe [83-85]. Ce phnomne est plus prcoce
chez lenfant en raison de la persistance du thymus. En cas de
greffe dplte en lymphocytes T ex vivo, la lymphopnie est
plus prolonge. linverse, la reconstitution immunitaire est plus
rapide aprs greffe de CSP quaprs greffe de moelle, probablement en raison du plus grand nombre de lymphocytes apports
par le greffon. La reconstitution immunitaire lymphocytaire est
plus longue aprs greffe de sang placentaire, peut-tre en raison
de la navet du systme immunitaire contenu dans le
greffon [86].
La majorit des patients perdent leur immunit vaccinale,
acquirent mal celle du donneur et doivent tre revaccins aprs
la greffe.
Ltude des sous-populations lymphocytaires permet de
montrer quil existe, aprs greffe familiale HLA-identique non
manipule, une lymphopnie CD4 pendant les six premiers
mois alors que le taux des lymphocytes CD8 et des cellules NK
redevient plus rapidement normal [83, 84].
Il existe en outre un dficit lymphocytaire qualitatif durant
les premiers mois postgreffe, mis en vidence par :
lutilisation de tests fonctionnels de prolifration et de
cytotoxicit ;
ltude de la production des cytokines ;
ltude de la transduction du signal ou ltude de la diversit
du rpertoire T [84].
Le dficit immunitaire postgreffe est major :
par lutilisation de traitements prventifs et curatifs de la
GVHD, dont la dpltion lymphocytaire T ex vivo ;
par la GVHD elle-mme ;
par lexistence dune disparit HLA entre le donneur et le
receveur.
Dficit immunitaire
Durant cette priode, la neutropnie, laltration de la barrire
digestive secondaire au traitement chimio- et/ou radiothrapique, lutilisation de cathters centraux sont autant de facteurs
contribuant au risque infectieux. Durant laplasie, la symptomatologie est souvent pauvre du fait de labsence de signe inflammatoire, et la fivre est souvent le seul signe dinfection. Le
pourcentage de fivre cliniquement ou microbiologiquement
documente varie selon les tudes entre 20 % et 65 %. Les
points dappel cliniques les plus frquents sont les foyers
pulmonaires, les infections des sites de cathter, les infections
point de dpart buccal ou pharyng.
Les infections trs prcoces aprs le dbut de laplasie sont
essentiellement des infections bactriennes alors que les
infections fongiques sont plus tardives.
Infections bactriennes.
Documentation microbiologique. Parmi les infections bactriennes documentes, environ 70 % sont dues des cocci Gram
positif (CGP) (principalement staphylocoques coagulase
ngative en rapport avec lutilisation de cathters veineux
centraux) et 30 % sont dues des bacilles Gram ngatif
(BGN) : entrobactries ou pyocyaniques (dont la plupart
proviennent du tube digestif). Plusieurs facteurs peuvent
expliquer lmergence croissante des infections CGP : lutilisation de voies veineuses centrales pour les staphylocoques
Il existe, schmatiquement, deux types de dficit immunitaire
aprs une allogreffe de CSH. Durant la phase prcoce, cest--dire
durant la priode de neutropnie secondaire au conditionnement,
il sagit dun dfaut de limmunit non spcifique qui saccompagne dun risque dinfections bactriennes et fongiques. Plus
tardivement surviennent les complications infectieuses en rapport
avec le dficit de limmunit spcifique. Le dficit de limmunit
spcifique postgreffe sexplique par les phnomnes suivants :
destruction du systme immunitaire du receveur par le
conditionnement de greffe ;
administration au receveur dun traitement prventif ou
curatif de la GVHD ;
immunosuppression induite par la GVHD.
La reconstitution immunitaire lymphocytaire postgreffe est
due aux cellules immunitaires du donneur contenues dans le
greffon ; durant les premiers mois postgreffe, ces cellules
prsentent un dficit qualitatif et quantitatif.
Mcanismes de la reconstitution immunitaire
lymphocytaire postgreffe
La reconstitution dune immunit spcifique aprs greffe de
CSH est lente, exposant les patients des risques infectieux et
Complications infectieuses
Pendant les premires semaines postgreffe, cest--dire
pendant la priode daplasie, le risque est celui dinfections
bactriennes et fungiques. Les infections virales ou microorganismes tels que Toxoplasma gondii ou Pneumocysti jiroveci
(anciennement carinii) surviennent en gnral plus tardivement
et sont dautant plus frquentes que le dficit de limmunit
spcifique est profond.
Prcoces (durant la priode daplasie) [87]
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
11
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
coagulase ngative et lutilisation de conditionnements de greffe
lourds, responsables dune toxicit muqueuse importante pour
les infections streptocoques.
Documentation clinique. Les infections pulmonaires sont
frquentes. Durant laplasie, la radiographie est parfois normale
malgr linfection, le foyer napparaissant qu la sortie daplasie. Le lavage bronchoalvolaire avec brossage endobronchique
est souvent peu contributif chez les patients neutropniques
sous antibiothrapie large spectre.
Les lsions anorectales peuvent tre le point de dpart de
cellulites extensives et ncrosantes.
La bouche est souvent le sige dune mucite importante et
peut tre le point de dpart dinfection streptococcique,
herptique ou candidosique.
Le tube digestif est souvent le point de dpart dinfection
BGN. Les coprocultures rgulires peuvent mettre en vidence
une prolifration bactrienne intestinale lorigine dune
dissmination hmatologique. Une dcontamination digestive
par des mdicaments non absorbables permet de diminuer
lincidence des septicmies BGN.
Conduite tenir. En raison du risque vital que reprsente une
infection chez laplasique, linstauration dune antibiothrapie,
en cas de fivre, est une urgence. Lantibiothrapie doit :
tre dirige contre les micro-organismes les plus immdiatement dangereux (les bacilles Gram ngatif) ;
tre rapidement bactricide ;
prsenter le moins de risque de slection de rsistance et
donc comporter idalement une association synergique.
Lassociation dune btalactamine active sur les BGN et dun
aminoside reste lassociation de rfrence en premire intention.
Infections fongiques. Le risque dinfection fongique augmente avec la dure daplasie. En labsence de traitement
prventif ou premptif, le risque est denviron 20 % si la dure
de la neutropnie est infrieure 20 jours, il atteint 40 % si elle
est suprieure 20 jours. Les champignons les plus souvent en
cause sont Candida et Aspergillus. Les infections fongiques
peuvent survenir galement au-del de la priode daplasie,
principalement chez les patients atteints de GVHD et traits par
corticothrapie.
Infection Candida. Le premier signe clinique reste souvent
la fivre inexplique, rsistante aux antibiotiques antibactriens.
Pour cette raison, la persistance de la fivre 48 72 heures aprs
une 2e ligne dantibiothrapie conduit la plupart des quipes
ajouter de faon empirique un traitement antifongique
systmique.
Le tube digestif peut tre le point de dpart dune candidose
systmique responsable de localisations cutanes, pulmonaires,
rnales, cardiaques, hpatiques ou musculaires.
Infection Aspergillus. Cest, par ordre de frquence, le
deuxime agent fongique responsable dinfections chez les
patients allogreffs. La voie de contamination la plus habituelle
est linhalation de spores. La prvention repose sur lisolement
des patients dans des chambres haut renouvellement dair
filtr. Les localisations les plus frquentes sont pulmonaires et
sinusiennes. La dissmination hmatogne peut tre responsable
de localisations crbrales, hpatiques, splniques, digestives. Les
signes vocateurs sont la fivre rsistant une antibiothrapie
large spectre, la toux, la dyspne, ventuellement des douleurs
thoraciques. La radiographie de thorax et le scanner pulmonaire
montrent des infiltrats avec souvent un aspect de halo et parfois
des images en grelot , quasi pathognomoniques. Les spores
aspergillaires sont inconstamment retrouves dans le produit de
lavage bronchoalvolaire. En revanche, la positivit de lantignmie aspergillaire chez un patient risque est dun grand
apport diagnostique.
Complications infectieuses tardives
Infections virales. Le dficit de limmunit spcifique se
traduit par une frquence leve dinfection par les virus du
groupe herps (CMV, Epstein-Barr virus [EBV], human herpes virus
1 [HHV-1], human herpes virus 2 [HHV-2], varicelle zona virus
[VZV], human herpes virus 6 [HHV-6]) [88].
Les infections CMV surviennent chez 60 % des patients
sropositifs avant la greffe et chez 30 % des patients srongatifs
greffs partir dun donneur sropositif. Le virus peut tre
lorigine dune maladie CMV (en particulier pneumopathie ou
colite) potentiellement mortelle en labsence de traitement.
Actuellement, la dtection des ractivations du CMV par
antignmie ou polymerase chain reaction (PCR) permet un
diagnostic prcoce et un traitement premptif (par ganciclovir
ou foscavir), ce qui a conduit une diminution importante de
la morbidit et de la mortalit due au CMV [89]. Si la plupart des
infections CMV sont actuellement contrles par ces mdicaments, il persiste des situations de dficit immunitaire profond
o le CMV peut tre responsable dune infection chronique
difficilement contrlable par les antiviraux. Dans ces situations,
le transfert de clones de lymphocytes T cytotoxiques spcifiques
du CMV a t utilis [90].
Virus de la varicelle et du zona. Le zona est secondaire une
ractivation du virus de la varicelle prsent dans lorganisme.
Chez les patients allogreffs, il est souvent tendu et parfois
extensif. Il doit tre trait trs rapidement par aciclovir.
HHV-1 et HHV-2. Les infections herps simplex virus sont
trs frquentes, touchant principalement la bouche, la peau, et
sont des facteurs aggravants des mucites secondaires au conditionnement de greffe.
HHV-6. Les ractivations de HHV-6, objectives par la positivit de la PCR, sont frquentes aprs allogreffe. La majorit de
ces ractivations sont asymptomatiques, mais certaines peuvent
tre responsables de fivre, de rashs cutans, de cytopnies ou
dencphalites qui doivent tre traites par ganciclovir et/ou
foscavir.
Hpatites B et C. Des ractivations des virus de lhpatite B ou
de lhpatite C peuvent tre observes aprs allogreffe de CSH
chez des patients porteurs chroniques ou mme, pour lhpatite
B, chez des patients ayant un statut de gurison (prsence
danticorps anti-HBs et anti-HBc). Le virus peut galement tre
transmis par le donneur. Ces ractivations ou ces infections se
manifestent dabord par une augmentation de la rplication
virale, favorise par le dficit immunitaire. Lors de la restauration dune cytotoxicit lymphode T, une hpatite aigu se
dveloppe avec parfois une dfaillance hpatique mortelle (dans
12 % 20 % des cas). En revanche, les porteurs chroniques du
virus de lhpatite B ne semblent pas exposs un risque accru
de maladie veino-occlusive du foie ou de GVHD hpatique.
Certaines donnes de la littrature suggrent que la greffe
ralise partir dun donneur immunis contre le virus de
lhpatite B peut protger le receveur dune ractivation virale,
voire induire chez celui-ci une sroconversion.
Les porteurs du virus de lhpatite C ont, aprs la greffe, un
risque plus important dvoluer vers la fibrose.
Autres infections virales. Ladnovirus peut tre responsable
dhpatites fulminantes, de pneumopathies, de syndromes
dactivation macrophagique. Sa rplication peut actuellement
tre dtecte dans le sang et dautres sites par PCR. Le BK virus
est responsable de cystites hmorragiques.
Infections tardives non virales. Le conditionnement de
greffe, en particulier lICT, entrane un hyposplnisme qui rend
les patients particulirement sensibles vis--vis des germes
encapsuls, dont le pneumocoque. Une prvention systmatique
est assure par la prise quotidienne de phnoxymthylpnicilline et la vaccination postgreffe. Une vaccination antiHaemophilus doit galement tre pratique aprs la greffe.
Les patients atteints dune GVHD traite par corticothrapie
sont sujets aux infections par Pneumocystis jiroveci et un
traitement prventif doit tre ralis par cotrimoxazole, ou
arosols de pentamidine.
Les infections par Toxoplasma gondii peuvent tre dues une
ractivation chez les patients sropositifs. Elles semblent plus
frquentes lorsque les patients sont greffs partir de donneurs
srongatifs (absence de transfert de limmunit spcifique du
donneur au receveur). Un traitement prventif (cotrimoxazole)
doit tre donn aux patients risque de ractivation. Le
diagnostic prcoce de ractivation peut tre ralis par PCR.
12
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
Les anguilluloses peuvent tre lorigine dun envahissement
massif du tube digestif et de pneumopathies. Les sujets risque
doivent recevoir de manire systmatique un traitement
prventif.
Noplasies secondaires
Lymphoprolifrations lies lEpstein-Barr virus
La majorit des syndromes lymphoprolifratifs postgreffe sont
associs lEBV. Le virus infecte les lymphocytes B et induit une
prolifration lymphocytaire B, dabord oligoclonale puis
monoclonale. Le contrle de ces lymphoprolifrations est assur
par les lymphocytes T spcifiques dantignes de lEBV, exprims
la surface des cellules infectes. Cela explique que ces
lymphoprolifrations surviennent principalement dans les
premiers mois postgreffe, au moment o le dficit immunitaire
est le plus important, et que leur frquence est troitement
corrle au degr dimmunodpression des patients greffs (de
0,4 % aprs greffe gno-identique non complique 24 % aprs
greffe dplte en lymphocytes T ex vivo). Les prolifrations se
dveloppent, dans la majorit des cas, partir des cellules du
donneur, mais peuvent survenir sur les lymphocytes B rsiduels
du receveur, surtout aprs greffes conditionnement non
myloablatif. voqu devant une fivre et un syndrome tumoral, le diagnostic est confirm par la prsence de cellules
tumorales exprimant le gnome de lEBV. Une rplication EBV
importante (mesure par la charge virale en PCR) est prdictive
du risque de dvelopper un syndrome lymphoprolifratif li
lEBV. Elle doit tre recherche chez les patients risque afin
dinstaurer un traitement prcoce. La rduction des traitements
immunosuppresseurs et la chimiothrapie donnent des rsultats
mdiocres. Plus rcemment, dautres approches ont prouv leur
efficacit telles que lutilisation danticorps monoclonaux antiB [91] . Dans la mesure o les lymphocytes T cytotoxiques
spcifiques de lEBV jouent un rle primordial dans le contrle
de linfection, linjection de lymphocytes totaux du donneur
permet de traiter les syndromes lymphoprolifratifs lis
lEBV [92]. Ce traitement peut cependant tre gnrateur de
GVHD svre. Pour cette raison, plusieurs quipes ont gnr in
vitro des lymphocytes T cytotoxiques spcifiques de lEBV et
montr lefficacit de ladministration de ces cellules, pour
prvenir ou traiter des syndromes lymphoprolifratifs lis
lEBV [93].
Tumeurs solides
Les patients traits par allogreffe de CSH ont un risque accru
de dvelopper un cancer. Chez les greffs qui survivent 10 ans
aprs la greffe, ce risque est estim 8,3 fois suprieur celui
observ dans la population gnrale. Lincidence cumule est de
6,7 % 15 ans. Dans cette population, il existe une augmentation de la frquence des mlanomes, des cancers de la cavit
buccale, du foie, du systme nerveux central, de la thyrode, des
os et des tissus mous. Les facteurs de risque principaux sont
lexistence dune GVHD chronique et lutilisation dun conditionnement comportant une haute dose dICT [94].
Autres complications
de lallogreffe
Complications prcoces
Pneumopathies interstitielles
Les pneumopathies interstitielles (PI) non bactriennes, non
fongiques constituaient, il y a quelques annes, une complication frquente et svre des allogreffes de CSH. Lagent infectieux en cause tait frquemment le CMV. Depuis le traitement
systmatique et prcoce des ractivations CMV, leur frquence
a beaucoup diminu. Actuellement, le lavage bronchoalvolaire
(LBA) permet souvent didentifier lagent infectieux responsable
de ces PI : virus du groupe herps, adnovirus, virus respiratoire
syncytial, ou Pneumocystis jiroveci.
Lorsque aucun agent pathogne nest retrouv, on parle de PI
idiopathique, dont la pathognie reste discute : agent pathogne inconnu, GVHD, toxicit des conditionnements ? Elles
compliquent 7 % 18 % des allogreffes avec une mdiane de
survenue dans les deuxime et troisime mois. Le taux de
mortalit excde 60 %. Les facteurs favorisant ces pneumopathies sont :
lutilisation dun conditionnement comportant une ICT
(surtout les ICT forte dose et les ICT non fractionnes) ;
les antcdents de radiothrapie pulmonaire ;
lexistence dinfections systmiques. La frquence des PI
idiopathiques est plus faible aprs autogreffe, suggrant que
la GVHD puisse favoriser la survenue de cette complication.
La symptomatologie associe de la fivre, une toux non
productive, une polypne et une hypoxie. Radiologiquement, il
existe des infiltrats diffus alvolaires et/ou interstitiels. Le lavage
bronchoalvolaire doit tre ralis pour liminer la responsabilit dun micro-organisme. Il nexiste plus quexceptionnellement dindication de biopsie pulmonaire. Aucun traitement
autre que symptomatique na prouv son efficacit. La corticothrapie na pas t value dans des essais prospectifs.
Maladie veino-occlusive du foie [95]
La maladie maladie veino-occlusive (MVO) du foie est une
complication secondaire la toxicit des traitements radiochimiothrapiques. Elle dbute dans les deux ou trois premires
semaines aprs la greffe. Il sagit dune obstruction primitivement non thrombotique des petites veines centrolobulaires
hpatiques qui complique entre 5 % et 20 % des allogreffes
aprs conditionnement myloablatif. Sa frquence est corrle
la lourdeur des traitements reus avant la greffe et celle du
conditionnement. Elle est moins frquente dans les greffes
conditionnements rduit. La prexistence dune atteinte hpatique, infectieuse ou toxique, constitue un facteur de risque.
Physiopathologie
Le dveloppement dune MVO se fait en deux tapes.
La premire est secondaire la toxicit du conditionnement
(en particulier de lICT et du busulfan). La toxicit du conditionnement serait due une dpltion des hpatocytes et des
cellules endothliales sinusodales en glutathion, altrant le
mtabolisme du cyclophosphamide. Parmi les autres substances
potentiellement hpatotoxiques, citons : la carmustine fortes
doses, le carboplatine et la cytarabine. Enfin, la dose totale
dICT est corrle la survenue et la svrit de la MVO.
La seconde tape est la survenue de microthromboses des
veines centrolobulaires responsables de la diminution du flux
veineux, de lhypertension portale et de lascite. Les mcanismes
du syndrome hpatornal responsables de la rtention hydrosode prcoce sont inconnus, mais peuvent mettre en jeu des
mdiateurs vasoactifs, entranant une vasoconstriction des
sinusodes hpatiques et des vaisseaux rnaux, sur un rein par
ailleurs pralablement ls par le conditionnement.
Diagnostic
Le diagnostic de MVO est voqu devant la triade clinique :
hpatomgalie douloureuse, prise de poids et ictre. Sur le plan
biologique, lhyperbilirubinmie prcde llvation des transaminases et des phosphatases alcalines, souvent modeste et
retarde. Il sy associe prcocement une thrombopnie rfractaire aux transfusions plaquettaires. Dans les formes graves, il
peut exister une insuffisance hpatocellulaire avec encphalopathie, une insuffisance rnale due lexistence dun troisime
secteur. Lchodoppler hpatique permet de visualiser lhpatomgalie, lascite et la diminution du flux hpatique, voire, un
stade avanc, une inversion du flux veineux portal. Dans les
situations o le diagnostic est difficile, la ponction-biopsie
hpatique (PBH) par voie transveineuse avec prise de la pression
intrahpatique est utile. Ltude histologique permet le diagnostic en montrant lobstruction veineuse.
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
13
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
Traitement prventif
Il est particulirement indiqu chez les patients risque :
antcdents de MVO, seconde transplantation, transaminases
leves avant la greffe et fibrose extensive ou cirrhose. Il
consiste avant tout adapter le conditionnement (diminution
des doses de busulfan ou de cyclophosphamide ou des doses
dirradiation) ou raliser un conditionnement non myloablatif. Quelques tudes ont de plus montr lintrt de lhparine
faible dose en perfusion continue ou de la dinoprogestone
(Prostine).
Traitement curatif
La majorit des MVO se rsolvant spontanment, le traitement est principalement symptomatique (transfusions de
plaquettes, diurtiques, ponctions dascites vacuatrices, etc.). Le
pronostic des MVO grave avec insuffisance hpatocellulaire et
insuffisance rnale reste sombre. Des rsultats intressants ont
cependant t rapports avec les traitements thrombolytiques
tels que le rh-tPA (activateur tissulaire du plasminogne recombinant humain), le dfibrotide, les prostaglandines, ou les
drivations portocaves.
Complications neurologiques
Des leucoencphalites dmylnisantes peuvent sobserver
aprs radiothrapie et chimiothrapie intrathcale. La succession
dune irradiation fractionne du systme nerveux central dose
leve, dune chimiothrapie intrathcale et dune ICT constitue
les conditions de survenue de ces complications. Rcemment
ont t rapportes, de manire non exceptionnelle, des
encphalites aprs lutilisation de fludarabine. Les encphalites
toxiques doivent tre diffrencies des leucoencphalites
multifocales progressives en rapport avec le JC virus ou des
exceptionnelles encphalites CMV. Dautres virus peuvent tre
responsables de mningites ou mningoencphalites ; il sagit
principalement des virus du groupe herps, dont lHHV-6, qui
est incrimin de manire non exceptionnelle chez les patients
prsentant des troubles neurologiques aprs allogreffe.
Complications tardives [96]
Complications oculaires
Aprs ICT dose unique, le risque de cataracte est estim
75 % 6 ans. Il est diminu aprs irradiation fractionne et
aprs des conditionnements sans ICT. Les corticodes utiliss de
faon prolonge pour le traitement dune GVHD aggravent ce
risque.
Retentissement hormonal
Complications thyrodiennes
Un dysfonctionnement thyrodien biologique est retrouv
chez environ la moiti des transplants distance de la greffe ;
chez 80 % dentre eux cependant, une compensation par
augmentation de la thyroid stimulating hormone (TSH) est
observe.
Complications gonadiques
Le conditionnement de greffe entrane des dysfonctionnements gonadiques. Ces atteintes sont dues lutilisation
dalkylants haute dose et lirradiation. Chez lhomme, la
fonction endocrinienne (production de testostrone) est rarement gravement altre, mais il existe une atteinte frquente de
la spermatogense. Une strilit dfinitive est observe chez la
quasi-totalit des hommes traits par busulfan ou ICT, alors
quil existe une restauration de la fonction exocrine chez 60 %
des patients conditionns par cyclophosphamide seul.
Chez la femme, le risque de strilit est fortement corrl
lge au moment de la greffe et au type de conditionnement
utilis. Ainsi, aprs un conditionnement comportant du cyclophosphamide ou du melphalan haute dose, la majorit des
patientes ont une restauration de la fonction ovarienne (dfinie
par une normalisation des taux de luteinizing hormone [LH],
follicle stimulating hormone [FSH] et estradiol, et la rapparition
de rgles). Ce phnomne est dautant plus frquent que les
patientes sont plus jeunes au moment de la greffe et ont reu
moins dalkylants avant le conditionnement. Le busulfan et
lICT dose myloablative entranent gnralement une
strilit. Un traitement hormonal substitutif doit tre donn en
cas de mnopause induite.
Dans les rares cas de grossesse spontane rapporte aprs
allogreffe conditionne par une ICT, les risques de fausse
couche, prmaturit et petits poids de naissance sont plus
importants que dans la population gnrale. Quand la situation
hmatologique le permet, des techniques de prservation de la
fertilit sont proposes avant la greffe aux receveurs jeunes
risque de strilit postgreffe : cryoconservation de sperme,
conglation de tissu ovarien, prlvement dovocytes pour
fcondation in vitro lorsque cela est possible.
Retentissement sur la croissance
Aprs ICT, un retard de croissance en rapport avec un dficit
de scrtion dhormone de croissance doit tre recherch et
trait. Lirradiation propre du squelette peut, surtout chez le trs
jeune enfant, contribuer ce dfaut de croissance.
Rechutes aprs allogreffe
de cellules souches
hmatopotiques
pour hmopathies malignes
La plupart des rechutes surviennent dans les 2 ans qui
suivent la greffe : aprs ce dlai, la rechute est rare, et elle
devient exceptionnelle aprs 5 ans. La trs grande majorit des
rechutes surviennent sur les cellules de lhte, tmoignant de la
persistance de cellules leucmiques rsiduelles aprs le conditionnement et de leur chappement limmunosurveillance du
systme immunitaire du donneur. Il a cependant t rapport
des cas exceptionnels de rechute survenue sur les cellules du
donneur.
Facteurs favorisants
Certains facteurs favorisent les rechutes postgreffe. Les
principaux sont les suivants :
la greffe ralise en phase avance de la maladie. Les patients
greffs en pousse dune hmopathie maligne ont en effet un
risque particulirement lev de rechute. Pour les patients
greffs en rmission complte (RC), le risque de rechute est
plus important en deuxime ou en troisime RC quen
premire RC. Pour les patients atteints de LMC, le risque de
rechute postgreffe est plus important si la greffe est ralise
en phase dacclration ou de transformation plutt quen
phase chronique ;
la prophylaxie de la GVHD comportant une dpltion T ex
vivo ;
labsence de GVHD.
Dtection de la rechute
Il existe actuellement des techniques permettant de diagnostiquer les rechutes prcocement.
Ainsi, pour certaines hmopathies, les techniques de biologie
molculaire permettent de dtecter, avec une grande sensibilit,
un transcrit chimrique ou un rarrangement gnique et
constituent un outil important dans le diagnostic prcoce des
rechutes aprs greffe. Ces techniques sont ralises couramment
pour le suivi des LMC et leur positivit est prdictive de la
rechute [97]. Ltude de la maladie rsiduelle par les techniques
de biologie molculaire peut galement tre ralise pour
14
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
certaines leucmies aigus mylodes ou lymphoblastiques. En
labsence de marqueur spcifique de la leucmie, ltude du
chimrisme postgreffe peut tre un bon marqueur prcoce de
rechute : la rapparition de marqueur spcifique du receveur
prcde la dtection des cellules leucmiques dans le sang [98].
Traitement de la rechute
La prise en charge de la rechute est diffrente en fonction du
dlai de survenue par rapport la greffe (rechute prcoce ou
tardive) et de limportance de cette rechute (molculaire,
cytogntique, hmatologique ou clinique).
La chimiothrapie seule peut parfois donner des rsultats
temporairement satisfaisants. En cas de rechute tardive (suprieure 1 an), des tentatives de deuxime greffe ont t
effectues. Malgr certains succs, les rsultats sont souvent
dcevants. Dans la plupart des cas, un conditionnement non
myloablatif sera choisi pour limiter la toxicit du deuxime
conditionnement.
Linjection de lymphocytes du donneur (donor lymphocyte
injection [DLI]) a transform le pronostic des rechutes postgreffe
des LMC [99]. Ces lymphocytes sont recueillis par cytaphrse
chez le donneur et injects au patient. Ils ne sont pas rejets car,
si la rechute est dtecte prcocement, lhmatopose rsiduelle
et limmunit restent le plus souvent en majorit celles du
donneur. La quantit de lymphocytes injecte varie de 107
2 108 CD3/kg de receveur. Les DLI sont plus efficaces lorsque
la rechute est peu importante. En cas de rechute cytogntique
ou molculaire de LMC, elles permettent dobtenir une rmission molculaire chez plus de 70 % des patients. Leffet des DLI
est souvent retard et peut napparatre que plusieurs mois aprs
linjection. Linjection de DLI peut aussi provoquer une GVHD
et une insuffisance mdullaire. Les DLI sont plus rarement
efficaces dans les rechutes de LAM (un quart des cas) et,
exceptionnellement, dans les rechutes de leucmie aigu
lymphoblastique (LAL). Des succs plus frquents seraient
observs dans des rechutes de mylome, de leucmie lymphode
chronique, voire de lymphome de bas grade de malignit [100].
Voies de dveloppement
et perspectives davenir
Ces dernires annes ont t marques par des changements
majeurs dans les modalits de ralisation des allogreffes de CSH.
En voici les principaux :
dveloppement trs important des greffes conditionnement
rduit, permettant la ralisation dallogreffes chez des patients
plus gs et plus fragiles ;
possibilit de raliser des allogreffes partir de greffons de
CSP, permettant de diminuer le risque de rejet dans les greffes
conditionnement rduit, les greffes dpltes en lymphocytes T, et les greffes en situation de HLA-discordante ;
expansion des fichiers de donneurs volontaires et dveloppement de techniques performantes de typage HLA ayant
permis damliorer le pronostic des patients greffs partir de
donneurs volontaires HLA-identiques ;
dveloppement des greffes de sang placentaire, avec de
nouvelles modalits (conditionnements non myloablatifs et
doubles greffes), permettant dtendre les indications aux
receveurs adultes.
Les voies de recherche actuelles concernent principalement le
domaine de limmunomodulation postgreffe, dans le but de
diminuer la toxicit lie la greffe et de renforcer son effet
antileucmique. Il sagit principalement de travaux concernant
le contrle spcifique de la GVHD et le renforcement de leffet
antitumoral.
Contrle de la maladie du greffon
contre lhte
Contrle de la maladie du greffon contre lhte
par transduction dun gne suicide aux
lymphocytes du donneur
Les gnes suicides confrent aux cellules transduites de
nouvelles proprits mtaboliques qui leur permettent de
transformer des prodrogues inactives en composs hautement
toxiques. Ainsi, le gne de la thymidine kinase du virus herps
simplex de type 1 (HS-tk) confre aux cellules qui lexpriment
une sensibilit des analogues nuclosidiques comme le
ganciclovir (DHPG) [101] . Dans ce systme, la toxicit est
restreinte aux seules cellules en division. Lors de la GVHD, les
cellules actives en division sont en majorit les lymphocytes T
alloractifs du donneur. Si ces lymphocytes I contiennent le
gne HS-tk, ladministration de ganciclovir au receveur doit
permettre de les dtruire spcifiquement.
En pratique, cette approche consiste :
raliser une greffe de CSH dplte en lymphocytes T ;
transfecter ex vivo les lymphocytes T du donneur avec le
gne HS-tk ;
injecter les lymphocytes transfects au receveur ;
administrer au receveur du ganciclovir, en cas de GVHD,
pour dtruire les lymphocytes alloractifs. Cette technique
permet de contrler efficacement la GVHD en tentant de
maintenir la rponse immunitaire des lymphocytes non
alloractifs ; son utilisation est cependant limite par sa
lourdeur technique et doit tre rserve des situations
haut risque de GVHD [102].
Injection de cellules souches msenchymateuses
(CSM) allogniques
Les cellules souches msenchymateuses (CSM) sont dfinies,
in vitro, comme une population de cellules homognes,
daspect fibroblastique, obtenue partir de la moelle osseuse par
adhsion au plastique et capables de se diffrencier en trois
lignes cellulaires : les chondrocytes, les ostoblastes et les
adipocytes. Paralllement, par la scrtion de cytokines, les CSM
jouent un rle majeur dans le soutien de lhmatopose et la
prise de greffe. Les CSM possdent galement des proprits
immunomodulatrices, ce qui a justifi leur utilisation dans le
traitement de la GVHD. ltat basal, les CSM sont trs peu
nombreuses dans la moelle osseuse. Leur culture in vitro permet
leur expansion pour leur utilisation en recherche et dans des
applications cliniques.
La premire utilisation des CSM dans le traitement prventif
de la GVHD a t rapporte par Lee en 2002. Une tude plus
large a rapport lutilisation prventive de CSM chez 46 patients
recevant une allogreffe familiale HLA-identique [103]. Cette tude
dmontre labsence de toxicit des CSM, mais les cellules ne
sont dtectes que chez 11 % des receveurs. Dans cette tude
non comparative, la vitesse de reconstitution hmatopotique
et lincidence de la GVHD ne paraissent pas diffrentes de celles
observes dans des sries historiques. Pour valuer dune
manire plus prcise lintrt des CSM dans le traitement
prventif de la GVHD, la Socit franaise de greffe de moelle
et de thrapie cellulaire a mis en place une tude randomise
portant sur ladministration ou non de CSM aprs allogreffe
familiale ou non apparente HLA-identique.
Paralllement, les CSM ont t values dans le traitement
curatif de la GVHD pour leur effet immunomodulateur, dcrit
in vitro chez lhomme, et leur capacit, dcrite dans les modles
animaux, rparer les tissus lss. Le Blanc et al. ont t les
premiers a rapporter le bnfice des CSM chez un patient
prsentant une GVHD svre (grade IV, rsistante au traitement) [66]. Rcemment, une tude rtrospective a collig 55 cas
de patients traits, en Europe, par des CSM pour des GVHD
svres corticorsistantes. Le taux de rponses de 69 %, est trs
encourageant, mais ces rsultats mritent dtre confirms dans
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
15
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
une plus grande cohorte de patients, dautant que la prsence
des CSM dans les organes cibles de la GVHD na t que trs
rarement documente.
Rfrences
[1]
Amlioration de leffet antitumoral
Intrt des lymphocytes T rgulateurs
Les lymphocytes T rgulateurs (Treg) reprsentent une souspopulation de lymphocytes CD4+ qui expriment fortement le
CD25 et jouent un rle fondamental dans les phnomnes de
tolrance. Dans les modles murins, il a t montr que ces
cellules taient capables de prvenir et de traiter la GVHD, tout
en prservant la GVL [104]. Chez lhomme, il a t montr, dans
plusieurs tudes, une corrlation entre le contenu du greffon en
Treg et lincidence de la GVHD ; ces rsultats ne sont cependant
pas confirms dans toutes les tudes. ce jour, lintrt des Treg
dans le traitement de la GVHD reste dmontrer chez
lhomme [105] . Paralllement, des approches consistant
dplter les DLI en Treg pour accrotre leffet antitumoral sont
actuellement en cours.
[2]
[3]
[4]
[5]
Injection de cellules natural killer actives
En situation HLA-incompatibles, les cellules NK du donneur
peuvent dtruire les cellules leucmiques du receveur. En effet,
dans ce type de greffe, labsence dinteraction entre les rcepteurs inhibiteurs des cellules NK du donneur (KIR) et les
molcules HLA de classe I exprimes la surface des cellules
leucmiques du receveur peut expliquer la lyse des cellules
leucmiques par les cellules NK du donneur. Cependant, il a t
montr quaprs greffe haplo-identique, les cellules NK prsentes
chez le receveur taient immatures et non fonctionnelles [47].
Pour accrotre leffet antitumoral NK aprs greffe haploidentique, des quipes ont inject au receveur des cellules NK
du donneur slectionnes et actives ex vivo [106].
Une approche similaire a par ailleurs t applique en dehors
de tout contexte dallogreffe de CSH : elle consiste en linjection
des patients leucmiques de cellules NK haplo-identiques
actives, aprs ladministration au receveur dun conditionnement immunosuppresseur ayant pour but de prvenir le rejet
des cellules NK par le systme immunitaire du receveur [107].
[6]
[7]
[8]
[9]
[10]
Points forts
Dans les hmopathies malignes, lallogreffe constitue
une immunothrapie antitumorale : le systme
immunitaire du donneur permet la destruction des
cellules tumorales du receveur.
La diffrence dantignes majeurs ou mineurs
dhistocompatibilit entre le donneur et le receveur
permet dexpliquer leffet :
C de la maladie du greffon contre lhte (GVHD) ;
C du greffon contre la leucmie (GVL) ;
C de rejet (HVG : host versus graf greffon contre
lhte).
La GVL et la GVHD sont corrles : lincidence de
rechute est plus faible chez les patients ayant dvelopp
une GVHD.
Le conditionnement de greffe administr au receveur
doit imprativement tre immunosuppresseur pour
prvenir le rejet du greffon par les cellules du systme
immunitaire du receveur.
La plus faible immunognicit des greffons de sang
placentaire permet la ralisation de lallogreffe en situation
partiellement HLA-incompatible.
[11]
[12]
[13]
[14]
[15]
[16]
Storb R, Yu C, Wagner JL, Deeg HJ, Nash RA, Kiem HP, et al. Stable
mixed hematopoietic chimerism in DLA-identical littermate dogs
given sublethal total body irradiation before and pharmacological
immunosuppression after marrow transplantation. Blood 1997;89:
3048-54.
Slavin S, Nagler A, Naparstek E, Kapelushnik Y, Aker M, Cividalli G,
et al. Nonmyeloablative stem cell transplantation and cell therapy as an
alternative to conventional bone marrow transplantation with lethal
cytoreduction for the treatment of malignant and nonmalignant
hematologic diseases. Blood 1998;91:756-63.
Clift RA, Buckner CD, Appelbaum FR, Bearman SI, Petersen FB,
Fisher LD, et al. Allogeneic marrow transplantation in patients with
acute myeloid leukemia in first remission: a randomized trial of two
irradiation regimens. Blood 1990;76:1867-71.
Cosset JM, Baume D, Pico JL, Shank B, Girinski T, Benhamou E, et al.
Single dose versus hyperfractionated total body irradiation before
allogeneic bone marrow transplantation: a non-randomized comparative study of 54 patients at the Institut Gustave-Roussy. Radiother
Oncol 1989;15:151-60.
Thomas ED, Buckner CD, Banaji M, Clift RA, Fefer A, Flournoy N,
et al. One hundred patients with acute leukemia treated by
chemotherapy, total body irradiation, and allogeneic marrow transplantation. Blood 1977;49:511-33.
Santos GW, Tutschka PJ, Brookmeyer R, Saral R, Beschorner WE,
Bias WB, et al. Marrow transplantation for acute nonlymphocytic
leukemia after treatment with busulfan and cyclophosphamide. N Engl
J Med 1983;309:1347-53.
Ringden O, Remberger M, Ruutu T, Nikoskelainen J, Volin L,
Vindelov L, et al. Increased risk of chronic graft-versus-host disease,
obstructive bronchiolitis, and alopecia with busulfan versus total body
irradiation: long-term results of a randomized trial in allogeneic
marrow recipients with leukemia. Nordic Bone Marrow Transplantation Group. Blood 1999;93:2196-201.
Devergie A, Blaise D, Attal M, Tigaud JD, Jouet JP, Vernant JP, et al.
Allogeneic bone marrow transplantation for chronic myeloid leukemia
in first chronic phase: a randomized trial of busulfan-cytoxan versus
cytoxan-total body irradiation as preparative regimen: a report from the
French Society of Bone Marrow Graft (SFGM). Blood 1995;85:
2263-8.
Blaise D, Maraninchi D, Archimbaud E, Reiffers J, Devergie A,
Jouet JP, et al. Allogeneic BMT for AML in first remission: a
randomized trial of a busulfan-Cytoxan versus cytoxan-TBI as
preparative regimen: a report from the Group dtudes de la greffe de
Moelle Osseuse. Blood 1992;79:2578-82.
Soci G, Clift RA, Blaise D, Devergie A, Ringden O, Martin PJ, et al.
Busulfan plus cyclophosphamide compared with total-body irradiation
plus cyclophosphamide before marrow transplantation for myeloid
leukemia: long-term follow-up of 4 randomized studies. Blood 2001;
98:3569-74.
Champlin RE, Perez WS, Passweg JR, Klein JP, Camitta BM,
Gluckman E, et al. Bone marrow transplantation for severe aplastic
anemia: a randomized controlled study of conditioning regimens.
Blood 2007;109:4582-5.
Storb R, Raff RF,Appelbaum FR, Deeg HJ, Graham TC, Schuening FG,
et al. DLA-identical bone marrow grafts after low-dose total body
irradiation: the effect of canine recombinant hematopoietic growth
factors. Blood 1994;84:3558-66.
Terenzi A, Aristei C, Aversa F, Perruccio K, Chionne F, Raymondi C,
et al. Efficacy of fludarabine as an immunosuppressor for bone marrow
transplantation conditioning: preliminary results. Transplant Proc
1996;28:3101.
Kassim AA, Chinratanalab W, Ferrara JL, Mineishi S. Reduced
intensity allogenic hematopoietic stem cell transplantation for acute
leukemias: what is the best recipe? Bone Marrow Transplant 2005;36:
565-74.
Diaconescu R, Flowers CR, Storer B, Sorror ML, Maris MB,
Maloney DG, et al. Morbidity and mortality with nonmyeloablative
compared with myeloablative conditioning before hematopoietic cell
transplantation from HLA-matched related donors. Blood 2004;104:
1550-8.
Storb RF, Champlin R, Riddell SR, Murata M, Bryant S, Warren EH.
Non-myeloablative transplants for malignant disease. Hematology (Am
Soc Hematol Educ Program) 2001:375-91.
16
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
[17] Giralt S, Thall PF, Khouri I, Wang X, Braunschweig I, Ippolitti C, et al.
Melphalan and purine analog-containing preparative regimens:
reduced-intensity conditioning for patients with hematologic
malignancies undergoing allogeneic progenitor cell transplantation.
Blood 2001;97:631-7.
[18] Bensinger WI, Weaver CH, Appelbaum FR. Transplantation of
allogeneic peripheral blood stem cells mobilized by recombinant human
granulocyte colony-stimulating factor. Blood 1995;86:836-7.
[19] Bensinger WI, Martin PJ, Storer B, Clift R, Forman SJ, Negrin R, et al.
Transplantation of bone marrow as compared with peripheral-blood
cells from HLA-identical relatives in patients with hematologic
cancers. N Engl J Med 2001;344:175-81.
[20] Schmitz N, Beksac M, Hasenclever D, Bacigalupo A, Ruutu T,
Nagler A, et al. Transplantation of mobilized peripheral blood cells to
HLA-identical siblings with standard-risk leukemia. Blood 2002;100:
761-7.
[21] Blaise D, Kuentz M, Fortanier C, Bourhis JH, Milpied N, Sutton L,
et al. Randomized trial of bone marrow versus lenograstim-primed
blood cell allogeneic transplantation in patients with early-stage
leukemia: a report from the Societe Franaise de Greffe de Moelle.
J Clin Oncol 2000;18:537-46.
[22] Couban S, Simpson DR, Barnett MJ, Bredeson C, Hubesch L, HowsonJan K, et al. A randomized multicenter comparison of bone marrow and
peripheral blood in recipients of matched sibling allogeneic transplants
for myeloid malignancies. Blood 2002;100:1525-31.
[23] Stem Cell Trialists Collaborative Group. Allogeneic peripheral blood
stem-cell compared with bone marrow transplantation in the
management of hematologic malignancies: an individual patient data
meta-analysis of nine randomized trials. J Clin Oncol 2005;23:
5074-87.
[24] Zaucha JM, Gooley T, Bensinger WI, Heimfeld S, Chauncey TR,
Zaucha R, et al. CD34 cell dose in granulocyte colony-stimulating
factor-mobilized peripheral blood mononuclear cell grafts affects
engraftment kinetics and development of extensive chronic graftversus-host disease after human leukocyte antigen-identical sibling
transplantation. Blood 2001;98:3221-7.
[25] Dhdin N, Chamakhi I, Perrault C. Evidence that donor intrinsic
response to G-CSF is the best predictor of acute graft-vs-host disease
following allogeneic peripheral blood stem cell transplantation. Exp
Hematol 2006;34:107-14.
[26] Przepiorka D, Smith TL, Folloder J, Khouri I, Ueno NT, Mehra R, et al.
Risk factors for acute graft-versus-host disease after allogeneic blood
stem cell transplantation. Blood 1999;94:1465-70.
[27] Mohty M, Bilger K, Jourdan E, Kuentz M, Michallet M, Bourhis JH,
et al. Higher doses of CD34+ peripheral blood stem cells are associated
with increased mortality from chronic graft-versus-host disease after
allogeneic HLA-identical sibling transplantation. Leukemia 2003;17:
869-75.
[28] Pan L, Delmonte JJ, Jalonene CK, Ferrara JL. Treatment of donor mice
with granulocyte colony-stimulating factor polarizes donor T
lymphocytes toward type-2 cytokine production and reduces severity
of experimental graft-versus-host disease. Blood 1995;86:4422-9.
[29] Mielcarek M, Martin PJ, Torok-Storb B. Suppression of alloantigeninduced T-cell proliferation by CD14+ cells derived from granulocyte
colony-stimulating factor-mobilized peripheral blood mononuclear
cells. Blood 1997;89:1629-34.
[30] Arpinati M, Green CL, Heimfeld S, Heuser JE, Anasetti C.
Granulocyte-colony stimulating factor mobilizes T helper 2-inducing
dendritic cells. Blood 2000;95:2484-90.
[31] Miller JS, Propser F, McCullar V. Natural killer (NK) cells are
functionally abnormal and NK cell progenitors are diminished in
granulocyte colony-stimulating factor-mobilized peripheral blood
progenitor cell collections. Blood 1997;90:3098-105.
[32] Gluckman E, Broxmeyer HE, Auerbach AD, Friedman HS,
Douglas GW, Devergie A. Hematopoietic reconstitution in a patient
with Fanconis anemia by means of umbilical-cord blood from an
HLA-identical sibling. N Engl J Med 1989;321:1174-8.
[33] Kurtzberg J, Laughlin M, Graham ML, Smith C, Olson JF, Halperin EC,
et al. Placental blood as a source of hematopoietic stem cells for
transplantation into unrelated recipients. N Engl J Med 1996;335:
157-66.
[34] Gluckman E, Rocha V, Boyer-Chammard A, Locatelli F, Arcese W,
Pasquini R, et al. Outcome of cord-blood transplantation from related
and unrelated donors. Eurocord Transplant Group and the European
Blood and Marrow Transplantation Group. N Engl J Med 1997;337:
373-81.
[35] Rocha V, Wagner Jr. JE, Sobocinski KA, Klein JP, Zhang MJ,
Horowitz MM, et al. Graft-versus-host disease in children who have
received a cord-blood or bone marrow transplant from an HLAidentical sibling. Eurocord and International Bone Marrow Transplant
Registry Working Committee on Alternative Donor and Stem Cell
Sources. N Engl J Med 2000;342:1846-54.
[36] Barker JN, Davies SM, DeFor T, Ramsay NK, Weisdorf DJ, Wagner JE.
Survival after transplantation of unrelated donor umbilical cord blood
is comparable to that of human leukocyte antigen-matched unrelated
donor bone marrow: results of a matched-pair analysis. Blood 2001;97:
2957-61.
[37] Rocha V, Cornish J, Sievers EL, Filipovich A, Locatelli F, Peters C,
et al. Comparison of outcomes of unrelated bone marrow and umbilical
cord blood transplants in children with acute leukemia. Blood 2001;97:
2962-71.
[38] Rocha V, Labopin M, Sanz G,Arcese W, Schwerdtfeger R, BosiA, et al.
Transplants of umbilical-cord blood or bone marrow from unrelated
donors in adults with acute leukemia. N Engl J Med 2004;351:2276-85.
[39] Laughlin MJ, Eapen M, Rubinstein P, Wagner JE, Zhang MJ,
Champlin RE, et al. Outcomes after transplantation of cord blood or
bone marrow from unrelated donors in adults with leukemia. N Engl
J Med 2004;351:2265-75.
[40] Takahashi S, Iseki T, Ooi J, Tomonari A, Takasugi K,
Shimohakamada Y, et al. Single-institute comparative analysis of
unrelated bone marrow transplantation and cord blood transplantation
for adult patients with hematologic malignancies. Blood 2004;104:
3813-20.
[41] Barker JN, Weisdorf DJ, DeFor TE, Blazar BR, Miller JS, Wagner JE.
Rapid and complete donor chimerism in adult recipients of unrelated
donor umbilical cord blood transplantation after reduced-intensity
conditioning. Blood 2003;102:1915-9.
[42] Barker JN, Weisdorf DJ, DeFor TE, Blazar BR, McGlave PB, Miller JS,
et al. Transplantation of 2 partially HLA-matched umbilical cord blood
units to enhance engraftment in adults with hematologic malignancy.
Blood 2005;105:1343-7.
[43] Scott I, OShea J, Bunce M, Tiercy JM, Arguello JR, Firman H, et al.
Molecular typing shows a high level of HLA class I incompatibility
in serologically well matched donor/patient pairs: implications
for unrelated bone marrow donor selection. Blood 1998;92:
4864-71.
[44] Yakoub-Agha I, Mesnil F, Kuentz M, Boiron JM, Ifrah N, Milpied N,
et al. Allogeneic marrow stem-cell transplantation from human
leukocyte antigen-identical siblings versus human leukocyte antigenallelic-matched unrelated donors (10/10) in patients with standard-risk
hematologic malignancy: a prospective study from the French Society
of Bone Marrow Transplantation and Cell Therapy. J Clin Oncol 2006;
24:5695-702.
[45] Reisner Y, Martelli MF. Bone marrow transplantation across HLA
barriers by increasing the number of transplanted cells. Immunol Today
1995;16:437-40.
[46] Aversa F, Tabilio A, Velardi A, Cunningham I, Terenzi A, Falzetti F,
et al. Treatment of high-risk acute leukemia with T-cell-depleted stem
cells from related donors with one fully mismatched HLA haplotype. N
Engl J Med 1998;339:1186-93.
[47] Nguyen S, Dhedin N, Vernant JP, Kuentz M, Al Jijakli A, RouasFreiss N, et al. NK-cell reconstitution after haploidentical
hematopoietic stem-cell transplantations: immaturity of NK cells and
inhibitory effect of NKG2A override GvL effect. Blood 2005;105:
4135-42.
[48] Reddy P, Ferrara JL. Immunobiology of acute graft-versus-host
disease. Blood Rev 2003;17:187-94.
[49] Thornhill MH, Wellicome SM, Mahiouz DL, Lanchbury JS, KyanAung U, Haskard DO. Tumor necrosis factor combines with IL-4 or
IFN-gamma to selectively enhance endothelial cell adhesiveness for T
cells. The contribution of vascular cell adhesion molecule-1-dependent
and -independent binding mechanisms. J Immunol 1991;146:592-8.
[50] Wysocki CA, Panoskaltsis-Mortari A, Blazar BR, Serody JS.
Leukocyte migration and graft-versus-host disease. Blood 2005;105:
4191-9.
[51] Horowitz ME, Sullivan KM. Chronic graft-versus-host disease. Blood
Rev 2006;20:15-27.
[52] Filipovich AH, Weisdorf D, Pavletic S, Socie G, Wingard JR, Lee SJ,
et al. National Institutes of Health consensus development project on
criteria for clinical trials in chronic graft-versus-host disease: I.
Diagnosis and staging working group report. Biol Blood Marrow
Transplant 2005;11:945-56.
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
17
13-061-A-10 Allogreffe de cellules souches hmatopotiques : ralisation et complications
[53] Glucksberg H, Storb R, Fefer A, Buckner CD, Neiman PE, Clift RA,
et al. Clinical manifestations of graft-versus-host disease in human
recipients of marrow from HLA-matched sibling donors. Transplantation 1974;18:295-304.
[54] Storb R, Deeg HJ, Whitehead J, Appelbaum F, Beatty P, Bensinger W,
et al. Methotrexate and cyclosporine compared with cyclosporine alone
for prophylaxis of acute graft versus host disease after marrow transplantation for leukemia. N Engl J Med 1986;314:729-35.
[55] Antin JH, Kim HT, Cutler C, Ho VT, Lee SJ, Miklos DB, et al.
Sirolimus, tacrolimus, and low-dose methotrexate for graft-versus-host
disease prophylaxis in mismatched related donor or unrelated donor
transplantation. Blood 2003;102:1601-5.
[56] Cutler C, Li S, Ho VT, Koreth J, Alyea E, Soiffer RJ, et al. Extended
follow-up of methotrexate-free immunosuppression using sirolimus
and tacrolimus in related and unrelated donor peripheral blood stem
cell transplantation. Blood 2007;109:3108-14.
[57] Ruutu T, Volin L, Parkkali T, Juvonen E, Elonen E. Cyclosporine,
methotrexate, and methylprednisolone compared with cyclosporine
and methotrexate for the prevention of graft-versus-host disease in bone
marrow transplantation from HLA-identical sibling donor: a
prospective randomized study. Blood 2000;96:2391-8.
[58] Herve P, Cahn JY, Flesch M, Plouvier E, Racadot E, Noir A, et al.
Successful graft-versus-host disease prevention without graft failure in
32 HLA-identical allogeneic bone marrow transplantations with
marrow depleted of T cells by monoclonal antibodies and complement.
Blood 1987;69:388-93.
[59] Maraninchi D, Gluckman E, Blaise D, Guyotat D, Rio B, Pico JL, et al.
Impact of T-cell depletion on outcome of allogeneic bone-marrow
transplantation for standard-risk leukaemias. Lancet 1987;2:175-8.
[60] Deeg HJ. How I treat refractory acute GVHD. Blood 2007;109:
4119-26.
[61] Doney KC, Weiden PL, Storb R, Thomas ED. Treatment of graftversus-host disease in human allogeneic marrow graft recipients: a
randomized trial comparing antithymocyte globulin and
corticosteroids. Am J Hematol 1981;11:1-8.
[62] Bay JO, Dhdin N, Goerner M, Vannier JP, Marie-Cardine A,
Stamatoullas A, et al. Inolimomab in steroid-refractory acute graftversus-host disease following allogeneic hematopoietic stem cell
transplantation: retrospective analysis and comparison with other
interleukin-2 receptor antibodies. Transplantation 2005;80:782-8.
[63] Levine JE, Paczesny S, Mineishi S, Braun T, Choi SW, Hutchinson RJ,
et al. Etanercept plus methylprednisolone as initial therapy for acute
graft-versus-host disease. Blood 2008;111:2470-5.
[64] Ho VT, Cutler C. Current and novel therapies in acute GVHD. Best
Pract Res Clin Haematol 2008;21:223-37.
[65] Kanold J, Merlin E, Halle P, Paillard C, Marabelle A, Rapatel C, et al.
Photopheresis in pediatric graft-versus-host disease after allogeneic
marrow transplantation: clinical practice guidelines based on field
experience and review of the literature. Transfusion 2007;47:2276-89.
[66] Le Blanc K, Frassoni F, Ball L, Locatelli F, Roelofs H, Lewis I, et al.
Mesenchymal stem cells for treatment of steroid-resistant, severe, acute
graft-versus-host disease: a phase II study. Lancet 2008;371:1579-86.
[67] Gilman AL, Serody J. Diagnosis and treatment of chronic graft-versushost disease. Semin Hematol 2006;43:70-80.
[68] Guihot A, Becquemin MH, Couderc LJ, Randrianarivelo O, Rivaud E,
Philippe B, et al. Telemetric monitoring of pulmonary function after
allogeneic hematopoietic stem cell transplantation. Transplantation
2007;83:554-60.
[69] Shulman HM, Sullivan KM, Weiden PL, McDonald GB, Striker GE,
Sale GE, et al. Chronic graft-versus host syndrome in man. A long-term
clinicopathologic study of 20 Seattle patients. Am J Med 1980;69:
204-17.
[70] Mohty M, Kuentz M, Michallet M, Milpied N, Sutton L, Jouet JP, et al.
Chronic graft-versus-host disease after allogeneic blood stem cell
transplantation: long-term results of a randomized study. Blood 2002;
100:3128-34.
[71] Flowers ME, Parker PM, Johnston LJ, Matos AV, Storer B,
Bensinger WI, et al. Comparison of chronic graft-versus-host disease
after transplantation of peripheral blood stem cells versus bone marrow
in allogeneic recipients: long-term follow-up of a randomized trial.
Blood 2002;100:415-9.
[72] Sullivan KM, Witherspoon RP, Storb R, Deeg HJ, Dahlberg S,
Sanders JE, et al. Alternating-day cyclosporine and prednisone for
treatment of high-risk chronic graft-v-host disease. Blood 1988;72:
555-61.
[73] Couriel DR, Saliba R, Escaln MP, Hsu Y, Ghosh S, Ippoliti C, et al.
Sirolimus in combination with tacrolimus and corticosteroids for the
treatment of resistant chronic graft-versus-host disease. Br J Haematol
2005;130:409-17.
[74] Cutler C, Miklos D, Kim HT, Treister N, Woo SB, Bienfang D, et al.
Rituximab for steroid-refractory chronic graft-versus-host disease.
Blood 2006;108:756-62.
[75] Greinix HT, Volc-Platzer B, Rabitsch W, Gmeinhart B, GuevaraPineda C, Kalhs P, et al. Successful use of extracorporeal
photochemotherapy in the treatment of severe acute and chronic graftversus-host disease. Blood 1998;92:3098-104.
[76] Koh MB, Prentice HG, Lowdell MW. Selective removal of alloreactive
cells from haematopoietic stem cell grafts: graft engineering for GVHD
prophylaxis. Bone Marrow Transplant 1999;23:1071-9.
[77] Montagna D, Yvon E, Calcaterra V, Comoli P, Locatelli F, Maccario R,
et al. Depletion of alloreactive T cells by a specific anti-interleukin-2
receptor p55 chain immunotoxin does not impair in vitro antileukemia
and antiviral activity. Blood 1999;93:3550-7.
[78] Guinan EC, Boussiotis VA, Neuberg D, Brennan LL, Hirano N,
Nadler LM, et al. Transplantation of anergic histoincompatible bone
marrow allografts. N Engl J Med 1999;340:1704-14.
[79] Aversa F, Tabilio A, Terenzi A, Velardi A, Falzetti F, Giannoni C, et al.
Successful engraftment of T-cell-depleted haploidentical three-loci
incompatible transplants in leukemia patients by addition of
recombinant human granulocyte colony-stimulating factor-mobilized
peripheral blood progenitor cells to bone marrow inoculum. Blood
1994;84:3948-55.
[80] Weiden PL, Sullivan KM, Flournoy N, Storb R, Thomas ED.
Antileukemic effect of chronic graft-versus-host disease: contribution
to improved survival after allogeneic marrow transplantation. N Engl
J Med 1981;304:1529-33.
[81] Horowitz MM, Gale RP, Sondel PM, Goldman JM, Kersey J, Kolb HJ,
et al. Graft-versus-leukemia reactions after bone marrow transplantation. Blood 1990;75:555-62.
[82] Ruggeri L, Capanni M, Urbani E, Perruccio K, Shlomchik WD, TostiA,
et al. Effectiveness of donor natural killer cell alloreactivity in
mismatched hematopoietic transplants. Science 2002;295:2097-100.
[83] Mackall CL, Granger L, Sheard MA, Cepeda R, Gress RE. T-cell
regeneration after bone marrow transplantation: differential CD45
isoform expression on thymic-derived versus thymic-independent
progeny. Blood 1993;82:2585-94.
[84] Mackall CL, Hakim FT, Gress RE. T-cell regeneration: all repertoires
are not created equal. Immunol Today 1997;18:245-51.
[85] Hazenberg MD, Otto SA, de Pauw ES, Roelofs H, Fibbe WE,
Hamann D, et al. T-cell receptor excision circle and T-cell dynamics
after allogeneic stem cell transplantation are related to clinical events.
Blood 2002;99:3449-53.
[86] Komanduri KV, St John LS, de Lima M, McMannis J, Rosinski S,
McNiece I, et al. Delayed immune reconstitution after cord Blood transplantation is characterized by impaired thymopoiesis and late memory
T-cell skewing. Blood 2007;110:4543-51.
[87] Cordonnier C. Fungal infections: current diagnosis and treatment.
Hematol J 2004;5(suppl3):S59-S62.
[88] Ljungman P, de la Camara R, Cordonnier C, Einsele H, Engelhard D,
Reusser P, et al. Management of CMV, HHV-6, HHV-7 and Kaposisarcoma herpesvirus (HHV-8) infections in patients with hematological
malignancies and after SCT. Bone Marrow Transplant 2008;42:1-4.
[89] Stocchi R, Ward KN, Fanin R, Baccarani M, Apperley JF. Management
of human cytomegalovirus infection and disease after allogeneic bone
marrow transplantation. Haematologica 1999;84:71-9.
[90] Walter EA, Greenberg PD, Gilbert MJ, Finch RJ, Watanabe KS,
Thomas ED, et al. Reconstitution of cellular immunity against
cytomegalovirus in recipients of allogeneic bone marrow by transfer of
T-cell clones from the donor. N Engl J Med 1995;333:1038-44.
[91] Kuehnle I, Huls MH, Liu Z, Semmelmann M, Krance RA, Brenner MK,
et al. CD20 monoclonal antibody (rituximab) for therapy of EpsteinBarr virus lymphoma after hemopoietic stem-cell transplantation.
Blood 2000;95:1502-5.
[92] Papadopoulos EB, Ladanyi M, Emanuel D, Mackinnon S, Boulad F,
Carabasi MH, et al. Infusions of donor leukocytes to treat Epstein-Barr
virus-associated lymphoproliferative disorders after allogeneic bone
marrow transplantation. N Engl J Med 1994;330:1185-91.
[93] OReilly RJ, Small TN, Papadopoulos E, Lucas K, Lacerda J,
Koulova L. Biology and adoptive cell therapy of Epstein-Barr virusassociated lymphoproliferative disorders in recipients of marrow
allografts. Immunol Rev 1997;157:195-216.
18
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Hmatologie
Allogreffe de cellules souches hmatopotiques : ralisation et complications 13-061-A-10
[94] Curtis RE, Rowlings PA, Deeg HJ, Shriner DA, Socie G, Travis LB,
et al. Solid cancers after bone marrow transplantation. N Engl J Med
1997;336:897-904.
[95] Carreras E, Bertz H, Arcese W, Vernant JP, Toms JF, Hagglund H, et al.
Incidence and outcome of hepatic veno-occlusive disease after blood or
marrow transplantation: a prospective cohort study of the European
Group for Blood and Marrow Transplantation. European Group for
Blood and Marrow Transplantation Chronic Leukemia Working Party.
Blood 1998;92:3599-604.
[96] Soci G, Salooja N, CohenA, RovelliA, Carreras E, LocasciulliA, et al.
Late Effects Working Party of the European Study Group for Blood and
Marrow Transplantation. Nonmalignant late effects after allogeneic
stem cell transplantation. Blood 2003;101:3373-85.
[97] Drobyski WR, Endean DJ, Klein JP, Hessner MJ. Detection of
BCR/ABL RNA transcripts using the polymerase chain reaction is
highly predictive for relapse in patients transplanted with unrelated
marrow grafts for chronic myelogenous leukaemia. Br J Haematol
1997;98:458-66.
[98] Kim DH, Jung HD, Kwack DH, Lee NY, Sohn SK, Baek JH, et al.
Predicting outcomes of HLA-identical allogeneic stem cell transplants
from variable number of tandem repeat disparity between donors and
recipients. Haematologica 2006;91:71-7.
[99] Dazzi F, Szydlo RM, Cross NC, Craddock C, Kaeda J, Kanfer E, et al.
Durability of responses following donor lymphocyte infusions for
patients who relapse after allogeneic stem cell transplantation for
chronic myeloid leukemia. Blood 2000;96:2712-6.
[100] Porter D, Levine JE. Graft-versus-host disease and graft-versusleukemia after donor leukocyte infusion. Semin Hematol 2006;43:
53-61.
[101] Cohen JL, Boyer O, Thomas-Vaslin V, Klatzmann D. Suicide genemediated modulation of graft-versus-host disease. Leuk Lymphoma
1999;34:473-80.
[102] Ciceri F, Bonini C, Marktel S, Zappone E, Servida P, Bernardi M, et al.
Antitumor effects of HSV-TK-engineered donor lymphocytes after
allogeneic stem-cell transplantation. Blood 2007;109:4698-707.
[103] Lazarus HM, Koc ON, Devine SM, Curtin P, Maziarz RT, Holland HK,
et al. Cotransplantation of HLA-identical sibling culture-expanded
mesenchymal stem cells and hematopoietic stem cells in hematologic
malignancy patients. Biol Blood Marrow Transplant 2005;5:389-98.
[104] Edinger M, Hoffmann P, Ermann J, Drago K, Fathman CG, Strober S,
et al. CD4+CD25+ regulatory T cells preserve graft-versus-tumor
activity while inhibiting graft-versus-host disease after bone marrow
transplantation. Nat Med 2003;9:1144-50.
[105] Hoffmann P, Edinger M. CD4+CD25+ regulatory T cells and graftversus-host disease. Semin Hematol 2006;43:62-9.
[106] Passweg JR, Tichelli A, Meyer-Monard S, Heim D, Stern M, Khne T,
et al. Purified donor NK-lymphocyte infusion to consolidate
engraftment after haploidentical stem cell transplantation. Leukemia
2004;18:1835-8.
[107] Miller JS, Soignier Y, Panoskaltsis-Mortari A, McNearney SA,
Yun GH, Fautsch SK, et al. Successful adoptive transfer and in vivo
expansion of human haploidentical NK cells in patients with cancer.
Blood 2005;105:3051-7.
N. Dhdin (nathalie.dhedin@psl.aphp.fr).
Service dhmatologie clinique, Hpital Piti-Salptrire, 83, boulevard de lHpital, 75651 Paris cedex 13, France.
Laboratoire dimmunologie cellulaire et tissulaire, Inserm UMR-S 945, Hpital Piti-Salptrire, 83, boulevard de lHpital, 75651 Paris cedex 13, France.
J.-P. Vernant.
Service dhmatologie clinique, Hpital Piti-Salptrire, 83, boulevard de lHpital, 75651 Paris cedex 13, France.
Toute rfrence cet article doit porter la mention : Dhdin N., Vernant J.-P. Allogreffe de cellules souches hmatopotiques : ralisation et complications.
EMC (Elsevier Masson SAS, Paris), Hmatologie, 13-061-A-10, 2010.
Disponibles sur www.em-consulte.com
Arbres
dcisionnels
Iconographies
supplmentaires
Vidos /
Animations
Documents
lgaux
Information
au patient
Hmatologie
2011 Elsevier Masson SAS. Tous droits rservs. - Document tlcharg le 14/06/2011 par Faculte de Medecine et Pharmacie RABAT (53125)
Informations
supplmentaires
Autovaluations
Cas
clinique
19
S-ar putea să vă placă și
- Anomalies Constitutionnelles de La Coagulation Prédisposant À La Thrombose 2007 EMCDocument18 paginiAnomalies Constitutionnelles de La Coagulation Prédisposant À La Thrombose 2007 EMCJankis KhanÎncă nu există evaluări
- DermatophytiesDocument35 paginiDermatophytiesJankis KhanÎncă nu există evaluări
- Cytologie Médullaire 2010 EMCDocument8 paginiCytologie Médullaire 2010 EMCJankis KhanÎncă nu există evaluări
- Streptocoques CoursDocument53 paginiStreptocoques CoursJankis KhanÎncă nu există evaluări
- Summer Scent Schubert-SerenadeDocument2 paginiSummer Scent Schubert-SerenadeJankis KhanÎncă nu există evaluări
- 2sc 2 09Document1 pagină2sc 2 09benjedidiachokriÎncă nu există evaluări
- API Sup Sie Wincc1Document2 paginiAPI Sup Sie Wincc1nattab34Încă nu există evaluări
- NgambayDocument197 paginiNgambayChristophe Garnier100% (1)
- m5t-10-200k-vfr-12 21 Aa XX 112 31-bd CompressedDocument8 paginim5t-10-200k-vfr-12 21 Aa XX 112 31-bd CompressedChef Sav Lift YdeÎncă nu există evaluări
- 1-Introduction Au Domaine Du DécisionnelDocument3 pagini1-Introduction Au Domaine Du DécisionnelMohamed HamritÎncă nu există evaluări
- Campagne Marketing WhatsappDocument6 paginiCampagne Marketing Whatsappking666Încă nu există evaluări
- Solution Exercice InterpolationDocument4 paginiSolution Exercice InterpolationNivek LenasarienÎncă nu există evaluări
- Exo13 CorigéDocument76 paginiExo13 CorigéYoussef EL MliliÎncă nu există evaluări
- 25 Stromausfall GD FRDocument13 pagini25 Stromausfall GD FRMAXÎncă nu există evaluări
- Wa0055.Document2 paginiWa0055.Reine KengniÎncă nu există evaluări
- Programme SAFEXDocument1 paginăProgramme SAFEXdjmidouÎncă nu există evaluări
- Construction Des RoutesDocument32 paginiConstruction Des RoutesOmar HabybyÎncă nu există evaluări
- Partie RhétoriqueDocument6 paginiPartie RhétoriqueManal YassineÎncă nu există evaluări
- Strength Training Workshop by SlidesgoDocument48 paginiStrength Training Workshop by Slidesgoblilita soundousÎncă nu există evaluări
- Cours 6 - AMDEC PDFDocument27 paginiCours 6 - AMDEC PDFOussama ElbattatÎncă nu există evaluări
- Process Legal de Construction en CI EAA 29 11 2023Document31 paginiProcess Legal de Construction en CI EAA 29 11 2023kvistel1987100% (1)
- Controle Qualité Produit Vf1Document58 paginiControle Qualité Produit Vf1Khaled KalaiÎncă nu există evaluări
- Electronique Numérique S1 2021Document52 paginiElectronique Numérique S1 2021Hamadoun Abba Kanne DialloÎncă nu există evaluări
- Exercices OndesDocument8 paginiExercices OndesAmine El AmeriÎncă nu există evaluări
- Cours Node JS 4Document2 paginiCours Node JS 4Mohamed Ramy MahjoubÎncă nu există evaluări
- Cours de Statisques Descriptives Et Inférentielles IUT2Document31 paginiCours de Statisques Descriptives Et Inférentielles IUT2Patman MutomboÎncă nu există evaluări
- Distributeru de BonbonsDocument22 paginiDistributeru de BonbonsKanouni OussamaÎncă nu există evaluări
- Exposé RFIDocument8 paginiExposé RFIEbenezer Egbakotan0% (1)
- 35 Conseils Pour Réussir Un Lotissement PDFDocument24 pagini35 Conseils Pour Réussir Un Lotissement PDFamical1955100% (1)
- Sohim 0398-3811 1985 Edc 7 1 939Document532 paginiSohim 0398-3811 1985 Edc 7 1 939Zanj Al-JahizÎncă nu există evaluări
- INTRODUCTION AU SYMBOLISME TOTÉMIQUE ANIMAL (PDF) (PDFDrive)Document170 paginiINTRODUCTION AU SYMBOLISME TOTÉMIQUE ANIMAL (PDF) (PDFDrive)cherruaultÎncă nu există evaluări
- 1dlstdix12 NDocument10 pagini1dlstdix12 NfranckyvesÎncă nu există evaluări
- Exam Proba ENIT Avril 2021Document3 paginiExam Proba ENIT Avril 2021Sadok BouzidÎncă nu există evaluări
- RapportDocument19 paginiRapportGuillaume TasseryÎncă nu există evaluări
- TP N°18.1 - Corrosion Et Protection Du FerDocument14 paginiTP N°18.1 - Corrosion Et Protection Du FerWael MaatougÎncă nu există evaluări