Documente Academic
Documente Profesional
Documente Cultură
Valoracion
Încărcat de
708170Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Valoracion
Încărcat de
708170Drepturi de autor:
Formate disponibile
1.- Objetivos.
- El objetivo de la practica es el de aprender a preparar soluciones
de concentracin dada, ya que la mayor parte de las reacciones qumicas tienen
lugar en forma de solucin.
Adems de determinar la concentracin de una disolucin problema usando otra
de concentracin conocida.
2.- Marco terico.- En la prctica se aprendi que es una solucin, que es
fraccin molar, molaridad, molalidad, normalidad y porcentaje en peso.
Adems de lo que es neutralizacin acido-base.
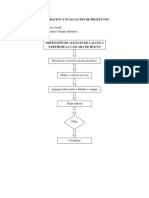
3.- Realizacin de la prctica.- Primero se disolvi en agua el carbonato de sodio
y el hidrxido de sodio, previamente calculando la cantidad que se deba de pesar.
Luego de conocer las cantidades se las peso en el vidrio de reloj y Lugo se las
llevo al matraz.
Luego de tener estas soluciones se coloco en la bureta el acido clorhdrico, las
otras dos soluciones de carbonato de sodio e hidrxido de sodio se les aadi un
poco de indicador para el carbonato el naranja de metilo y para el hidrxido la
fenoptaleina.
3.1.- Materiales.- Vidrio de reloj, vaso de precipitado, matraz aforado, varilla,
pipeta, matraz erlenmeyer, soporte de bureta, bureta y embudo.
3.2.- Reactivos.- Hidrxido de sido, carbonato de sodio, acido clorhdrico y los
indicadores.
3.3.- Equipo.- Balanza.
3.4.- Procesamiento experimental.- Se peso en el vidrio de reloj la cantidad de
hidrxido y carbonato de sodio calculado por formula se lo coloca en el matraz
aforado con un poco de agua.
Luego se colocan en los matraces aforados y se les adiciona un poco de indicador,
esto es para que al hacer verter el acido clorhdrico este cambie de color y de esta
forma neutralizar el acido o la base, esto se nota ya que cambia de color.
4.- Observaciones.- Se observa que es necesario calcular previamente la
cantidad necesaria que se debe de utilizar en una solucin.
Solo se calculo o se utilizaron los valores en valencias de normalidad.
Se ve que el color cambia de las dos soluciones a aadir el indicador y el acido
clorhdrico.
5.- Clculos y resultados.HCl = (1.19*36*10)/36.5 = 11.75
V=200ml
V = (200ml*0.1N)/11.74 = 1.7ml
NaCO; w= (0.1eq/L * 106gr/eq * 0.1L)/2
W= 0.53gr
V=100ml
NaOH; w= (0.1eq/L * 40gr/eq * 0.1L)/1
W= 0.4gr
V=100ml
Para la valoracin:
Para el carbonato de sodio (acido clorhdrico)
Concentracin = 0.1N
Volumen = 10ml
Volumen de acido clorhdrico gastado = 7.58ml (promedio)
Concentracin de acido clorhdrico = (0.1N * 10ml)/7.58ml = 0.13N
Para el hidrxido de sodio
Concentracin =?
Volumen = 100ml
Concentracin de hidro9xido de sodio = (0.13N * 9.98ml)/10ml = 0.13N
6.- Conclusiones.- Sobre mis observaciones concluyo que:
Del clculo esto es necesario ya nos ayuda a saber cuanto se debe de utilizar una
cantidad de un reactivo para una determinada solucin.
Sobre el uso solo de la valoracin en normalidad, concluyo que esto se debe a
que se usa este valor en la valoracin.
Por ultimo sobre el cambio de color, este cambia al aadir el indicador y el acido
clorhdrico, para el carbonato de sodio, este es de color naranja el verter gota a
gota el acido clorhdrico este cambia a un color rojo esto nos dice que esta siendo
neutralizado. Mientras que para el hidrxido de sodio, este es de color rosa y se
vuelve incoloro, ya que el indicador esta haciendo efecto.
7.- Cuestionario.1.- Por qu no se utiliza una probeta para la preparacin de soluciones?
R.- No se hace uso de la probeta ya que no se sabe cuanto o no se puede calcular
cuanto del compuesto hay que colocar.
2.- Defina los siguientes trminos; solote solvente.
R.- Soluto, segn yo el soluto es el que se disuelve, esta en pequeas cantidades,
es solid.
Solvente, o disolvente es el que esta en mayor cantidad, esta en mayor cantidad
que el soluto y esta en estado liquido.
3.- Qu es una reaccin de neutralizacin?
R.- Es una reaccin en la que existe un acido y se lo combina con una base y de
esta forma la base neutralice al acido y se conviertan en sal.
4.- Justifique el empleo de la fenoptaleina como indicador.
R.- Se hace uso de la fenoptaleina por que este hace cambiar de color a todos los
cidos.
S-ar putea să vă placă și
- Caso BimboDocument26 paginiCaso BimboManuel Puemape Vallejos100% (1)
- 7p's de Coca ColaDocument2 pagini7p's de Coca ColaChuck AndradeÎncă nu există evaluări
- Aditivos AlimentariosDocument60 paginiAditivos AlimentariosRozaMagallonÎncă nu există evaluări
- Ley de BoyleDocument6 paginiLey de Boyle708170Încă nu există evaluări
- Obtencion Del Estaño Metalico A Partir Del Mineral CasiteritaDocument5 paginiObtencion Del Estaño Metalico A Partir Del Mineral Casiterita708170Încă nu există evaluări
- ViscosidadDocument6 paginiViscosidad708170Încă nu există evaluări
- Calor Especifico de LiquidosDocument8 paginiCalor Especifico de Liquidos708170Încă nu există evaluări
- Constante de EquilibrioDocument5 paginiConstante de Equilibrio708170Încă nu există evaluări
- Calor EspecificoDocument7 paginiCalor Especifico708170Încă nu există evaluări
- Uso de Graficas en La Parte ExperimentalDocument2 paginiUso de Graficas en La Parte Experimental708170Încă nu există evaluări
- Propiedades Magnéticas de La MateriaDocument12 paginiPropiedades Magnéticas de La Materia708170Încă nu există evaluări
- Simbologia y Manejo de InstrumentosDocument15 paginiSimbologia y Manejo de Instrumentos708170Încă nu există evaluări
- Calor de CombustionDocument5 paginiCalor de Combustion708170Încă nu există evaluări
- Estudio de La Cinética de Oxidación de Etanol Por Medio de Espectrofotometría VisibleDocument7 paginiEstudio de La Cinética de Oxidación de Etanol Por Medio de Espectrofotometría Visible708170Încă nu există evaluări
- Ejemplo de Manual de Calidad ISO-9001Document17 paginiEjemplo de Manual de Calidad ISO-9001708170Încă nu există evaluări
- Termodinámica de Las Pilas GalvánicasDocument8 paginiTermodinámica de Las Pilas Galvánicas708170Încă nu există evaluări
- Electroquímica Conductividad de DisolucionesDocument8 paginiElectroquímica Conductividad de Disoluciones708170Încă nu există evaluări
- Fundicion de Precipitados de OroDocument15 paginiFundicion de Precipitados de OroCarlos Tolentino Tazo100% (3)
- Propiedades Quimicas de Hidrocarburos AromaticosDocument7 paginiPropiedades Quimicas de Hidrocarburos Aromaticos708170Încă nu există evaluări
- Refracción de La LuzDocument12 paginiRefracción de La Luz708170Încă nu există evaluări
- Documento CompletoDocument10 paginiDocumento Completo708170Încă nu există evaluări
- HNO de Moles ZN Moles HNO Moles ZN G ZN Mol ZN GDocument4 paginiHNO de Moles ZN Moles HNO Moles ZN G ZN Mol ZN G708170Încă nu există evaluări
- OtrosDocument8 paginiOtros708170Încă nu există evaluări
- Solicit UdDocument1 paginăSolicit Ud708170Încă nu există evaluări
- Sistema de Gestión de La CalidadDocument2 paginiSistema de Gestión de La Calidad708170Încă nu există evaluări
- AplicacionesDocument7 paginiAplicaciones708170Încă nu există evaluări
- Electroquímica Conductividad de DisolucionesDocument8 paginiElectroquímica Conductividad de Disoluciones708170Încă nu există evaluări
- Universidad Autónoma "Tomas Frias" Facultad de Ciencias Puras Carrera de QuímicaDocument15 paginiUniversidad Autónoma "Tomas Frias" Facultad de Ciencias Puras Carrera de Química708170Încă nu există evaluări
- Método Potenciométricas DirectasDocument5 paginiMétodo Potenciométricas Directas708170Încă nu există evaluări
- Default IdDocument1 paginăDefault IdHenry Franz Flores NicolásÎncă nu există evaluări
- Obtención de Acetato de AmonioDocument1 paginăObtención de Acetato de Amonio708170Încă nu există evaluări
- Determinación de Na y KDocument10 paginiDeterminación de Na y K708170Încă nu există evaluări
- Universidad Autónoma "Tomas Frias" Facultad de Ciencias Puras Carrera de QuímicaDocument9 paginiUniversidad Autónoma "Tomas Frias" Facultad de Ciencias Puras Carrera de Química708170Încă nu există evaluări
- Factibilidad Tecnica y Economica de La Produccion de AlcaparrasDocument39 paginiFactibilidad Tecnica y Economica de La Produccion de AlcaparrasBodega Saldungaray100% (1)
- Ingredientes para Pizza CaseraDocument10 paginiIngredientes para Pizza CaseraEddy Marcelo Marze GonzalesÎncă nu există evaluări
- Manuaal de Getion de Almacen y ComprasDocument109 paginiManuaal de Getion de Almacen y ComprasBar BittersÎncă nu există evaluări
- NescafeDocument23 paginiNescafeDiego NC100% (1)
- Práctica Iv Equilibrio QuímicoDocument7 paginiPráctica Iv Equilibrio QuímicoVivi Mar CSiÎncă nu există evaluări
- Tecnicas para Trabajar Con FoamiDocument4 paginiTecnicas para Trabajar Con FoamiElena Domínguez MarínÎncă nu există evaluări
- Maquinado Convencional Por Arranque de VirutaDocument30 paginiMaquinado Convencional Por Arranque de VirutaAlejandro Flope100% (3)
- INFORME 1 - Procedimiento ExperimentalDocument6 paginiINFORME 1 - Procedimiento ExperimentalMaura Bazan CarhuaricraÎncă nu există evaluări
- Propuesta de Valor CNCDocument1 paginăPropuesta de Valor CNCValentina Arrieta VelascoÎncă nu există evaluări
- Cotizacion Sillas GerencialesDocument10 paginiCotizacion Sillas GerencialesAbelardo ContrerasÎncă nu există evaluări
- Dotación Del AguaDocument9 paginiDotación Del AguaEder MolinaÎncă nu există evaluări
- Procesos de Produccion TextilDocument42 paginiProcesos de Produccion TextilJoel Julca Garcia100% (1)
- PERFILDocument38 paginiPERFILeverthÎncă nu există evaluări
- FLUJO GRAMA Nectar - MermaladaDocument4 paginiFLUJO GRAMA Nectar - MermaladaAJ CarlosÎncă nu există evaluări
- Gestion de RestaurantesDocument15 paginiGestion de RestaurantesDiana CastilloÎncă nu există evaluări
- Empaques Camara de ComercioDocument49 paginiEmpaques Camara de ComercioClau_CanoÎncă nu există evaluări
- Procesamiento de La Pasta de TomateDocument13 paginiProcesamiento de La Pasta de TomateDavid PompaÎncă nu există evaluări
- Tema 5.defectos en SoldaduraDocument83 paginiTema 5.defectos en SoldaduraDeivid William Torres100% (1)
- Tipos de CementoDocument20 paginiTipos de CementoMiguel Angel Diaz Vargas100% (1)
- Lista de Materiales Sala CunaDocument1 paginăLista de Materiales Sala CunaJardin Infantil PulmahueÎncă nu există evaluări
- Golosinas y Productos de Confitería PDFDocument60 paginiGolosinas y Productos de Confitería PDFFelipe Florian Santiago GomezÎncă nu există evaluări
- Enzimas en Los AlimentosDocument40 paginiEnzimas en Los AlimentosNeftalí CorralejoÎncă nu există evaluări
- Balance de Masa y Energía para La Elbaboración de ManjarDocument6 paginiBalance de Masa y Energía para La Elbaboración de ManjarEdison OrtizÎncă nu există evaluări
- Certificacion Tipo Inspeccion Federal Tif 2014 PDFDocument29 paginiCertificacion Tipo Inspeccion Federal Tif 2014 PDFJonÎncă nu există evaluări
- Iknitts - Patron para Tejer Un Cardigan Con Botones y Bolsillos PDFDocument6 paginiIknitts - Patron para Tejer Un Cardigan Con Botones y Bolsillos PDFMacarena Ailing Vidal Vargas100% (1)
- Plan de NegociosDocument20 paginiPlan de NegociosElvis Yonatan BCÎncă nu există evaluări
- Chorizo VerdeDocument14 paginiChorizo VerdeZayra Nayeli Molina Cozar100% (1)