Documente Academic
Documente Profesional
Documente Cultură
DS
Încărcat de
Cristian Ccarhuas PerezDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
DS
Încărcat de
Cristian Ccarhuas PerezDrepturi de autor:
Formate disponibile
Destilacin Simpleo
Laboratorio de Procesos de Separacino
Equipo 4
Verano 2008
Mxico D.F., 4 de junio de 2008e
Alumnos:
Francisco Jos Guerra Millnea
fjguerra@mac.com
Cecilia Malln Wiecherse
ceci mallen@yahoo.com
Adelwart Struck Garza
adelwartsg@hotmail.com
Tamara Varela Vega
tammy varela@yahoo.com
Asesor:
M.C. Angel G. Zitlalpopoca Soriano
angelgzs@hotmail.com
Resumen
La destilacin simple es una operacin unitaria muy utilizada para lle-oo
var a cabo separaciones parciales de mezclas con componentes voltiles.a
Esta operacin muestra la importancia de explotar las diferentes propieda-o
des de los componentes que forman una mezcla, ya que de manera sencilla
se pueden separar sin tener que recurrir a mtodos quemicos o fsicos msa
complicados. A lo largo de la prctica se determinaron los diagramas dea
equilibrio etanol-agua a diferentes presiones y se compararon con los valores experimentales. Asimismo se obtuvo la concentracin promedio tericaoo
y la experimental. A lo largo del reporte se precisa la metodolog seguida.a
Universidad Iberoamericana
Indice
Laboratorio de Procesos de Separacin, Verano 2008o
1. Objetivos
2. Introduccino
3. Marco Tericoo
4. Procedimiento Experimental
5. Resultados
6. Anlisisa
12
7. Conclusiones
14
A. Tablas de Interpolacino
14
B. Cdigo de Matlab utilizadoo
14
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
1.
Laboratorio de Procesos de Separacin, Verano 2008o
Objetivos
Comprender y analizar los principios bsicos de la destilacin simple in-ao
termitente, utilizando las ecuaciones y diagramas pertinentes.
Determinar en forma prctica el comportamiento de una mezcla etanol-a
agua al ser sometida a este tipo de destilacin.o
2.
Introduccino
La destilacin simple es una operacin en la cual se produce la vaporizacinooo
de un material por la aplicacin de calor; el mtodo es empleado en la industriaoe
de capacidad moderada y pequea, para llevar a cabo separaciones parciales den
los componentes ms voltiles de mezclas de laaquidos miscibles.
Normalmente, la mezcla lquida es cargada en lotes a un recipiente y sometida a ebullicin. Los vapores que se desprenden se eliminan continuamente, seo
condensan y se recolectan sin permitir que tenga lugar ninguna condensacino
parcial ni retorno al recipiente en donde se lleva a cabo el calentamiento y ebullicin de la mezcla.o
La primera porcin del destilado ser la ms rica en el componente msoaaa
voltil y conforme contina la destilacin, el producto evaporado se va empo-auo
breciendo. Por lo tanto, el destilado puede recolectarse en varios lotes separados,
llamados fracciones, obtenindose as una serie de productos destilados de dife-e
rente grado de pureza.
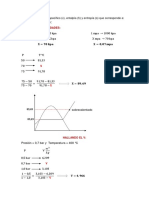
El principio de la destilacin simple intermitente, puede ilustrarse fcilmenteoa
haciendo referencia a un diagrama de equilibrio lquido - vapor, como el que se
muestra en la gura 1. En ste sistema, si una mezcla que contiene 25 % mole
de alcohol etlico en agua se carga en el recipiente hervidor de un sistema de
destilacin simple intermitente y se calienta, la mezcla empezar a ebullir a unaoa
temperatura de 82.5 C. A sta temperatura, la composicin del vapor en equi-eo
librio con el lquido es de 55 % mol de alcohol etlico en agua.
As conforme la vaporizacin transcurre, se separan y condensan los vapores,o
y la cantidad del lquido en el recipiente va disminuyendo progresivamente, al
igual que el contenido del componente ms voltil en el laaquido y el vapor, y la
temperatura de ebullicin del loquido en el recipiente va aumentando.
El aparato utilizado para la destilacin simple en el laboratorio es el alam-o
bique, como se muestra en la Figura 2.1. Consta de un recipiente donde se
almacena la mezcla a la que se le aplica calor, un condensador donde se enfran
los vapores generados, llevndolos de nuevo al estado laquido y un recipiente
donde se almacena el lquido concentrado.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Figura 2.1: Diagrama esquemtico de un equipo de destilacin simple.ao
Normalmente en la industria esta operacin se realiza por lotes cargndoseoa
a un recipiente y sometindose a ebullicin. Los vapores que se desprenden seeo
eliminan continuamente, se condensan y se recolectan.
La primera porcin del destilado ser la ms rica en el componente msoaaa
voltil y conforme contina la destilacin, el producto evaporado se va empo-auo
breciendo. Por lo tanto, el destilado puede recolectarse en varios lotes separados,
llamados fracciones, obtenindose as una serie de productos destilados de dife-e
rente grado de pureza.
En el caso de la mezcla etanol-agua nos encontramos con una destilacino
azeotrpica, ya que usando tcnicas normales de destilacin, el etanol slo pue-oeoo
de ser puricado a aproximadamente el 95 %. Una vez que se encuentra en una
concentracin de 95/5 % etanol-agua, los coecientes de actividad del agua y delo
etanol son iguales, entonces la concentracin del vapor de la mezcla tambin esoe
de 95/5 % etanol-agua, por lo tanto destilaciones posteriores son inefectivas.
Cuando se requieren concentraciones de alcohol mayores, por ejemplo cuando
se usa como aditivo para la gasolina, el azetropo 95/5 % debe romperse parao
lograr una mayor concentracin. Algunos de los mtodos para lograrlo son losoe
siguientes:
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Adicin de un material como agente de separacin. Por ejemplo, la adi-oo
cin de benceno a la mezcla cambia la interaccin molecular y elimina eloo
azetropo. La desventaja, es la necesidad de otra separacin para retiraroo
el benceno.
La variacin de presin en la destilacin. Se basa en el hecho de queooo
un azetropo depende de la presin y tambin que no es un rango deooe
concentraciones que no pueden ser destiladas, sino el punto en el que los
coecientes de actividad se cruzan. Si el azetropo se salta, la destilacinoo
puede continuar.
3.
Marco Tericoo
El vapor que se desprende en una destilacin diferencial verdadera, est enoa
cualquier momento en equilibrio con el lquido del cual se forma, pero cambia
continuamente de composicin. Por lo tanto, la aproximacin matemtica debeooa
ser diferencial.
Si suponemos que en cualquier momento durante el desarrollo de la destilacin hay L moles de loquido en el destilador, con una composicin x a y queo
se evapora una cantidad V de moles en el destilador, de composicin y a (eno
equilibrio con xa ), se tiene el siguiente balance de materia:
Entrada Salida + Generacin = Acumulacinoo
Como no hay entrada continua al sistema ni reaccin en el mismo, los trmi-oe
nos de entrada y generacin se elimina de modo que el balance global queda:o
tt
(0 V ) t = L|tt L|t
(3.1)
Aplicndose los teoremas de valor medio del clculo diferencial e integral seaa
tiene:
(t t t) (V ) |z = (t t t)
L
tz
(3.2)
En donde z es un punto dentro del intervalo t + t.
Dividiendo entre t cuando el lmite t 0 y para cualquier t:
(V ) =
L
tz
(3.3)
Por otro lado el balance para el componente A es el siguiente:
tt
(0 V yd) t = Lx|tt Lx|t
(3.4)
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
De igual manera llegamos a la siguiente ecuacin:o
Lx
t
(V yd) =
(3.5)
Lx
t
Sustituyendo (3.3) en (3.5) y separando la integral
L
t
se tiene:
L (x) x (L)
tt
Multiplicando por dt, y reagrupando trminos:e
yd =
(yd x) L =
L
=
L
L
L0
L
L
Lx
(3.7)
x
yd x
xL
=
xL0
(3.6)
x
yd x
(3.8)
(3.9)
Integrando el lado izquierdo de la ecuacin (3.9):o
xL
L
x
ln=
yd x
xL0
L0
El lado derecho de la ecuacin puede ser integrado directamente si y puedeo
expresarse en trminos de x, como en el caso especial donde se pueda aplicar lae
ley de Raoult o la de Henry, o bien entre lmites de composicin en donde existeo
una relacin casi lineal entre x y y.o
(3.10)
Cuando se dispone de datos experimentales piloto o de planta, el mtodo msea
simple y general para evaluar esta integral es el grco, en donde se asientana
1valores de yx vs. x y se determina el rea bajo la curva entre los lamites xL 0
y xL.
4.
Procedimiento Experimental
La prctica se realiz armando un equipo de destilacin simple, como seaoo
muestra en la Figura 2.1. Se colocaron 200mL de una mezcla compuesta por
50 % agua y 50 % alcohol en volumen. El alcohol utilizado ten una concentra-a
cin del 94 % en volumen.o
Se comenz a calentar el equipo para lograr separar la mezcla por medio deo
una destilacin, es decir, aprovechando las diferencias entre el punto de ebulli-o
cin de los componentes. Al caer la primera gota, se registr la temperatura yoo
se midi el o ndice de refraccin tanto del residuo como del destilado, repitiendoo
esto cada C que aumentaba. Se midi la densidad, el volumen inicial y nal,o
de la mezcla, del residuo y del destilado.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
5.
Laboratorio de Procesos de Separacin, Verano 2008o
Resultados
Los resultados experimentales se muestran en las Tablas 5.1 5.2. El % peso
se obtuvo utilizando una correlacin grca proporcionada por el Instructor eoa
interpolando como se indica en la Tabla A.1 del Apndice A.e
Tabla 5.1: Datos Experimentales.
Teb
[ C]
83
84
85
86
87
88
89
89
yprom
Destilado
Indice de% Peso
Refraccino
[ %]
1.363854.9864
1.360844.1210
1.361044.6430
1.359640.9894
1.355832.4347
1.351024.6053
1.348821.5900
1.343614.6675
1.346218.0882
fr mol
[]
0.2150
0.1725
0.1745
0.1603
0.1268
0.0962
0.0844
0.0573
0.0707
Residuo
Indice de% Peso
Refraccino
[ %]
1.33482.2442
1.33461.9325
1.33461.9325
1.33400.9974
1.33380.6857
1.33360.3740
1.33300.0000
1.33300.0000
fr mol
[]
0.0088
0.0076
0.0076
0.0039
0.0027
0.0015
0.0000
0.0000
Tabla 5.2: Datos Experimentales.
Volumen:
Densidad:
Destilado
18 mL
g0.950 mL @ 19.1 C
Residuo
172 mL
g0.972 mL @ 72.0 C
Utilizando el cdigo de Matlab que se muestra en el Apndice B es posibleoe
obtener los diagramas de equilibrio para la mezcla etanol-agua a diferentes temperaturas. Las Figuras 5.1 - 5.4 muestran los resultados obtenidos. La presino
de operacin se calcul utilizando la ecuacin de Antoine para la temperaturaooo
de la primera gota de destilado, como se muestra en el cdigo del Apndice B.oe
Las Figuras 5.1 - 5.3 muestran la comparacin del equilibrio ideal, real y ex-o
perimental a una determinada presin, mientras que la Figura 5.4 compara loso
equilibrios real e ideal a presin atmosfrica y la presin de operacin calculada.oeoo
1Las
Figuras 5.5 - 5.7 muestran la grca yx vs. x para las diferentes pre-a
1siones estudiadas. La Figura 5.8 muestra la grca yx vs. x para los
valoresa
experimentales. Estas grcas fueron utilizadas para calcular la integral de laa
ecuacin (3.10).o
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Figura 5.1: Diagrama Txy para etanol-agua a 760mmHg.
Figura 5.2: Diagrama Txy para etanol-agua a 550mmHg.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Figura 5.3: Diagrama Txy para etanol-agua a 913mmHg.
Figura 5.4: Diagrama Txy para etanol-agua a 760mmHg y 913mmHg.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Figura 5.5: Diagrama
1
yx
vs. x a 760mmHg.
Figura 5.6: Diagrama
1
yx
vs. x a 550mmHg.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
10
Universidad Iberoamericana
Figura 5.7: Diagrama
Figura 5.8: Diagrama
F. J. Guerra, C. Malln, A. Struck, T. Varelae
Laboratorio de Procesos de Separacin, Verano 2008o
1
yx
1
yx
vs. x a 913mmHg.
vs. x experimental.
11
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Con ayuda del cdigo que se muestra en el Apndice B se calcul el reaoeoa
bajo de la curva de las Figuras 5.5 - 5.8. La Tabla 5.3 muestra los valores de la
integral obtenidos por los distintos mtodos. La presin corresponde unicamenteeo
al valor terico.o
Tabla 5.3: Integrales.
Presino
760mmHg
550mmHg
913mmHg
Tericoo
-1.8657
-1.9130
-2.0374
Lln L0
Experimental
-0.1508
-0.0661
Con ayuda del cdigo que se muestra en el Apndice B es posible calcularoe
la concentracin terica promedio. La concentracin experimental se obtuvoooo
interpolando, utilizando el valor de la Tabla 5.1, como se muestra en la Tabla
A.1. La Tabla 5.4 muestra los valores de la concentracin del destilado. Lao
presin corresponde unicamente al valor calculado.o
Tabla 5.4: Concentracin.o
Presino
760mmHg
550mmHg
913mmHg
6.
Calculado
[frmol ]
0.0862
0.1090
0.2475
Experimental
[frmol ]
0.0707
%error
[ %]
21.93
54.11
250.04
Anlisisa
A lo largo del reporte se utilizan tres diferentes presiones para realizar todos
los clculos. La atmosfrica (760mmHg), la [resin terica en Santa Fe, Ciudadaeoo
de Mxico (550mmHg) y la presin de operacin real (913mmHg), calculadaeoo
con la ecuacin de Antoine y la temperatura de la primera gota de destilado.o
Es evidente que el resultado obtenido es absurdo, pues la Universidad Iberoamericana se encuentra a aproximadamente 2600 msnm. Es posible que debido a
la tensin supercial de los loquidos, la primera gota haya resbalado lentamente
por la pared del equipo, demorando as la espera y permitiendo un aumento sig-
nicativo en la temperatura. No obstante, como se mencion, todos los clculosoa
se realizaron con las tres presiones.
Si se observan las Figuras 5.1 - 5.3 es posible observar que la aproximacin de Margules corrige signicativamente el equilibrio ideal para una mezclao
de etanol-agua. Asimismo se observa la formacin de un azetropo al llegaroo
F. J. Guerra, C. Malln, A. Struck, T. Varelae
12
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
a una concentracin de aproximadamente 95 %. Para nes de los diagramas, elo
azetropo se dubuj cuando la diferencia entre x y y fuera menor o igual a 0.025.oo
De esta forma es posible armar que ya no existe una diferencia signicativa
entre las dos curvas del diagrama y por ello se consider para nes prcticos co-oa
mo azetropo. Asimismo es posible armar que a menor presin, menor ser laooa
temperatura del azetropo. La Figura 5.4 muestra claramente cmo a menoroo
presin, se desplaza el equilibrio hacia abajo y por ello disminuye la tempera-o
tura del azetropo.o
Los datos experimentales se muestran en las Figuras 5.1 - 5.3. Como era de
esperarse, los datos no corresponden en lo absoluto con el equilibrio terico ao
913mmHg. No obstante, se ajustan de forma aceptable al equilibrio a 550mmHg
y cabe recordar que la presin de operacin en Santa Fe deber ser cercana aooa
los 550mmHg. Si bien no se tiene una curva sucientemente abundante como
para cubrir todo el equilibrio, es posible argumentar que las temperaturas bajas
no se pudieron obtener, pues se estaba en espera de la primera gota. El hecho de
que la gota haya salido del equipo ms de 10 C despus de lo esperado, afectaae
la presin calculada, ms no el equilibrio, pues la concentracin se midi direc-oaoo
tamente de las gotas que caan.
Para el caso de las integrales, las Figuras 5.5 - 5.7 muestran que las curvas
a diferentes presiones son muy similares. No nbstante, con base en la Tabla 5.3
no es posible mencionar una relacin directa entre la presin y la magnitud deloo
valor. El valor experimental obtenido es un orden de magnitud ms pequeoan
que los valores tericos. Esto no es de sorprender si se observa la Figura 5.8. Alo
haber obtenido pocos valores para la muestra experimental se tiene una curva
igualmente pequea. Automticamente, por esto, el valor de la integral ser denaa
menor magnitud. Nuevamente se hace maniesto el error de la temperatura de
la primera gota. No obstante, los dos valores experimentales, el del lado izquierdo de la ecuacin (3.10) y el valor de la integral se encuentran en el mismoo
orden de magnitud.
La concentracin promedio del destilado se muestra en la Tabla 5.4. Si bieno
los errores porcentuales son considerables, el orden de magnitud de los resultados es el mismo. Curiosamente el menor error, del 20 % se obtiene contra el valor
terico de la concentracin promedio a 760mmHg. Se esperar que el error aooa
550mmHg fuera menor, pues una presin ms cercana a la que se est operando.oaa
Para el clculo de la concentracin promedio se asumi que en el rango de tem-aoo
peraturas experimentales la distribucin de las gotas de destilado es homognea,oe
es decir, que por cada C que aumenta la temperatura cae un nmero determi-u
nado de gotas y que la concentracin de las mismas var linealmente. Debidooa
a estas asunciones no resulta sorpresivo que los porcentajes de error sean de tal
magnitud.
F. J. Guerra, C. Malln, A. Struck, T. Varelae
13
Universidad Iberoamericana
7.
Laboratorio de Procesos de Separacin, Verano 2008o
Conclusiones
La destilacin simple es una operacin unitaria muy utilizada para llevar aoo
cabo separaciones parciales de mezclas con componentes voltiles. Esta opera-a
cin muestra la importancia de explotar las diferentes propiedades de los com-o
ponentes que forman una mezcla, ya que de manera sencilla se pueden separar
sin tener que recurrir a mtodos quemicos o fsicos ms complicados.a
La correlacin de margules es una herramiente muy util para transformaro
una curva de equilibrio ideal en una curva, que si bien no es real, se aproxima
considerablemente a la realidad. Esta correccin nos permite ver el azetropo,oo
situacin imposible en un diagrama ideal.o
Al disminuir la presin de operacin la curva de equilibrio se desplaza haciaoo
abajo y a la izquierda; de esta forma disminuye tambin la temperatura dele
azetropo.o
Con base en los resultados obtenidos es posible concluir que se llev a caboo
una experimentacin correcta. Los errores si bien se pudieron haber minimizadoo
son intrnsecos a la experimentacin. No obstante, los objetivos fueron satisfe-o
chos. El equilibrio para la mezcla etanol-agua no slo se calcul de forma ideal,oo
sino que se utiliz la correccin de Margules para obtener resultados mucho msooa
cercanos a la realidad.
Logic will get you from A to B.
Imagination will take you everywhere.
- A. Einstein
Referencias
[1] Robert H. Perry, Don W. Green, and James O. Maloney. Perrys Chemical
Engineers Handbook. McGraw-Hill, 7th edition, 1999.
A.
Tablas de Interpolacino
B.
Cdigo de Matlab utilizadoo
%% Laboratorio de Procesos de Separacion
% Verano 2008
%
%
% Programa para obtener la grafica T xy
% para agua y etanol ideal y utilizando
% la correccion de Margules
F. J. Guerra, C. Malln, A. Struck, T. Varelae
14
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
Tabla A.1: Tabla de Interpolacin.o
Destilado
Residuo
x
1.3638
1.3608
1.3610
1.3596
1.3558
1.3510
1.3488
1.3436
1.3348
1.3346
1.3346
1.3340
1.3338
1.3336
1.3330
1.3330
1.3462
x1
1.3615
1.3588
1.3588
1.3588
1.3544
1.3508
1.3479
1.3411
1.3334
1.3334
1.3334
1.3334
1.3334
1.3334
1.3334
1.3334
1.3458
x2
1.3641
1.3615
1.3615
1.3615
1.3565
1.3519
1.3492
1.3458
1.3372
1.3372
1.3372
1.3372
1.3372
1.3372
1.3372
1.3372
1.3479
y1
46.0000
38.9800
38.9800
38.9800
29.8700
24.2100
20.3500
11.3300
0.0000
0.0000
0.0000
0.0000
0.0000
0.0000
0.0000
0.0000
17.5600
y2
56.0900
46.0000
46.0000
46.0000
33.8200
26.0600
22.1100
17.5600
6.0000
6.0000
6.0000
6.0000
6.0000
6.0000
6.0000
6.0000
20.3500
y
54.9864
44.1210
44.6430
40.9894
32.4347
24.6053
21.5900
14.6675
2.2442
1.9325
1.9325
0.9974
0.6857
0.3740
0.0000
0.0000
18.0882
Destilado Final
% Rene Huerta
% noviembre 2004
%
%
% modificado por:
% Francisco Jose Guerra Millan
%%
Inicio
function DS
clc; clear all;
global A B C T Pt AM i j
% indice para las figuras
fig=1;
%% Datos Experimentales
L0
L
= 200; % mL (volumen inicial)
= 172; % mL (volumen residuo)
F. J. Guerra, C. Malln, A. Struck, T. Varelae
15
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
x0
xf
= 0.47; % frmol (concentracion inicial)
= 0.0015; % frmol (concentracion residuo)
Texp
= [83 84 85 86 87 88 89 89]; % [oC]
xdest = [0.2150 0.1725 0.1745 0.1603 0.1268 0.0962 0.0844 0.0573];
xres
= [0.0088 0.0076 0.0076 0.0039 0.0027 0.0015 0.0000 0.0000];
%% Datos
% nombre de los componentes
componente1=[etanol];
componente2=[agua];
% Constantes de Antoine para componente1 y componente2
% ln(Ps(i)) = A(i) - B(i) / (C(i)+T)
A = [8.1122 8.0713];
B = [1592.864 1730.630];
C = [226.184 233.426];
% Coeficientes de Margules
AM=[1.6022 0.7947]; % [A12 A21]
% Calculo de la presion real
Tebexp = Texp(1);
Preal = 10^(A(1)-B(1)/(C(1)+Tebexp));
% Pt = preion de trabajo
Pt = [760 550 Preal]; % mmHg (presion de trabajo [atm ... ref])
for j = 1:length(Pt),
for i = 1:length(A),
Teb(i,j) = B(i)/(A(i)-log10(Pt(j)))-C(i);
end
Trange = linspace(Teb(1,j),Teb(2,j));
F. J. Guerra, C. Malln, A. Struck, T. Varelae
16
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
T(:,j) = Trange;
for i = 1:length(T)
Ps1(i,j) = 10^(A(1)-B(1)/(C(1)+T(i,j)));
Ps2(i,j) = 10^(A(2)-B(2)/(C(2)+T(i,j)));
K1(i,j) = Ps1(i,j)/Pt(j);
K2(i,j) = Ps2(i,j)/Pt(j);
x1(i,j) = (1-K2(i,j))/(K1(i,j)-K2(i,j));
x2(i,j) = (1-K1(i,j))/(K2(i,j)-K1(i,j));
y1(i,j) = K1(i,j)*(K2(i,j)-1)/(K2(i,j)-K1(i,j));
y2(i,j) = K2(i,j)*(K1(i,j)-1)/(K1(i,j)-K2(i,j));
xini = [x1(i,j) x2(i,j) y1(i,j) y2(i,j)];
[fun val flag] = fsolve(@margules,xini);
xM1(i,j) = fun(1);
xM2(i,j) = fun(2);
yM1(i,j) = fun(3);
yM2(i,j) = fun(4);
funx(i,j) = 1/(yM1(i,j)-xM1(i,j));
Tc(i,j) = T(i,j); % eventual conversion K --> C
end
% para los limites de la inegral
[val0(j) pos0(j)] = min(abs(xM1(:,j)-x0));
[valf(j) posf(j)] = min(abs(xM1(:,j)-xf));
% para la concentracion promedio
[val00(j) pos00(j)] = min(abs(T(:,j)-Texp(1)));
[valff(j) posff(j)] = min(abs(T(:,j)-Texp(end)));
pos = ceil(length(yM1(:,j))/2);
while yM1(pos,j)-xM1(pos,j)>0.025,
pos=pos-1;
end
az=Tc(pos,j);
figure(fig)
plot(x1(:,j),Tc(:,j),:,xM1(:,j),Tc(:,j),xres,Texp,-.)
hold on
plot([0 1],[Tc(pos,j) Tc(pos,j)],k--,LineWidth,1.5)
F. J. Guerra, C. Malln, A. Struck, T. Varelae
17
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
hold on
plot(y1(:,j),Tc(:,j),:,yM1(:,j),Tc(:,j),xdest,Texp,-.)
title([Diagrama Txy para componente1 - componente2...
@ num2str(Pt(j)) mmHg],...
FontSize,12,FontWeight,Bold)
xlabel([fraccion mol componente1])
ylabel(Temperatura [^oC])
axis([0 1 floor(Tc(1,j)) ceil(Tc(end,j))])
legend(Ideal,Margules,...
Experimental,[Azeotropo @ num2str(Tc(pos,j)) ^oC],0)
grid
hold off
fig=fig+1;
end
%% Ultimos Plots
% Comparacion
figure(fig)
title([Diagrama Txy para componente1 - componente2],...
FontSize,12,FontWeight,Bold)
line(x1(:,1),Tc(:,1),Color,r,LineStyle,--);
line(xM1(:,1),Tc(:,1),Color,r);
line(y1(:,1),Tc(:,1),Color,r,LineStyle,--);
line(yM1(:,1),Tc(:,1),Color,r);
legend(Ideal,Margules,0)
axis([0 1 floor(min([Tc(1,1) Tc(1,end)]))...
ceil(max([Tc(end,1) Tc(end,end)]))]);
ax1 = gca;
set(ax1,XColor,k,YColor,r);
ylabel([Temperatura [^oC] @ num2str(Pt(1)) mmHg])
ax2 = axes(Position,get(ax1,Position),...
XAxisLocation,bottom,...
YAxisLocation,right,...
Color,none,...
XColor,k,YColor,b);
ylabel([Temperatura [^oC] @ num2str(Pt(end)) mmHg])
line(x1(:,end),Tc(:,end),Color,b,Parent,ax2,LineStyle,-.);
line(xM1(:,end),Tc(:,end),Color,b,Parent,ax2);
line(y1(:,end),Tc(:,end),Color,b,Parent,ax2,LineStyle,-.);
F. J. Guerra, C. Malln, A. Struck, T. Varelae
18
Universidad Iberoamericana
Laboratorio de Procesos de Separacin, Verano 2008o
line(yM1(:,end),Tc(:,end),Color,b,Parent,ax2);
for i=1:length(Pt),
conc(i)
= (yM1(pos00(i),i)-yM1(posff(i),i))/2;
legend(Ideal,Margules,0)
end
axis([0 1 floor(min([Tc(1,1) Tc(1,end)]))...
ceil(max([Tc(end,1) Tc(end,end)]))]);
conc=conc
xlabel([fraccion mol componente1])
err=((conc-0.0707)/0.0707)*100
%% Function
grid
fig=fig+1;
function f= margules(x)
%% Calculos
global A B C T Pt AM i j
% integrales
x1=x(1);
x2=x(2);
for i=1:length(Pt),
funxrec = funx(pos0(i):posf(i),i);
int_teo(i)
y1=x(3); = trapz(xM1(pos0(i):posf(i),i),funxrec);
y2=x(4);
figure(fig)
plot(xM1(pos0(i):posf(i),i),funxrec)
Ps1(i,j) = 10^(A(1)-B(1)/(C(1)+T(i,j)));
xlabel(x)
Ps2(i,j)
= 10^(A(2)-B(2)/(C(2)+T(i,j)));
ylabel(1/(y-x))
axis([0 1 0 ceil(funxrec(end))+10-mod(ceil(funxrec(end)),10)])
gamma1(i,j)
= exp(x2^2*(AM(1)+2*(AM(2)-AM(1))*x1));
grid
gamma2(i,j)
fig=fig+1; = exp(x1^2*(AM(2)+2*(AM(1)-AM(2))*x2));
end
KM1(i,j) = gamma1(i,j)*Ps1(i,j)/Pt(j);
KM2(i,j) = gamma2(i,j)*Ps2(i,j)/Pt(j);
int_teo=int_teo % a diferentes presiones
f(1)=(1-KM2(i,j))/(KM1(i,j)-KM2(i,j))-x1;
f(2)=(1-KM1(i,j))/(KM2(i,j)-KM1(i,j))-x2;
der = log(L/L0)
f(3)=KM1(i,j)*(1-KM2(i,j))/(KM1(i,j)-KM2(i,j))-y1;
f(4)=KM2(i,j)*(1-KM1(i,j))/(KM2(i,j)-KM1(i,j))-y2;
funx_exp=1./(xdest-xres);
int_exp = trapz(xres,funx_exp)
% Grafica 1/(y-x) vs. x
figure(fig)
plot(xres,1./(xdest-xres))
xlabel(x)
ylabel(1/(y-x))
axis([0 1 0 ceil(funx_exp(end))+10-mod(ceil(funx_exp(end)),10)])
grid
fig=fig+1;
% concentracion
F. J. Guerra, C. Malln, A. Struck, T. Varelae
19
20
S-ar putea să vă placă și
- 2 DISENO-PUENTES+ (Presentacion)Document59 pagini2 DISENO-PUENTES+ (Presentacion)Victor AndradeÎncă nu există evaluări
- Primer Informe de Puentes PDFDocument28 paginiPrimer Informe de Puentes PDFCristian Ccarhuas PerezÎncă nu există evaluări
- 2 DISENO-PUENTES+ (Presentacion)Document59 pagini2 DISENO-PUENTES+ (Presentacion)Victor AndradeÎncă nu există evaluări
- 2 DISENO-PUENTES+ (Presentacion)Document59 pagini2 DISENO-PUENTES+ (Presentacion)Victor AndradeÎncă nu există evaluări
- Estudios Realizados para Puentebaluarte PDFDocument49 paginiEstudios Realizados para Puentebaluarte PDFDEISY SAMANIEGOÎncă nu există evaluări
- Monografia Del Agua PDFDocument59 paginiMonografia Del Agua PDFKay CM de Armstrong74% (38)
- Desarrollo SostenibleDocument7 paginiDesarrollo SostenibleCristian Ccarhuas PerezÎncă nu există evaluări
- Carga de Servicio Q EfectivoDocument7 paginiCarga de Servicio Q EfectivoCristian Ccarhuas PerezÎncă nu există evaluări
- AuditoriaDocument2 paginiAuditoriaCristian Ccarhuas PerezÎncă nu există evaluări
- ComunicacionDocument3 paginiComunicacionCristian Ccarhuas PerezÎncă nu există evaluări
- Diagnóstico Del Agua en Las Americas 2605014Document33 paginiDiagnóstico Del Agua en Las Americas 2605014Oscar RojasÎncă nu există evaluări
- ProyectoDocument89 paginiProyectoCristian Ccarhuas PerezÎncă nu există evaluări
- Hidroelectrica EIADocument74 paginiHidroelectrica EIAcali1984Încă nu există evaluări
- Hidroelectrica EIADocument74 paginiHidroelectrica EIAcali1984Încă nu există evaluări
- Suelos Remediacion 1Document1 paginăSuelos Remediacion 1Cristian Ccarhuas PerezÎncă nu există evaluări
- Norma A10 ModificacionesDocument42 paginiNorma A10 ModificacionesAlexander De La CruzÎncă nu există evaluări
- Valoracion EconomicaDocument13 paginiValoracion EconomicaCristian Ccarhuas PerezÎncă nu există evaluări
- Convocatoria Bio-Restauracio n2014 PDFDocument1 paginăConvocatoria Bio-Restauracio n2014 PDFJeniffer Rojas O.Încă nu există evaluări
- Valoracion EconomicaDocument13 paginiValoracion EconomicaCristian Ccarhuas PerezÎncă nu există evaluări
- Valoracion EconomicaDocument13 paginiValoracion EconomicaCristian Ccarhuas PerezÎncă nu există evaluări
- Valoracion EconomicaDocument13 paginiValoracion EconomicaCristian Ccarhuas PerezÎncă nu există evaluări
- 1Document14 pagini1chaito0% (1)
- 4 RT 6Document2 pagini4 RT 6Luis C. A. A.Încă nu există evaluări
- Análisis mecanismos planos métodos gráficos analíticosDocument3 paginiAnálisis mecanismos planos métodos gráficos analíticosMarieLa Narváez100% (4)
- Ejercicios RobDocument5 paginiEjercicios RobmaluÎncă nu există evaluări
- Guía Problemas de EntropíaDocument3 paginiGuía Problemas de EntropíaFabián Lezama DezaÎncă nu există evaluări
- PTS-004 Procedimiento SoldadurasDocument8 paginiPTS-004 Procedimiento SoldadurasXenia VelosoÎncă nu există evaluări
- EspectrofotometriaDocument18 paginiEspectrofotometriaMarcela Zamorano RÎncă nu există evaluări
- Informe Ensayo de Tracción Acero 1020Document5 paginiInforme Ensayo de Tracción Acero 1020Edwin R RiveraÎncă nu există evaluări
- Informe de Equilibrio de Un Cuerpo RigidoDocument19 paginiInforme de Equilibrio de Un Cuerpo Rigidopedrito100% (1)
- Transporte de fluidos en tuberíasDocument74 paginiTransporte de fluidos en tuberíasLuis LopezÎncă nu există evaluări
- 396861-Article Text-577296-1-10-20220207Document7 pagini396861-Article Text-577296-1-10-20220207Sergio VasquezÎncă nu există evaluări
- 1.3 Distribucion Electronica Modelo Atã'mico de BohrDocument33 pagini1.3 Distribucion Electronica Modelo Atã'mico de Bohrismael martinezÎncă nu există evaluări
- Quimica Pre Ii (1era Clase)Document7 paginiQuimica Pre Ii (1era Clase)Stuart AlmondÎncă nu există evaluări
- S06.s1. - (ACV-S06) Autoevaluación 6 - FISICOQUIMICA (8837)Document6 paginiS06.s1. - (ACV-S06) Autoevaluación 6 - FISICOQUIMICA (8837)Larry Bill Miguel RodriguezÎncă nu există evaluări
- Informe Inorganica Práctica 2Document14 paginiInforme Inorganica Práctica 2Dessirè Kasandra BerrocalÎncă nu există evaluări
- Arroyo-Vences - Villalaz - Trabajo #3 - ConcretoDocument28 paginiArroyo-Vences - Villalaz - Trabajo #3 - ConcretoENRIQUE ARROYOÎncă nu există evaluări
- Ensayo Normas MaderaDocument5 paginiEnsayo Normas MaderaDÎncă nu există evaluări
- Gases Ideales y RealesDocument87 paginiGases Ideales y RealesAlesi Alvaro Tovar100% (1)
- Resistencia Al Avance (Practica)Document7 paginiResistencia Al Avance (Practica)carlos alberto ortiz martinezÎncă nu există evaluări
- Documentos ETS ORD ENERO16 IQPDocument2 paginiDocumentos ETS ORD ENERO16 IQPZabellzaroch GerdenheimÎncă nu există evaluări
- Tren de RodajeDocument162 paginiTren de RodajeGerardo Balbuena Caro100% (1)
- Mecanica Trabajo 1Document20 paginiMecanica Trabajo 1Daniel CaychoÎncă nu există evaluări
- Propiedades de Los Cuerpos SólidosDocument17 paginiPropiedades de Los Cuerpos SólidosLuna Granados Dania MichelÎncă nu există evaluări
- Captar agua de la nieblaDocument3 paginiCaptar agua de la nieblaEliZabeTh FaUstOrÎncă nu există evaluări
- El Principio de EntropíaDocument3 paginiEl Principio de EntropíaSebasthian ValerÎncă nu există evaluări
- Catálisis Enzimática PDFDocument6 paginiCatálisis Enzimática PDFClaudia RadaÎncă nu există evaluări
- Temperatura de Saturación AdiabáticaDocument9 paginiTemperatura de Saturación AdiabáticaOsvaldoÎncă nu există evaluări
- Clase 1Document19 paginiClase 1Ana Maria ParraÎncă nu există evaluări
- Guía Equilibrio QuímicoDocument2 paginiGuía Equilibrio Químicobenjamin molinaÎncă nu există evaluări
- Practica N°4Document7 paginiPractica N°4mijaheel ferrufinoÎncă nu există evaluări