Documente Academic
Documente Profesional
Documente Cultură
Obtención isobutilo 40
Încărcat de
Sam TorresTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Obtención isobutilo 40
Încărcat de
Sam TorresDrepturi de autor:
Formate disponibile
OBTENCIN DE ACETATO DE ISOBUTILO MEDIANTE LA SNTESIS DE FISCHER
Resumen: La esterificacin de Fischer-Speier o esterificacin de Fischer es un tipo especial de esterificacin que
consiste en la formacin de un ster por reflujo de un cido carboxlico y un alcohol, en presencia de un catalizador
cido. Durante el desarrollo del laboratorio se utilizara este procedimiento para obtener acetato de isobutilo a partir de
alcohol isobutilico y cido actico glacial.
Palabras Clave: IR, alcohol isobutlico, cido actico, SN
Abstract: The Fischer-Speier esterification or Fischer esterification is a special type of esterification, which consist in the
formation of an ester by refluxing a carboxylic acid and an alcohol in the presence of an acid catalyst. During the
development of this laboratory this procedure is used to obtain isobutyl acetate from isobutyl alcohol and glacial acetic
acid.
Key words: IR, isobutyl acetate, acetic acid , isobutyl alcohol, SN
INTRODUCCIN
En qumica orgnica, el termino ster normalmente se
refiere a un ster de un cido carboxlico, a menos que
se especifique algn otro tipo de ster. Al reemplazar el
grupo OH de un cido carboxlico por el grupo OR
de un alcohol, se produce un ster carboxlico.
Imagen 1: Reaccin General Esterificacin de
Fischer.
La reaccin fue descrita por vez primera por Emil
Fischer y Arthur Speier en 1895.
La mayora de cidos carboxlicos son aptos para la
reaccin, pero el alcohol debe ser generalmente un
alcohol primario o secundario. Los alcoholes terciarios
son susceptibles a la eliminacin, y los fenoles suelen
ser muy poco reactivos para dar rendimientos tiles. Los
catalizadores ms comnmente usados para una
esterificacin de Fischer incluyen al cido sulfrico,
cido tsico y un cido de Lewis como el triflato de
escandio (III).Para sustratos ms valiosos o sensibles
(por ejemplo, biomateriales), suele usarse DCC. La
reaccin suele llevarse a cabo sin un solvente,
particularmente cuando hay un gran exceso de
reactante, o en un solvente no polar. Los tiempos de
reaccin comunes varande 1 a 10 horas a temperaturas
de 60-110C. [1]
La esterificacin de Fischer convierte de manera directa
a los cidos carboxlicos y a los alcoholes en steres por
medio de una sustitucin nucleoflica sobre el grupo
acilo catalizada por cido. El grupo carbonilo del cido
carboxlico no es lo suficientemente electroflico para ser
atacado por un alcohol. El catalizador cido protona el
grupo carbonilo y lo activa hacia el ataque nucleoflico.
El ataque por el alcohol, seguido por la prdida de un
protn, produce hidrato de un ster. La prdida del agua
del hidrato del ster ocurre por el mismo mecanismo
que la perdida de agua del hidrato de una cetona. La
protonacin de cualquiera de los dos grupos hidroxilo
permite que salga como agua, formando un catin
estabilizado por resonancia. La prdida del segundo
grupo hidroxilo forma el ster. [2]
La reaccin es de equilibrio por lo que una vez
alcanzado ste, an quedarn cantidades apreciables
de los reactivos de partida junto con los productos de
reaccin. La reaccin no obstante, se puede desplazar
hacia la formacin de productos mediante la adicin de
un exceso de uno de los reactivos, el ms barato y/
ms fcil de eliminar de la mezcla de reaccin
normalmente.[3]
Los pasos para la esterificacin de Fischer son:
Imagen 2: Mecanismo General de esterificacin de
Fischer.
Mecanismo
El mecanismo de reaccin para esta reaccin tiene
varios pasos:
1. Se transfiere un protn del catalizador cido al
oxgeno del grupo carbonilo carboxlico,
2.
3.
4.
5.
incrementando el carcter electrfilo del carbono
carbonlico.
El carbono carbonlico es, a continuacin,
atacado por el tomo de oxgeno nucleoflico del
alcohol.
Se transfiere un protn del catin oxonio a una
segunda molcula de alcohol, dando lugar a un
complejo activado.
La protonacin de uno de los grupos hidroxilo
del complejo activado conduce a un nuevo ion
oxonio.
La prdida de agua del ltimo ion oxonio, y la
posterior desprotonacin da lugar al ster
Las reacciones de esterificacin se efectan bajo
catlisis cida, puesto que en ausencia de cidos
fuertes estas reacciones proceden de forma muy lenta.
Si est presente una cantidad cataltica de cido el
equilibrio se alcanza al cabo de unas horas, calentando
a reflujo una mezcla del cido carboxlico y del alcohol.
Para desplazar el equilibrio hacia la formacin del ster
se aade un exceso del cido carboxlico o del alcohol.
Tambin se puede aumentar la proporcin de ster en el
equilibrio eliminando el agua formada en la reaccin.
METODOLOGA
Se colocan 10 mL de alcohol isobutlico en una probeta
y se registra el peso. El alcohol se adiciona a un baln
que hace parte del montaje para reflujo. En la misma
probeta graduada, sin limpiar o lavar, se pesa o se mide
la cantidad en mililitros calculado de cido actico
glacial a emplear en la sntesis, de acuerdo con la
relacin estequiomtrica 1,0 (alcohol isobutlico): 2,5
(cido actico glacial) y adicionar el contenido de la
probeta al baln. Luego usando una pipeta graduada se
adiciona 1 mL de cido sulfrico concentrado, se mezcla
inmediatamente el contenido del baln con agitacin
manual por varios segundos. Se aade un par de
piedras porosas (preferiblemente de vidrio ya que el
medio cido ataca los carbonatos del mrmol o de la
porcelana) o un agitador magntico y se vuelve a
conectar el baln al sistema. En seguida, se lleva a cabo
el reflujo. El sistema es expuesto al calentamiento
continuo bajo reflujo por 60-75 minutos. Se debe permitir
que la mezcla llegue a temperatura ambiente. Una vez
el sistema se encuentra a temperatura ambiente se
procede a desarmar el aparato de reflujo y empleando
un embudo convencional se transfiere la mezcla de
reaccin, con cuidado de no trasvasar las piedras de
ebullicin, a un embudo de separacin. Asegurese de
que la llave de paso del embudo este cerrada. Se aade
10 mL de agua, se tapa el embudo y se mezclan las
fases mediante agitacin suave y con ventilacin
peridica. Deje que se separen las fases y seguido se
destapa el embudo y se separa la capa acuosa inferior a
travs de la llave de paso en un vaso de precipitados u
otro recipiente adecuado. A continuacin, se extrae la
capa orgnica con 15 mL de una solucin de
bicarbonato de sodio el 5% tal como se hizo
previamente con agua. Se Lava la fase orgnica una vez
ms con 15 mL de una solucin saturada de cloruro de
sodio. La fase orgnica que mayoritariamente es el ster
crudo se transfiere a un erlenmeyer limpio y seco de
100-150 mL, el cual previamente se ha colocado
aproximadamente 1 g de sulfato de sodio anhidro
granular. La mezcla se debe dejar reposar durante 10-15
minutos, mientras se prepara el aparato de destilacin
simple. Si en la mezcla presenta resistencia a fluir,
turbidez o gotas de agua obvias, se debe transferir el
ster a un nuevo Erlenmeyer limpio y seco y aadir de
nuevo 0,5 g de sulfato de sodio anhidro para completar
el secado. Luego de armar el aparato para llevar a cabo
la destilacin, la muestra de ster crudo es transferida al
baln de destilacin. El baln recolector donde se
recoger el producto se debe sumergir en un vaso con
hielo para garantizar la condensacin y para reducir los
olores. El baln debe ser pesado previamente para
poder determinar al final de la destilacin el rendimiento
de la reaccin. Se debe buscar el punto de ebullicin
de su producto esperado. Se contina la destilacin
hasta que slo una o dos gotas de lquido permanecern
en el baln de destilacin. Se calcula el porcentaje del
rendimiento del ster, se toma un espectro infrarrojo
(con el objeto de Interpretarlo y adems compararlo con
el espectro que se reproduce en la literatura o bases de
datos). Finalmente el grupo funcional ms relevante se
debe confirmar con la prueba de hidroxmato, un
ensayo de identificacin positivo para steres. Los
steres reaccionan con hidroxilamina en presencia de
bases fuertes produciendo cidos hidroxmicos, los
cuales forman complejos de color prpura intenso con el
ion frrico constituyendo esto una prueba de
reconocimiento de steres conocida como el ensayo del
hidroxamato
RESULTADOS Y ANLSIS
La sustancia que se trat de sintetizar fue el acetato de
isobutlo.
El punto de ebullicin terico del compuesto es de
118C. No se logr determinar debido a que el reflujo
tom demasiado tiempo, pero sta informacin siempre
es necesaria para identificar la pureza del reactivo.
Imagen 3: Frmula del acetato de Isobutilo.
La prueba con hidroxilamina para producir cidos
hidroxmicos, que dan una coloracin prpura o roja
intensa con FeCl3. (Debe advertirse que los cidos
carboxlicos, haluros de acilo, fenoles y enoles
interfieren en esta reaccin; si tenemos presente un
cido, tambin debera dar positivo el test anterior). [6]
El mecanismo que se propone es el siguiente:
Imagen 5: identificacin de esteres con la formacin
del cido hidroxmico.
La sustancia presenta el siguiente espectro IR:
Imagen 4: Mecanismo para la obtencin de acetato
de isobutilo.
El mecanismo que se plantea para la obtencin de este
compuesto es una esterificacin de Fischer. En ella
ocurre un mecanismo de tipo nucleoflico entre el
oxgeno del alcohol y el carbono perteneciente al grupo
carboxlico. El protn va hacia el grupo hidroxilo que
tiene el cido, el cual luego ser eliminado a modo de
agua. El catalizador en estas reacciones se utiliza para
incrementar la carga parcial positiva existente sobre el
carbono, a travs de protonacin de un oxgeno de la
sustancia cida.[5] La trasferencia de protones entre
tomos de oxgeno es muy rpida. El mecanismo al ser
un equilibrio las contantes que se usan no son muy
grandes. Puede desplazarse a la derecha usando un
exceso de alguno de los dos reactivos o eliminando uno
de los productos. Por ejemplo, en la formacin de
esteres de etilo, con frecuencia se utiliza etanol en
exceso para desplazar el equilibrio lo ms que se pueda
hacia el ster. Alternamente, el agua puede eliminarse
por destilacin o adicionando un agente deshidratante
como sulfato de magnesio. Este mecanismo con
alcoholes es el ms econmico para la sntesis de
esteres, la otra forma de sntesis pero es ms costosa
que la descrita es utilizando cloruros de cido. [2]
Imagen 6: Espectro IR por la SDBS
El espectro IR nos identifica principalmente
la banda ancha de carbonilo (C=O) sobre los
1746 cm-. Para los esteres tambin la banda
que los identifica, es una ancha y otra corta,
que nos describe la tensin C-O entre los
1000 y 1300 cm-. La presencia de grupo
isopropilo se detecta por la aparicin de un
doblete simtrico (1385 y 1368 cm- 1). Los
carbonos Sp3 se encuentran cercanos a los
3000 y 2800 cm-1 respectivamente.
CONCLUSIONES
La sntesis de Fischer es una de las formas
ms sencillas para obtener steres haciendo
reaccionar un cido carboxlico y un alcohol
primario. sta sntesis es un mecanismo de
sustitucin de tipo nucleoflico entre el oxgeno del
alcohol y el carbono perteneciente al grupo carboxlico.
La prueba con la hidroxilamina nos permite identificar
cualitativamente el steres obtenido creando un cido
hidroxmico. En el laboratorio se debe tener en cuenta
las condiciones en que se hace el reflujo, tratando de
que los reactivos tengan la mayor pureza posible, ya
que pueden existir sustancias que intervengan en el
equilibrio que se plantea. El punto de ebullicin y el
espectro IR son de gran importancia para la verificacin
del compuesto que se desea obtener.
BIBLIOGRAFA
[1] Wade L.G. (2011). Qumica Orgnica V I. Mxido
D.F: Pearson.
[2] Wade L.G. (2011). Qumica Orgnica V II. Mxido
D.F: Pearson.
[3] UNIVERSIDAD DE JAN. Departamento de Qumica
Inorgnica
y
Orgnica
(http://www4.ujaen.es/~amarchal/Guion%20de
%20practicas.pdf)
[4] Cruz S; Lpez C; Haro C; Barba C. (2012). Manual
de Prcticas de Laboratorio Qumica Orgnica I. Mxico
D.F: Ed Universidad Autnoma de Metropolitana Unidad
Iztapalapa.
[5] Beyer H; Wolfgang W. (1987). Manual de qumica
orgnica. Barcelona: Editorial Revert [6] Morrison T;
Boyd N. (1987). Qiumica Orgnica. Mxico D.F:
Pearson.
[6]
Universidad
Autnoma
de
Mxico
(http://depa.fquim.unam.mx/~fercor/RESUMENSN.pdf)
[7] Spectral Database for Organic Compounds, SDBS.
National Institute of Advanced Industrial Science and
Technology
(AIST),
Japan
(http://sdbs.db.aist.go.jp/sdbs/cgibin/direct_frame_top.cgi)
S-ar putea să vă placă și
- Practica 2 Cromatografia Por AdsorcionDocument5 paginiPractica 2 Cromatografia Por AdsorcionJordan Josue TorresÎncă nu există evaluări
- Práctica 9 Determinación de La Actividad de La Deshidrogenasa Láctica (LDH)Document6 paginiPráctica 9 Determinación de La Actividad de La Deshidrogenasa Láctica (LDH)Iridian ArÎncă nu există evaluări
- Practica 4Document3 paginiPractica 4CAROLINA HERRERAÎncă nu există evaluări
- Actividad MicrobianaDocument3 paginiActividad MicrobianaDiego De AlvaÎncă nu există evaluări
- Reporte Practica 8 FosfolípidosDocument2 paginiReporte Practica 8 FosfolípidosAlex DVÎncă nu există evaluări
- Práctica 9. Reacciones de Oxido-ReducciónDocument9 paginiPráctica 9. Reacciones de Oxido-ReducciónBrenda HernandezÎncă nu există evaluări
- TRATAMIENTOS PREVIOS AL PROCESAMIENTO DE FRUTAS Y VERDURASDocument7 paginiTRATAMIENTOS PREVIOS AL PROCESAMIENTO DE FRUTAS Y VERDURASAlbafika De PiscisÎncă nu există evaluări
- Reporte de Bomba de CalorDocument10 paginiReporte de Bomba de CalorAxel jair Garcia sanchezÎncă nu există evaluări
- Reporte 5Document4 paginiReporte 5ivanovich hernandezÎncă nu există evaluări
- P8 Mermelada Ok Ok OkDocument45 paginiP8 Mermelada Ok Ok OkOz HdzÎncă nu există evaluări
- Separación e Identificación de Aminoácidos de Jugo de Fruta Por Cromatografía Bidimensional en Capa FinaDocument8 paginiSeparación e Identificación de Aminoácidos de Jugo de Fruta Por Cromatografía Bidimensional en Capa FinaEmanuel100% (1)
- Azul de Metileno y FlouresceinaDocument8 paginiAzul de Metileno y FlouresceinaMoniqa DiiazÎncă nu există evaluări
- Cuestionario de Química Orgánica Practica 7Document2 paginiCuestionario de Química Orgánica Practica 7Evelyn Jim 3295Încă nu există evaluări
- Práctica 9 Adicion Nucleofilica y CondensacionDocument6 paginiPráctica 9 Adicion Nucleofilica y CondensacionGreciaFabiola100% (1)
- Síntesis de polimetacrilato de metilo mediante polimerización por radicales libresDocument22 paginiSíntesis de polimetacrilato de metilo mediante polimerización por radicales libresAlonso JimenezÎncă nu există evaluări
- Curva Tipo de Azúcares ReductoresDocument2 paginiCurva Tipo de Azúcares ReductoresMar Dz HÎncă nu există evaluări
- Bitacora de TrabajoP3Document3 paginiBitacora de TrabajoP3Alexis GudiñoÎncă nu există evaluări
- Carbohidratos y Acidos OrganicosDocument5 paginiCarbohidratos y Acidos OrganicosLalo Tolentino100% (1)
- Cinetica LactasaDocument122 paginiCinetica LactasaalvarezriÎncă nu există evaluări
- Seminario Síntesis A Micro-Escala de Ácido FumárcicoDocument54 paginiSeminario Síntesis A Micro-Escala de Ácido FumárcicojorgeÎncă nu există evaluări
- Sintesis de 2 3 DifenilquinozxalinaDocument3 paginiSintesis de 2 3 DifenilquinozxalinaEndelyon ReiÎncă nu există evaluări
- Separación de Fosfolípidos Por Cromatografía en Capa Fina y Determinación de Colesterol en La Yema de Huevo Colesterol en La Yema de HuevoDocument2 paginiSeparación de Fosfolípidos Por Cromatografía en Capa Fina y Determinación de Colesterol en La Yema de Huevo Colesterol en La Yema de HuevoLuis RojasÎncă nu există evaluări
- 06 Laboratorio N°6 Extracción y Determinación de ColesterolDocument3 pagini06 Laboratorio N°6 Extracción y Determinación de ColesterolMacarena Fernanda LizamaÎncă nu există evaluări
- Aislamiento microorganismos industrialesDocument6 paginiAislamiento microorganismos industrialesFernandoVTÎncă nu există evaluări
- RolandoDocument4 paginiRolandoEfraínÎncă nu există evaluări
- Valoraciones Precipitación ComplejosDocument29 paginiValoraciones Precipitación ComplejosGustavo BarrazaÎncă nu există evaluări
- Diagrama de Purificación Parcial de Lisozima de Clara de HuevoDocument1 paginăDiagrama de Purificación Parcial de Lisozima de Clara de HuevoXimena SánchezÎncă nu există evaluări
- CromatografíaDocument30 paginiCromatografíaBasthean Francisco Pino CabezasÎncă nu există evaluări
- Reporte Practica 3Document9 paginiReporte Practica 3Hernández Caudillo DarianaÎncă nu există evaluări
- Reporte de Práctica 14.Document4 paginiReporte de Práctica 14.Daniela IbarraÎncă nu există evaluări
- Catálisis enzimática: Mecanismo de acción de la quimotripsinaDocument3 paginiCatálisis enzimática: Mecanismo de acción de la quimotripsinaconniewlgÎncă nu există evaluări
- Elaboración de mermelada de fresa: Balance de masa y energíaDocument9 paginiElaboración de mermelada de fresa: Balance de masa y energíaAlbafika De PiscisÎncă nu există evaluări
- Guía primer parcial biotecnología vegetalDocument14 paginiGuía primer parcial biotecnología vegetalALEJANDRO ALVARADOÎncă nu există evaluări
- Introducción a las azlactonasDocument3 paginiIntroducción a las azlactonasJohn Gerardo Razuri100% (1)
- Hidrólisis. A. González, 2009Document3 paginiHidrólisis. A. González, 2009jose andres pino riosÎncă nu există evaluări
- Practica4-Kassandra Balbuena - E9Document2 paginiPractica4-Kassandra Balbuena - E9Kassandra Balbuena MadridÎncă nu există evaluări
- Indicadores Acido Base M NitrofenolDocument3 paginiIndicadores Acido Base M NitrofenolVero Sáenz TÎncă nu există evaluări
- Gaden TraducidoDocument17 paginiGaden TraducidoAdriana RamosÎncă nu există evaluări
- Practica 1 de Inmunologia BasicaDocument3 paginiPractica 1 de Inmunologia BasicaPedro Soto0% (1)
- Reporte Práctica 5. Síntesis de 2,3-Difenilquinoxalina. Equipo 8. 3QM3Document7 paginiReporte Práctica 5. Síntesis de 2,3-Difenilquinoxalina. Equipo 8. 3QM3IvanÎncă nu există evaluări
- Tarea Metabolismo 1Document2 paginiTarea Metabolismo 1Jordan Josue Torres0% (2)
- Pract 5 TermoquimicaDocument10 paginiPract 5 TermoquimicaIsaac VeraÎncă nu există evaluări
- P10 Preparación y Valoración de Disoluciones Ácido-BaseDocument11 paginiP10 Preparación y Valoración de Disoluciones Ácido-BaseAstrid CortesÎncă nu există evaluări
- FQ - 2QV1 - Eq. 1 - P. 9 Adsorción IDocument10 paginiFQ - 2QV1 - Eq. 1 - P. 9 Adsorción IJesus Alberto Martinez GutierrezÎncă nu există evaluări
- Calor Especifico Del Cuerpo HumanoDocument7 paginiCalor Especifico Del Cuerpo HumanoMichelle CorredorÎncă nu există evaluări
- Cap°tulo 9Document28 paginiCap°tulo 9Miguel DiazÎncă nu există evaluări
- Respuesta levadura fríoDocument13 paginiRespuesta levadura fríoKenia VilchisÎncă nu există evaluări
- Propionato !!Document11 paginiPropionato !!Luis PerezÎncă nu există evaluări
- Práctica 2 MezcladoDocument11 paginiPráctica 2 MezcladoIlseÎncă nu există evaluări
- Isotermas de Adorsión.Document8 paginiIsotermas de Adorsión.96884643*50% (2)
- Reacciones AnapleroticasDocument17 paginiReacciones AnapleroticasMaria RivasÎncă nu există evaluări
- Practica 1 Seguridad y Normatividad en El Laboratorio1Document4 paginiPractica 1 Seguridad y Normatividad en El Laboratorio1Gustavo Gama DuarteÎncă nu există evaluări
- Disoluciones RegularesDocument8 paginiDisoluciones RegularesDiego GabrielÎncă nu există evaluări
- Caracterizacion de Glucogeno 2Document3 paginiCaracterizacion de Glucogeno 2Jorge Luis OlivarÎncă nu există evaluări
- Induccion de Mutantes en Escherichia Coli 1Document84 paginiInduccion de Mutantes en Escherichia Coli 1Encb IpnÎncă nu există evaluări
- Determinacion de Proteinas Por El Metodo de Lowry Y BradfordDocument3 paginiDeterminacion de Proteinas Por El Metodo de Lowry Y BradfordMiriam N. Rivera Pinedo0% (3)
- Reporte PolimerizaciónDocument6 paginiReporte PolimerizaciónMaría José Rosales RealÎncă nu există evaluări
- Efecto temperatura incubación crecimiento microbianoDocument11 paginiEfecto temperatura incubación crecimiento microbianoNelly Aidee Avila LagunaÎncă nu există evaluări
- Practica Oxidacion Biologica de Etanol Equipo 5 7IM1Document15 paginiPractica Oxidacion Biologica de Etanol Equipo 5 7IM1Adriana RamosÎncă nu există evaluări
- Cálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaDe la EverandCálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaEvaluare: 5 din 5 stele5/5 (1)
- TECNICASDocument1 paginăTECNICASSam TorresÎncă nu există evaluări
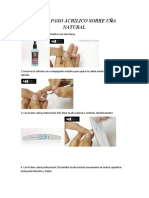
- Paso A Paso Acrilico Sobre Uña Natural EscritoDocument5 paginiPaso A Paso Acrilico Sobre Uña Natural EscritoSam TorresÎncă nu există evaluări
- Manual de BioseguridadDocument3 paginiManual de BioseguridadSam TorresÎncă nu există evaluări
- Estequiometria - Aplicados A La Vida DiariaDocument20 paginiEstequiometria - Aplicados A La Vida DiariaJuan Carlos Ríos Martínez50% (2)
- EnergyDocument3 paginiEnergySam Torres0% (1)
- Metodo CientíficoDocument3 paginiMetodo CientíficoSam TorresÎncă nu există evaluări
- CélulaDocument8 paginiCélulaSam TorresÎncă nu există evaluări
- Gruposfuncionales 2934Document1 paginăGruposfuncionales 2934Katerine GarcíaÎncă nu există evaluări
- Ciencia, Tecnología e Innovación para El Desarrollo y La Cohesión SocialDocument2 paginiCiencia, Tecnología e Innovación para El Desarrollo y La Cohesión SocialSam TorresÎncă nu există evaluări
- CompetenciasDocument8 paginiCompetenciasSam TorresÎncă nu există evaluări
- Preparación de disoluciones y valoración de ácido sulfúricoDocument4 paginiPreparación de disoluciones y valoración de ácido sulfúricoSam TorresÎncă nu există evaluări
- CompetenciasDocument8 paginiCompetenciasSam TorresÎncă nu există evaluări
- Ficha - Consciencia Animal y CognicionDocument2 paginiFicha - Consciencia Animal y CognicionSam TorresÎncă nu există evaluări
- Unidad Quimica OrganicaDocument27 paginiUnidad Quimica OrganicaNicolas Araya100% (1)
- MetacogniciónDocument1 paginăMetacogniciónSam TorresÎncă nu există evaluări
- MetacogniciónDocument1 paginăMetacogniciónSam TorresÎncă nu există evaluări
- Evaluación de Nanopartículas de Óxido de HierroDocument14 paginiEvaluación de Nanopartículas de Óxido de HierroSam TorresÎncă nu există evaluări
- Limites y Ecuación de La RectaDocument5 paginiLimites y Ecuación de La RectaSam TorresÎncă nu există evaluări
- FULLERENOS Y GRAFENOS UltimoDocument15 paginiFULLERENOS Y GRAFENOS UltimoSam TorresÎncă nu există evaluări
- Obtención de La Acetoacetato de BencilaminaDocument6 paginiObtención de La Acetoacetato de BencilaminaSam TorresÎncă nu există evaluări
- Violencia-Intrafamiliar y ResilienciaDocument7 paginiViolencia-Intrafamiliar y ResilienciaSam TorresÎncă nu există evaluări
- Tecnica de Investigacion DocumentalDocument3 paginiTecnica de Investigacion DocumentalSam TorresÎncă nu există evaluări
- AzúcarDocument2 paginiAzúcarSam TorresÎncă nu există evaluări
- Fullerenos y GrafenosDocument15 paginiFullerenos y GrafenosSam TorresÎncă nu există evaluări
- Practica Social Trabajo ViolenciaDocument18 paginiPractica Social Trabajo ViolenciaSam TorresÎncă nu există evaluări
- GLICOSIDOSDocument14 paginiGLICOSIDOSGabixit Perez MaytaÎncă nu există evaluări
- NeurotransmisoresDocument1 paginăNeurotransmisoresSam TorresÎncă nu există evaluări
- Violencia-Intrafamiliar y ResilienciaDocument7 paginiViolencia-Intrafamiliar y ResilienciaSam TorresÎncă nu există evaluări
- Análisis Fitoquíco Preliminar Parte 2 II - 2016Document3 paginiAnálisis Fitoquíco Preliminar Parte 2 II - 2016Sam TorresÎncă nu există evaluări
- Telomeros y TelomerasaDocument5 paginiTelomeros y TelomerasaSam TorresÎncă nu există evaluări
- Problemas Resueltos de La Lección 6Document31 paginiProblemas Resueltos de La Lección 6Ayde Rosario Alconz IngalaÎncă nu există evaluări
- Estadística II: Intervalos de confianza para medias y proporcionesDocument2 paginiEstadística II: Intervalos de confianza para medias y proporcionesFernando Prasca100% (1)
- PorcentajesDocument6 paginiPorcentajesObeth DominguezÎncă nu există evaluări
- PDF Aptitud Numerica Ejercicios Resueltos Enes SnnaDocument15 paginiPDF Aptitud Numerica Ejercicios Resueltos Enes SnnaCarlos SánchezÎncă nu există evaluări
- Tomografías eléctricas resistivas para estudiar el subsuelo de La PazDocument32 paginiTomografías eléctricas resistivas para estudiar el subsuelo de La PazAP JC100% (1)
- Libro Analisis MultivarianteDocument215 paginiLibro Analisis MultivarianteFrutos ConservasÎncă nu există evaluări
- Ferromagnetismo, Ferrimagnetismo y SuperparamagnetismoDocument15 paginiFerromagnetismo, Ferrimagnetismo y SuperparamagnetismoJeysa Paola Colque AtahuichiÎncă nu există evaluări
- Guia 5 Difusion y Transporte 2023Document7 paginiGuia 5 Difusion y Transporte 2023Lu FinochiettoÎncă nu există evaluări
- Leyes Que Rigen El Comportamiento de FluidosDocument4 paginiLeyes Que Rigen El Comportamiento de FluidosCristian Rodrigo Kll GtÎncă nu există evaluări
- Trea Unidad Didáctica 1 (Nelson Vaca)Document30 paginiTrea Unidad Didáctica 1 (Nelson Vaca)Nelson Vaca100% (1)
- Problemas de Bromatologia II KjeldahlDocument2 paginiProblemas de Bromatologia II KjeldahlRichard CTÎncă nu există evaluări
- Jesús Biel - Curso Sobre El Formalismo y Los Métodos de La Termodinámica Vol 2Document568 paginiJesús Biel - Curso Sobre El Formalismo y Los Métodos de La Termodinámica Vol 2Elizabeth Hammon25% (4)
- Método GráficoDocument49 paginiMétodo Gráficoroger gonzalezÎncă nu există evaluări
- LocomotoraDocument29 paginiLocomotoraFabio RomeroÎncă nu există evaluări
- Analitica Nº4 OrginalDocument15 paginiAnalitica Nº4 OrginalMedaly Roos Rojas PaucarÎncă nu există evaluări
- TEXTO. Arranque de Motores y Armado de Tableros.-1Document25 paginiTEXTO. Arranque de Motores y Armado de Tableros.-1Eddy Terceros PanozoÎncă nu există evaluări
- Factor volumétrico de formación de gas (βg): relación entre volúmenes de gas en yacimiento y superficieDocument2 paginiFactor volumétrico de formación de gas (βg): relación entre volúmenes de gas en yacimiento y superficieJulio Mauricio GarciaÎncă nu există evaluări
- Introducción A Interactive PhysicsDocument7 paginiIntroducción A Interactive PhysicsAlexander TubónÎncă nu există evaluări
- Ingenieria UnsaDocument10 paginiIngenieria UnsaIgnacioÎncă nu există evaluări
- Cuestionario TEMA 7Document5 paginiCuestionario TEMA 7paola poma gutierrezÎncă nu există evaluări
- PDF 1 Desigualdades Lineales 1variable m1 l2Document17 paginiPDF 1 Desigualdades Lineales 1variable m1 l2Fabian Gomez AlvarezÎncă nu există evaluări
- Tesis Estimulacion MatricialDocument26 paginiTesis Estimulacion MatricialMaria Valentina Farias Alvarez100% (1)
- MarcoDocument6 paginiMarcoBriiznaa VtÎncă nu există evaluări
- Lab.4 QMC 1206 Mitma Quezada RaysaDocument13 paginiLab.4 QMC 1206 Mitma Quezada RaysaRaysa Mitma QuezadaÎncă nu există evaluări
- DEVASC Module 3Document95 paginiDEVASC Module 3Brian Villota Ceballos100% (1)
- Manuales de Cocinas Enxuta 2016Document32 paginiManuales de Cocinas Enxuta 2016Rony CarroÎncă nu există evaluări
- Instituto Superior Tecnológico Privado CanchisDocument4 paginiInstituto Superior Tecnológico Privado CanchisAnonymous TxthrOvFmAÎncă nu există evaluări
- Contenido - Dino Alexander Amaqui H. Arreglo para Fritz1111111Document42 paginiContenido - Dino Alexander Amaqui H. Arreglo para Fritz1111111jorgeÎncă nu există evaluări
- Anillar PistonesDocument8 paginiAnillar PistonesPedro Luis Mendoza DiazÎncă nu există evaluări
- Raz. Matemático Anual Ade 2015 PDFDocument128 paginiRaz. Matemático Anual Ade 2015 PDFZolo C K Nada C50% (2)