Documente Academic
Documente Profesional
Documente Cultură
Manual de Balance Térmico de Calderos 2
Încărcat de
AbelEnRoTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Manual de Balance Térmico de Calderos 2
Încărcat de
AbelEnRoDrepturi de autor:
Formate disponibile
LABORATORIO DE TERMOHIDRAULICA II
VIII SEMESTRE
MANUAL PARA ENSAYO DE
BALANCE TRMICO DE
GENERADOR DE VAPOR
DR. MARIO MIGUEL HUATUCO GONZALES
DOCENTE Y JEFE DE PRCTICAS
HUANCAYO, 2009-II
I.
RESUMEN
Los generadores de vapor, que aun se conoce como calderas, producen vapor a partir del agua
liquida, existe muchos pasos en el funcionamiento de un generador de vapor, pero, bsicamente,
el agua entra al tambor principal a una temperatura menor que la de saturacin. Luego pasa de
este tambor a un banco de tubos donde es calentada hasta alcanzar su punto de saturacin y se
produce evaporacin. Los gases calientes que son utilizados para calentar y evaporar el agua
pueden provenir de la quema del combustible en el hogar de la caldera, o ser el escape de alta
temperatura proveniente de un motor Diesel o de una turbina de gas. La mezcla de vapor y agua
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
entra al tambor de vapor, donde este ultimo se acumula en su parte superior y el agua recircula
hacia los tubos, el vapor, que ahora ya esta saturado, pasa por los tubos del sobrecalentador,
donde su temperatura se incrementa por la transferencia de calor adicional que proviene de los
gases calientes.
1.
2.
3.
4.
5.
6.
7.
8.
II.
OBJETIVOS
Llevar a cabo el balance trmico del generador de vapor mediante el analizador ORSAT,
teniendo en cuenta que del diagnostico dependen de las medidas que se tomaran para llegar
a una buena eficiencia de funcionamiento.
Determinar experimentalmente el consumo de combustible (flujo de combustible)
Determinar experimentalmente la produccin de vapor.
Calcular la relacin aire combustible aire, terico, igualmente el clculo del exceso de aire.
Estimar el calor til durante el proceso de generacin de vapor.
Determinar el calor perdido por varios procesos de transferencia (radiacin, correccin y
otros)
Clculo de HPc caldera.
Representar grficamente el balance trmico, mediante el diagrama de SANKEY.
Ecuacin de reaccin qumica
Es una expresin cuantitativa de las sustancias y de las proporciones es que esta interviene en el
proceso de combustin que describe un proceso de combustin dando en la medida en que
mantenga las proporciones en que estn presente las sustancias participantes, en conclusin nos
indica la primera como ocurre la combustin.
Ejemplo:
C + O2 CO2
Reactivos Producto
Aire terico o estequiometrico
Es la cantidad mnima de aire capas de proporcionar el oxigeno suficiente para la combustin
completa del carbono, hidrogeno y otros elementos de combustible susceptibles a ser oxidados,
esto implica que no existen oxigeno entre los productos. En la prctica no es posible una
combustin absolutamente completa con aire terico, salvo empleando aire en cantidad mayor de
la tericamente necesaria.
Aire real
Es la cantidad total del aire que se suministra para iniciar la combustin.
Mezcla estequiometrica
Es toda mezcla que contiene exactamente aire y combustible en proporciones mnimas para
producir una combustin completa, es decir una combustin ser completa si sus reactivos son
una mezcla estequiomtrica. Ntese que en toda mezcla estequiomtrica el aire que participa es
el aire terico.
Relacin Aire Combustible
Es de concepto entre la masa de aire y la masa de combustible utilizado en la combustin se
expresa en Kg. De aire por Kg. De combustible.
ra/c=ma/mc
ma: masa de aire, puede estar dada en peso de sus componentes moleculares.
Mc: Masa de combustible, tambin puede darse en funcin de sus pesos moleculares.
Poder Calorfico
El poder calorfico o calor de reaccin expresan el calor transmitido durante el proceso de la
combustin a temperatura constante. Es el calor que genera el combustible.
Poder Calorfico a Presin Constante
En el caso de un proceso de flujo y estado estable o de presin constante segn la primera ley de
la termodinmica, el poder calorfico es igual al calor negativo de la entalpa de la combustin. Por
tal razn, sta transmisin para los procesos de combustin es:
q = Hp Hr
PC = q
mc
mc:
molecular
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 2
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
q: Energa generada por el combustible
Hp:
Entalpa de formacin del producto
Hr:
Entalpa de los reactivos.
REACTIVOS: Es la resistencia que va a participar en la combustin; como el combustible y el
carburante que son los dos tipos.
Carburante, es el medio que permite la reaccin qumica del combustible durante el proceso de la
combustin, ejemplo O2
COMBUSTIN IDEAL O TERICA
Es aquella combustin completa en la cual l oxigeno suministrado es el mnimo indispensable.
Toda combustin completa con aire terico implica que no existir oxigeno entre los productos.
Se supone que la masa total de los reactivos debe ser igual a la masa total del producto. Es decir,
la combustin ideal pueden expresarla por una ecuacin qumica balanceada.
Ejemplo: Combustin del carbono
C
12 kg
6 kg
+
+
+
O2
32 kg
16 kg
CO2
44 kg
22 kg
COMBUSTION COMPLETA
Son aquella en la que todos los elementos oxidantes del combustible se oxidan completamente
esto es el C se oxida hasta CO2 y el H hasta H2O, etc.
COMBUSTIN INCOMPLETA
Es aquella tal que en sus productos hay elementos o sustancias combustibles como CO o
Combustible vivo. La mayora de los procesos reales de combustin tienen un cierto grado de in
completitud
COMBUSTIN DE AIRE
Debido a que el oxigeno puro es poco frecuente encontrar el oxigeno en el aire para llevar acabo
la combustin.
La composicin volumtrica del aire atmosfrico es: 21% de oxigeno, 78% de nitrgeno y 1% den
otros gases (Argn, Nen, Hidrgenos) CO2, Helio vapor de agua.
DETERMINACIN DEL FLUJO DE COMBUSTIBLE (mc)
Teniendo en cuanta el desnivel del tanque de depsito del combustible, por ejemplo:
Figura
Teniendo en cuenta la figura anterior.
Masa de combustible gastado: mc
Pc
=
51.6 lbs/pie3 (densidad del petrleo DIESEL N 2
mc
=
(rea de tanque de combustible) x hc x pc
mc
(Dc)2 * hc * pc
4
hc
=
hi hf: Variacin de altura
mc = (13,875)2 pul2 * 2 pul * 34,6 lbs * pie3
4
pie3
(12 pul)3
mc
=
9,55 lbs
As mismo esta masa de combustible (m c) fue consumida en el tiempo (tc) por tanto el flujo de
combustible (mc) ser:
mc
=
mc
=
9,55 lbs * 69 min
Ic
6,28min
hora
mc
=
91,2 lbs/hora
Donde:
Dc
=
dimetro del cilindro
tc
=
6,28 min
EXCESO DEL AIRE
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 3
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
Se define por la reaccin de masa de aire Combustible real entre la terica.
%exceso de aire
=
(ra/c)real * 100 100
(ra/c)terica
donde: ra/c= ma/ mc = Flujo de masa de aire
Flujo de masa de combustible
CALOR UTIL:
Se define por: Q1=mv/mc*(h)
Donde mv: masa de vapor
Mc: masa de combustible
h: variacin en cantidad
CALOR PERDIDO EN GASES DE ESCAPE (Q2)
Esta perdida de calor asociado principalmente el calor sensible de monxido de carbono por
monxido de azufre. Puede evaluarse por la siguiente expresin Q2=Tg-Ta/F*PCI*100
Donde :
Mg = flujo de gases de chimenea m3/h
Cg = calor especifico medio de los gases de chimenea
Tg = temperatura de gases de chimenea (c.)
Ta = temperatura del aire ambiente(c)
F = Consumo de combustible Kg/h
PCI = poder calorfico inferios del combustible (Kj/Kg.)
EQUIPOS Y/O MATERIALES
Generador de vapor
Mquina que permite la transformacin de la energa qumica del combustible en energa trmica
del agua.
Componentes:
Cmara de Combustin: Lugar para una buen combustin se requiere una adecuada relacin
aire/combustible y de condiciones adecuadas de la cmara para la formacin de torbellinos
(permite mezcla optima de combustible), del tamao de la cmara de acuerdo al tamao de a
flama, etc.
El diseo de la cmara de combustin requiere de conocimiento sobre dinmica de fluidos
transferencia de calor masa, conocimiento de materiales de fabricacin (las temperaturas,
llegan a 1600 C).
Quemador: Son pulverizadores que inyectan el combustible lquido dentro de la cmara de
combustin.
Las calderas de combustible slido adems necesitan de otros elementos que puede ser
pulverizadores, parrillas o dispositivos especial para lecho fluidisante.
Bomba de alimentacin de agua
Elemento de agua del proceso que adems de esta existen otra que ayuda a la circulacin
forzada.
Chimenea
Lugar por donde se descarga los gases a la atmsfera el fenmeno que produce el
movimiento se le denomina tiro la descarga de gases puede ser o no con ayuda de un
ventilador, dependiendo del tiro o desarrollo.
Manmetro bourdon
Es el ms comn de los manmetros de formacin elstica.
Se utilizan para medir presiones de lquidos y gases por encima de tres Kg. Por
centmetro cuadrado.
Su rango de trabajo varia de 0 a 98 megapascal.
Requieren atencin peridica por cuanto llegan a sufrir deformacin permanente.
Son susceptibles a altas temperaturas y al ataque del fluido corrosivo.
Es muy sensible a las vibraciones
Posee una precisin de 0.25 a 2 del fondo de escala
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 4
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
El gasoanalizador Orsat
Es un conjunto de elementos llamado comnmente analizador de gas, se emplea
frecuentemente en los laboratorios para la determinacin cuantitativa de la composicin de los
gases al realizar trabajos de investigacin como al efectuar estudios especiales en mayor ajustes
de distintas instalaciones termotecnias industriales, para el ensayo o generador de vapor, hornos,
etc. El anlisis que se llevar a cabo es de tipo volumtrico en base seca, esto es as porque el
anlisis se realiza a la temperatura ambiente que es considerablemente inferior a la del punto de
roci en los productos de la combustin de la mayora de los hidrocarburos combustibles. Adems
el gas permanece saturado, durante el proceso de anlisis que tienen lugar a temperatura y
presin constante. Los elementos a determinar por medio del analizador ORSAT son CO 2, O2 y
CO de una muestra de productos.
En el analizador consta de los siguientes elementos:
1. Barreta de medicin graduada
2. Pipetas de absorcin A, B, C, conteniendo cada uno un reactivo, apropiado para la absorcin
de CO2, O2 y CO respectivamente
Y conexin pata las muestras o toma de muestras c
3.
Vlvula de tres vas que tienen las siguientes posiciones:
a) Comunicacin de la conexin G con el ambiente.
b) Comunicacin de la conexin G con la varita de medicin
c) Comunicacin de la bureta de medicin con las pipetas de absorcin.
PROCEDIMIENTO PARA EL CLCULO DEL GAS DE COMBUSTIBLE EN ANALIZADOR
ORSAT1. Se conecta con el tubo de gases de escape de donde se recoge la muestra a analizarse
debajo que fluyan al exterior un rato. Oposicin de la vlvula de tres vas.
2. Luego se toma una muestra dejando pasar los gases hacia la tubera medidora (posicin 2
de la vlvula de tras vas). Este proceso se repite dos o tres veces con el afn de purgar
los gases que existen en la bureta medidora.
3. Luego estando llena la bureta medidora con los productos de la convulsin cuyo volumen
debemos medir cuidadosamente y ayudados por la bureta niveladora (que contiene agua
mercurio o salmera) subindola y bajndola.
4. Se deja pasar el gas a la pipeta a la posicin 3 de la vlvula de 3 das que contiene
hidrxido de potasio que absorbe el dixido de carbono, del gas remanente se regresa a la
tubera medidora y se determina su volumen la diferencia de la bureta con volumen,
especial con este ltimo representa el dixido de carbono en la muestra.
5. De forma anloga se va haciendo pasar el resto por las pipetas B y C; la pipeta B contiene
solucin de cido piroglico que absorbe el oxigeno y la pipeta contiene solucin de cloruro
para absorber el CO2
6. El gas que no se absorbe que queda despus de extraer el CO2, CO y O2 se supondr que
es nitrgeno(N2)
TOMA DE DATOS
Temperatura bulbo seco o ambiental (TES):=710F
Temperatura bulbo hmedo ambiental(TEH) =670F
Temperatura agua de alimentacin (Ta) = 200C=680F
Temperatura del combustible (Tc) =240C =75,20F
Temperatura de gases de escape (Tg) = 3650C=6890F
Presin de salida del vapor (Pv) = 90PSI
Desnivel en tanque de combustible = 32.5mm
Desnivel del tanque de agua = a 30mm
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 5
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
Tiempo en que suceden los desniveles del agua ta 6.31min.
Tiempo en que suceden los niveles del combustible tc=5.25min.
Con analizador ORZAT
%co2=10%
%co =3.5%
%o2 = 0.5%
%N2 = 86%
CARACTERSTICAS TCNICAS DEL CALDERO
Especificaciones tcnicas del caldero
Fabricado por:
Marca:
Ao de fabricacin
Tipo:
Fases o pasos:
Potencia :
1985
Piro tubulares
Tres pasos
40HP
Superficie de calentamiento:
200pies
Produccin de vapor :
vapor saturado
Presin de diseo :
Pmax.de trabajo 150PSI
Presin de trabajo:
(90-150)PSI regulable
Combustible que quema:
Diesel 2
Estas son algunas de las caractersticas tcnicas del caldero de la Universidad Nacional de
Ingeniera para realizar el avance trmico
BALANCE TRMICO
1.
2.
Determinacin del flujo de vapor:
Formula :
mv =((D v)2/4)*hv
Donde :
Dv =43m dimetro de tanque de agua
h = 3/2.54m diferencia de altura
t =6.52min tiempo de desnivel
=56.16*10*123 densidad del agua
entonces:
mv =513.2Lb/h
Determinacin del fluyo de combustible
Formula
mc=(Dc2/4)* hcc
Donde:
Dc =13.875mm dimetro del tanque de combustible
h= diferencia de altura de tanque
c= 54.6/123 densidad del combustible
entonces:
mc=67.672Lb/h
3. Anlisis de los gases de escape con los datos obtenidos
CxHy+b(O2+3.76N2) 10CO2+3.6O2+0.5CO+85.9N2+gH2O
x=10.5; b=22.85; g=18; y=36
Determinacin de la relacin aire combustible:
(ra/c)r=b(O2+3.76N2)/CxHy=19.363
C7 H15+B(O2+3.76N2) 7CO2+40.42 N2+7.5H2O
B=10.75
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 6
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
(ra/c)t=B(O2+3.76N2)/C3H15= 14.91
Calculo del exceso de aire
e=(ra/c)r/(ra/c)t-1= 29.87%
Calculo de las perdidas en el proceso de produccin de vapor
1.
Calculo del calor til
Q1=(mv/mc)(h2-h1)
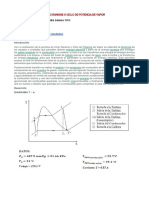
Calculo de h2 con 90 PSI de presin segn tabla
h2=1185.9BTU/Lb.
Tambin segn la tabla con la temperatura del agua que es de 680 F: h1=36.09 BTU/Lb.
Entonces Q1:= 8720 BTU/Lb.
2.
Calor perdido por gases de escape
Q2=mg*Cpg(Tg-Tbs)
Considerando los productos de la combustin
% CO2+%CO+%O2+%H2O+%N2
as mismo tenemos la cantidad de carbono
C=12(%CO2+%CO)Lb. De carbono
Tambin tenemos la composicin del combustible en peso:85% C ; 15% H
Mg=((4(%CO2)+%O+700)/3(%CO2+%CO))*0.85=20.06Lb gas/Lb com.
Q2=2961.65BTU/Lb.
3.
Calor perdido de evaporacin del agua en formacin
Q3=9H(1*(202*Tc)+970.3+0.46(Tg*212))
Donde H=15% ; % del hidrogeno del combustible
1*(202-Tc)= 970.3 BTU/Lb
calor latente de vaporizacin de agua en formacin
0.16(Tg-212)TBU/Lb.= elevacin de temperatura del agua en formacin desde 212 0F hasta la
temperatura de los gases; por lo tanto:
Q3=1790.8BTU/Lb.
4.
Calor perdido por evaporacin de la humedad superficial del combustible
Q4=W(12.-Tc)+970.3+0.46(Tg-202)
W= a cantidad de humedad sobre libras de combustible
Q4= Es solo significativo en combustibles slidos
Entonces Q4=0; por ser un combustible liquido.
5.
Calor perdido por combustin incompleta
Q5=(%CO/(%CO2+%CO))*(CO2-2CO)*C
2CO=3960
CO2=14150
Por lo tanto Q5=(0.5/(10+0.5))*(14150-3960)*0.85
=112.45BTU/Lb. Combustible
9. Calculo del HP de la caldera (HPc)
Hp c
Q1 xme
33500 BTU / Hr .HP
Hp c
8720.001x 67.672
33500
HPc= 17.61
10. Evaporizacin equivalente
Ee= Fc x mv
Clculo del factor de evaporizacin
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 7
UNCP-FIM
Fc=
Fc=
h 2 h1
970.3
LABORATORIO DE TERMOHIDRULICA II
Entalpias
Calorlaten te.del.vapor..de.agua
=
1185.9 36.09
970.3
= 1.19
610.421
lb.devapor.equivalente
Hr
Reemplazando Ee =
11. Produccin del caldero (Pv)
Pv= Ee/mc
Pv=
610.71lb.de.vapor.equivalente
67672.lb.combustible.Hr
lb.de.vapor.equivalente
lb.combustible.Hr
Pv= 9.02
12. RATING(%R)
donde:
Q1
: Calor ganado por el agua o calor til.
Sc
: Superficie del calentamiento del generador de vapor.
8720.001x10
200 x33500
%R=
%R= 1.3
13. Eficiencia ()
Q1
Pc
8720.001
19300
45.18%
CONCLUSIONES
RECOMENDACIONES
BIBLIOGRAFA.
A)
1.
2.
3.
B)
4.
5.
6.
7.
BASICA:
ACEVEDO, Neto. Manual de Hidrulica. Ed. HARLA. Mxico, 1969.
MARXS. Manual del Ingeniero Mecnico. Edit. McGraw Hill. Mxico, 1992.
SEYMOUR- DOOLITTLE, Jesse. El Laboratorio del Ingeniero Mecnico. Ed. HASA.
Buenos Aires
COMPLEMENTARIA
A. MANRIQUE, Jos. S. CARDENAS, Rafael. Termodinmica. Ed. HARLA. Mxico. 1993.
HUATUCO GONZALES, Mario. Manual de Laboratorio de Termohidrulica. UNCP.
Huancayo.1999
HUATUCO GONZALES, Mario. Manual de Laboratorio de Termohidrulica
L. MOTT, Robert. Mecnica de Fluidos Aplicada. Ed. Prentice-Hall Hispanoamericana S.A.
Mxico. 1996.
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 8
UNCP-FIM
LABORATORIO DE TERMOHIDRULICA II
8. MATAIX, Claudio. Mecnica de Fluidos y Mquina Hidrulicas. Ed. HARLA. Mxico. 1993.
9. POTTER C, Merle. WIGGERT C, David. 1998. Mecnica de Fluidos. Editorial Prentice Hall.
Mxico.
10. STREETER-WYLIE. Mecnica de los Fluidos. Ed. McGraw Hill. Mxico 2000.
11. SHAMES, Irvin H. Mecnica de Fluidos. Ed. Mc Graw Hill. Madrid,1996.
12. UGARTE P, F. Mecnica de Fluidos, Teora y Problemas. Ed. San Marcos. Lima, 1990.
13. UNI. Laboratorio de Ingeniera Mecnica II. Lima 1998.
14. VIEJO ZUBICARAY. Manuel. Bombas; Teora, Diseo y Aplicaciones. Ed. Limusa S.A. Mxico,
2002.
15. Prigogine, Y. Introduccin a la Termodinmica de los Procesos Irreversibles. Selecciones
Cientficas, Madrid, 1974.
DR. MARIO HUATUCO GONZALES
2009-II
Pgina 9
S-ar putea să vă placă și
- Mantenimiento de motores térmicos de dos y cuatro tiempos. TMVG0409De la EverandMantenimiento de motores térmicos de dos y cuatro tiempos. TMVG0409Evaluare: 4 din 5 stele4/5 (1)
- MF1165_3 - Instalaciones de ventilación-ExtracciónDe la EverandMF1165_3 - Instalaciones de ventilación-ExtracciónÎncă nu există evaluări
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe la EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSEvaluare: 4.5 din 5 stele4.5/5 (7)
- Exceso de AireDocument11 paginiExceso de AirevCPÎncă nu există evaluări
- El Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaDe la EverandEl Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaÎncă nu există evaluări
- Valores Óptimos CombustiónDocument11 paginiValores Óptimos CombustiónLucasÎncă nu există evaluări
- Balance Termico de Una Caldera 4Document17 paginiBalance Termico de Una Caldera 4paul_tinizarayÎncă nu există evaluări
- Unidad 3: Calderas de vaporDocument20 paginiUnidad 3: Calderas de vaporGuillermo SosaÎncă nu există evaluări
- Ingeniería química. Soluciones a los problemas del tomo IDe la EverandIngeniería química. Soluciones a los problemas del tomo IÎncă nu există evaluări
- Eficiencia Térmica de CalderaDocument16 paginiEficiencia Térmica de CalderaPavel Lorenzo LimiaÎncă nu există evaluări
- Maquinas y Equipos Termicos IDocument8 paginiMaquinas y Equipos Termicos Icarlos978Încă nu există evaluări
- Laboratorio CalderaDocument17 paginiLaboratorio CalderaNelson Valentin Castillo AranaÎncă nu există evaluări
- Contrato de Venta de Gas Natural Al BrasilDocument38 paginiContrato de Venta de Gas Natural Al BrasilMotor Gonzales100% (2)
- Combustión balance materiaDocument6 paginiCombustión balance materiaMARIEL XIOMARA COLONIO CAMARGO100% (1)
- Calibración y Puesta A Punto Del Sistema GLPDocument12 paginiCalibración y Puesta A Punto Del Sistema GLPDavid Jimenez100% (2)
- Eficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108De la EverandEficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108Încă nu există evaluări
- 8 Ciclos Termodinamicos Parte IIIDocument18 pagini8 Ciclos Termodinamicos Parte IIIANTHONY FRANCESCO SAAVEDRA AGURTOÎncă nu există evaluări
- Determinacion de La Eficiencia Termica en Calderos Pirotubulares FinalDocument13 paginiDeterminacion de La Eficiencia Termica en Calderos Pirotubulares FinalKris Andreé Pérez0% (1)
- COMPORTAMIENTO DEL FUEGO: Cómo se inicia y propaga el fuegoDocument80 paginiCOMPORTAMIENTO DEL FUEGO: Cómo se inicia y propaga el fuegoARKAniandoÎncă nu există evaluări
- Termotecnia: Combustión y caloresDocument49 paginiTermotecnia: Combustión y caloresDario Riveros RomeroÎncă nu există evaluări
- Poder Calorifico de Fluidos de HidrocarburosDocument11 paginiPoder Calorifico de Fluidos de HidrocarburosFredy NavasÎncă nu există evaluări
- Camara Hilton FinalDocument20 paginiCamara Hilton FinalJulio César Canahuire VilcaÎncă nu există evaluări
- Maquinas Termicas Combustion 1Document11 paginiMaquinas Termicas Combustion 1armandoclaÎncă nu există evaluări
- Mezclas Reactivas de Gases, Ciclos Binarios, Plantas Nucleares y Ciclos Combinados Termodinamica IIDocument20 paginiMezclas Reactivas de Gases, Ciclos Binarios, Plantas Nucleares y Ciclos Combinados Termodinamica IIMilton MurilloÎncă nu există evaluări
- N 6 Laboratorio Camara HiltonDocument35 paginiN 6 Laboratorio Camara HiltonVictor AlejandroÎncă nu există evaluări
- Eficiencia térmica calderaDocument15 paginiEficiencia térmica calderaLuis SalinasÎncă nu există evaluări
- Sistema alimentación y combustión calderoDocument42 paginiSistema alimentación y combustión calderoLucila Daisyde Iparraguirre ToledoÎncă nu există evaluări
- Determinacion de La Eficiencia Termica en Calderos PirotubularesDocument17 paginiDeterminacion de La Eficiencia Termica en Calderos PirotubularesDeyner Ayala RamosÎncă nu există evaluări
- Camara de Combustion HiltonDocument20 paginiCamara de Combustion HiltonJavier Macedo RamosÎncă nu există evaluări
- COMB Publicar PDFDocument32 paginiCOMB Publicar PDFOttofrech86Încă nu există evaluări
- Balance energía sistema caldera economizadorDocument20 paginiBalance energía sistema caldera economizadorEvita Eva Aricochea Vasquez100% (2)
- Analisis Teórico de La Combustión en Quemadores de Gas NaturalDocument9 paginiAnalisis Teórico de La Combustión en Quemadores de Gas NaturalKarinaChavezÎncă nu există evaluări
- Ciclo Rankine o Ciclo de Potencia de VaporDocument13 paginiCiclo Rankine o Ciclo de Potencia de VaporAndres Sanga TitoÎncă nu există evaluări
- Informe Labo 6Document17 paginiInforme Labo 6Fernando CortezÎncă nu există evaluări
- Análisis teórico combustión gas naturalDocument6 paginiAnálisis teórico combustión gas naturalcajaca0% (1)
- Informe Camara HiltonDocument23 paginiInforme Camara HiltonJesus UgarteÎncă nu există evaluări
- CCE - APUNTES 2B Lectura - 1S 2022Document36 paginiCCE - APUNTES 2B Lectura - 1S 2022CristoferÎncă nu există evaluări
- Maquinas y Equipos Térmicos IDocument18 paginiMaquinas y Equipos Térmicos INestor CoronaÎncă nu există evaluări
- Caldera vapor UNC Bogotá informe 11 eficienciaDocument18 paginiCaldera vapor UNC Bogotá informe 11 eficienciaAndrés Esteban Granada ZapataÎncă nu există evaluări
- CombustiónDocument37 paginiCombustiónJonathan VeraÎncă nu există evaluări
- Ahorro de Energía en Los Generadores de VaporDocument10 paginiAhorro de Energía en Los Generadores de VaporWilder Clemente Faria MutundaÎncă nu există evaluări
- Ciclo Rankine o Ciclo Potencia VaporDocument15 paginiCiclo Rankine o Ciclo Potencia VaporEric CesiasÎncă nu există evaluări
- Balances CalderaDocument12 paginiBalances CalderaCristian JaraÎncă nu există evaluări
- Camara de Combustion HiltonDocument22 paginiCamara de Combustion Hiltonpeskador28Încă nu există evaluări
- Informe Cámara HiltonDocument20 paginiInforme Cámara HiltonAbelardo Jozhitoh LokitohÎncă nu există evaluări
- Combustibles y CombustionDocument15 paginiCombustibles y CombustionMilton Juan Fernando VilcaÎncă nu există evaluări
- Proceso de Obtencion de AmoniacoDocument11 paginiProceso de Obtencion de AmoniacoJose Luis Caity chivacoÎncă nu există evaluări
- 1-Principios de CombustiónDocument15 pagini1-Principios de CombustiónkokeinÎncă nu există evaluări
- Ac.5.Inv-doc-gonzalez Melo Jose DavidDocument15 paginiAc.5.Inv-doc-gonzalez Melo Jose DavidJosé GonzálezÎncă nu există evaluări
- Producción de Gas de SíntesisDocument11 paginiProducción de Gas de SíntesisJosmary Romero100% (1)
- Cálculos rendimiento energético caldera método indirectoDocument7 paginiCálculos rendimiento energético caldera método indirectoBrayan VFÎncă nu există evaluări
- Estequiometria de La Combustion LJGG 19011135Document8 paginiEstequiometria de La Combustion LJGG 19011135Luis Jaime GonzalezÎncă nu există evaluări
- Combustion y CombustiblesDocument23 paginiCombustion y CombustiblesOrlando Marvin Salguero PardoÎncă nu există evaluări
- Poder Calorífico de Los CombustiblesDocument11 paginiPoder Calorífico de Los CombustiblesRoberth Sallago EspinozaÎncă nu există evaluări
- Análisis de la combustión en quemadores de gas naturalDocument5 paginiAnálisis de la combustión en quemadores de gas naturaljohnneracalÎncă nu există evaluări
- Motores Diesel GLPDocument36 paginiMotores Diesel GLPsami240sx100% (3)
- Bomba de JunkerDocument7 paginiBomba de JunkerDamian SolorzanoÎncă nu există evaluări
- Combustion y CombustiblesDocument21 paginiCombustion y CombustiblesLuis Fortunato Caso PalpaÎncă nu există evaluări
- CombustiónDocument70 paginiCombustiónOrlando Manriquez LÎncă nu există evaluări
- Incinerador Termal TerminadoDocument23 paginiIncinerador Termal TerminadoAlex Alejandro Huamani0% (1)
- 9 - INTERCAMBIADORES EN CALDERAS Parte 2Document31 pagini9 - INTERCAMBIADORES EN CALDERAS Parte 2Ducardo Leon Molina LopezÎncă nu există evaluări
- Generación energía pajaDocument26 paginiGeneración energía pajaralozano33Încă nu există evaluări
- Examen Final Mec 2431Document2 paginiExamen Final Mec 2431Luis M. ChamosoÎncă nu există evaluări
- RESUMEN DEL LIBRO MCI PAYRI 1ra FaseDocument41 paginiRESUMEN DEL LIBRO MCI PAYRI 1ra Fasecarlos enriqueÎncă nu există evaluări
- Taller # 5 FisicoquimicaDocument6 paginiTaller # 5 FisicoquimicaMary Yorgelis LeguízamonÎncă nu există evaluări
- Olefinas en El GLPDocument5 paginiOlefinas en El GLPyauliyacuÎncă nu există evaluări
- Termodinámica - Taller Segunda Ley de CarnotDocument1 paginăTermodinámica - Taller Segunda Ley de CarnotDaniela LaraÎncă nu există evaluări
- Termo CocinaDocument21 paginiTermo CocinaIsaias Garcia SanchezÎncă nu există evaluări
- Blanco Clavijo, Jorge Eleazar - 2017 PDFDocument150 paginiBlanco Clavijo, Jorge Eleazar - 2017 PDFWilliam MontesdeOcaÎncă nu există evaluări
- Labo 2. Bomba Calorimetrica de Junker - FIME UNACDocument10 paginiLabo 2. Bomba Calorimetrica de Junker - FIME UNACLucas Andres Yanac Durand100% (2)
- Combustibles SolidosDocument5 paginiCombustibles SolidosJorge Rosado Huerta100% (1)
- Proceso Baterias de CokDocument49 paginiProceso Baterias de CokMartha Liliana Rincon CabreraÎncă nu există evaluări
- Informe EPEyR CT ParamongaDocument21 paginiInforme EPEyR CT ParamongaJason ContrerasÎncă nu există evaluări
- 1Document27 pagini1Cesar Rojas MendozaÎncă nu există evaluări
- TransDocument2 paginiTransMario RiveraÎncă nu există evaluări
- Caldera vapor UNC Bogotá informe 11 eficienciaDocument18 paginiCaldera vapor UNC Bogotá informe 11 eficienciaAndrés Esteban Granada ZapataÎncă nu există evaluări
- Informe de Propiedades Físicas y QuímicasDocument20 paginiInforme de Propiedades Físicas y QuímicasJosè MirandaÎncă nu există evaluări
- Practica 9 Calor de CombustionDocument12 paginiPractica 9 Calor de CombustionJuan Fermin PachecoÎncă nu există evaluări
- Unidades Tematicas Que Se Consideran en El Examen para Optar A Operador Segun Articulo #80 PDFDocument3 paginiUnidades Tematicas Que Se Consideran en El Examen para Optar A Operador Segun Articulo #80 PDFespartako2008Încă nu există evaluări
- 1.metalurgia GeneralDocument20 pagini1.metalurgia GeneralAlegil90Încă nu există evaluări
- Poder calorífico Diésel-2Document13 paginiPoder calorífico Diésel-2Carlos Mujica SaucedoÎncă nu există evaluări
- Práctica 1 - Determinación Poder CaloríficoDocument5 paginiPráctica 1 - Determinación Poder CaloríficoMeli GaviganÎncă nu există evaluări
- Trabajo Práctico #2 - 2020 CombustiblesDocument2 paginiTrabajo Práctico #2 - 2020 CombustiblesJose BenitezÎncă nu există evaluări
- Manual de Calculo y Diseño Conceptos Generales Gas Natural y Placas SolaresDocument120 paginiManual de Calculo y Diseño Conceptos Generales Gas Natural y Placas Solaresventas.juguetes9Încă nu există evaluări
- Agentes MetalurgicosDocument31 paginiAgentes MetalurgicosGiseeTaricoÎncă nu există evaluări