Documente Academic
Documente Profesional
Documente Cultură
Cours
Încărcat de
Mocanu BiancaDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Cours
Încărcat de
Mocanu BiancaDrepturi de autor:
Formate disponibile
- Support de Cours (Version PDF) -
Mtabolisme protique
Collge des Enseignants de Nutrition
Date de cration du document
2010-2011
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Table
des
matires
I Gnralits ....................................................................................................................................... 3
II La synthse protique ....................................................................................................................7
III La dgradation irrversible des acides amins (ou catabolisme oxydatif des acides amins,
ne pas confondre avec la protolyse) ...............................................................................................9
IV La protolyse (ou catabolisme protique) ................................................................................ 11
V Les apports en acides amins exognes ...................................................................................... 13
VI Synthse des acides amins non essentiels ................................................................................14
VII Les moyens dexploration du mtabolisme protique in vivo ...............................................16
VIII Rgulation du mtabolisme des protines ............................................................................. 20
IX Besoins en azote et en acides amins et sources protiques alimentaires ..............................25
NOTE(S) DU CHAPITRE ................................................................................................................ 30
X Annexes.......................................................................................................................................... 30
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Points comprendre
Les protines sont renouvelles en permanence par des processus biochimiques
consommant de lnergie et associant synthse et catabolisme protique. Le
renouvellement protique est modul par de multiples facteurs nutritionnels et
hormonaux et au cours de diverses situations pathologiques.
Le maintien de la masse des protines corporelles rsulte de lquilibre entre
synthse et catabolisme protique selon un rythme dpendant des apports
alimentaires. La rgulation du mtabolisme protique par les hormones et les
substrats nergtiques sexerce soit sur la synthse, soit sur le catabolisme, soit sur
les deux pour promouvoir lanabolisme ou un catabolisme protique net.
Les mthodes dexploration du mtabolisme protique ont des limites qui doivent
tre considres lors de leur application pour lvaluation clinique ou la recherche
fondamentale.
Les besoins en protines doivent tre assurs par un apport suffisant la fois en
azote et en acides amins essentiels, par lingestion de protines dorigine animale
et/ou vgtale.
GNRALITS
Une protine est une molcule comportant de lazote et compose dune squence
dacides amins (au nombre de 20) relis par des liaisons peptidiques. La squence
dtermine la structure primaire de la protine, la configuration de la chaine peptidique dans
lespace dtermine les structures secondaires et tertiaires, lassociation de plusieurs
chanes peptidiques dtermine la structure quaternaire. Par convention, une protine
comportant moins de 50 acides amins est appele peptide. La taille dune protine est
extrmement variable de quelques centaines plusieurs millions de kilo-daltons. De mme,
les protines ont de trs nombreuses fonctions : protines de structure (collagne...),
protines contractiles (myosine...), protines de transport (albumine...), protines
immunitaires (immunoglobulines), protines enzymatiques, hormones, rcepteurs, etc.
Malgr ces structures et fonctions trs variables, toutes les protines ont en commun une
proprit, leur renouvellement permanent schmatis sur la figure 1.
- Universit Mdicale Virtuelle Francophone -
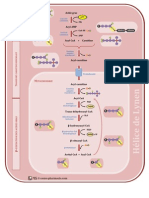
- Support de Cours (Version PDF) 1. Schma gnral du mtabolisme protique chez lhomme
Paramtres cintiques du mtabolisme protique
Les principales voies de production et dutilisation des acides amins et des protines sont
indiques sur le schma et les chiffres indiqus titre indicatif correspondent
approximativement aux valeurs observes chez ladulte en bonne sant :
la synthse protique : elle se fait partir dun pool (compartiment) dacides
amins libres de trs petite taille, environ 70 g (soit moins de 1 % des acides amins
de lorganisme) lui-mme compartiment en 2 pools extra-cellulaire et
intracellulaire, ce dernier reprsentant environ 95 % des acides amins libres et tant
le vritable prcurseur de la synthse,
la protolyse (ou dgradation protique) librant des acides amins dans le pool,
ces deux phnomnes de synthse protique et de protolyse sont simultans et
constituent le renouvellement protique. Lquilibre entre synthse et protolyse
est responsable de la conservation de la masse protique. Une synthse suprieure
la protolyse rsulte en un gain protique net (ou accrtion protique)
improprement appel anabolisme protique. A contrario, une protolyse suprieure
la synthse rsultera en une diminution de la masse protique,
la dgradation irrversible des acides amins correspond loxydation de ces
derniers et rsulte en une production dazote et de CO2
les apports protiques compensent les pertes dacides amins, la diffrence entre
apports et pertes constituant le bilan protique (ou bilan azot) et correspondant
galement la diffrence entre synthse et protolyse protique condition que la
taille du pool dacides amins libres ne varie pas, ce qui est le cas la plupart du
temps.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Renouvellement des protines
Il existe plusieurs dizaines de milliers de protines, diffrentes dans leurs structures et leurs
fonctions chez les mammifres.
Ces protines participent de faon trs variable au renouvellement protique global en
fonction de :
limportance quantitative de la protine considre et ce titre les organes les plus
importants sont le muscle, lintestin, le foie et la peau,
la rapidit du renouvellement de chaque protine considre individuellement.
Cette rapidit est trs variable
Ainsi, le renouvellement des protines musculaires reprsente environ 20 % du
renouvellement protique total, celui du foie environ 10 % (la masse hpatique est trs
infrieure la masse musculaire mais ses protines sont renouveles beaucoup plus
rapidement), les protines de la peau et du tube digestif constituant les deux autres
participants importants (environ 15 % chacun). Ces pourcentages indicatifs varient en
fonction de lge, et probablement de lespce. Dun point de vue nutritionnel, il est habituel
de considrer lensemble du mtabolisme protique selon ce schma gnral dont le
caractre trs (trop) global doit cependant tre gard en mmoire.
Les valeurs de renouvellement indiques sur le schma correspondent celles observes
chez un adulte de 70 kg en bon tat nutritionnel. Il est habituel dexprimer la synthse
protique et la protolyse par kg de poids corporel, ce qui correspond environ 4 g de
protine synthtise et dgrade par kg de poids et par jour. En labsence de croissance, la
masse protique reste stable et la synthse est donc gale la protolyse sur une priode de
24 h.
Les variations du renouvellement protique
Elles sont importantes en fonction de ltat physiologique et de diffrents tats
pathologiques :
selon lge : le renouvellement protique est beaucoup plus rapide chez le nouveaun (10 15 g/kg/jour), la synthse tant suprieure la protolyse, ce qui rsulte en
un gain protique 1 1,5 g de protine/kg/jour (correspondant un gain pondral
de 20 30 g/jour compos de 12 % de protines). Chez le sujet g, le
renouvellement protique semble ralenti mais est habituellement normal si la
rduction de masse maigre est considre.
selon ltat nutritionnel : le renouvellement protique diminue au cours du jene,
la protolyse restant suprieure la synthse protique, ce qui induit un bilan
protique ngatif
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF)
selon ltat pathologique : en rgle gnrale les situations dites cataboliques,
comme un syndrome inflammatoire, un traumatisme ou un sepsis, entranent une
augmentation importante du renouvellement protique qui peut tre multipli par 3
4, la protolyse tant cependant suprieure la synthse protique et rsultant en
des pertes protiques massives avec rduction de la masse protique musculaire.
Au total, ces trois situations soulignent la possible dissociation entre un gain protique
dune part (rsultat entre synthse et catabolisme) et une synthse protique dautre part :
une synthse protique leve (comme chez le patient brl ou traumatis) nest pas
forcment associe un gain protique (en raison dune protolyse accrue). Enfin, les
diffrentes variations constates au niveau du mtabolisme protique du corps entier ne
portent pas de faon similaire sur le mtabolisme des diffrents compartiments protiques :
ainsi au cours des situations cataboliques, lacclration du renouvellement protique
hpatique participe de faon majoritaire lacclration du renouvellement protique global
(synthse de protines inflammatoires), le muscle devenant un organe majoritairement
producteur dacides amins (stimulation de la protolyse musculaire).
Quelle est la finalit du renouvellement protique ?
Lexistence dun renouvellement protique relativement rapide permet une meilleure
adaptation aux diffrentes circonstances nutritionnelles et physiopathologiques. Il permet
galement llimination de protines vieillies ne pouvant plus remplir leurs fonctions
physiologiques de faon satisfaisante. Enfin, son rle dans la reconnaissance immunitaire
par la gnration de peptides est important. Par rapport la figure du schma gnral, nous
considrerons le pool dacides amins libres comme lment central du mtabolisme
protique et envisagerons successivement les voies dutilisation des acides amins et les
voies de production de ces acides amins. Le mtabolisme de chaque acide amin ne sera
pas considr individuellement (bien que quelques exemples soient donns) mais en
relation avec le mtabolisme protique vu sous un angle nutritionnel.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
II LA SYNTHSE PROTIQUE
Pntration intracellulaire des acides amins
Les acides amins libres circulant pntrent dabord lintrieur des cellules laide de
transporteurs dont il existe au moins quatre types, chacun tant commun plusieurs acides
amins. On distingue :
un transporteur pour les acides amins neutres dont il existe plusieurs formes. La
plupart de ces transporteurs sont sodium-dpendants et consomment de lnergie,
un transporteur pour les acides amins basiques : lysine (et cystine),
un transporteur pour les acides amins dicarboxyliques (aspartate, glutamate),
un transporteur pour les imino acides (proline).
Compte-tenu de la non spcificit de la plupart de ces transporteurs, il peut exister des
phnomnes de comptition entre les diffrents acides amins en cas de dsquilibre
majeur entre les concentrations des acides amins dpendant dun mme transporteur.
Les aminoacyl-ARNt
Ce compartiment est en fait le vritable prcurseur de la synthse protique et de taille
extrmement rduite. Avant dtre utilis pour la synthse protique, un acide amin doit
tre activ ou charg par un ARNt sous linfluence dune aminoacyl-ARNt synthtase. Il
existe vingt aminoacyl-ARNt synthtases, chacune tant spcifique dun acide amin. La
controverse persiste pour savoir si lactivation par lARNt se fait exclusivement partir du
pool dacide amin intracellulaire libre ou galement et au moins partiellement partir du
pool dacide amin extra-cellulaire.
La synthse protique proprement dite
Seules les grandes tapes en seront rappeles ici :
transcription de lADN en ARNm : initiation puis longation, catalyse par lARN
polymrase. LARNm contient des parties qui sexpriment (exons) ou non (introns)
puis les introns sont limins.
traduction de lARNm en un peptide : cette traduction se fait sur les ribosomes (qui
sont les tablis de la synthse protique). En gnral, il existe plusieurs
ribosomes sur un mme brin dARNm qui est donc traduit simultanment. Cette
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
agrgation de ribosomes en polysomes peut tre visualise en microscopie
lectronique et constitue un tmoin morphologique de lactivit de synthse
protique intracellulaire. Linteraction entre les groupes de trois bases de lARNm
(codons) et les anti-codons de lARNt correspond la lecture du code gntique. Les
trois tapes successives de la synthse dun peptide sont linitiation, llongation et
la terminaison qui ncessitent ces diffrents niveaux des facteurs spcifiques (IF,
EF, RF), des enzymes (peptides transfrases) et surtout de lnergie sous forme de
GTP et dATP. On distingue classiquement la capacit de traduction et son
efficacit : la capacit ribosomale correspond aux possibilits de synthse maximum
dune protine par une cellule et sexprime en quantit dARN disponible par
rapport la quantit de protine tissulaire. Lefficacit ribosomale correspond
lactivit de la synthse protique rapporte la quantit dARN prsent.
la maturation : elle correspond aux multiples phnomnes post-traductionnels qui
vont permettre dobtenir une protine fonctionnelle partir du peptide dtach de
lARNm et qui pour linstant na quune structure primaire. Cette protine peut
rester intracellulaire mais peut galement tre exporte vers dautres tissus suivant
alors la voie scrtoire du rticulum endoplasmique puis de lappareil de Golgi. Au
cours de ces diffrentes tapes lintrieur de la cellule, les protines subissent donc
diffrentes modifications :
acquisition des structures secondaires, tertiaires et quaternaires (par exemple,
acquisition de ponts disulfures),
glycosylation,
coupures de pr-protines pour arriver la forme fonctionnelle (par exemple,
coupure de la pro-insuline en insuline),
modifications de certains acides amins (par exemple, mthylation de lhistidine
conduisant la 3 mthyl-histidine, hydroxylation de la proline en
hydroxyproline...). Globalement deux points essentiels sont souligner concernant
la synthse protique :
labsence ou la faible disponibilit dun seul acide amin suffit ralentir, voire
bloquer lensemble des synthses protiques (concept dacide amin limitant la
synthse),
la synthse protique consomme une quantit importante dnergie Daprs la
stoechiomtrie des diffrentes ractions le cot nergtique de la synthse protique
est de lordre de 0,85 kcal/g de protine synthtise. Ceci reprsente un cot
minimum, les estimations obtenues in vivo chez lhomme tant de 1 kcal/g de
protine synthtise.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
III LA DGRADATION IRRVERSIBLE DES ACIDES AMINS (OU
CATABOLISME OXYDATIF DES ACIDES AMINS, NE PAS
CONFONDRE AVEC LA PROTOLYSE)
Dsamination
Ltape initiale de loxydation de la plupart des acides amins est le transfert rversible du
groupement alpha-amin sur lalpha-ctoglutarate, produisant lacide alpha-ctonique
(ctoacide) correspondant selon la raction indique ci-dessous.
AA - NH2 + alpha-ctoglutarate ctoacide + glutamate Le groupe amin maintenant
port par le glutamate sera ultrieurement redistribu vers dautres acides amins.
limination de lazote
Le glutamate form est converti en glutamine (glutamine synthtase) qui permet le transfert
de lammoniac (toxique sous sa forme libre) sous une forme neutre entre les diffrents
organes et en particulier vers le foie. Dautres acides amins, telle que lalanine participent
galement ce transfert.
Dans le foie, la glutamine redonne du glutamate et de lammoniac et cest le cycle de lure
qui permet llimination de lexcs dammoniac sous une forme neutre, hydrosoluble et
concentre (lure comprenant 2 atomes dazote par molcule). Les deux atomes dazote qui
seront limins viennent pour lun de lammoniac driv du glutamate, activ sous forme
de carbamoyl phosphate et pour lautre de laspartate, lui-mme issu de la transamination
de loxaloactate par le glutamate.
Lure, produit terminal du mtabolisme protique, peut diffuser en partie dans lintestin
o elle est dgrade par des urases bactriennes produisant de lammoniac qui peut tre
rabsorb et revenir au foie. Ce mcanisme de sauvetage de lazote pourrait jouer un
rle non ngligeable dans lpargne protique relative au cours du jene prolong. La
rgulation du cycle se fait au niveau de la synthse du carbamoyl phosphate et des
concentrations des diffrents intermdiaires du site de lure. Ce cycle est consommateur
dnergie.
La voie prfrentielle dlimination de lazote en excs est le cycle de lure, mais lazote
peut galement tre limin par le rein sous forme dammoniac, qui reprsente environ 20
% de lazote urinaire total. Cette proportion augmente dans les circonstances cataboliques,
le jene, lacidose et les insuffisances hpatiques.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Destine des radicaux carbons des acides amins
Cette destine varie selon lacide amin et galement selon les organes, la plupart des acides
amins lexception des acides amins branchs ayant une dgradation oxydative
essentiellement hpatique. Schmatiquement, le radical carbon (ctoacide) peut avoir deux
destines :
il peut tre ramin soit en un acide amin identique, soit en un autre acide amin
aprs modification conduisant alors la synthse dacides amins non essentiels,
il peut tre irrversiblement dtruit et fournir de lnergie directement ou
indirectement, ses carbones tant incorpors dans dautres substrats nergtiques,
glucose ou corps ctoniques. Tous les acides amins sont noglucogniques
Acides amins prcurseurs de composs actifs
Les acides amins ou leurs radicaux carbons peuvent tre les prcurseurs de composs
biologiquement actifs. Ainsi phnylalanine et tyrosine sont les prcurseurs des hormones
thyrodiennes et des catcholamines, lhistidine est un prcurseur de lhistamine, larginine
est un prcurseur du NO, le glutamate un prcurseur du GABA (neurotransmetteur),
aspartate, glycine et glutamate sont des prcurseurs des bases purique et pyrimidique... Ces
voies de transformation sont quantitativement minimes en terme de nutrition protique
stricto sensu, ce qui nenlve rien leurs rles physiologiques essentiels.
Du point de vue du mtabolisme protique, la notion essentielle considrer est celle de
pertes irrversibles dun acide amin pour la synthse protique. En rgle gnrale,
jusquaux cto acides, il est possible de remonter un acide amin par ramination,
lacide amin pouvant tre rincorpor dans une protine. Par contre, une fois les tapes
doxydation irrversibles franchies (ces tapes tant plus ou moins proches de la
dsamination selon lacide amin considr), lacide amin estdfinitivement perdu
pour le mtabolisme protique. titre dexemple, les deux premires ractions de
dgradation des acides amins branchs sont indiques ci-dessous.
1) Leucine + alpha-ctoglutarate ctoisocaproate + glutamate (rversible)
2) ctoisocaproate isovaleryl CoA (irrversible) + CO2
Ltape irrversible (2) est la dcarboxylation en position 1, toute remonte vers lacide
amin devient alors impossible. Cest au niveau de cette tape que sexerce une rgulation
hormonale et nutritionnelle particulirement fine.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Rle signalling des acides amins
De plus en plus de travaux voquent la possibilit que les acides amins remplissent une
fonction de signalisation vis vis de certains phnomnes cellulaires. Ainsi la leucine aurait
la capacit de stimuler dans le muscle la phosphorylation de certaines protines impliques
dans linitiation de la traduction cellulaire. Ces voies de signalisation seraient communes
avec celles de linsuline. De la mme manire, les neurones pourraient rpondre des
concentrations variables en acides amins par lactivation de voies spcifiques. Malgr la
solidit des travaux dans ces domaines, le mode de transmission du signal reste encore
inconnu (senseur, rcepteur).
IV LA PROTOLYSE (OU CATABOLISME PROTIQUE)
Elle constitue la principale source dacides amins pour lorganisme (75 % contre 25 %
pour les apports). Ses mcanismes ont t beaucoup moins tudis que ceux de la synthse
protique, en particulier en raison de difficults mthodologiques mais il sagit
certainement du domaine o la progression des connaissances a t la plus rapide au cours
des dix dernires annes. En rgle gnrale, les protines sont dgrades par des enzymes
protolytiques, les protases (ou hydrolases) rparties en trois systmes principaux :
Le systme lysosomal
Les enzymes concernes sont des protases actives en milieu acide, les cathepsines,
dnommes en fonction de lacide amin de leur site actif (cystine protinase : cathepsines
B, C, H, L, S, aspartate protinases : cathepsines D et E ; srine protinase : cathepsine G).
Ces enzymes sont localises essentiellement lintrieur des vsicules lysosomales qui
incorporent par endocytose les protines dgrader. Elles agissent essentiellement sur les
protines intracellulaires demi-vie longue, sur les membranes cellulaires, et sur les
protines extra cellulaires. Lendocytose peut galement concerner un fragment dorganite
voire un organite entier (macro autophagie). lintrieur de la vsicule, les cathepsines
vont dgrader la protine substrat en peptides et en acides ami-ns qui seront librs dans
le cytosol. Le type de cathepsine et de faon gnrale limportance de la protolyse
lysosomale varie selon lorgane considr : ce mode de dgradation est particulirement
important dans les organes renouvellement protique rapide (foie). Il ncessite de
lnergie sous forme dATP pour maintenir le pH acide lintrieur des lysosomes.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Le systme calpane-capastatine
Les calpanes (au nombre de trois) sont des protases cytosoliques dont lactivit est
troitement fonction de la concentration intracellulaire en calcium. Elles sont plus
spcialises dans la dgradation des protines du cytosquelette. La calpastatine est un
inhibiteur puissant des calpanes, lactivit protolytique globale dpendant de lquilibre
entre calpanes et calpastatine.
Le protasome (systme ATP dpendant)
Il sagit dun volumineux complexe enzymatique compos de nombreuses sous-units dont
deux formes, le protasome 20 S et le protasome 26 S ont t identifies. Les substrats
prfrentiels de ce protasome sont les protines intracellulaires normales, quelles soient
demi-vie courte ou longue mais aussi les protines anormales. Pralablement laction du
protasome 26 S, un marquage pralable de la protine dgrader par lubiquitine est
ncessaire. Lubiquitine est un petit peptide de 76 amins dont la squence est extrmement
conserve chez les eucaryotes. Il se fixe sur les protines dgrader (par liaison covalente
au niveau des rsidus lysine de la protine). Une fois la protine poly-ubiquitine, elle est
recon-nue par le protasome qui la dgrade en acides amins et en peptides courts
relchant lubiquitine qui peut alors tre rutilise. Lensemble de la raction ncessite
plusieurs enzymes, protines porteuses et co-facteurs. Surtout, la raction consomme de
lATP deux niveaux, dune part au moment de lubiquitination, dautre part au moment
de lintervention du protasome. Cette voie ATP dpendante reprsente probablement la
majorit de la protolyse au niveau musculaire. Elle est finement rgule par les
circonstances nutritionnelles et hormonales.
Les signaux de la protolyse
Une question fondamentale et encore non rsolue est la suivante : comment les diffrents
systmes protolytiques savent-ils quelle protine dgrader et quelle vitesse ? En
labsence de tels systmes de reconnaissance, on pourrait imaginer une protolyse continue
incontrlable et rapidement lthale. Il est clair quil existe un mcanisme de ciblage des
protines permettant de dsigner tel ou tel systme ce qui doit tre dgrad ou non. Ce
ciblage est fonction du poids molculaire, du degr de glycolysation, du point isolectrique,
mais des systmes plus spcifiques commencent tre identifis :
Identit de lacide amin N-terminal de la protine : certains acides amins N
terminaux sont stabilisants (par exemple mthionine, glycine) et ports par des
protines demi-vie longue, dautres sont dstabilisants (lysine, aspartate,
tryptophane) et donc ports par des protines demi-vie courte. Lacide amin N
terminal peut, au cours de la vie de la protine, tre modifi (asparagine
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
transforme en aspartate), ou peut recevoir un acide amin dstabilisant
supplmentaire, ou peut au contraire tre protg par une actylation (la
dsactylation exposant alors un acide amin dstabilisant).
les squences signal : il a t mis en vidence de courtes squences dacides
amins dnommes selon la nomenclature des acides amins avec une lettre
(squence KFERQ ou PEST, le K correspondant la glycine, le F la phnylalanine,
etc.). Ces motifs, inclus dans la squence primaire de la protine, deviendraient
exposs au fur et mesure du vieillissement de la protine par modification des
structures secondaires et tertiaires, lapparition du motif tant alors le signal pour la
dgradation de la protine.
Cependant, lheure actuelle, ces deux mcanismes ne concernent que quelques protines
et les signaux conduisant la dgradation de la majorit des protines restent mystrieux.
Au total, les points essentiels retenir sur la protolyse sont :
la notion que la protolyse consomme de lnergie En raison de la mutiplicit des
systmes protolytiques et de la moins bonne connaissance de la stoechiomtrie des
diffrentes ractions, il est difficile destimer, comme pour la synthse protique, un
cot nergtique du protolyse protique. En tout tat de cause, ce cot est
probablement lev.
la protolyse est tout autant que la synthse protique un phnomne trs bien
rgul par les conditions nutritionnelles et hormonales, mme si cette rgulation est
actuellement mal connue.
V LES APPORTS EN ACIDES AMINS EXOGNES
Ceci correspond lapport alimentaire en protines qui subissent aprs leur ingestion une
dnaturation par lacide chlorhydrique gastrique, une digestion enzymatique par la pepsine
et surtout les enzymes pancratiques (trypsine, chymotrypsine, lastase) et
carboxypeptidase, librant ainsi des acides amins et des di- et tripeptides qui sont absorbs
au niveau des villosits (cf. cours Physiologie Digestive). Les apports reprsentent chez un
adulte en pays dvelopp de 1 g 1,5 g de protine/jour (soit 70 g 100 g).
Seules quelques remarques permettant une meilleure comprhension du mtabolisme
protique seront faites ici :
la quantit dacides amins absorbe par le grle nest pas de 70 g 100 g mais
comprend en plus des protines ingres les protines scrtes par le tube
digestif sous forme denzymes, de mucus, de dbrits cellulaires... Ces protines
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
scrtes reprsentent environ 50 g et cest donc un total quotidien de 150 g
dacides amins qui vont arriver dans la veine porte,
le premier organe rencontr par les acides amins absorbs est le foie. Seule une
fraction des acides amins absorbs passe dans la circulation gnrale, le reste tant
transamin, oxyd ou incorpor dans les synthses protiques hpatiques. Ce
phnomne dextraction splanchnique
enfin il est intressant de constater qu partir dune protine alimentaire de
structure extrmement complexe, lorganisme dgrade cette protine en ses units
constitutives (les acides amins), pour reconstruire ultrieurement une protine tout
aussi complexe qui peut tre peine diffrente structurellement (par exemple pour
les protines myofibrillaires) de la protine ingre. Ce phnomne de dgradation
et de synthse est rendu indispensable par la spcificit despce des diffrentes
protines et va ncessiter une importante dpense nergtique.
VI SYNTHSE DES ACIDES AMINS NON ESSENTIELS
La premire tape de la dgradation des acides amins est habituellement une
dsamination. Cette raction est bi-directionnelle et un radical carbon (cto acide ou ctoanalogue ) peut rcuprer une fonction amine pour resynthtiser un acide amin. Seule la
lysine et la thronine ne peuvent tre resynthtises partir du radical carbon.
Un acide amin est dit essentiel lorsquil ne peut tre synthtis par lorganisme ce qui
implique quil doit tre apport par lalimentation. La liste des acides amins essentiels et
non essentiels chez lhomme est indique sur le tableau I. Dans certaines circonstances, un
acide amin peut devenir conditionnellement essentiel en raison par exemple dun besoin
particulirement lev ou dune immaturit des voies enzymatiques de synthse des novo,
par exemple chez le nouveau-n.
La finalit des ractions de transamination est de redistribuer lazote ingr de faon
adquate entre les diffrents acides amins ncessaires la synthse protique. Cette
redistribution dazote a t bien dmontre par ladministration dazote 15 qui, quelle que
soit la forme sous laquelle il est administr (15N glycine, par exemple) se retrouve
rapidement sur lensemble des acides amins libres de lorganisme. Ce phnomne peut
tre mis profit au cours de linsuffisance rnale, circonstance dans laquelle les apports
dazote doivent tre limits pour viter une augmentation trop importante de lure
plasmatique mais doivent cependant tre suffisants pour permettre une synthse protique
correcte et un bon tat nutritionnel. On peut alors remplacer lapport en acides amins
essentiels par lapport de leur cto-analogues qui namnent pas dazote mais vont toutefois
pouvoir tre ramins en acides amins, utiliss dans la synthse protique (sauf pour la
lysine et la thronine).
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Parmi les acides amins non essentiels, deux sont considrs comme particulirement
importants, lalanine et la glutamine :
le radical carbon de lalanine est fourni par le pyruvate lui-mme issu de la
glycolyse musculaire. Le pyruvate est transamin par le glutamate pour former de
lalanine. Lalanine forme, libre par le muscle, va tre utilise par le foie o son
radical carbon servira la noglucognse, son azote tant transfr sur le
glutamate tablissant ainsi un cycle alanine-glucose
la glutamine est lacide amin le plus abondant dans le plasma. Glutamate et
glutamine sont interconvertis par la glutaminase (Glutamine Glutamate) et la
glutamine syn-thtase (Glutamate Glutamine), chaque organe privilgiant lune
ou lautre voie, ce qui conduit la notion dorgane exportateur et importateur de
glutamine. Sa fonction principale est le transport dazote sous forme neutre. La
glutamine est produite par plusieurs organes, essentiellement le muscle, et est
utilise principalement par lentrocyte dont elle reprsente le substrat
nergtique majoritaire
Tableau I. Acides amins essentiels et non essentiels
Essentiels
Histidine
Leucine
Isoleucine
Valine
Isoleucine
Mthionine
Phenylalanine
Tryptophane
Thronine
Non essentiels
Alanine
Glutamine
Glutamate
Aspartate
Asparagine
Cystine
Proline
Glycine
Arginine
Tyrosine
Srine
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
VII LES MOYENS DEXPLORATION DU MTABOLISME PROTIQUE
IN VIVO
La quantification de la masse protique totale de lorganisme est effectue par des mthodes
de composition corporelle. lexception de la mesure de lazote corporel total par
activation neutronique, mthode lourde exclusivement destine la recherche, il nexiste
pas de mesure directe de la masse protique, qui est dduite de la mesure dautres
compartiments (masse grasse, eau corporelle).
Le bilan azot
Lquation de base du bilan azot est la suivante :
bilan = apport dazote (azote urinaire + azote fcal + autres pertes azotes)
Par dfinition, le bilan azot indique lvolution nette de la masse protique, sous rserve
que le compartiment de lazote non protique (cest--dire le compartiment dacides amins
libres et surtout lure) reste stable pendant la priode de mesure. Il est positif lorsque la
masse protique saccrot, cest le cas en priode de croissance, proche de zro chez un
adulte dont la masse protique est constante, et ngatif dans des circonstances
pathologiques accompagnes dune fonte protique.
Bien que conceptuellement simple, le bilan azot est de ralisation dlicate si une bonne
prcision est recherche. Parmi les problmes pratiques, on peut citer :
lazote urinaire reprsente la majeure partie de lexcrtion azote (90 % chez
ladulte), le recueil des urines doit tre mticuleux. Le simple dosage dure urinaire
(80 % de lazote urinaire, mais cette proportion peut varier) peut tre une indication
suffisante en clinique mais le dosage de lazote total
la quantification des apports est difficile en dehors des situations de nutrition
artificielle, le dosage effectif de lazote ingr (mthode des plateaux dupliqus) est
prfrable celui de lestimation par les tables de composition alimentaire.
lexcrtion azote fcale est en principe faible (10 % 15 % des pertes azotes). Il ne
faut pas oublier de prendre en compte lexcrtion azote des fistules digestives
lorsquelles existent.
les pertes insensibles (sueurs, desquamations, phanres...) reprsentent environ 10
mg dazote par kg par jour dans des circonstances normales.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Globalement un bilan azot fiable doit tre pratiqu sur une priode minimum de 3 5
jours. Il sagit donc dun examen relativement lourd en pratique clinique. On peut lui
substituer le seul dosage dazote urinaire dj trs informatif pour le suivi dune
alimentation artificielle. Signalons enfin que compte tenu de la tendance la surestimation
des entres et la sous estimation des pertes, les bilans azots sont quasi
systmatiquement survalus.
La chromatographie des acides amins
La mesure des concentrations plasmatiques en acides amins est parfois propose comme
tmoin de ltat nutritionnel. Bien que cette concentration soit abaisse au cours des
malnutritions protiques svres, son intrt est minime en pratique courante : les acides
amins plasma-tiques ne reprsentant quun faible pourcentage des acides amins totaux et
leur concentration dpend de lquilibre entre synthse, protolyse et oxydation, ce qui la
rend dinterprtation difficile. Il sagit de plus dun dosage assez dlicat.
Les mthodes dynamiques
Ces mthodes ont en commun dtre plus invasives et de ncessiter des techniques
analytiques plus lourdes, elles sont encore rserves au domaine de la recherche.
Les mthodes dynamiques locales (diffrences artrio-veineuses)
La mthode consiste tablir un bilan des acides amins de part et dautre dun organe ou
dun tissu. Chez lhomme, la mthode a t essentiellement pratique sur des segments de
membres (avant-bras et membre infrieur) et reflte donc surtout le mtabolisme protique
musculaire. Connaissant les concentrations artrielles et veineuses des diffrents acides
amins ainsi que le dbit sanguin, on peut dduire pour chaque acide amin un bilan net
positif ou ngatif selon ltat nutritionnel. Ladjonction de traceurs permet galement laccs
la synthse et la protolyse musculaire. Le transport des acides amins dans le muscle
peut aussi tre calcul si une biopsie est ajoute. Linconvnient de la mthode est dordre
pratique puisquelle ncessite un cathtrisme artriel.
Les mthodes dynamiques globales
Elles donnent accs la synthse et la protolyse au niveau du corps entier ainsi qu
loxydation des acides amins. Elles ncessitent lutilisation de traceurs qui, en France, sont
exclusivement des acides amins marqus avec des isotopes stables non radioactifs (carbone
13, deutrium ou azote 15). Ces traceurs, inoffensifs, ont linconvnient de ncessiter pour le
dosage un spectromtre de masse, appareil complexe et coteux.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Le principe gnral de la mthode est celui de la dilution isotopique (Annexe I). Le dbit
de production dun acide amin est calcul en mesurant la dilution dun acide amin
marqu introduit dans lorganisme. Le rapport de dilution (acide amin marqu/non
marqu) est inversement proportionnel au dbit de production de lacide amin. ltat
stationnaire (concentrations stables), ce dbit de production est gal au dbit dutilisation.
Lensemble production-utilisation constituant le dbit de renouvellement de lacide amin.
La destine de lacide amin peut galement tre quantifie dans certaines voies
mtaboliques si lon suit le traceur dans lorganisme. On mesure ainsi loxydation dun
acide amin en collectant dans les gaz expirs le CO2 marqu rcupr aprs
administration dun acide amin marqu au carbone 13.
La mthode la plus couramment utilise chez lhomme est celle dite des prcurseurs o
lacide amin utilis est la leucine. Le modle est dcrit sur la figure en annexe I. Dans cette
situation, le dbit de leucine issu des protines est un index de la dgradation protique.
Le dbit dutilisation de la leucine comporte deux composantes : le flux de leucine
incorpor dans les protines, index de la synthse protique, et loxydation de la leucine.
Cette oxydation de la leucine est mesure, on en dduit par soustraction un index de la
synthse protique.
Lors de la prise alimentaire, ladjonction dun traceur dans le repas permet de mesurer
lextraction splanchnique des acides amins et de corriger la protolyse pour la quantit
dacides amins utilise au niveau des tissus splanchniques (foie, intestin). Les flux dacides
amins dtourns vers la synthse ou provenant de la protolyse peuvent tre convertis en
flux de protines sur la base dun contenu moyen de lacide amin choisi dans les protines
totales de lorganisme (8 % pour la leucine et 4 % pour la phnylalanine). La
reprsentativit de lacide amin vis--vis du mtabolisme protique corps entier est
donc un point crucial et va dterminer le choix de cet acide amin.
La plupart des tudes utilisent la leucine, acide amin essentiel, dont la dgradation
oxydative est simple, se droule la fois dans le foie et dans le muscle (alors que la majeure
partie des autres acides amins ont une oxydation essentiellement hpatique), et dont
lanalyse en spectromtrie de masse est relativement facile.
Ce modle largement utilis et dont ont t drivs les chiffres indiqus dans lintroduction
pose cependant un certain nombre de problmes :
Lacide amin rellement prcurseur de la synthse protique nest pas un acide
amin plasmatique mais un acide amin intracellulaire et plus prcisment un acide
amin li lARNt. Ce pool nest pas accessible au prlvement chez lhomme
moins de pratiquer des biopsies. On peut sen approcher en mesurant le marquage
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
non plus dans la leucine plasmatique mais dans le ctoisocaproate, produit de
transamination de la leucine plus reprsentatif du marquage intracellulaire.
Une mesure quantitative prcise de loxydation de la leucine est difficile
(rcupration incomplte du CO2
Il sagit de mesures au niveau du corps entier ne renseignant pas sur lvolution du
mtabolisme protique au niveau dun tissu donn.
Les mesures de synthse de protines spcifiques
Aprs introduction dun traceur dans lorganisme (soit par perfusion continue, soit par la
mthode dite de surcharge ), on peut mesurer lincorporation du traceur au cours du
temps dans la protine considre. En dehors de relles difficults analytiques, la mthode
est relativement facile pour la mesure des dbits de synthse de protines circulantes
(albumine, apolipoprotine...) mais savre plus difficile pour la mesure de synthse de
protines tissulaires comme le muscle puisque lon doit alors recourir une biopsie. Il est
galement ncessaire de distinguer les diffrentes fractions protiques au sein dun tissu,
cest dire de dvelopper des mthodes permettant lanalyse fine de la rgulation des
protines spcifiques musculaires. partir dune biopsie musculaire, il est possible de
sparer les protines myofibrillaires, mitochondriales et sarcoplasmiques pour mesurer leur
vitesse de synthse respective. Dans un avenir proche, des mthodes plus sophistiques
devraient permettre lidentification, la purification et la mesure de trs faibles quantits de
protines pour ltude de leur rgulation et de leurs fonctions dans lorganisme. Cette
nouvelle re de recherche dont le dveloppement est assimilable ltude du gnome
prfigure ce domaine effervescent que lon nomme le protome ou le mtabolome.
En conclusion, le choix dune mthode dexploration du mtabolisme protique va
essentiellement dpendre des possibilits techniques disponibles et de la question pose
en pratique clinique, dans le cas par exemple dune alimentation artificielle, la
mthode choisie doit tre simple et rapide. On choisira de suivre, par exemple
lazote (ou lure) urinaire, la 3 mthyl-histidine, ou encore lvolution des protines
de transport (cf. chapitre spcifique).
lorsquun bilan protique net court terme (quelques jours) doit tre mesur, le
bilan azot est lexamen de choix.
lorsquun bilan protique net sur plusieurs semaines doit tre valu, cest une
estimation de masse protique quil faudra pratiquer (cf. composition corporelle).
enfin, les tudes portant sur la rgulation de la synthse et du protolyse protique
ncessiteront lutilisation de mthodes dynamiques ventuellement associes des
techniques de biologie molculaires. Cette approche intgrative permet de prciser
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
les mcanismes intimes lorigine dun gain ou dune perte dune ou plusieurs
protines.
Annexe 1 : Principe de dilution isotopique
VIII RGULATION DU MTABOLISME DES PROTINES
Cette rgulation est dune part hormonale, dautre part nutritionnelle (cest--dire par les
substrats eux-mmes). Cette distinction est artificielle puisque dans la majorit des
circonstances physiologiques, ces deux modes de rgulation sont simultans et agissent en
synergie lors de la prise alimentaire.
Rgulation hormonale
Les hormones peuvent tre anabolisantes (favorisant le gain protique) ou catabolisantes
(favorisant la perte protique).
Linsuline
Il sagit dune hormone anabolisante indispensable au gain protique et la croissance. Son
mcanisme daction en terme de synthse et de protolyse continue cependant faire lobjet
dune vive controverse. Un gain protique peut en effet tre obtenu par augmentation de la
synthse protique, par rduction de la protolyse ou par les deux phnomnes combins.
Au niveau cellulaire et molculaire, linsuline augmente la synthse protique en stimulant
la transcription et la traduction. Au niveau tissulaire, linsuline stimule la synthse
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
protique musculaire en particulier chez lanimal jeune en croissance ou lorsquelle est
utilise dose pharmacologique ou lorsque de linsuline est rajoute partir dune situation
totalement insulino-prive. Cette dernire situation est frquente in vitro o sont volontiers
compars des milieux avec et sans insuline ne refltant pas la ralit physiologique
o linsuline nest jamais compltement absente.
Chez ladulte, et en particulier chez lhomme, linsuline est anabolisante essentiellement par
une rduction de la protolyse que ce soit au niveau du corps entier ou du muscle. Dans
cette situation, linsuline ne semble pas avoir deffet sur la synthse protique. En dehors de
problmes mthodologiques, cette apparente dissociation des effets de linsuline semble
tre lie essentiellement lge, les tudes animales ayant lieu presque exclusivement sur
des animaux en croissance alors qu linverse, aucune tude de ce type nest disponible
chez lenfant. Par ailleurs, leffet stimulant de linsuline sur un tissu peut tre contrebalanc
par un effet inhibiteur sur la synthse protique dautres tissus comme le suggrent des
tudes rcentes de cathterismes tissulaires multiples.
Lhormone de croissance
Elle est anabolisante essentiellement par un effet stimulant de la synthse protique
agissant directement et par lintermdiaire des facteurs de croissance (IGF1). Cette proprit
pourrait tre exploite chez lhomme pour prvenir la fonte musculaire du sujet g (et de
faon illgale dans les milieux sportifs pour augmenter la masse musculaire). Lhormone de
croissance bovine dont le mcanisme daction est similaire est largement utilise pour
augmenter la production de lait chez la vache.
Les catcholamines
Contrairement lide couramment reue, il est bien dmontr maintenant que les
catcholamines ne sont pas des hormones catabolisantes vis--vis du mtabolisme
protique. Selon les auteurs, elles rduisent la protolyse ou augmentent la synthse
protique, lapplication la plus classique de ces proprits anabolisantes tant lutilisation
de bta-agonistes de type clembutrol pour la production de viande de boucherie. En tout
tat de cause, ce ne sont donc pas les catcholamines hormones de stress qui sont
responsables de la fonte musculaire des patients de ranimation.
Les glucorticodes
Ils sont catabolisants par laugmentation de la protolyse musculaire et par linhibition de
la traduction des protines comme en tmoignent les fontes protiques constates lors des
hypercorticismes (maladie de Cushing) ou des traitements glucocorticodes au long cours.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Les hormones thyrodiennes et le glucagon
Ils ont des effets plus complexes :
en ce qui concerne les hormones thyrodiennes, lhyperthyrodie induit une fonte
musculaire suggrant une augmentation de la protolyse et galement une rduction des
synthses protiques dans diffrents tissus. Cependant, ces phnomnes et en particulier la
rduction de synthse protique sont retrouvs galement dans les situations
dhypothyrodie et lon sait galement que les hormones thyrodiennes sont indispensables
la croissance. Il est donc difficile de classer les hormones thyrodiennes comme
anabolisantes ou catabolisantes et lon peut dire quun niveau optimal moyen dhormone
thyrodienne est ncessaire un bon quilibre entre synthse et dgradation.
en ce qui concerne le glucagon, son importance relle dans la rgulation du mtabolisme
protique est conteste et semble se situer surtout au niveau du mtabolisme splanchnique
des acides amins. Malgr des donnes contradictoires, un effet catabolisant semble
prdominant.
Les cytokines (TNF, interleukines)
Elles sont catabolisantes au niveau du muscle. Leurs effets varient selon les cytokines et les
tissus. Les cytokines comme TNF agissent en synergie avec le cortisol et la combinaison de
leurs effets provoque une protolyse rapide et massive lorigine dune fonte protique
musculaire.
Rgulation nutritionnelle
Elle sera envisage sous deux aspects :
dabord la rgulation par les substrats eux-mmes , quil sagisse des acides amins
ou des autres substrats nergtiques,
ensuite lvolution du mtabolisme protique au cours des diffrentes circonstances
nutritionnelles que sont le repas et le jene
Rgulation par les substrats
a) les acides amins : que ce soit in vitro ou in vivo, les acides amins stimulent
globalement la synthse protique. Cet effet est particulirement net pour les acides amins
branchs, cette spcificit ne stant toutefois pas traduite par une efficacit particulire des
soluts enrichis en acides amins branchs en raison dune possible comptition entre les
acides amins.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
b) les autres substrats nergtiques : de faon gnrale, un apport nergtique suffisant est
indispensable au maintien dun bilan azot neutre ou positif. La source des apports
nergtiques nest pas indiffrente et classiquement, les glucides auraient un effet dpargne
azote suprieur celui des lipides au moins dans des circonstances dapport nergtique
limit. Cette notion est trs discute voire errone pour certains et de toute faon, nest plus
vrai lorsque les apports nergtiques sont excdentaires.
Cette liaison entre apports nergtiques et mtabolisme protique relve de plusieurs
mcanismes complmentaires :
le renouvellement protique (synthse mais aussi protolyse) est un
consommateur dnergie important. Une limitation de lapport nergtique se
traduira donc par son ralentissement.
les acides amins et le glucose sont en comptition au niveau de loxydation
mitochondriale par un mcanisme similaire celui du cycle de Randle entre glucose
et lipides. Un dficit dapports en ces substrats nergtiques se traduira donc par
une oxydation plus importante des acides amins qui ne seront plus disponibles
pour la synthse protique.
certains substrats (acides gras chaine moyenne par exemple) peuvent avoir un
effet spcifique dactivation des enzymes de dgradation des acides amins.
les substrats nergtiques agissent enfin par lintermdiaire des hormones et en
particulier, par linsuline (glucose insuline rduction de la protolyse).
Rgulation du mtabolisme protique au cours de diffrents tats nutritionnels
On dfinit trois tats successifs en physiologie de la nutrition :
ltat nourri correspond la priode pendant laquelle des nutriments ingrs
arrivent du tube digestif dans la circulation. Selon le type de nutriments, il dure
entre 3 et 8 heures aprs un repas.
ltat post-absorptif correspond aux 12 18 heures suivant ltat nourri, cest--dire
le matin jeun.
Il est suivi par le jene, soit court (2 3 jours), soit prolong (suprieur 3 jours).
Lvolution gnrale du mtabolisme protique est la suivante :
a) ltat post-absorptif,
la synthse, la protolyse et loxydation sont leur niveau basal, la protolyse tant
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
lgrement suprieure la synthse et lorganisme tant donc en bilan ngatif. Ce niveau
basal de renouvellement protique dpend des apports protiques des jours prcdant, il
est acclr en cas dapports importants, rduit en cas dapports faibles. Au niveau
tissulaire, dans cette circonstance, le muscle est un producteur net dacides amins en
quantit modre.
b) Lors dun repas (tat nourri) :
par des mcanismes lis la fois lapport en substrats et lhyperinsulinisme, lorganisme
est alors en bilan positif. Loxydation des acides amins dans le muscle (pour les acides
amins branchs) et surtout dans le foie, augmente massivement ce qui correspond un
azote urinaire lev. Cette augmentation est proportionnelle aux apports protiques et
correspond pour lorganisme un moyen dliminer les acides amins excdentaires, le but
recherch tant lobtention la fin dun nycthmre (tat nourri + tat post absorptif) dun
bilan azot nul. Ceci explique limpossibilit daugmenter la masse protique de
lorganisme par simple augmentation des apports protiques.
En ce qui concerne la synthse et la protolyse, le gain protique est obtenu au niveau du
foie, essentiellement par rduction de la protolyse et au niveau du muscle (qui ltat
nourri stocke des acides amins) par augmentation de la synthse protique, au moins chez
lanimal jeune en croissance. Au niveau du corps entier, les donnes restent plus
controverses : il existe indiscutablement une rduction de la protolyse globale au moment
du repas et peut tre une augmentation modre de synthse.
c) Lorganisme repasse ensuite ltat post absorptif puis au jene court :
De multiples modifications hormonales (diminution de linsulinmie) et des mtabolismes
(augmentation de la noglucognse, de la lipolyse puis de la ctognse) vont survenir.
Lors du jene court, la bilan azot est initialement fortement ngatif avec des pertesazotes
importantes. cette phase, la protolyse est leve, le muscle fournissant des acides amins
pour la no-glucognse et la synthse protique diminue lentement.
d) Au cours du jene long,
lexcrtion azote va diminuer pour se stabiliser aux environs de 50 mg/kg/jour, ce qui
constitue les pertes azotes obligatoires. La protolyse reste bien sr suprieure la
synthse (do le bilan ngatif) mais, globalement le renouvellement protique tend
diminuer avec des valeurs de protolyse qui sont rapidement infrieures ce quelles sont
ltat post absorptif. Cette pargne azote relative, permettant de minimiser la rduction de
la masse protique, est un mcanisme essentiel de dfense au cours du jene chez
lhomme et les mammifres. Il permet une survie prolonge de 40 60 jours, le dcs
survenant lorsque la masse protique descend en dessous dune valeur que lon peut
estimer 50 %-60 % de la masse initiale. Le mcanisme dpargne azote relative reste
inconnu, il ne semble pas hormonal, mais dpendrait plutt des substrats nergtiques
privilgis au cours du jene que sont les acides gras et les corps ctoniques.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
IX BESOINS EN AZOTE ET EN ACIDES AMINS ET SOURCES
PROTIQUES ALIMENTAIRES
Les besoins en azote et acides amins
Dfinitions
Le besoin dun individu en un nutriment (ici azote ou acide amin) est la quantit de ce
nutriment ncessaire au maintien dune fonction physiologique satisfaisante. Pour les
protines, on considre que le maintien dun bilan azot positif en phase de croissance ou
nul chez ladulte, tmoigne dun besoin satisfait. Sa valeur varie bien sr selon les individus
et leur tat physiopathologique (ge, sexe...). Lapport idal pour un individu est celui qui
couvre ses besoins.
Les apports conseills (Recommended Dietary Allowances ou RDA pour les USA et les
ANC pour la France) sont ceux qui permettent la couverture des besoins dune population
donne. Par dfinition, ces apports sont suprieurs aux besoins de la majorit (cf.note : (97,5
%)) des individus composant cette population. On considre en effet, tout au moins en ce
qui concerne lazote et les acides amins, quil ny a pas dinconvnient apporter une
quantit suprieure aux besoins rels. Les niveaux officiels des besoins et apports font
lobjet de confrences de consensus rgulires entre les grands organismes internationaux
(OMS, FAO, etc.). Les chiffres varient donc lgrement au fil des annes. En ce qui concerne
les protines, les besoins doivent tre envisags deux niveaux, dune part en terme de
besoin azot total, dautre part en terme dacides amins essentiels, la qualit de lazote
amen ntant pas indiffrente.
Les besoins en azote
Ils ont t dtermins en mesurant la quantit minimum dazote ingr sous forme de
protines doeufs ou de lait (protine de haute qualit) qui permet de garder un bilan azot
neutre (chez ladulte). Le chiffre obtenu sur un petit groupe dindividus adultes en bonne
sant est en moyenne de 0,6 g de protines/kg/j. Le coefficient de variation de cette
moyenne est de 12,5 %, qui correspond des apports individuels variant de 0,45 0,75
g/kg/j (0,75 g/kg. j correspondant donc la moyenne + 2 DS). Ce dernier chiffre, arrondi
0,8 g/kg/j est donc retenu comme lapport conseill permettant de couvrir les besoins dune
population normale adulte. Ce besoin est trs largement couvert dans les pays dvelopps
o les apports sont de lordre de 1,2 1,5 g/kg/j. Les apports conseills (et les besoins) sont
plus levs chez le nourrisson (2,2 g/kg/j), dcroissent progressivement jusqu lge
adulte (0,8 g/kg/j), augmentent au cours de la grossesse et au cours de la lactation (+ 5 +
15 g de protine/j). Lorsque les besoins sont exprims en valeurs absolues, ils sont peu
prs constants pendant la premire anne de vie ( 10 g/j). Ils restent mal connus chez le
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
sujet g probablement peu diffrents de ceux de ladulte voire suprieurs (1 1,2 g/kg/j).
Lexactitude des bilans azots est ici un lment essentiel pour apprcier ces besoins
puisque la surestimation de la balance conduira la sous-estimation des besoins. De mme
une attention particulire doit tre apporte au contenu nergtique du rgime sous
lequel a t dtermin le besoin : un apport nergtique excdentaire rsultera en une
dposition protique (ce qui correspond laugmentation de la masse maigre au cours de
lobsit) et rsultera en une sous-estimation des besoins.
Les besoins en acides amins
Ils sont dtermins par la mthode suivante : des sujets reoivent une alimentation
parfaitement quilibre contenant tous les nutriments et tous les acides amins en quantit
suffisante lexception de lacide amin dont on veut mesurer le besoin. En labsence de cet
acide amin, le bilan azot est ngatif ce qui illustre le fait que labsence dun seul acide
amin suffit ralentir la synthse protique (notion dacide amin limitant). Lapport en cet
acide amin est alors progressivement augment : lorsque le bilan azot se positive, le
besoin est alors couvert.
L encore, la qualit des rsultats obtenus dpend de lexactitude du bilan azot. Les
rsultats obtenus par cette mthode sont actuellement contests par certains groupes qui
ont propos de mesurer non plus le bilan azot mais loxydation de lacide amin par des
mthodes isotopiques. Cette oxydation reste minimale tant que les besoins de la synthse
protique ne sont pas couverts puis augmente rgulirement ds que le besoin est atteint.
Les rsultats obtenus par cette mthode sont deux trois fois suprieurs ceux obtenus
classiquement. Pour linstant, les recommandations alimentaires internationales sen
tiennent aux chiffres obtenus par la mthode classique.
Les besoins de chacun des neuf acides amins pour lensemble des acides amins essentiels
sont, selon lacide amin, de 30 150 mg/kg/j chez le nourrisson (au total 750 mg/kg/j) et
seulement de 5 15 mg/kg/j (au total 80 mg/kg/j) chez ladulte. Ceci correspond aux
besoins importants de la synthse protique en priode de croissance. Les acides amins
essentiels doivent donc reprsenter chez le nourrisson plus du tiers de lazote total
apport (ce qui signifie que les protines alimentaires devront tre de haute qualit, cf
infra). Chez ladulte, cest seulement 10 % de la ration azote qui devra tre compose
dacides amins essentiels.
Enfin certains acides amins peuvent tre conditionnellement essentiels, ce qui signifie
que, loccasion dune circonstance physiopathologique donne, leur synthse endogne
nest pas suffisante pour couvrir les besoins. Cest le cas de la cystine et de la tyrosine qui
peuvent normalement tre obtenues partir de la mthionine et de la phnylalanine
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
respectivement. Dans des circonstances telles que la prmaturit et linsuffisance hpatique,
ces conversions seront insuffisantes pour couvrir les besoins et un apport exogne devient
donc ncessaire. De la mme faon, il est probable que les acides amins du cycle de lure
(arginine, ornithine et citrulline) deviennent conditionnellement essentiels au cours des
insuffisances hpatiques et peut tre pour larginine en priode de croissance rapide. Il faut
enfin citer le cas de la taurine, acide amin libre abondant dans lorganisme mais non
incorpor dans les protines. La taurine est amene en quantit suffisante par le lait de
femme mais pas par le lait de vache et un dficit dapport en taurine peut rsulter en des
anomalies de la fonction rtinienne.
Enfin, il faut se souvenir que les critres d essentialit sont troitement fonction de ltat
physiologique. Il est trs probable que les besoins rels de plusieurs acides amins au cours
des tats cataboliques, ou septiques sont diffrents des besoins dcrits ici qui se rapportent
uniquement lindividu normal.
Les sources protiques alimentaires
Notion de qualit dune protine
Toutes les protines ne sont pas quivalentes pour remplir les besoins. La qualit (ou valeur
nutritionnelle) dune protine se dfinit comme lefficacit avec laquelle cette protine
satisfait au besoin la fois en azote et en acides amins. Le critre le plus classique de
qualit est la valeur biologique dfinit comme suit :
valeur biologique = fraction de lazote apport retenu
par lorganisme/azote absorb par lintestin une valeur biologique de 100 est donc une
protine dont lazote absorb est efficace 100 % pour remplacer les pertes azotes
endognes. Un autre critre couramment utilis est lutilisation protique nette :
utilisation protique nette = fraction de lazote retenu/ azote ingr.
Dautres paramtres tels que le coefficient defficacit protique (CEP) ou le coefficient
defficacit protique net (bass sur les gains pondraux) sont galement couramment
utiliss. La mesure de ces diffrents paramtres est plus ou moins facile selon le dosage
requis (gain de poids ou dosage dazote). Surtout, elle dpend du niveau dapport
protique puisque niveau dapport protique lev, la proportion dazote retenu ne sera
pas augmente et la valeur biologique de la protine sera donc sous-estime. Enfin la
qualit dune protine a t volontiers teste chez lanimal de laboratoire, en particulier
chez le rat, dont les besoins sont diffrents de ceux de lhomme.
Cette valeur biologique globale dpend en fait de la structure intrinsque de la protine et
galement de la faon dont les acides amins constituants sont absorbs par le tube digestif.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
a) Lindice chimique :
il est inhrent une protine donne et se dfinit comme suit :
indice chimique = mg dun acide amin essentiel dans 1 g de protine/mg du mme
acide amin essentiel dans 1 g de protine de rfrence.
La protine de rfrence la plus courante est lalbumine de luf. Par exemple, si on
considre la quantit de lysine contenue dans la farine de bl (35 mg/g de protine)
rapporte celle contenue dans lalbumine (70 mg/g de protine) on arrive un indice
chimique pour la lysine et pour la protine de bl de 50 % (35/70). En thorie, lindice
chimique doit tre dtermin pour chaque acide amin essentiel dans une protine donne.
En pratique, on se contente dindiquer lindice chimique le plus bas parmi ceux des
diffrents acides amins, cet acide amin tant appel acide amin limitant (en pratique
sont concerns, la lysine, les acides amins soufrs et le tryptophane). Lalbumine de luf a
t longtemps utilise comme protine de rfrence, mais actuellement la composition de la
protine de rfrence est dtermine en fonction des besoins propres chaque situation
(nouveau-ns, nourrissons, enfants...).
b) La digestibilit est dfinie comme la capacit du tube digestif absorber effectivement
lazote ingr et se calcule comme suit :
azote ingr azote fcal 100
digestibilit = ------------------------------------------------------------------------------azote ingr
La digestibilit vraie inclue de plus une correction pour les pertes azotes fcales
obligatoires. La digestibilit dpend de la structure de la protine elle-mme mais
galement des ventuelles modifications que cette structure a pu subir au cours de la
prparation des aliments. La modification la plus classique est celle obtenue par la raction
de Maillard. Il sagit de la liaison dun sucre rducteur avec le groupe amin libre de la
lysine rsultant en un blocage de celle-ci. Cette lysine ne pourra donc plus tre absorbe
et 10 % 40 % de la lysine ingre (ce chiffre variant selon le mode de cuisson) seront donc
non disponibles, ce qui rduit dautant la digestibilit de la protine. Enfin, les interactions
avec dautres nutriments (en particulier les fibres et les polyphnols) peuvent jouer sur la
digestibilit dune protine.
Au total, la digestibilit est de 95 % 98 % pour les protines animales et de 75 % 95 %
pour les protines vgtales.
Lutilisation protique nette se rsume donc au produit de la digestibilit par lindice
chimique : elle est de 40 % environ pour les protines vgtales de type mas ou mil, 70 %
pour les protines de viande, 87 % pour lalbumine de luf et 95 % pour le lait de femme.
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
Les sources protiques alimentaires
Les protines alimentaires sont classiquement divises en protines animales (viande,
poisson, laitage et ufs) et en protines vgtales (crales et lgumineuses). La richesse en
protines des aliments varie considrablement (pain 2,7 % ; viande 18 % ; fromage et
lgumes secs : environ 25 % , exprime en pourcentage du poids total de laliment).
Comme vu plus haut, la qualit de la protine est galement importante considrer.
Classiquement les protines vgtales sont de qualit infrieure aux protines animales
en raison dune digestibilit plus basse et dun moindre contenu en acides amins
essentiels, en particulier lysine et acides amins soufrs. La densit protique basse et la
faible qualit des protines vgtales expliquent trs largement lextrme frquence des
malnutritions protiques dans les pays en voie de dveloppement en particulier chez
lenfant, trs sensible des apports insuffisants en acides amins essentiels. Il est cependant
tout fait possible dobtenir un apport en acides amins essentiels suffisant avec des
protines vgtales en prenant simplement soin de combiner des protines dont lacide
amin limitant nest pas le mme (protines de crales pauvre en lysine mais normalement
riche en acides amins soufrs et protines de lgumineuses pauvres en acides amins
soufrs mais normalement riches en lysine). Cette tactique est volontiers adopte dans
les rgimes vgtariens.
Le principe de dilution isotopique est le suivant (prenons ici lexemple de la leucine). On
souhaite mesurer le dbit de production de la leucine, cest--dire la quantit de leucine
arrivant dans le plasma par unit de temps (leucine issue soit de la protolyse, soit de la prise
alimentaire). On introduit dans le plasma un traceur, la leucine marque (Dbit Leu*) un
dbit connu et constant (en mol/kg/min) laide dun pousse seringue. Lorsque ltat
dquilibre est atteint (stabilit des enrichissements isotopiques mesurs posteriori), on
dmontre que le rapport des dbits de production de leucine marque et non marque est
gal au rapport de leurs concentrations respectives, ce qui scrit :
Production Leucine/Dbit Leu* = Leu/Leu*
ou encore
Production Leucine = Dbit Leu*/( Leu*/Leu)
Le dbit de traceur tant connu, le rapport [Leu*/Leu] mesur (spectromtrie de masse), on en
dduit le dbit de Production de leucine. Cette quation simple nest valable qu ltat
stationnaire, cest--dire lorsque ni Leu] ni Leu* ne varient pendant la priode de mesure.
Dans ces conditions, le dbit de production (correspondant la somme apports exognes +
protolyse) est gal au dbit dutilisation (soit synthse protique + oxydation). En dautres
termes, ltat stationnaire le pool plasmatique ne variant pas, ce qui entre est gal ce
qui sort . Cette contrainte dobtention dun tat stationnaire est lune des limites de
lutilisation des traceurs, vidente par exemple au cours de ltude des repas o la stabilit
- Universit Mdicale Virtuelle Francophone -
- Support de Cours (Version PDF) -
des concentrations est difficile obtenir. La ncessit de travailler une fois lquilibre atteint
explique le dlai impos (environ 2 heures pour la leucine) aprs le dbut de la perfusion
pour obtenir des prlvements significatifs.
NOTE(S) DU CHAPITRE
(97,5 %) : Les apports recommands sont dfinis comme les apports couvrant les besoins
moyens + 2 dviations standards (soit, par dfinition, 97,5 % de la population) + un
supplment variable selon les experts.
X ANNEXES
BIBLIOGRAPHIE
[1] Devlin TM Ed., : Textbook of Biochemistry. Wiley Liss, New York 1992.
Biochimie de la synthse protique (rgulations).
[2] Young V.R., Yu Y.M., Fukagawa N.K. : Energy and protein turnover. In
Energy metabolism , JM. Kinney, H.N. Tucker ed., Raven Press, New York, 1992
(relations nergie/protines).
[4] Beaufrere B., Attaix D. : Mtabolisme protique. In Trait de Nutrition
artificielle de ladulte SFNEP, X. Leverve, J. Cosnes, P. Erny, M. Hasselmann Ed.,
2001, 63-80.
[5] Dossiers scientifiques de lIFN : les protines n 9 Tome I et II.
[6] Martin A. : Apports nutritionnels conseills. Tec & Doc. Lavoisier, Paris 2001.
[7] Boirie Y, Walrand S, Beaufrre B. : Control of amino acid metabolism by lipids,
ketone bodies, and glucose substrates. In Metabolic and therapeutic aspects of
amino acids in Clinical Nutrition, LA Cynober Ed, CRC Press, Boca Raton 2004, 241252
3] Mc Nurlan M.A., Garlick P. : Influence of nutrient intake on protein turnover.
Diab. Metab. Rev., 1989, 5, 165189 (rgulation nutritionnelle).
- Universit Mdicale Virtuelle Francophone -
S-ar putea să vă placă și
- Annatut27 UE2 Biologie Cellulaire 2012 2013Document51 paginiAnnatut27 UE2 Biologie Cellulaire 2012 2013Mohamed hicham AllamÎncă nu există evaluări
- Acides AminesDocument11 paginiAcides Aminesislmioun100% (1)
- 2.-Biosynthèse Des ProtéinesDocument65 pagini2.-Biosynthèse Des Protéinesmido benÎncă nu există evaluări
- Le Complexe Majeur Dhistocompatibilité 2018 CopieDocument10 paginiLe Complexe Majeur Dhistocompatibilité 2018 Copietara mourad100% (1)
- Orar Sem 1 S1 Forma FinalaDocument91 paginiOrar Sem 1 S1 Forma FinalaMocanu BiancaÎncă nu există evaluări
- Cycle KrebsDocument1 paginăCycle Krebsgeorgi.annaÎncă nu există evaluări
- Orar Sem 1 S1 Forma FinalaDocument91 paginiOrar Sem 1 S1 Forma FinalaMocanu BiancaÎncă nu există evaluări
- Beta Oxidarea Ac GrasiDocument1 paginăBeta Oxidarea Ac GrasiAndra ValentinaÎncă nu există evaluări
- Biosinteza Ac GrasiDocument1 paginăBiosinteza Ac GrasiCami ManailaÎncă nu există evaluări
- Chimie FR 2013 SecondaireDocument4 paginiChimie FR 2013 SecondaireMocanu BiancaÎncă nu există evaluări
- Le Système UbiquitineDocument6 paginiLe Système UbiquitineJoie De VivreÎncă nu există evaluări
- Thése: Membres Du JuryDocument221 paginiThése: Membres Du JuryantoinegoisnardÎncă nu există evaluări
- COURS Biochimie Des Aliments Et RégulationDocument52 paginiCOURS Biochimie Des Aliments Et RégulationSiremÎncă nu există evaluări
- Immunologie Moléculaire: M Ba Université F.M.Constantine M Moussaoui SDocument2 paginiImmunologie Moléculaire: M Ba Université F.M.Constantine M Moussaoui Sjiji doctoÎncă nu există evaluări
- CEG DegradationDocument37 paginiCEG DegradationAmina-Amel elhaffafÎncă nu există evaluări
- 2015LIL2S007Document281 pagini2015LIL2S007Oum Elkhir BELHADADÎncă nu există evaluări
- Biochimie Des Animaux Domestiques I Synthèse: Objet Du CoursDocument62 paginiBiochimie Des Animaux Domestiques I Synthèse: Objet Du CoursJustin DrouetÎncă nu există evaluări
- Métabolisme Des Protéines Et Des Acides Aminés: Chapitre ChapitreDocument14 paginiMétabolisme Des Protéines Et Des Acides Aminés: Chapitre ChapitreZineb DahmaniÎncă nu există evaluări
- C1 ProteasomeDocument49 paginiC1 ProteasomeCristina Cevallos CampañaÎncă nu există evaluări
- Manuel de Spectrometrie de Masse A L Usage Des Biochimistes Avec CD Rom - SommaireDocument28 paginiManuel de Spectrometrie de Masse A L Usage Des Biochimistes Avec CD Rom - SommaireSAWADOGO ABDOUGANIÎncă nu există evaluări
- Compartimentation Cellulaire L1 23-24Document39 paginiCompartimentation Cellulaire L1 23-24kerradanaiskatiaÎncă nu există evaluări
- EndocytoseDocument15 paginiEndocytosek.aitaliÎncă nu există evaluări
- 1a Pathobiologie Cellulaire Chap 1 Intro-Muco 210223-Fusionné-CompresséDocument286 pagini1a Pathobiologie Cellulaire Chap 1 Intro-Muco 210223-Fusionné-CompresséjeannendangangÎncă nu există evaluări
- Cours ProtéineDocument111 paginiCours ProtéinesaliÎncă nu există evaluări
- Biologie Moléculaire Des Plantes - 8 NovembreDocument16 paginiBiologie Moléculaire Des Plantes - 8 Novembrezuzusmail12Încă nu există evaluări