Documente Academic
Documente Profesional
Documente Cultură
Tema-1 Reacciones Quimicas
Încărcat de
Claudio Adrían Carmona GarcíaDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Tema-1 Reacciones Quimicas
Încărcat de
Claudio Adrían Carmona GarcíaDrepturi de autor:
Formate disponibile
RAQUEL NAVARRO DELGADO
GRADO
REACCIN QUMICA: UNIDAD DIDCTICA 1
TEMA 1: FUNDAMENTOS
1.1.- Por qu estudiar Qumica: El reto de la Qumica en el nuevo siglo: 1.2.- Objeto de la Qumica. 1.3.Medida de la materia: Unidades SI. 1.4.- La incertidumbre en las medidas cientficas. Errores sistemticos y
accidentales. Diferencia entre precisin y exactitud.1.5.- Cifras significativas. La ecuacin qumica y las
relaciones de masa: 1.6.- Ecuaciones qumicas. 1.7.- Significado cuantitativo de las ecuaciones qumicas.
Como utilizar la estequiometria de una reaccin: 1.8.- Distintos tipos de clculos estequiomtricos. 1.9.Los lmites de una reaccin: Rendimiento de una reaccin. Reactivo limitante.
ESQUEMA/RESUMEN
1.1.- Por qu estudiar Qumica: El reto de la Qumica en el nuevo siglo:
Salud y medicina
La energa y el ambiente
Materiales y tecnologa
Alimentos y agricultura.
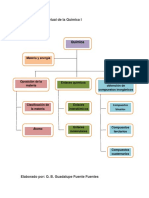
1.2.- Objeto de la Qumica:
Qu estudia la Qumica y cmo lo estudia?
Ramas de la Qumica.
1.3.- Medida de la materia: Unidades SI.
El sistema internacional de unidades (SI). Unidades bsicas.
Unidades derivadas.
Conversin de unidades.
Escalas de temperatura
1.4.- La incertidumbre en las medidas cientficas
Errores sistemticos y accidentales.
Diferencia entre precisin y exactitud.
1.5.- Cifras significativas.
LA ECUACIN QUMICA Y LAS RELACIONES DE MASA
1.6- Ecuaciones qumicas
Evidencia experimental de una reaccin qumica
o formacin de un precipitado
1
RAQUEL NAVARRO DELGADO
o de un gas
o cambio de color, etc.
Modo abreviado de expresar las reacciones qumicas: ecuaciones qumicas.
1.7.- Significado cuantitativo de las ecuaciones qumicas
Como ajustar las ecuaciones qumicas
COMO UTILIZAR LA ESTEQUIOMETRA DE UNA REACCIN
1.8.-. Distintos tipos de clculos estequiomtricos
Predicciones mol a mol.
Predicciones masa-masa
1.9.- Los lmites de una reaccin:
Rendimiento de una reaccin.
Reactivo limitante.
COMPETENCIAS:
Con este tema se intenta que el alumno adquiera la competencia de:
Enfrentarse a algunos de los problemas a los que la Qumica debe dar respuesta en este siglo, en
campos esenciales para el hombre.
Descubrir que el conocimiento en Qumica no se logra slo a partir de la experimentacin, sino
tambin formulando preguntas, planteando hiptesis y comprobando las mismas.
Discernir entre las distintas formas de expresar las medidas y clculos que realice.
Aprenda el significado de los coeficientes estequiomtricos presentes en una reaccin qumica, sea
capaz de ajustar reacciones y aplique con soltura los conceptos de mol, volumen molar, frmula
emprica, frmula molecular, etc. a la resolucin de distintos tipos de clculos estequiomtricos.
Aplique lo aprendido acerca de cifras significativas, clculo de errores, etc.
OBJETIVOS ESPECFICOS DE APRENDIZAJE:
1. Enumerar algunos de los problemas la Qumica debe intentar resolver en este siglo
2. Identificar cul es el objeto de estudio de la Qumica.
3. Explicar cundo la Qumica se eleva a la categora de Ciencia.
4. Saber expresar los resultados (unidades, cifras significativas, etc.)
5. Explicar el significado de los coeficientes estequiomtricos presentes en una reaccin qumica.
6. Ajustar una ecuacin qumica y especificar la informacin que de ella puede extraerse.
7. Realizar distintos tipos de clculos estequiomtricos para cualquier par de especies involucradas en una
reaccin qumica.
8. Calcular el volumen de disolucin necesario para llevar a cabo una reaccin, dadas la correspondiente
reaccin qumica igualada y la concentracin del reactivo.
2
RAQUEL NAVARRO DELGADO
9. Identificar el reactivo limitante de una reaccin y calcular la cantidad en exceso del reactivo sobrante, a
partir de la masa inicial de cada reactivo.
10. Calcular el rendimiento terico y porcentual de los productos de una reaccin, dada la masa de los
reactivos de partida.
11. Utilizar el reactivo limitante para calcular el rendimiento de un producto.
12. Determinar la composicin porcentual en masa de un compuesto.
13. Dada la composicin porcentual en masa de un compuesto, deducir su frmula emprica.
14. Determinar la frmula emprica de un compuesto orgnico a partir de un anlisis de combustin del
compuesto.
15. Describir los principales pasos que se deben seguir para hallar la frmula molecular de un compuesto.
16. Dada la composicin porcentual en masa de un compuesto y su masa molar aproximada, deducir su
frmula molecular.
17. Usar el nmero correcto de cifras significativas cuando se expresan mediciones y resultados de los
clculos.
TRMINOS Y CONCEPTOS SIGNIFICATIVOS DEFINIDOS EN ESTE TEMA
Cifras significativas.
Cantidad estequiomtrica
Ecuacin qumica
Estequiometria
Exactitud.
Masa.
Materia.
Modelos.
Precisin.
Reaccin ajustada
Reaccin qumica.
Rendimiento
Reactivo en exceso
Reactivo limitante
Sustancia.
DESARROLLO DEL TEMA
Probablemente esta no es la primera vez que decide estudiar Qumica, y por tanto ya te han dicho cul es el
objeto de esta Ciencia y conoce la tarea a que se enfrenta y el esfuerzo que exige. Por otra parte, si como es
lo ms comn y deseable ha cursado ya la asignatura de Principios bsicos de Qumica y Estructura
prcticamente el primer tema de sta disciplina ya lo ha estudiado. Slo tendr que repasarlo. No obstante se
incluye en esta disciplina porque:
Los conceptos que se manejan son bsicos para el estudio cuantitativo de los temas
dedicados a Reacciones Qumicas, y
Al no ser obligatorio, puede darse el caso de que algn alumno estudie esta asignatura sin
haber cursado previamente la anteriormente citada.
1.1.- Por qu estudiar Qumica: El reto de la Qumica en el nuevo siglo:
En estos tiempos de crisis todos somos conscientes de la importancia que tiene el conocimiento para la
economa mundial y el bienestar de la humanidad, y en este contexto, no conviene olvidar la aportacin de la
Ciencia en general, y de la Qumica en particular, al crecimiento sin precedentes de las ltimas dcadas.
3
RAQUEL NAVARRO DELGADO
Frente a la Qumica hay posiciones muy contrapuestas. Para unos es una Ciencia casi, casi perversa, quien
no ha escuchado decir: Este vino es malo, tiene mucha Qumica, o expresiones similares? (Por cierto, los
qumicos tambin cuidan de que los procesos de fermentacin de la uva se desarrollen del modo ms ptimo
posible). Para otros es inimaginable vivir sin ella, y para m que estos ltimos tienen razn. La Qumica no es
el problema, es la solucin. Eso mismo opina la American Chemical Society, cuyo esfuerzo para hacernos
llegar lo que sera nuestra vida cotidiana sin esta Ciencia lo ha plasmado en un corto video (duracin de
menos de 2 minutos) de lo que sera un da sin qumica. Por supuesto el video est editado en blanco y
negro, pues tenemos colores gracias a la qumica.
El video lo pueden encontrar en http://bytesizescience.com/index.cfm/2011/1/20/A-Day-Without-Chemistry.
Ya antes se haban editado videos similares, pero con la muestra de uno basta. El resto lo podemos poner
cada uno de nosotros con slo pensar un poco. S, la qumica est tan presente en cada faceta de nuestra
vida diaria que ha pasado a integrarse en nuestro entorno como habitual y a pasar desapercibida.
La ONU declar 2011 Ao Internacional de la Qumica, bajo el lema La Qumica: nuestra vida, nuestro
futuro. Esperemos que esta conmemoracin haya contribuido a que la humanidad haya adquirido una mejor
conciencia acerca de la importancia de la qumica en la sostenibilidad del planeta y en la mejora de nuestra
vida. Piense en su aportacin en campos tan diversos como la alimentacin, la salud, el medio ambiente, la
energa, los nuevos materiales, la cohesin social, el desarrollo econmico, etc., etc.
Cmo alimentar a la poblacin mundial, que crece con rapidez? La produccin agrcola depende no slo de
la riqueza del suelo y del riego, sino que hay que eliminar los insectos y las enfermedades que daan a los
cultivos, y la maleza que consume parte de los nutrientes necesarios para el cultivo. Hasta ahora, los
agricultores utilizan fundamentalmente fertilizantes y herbicidas, potentes sustancias qumicas que con
frecuencia han tenido efectos dainos. Para satisfacer las demandas alimenticias del siglo XXI, deben idearse
nuevas estrategias para la agricultura. Un camino ya iniciado y con xitos es la utilizacin de biotecnologa.
Por ejemplo, se sabe que un tipo de bacteria produce una molcula proteica que es txica para las orugas. Si
se incorpora en los cultivos el gen que codifica dicha toxina las plantas se protegen por s mismas, y que ya
no es necesario utilizar herbicidas.
Cmo olvidar la aportacin de los qumicos a la industria farmacutica? En el siglo XX se desarrollaron
potentes frmacos para tratar el cncer, el SIDA y muchas otras enfermedades, con pocos o nulos efectos
colaterales, as como para evitar el rechazo en trasplantes de rganos. Cmo no recordar las vacunas y
antibiticos que hacen posible prevenir la diseminacin de enfermedades microbianas? Ya a finales del siglo
pasado se inici la terapia gnica. Esta terapia promete ser la gran revolucin de la medicina en este siglo.
Tenga en cuenta que muchas enfermedades se producen por el deterioro de uno o ms genes implicados en
las defensas del cuerpo. En la terapia gnica, se introduce en la clula de un paciente un gen sano
seleccionado para curar o aliviar la enfermedad. Para llevar a cabo este procedimiento, los mdicos debes
tener un conocimiento suficientemente slido y profundo de las propiedades qumicas de los componentes
moleculares que estn implicados en el proceso de la enfermedad. A este conocimiento contribuyen los
investigadores qumicos
La contribucin de la Qumica al desarrollo de nuevos materiales ha permitido, por ejemplo, el acceso fcil,
rpido y econmico a nuevas tecnologas digitales como la banda ancha, Internet y los telfonos mviles.
Podramos extendernos mucho ms en este intento de mostrar todo lo que la Qumica puede y debe aportar
en este Siglo, pero basta con unas cuantas reflexiones. Aada usted, tras su reflexin otras muchas. Para
finalizar este epgrafe slo destacar que el ao 2011 estuvo tambin marcado por la conmemoracin del
centenario de la concesin del Premio Nobel de Qumica a Marie Curie, una oportunidad para reconocer la
contribucin de la mujer a la Ciencia en general (tambin era poseedora del Premio Nobel de Fsica) y
particularmente a la Qumica.
4
RAQUEL NAVARRO DELGADO
1.2.- Objeto de la Qumica:
En cualquier Ciencia hay siempre dos aspectos, que constituyen la base para establecer su identidad:
objeto y fines que se propone, y
modo en que puede cumplirlos y expresar su logro.
La Qumica es una de las disciplinas cientficas bsicas del mundo moderno, pero de qu trata? Quiz
podamos obtener algunas ideas acerca de su identidad actual si observamos que hacen los qumicos. En el
sentido ms amplio, los qumicos son gente que estudia la constitucin, propiedades y transformaciones de la
materia que constituye el universo, y que tienen como meta ltima el intentar explicar la gran profusin de
datos experimentales que obtienen, mediante una teora lo ms unitaria posible. Al estudiar la constitucin de
una sustancia, buscan no slo el conocimiento de su composicin, sino tambin la forma en que estn unidos
los diversos componentes, es decir, la estructura ntima de la materia. A continuacin, tratan de establecer
relaciones entre esa micro estructura y las dems propiedades fisicoqumicas. En ste aspecto concreto, la
Qumica de hoy, cada vez ms racional y deductiva, es una ciencia bastante distinta de la de siglos pasados,
de carcter completamente emprico.
El estudio de las reacciones qumicas ha conducido a los qumicos a cuestionarse dos vertientes de las
mismas.- por qu ocurren estas reacciones, y cmo ocurren. Esto les ha obligado a analizar aspectos tan
variados como la velocidad de las reacciones, los caminos por los que tienen lugar, sus efectos energticos,
las vas de sntesis de sustancias, etc. De aqu han surgido distintas especializaciones: Cinetoqumica,
Termoqumica, Metalurgia, Bioqumica, etc. Es de destacar que la obtencin de muchos de los nuevos
antibiticos, insecticidas, fertilizantes, nuevos plsticos y fibras sintticas, por citar slo algunos ejemplos, se
han basado, en gran parte, en conocimientos estructurales.
La explicacin racional de la Ciencia Qumica actual, que se ha desarrollado de modo vertiginoso en los
ltimos aos, implica una amplsima cobertura terica y una impresionante variedad de fenmenos. Si
intentamos explicarlo todo, corremos el grave peligro de convertirnos "en autmatas entrenados' como deca
Dainton, en pasivos receptores de una doctrina revelada, en vez de capacitarnos para resolver por nosotros
mismos nuevos problemas y aprender nuevas tcnicas, objetivos del proceso educativo, segn indicamos en
la introduccin. De ah que los programas actuales de la mayora de las disciplinas sean cada da ms
flexibles (existen experiencias de temarios estructurados en mdulos no rgidos y que eviten la sper
especializacin).
En esta disciplina abordaremos lo que yo llamara el corazn de la Qumica, como laten y se relacionan unas
sustancias con otras, y cules son las leyes que guan estas interacciones, las reacciones qumicas
1.3.- Medida de la materia: Unidades SI.
La Qumica es una Ciencia encuadrada dentro de las llamadas Ciencias experimentales con dos tipos
generales de propiedades igualmente importantes y complementarias: las propiedades cualitativas y las
cuantitativas. A poco que pensemos se nos ocurren montones de ejemplos. Aqu va uno de ellos: Un qumico
que investiga nuevos frmacos para una determinada enfermedad, no slo ha de buscar las propiedades
cualitativas que ha de tener la sustancia buscada para que sea efectiva, sino que ha de tener en cuenta
tambin la cantidad de sustancia, la dosis, que ha de administrar al enfermo para que sea segura, reduciendo
al mximo los posibles efectos adversos. Es por tanto importante fijar desde el principio como vamos a medir
la materia y que unidades vamos a utilizar.
A finales del siglo XVIII, durante la revolucin francesa, los cientficos convinieron en utilizar el sistema
mtrico de unidades, basado en mltiplos de 10, y por tanto bastante lgico y fcil de usar. Inclua lo que
hoy llamamos unidades bsicas: masa (el kilogramo), longitud (el metro), tiempo (el segundo) y temperatura y
fue adoptado en todo el mundo, excepto en los pases de habla inglesa. Con el tiempo se introdujeron nuevas
5
RAQUEL NAVARRO DELGADO
unidades para medir otros tipos de propiedades, como las propiedades elctricas, por ejemplo. Actualmente
los cientficos de todo el mundo, incluidos los de habla inglesa, comunican los resultados de sus
experimentos, independientemente del tipo de disciplina que cultiven, o del lugar del planeta en que se
encuentren, utilizando el Sistema Internacional de unidades (SI).
En la Tabla 1.1 se indican las unidades bsicas que utiliza el Sistema Internacional de Unidades. Todas las
dems unidades que podamos necesitar en la medida de cualquier otra propiedad se pueden obtener a partir
de estas unidades bsicas. Por ejemplo, la unidad derivada para expresar el volumen en el Sistema
Internacional es el m3 (m x m x m).
Tabla 1.1. Unidades bsicas del Sistema Internacional de Unidades (SI)
Propiedad
longitud
masa
tiempo
corriente elctrica
temperatura
cantidad de sustancia
intensidad luminosa
Nombre de la
unidad de medida
metro
kilogramo
segundo
amperio
kelvin
mol
candela
Smbolo
m
kg
s
A
K
mol
cd
El metro (m), utilizado como unidad de longitud, originalmente se estableci como la diezmillonsima parte
del cuadrante del meridiano terrestre, y hoy, con ms precisin, se define como la longitud del trayecto
recorrido en el vaco por la luz durante un tiempo de 1/299 792 458 de segundo
El kilogramo (kg), unidad de masa, equivalente a la de un cilindro de platino-iridio conservado en la Oficina
Internacional de Pesos y Medidas de Pars, y aproximadamente igual a la masa de 1000 centmetros cbicos
de agua a la temperatura de su mxima densidad, cuatro grados centgrados
El segundo (s) se emplea como unidad de tiempo y es equivalente a la sexagsima parte de un minuto de
tiempo. Se ha establecido como 9 192 631 770 perodos de la radiacin correspondiente a la transicin entre
los dos niveles hiperfinos del estado fundamental del tomo de cesio 133..
El amperio (A) es la unidad de intensidad de corriente elctrica del Sistema Internacional equivalente a la
intensidad de la corriente que, al circular por dos conductores paralelos, rectilneos, de longitud infinita, de
seccin circular despreciable y colocados a la distancia de un metro uno de otro en el vaco, origina entre
dichos conductores una fuerza de dos diezmillonsimas de newton por cada metro de conductor.
El Kelvin es la unidad de temperatura del Sistema Internacional. Es igual al grado centgrado, pero en la
escala de temperatura absoluta el 0 est fijado en -273,16C. Dicho de otro modo, es 1/273,16 de la
temperatura absoluta del punto triple del agua.
El mol (mol) , la unidad de cantidad qumica, es la cantidad de sustancia que contiene tantas entidades
elementales como tomos hay en exactamente 0.012 kg de carbono 12.
La candela (cd), que se utiliza como unidad de intensidad luminosa, es la sexagsima parte de la radiacin
emitida por un cuerpo negro a la temperatura de solidificacin del platino, por centmetro cuadrado.
Al igual que en el sistema mtrico, el Sistema Internacional de unidades dispone de una serie de prefijos,
relacionados con mltiplos, o submltiplos, de 10, a los que se les asigna un nombre especfico, y que
permiten expresar mas fcilmente los datos obtenidos. Los prefijos mas utilizados y su valor numrico se
6
RAQUEL NAVARRO DELGADO
recogen en la Tabla 1.2. Los nombres de las unidades a expresar se construyen a partir de la unidad bsica,
precedida por el prefijo que indica el mltiplo de 10 por el que ha de multiplicarse.
Submltiplos
Mltiplos
Tabla 1.2. Prefijos mas comnmente utilizados con las unidades SI
Prefijo
tera
giga
mega
kilo
hecto
deca
deci
centi
mili
micro
nano
pico
Smbolo
T
G
M
k
h
da
d
c
m
n
p
Factor
1.000.000.000.000 o 1012
1.000.000.000 o 109
1.000.000 o 106
1.000 o 103
100 o 102
10
1/10 o 10-1
1/100 o 10-2
1/1000 o 10-3
1/1.000.000 o 10-6
1/1.000.000.000 o 10-9
1/1.000.000.000.000 o 10-12
En resumen, la medida de una propiedad determinada de una muestra de una sustancia, por ejemplo, su
masa, conlleva el compararla con un patrn que tiene un valor conocido de la propiedad. En este caso el
kilogramo. La medida la expresamos como el producto de un nmero y una unidad. La unidad revela el patrn
con el que hemos comparado la cantidad medida. As, por ejemplo, cuando decimos que nuestra muestra
pesa 5 kg, queremos decir que la cantidad de sustancia que tenemos tiene una masa 5 veces superior a la
del patrn, que en este caso es el kg.
Como indicamos anteriormente las unidades bsicas del Sistema Internacional son las del Sistema mtrico, si
bien debe fijarse que de las tres escalas de temperatura que estn en uso actualmente, el SI ha escogido la
que expresa sus unidades en grados Kelvin (K). Para establecer una escala de temperatura es establecen
arbitrariamente dos puntos fijos, y se divide el intervalo entre ambos en un nmero de partes iguales a las que
se les denomina grado. Tanto la escala Fahrenheit, como la escala Celsius toman para esos dos puntos fijos
la temperatura a la que se funde el hielo, a la presin atmosfrica estndar, y la temperatura a la que el agua
hierve, a dicha presin atmosfrica estndar. La diferencia entre ambas est en que:
en la escala Fahrenheit, se definen los puntos de fusin y ebullicin normales del agua como
32F y 212F, respectivamente, y se divide el intervalo entre ambos en 180 partes iguales.
en la escala Celsius, los puntos de fusin y ebullicin normales del agua, se les asignan los
valores 0C, y 100C, respectivamente, y se divide el intervalo entre ambos en 100 partes iguales.
La escala Kelvin es una escala de temperaturas absoluta, ya que el cero de dicha escala no se basa en la
temperatura de fusin del agua, sino que se establece como cero la temperatura ms baja que puede
alcanzarse en teora (-273C). Tanto la escala Kelvin como la Celsius tienen unidades de la misma magnitud,
es decir, un grado Kelvin equivale a un grado Celsius. Consecuencia de ello es que los puntos de fusin y
ebullicin del agua, a la presin atmosfrica estndar, en la escala Kelvin sean iguales a 273 K, y 373 K,
respectivamente.
1.4.- La incertidumbre en las medidas cientficas
Es duro tener que afirmar que no podemos obtener el valor verdadero de una magnitud mediante la medida, y
es de suponer, por hiptesis, que dicho valor verdadero existe y es nico. Sin embargo, cualquier medida, con
7
RAQUEL NAVARRO DELGADO
independencia de su naturaleza, est ineludiblemente afectada por un error. Hay un conjunto de causas que
hacen que cada vez que intentamos medir una propiedad obtengamos un valor observado distinto.
Segn las fuentes de error podemos clasificar los errores en los siguientes tipos:
Errores de escala
Errores sistemticos
Errores accidentales, indeterminados o aleatorios
Imaginemos que tenemos un lquido cuyo volumen queremos conocer. Para ello lo vertemos en una probeta
como la que se muestra en la Figura 1.1. Si la probeta est graduada en divisiones de 1 mililitro podemos
deducir que el volumen se encuentra entre 14 y 15 mililitros. Algunos pensaran que la medida correcta sera
14,3; otros, quiz 14,4; etc. La ltima cifra es puramente especulativa, en ninguno de los casos podramos
afirmar que nuestra percepcin es la correcta, ya que la resolucin de la probeta utilizada es de 1mL.
Cualquier elemento o instrumento de medida tiene una resolucin dada, que es la diferencia mnima entre dos
valores contiguos de la magnitud medida, que el elemento o instrumento utilizado nos permite distinguir.
Esta limitacin de la resolucin da lugar a la aparicin de lo que llamamos
errores de escala, errores constantes y que afectan a todas las medidas
que hagamos con ese elemento o instrumento. Se valora en forma de error
absoluto como un medio de la unidad que corresponde a las divisiones
ms prximas de la escala de medida.
En nuestro ejemplo diremos que el error de escala sera 0,5 mL, y
expresaramos nuestra medida del volumen de lquido como 14,0 0.5 mL
Fig. 1.1.- Probeta graduada
Existen otra serie de errores sistemticos que afectan a las distintas
medidas de un modo constante y previsible, y que podemos evitar si
hacemos un anlisis cuidadoso del proceso de medida. Por ejemplo,
podemos cometer errores si utilizamos mtodos no apropiados.
Imaginemos que pesamos, sin tomar ninguna medida, una sustancia que es higroscpica, y que lo hacemos
en una balanza mal calibrada (error instrumental o de calibrado), y que para colmo derramamos una pequea
cantidad de sustancia sobre el plato de la balanza (error personal debido a la manipulacin de la muestra). En
resumen, existen diversas fuentes que generan errores sistemticos, y que siempre que sea posible
deberemos corregir. Cuando no sea posible los sumaremos al error de escala, y los trataremos como una
constante.
Adems de los anteriores existen una serie de errores accidentales, indeterminados o aleatorios que un
buen experimentador ha de tener en cuenta, y que son debidos a las fluctuaciones de las distintas variables
que influyen en el sistema., variables que no siempre son conocidas, y que son, por tanto, imprevisibles. Por
su carcter aleatorio estos errores se pueden tratar estadsticamente. Se pueden llevar a cabo varias
medidas y se promedian.
Diremos que una medida es tanto mas exacta cuanto menor sea la diferencia entre el valor verdadero y el
valor observado. Una medida ser tanto mas precisa cuanto menor sea su error relativo. La exactitud
expresa la correccin de una medida. La precisin muestra hasta que punto dicha medida es reproducible,
esto es, la proximidad de los resultados cuando la misma magnitud se mide varias veces. Como usted ya
podr deducir las medidas de precisin alta no siempre son exactas, ya que pueden venir afectadas por
errores altos. No obstante el experimentador siempre espera que sean ms exactas que las de precisin baja.
Aclaremos esto un poco ms. Supongamos que queremos conocer la masa de una muestra problema que
tenemos en el laboratorio. En dicho laboratorio disponemos de dos balanzas, una de ellas es un granatario
8
RAQUEL NAVARRO DELGADO
que tiene una resolucin de una dcima de gramo, y la otra una balanza analtica con una resolucin de una
milsima de gramo. Para promediar los errores llevamos a cabo tres medidas de la masa en cada una de las
balanzas. Los valores obtenidos son los siguientes:
Resolucin
1 Medida
2 Medida
3 Medida
Valor medio
Modo de expresar el resultado
Granatario
0.1g
7,7g
7,5g
7,6g
(21,18) / 3 = 7,6g
7,6 0,1g
Balanza analtica
0.001g
7,604
7,602
7,603
(22,809) / 3 = 7,603
7,603 0,001g
En el caso del granatario la precisin es baja. En el caso de la balanza analtica es mejor, podramos decir
que buena, aunque este es un trmino ambiguo ya que la bondad o no de una medida depende de la finalidad
de la misma.
1.5.- Cifras significativas.
Si analizamos los resultados obtenidos en el apartado anterior encontramos que en el caso del granatario, por
ejemplo, el primer dgito (7) se conoce con certeza, el segundo (6) puede variar debido a que fue estimado.
Podemos conocer la masa hasta la aproximacin de 0,1g. Por eso expresamos el resultado de la pesada
como 7,6 0,1g. Para un cientfico esto significa que el dato que maneja tiene dos cifras significativas. En
el caso de la balanza analtica (7,603 0,001g) el valor obtenido tiene 4 cifras significativas. El nmero de
cifras significativas nos da idea de la precisin de los datos que manejamos.
Quisiramos resaltar un hecho. Hemos indicado que los valores obtenidos tienen dos o cuatro cifras
significativas dependiendo de la balanza que hemos utilizado, y estas sern las cifras significativas que
tendrn dichos datos, aunque los expresemos de distintos modos, incluso aunque la medida la diramos con
mas de dos o cuatro cifras, respectivamente. Tomemos como ejemplo el resultado obtenido en la balanza
analtica (7,603 0,001g). Si en vez de expresar el resultado en gramos quisiramos darlo en kilogramos
pondramos: Masa= 0,007603 kg. De esta expresin de 7 dgitos slo 4 de ellos son significativos, los cuatro
ltimos. Dese cuenta que los ceros anteriores al nmero 7 no son significativos, mientras que si lo es el cero
contenido entre los nmeros 6 y 3.
Cmo saber cuando manejamos un dato el nmero de cifras significativas que tiene? Lo ms fcil es utilizar
la notacin exponencial. Supongamos que nos dicen que una muestra dada pesa 0,0056030g. Si expresamos
ese nmero en forma exponencial tendremos la expresin 5,6030 x 10-3g, en la que se deduce fcilmente
que el nmero de cifras significativas es 5. De este modo se concluye que los ceros anteriores al primer
nmero entero distinto de cero no son significativos. Si lo son, tanto los ceros comprendidos entre nmeros
distintos de cero, como los ceros del final. Por eso al dar el resultado de un experimento no es lo mismo poner
5,603 (4 cifras significativas, que indican que slo hemos podido medir con precisin de 4 cifras), que 5,6030
(cinco cifras significativas, que indican que hemos medido con una precisin de cinco cifras)
Es importante saber utilizar las cifras significativas en los clculos numricos que efectuemos. Un tema a
tener en cuenta es que la precisin no puede aumentar ni disminuir como resultado de los clculos en los que
intervienen las magnitudes medidas. As, por ejemplo, el resultado de una suma o resta de varios datos debe
expresarse con el mismo nmero de cifras decimales que la magnitud con menos cifras decimales. Por otra
parte, el resultado de una multiplicacin o de una divisin puede tener como mximo tantas cifras
significativas como la magnitud que se conoce con menor precisin en el clculo. De ah la necesidad de
redondear los resultados numricos. Lo ms correcto es operar con la totalidad de cifras de las que
dispongamos, y redondear el nmero que representa el resultado final dejando slo las cifras
9
RAQUEL NAVARRO DELGADO
significativas. La regla ms simple para el redondeo es aumentar el ltimo dgito significativo en una unidad
si el dgito siguiente es 5, 6, 7, 8 o 9, y dejar el ltimo dgito significativo sin cambiar, si el siguiente es 0, 1, 2,
3 4.
LA ECUACIN QUMICA Y LAS RELACIONES DE MASA:
1.6.- Ecuaciones qumicas.
Una reaccin qumica es un proceso mediante el que una sustancia qumica, o un conjunto de sustancias
iniciales, llamadas reactantes1, se transforman en otras nuevas, llamadas productos. Es decir, es un
proceso en el que tiene lugar una transformacin qumica. A veces esta transformacin es evidente porque
vara alguna propiedad fsica visible, se produce un cambio de color, la formacin de un precipitado, el
desprendimiento de un gas, la absorcin o emisin de calor, etc. Otras veces se necesita un anlisis qumico
detallado para comprobar que se han formado sustancias distintas a las originales. En cualquiera de los
casos, las reacciones qumicas se representan mediante ecuaciones qumicas, ecuaciones que nos permiten
expresar no slo de modo cualitativo la transformacin qumica que ha tenido lugar, sino tambin llegar a
establecer relaciones numricas cuantitativas entre los reactantes y los productos de la reaccin.
En resumen: La ecuacin qumica no es sino una expresin simblica abreviada que nos sirve para
representar a la correspondiente reaccin qumica. En esta representacin las frmulas de los reactantes se
escriben a la izquierda de la ecuacin, y las de los productos a la derecha. Ambos lados de la ecuacin se
conectan habitualmente mediante una flecha () () si se quiere indicar un estado de equilibrio, pocas
veces mediante el signo igual (=).
R (reactantes) P (productos)
1.7.- Significado cuantitativo de las ecuaciones qumicas.
El metanol puede obtenerse a partir del monxido de carbono (CO) y del hidrgeno (H2). Podemos describir
esta sntesis en palabras:
Monxido de carbono + hidrgeno metanol
O esquematizar la reaccin utilizando las frmulas qumicas de los reactantes y del producto:
CO + H2 CH3OH
Esta expresin que muestra lo esencial de lo que ocurre, las identidades de los reactantes y del producto
sintetizado, se conoce como ecuacin esquemtica, y es el resumen cualitativo de la reaccin que ha tenido
lugar. Sin embargo la ley de la conservacin de la materia nos indica que en una reaccin qumica
ordinaria los tomos ni se crean ni se destruyen, slo se reorganizan. Para cumplir con dicha ley habremos de
igualar el nmero total de tomos de cada elemento antes de reaccionar, y despus de haberlo hecho. Es
decir, adems de escribir las frmulas correctas de todas las especies qumicas que intervienen en la
reaccin, habremos de ponerles un nmero o coeficiente que indique cuantas especies de cada tipo
intervienen.
En nuestro caso, en la ecuacin esquemtica hay 2 hidrgenos ms a la derecha que a la izquierda. Para
equilibrar esta desigualdad nos bastar con poner un 2 delante del smbolo del hidrgeno molecular que
figura como reactante
CO + 2H2 CH3OH
A sta expresin resultante equilibrada se le conoce como ecuacin ajustada o mejor ecuacin
estequiomtrica (estequiometria, del griego stoicheon elemento y mtron medida). A los nmeros
antepuestos a las frmulas de las especies qumicas (al 2 antepuesto al smbolo del hidrgeno, en nuestro
1Se
denomina reactante a un reactivo que interviene en una reaccin qumica concreta. Se conoce como reactivo a cualquier
sustancia qumica disponible en un laboratorio
10
RAQUEL NAVARRO DELGADO
ejemplo) se les conocen como coeficientes estequiomtricos de las respectivas sustancias en esa reaccin
concreta. Cuando dicho coeficiente es igual a 1 no suele escribirse explcitamente.
Al ajustar una reaccin qumica nunca deben modificarse los subndices de las frmulas qumicas
representativas de las sustancias que intervienen, ya que esto implicara que actan especies qumicas
distintas a las que realmente lo hacen. Estaramos hablando de otra reaccin distinta. El ajuste ha de hacerse
modificando los coeficientes estequiomtricos de las distintas sustancias, hasta lograr equilibrar la reaccin
Existen distintos mtodos para ajustar las reacciones (algunos concretos, como los referentes a reacciones
de oxidacin-reduccin los veremos en su correspondiente tema), pero en muchos casos, el mtodo ms
sencillo surge de la pura inspeccin visual. En dicho caso le recomendamos una secuencia de puntos a
abordar, teniendo en cuenta que si en alguno de los dos miembros de la ecuacin qumica aparece algn
elemento libre, debe ser ste el ltimo en ajustarse:
1.- Ha de conocer todos los reactantes y productos que intervienen en la reaccin, as como sus respectivas
frmulas qumicas.
2.- Escriba la ecuacin esquemtica.
3.- Si en ambos lados de la ecuacin algn elemento aparece slo formando parte de un compuesto (distinto
en ambos lados, obviamente), debe ser el primero en ajustarse.
4.- Si intervienen tomos metlicos ajstense.
5.- Igualar los tomos no metlicos, exceptuando el hidrgeno y oxgeno. Proceda a continuacin a ajustar
hidrgeno y oxgeno, por ese orden.
6.- En el caso de que en alguno de los dos miembros de la ecuacin qumica aparezca algn elemento libre,
ajstelo.
7.- Compruebe que la ecuacin est ajustada. De no ser as, repita el procedimiento anterior sobre la
ecuacin obtenida en el primer intento, hasta conseguirlo.
El ajuste de ecuaciones no es difcil en general, pero a veces es suficientemente complejo como para requerir
haber adquirido una cierta destreza que se consigue con la prctica. Por ello le recomendamos que realice
ejercicios de ajuste de reacciones qumicas.
Muchas veces es importante reflejar en la ecuacin qumica otros tipos de informacin acerca de la reaccin
que est ocurriendo. Por ejemplo, el estado o forma fsica de los reactantes y productos, las condiciones de la
reaccin, etc.
El estado o forma fsica de los reactantes y productos se suelen indicar entre parntesis a la derecha de cada
una de las sustancias. Los smbolos habituales para indicarlos son: (s) slido; (l) lquido; (g) gas; (aq)
disolucin acuosa.
Las condiciones de la reaccin suelen indicarse encima o debajo de la flecha de la ecuacin.
As, en la sntesis del metanol deberamos poner:
;340 atms
CO(g) + 2H2 (g ) 350
C
CH 3OH (g )
ZnO ;Cr2O3
Con ello informamos de que:
la reaccin se lleva a cabo a 350C y bajo una presin de 340 atmsferas.
Intervienen como catalizadores el ZnO y Cr2O3.
En dichas condiciones todas las sustancias qumicas se encuentran en estado gaseoso.
Como un mol de cualquier sustancia contiene el mismo nmero de partculas unitarias (el nmero de
Avogadro), es equivalente hablar de relacin entre tomos o molculas que de relacin entre moles. Una
ecuacin ajustada nos permite, por tanto, realizar clculos de tipo cuantitativo. As, en nuestro ejemplo
11
RAQUEL NAVARRO DELGADO
podemos afirmar que la cantidad de sustancia equivalente a un mol de CO (28g), reaccionar con la cantidad
de hidrgeno molecular equivalente a 2 moles (4g), para producir 1 mol de metanol (32g).
COMO UTILIZAR LA ESTEQUIOMETRIA DE UNA REACCIN:
1.8.- Distintos tipos de clculos estequiomtricos.
La estequiometria permite realizar importantes aplicaciones prcticas, como, por ejemplo, predecir qu
cantidad de producto puede obtenerse en una reaccin, conociendo las cantidades de reactantes de las que
partimos.
Si en la reaccin indicada en el epgrafe anterior partiramos de 3 moles de H2, y quisiramos conocer
cuntos moles de metanol obtendramos, en abundancia del otro reactante, procederamos del modo
siguiente:
1.- Escribiramos la ecuacin estequiomtrica ( ajustada) de la reaccin qumica que tiene lugar:
;340 atms
CO(g) + 2H2 (g ) 350
C
CH 3OH (g )
ZnO ;Cr2O3
2.- Resumiramos la informacin que nos proporciona la ecuacin, escribiendo la relacin estequiomtrica
existente entre el reactante base del clculo (en nuestro caso el hidrgeno) y el producto de la reaccin:
2 moles de H2 1 mol de CH3OH
3.- Utilizariamos la anterior relacin estequiomtrica para determinar un factor de conversin que relaciona el
reactante dado, con el producto obtenido:
Pr oducto obtenido 1mol CH 3OH
, o lo que es lo mismo:
=
masa de reac tan te
2moles H 2
1mol CH 3OH
Cantidad de producto obtenido = (masa de reactante) x (
)
2moles H 2
1mol CH 3OH
Cantidad de CH3OH obtenido (en moles) = (3 moles de H2) x (
) = 1,5 moles de CH3OH
2moles H 2
En resumen: La ecuacin qumica equilibrada representativa de una reaccin qumica concreta, se utiliza para
determinar la relacin molar existente entre las distintas sustancias intervinientes, relaciones que permiten
calcular la cantidad de una sustancia a partir de la cantidad conocida de otra.
Estequiometria de reaccin
Moles de R
Relacin molar
Moles de P
A partir del concepto anterior de relacin molar pueden abordarse multitud de variantes de clculo:
Clculos masa-masa. Como hemos visto anteriormente la ecuacin qumica muestra las relaciones
existentes entre las cantidades (en moles) de cada reactante y producto. Teniendo en cuenta las
masas molares de cada sustancia pueden expresarse estas relaciones en trminos de masas
12
RAQUEL NAVARRO DELGADO
Clculos masa-volumen, ya que hay una proporcionalidad entre los moles de un gas y el volumen que
ocupan.
Clculos volumen-volumen: Relacin de los volmenes de los gases que intervienen en una reaccin,
que ser igual a su relacin molar, etc.
Veamos un ejemplo del primero de los tipos de clculo indicados, clculos masa-masa.
Supongamos que queremos conocer la masa de metanol obtenida a partir de 6 gramos de hidrgeno.
Para ello utilizaremos el diagrama indicado anteriormente, completado con un paso inicial y un paso final ms.
En primer lugar convertimos los gramos de reactante en moles de reactantes, posteriormente calculamos los
moles de producto obtenido teniendo en cuenta la relacin molar, y por ltimo convertimos los moles de
producto en masa de producto.
Estequiometria de reaccin
Masa
de R
nR=mR/MR
Moles de R
Relacin molar
Moles de P
mP = nPMP
Masa
de P
Teniendo en cuenta que las masas molares del H2 y del CH3OH son respectivamente iguales a 2 y 32,
tendremos:
6
gramos
de H2
Estequiometria de reaccin
nA=6/2=3
3moles de H2
1/2
(3/2)=1,5
moles de B
mB = 1,5x32
48g de
CH3OH
1.9.- Los lmites de una reaccin:
Hemos visto que es fcil calcular la cantidad de producto que podra obtenerse, partiendo de unas
determinadas cantidades de reactantes, apoyndonos en la ecuacin estequiomtrica de una reaccin, o a la
inversa, decidir que cantidad de producto necesitamos, y calcular las cantidades de reactantes que habremos
de poner. Hasta ahora, dichos clculos los hemos llevado a cabo suponiendo condiciones ideales, es decir:
que todos los reactivos tienen un 100% de pureza,
que reaccionan exactamente como se describe en la reaccin qumica, o dicho de otro modo, que no
se dan a la vez otra u otras reacciones secundarias en las que est tambin implicada alguna de las
sustancias de la reaccin propuesta.
Que las cantidades de todos los reactantes se encuentran en las proporciones estequiomtricas
indicadas en la ecuacin.
Que la reaccin se completa, es decir, que no llega a establecerse un estado de equilibrio, etc.
Sin embargo, en la mayora de las reacciones qumicas no se cumplen los supuestos anteriores. En principio,
la mayora son equilibrios qumicos, los reactivos que intervienen en ellas contienen impurezas, y alguno de
13
RAQUEL NAVARRO DELGADO
ellos, generalmente el ms barato, se encuentra en exceso. Por consiguiente, la cantidad real de producto
obtenido suele ser menor que la calculada a partir de la estequiometra de la reaccin. A la cantidad obtenida
suponiendo condiciones ideales se la conoce como cantidad terica.
1.9.a) Rendimiento de una reaccin.
Se conoce como rendimiento porcentual de una reaccin a la expresin:
Rendimiento porcentual= (cantidad real obtenida/cantidad terica)x100
y viene a dar idea de la eficacia de una determinada reaccin como mtodo de obtencin de un producto.
1.9.b). Reactivo limitante
Cuando en una reaccin qumica los reactantes no se encuentran en las cantidades determinadas por la
estequiometra de la reaccin, sino que alguno de ellos se encuentra en menor proporcin, los clculos han
de realizarse tomando como base dicho reactivo, al que se le denomina como reactivo limitante. El reactivo
limitante se utiliza completamente, de las cantidades relativas del resto de las sustancias queda parte sin
reaccionar.
Existen varios mtodos para establecer cul de los reactantes es el limitante. Uno de ellos es determinar cul
es el reactante que produce la menor cantidad de productos. Para ello:
1.- Calcule la cantidad de moles de cada reactante de la que disponemos.
2.- Seleccione uno cualquiera de los productos.
3.- Para cada reactante calcule cuantos moles del producto seleccionado pueden formarse.
El reactivo limitante ser aquel que produce la menor cantidad de producto.
Ejerctese en los diferentes tipos de clculos indicados anteriormente. Como ejemplos resuelva los ejercicios
de autocomprobacin que se proponen a continuacin.
Ejercicios de autocomprobacin
1.1.- De las siguientes unidades de medida, seale aquella que no sea una unidad bsica del Sistema
Internacional de Unidades:
a) la atmosfera
b) el grado Kelvin
c) el segundo
d) el metro
1.2.- Las cantidades que se expresan a continuacin son magnitudes determinadas experimentalmente:
A: (22,40 L); B: (0,00200 g); C: (6,022 x1023) y D: (0,452 km)
De las siguientes proposiciones seale la que considere correcta.
a) La cantidad B tiene 5 cifras significativas
b) Las cantidades B y D han sido expresadas con 3 cifras significativas.
c) Las cantidades A, C y D han sido expresadas con un n de cifras significativas igual a 4.
d) La cantidad que ha sido expresada con mayor nmero de cifras significativas es la C
1.3.- En una receta de cocina britnica leemos que el bizcocho que queremos hacer ha de ser horneado a
356F. Para seguir dicha receta al pie de la letra hemos de poner nuestro horno, que tiene la escala de
temperatura en grados Celsius, a:
a) 82C
b) 180C
c) 230C
d) 324C
1.4.-Una ecuacin qumica correspondiente a una reaccin qumica ordinaria, en la que slo intervienen
gases, se dice que est ajustada si:
a) El volumen de los productos es igual al volumen de los reaccionantes.
b) El nmero de moles de cada una de las sustancias que intervienen en la reaccin es un nmero entero.
14
RAQUEL NAVARRO DELGADO
c) El nmero total de tomos de cada elemento es el mismo en ambos miembros.
d) Se conserva la masa aunque no se conserve el nmero total de tomos de cada elemento.
1.5.- En la ecuacin: X HNO3 + P4 O10 4 HPO3 + 2N2O5 se ha indicado con una X el coeficiente
correspondiente al cido ntrico. Para que la reaccin est correctamente ajustada dicho coeficiente ha de ser
igual a:
a) 1
b) 2
c) 3
d) 4
1.6.- La combustin del propano se realiza segn la reaccin : C3H8 + 5O2 3CO2 + 4H2O
Cuntos gramos de CO2 se obtendrn si se hacen reaccionar 65 gramos de propano con 96 gramos de
oxgeno.?.
a) 195 g
b) 44 g
c) 79,2 g
d) Nada de lo dicho
Datos: Masas atmicas: C=12,0; H=1,0; O=16,0.
1.7.- El cloroformo. CHCl3, puede obtenerse segn la reaccin (sin ajustar):
CH4 + Cl2 HCl + CHCl3
Sabiendo que el rendimiento de la reaccin es del 75%, para obtener 100kg de cloroformo necesitaremos un
volumen de cloro, medido en condiciones normales, igual a:
a) 14,1 m3
b) 25,3 litros
c) 42,2 litros
d) 75,0 m3
Datos: Masas atmicas: C=12,0; H=1,01; Cl=35,5
Soluciones a los ejercicios de autocomprobacin
1.1.- Respuesta correcta a)
1.2.- Respuesta correcta b)
1.3.- Respuesta correcta b)
1.4.- Respuesta correcta c)
1.5.- Respuesta correcta d)
1.6.- Respuesta correcta c)
1.7.- Respuesta correcta d)
BIBLIOGRAFA BSICA
Este documento.
BIBLIOGRAFIA COMPLEMENTARIA
Atkins, Peter y Jones, Loretta: Principios de Qumica. Los caminos del descubrimiento; 5 ed.; Ed.
Mdica Panamericana, Buenos Aires (2012). Cap de Fundamentos, Introduccin y epgrafes H, L y M.
Petrucci, Ralph H; Herring, F.Geoffrey; Madura, J.D.; Bissonnete, C.: Qumica General 10 ed.; Pearson
Educacin, S.A., Madrid (2011). Caps 1, 4 y 5.
15
RAQUEL NAVARRO DELGADO
OTROS TEXTOS RECOMENDADOS
Atkins, Peter y Jones, Loretta: Qumica. Molculas, Materia, Cambio; 3 ed.; Ediciones Omega, S.A.,
Barcelona (1998). Caps. 2, 3 y 4.
Bailar, John C.; Moeller, Theral; Kleinberg, Jacob; Guss, Cyrus O.; Castellion, Mary E. y Metz, Clyde:
Qumica, Ed. Vicens-Vives, Barcelona (1983). Caps. 2 y 4
Brady, James E. y Holum, John R.: Fundamentals of Chemistry; 1 ed.; John Wiley and Sons, Inc., New
York (1981). Nota: Estos mismos autores han publicado tambin el texto Chemistry: The Study of
Matter and Its Changes; 2 ed.; de la misma editorial y publicado en 1995. Una 3 ed. de sta ltima
obra, en la que aparecen adems de los autores anteriores Russell, Joel, ha aparecido en el ao
2000. Cap. 3
Chang, Raymond: Qumica; 10 ed.; McGraw-Hill/ Interamericana Editores, S.A., Mxico (2010). Caps. 1
y3
Dickerson, Richard E.; Gray, Harry B. y Haight, Gilbert P.: Principios de Qumica; 3 ed.; Ed. Revert,
Barcelona (1983). Cap. 6
Ebbing, Darrell D.: Qumica General; 1 ed. en castellano, correspondiente a la 5 ed. inglesa; McGrawHill Interamericana, Mxico (1997).Caps. 1, 2 y 4.
Kneen, W.R.; Rogers, M.J.W. and Simpson, P.: Chemistry. Facts, patterns, and principles; 1 ed.;
Addison-Wesley, London (1972). Introduccin
Keenan,Charles W.; Kleinfelter,Donald C.; Wood,Jesse H.: General College Chemistry; 6 ed.; New York
(1980). Caps. 1 y 2.
McQuarrie, Donald A. y Rock, Peter A.: General Chemistry; 3rd ed.; W. H. Freeman and Company, New
York (1991). Caps. 1 y 5.
Moore, John W; Staniski, Conrad L.; Wood, James L.; Kotz, John C. y Joesten, Melvin D.: El mundo de la
Qumica. Conceptos y aplicaciones.2 ed. Addison Wesley Longman, Mxico (2000). Caps. 1, 2, 3 y
5.
Nebergall, William H.;. Holtzclaw, Henry F Jr. and Robinson William R.. "General Chemistry". D.C. Heath
and Co. Lexington, Mass. (1980). Caps. 2 y 3
Oxtoby, David W.; Gillis, H.P. and Nachtrieb, Norman H. Principles of Modern Chemistry; 4 ed.;
Saunders College Publishing, New York (1999). Caps. 1 y 2.
Robinson, William R.; Odom, Jerome D. and Holtzclaw, Henry F.,Jr. : General Chemistry; 10th ed.;
Houghton Mifflin Company, Boston (1997). Caps. 1 y 3.
Rosenberg, Jerome L.; Epstein, Lawrence M.: Qumica General; 7 ed.; McGraw-Hill, Madrid (1990).
Caps. 3 y 4.
Whitten,Kenneth W; Davis,Raymond E.and Peck,M.Larry:Qumica General, 3 ed. en castellano,
correspondiente a la 5 ed. inglesa, McGraw-Hill , Madrid (1998). Caps. 1, 2 y 3.
Pimentel, George C. y Spratley, Richard D.: Understanding Chemistry; 1 ed., Holden-Day, San
Francisco (1971). Cap. 1
Pilar Frank L: "Chemistry. The Universal Science". Addisson-Wesley, Reading, Mass. (1979). Cap.1
16
RAQUEL NAVARRO DELGADO
Gillispie, C. C.(editor): Dictionary of Scientific Biography, Charles Scribners Sons, New York (1981).
Vols 1-16.
Brock, W.H.: Historia de la Qumica, Alianza Editorial (Coleccin Ciencia y Tecnologa), Madrid (1998).
Lpez Cancio, Jos A.: Problemas de Qumica. Cuestiones y ejercicios, Prentice Hall, Madrid (2000).
Cap. 2.
Ruiz, Antonio; Pozas, Antonio; Lpez, Juan; Gonzlez, Beatriz: Qumica General; McGraw-Hill, Madrid
(1994). Cap. 4.
Bermejo, Francisco; Paz, Manuel; Bermejo, Adela; Paz, Isabel: 1000 Problemas resueltos de Qumica
General y sus fundamentos tericos, Ed. Paraninfo, Madrid (1996). Cap. VI.
Sienko, Michael J.: Problemas de Qumica, Ed. Revert, Barcelona (1976). Caps 2 a 5
L.K.Nask: "Stoichiometry",.Addison-Wesley (1966)
S.W.Benson: "Chemical Calculations"; 3 ed; Wiley,Nueva York.(1971)
ALGUNAS LECTURAS ATRAYENTES PARA LOS ALUMNOS
El mtodo cientfico en accin: poliagua. Petrucci, Ralph H; Harwood, William S y Herring,
F.Geoffrey.: Qumica General 8 ed.; Pearson Educacin, S.A., Madrid (2007), pg. 22.
Unidades y tomos en la trampa. Atkins, Peter y Jones, Loretta: Qumica. Molculas, Materia,
Cambio; 3 ed.; Ediciones Omega, S.A., Barcelona (1998), pg. 44.
Gases que provocan el efecto invernadero. Atkins, Peter y Jones, Loretta: Qumica. Molculas,
Materia, Cambio; 3 ed.; Ediciones Omega, S.A., Barcelona (1998), pg. 138.
La qumica industrial. Petrucci, Ralph H; Harwood, William S y Herring, F.Geoffrey.: Qumica
General 8 ed.; Pearson Educacin, S.A., Madrid (2007), pg. 128
LECTURAS ADICIONALES EN REVISTAS
"Creativity, Discovery and Science". R.A. Brown. J. Chem. Educ. 54, 720 (1977).
"Chemistry and Science": The Next Hundred Years". A.L. Hammond. Science, 185, 347 (1974).
"Prematurity and Uniqueness in Scientific Discovery". G.S. Stent. Scientific American. Dic. (1972).
"Physical versus Chemical Change". W.J. Gensler. J. Chem. Educ. 47, 154 (1970).
"Differentiating Physical and Chemical Changes". L.E. Strong. J. Chem. Educ. 47, 689 (1970).
"How can an instructor best introduce the topic of significant figures to students unfamiliar with
the concept?". R.A.Pacer. J.Chem.Educ. 77, 1435 (2000)
Precision and accuracy in measurements. A tale of four graduated cylinders. R.S.Treptow.
J.Chem. Educ. 75, 992 (1998)
"Basic principles of scale reading". G.D.Peckham. J.Chem. Educ. 71, 423 (1994)
17
S-ar putea să vă placă și
- Guia Quimica II Nuevo ModeloDocument19 paginiGuia Quimica II Nuevo ModeloPaola Denise RiquelmeÎncă nu există evaluări
- Qué es la químicaDocument6 paginiQué es la químicaLucy Nila Capani JuradoÎncă nu există evaluări
- Solucionario Tema 7 PDFDocument32 paginiSolucionario Tema 7 PDFmsa44100% (1)
- Bloque IDocument23 paginiBloque IGarcia Nuñez Jaime EmanuelÎncă nu există evaluări
- Módulo V Clase 4 NaturalesDocument21 paginiMódulo V Clase 4 NaturalesHernán EspíndolaÎncă nu există evaluări
- Modulo de Quimica PDFDocument128 paginiModulo de Quimica PDFIvan Cisneros100% (1)
- Cuál Es La Importancia de La QuímicaDocument4 paginiCuál Es La Importancia de La Químicaanabel castro maldonadoÎncă nu există evaluări
- ACTIVIDADES DE APRENDIZAJE B. 1 Cobach P1Document7 paginiACTIVIDADES DE APRENDIZAJE B. 1 Cobach P1Jesus AngelÎncă nu există evaluări
- Cuál Es La Importancia de La QuímicaDocument4 paginiCuál Es La Importancia de La Químicaanabel castro maldonadoÎncă nu există evaluări
- Copia de Diseño Instruccional - QUIMICA - IDocument58 paginiCopia de Diseño Instruccional - QUIMICA - IOrlando Zamora PeinadoÎncă nu există evaluări
- Cuál Es La Importancia de La QuimicaDocument2 paginiCuál Es La Importancia de La QuimicaEiraÎncă nu există evaluări
- Taller Reconoce La Química Como Una Herramienta para La Vida 2018Document14 paginiTaller Reconoce La Química Como Una Herramienta para La Vida 2018Sofia CastilloÎncă nu există evaluări
- Ramas de la quimicaDocument3 paginiRamas de la quimicaFundacion ProgresarÎncă nu există evaluări
- Guia 1 Tco Cocina Ciencias Naturales QuimicaDocument23 paginiGuia 1 Tco Cocina Ciencias Naturales QuimicaDaniela DuqueÎncă nu există evaluări
- Syllabus FisicoquimicaDocument83 paginiSyllabus FisicoquimicaJacky LeónÎncă nu există evaluări
- Temario Quimica 2 Bachillerato ValenciaDocument11 paginiTemario Quimica 2 Bachillerato ValenciaMerche García SáezÎncă nu există evaluări
- Módulo QuímicaDocument61 paginiMódulo QuímicaRoberto AbedÎncă nu există evaluări
- Proyecto Quimica.Document15 paginiProyecto Quimica.Alejandro BravoÎncă nu există evaluări
- Modulo QuimicaDocument61 paginiModulo QuimicaRoberto AbedÎncă nu există evaluări
- Proyecto Científico 2 Quimica 1ro Ing. Jose QuingaDocument8 paginiProyecto Científico 2 Quimica 1ro Ing. Jose QuingaYomira MurilloÎncă nu există evaluări
- Apunte PIT QUIMICA CuatrimestralDocument50 paginiApunte PIT QUIMICA CuatrimestralMarcos Pozo SchwindtÎncă nu există evaluări
- Compendio de Talleres y Conferencias PDFDocument179 paginiCompendio de Talleres y Conferencias PDFNicolas Gómez Martínez0% (1)
- QuimicaClinica FARIASDocument680 paginiQuimicaClinica FARIASMedicina Nos traumoÎncă nu există evaluări
- Clase 1quimica Concepto y AplicacionesDocument4 paginiClase 1quimica Concepto y AplicacionesEliana RamosÎncă nu există evaluări
- Balance de Materia y Energia Hernan AlvarezDocument3 paginiBalance de Materia y Energia Hernan AlvarezjuanÎncă nu există evaluări
- ACTIVIDADES DE APRENDIZAJE B. 1 QUIMICADocument6 paginiACTIVIDADES DE APRENDIZAJE B. 1 QUIMICAJesus AngelÎncă nu există evaluări
- Bioquímica general UNAL-AL: SilaboDocument7 paginiBioquímica general UNAL-AL: SilaboJaime Alberto Mori CastroÎncă nu există evaluări
- programa-fisico-quimica-aplicada-2016Document4 paginiprograma-fisico-quimica-aplicada-2016EsteffÎncă nu există evaluări
- 2024 ICA Modulo Qca MVDocument37 pagini2024 ICA Modulo Qca MVrenemartinbaez2006Încă nu există evaluări
- Qui U1 A1 SaarDocument4 paginiQui U1 A1 SaarSarahi Alvarez100% (1)
- Guia 1 Pablo Ramella 3ero 2023Document9 paginiGuia 1 Pablo Ramella 3ero 2023yanina CastroÎncă nu există evaluări
- NQUI U1 ContenidoDocument50 paginiNQUI U1 ContenidoCarolina RubioÎncă nu există evaluări
- QM 10° Unidad de AutoaprendizajeDocument22 paginiQM 10° Unidad de AutoaprendizajeOliver Aparicio RiveraÎncă nu există evaluări
- Sec. Did. Ev.1 Qi-2023 CorregidaDocument40 paginiSec. Did. Ev.1 Qi-2023 CorregidaEmanuel RubioÎncă nu există evaluări
- Reaccion Quimica en La Industria 11 B CidmiDocument12 paginiReaccion Quimica en La Industria 11 B Cidmialaihernandez30Încă nu există evaluări
- Carta Descriptiva Bioquimica 2015 20128 Quimica y FarmaciaDocument25 paginiCarta Descriptiva Bioquimica 2015 20128 Quimica y FarmaciaMaria Angelica SaltarinÎncă nu există evaluări
- Quimica y Vida Cotidiana - EnsayoDocument3 paginiQuimica y Vida Cotidiana - EnsayoMartin MendietaÎncă nu există evaluări
- Papel Del Método Científico en La Solución de Problemas QuímicosDocument13 paginiPapel Del Método Científico en La Solución de Problemas QuímicosPeter CacheÎncă nu există evaluări
- Plan de Clases AgroquímicosDocument11 paginiPlan de Clases AgroquímicosMatias Emiliano BassoÎncă nu există evaluări
- Tarea JhonDocument2 paginiTarea Jhonkaterine CaroÎncă nu există evaluări
- Segunda ActividadDocument3 paginiSegunda ActividadMagaña Ruiz Juanita AimeÎncă nu există evaluări
- Materia y Energia Unidad I Química IDocument36 paginiMateria y Energia Unidad I Química IJose Antonio MartinezÎncă nu există evaluări
- RamasQuímicaDocument3 paginiRamasQuímicaCristhian Junior López ChanaméÎncă nu există evaluări
- Universidad Autónoma Del Carmen: Escuela Preparatoria DiurnaDocument41 paginiUniversidad Autónoma Del Carmen: Escuela Preparatoria DiurnasasaÎncă nu există evaluări
- Sintesis y La Importancia de La QuimicaDocument4 paginiSintesis y La Importancia de La QuimicaMARIA FERNANDA SAENZ DE VITERI SANTOSÎncă nu există evaluări
- Importancia de La Química en La ActualidadDocument4 paginiImportancia de La Química en La ActualidadAngel H Abasolo100% (1)
- 10 Química Actividad 1Document3 pagini10 Química Actividad 1Arantza TrujilloÎncă nu există evaluări
- Quimica CR 2017-2Document3 paginiQuimica CR 2017-2Jimmy Anderson Huaman LlanosÎncă nu există evaluări
- Planificacion QuimicaDocument7 paginiPlanificacion Quimicacorina rodad ricoÎncă nu există evaluări
- Química - Bloque 1Document7 paginiQuímica - Bloque 1Agustín AltamiraÎncă nu există evaluări
- Guia de Reforzamiento, 10º 2021Document10 paginiGuia de Reforzamiento, 10º 2021Isaias CaicedoÎncă nu există evaluări
- Quimica IntegralDocument4 paginiQuimica IntegralGustavo Adolfo Taborda OsorioÎncă nu există evaluări
- Manual Bioquimica Clinica - Corregido Julio 2013Document61 paginiManual Bioquimica Clinica - Corregido Julio 2013Lidia Carolina Rivera TapiaÎncă nu există evaluări
- Química Ingreso 2023Document163 paginiQuímica Ingreso 2023Josefina AresÎncă nu există evaluări
- Formato Cuadernillo Campeche QUÍMICAII 2021Document113 paginiFormato Cuadernillo Campeche QUÍMICAII 2021Javier Caballero100% (1)
- Introdución A La QuímicaDocument15 paginiIntrodución A La QuímicaAngela FerminÎncă nu există evaluări
- FISICOQUIMICADocument94 paginiFISICOQUIMICAJavier IngarÎncă nu există evaluări
- La Vida Útil de los Alimentos y sus Principales Reacciones: ¿Qué pasa en los alimentos con el tiempo?De la EverandLa Vida Útil de los Alimentos y sus Principales Reacciones: ¿Qué pasa en los alimentos con el tiempo?Evaluare: 2 din 5 stele2/5 (1)
- Comentario Del Libro Ingenieros y Las Torres de MarfilDocument2 paginiComentario Del Libro Ingenieros y Las Torres de Marfilmijaelc15Încă nu există evaluări
- Proc Compresor de AireDocument16 paginiProc Compresor de AireEsteban MoralesÎncă nu există evaluări
- Programación Orientada A ObjetosDocument137 paginiProgramación Orientada A ObjetospolouserÎncă nu există evaluări
- Planificacion La FotografiaDocument5 paginiPlanificacion La FotografiaAndres RugelÎncă nu există evaluări
- 01 - Todos Somos BuscadoresDocument22 pagini01 - Todos Somos Buscadorescaminodeidentidad100% (1)
- Auditoría inalámbrica-Recomendaciones para reducir riesgosDocument3 paginiAuditoría inalámbrica-Recomendaciones para reducir riesgosf_ibarraÎncă nu există evaluări
- Glenium 1303 - Ficha TécnicaDocument2 paginiGlenium 1303 - Ficha Técnicavidalarcos2Încă nu există evaluări
- Valdivia Altez YhersonDocument2 paginiValdivia Altez YhersonAndy ChavezÎncă nu există evaluări
- Choques elásticos e inelásticosDocument3 paginiChoques elásticos e inelásticosYoshiAngelGonzalezMontenegroÎncă nu există evaluări
- Creación de tablas en Access - Ejercicios prácticosDocument2 paginiCreación de tablas en Access - Ejercicios prácticosAnita Mejía Chi Ham100% (1)
- Campo Magnético de Un SolenoideDocument5 paginiCampo Magnético de Un SolenoideAlejandro AtenciaÎncă nu există evaluări
- 07 - 12 FICHA DE TRABAJO PERSONAL (Autoguardado)Document4 pagini07 - 12 FICHA DE TRABAJO PERSONAL (Autoguardado)Evelin Florcia Villalba HuayreÎncă nu există evaluări
- NullDocument4 paginiNullSaul VegaÎncă nu există evaluări
- Negociar Es Fácil, Si Se Sabe ComoDocument8 paginiNegociar Es Fácil, Si Se Sabe ComoCesar Murga0% (1)
- MUR Formato Nro 1 Inspeccion Antes de Lavado 777FGDocument3 paginiMUR Formato Nro 1 Inspeccion Antes de Lavado 777FGJuan MedranoÎncă nu există evaluări
- Acciones Preventivas y CorrecivasDocument1 paginăAcciones Preventivas y Correcivasedwar mauricio suarez quinteroÎncă nu există evaluări
- Fundamentos RFID PresentacionDocument27 paginiFundamentos RFID PresentacionSergio E. Hernandez R.100% (1)
- Apuntes Psicometria 1Document90 paginiApuntes Psicometria 1Mary V LanderosÎncă nu există evaluări
- Ejercicios de VigasDocument22 paginiEjercicios de VigasNohely VillavicencioÎncă nu există evaluări
- Energía histórica: Fuentes y conversiónDocument4 paginiEnergía histórica: Fuentes y conversiónPamela BellendirÎncă nu există evaluări
- Gases medicinales e instalacionesDocument18 paginiGases medicinales e instalacionesIvonn OchoaÎncă nu există evaluări
- Recommended Cementation For Monolithic Zirconia CrownsDocument4 paginiRecommended Cementation For Monolithic Zirconia CrownsEduardo MondragonÎncă nu există evaluări
- Teoría de La Imagen: Unidad 1 Tema 2Document52 paginiTeoría de La Imagen: Unidad 1 Tema 2Mendez ErikaÎncă nu există evaluări
- Elementos de Una Cristología en Lenguaje SecularDocument18 paginiElementos de Una Cristología en Lenguaje SecularJoaquin Platero RyūÎncă nu există evaluări
- Metabolismo GeneralidadesDocument77 paginiMetabolismo GeneralidadesNestorArturoUchuyaCulquiÎncă nu există evaluări
- Infografía Proceso de BúsquedaDocument6 paginiInfografía Proceso de Búsquedanacho gonzalezÎncă nu există evaluări
- Planificación gubernamental corto y mediano plazoDocument62 paginiPlanificación gubernamental corto y mediano plazoSuzet Jaillita QuiñonesÎncă nu există evaluări
- Electrocentro S.A. UU - nn-hCODocument53 paginiElectrocentro S.A. UU - nn-hCOMiguel SotoÎncă nu există evaluări
- Estrategia océano azul StarbucksDocument7 paginiEstrategia océano azul StarbucksmaxÎncă nu există evaluări