Documente Academic
Documente Profesional
Documente Cultură
INFORME-2 Analisis Cualitativo
Încărcat de
Pedro Santiago Salcedo GutierrezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
INFORME-2 Analisis Cualitativo
Încărcat de
Pedro Santiago Salcedo GutierrezDrepturi de autor:
Formate disponibile
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
1. OBJETIVOS
El objetivo del presente informe hace puntuacin sobre el proceso
conocido como Marcha de Cationes. A travs del mismo, una
solucin puede arrojar los elementos que contiene, pudiendo lograr de
esta manera alcanzar el conocimiento sobre algo hasta el momento
no detectado.
Si bien existen otras tcnicas usadas para conocer el contenido en
elementos de una disolucin tomada de una muestra desconocida,
adems de que estos dictan en detalle la cantidad de elementos
encontrados y su proporcin en la muesta, los mismos son muy
costosos en tiempo y dinero lo cual hace del procedimiento Marcha
de Cationes una solucin adoptada en la gran mayora de los casos,
dnde lo que se necesita encontrar son simplemente qu elementos
se encuentran presentes en una muestra desconocida, y no es
necesario conocer la cantidad de cada uno presente en el mismo.
Determinar analticamente los
identificndolos en cada proceso.
cationes
de
los
grupos
2. FUNDAMENTO TERICO
El Anlisis Cualitativo tiene por objeto el reconocimiento o identificacin de
los elementos o de los grupos qumicos presentes en una muestra. Por
tanto, esta parte de la Qumica Analtica estudia los medios para poder
llevar a cabo las mencionadas identificaciones. La base en la que se
fundamentan la mayora de los procesos analticos cualitativos son las
reacciones qumicas , si bien, hay que mencionar que los mtodos
instrumentales, basados en principios fsicos o fisicoqumicos, han
colaborado, a veces de forma decisiva, a la resolucin de un gran nmero
de problemas de anlisis cualitativo. En este sentido, se tratarn
nicamente algunos aspectos del anlisis cualitativo clsico, reservando las
aplicaciones de los mtodos instrumentales para cuando el alumno estudie
con cierta profundidad los citados mtodos.
MARCHA DE CATIONES
La marcha de cationes (tambin conocida como marcha analtica o marcha
de Bunsen, se resume como un proceso tcnico y sistemtico para la
identificacin de iones orgnicos en una disolucin a travs de la formacin
Pgina
1
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
de complejos o sales de color nico y caracterstico. Este proceso en sntesis
consiste en tomar la muestra y hacerla reaccionar agregando cationes o
aniones, y observando el color resultante luego de la reaccin.
Debido a este color se pueden dividir los posibles resultados en grupos e ir
continuando hasta llegar al objetivo deseado. Hasta cierto punto esto se ha
logrado tabular manualmente, pero existen situaciones en las cuales se
requiere continuar con un anlisis ms complejo para poder lograr separar
la totalidad de elementos que componen la muestra con el fin de
determinarlos.
De acuerdo a esto, existen cinco Reactivos de Grupo, a saber:
3. PARTE EXPERIMENTAL
3.1.
EXPERIMENTO N 1:
a) OBSERVACIONES
Al agregar suficiente
HCl(ac )
6M a la muestra se observa la
formacin de un precipitado blanco en la base del tubo de
ensayo
Al centrifugar y decantar la muestra anterior obtenemos una
H 2 O2
solucin transparente. Al agregar
a la solucin
resultante se torna violeta al 5%.
Pgina
2
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
La muestra anterior se torna anaranjado oscuro luego de
N H4I
calentar a bao maria , al agregarle 1 gota de
y luego
de evaporarla casi a seco notamos un color verde oscuro, al
HCl(ac)
aadirle 15 gotas de
y 12 gotas de tiocetamida a la
solucin anterior, esta se torna mostaza no traslucido, al
comprobar el PH de la solucin podemos ver el papel. De
color
verde
pizarra,
para
finalizar
esta
parte
del
experimento,centrifugamos, decantamos y veremos que el
precipitado es de color negro.
Al aadir agua de bromo a la solucin anterior no muestra
N H 4 Cl
cambio aparente. Al agregar cristales de
, estos se
disuelven pero al agregar una considerable cantidad obtenemos
una solucin saturada
Al aadir N H 4 OH
a la solucin saturada se observ la
formacin de un precipitado color verde muy oscuro
De la etapa anterior, despus de centrifugacin se obtiene la
sedimentacin de un precipitado color marron claro.
Al calentar esta solucin con precipitado, el precipitado cambia
de color de marrn claro a negro.
Al agregar el HNO3 la solucin se torna blanquecina, pero al
calentarla se torna de color amarillo.
Al adicionar las 10 gotas de H2O con las 10 gotas de NH4Cl a
solucin se torna incolora.
Finalmente al agregar las 5 gotas de NH4OH la solucin sigue
siendo incolora
b) ECUACIONES QUIMICAS
CATIONES DEL
PRIMER
GRUPO
Pgina
3
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
Cl(ac)
+
H (ac) +
HCl(ac )
Cl
(ac) AgCl(s) blanco
Ag+
(ac)+
2Cl (ac) Pb Cl2(s) blanco
2+
Pb(ac) +
Cl(ac) Hg2 Cl2(s) blanco
2+
Hg(ac) +2
H (ac)
2
S (ac ) +2
H 2 S+ HO 2
2
S (ac) HgS (s) negro
2+
Hg (ac) +
Pgina
4
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
S (ac) PbS(s) negro
2+
Pb(ac) +
S 2
(ac) CuS (s) negro
Cu2+
(ac) +
S 2
(ac) CdS (s) amarillo
2+
Cd(ac)
+
S (ac) Bi2 S 3(s) marron
3+
2 Bi(ac) +3
S 2
(ac) Sn S 2(s)
Sn(4+
ac ) + 2
CATIONES DEL
SEGUNDO
GRUPO
S (ac) As2 S 3(s )
3+
2 As(ac) +3
S (ac) Sb2 S 3(s )
3+
2 Sb(ac) +3
3 OH (ac) Fe (OH )3(s ) naranjamarron
3+
Fe(ac) +
CATIONES DEL
TERCER GRUPO
(HIDROXIDOS)
Pgina
5
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
2OH (ac) Mn (OH )2(s ) blanco o caf
2+
Mn(ac )+
3 OH (ac) Al (OH )3(s) incoloro o blanco
3+
Al(ac) +
3 OH
(ac) Cr (OH )3(s) verde
Cr3(ac+)+
Solucin: Ni(NH3)62+, Co(NH3)62+, Zn(NH3)62+, cationes del grupo IV y V
2+
( N H 3)6 (ac)
2+
(ac) +6 N H 3(ac)=
Co(N H 3 )2+
6 (ac)
2+
Co(ac) +6 N H 3(ac)=
Zn( N H 3 )26 +(ac)
+
Zn2(ac)
+ 6 N H 3(ac) =
Al agregar a la solucin CH3CSNH2 y proporcionarle calor, obtenemos:
Disociacin:
+
+ H (ac)
H 2 S( ac )+ H 2 O=H S(ac)
Pgina
6
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
+
2+ H (ac )
+ H 2 O=S(ac)
H S(ac
)
Reaccion Total
+
2+2 H(ac)
H 2 S( ac )=S(ac)
CATIONES DEL
TERCER GRUPO
(SULFUROS)
Entonces
2=NiS(s) +6 N H 3(ac)
( N H 3 )2+
6 (ac)+ S(ac)
2=cos(s )+ 6 N H 3(ac)
Co( N H 3)2+
6 (ac) +S (ac)
2=ZnS(s) +6 N H 3(ac)
Zn( N H 3 )36+(ac) + S(ac)
Solucin: Ba(NO3)2(S) , Sr(NO3)2(S) , Ca(NO3)2(S) (precipitados que se
obtienen de la vaporizacin con el HNO3(AC)) y cationes V
Con NH4Cl(AC) :
2++2 N O3(ac )
Ba(N O3 )2( s )+ H 2 O=B a(ac)
2++2 N O3 (ac)
Sr (N O3 )2 (s )+ H 2 O=Sr(ac)
Pgina
7
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
2+ +2 N O3 (ac)
Ca( N O 3 )2 (s )+H 2 O=C a(ac)
Disociacin del NH4Cl
++Cl (ac )
NH 4 Cl (ac )=NH 4 (ac)
+
+=N H 4 OH + H (ac )
NH 4 ( ac )
2
+ +C O3(ac )
( N H 4 ) C O3(ac )=NH 4 (ac )
Finalmente obtenemos:
2=BaCO 3 ( ac )
2+ +C O3 (ac )
Ba(ac )
2=SrC O 3 (ac )
2+ +C O 3 (ac )
Sr (ac )
2=CaC O3 (ac )
2+ +C O3 (ac )
Ca ( ac )
Pgina
8
CATIONES
DEL CUARTO
GRUPO
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
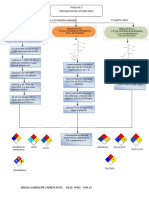
c) DIAGRAMA DE PROCESO
SOLUCIO
N
MUESTRA
Calentar a
bao maria y
agregar 1
gota de
NH4I 1M y
agrega
evaporar
Centrifugar
Centrifugar
y
decantar.A
y decantar.A
la
la solucion
solucion
restante
restante
agregarle
agregarle
H
H22O
O22 ::
A la solucion
agregar
restante
12 gotas
evaporarlo
ph
de
Calent
Agregar
hasta 1mL y
tiocetami
0,5.Centrifu
HCl
0,6M
ar
10
agregarle
da y
1M
gar
igual
min
decantar
cantidad de
agua de
bromo
Saturar
con
cristales
de NH4Cl
Agreg
ar
NH4O
H 15M
Pgina
9
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
Agregar
8 gotas
de
CH3CSN
H2
Evaporar la
solucin,se
torna
amarillo
tenue
Agregar
agua,
NH4Cl,
NH4OH
Calentar la
solucin,
centrifugar
y decantar
De la
solucin
que
restante
evaporar,
agregar
HNO3
d) CONCLUSIONES
HCl(ac)
Se utiliza
Agregar
por
timo
(NH44)22CO
3
3
solo hasta que precipite puesto que si
aadimos en exceso se formaran complejos solubles. Al agregar
HCl(ac )
al sistema en equilibrio aumenta la cantidad de solido (
AgCl(s )
PbCl 2(s )
Hg 2 Cl 2(s)
es
decir
disminuye
la
solubilidad logrando que los slidos del primer grupo precipiten.
El precipitado blanco formado en el primer proceso(al aadir
HCl(ac )
a la muestra original) es debido a los compuestos del
primer grupo
AgCl(s )
PbCl 2(s )
Pgina
10
Hg 2 Cl 2(s)
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
En el segundo proceso la acidez debe ser alta, ya que si
disminuye se formara un precipitado blando que no son
compuestos de sulfuros.
Los compuestos del tercer grupo (hidrxidos) precipitan cuando
la muestra llega hacer alcalina esto gracias al cloruro de
amonio y al hidrxido de amonio. El precipitado en conjunto
tiene un color marrn
Se not la pesencia de los ions Ni2+, Co2+, Zn2+ al tata la
solucin con CH3CSNH2 debido a ue la concentracin del S2- es
mayor en medio alcalino, lo cual permite que se d la
precipitacin de estos iones.
Los sulfuros son ms solubles que los iones del 2 grupo
El precipitado amarillo tenue evidencia la presencia de los
cationes del 3 grupo.
Comprobamos que los alcalinos trreos son los nicos que
pueden precipitar con el carbonato amnico
Se comprueba que los nitratos obtenidos de la solucin del paso
anterior son isolubles en HNO3 concentrado
El Kps de las sales de carbonato es pequeo, por lo cual
precipitan al agregar (NH4)2CO3
Los carbonatos (BaCO3, SrCO3, CaCO3) son insolubles en agua
Los carbonatos se lograron identificar debido al color del
precipitado blanco.
4. USOS INDUSTRIALES DE LOS IONES ESTUDIADOS
COMPUESTOS
USOS INDUSTRIALES
N H 4 I (ac)
Es
utilizado
preferentemente
como
explosivo de iniciacin, pues es muy
inestable y la liberacin de energa trmica
es muy baja.
Pgina
11
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
H 2 O2
En la industria alimenticia se usa
mucho para blanquear quesos, pollos,
carnes, huesos, y tambin se usa en el
proceso para la elaboracin de aceites
vegetales.
En la industria qumica se usa como
reactivo, y es muy importante en la
elaboracin de frmacos. Se est usando
tambin para blanqueos dentales.
COMPUESTOS
tioacetamida
C5 H 5 NS )
USOS INDUSTRIALES
Para usos de laboratorio, anlisis,
investigacin y qumica fina.
Se
utiliza
en
la
produccin
de
catalizadores, estabilizadores, inhibidores
de
la
polimerizacin,
galvanoplastia,
aditivos
productos
de
qumicos
fotogrficos, pesticidas, agentes auxiliares
de teido y agentes de procesamiento.
Tambin se utiliza como un polmero que
agentes
de
curado,
agentes
de
reticulacin, aditivos de caucho y de
Pgina
12
MARCHA ANALTICA DE SEPARACIN DE CATIONES EN GRUPOS
materias primas farmacuticas.
5. BIBLIOGRAFIA
Wikipedia, La Enciclopedia Libre. Tioacetamida. Recuperado de
http://pt.wikipedia.org/wiki/Tioacetamida
Wikipedia, La Enciclopedia Libre. Yoduro de amonio. Recuperado de
http://es.wikipedia.org/wiki/Yoduro_de_amonio
CTR scientist. Hoja de datos de seguridad. Recuperado de
http://www.ctr.com.mx/pdfcert/Tioacetamida.pdf
Pgina
13
S-ar putea să vă placă și
- Campo Magnetico TerrestreDocument15 paginiCampo Magnetico TerrestrePedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Campo Magnetico 100 AcabadoDocument15 paginiCampo Magnetico 100 AcabadoPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Corriente Alterna ProblemasDocument4 paginiCorriente Alterna ProblemasPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Pueba de Lucas y de YodoformoDocument7 paginiPueba de Lucas y de YodoformoPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Labo Quimica OrganicaDocument4 paginiLabo Quimica OrganicaPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Técnicas de Destilación y Temperatura de EbulliciónDocument8 paginiTécnicas de Destilación y Temperatura de EbulliciónPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- ClorofluorcarbonadosDocument6 paginiClorofluorcarbonadosPedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Fisicoquimica Informe N°7Document15 paginiFisicoquimica Informe N°7Pedro Santiago Salcedo GutierrezÎncă nu există evaluări
- Metales de La Triada Del HierroDocument11 paginiMetales de La Triada Del HierroPedro Santiago Salcedo Gutierrez100% (1)
- Memorías de Calculo STARD Fería de Ganado MarinillaDocument34 paginiMemorías de Calculo STARD Fería de Ganado MarinillaJulio BuendiaÎncă nu există evaluări
- Producto 2Document20 paginiProducto 2Eduardo Vilca calla100% (1)
- Aplicación Química A La AgriculturaDocument8 paginiAplicación Química A La AgriculturaSamuel ArangoÎncă nu există evaluări
- PRÁCTICA # 2 CALOR DE MEZCLA Chan ChanDocument19 paginiPRÁCTICA # 2 CALOR DE MEZCLA Chan ChanLUAR PADRONÎncă nu există evaluări
- Informe 3 - CristalizacionDocument13 paginiInforme 3 - CristalizacionWendy Alva100% (1)
- Cinética de Las Reacciones Químicas: October 2019Document6 paginiCinética de Las Reacciones Químicas: October 2019KEVIN PAUL DOMINGUEZ VALENCIAÎncă nu există evaluări
- copia-en-la-nube-Productos-Fritos 2Document3 paginicopia-en-la-nube-Productos-Fritos 2Yissel López RodríguezÎncă nu există evaluări
- Cemento Solvente de PVC Blanco - Verde y CPVC FDSDocument4 paginiCemento Solvente de PVC Blanco - Verde y CPVC FDSHS Junior DuvalÎncă nu există evaluări
- Val #007 - Ad Febrero 2022Document34 paginiVal #007 - Ad Febrero 2022Jessica TatianaÎncă nu există evaluări
- Aplicaciones de E.DDocument7 paginiAplicaciones de E.DMicaela Guerra NoriegaÎncă nu există evaluări
- Simulacion de Procesos Quimicos: Universidad Nacional Del Altiplano Facultad de Ingenieria QuimicaDocument19 paginiSimulacion de Procesos Quimicos: Universidad Nacional Del Altiplano Facultad de Ingenieria Quimicaelia melayde rosello ccasaÎncă nu există evaluări
- InformeDocument13 paginiInformeMartin TorresÎncă nu există evaluări
- Contenido Semana 1 Farmacologia Podologia 2022Document87 paginiContenido Semana 1 Farmacologia Podologia 2022Belen Dafne100% (1)
- Lipoproteinas HDLDocument6 paginiLipoproteinas HDLMilene PonceÎncă nu există evaluări
- Protocolo Yodimetria - JMGDocument7 paginiProtocolo Yodimetria - JMGAlan VilchisÎncă nu există evaluări
- Examen HQSEDocument314 paginiExamen HQSEesli100% (1)
- Materiales Aglutinantes y El ConcretoDocument46 paginiMateriales Aglutinantes y El ConcretoFabio OtxoaÎncă nu există evaluări
- Aldehidos y Cetonas en La IndustriaDocument3 paginiAldehidos y Cetonas en La IndustriaCristel Mendoza TincopaÎncă nu există evaluări
- Tubo PitotDocument3 paginiTubo PitotEstefy AllaucaÎncă nu există evaluări
- Descargadores MTDocument6 paginiDescargadores MTJuan Manuel NeiraÎncă nu există evaluări
- Proyecto de Aula - QuimicaDocument53 paginiProyecto de Aula - QuimicaDanielaÎncă nu există evaluări
- Ensayos de LabDocument8 paginiEnsayos de LabLizeth Juliana Arenas CardenasÎncă nu există evaluări
- Qué Es La Tabla Periódica de Los ElementosDocument7 paginiQué Es La Tabla Periódica de Los ElementosJean Carlos Páez RamírezÎncă nu există evaluări
- ClorometilDocument2 paginiClorometilmarita3yahuana3guerr100% (1)
- Clase Cap 12 - 2020Document32 paginiClase Cap 12 - 2020JOSE DANIEL AGUIRRE ACOSTAÎncă nu există evaluări
- Marco TeoricoDocument3 paginiMarco TeoricoLuis Martinez100% (1)
- Preparación Del Sistema IndolDocument1 paginăPreparación Del Sistema Indolangie creyesÎncă nu există evaluări
- Flotacion de MineralesDocument47 paginiFlotacion de MineralesVictor Alvarez100% (4)
- Informe de Intervalo de VireDocument6 paginiInforme de Intervalo de VireBereniceÎncă nu există evaluări
- Maquinas TermicasDocument5 paginiMaquinas TermicasING. Miguel Angel Sanchez MonzonÎncă nu există evaluări