Documente Academic
Documente Profesional
Documente Cultură
1 Conductividad Electrica
Încărcat de
Mary SalasarDescriere originală:
Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
1 Conductividad Electrica
Încărcat de
Mary SalasarDrepturi de autor:
Formate disponibile
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
PRACTICA N 1
CONDUCTIVIDAD ELECTRICA
1. INTRODUCCION
El desarrollo de la Ciencia y Tecnologa actuales implican la generacin y aplicacin del
conocimiento en muchas reas y consecuentemente el estudiante de Ingeniera debe estar al tanto de los
mismos, sin embargo, debido a la actualizacin poco frecuente de los programas y planes de estudio y
por las limitaciones propias de semestres de apenas cuatro meses de actividades acadmicas, es difcil
la actualizacin del estudiante en dichos conocimientos.
En ello tambin los trabajos de investigacin no funciona de la manera deseada, ya que las fuentes
de informacin consultadas con mayor frecuencia son las virtuales ofrecidas por el internet, donde
dichos datos no muchas veces no son confiables; de ese modo, surge la idea de plantear temas de gran
inters para el desarrollo de nuestras capacidades y de la ciencia en general.
En el presente informe, se estudiara el proceso de conductividad elctrica en medios acuosos,
como lo son las disoluciones; y la conductividad elctrica en dichos medios. Se analizaran varias
situaciones en las que influir de manera significativa la naturaleza de las disoluciones. De antemano se
propondrn los datos tericos necesarios para un completo entendimiento de los fenmenos de estudio.
MARCO TEORICO
2. CONCEPTUALIZACION
Conductividad elctrica.- La conductividad elctrica es la capacidad de un cuerpo o medio
para conducir la corriente elctrica.
Conductor.- Un conductor elctrico es aquel cuerpo que puesto en contacto con un cuerpo
cargado de electricidad trasmite est a todos los puntos de superficie. Los mejores conductores
Pgina 1
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
son los elementos metlicos, especialmente oro, plata(es el ms conductor), el cobre, el
aluminio, etc.
Semiconductor.- Es una sustancia que se comporta como conductor o como aislante
dependiendo del campo elctrico o la temperatura en el que se encuentre, capaz de conducir la
electricidad mejor que un aislante, pero peor que un metal. El elemento semiconductor ms
usado es el silicio.
Aislante.- Un aislante es una sustancia que no conduce electricidad bajo condiciones normales.
La principal caracterstica de los aislantes es que tienen muy pocos o ningunos electrones libres
bajo condiciones normales. Todos los electrones de un aislante estn unidos a sus tomos
mediante fuerzas de gran magnitud. Ejemplos mica, porcelana, vidrio, etc.
Electrolitos y no electrolitos.- los electrolitos son sustancias que en disolucin acuosa forman
iones que son capaces de conducir la corriente elctrica, los no electrolitos no forman iones en
disolucin acuosa, por tal motivo no conducen la corriente elctrica. Son electrolitos los
compuestos formados por enlaces inicos como las sales; y no electrolitos la mayora de los
compuestos orgnicos.
3. OBJETIVOS
3.1. OBJETIVO GENERAL
Determinar q sustancias son conductoras.
3.2. OBJETIVOS ESPECIFICOS
Observar el efecto de la electricidad sobre los electrodos.
Diferenciar las sustancias electrolticas de las no electrolticas.
Graficar el comportamiento de la conductividad de una solucin de cloruro de sodio a
varias concentraciones.
MARCO PRCTICO
4. MATERIALES Y REACTIVOS
Materiales.
Fuente de alimentacin.
Electrodos de cobre.
Pgina 2
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
Mdulos de celda de ensayo.
Corriente con el clip cocodrilo.
Cubierta de soluciones.
Cables de conexin.
Vasos de precipitado (vidrio).
Foquitos.
Reactivos.
Agua destilada.
Solucin de azcar.
Cloruro de sodio (NaCl)
Hidrxido de sodio (NaOH)
cido clorhdrico (HCl)
cido actico.
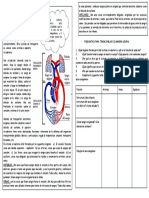
5. ESQUEMA DE LA PRACTICA
MULTITESTER
ELECTRODOS
CUBAS
BOMBILLA DE LUZ
CONECCION A LA FUENTE DE ENERGIA
6. PROCEDIMIENTO DE LA PRACTICA
- Prepare la serie de vasos contenedores de las diferentes soluciones.
- Disponga el circuito esquematizado y asegrese que la fuente este apagada.
- Conecte un electrodo de cobre por medio del cable rojo insertando el voltmetro en serie.
- Conecte el otro electrodo a la fuente con una bombilla a la fuente.
- Sumerja los electrodos en cada solucin y encienda la fuente.
- Apague la fuente despus de cada observacin y enjuague los electrodos con agua destilada
despus de cada uso.
7. TABULACION DE DATOS EXPERIMENTALES Y ANALITICOS
Pgina 3
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
7.1. Clasificacin de electrolitos y no electrolitos segn la intensidad de la luz producida por la
corriente elctrica conducida
Solucin
Brillo de Luz
Luz dbil
Sin Luz
Corriente mA
H2O
Azcar
cido actico
BAJA
62 74
HCl
ALTA
110 120
NaCl
MEDIA
150 158
NaOH
MEDIA
143 153
7.2. Intensidad de corriente en funcin de la Concentracin de NaCl
Concentracin (M)
0.1
0.20
0.35
0.5
0.6
0.7
Intensidad (A)
0.07
0.15
0.23
0.31
0.38
0.44
8. CONDUCTIVIDAD EN FUNCION DE LA CONCENTRACION
Se prepararon disoluciones de cloruro de sodio a varias concentraciones.
Se determin la intensidad de corriente transmitida.
Se grafic el comportamiento de nuestros datos.
Se ajust a una funcin lineal.
Pgina 4
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
Intensidad vs. Concentracion
0.5
f(x) = 0.62x + 0.01
R = 1
0.4
0.3
INTENSIDAD (A)
0.2
0.1
0
0
0.1
0.2
0.3
0.4
0.5
0.6
CONCENTRACION (NaCl)
I (C)=0.6157C +0.0102
Pgina 5
0.7
0.8
LABORATORIO DE ELECTROQUIMICA (QMC 225)
Conductividad Elctrica
Universidad Mayor Real y Pontificia de San Francisco Xavier de Chuquisaca
Esta es la ecuacin para la intensidad de corriente transmitida a cualquier concentracin
de una disolucin de cloruro de sodio.
9. CONCLUSIONES
Se pudo observar el comportamiento de las sustancias electrolticas, y la teora de la
conductividad, en el esquema propuesto.
El anlisis cualitativo de nuestro sistema nos dio a conocer que es de mucha importancia tomar
en cuenta la distancia entre electrodos en el momento de la reaccin puesto que a mayor
distancia los iones demoran ms tiempo en migrar, y en los ensayos de varias especies o
sustancias en disolucin acuosa esto es perjudicial si tomamos en cuenta que deben realizarse
en las mismas condiciones para poder realizar la respectiva evaluacin comparativa.
Se concluye que la intensidad de corriente conducida por una disolucin acuosa es directamente
proporcional a la concentracin del electrolito en ella. Es decir a mayor concentracin, mayor es
la conductividad del medio.
Pgina 6
S-ar putea să vă placă și
- Laboratorio Quimica RedoxDocument6 paginiLaboratorio Quimica RedoxjosipÎncă nu există evaluări
- Conductancia Por Medio de ElectrolitosDocument8 paginiConductancia Por Medio de ElectrolitosAngheloHolguinSilvaÎncă nu există evaluări
- FQ 06 ElectroquimicaDocument20 paginiFQ 06 ElectroquimicaGian Marco Escobar CruzÎncă nu există evaluări
- P7 CorrosionDocument7 paginiP7 CorrosionJuan Carlos AzuaraÎncă nu există evaluări
- Celdas GalvanicasDocument7 paginiCeldas GalvanicasAlexander EspinozaÎncă nu există evaluări
- PRACTICA 1 ElectrolitosDocument9 paginiPRACTICA 1 ElectrolitosSaúl RodríguezÎncă nu există evaluări
- Informe de Quimica-N°2Document10 paginiInforme de Quimica-N°2JAN POL GUTIERREZ CHAVEZÎncă nu există evaluări
- 5 Celdas GalvanicasDocument3 pagini5 Celdas GalvanicasLuis Córdova CoxÎncă nu există evaluări
- Practica N°1Document9 paginiPractica N°1mijaheel ferrufinoÎncă nu există evaluări
- Informe Del Agua y La TierraDocument6 paginiInforme Del Agua y La TierraNoelia Lizárraga CenasÎncă nu există evaluări
- INFORME #001 Instalacion y Reconocimiento de Celdas ElectroquimicasDocument5 paginiINFORME #001 Instalacion y Reconocimiento de Celdas ElectroquimicasNoemi Quispe VillacortaÎncă nu există evaluări
- Practica de Laboratorio N°6Document6 paginiPractica de Laboratorio N°6marlon20495Încă nu există evaluări
- Informe N1-Ley de Ohm Aplicada en La ElectroquimicaDocument27 paginiInforme N1-Ley de Ohm Aplicada en La ElectroquimicaIrene Hinostroza0% (1)
- FQ 06 ElectroquimicaDocument19 paginiFQ 06 ElectroquimicaMegy Silva100% (2)
- Practico 1 (Electroquimica)Document7 paginiPractico 1 (Electroquimica)Anabel VargasÎncă nu există evaluări
- Laboratorio #01. Celdas Electrolíticas y Medición de Variables de OperaciónDocument28 paginiLaboratorio #01. Celdas Electrolíticas y Medición de Variables de OperaciónRodrigo MontoyaÎncă nu există evaluări
- Conductividad de Soluciones ElectróliticasDocument12 paginiConductividad de Soluciones ElectróliticasVictor Mauricio Ugarte MamaniÎncă nu există evaluări
- Texto de PRACTICAS LAB. ELECTROQUIMICADocument26 paginiTexto de PRACTICAS LAB. ELECTROQUIMICAMayra DayanaÎncă nu există evaluări
- Practica 1Document8 paginiPractica 1mayra dayana mamani gonzalesÎncă nu există evaluări
- Proyecto de Electrólisis Quimica 1Document12 paginiProyecto de Electrólisis Quimica 1Hernandez LeiverÎncă nu există evaluări
- InformeDocument8 paginiInformeXimena Ramos QuispeÎncă nu există evaluări
- QUIMICA7Document5 paginiQUIMICA7Fredd Gandhi Simon InzaÎncă nu există evaluări
- Portafolio QuimicaDocument165 paginiPortafolio QuimicaValeria LeónÎncă nu există evaluări
- Celdas VoltaicasDocument6 paginiCeldas VoltaicasUvexclearÎncă nu există evaluări
- Laboratorio Quimica ElectroquimicaDocument13 paginiLaboratorio Quimica ElectroquimicaCarlos Alberto SacsaÎncă nu există evaluări
- Laboratorio 1 de CorrosionDocument13 paginiLaboratorio 1 de CorrosionAntonio RamirezÎncă nu există evaluări
- Informe de Serie Galvanica Formato Listo para ImprimirDocument10 paginiInforme de Serie Galvanica Formato Listo para ImprimirDiego PabonÎncă nu există evaluări
- Celda ElectroquímicaDocument19 paginiCelda ElectroquímicaIvette JimenezÎncă nu există evaluări
- Celdas VoltaicasDocument5 paginiCeldas VoltaicasFernando Sanchez CarbajalÎncă nu există evaluări
- Ley de Ohm - Grupo - 10Document26 paginiLey de Ohm - Grupo - 10Irene HinostrozaÎncă nu există evaluări
- Química y ElectricidadDocument9 paginiQuímica y ElectricidadJosé Ángel López EstradaÎncă nu există evaluări
- Informe Del Experimento de QuimicaDocument3 paginiInforme Del Experimento de QuimicaLuis Cepeda50% (2)
- Electroquimica - Informe 2Document14 paginiElectroquimica - Informe 2FernandaÎncă nu există evaluări
- Practica 5 Quimica BasicaDocument13 paginiPractica 5 Quimica BasicaAxel Dávila PozasÎncă nu există evaluări
- Electroquimica-Pilas Laboratorio Fiee UniDocument3 paginiElectroquimica-Pilas Laboratorio Fiee Unistone_c35Încă nu există evaluări
- Practica 5 ElectroquimicaDocument11 paginiPractica 5 ElectroquimicaDaniel SalcedoÎncă nu există evaluări
- Practica QuimicaDocument16 paginiPractica QuimicaantonÎncă nu există evaluări
- Pilas 11Document8 paginiPilas 11esther valeria lauraÎncă nu există evaluări
- Practica 12 - Celdas Galvanicas y Celdas ElectroliticasDocument5 paginiPractica 12 - Celdas Galvanicas y Celdas ElectroliticasPaul Mantilla100% (1)
- Lab 10 Gean FQ IIDocument7 paginiLab 10 Gean FQ IIGean Aguilar C.Încă nu există evaluări
- ELECTROQUÍMICADocument12 paginiELECTROQUÍMICAROMINA NICOLL YNGA SANDOVALÎncă nu există evaluări
- Electroquímica UNASAMDocument15 paginiElectroquímica UNASAMMaycol Richard Leyva PatricioÎncă nu există evaluări
- Celdas ElectroquimicasDocument9 paginiCeldas ElectroquimicasRicardo Catacora LeónÎncă nu există evaluări
- ANALITICA ConductrimetriaDocument7 paginiANALITICA ConductrimetriaJoel Daniel Laura FuñoÎncă nu există evaluări
- Proyecto Cargador SolarDocument6 paginiProyecto Cargador SolarFabrizzio Raúl Palomino PradoÎncă nu există evaluări
- Practica 9 Celda GalvanicaDocument2 paginiPractica 9 Celda GalvanicaScalerFitÎncă nu există evaluări
- Resultado de Aprendizaje 3Document5 paginiResultado de Aprendizaje 3Karly TreviñoÎncă nu există evaluări
- Laboratorio #5 Celdas GalvanicasDocument5 paginiLaboratorio #5 Celdas GalvanicasCarlos Bryan AvilaÎncă nu există evaluări
- Lab 01 Electroquímica 2019 IDocument3 paginiLab 01 Electroquímica 2019 IAngella GiannottiÎncă nu există evaluări
- Determinación Electrogravimétrica de Zinc y CobreDocument13 paginiDeterminación Electrogravimétrica de Zinc y CobreingrossÎncă nu există evaluări
- Marco TeóricoDocument16 paginiMarco TeóricoHugo CortezÎncă nu există evaluări
- Practica 5 CorrecionDocument8 paginiPractica 5 CorrecionCristian Alejandro Ramirez BernalÎncă nu există evaluări
- 1PM21 Equipo3 Practica9Document20 pagini1PM21 Equipo3 Practica9Andres HCÎncă nu există evaluări
- Práctica N 2 Pila DaniellDocument4 paginiPráctica N 2 Pila DaniellMilagros Gonzales100% (1)
- Electroquimica FISICOQUIMICA I Practica #06 2016 1Document17 paginiElectroquimica FISICOQUIMICA I Practica #06 2016 1nelvaÎncă nu există evaluări
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe la EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaÎncă nu există evaluări
- G.didactica 05 EdeA 03 - FichaDocument6 paginiG.didactica 05 EdeA 03 - FichaFabian Esteban100% (1)
- Tema 4 TRANSFORMACIONES GEOMETRICAS 2o Bach Part A INVERSION-V8Document58 paginiTema 4 TRANSFORMACIONES GEOMETRICAS 2o Bach Part A INVERSION-V8Francisco Aguilar GuzmanÎncă nu există evaluări
- 19 Copias A ColorDocument1 pagină19 Copias A ColorMica LeguizamonÎncă nu există evaluări
- Comportamiento Del ConsumidorDocument13 paginiComportamiento Del Consumidoroctavio cruz escobarÎncă nu există evaluări
- Sesion CCSS Independencia 13 Colonias AmericanasDocument6 paginiSesion CCSS Independencia 13 Colonias Americanasyery ysabel paredes crespinÎncă nu există evaluări
- MANUAL DE POLiTICAS Y PROCEDIMIENTOS PARA EL ESTUDIANTE DEL CIDEBDocument14 paginiMANUAL DE POLiTICAS Y PROCEDIMIENTOS PARA EL ESTUDIANTE DEL CIDEBInspección Zona4Încă nu există evaluări
- Practica Pre Profesional 020 2021 MimpDocument4 paginiPractica Pre Profesional 020 2021 MimpDavid Enríquez CubillasÎncă nu există evaluări
- Listado de Venta Bienes Adquiridos CajaDeAhorros 2Document10 paginiListado de Venta Bienes Adquiridos CajaDeAhorros 2Leonora Elizabeth Miranda FloresÎncă nu există evaluări
- Semana 06 Mci CompresionDocument26 paginiSemana 06 Mci CompresionCristian Rey SanchezÎncă nu există evaluări
- Universidad TécnicaDocument12 paginiUniversidad TécnicaPaulina CobeñaÎncă nu există evaluări
- Trabajo Final - Métodos para El Desarrollo de Competencias Fuera Del TrabajoDocument9 paginiTrabajo Final - Métodos para El Desarrollo de Competencias Fuera Del TrabajoAnaÎncă nu există evaluări
- Percepcion Visual PorterosDocument17 paginiPercepcion Visual Porterosjuanjoromi100% (1)
- Caso ClinicoDocument4 paginiCaso ClinicoPaola GutiérrezÎncă nu există evaluări
- Evaluación Interna FISICADocument2 paginiEvaluación Interna FISICAGabriel SeinerÎncă nu există evaluări
- Cálculo de Momentos de Empotramiento de 2 Cargas PuntualesDocument6 paginiCálculo de Momentos de Empotramiento de 2 Cargas PuntualesAlbert Richard Miranda SivilaÎncă nu există evaluări
- s3 MH - DispersionDocument18 paginis3 MH - DispersionJulio Augusto De LuqueÎncă nu există evaluări
- Installation GuideDocument40 paginiInstallation Guidegeny965809Încă nu există evaluări
- Costos UnitariosDocument33 paginiCostos UnitariosmilenaÎncă nu există evaluări
- DEMANDA DE AMPARO TEUNI VS UNI DERECHO A LA EDUCACIÓN LMTB FINAL FinalDocument23 paginiDEMANDA DE AMPARO TEUNI VS UNI DERECHO A LA EDUCACIÓN LMTB FINAL FinalJAFET_123Încă nu există evaluări
- Manual de Vigia Nm343Document15 paginiManual de Vigia Nm343Heriberto de la CruzÎncă nu există evaluări
- La Excepción y La NormaDocument14 paginiLa Excepción y La NormazapruderÎncă nu există evaluări
- Apus Panama 23-12Document102 paginiApus Panama 23-12Fernando SanchezÎncă nu există evaluări
- Manual de Hardware Abb Acs600Document88 paginiManual de Hardware Abb Acs600Javier Manso LoredoÎncă nu există evaluări
- Informe de Cierre Del Proceso de InscripcionesDocument11 paginiInforme de Cierre Del Proceso de InscripcionesTIAGOÎncă nu există evaluări
- 2 RotulaciónDocument8 pagini2 RotulaciónAlejoÎncă nu există evaluări
- Trabajo Pensamiento AlgoritmicoDocument5 paginiTrabajo Pensamiento AlgoritmicoJarrison VelezÎncă nu există evaluări
- Formato Diagnóstico de La OrganizaciónDocument6 paginiFormato Diagnóstico de La OrganizaciónFERNANDOPG0% (1)
- Manual TOP DOG CorregidoDocument41 paginiManual TOP DOG CorregidoAlexis Briseño100% (2)
- Modelo Productivo SocialistaDocument4 paginiModelo Productivo SocialistamariaÎncă nu există evaluări
- Pruebas ProyectivasDocument6 paginiPruebas ProyectivasjuditloÎncă nu există evaluări