Documente Academic
Documente Profesional
Documente Cultură
Practica Concentracion de Enzima
Încărcat de
Dante LlerenaDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Practica Concentracion de Enzima
Încărcat de
Dante LlerenaDrepturi de autor:
Formate disponibile
INSTITUTO POLITECNICO NACIONAL
Escuela Nacional de Ciencias Bilgicas
Ingeniera en Sistemas Ambientales
Practica: Efecto de la concentracin de enzima sobre la velocidad de reaccin
Alumnos: Cantera Trejo Susana Isabel;Dante Llerena Olivares.
Asignatura: Bioqumica Fundamental. Laboratorio.
Profesores: Roco Guzmn Ibarra; Albany Resndiz Mora;
Carlos Wong Baeza; Doris Neri Cortes.
Grupo: 4AM1
Seccin 2
Equipo 11
INTRODUCCION
La velocidad de la reaccin es directamente proporcional a la concentracin de la enzima a cualquier
concentracin de substrato. Por ejemplo, si la concentracin de enzima es disminuida a la mitad, la velocidad
inicial de la reaccin (Vo) es reducida tambin a la mitad de la original.
La velocidad de transformacin de los sustratos de una reaccin en los correspondientes productos, mediante
una enzima y bajo condiciones de estado estacionario, es dependiente tanto de las concentraciones de la
enzima como de los sustratos. Normalmente, esa dependencia puede ser expresada matemticamente por la
ecuacin de Michaelis-Menten:
V max . [ S ]
Veloc .=
Km+ [ S ]
Esta ecuacin predice que la velocidad de formacin de producto es saturable con respecto al sustrato, es
decir existe una concentracin de sustrato a partir del cual la Veloc. no aumenta de forma significativa.
La Vmax se denomina velocidad mxima, y depende de la concentracin de enzima segn una relacin lineal:
Vmax = k2 [E]
El Km es un parmetro que depende de la afinidad de la enzima por el sustrato y que se denomina constante
de Michaelis.
La actividad cataltica de las enzimas depende estrictamente de la conformacin de la protena enzimtica, es
decir de su estructura tridimensional. Por ello, los cambios conformacionales suelen ir asociados a cambios en
la eficacia cataltica de las enzimas.
La velocidad de la reaccin con respecto a la concentracin de enzima tiene la forma lineal de modo grafico:
OBJETIVOS
Observar el efecto de la concentracin de la enzima sobre la velocidad de la reaccin enzimtica.
RESULTADOS OBTENIDOS
Una vez concluida la sesin experimental se obtuvieron los tubos con las siguientes tonalidades:
Y al leer cada muestra en el espectrofotmetro a 540 nm se obtuvieron los siguientes resultados:
Blanco Problemas
Parmetros a medir y/o calcular
T 1 2 3 4 5
Absorbencia = 540 nm 0.0 0.026 0.066 0.063 0.149 0.176
(moles) Azcar reductor/2 ml 0 1 2 4 8 10
Velocidad (unidades de invertasa) 0 0.1 0.2 0.4 0.8 1
Concentracin de enzima
0 0.5 1 1.5 2 2.5
(moles/ml)
CALCULOS
Glucosa 0.005 M
Fructuosa 0.005 M
G+ F 0.010 M
0.010 moles de A.R. 1000 ml
X 0.1 ml
X = 1x10-6 moles de A.R.
X = 1 mol de A.R./2.0 ml
Calculo de las unidades de intervasa:
[ moles sacarosa ]
Vo=actividad= =U . I
min .
Ejemplo para el Problema 1:
[ A . R ./ 2 ml ] /2 [ A . R ./2 ml ] 1
Vo=actividad= = = =0.1U . I
5 min . 10 min . 10
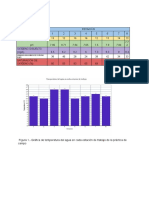
Concentracin de enzima (moles/ml) vs velocidad de reaccin
3
2.5
1.5
0.5
0
0 0.2 0.4 0.6 0.8 1 1.2
Discusin
Visualmente se presento una coloracin distinta gradual e incrementando en cada uno de los tubos en
estudio, el tubo muestra no presento coloracin independiente de la brindada por el 3-5 DNS, tomndolo as
para poder realizar mediadas de la absorbencia logrando as determinar una velocidad de reaccin de y por
medio de nuestro grfico poder apreciar mejor los cambios suscitados en los tubos en estudio.
Conclusin
Al realizar un anlisis cualitativo y corroborarlo cuantitativamente con el espectrofotmetro, se pudo
determinar la grafica que ilustra mejor el comportamiento de la velocidad de reaccin de la invertasa con la
sacarosa, en presencia de cambios de la concentracin de enzima. Se comprueba que hay una
proporcionalidad entre la velocidad de reaccin y la concentracin de enzima.
Bibliografa
https://es.scribd.com/doc/72893397/31-INVERTASA-ENSAYO
http://documents.mx/documents/32-invertasa-cineticapdf.html
S-ar putea să vă placă și
- Practica Determinacion de Especies Alcalinas - Q. AnaliticaDocument6 paginiPractica Determinacion de Especies Alcalinas - Q. AnaliticaYoali Asiain LeconaÎncă nu există evaluări
- Practica 5Document18 paginiPractica 5Gonzalo UribeÎncă nu există evaluări
- Bitácora-Efecto de La Concentración de Enzima Sobre La Velocidad de Reacción-Efecto Del PH Sobre La Velocidad de ReacciónDocument5 paginiBitácora-Efecto de La Concentración de Enzima Sobre La Velocidad de Reacción-Efecto Del PH Sobre La Velocidad de ReacciónDynarko RuizÎncă nu există evaluări
- Bitacora Bioquimica Practica 3 Reacciones ProteinasDocument3 paginiBitacora Bioquimica Practica 3 Reacciones ProteinasDiego AmrÎncă nu există evaluări
- Reacciones de Proteínas IDocument3 paginiReacciones de Proteínas IEmriel96100% (1)
- Deshidrogena SuccínicaDocument1 paginăDeshidrogena SuccínicaAngel BeltranÎncă nu există evaluări
- Reporte 1 Fisiología CelularDocument10 paginiReporte 1 Fisiología CelularMonserrat Blanquel GarcíaÎncă nu există evaluări
- Practica 1 FisiologiaDocument17 paginiPractica 1 FisiologiaJocee SqadeliiqÎncă nu există evaluări
- Practica 2 Report eDocument10 paginiPractica 2 Report eEdson GonzalezÎncă nu există evaluări
- Cinemática Enzimática 5.1Document2 paginiCinemática Enzimática 5.1Eduardo Alonso50% (2)
- Práctica 2 - Determinación de Humedad Por Pérdida de Peso en Estufa A Presión NormalDocument11 paginiPráctica 2 - Determinación de Humedad Por Pérdida de Peso en Estufa A Presión NormalKira LÎncă nu există evaluări
- Cuestionario Práctica 7 ESTRUCTURA EXTERNA E INTERNA DE LA HOJA.Document2 paginiCuestionario Práctica 7 ESTRUCTURA EXTERNA E INTERNA DE LA HOJA.Mar Dz HÎncă nu există evaluări
- Práctica 1. Vías de AdministraciónDocument17 paginiPráctica 1. Vías de AdministraciónFernando Victoria100% (1)
- Efecto de Concentración de Sustrato e Inhibición Enzimática.Document2 paginiEfecto de Concentración de Sustrato e Inhibición Enzimática.H VandortÎncă nu există evaluări
- Efecto de La Temperatura en Los MicroorganismosDocument11 paginiEfecto de La Temperatura en Los MicroorganismosNelly Aidee Avila LagunaÎncă nu există evaluări
- Práctica Nutrición MineralDocument5 paginiPráctica Nutrición MineralMelani VSÎncă nu există evaluări
- An - Lisis de La Calidad Del Agua I Determinaciones Fisicoqu - MicasDocument7 paginiAn - Lisis de La Calidad Del Agua I Determinaciones Fisicoqu - MicasEdwin CruzÎncă nu există evaluări
- Practica 2 Ecologia MicrobianaDocument5 paginiPractica 2 Ecologia MicrobianaMiguel LunaÎncă nu există evaluări
- Seminario Práctica 5 EcoDocument29 paginiSeminario Práctica 5 EcoFernando VictoriaÎncă nu există evaluări
- 3fm1 - Morales Vargas Citlali - Villada Victoria Vianney - Determinación de Aminoácidos Terminales Con Grupo Alfa Amino LibreDocument4 pagini3fm1 - Morales Vargas Citlali - Villada Victoria Vianney - Determinación de Aminoácidos Terminales Con Grupo Alfa Amino LibreVianney VilladaÎncă nu există evaluări
- Práctica 4. Adsorción II. Versión 2Document4 paginiPráctica 4. Adsorción II. Versión 2Gibran Meza CastrejonÎncă nu există evaluări
- Practrica 6 Sintesis AcidoacetilsalisilicoDocument3 paginiPractrica 6 Sintesis AcidoacetilsalisilicoHugoÎncă nu există evaluări
- Curva Tipo ColesterolDocument2 paginiCurva Tipo ColesterolGuerrillaScribdÎncă nu există evaluări
- Examen BotanicaDocument8 paginiExamen BotanicaAngel Ortega GasparÎncă nu există evaluări
- DNADocument2 paginiDNALi ClementeÎncă nu există evaluări
- Pract 3 Metodo de SangerDocument3 paginiPract 3 Metodo de SangerRay torresÎncă nu există evaluări
- Seminario Equipo 3 Pract 2Document38 paginiSeminario Equipo 3 Pract 2Gibran Meza CastrejonÎncă nu există evaluări
- Seminario Equipo 4Document35 paginiSeminario Equipo 4Castillo Nájera SamanthaÎncă nu există evaluări
- Presentación - Proyecto de Titulación 2Document47 paginiPresentación - Proyecto de Titulación 2BlackPork54Încă nu există evaluări
- ADSORCIÓN I ESTUDIO DE LA ADSORCION SOLIDO SOLUCION - Watermark PDFDocument11 paginiADSORCIÓN I ESTUDIO DE LA ADSORCION SOLIDO SOLUCION - Watermark PDFHelenÎncă nu există evaluări
- Bitácora de Práctica 4.4. Obtención de DNA PlasmídicoDocument3 paginiBitácora de Práctica 4.4. Obtención de DNA PlasmídicoOz HdzÎncă nu există evaluări
- Discusion SuelosDocument60 paginiDiscusion SuelosVickyCervantesÎncă nu există evaluări
- Efecto de La Temperatura Sobre La Velocidad de ReaccionDocument4 paginiEfecto de La Temperatura Sobre La Velocidad de ReaccionNathan Ulises Reyes JimenezÎncă nu există evaluări
- Práctica 3. PrecipitaciónDocument3 paginiPráctica 3. PrecipitaciónEli Medrano100% (1)
- Practica 11Document3 paginiPractica 11Karen9DiazÎncă nu există evaluări
- Reporte 8 QODocument18 paginiReporte 8 QOrauljcÎncă nu există evaluări
- Reporte Práctica 5. Síntesis de 2,3-Difenilquinoxalina. Equipo 8. 3QM3Document7 paginiReporte Práctica 5. Síntesis de 2,3-Difenilquinoxalina. Equipo 8. 3QM3IvanÎncă nu există evaluări
- Metodo de SangerDocument3 paginiMetodo de SangerBlankita AguirreÎncă nu există evaluări
- Practica AutonomoDocument2 paginiPractica AutonomoHéctor BalmoriÎncă nu există evaluări
- Presentación PP de Actinomicetos ENCBDocument6 paginiPresentación PP de Actinomicetos ENCBLilu Wrathe TempestÎncă nu există evaluări
- Introduccion: ResultadosDocument3 paginiIntroduccion: ResultadosLuis RojasÎncă nu există evaluări
- Curva Tipo Azucares ReductoresDocument2 paginiCurva Tipo Azucares ReductoresJeeniffer CookieeÎncă nu există evaluări
- Practica 13Document1 paginăPractica 13Yazmin Olivares0% (1)
- Cuantificación de Células Formadoras de Colonias Mediante JerneDocument24 paginiCuantificación de Células Formadoras de Colonias Mediante JerneJosé ManuelÎncă nu există evaluări
- Cromatografia Por AdsorcionDocument3 paginiCromatografia Por AdsorcionLi ClementeÎncă nu există evaluări
- Gutiérrez - Ramírez - Erick - 7QV1 - Eq4 - 06-09-2021 - Reporte Práctica 2Document5 paginiGutiérrez - Ramírez - Erick - 7QV1 - Eq4 - 06-09-2021 - Reporte Práctica 2Erick GutierrezÎncă nu există evaluări
- Gama GlobulinaDocument17 paginiGama GlobulinaPamelaÎncă nu există evaluări
- Caracterizacion de Glucogeno 2Document3 paginiCaracterizacion de Glucogeno 2Jorge Luis OlivarÎncă nu există evaluări
- Efecto de La Temperatura en La InvertasaDocument4 paginiEfecto de La Temperatura en La InvertasaAlexandra HernándezÎncă nu există evaluări
- ReporteAuxinas GuardiánAldamaAndrés 4QM1Document5 paginiReporteAuxinas GuardiánAldamaAndrés 4QM1Andy AldamaÎncă nu există evaluări
- DNA PlasmídicoDocument2 paginiDNA PlasmídicoSuarez GOmez Alexis GabrielÎncă nu există evaluări
- P12 ToxicidadDocument4 paginiP12 ToxicidadJonathan R. EstradaÎncă nu există evaluări
- Practica 4 y 5 FISIOLOGIADocument26 paginiPractica 4 y 5 FISIOLOGIAPauPauSánchezÎncă nu există evaluări
- Practica 1. SangerDocument4 paginiPractica 1. SangerApolinar Aguilar BautistaÎncă nu există evaluări
- Práctica 5 AuxinasDocument4 paginiPráctica 5 AuxinasKenia AvilaÎncă nu există evaluări
- Practica 5 Potencial de Accion y Simulacion Por ComputadoraDocument22 paginiPractica 5 Potencial de Accion y Simulacion Por ComputadoraAndresDuranÎncă nu există evaluări
- Efecto de Los Colorantes Sobre El Crecimiento deDocument21 paginiEfecto de Los Colorantes Sobre El Crecimiento dedaniel ToledoÎncă nu există evaluări
- Bitacora 4. Curva Tipo Azucares ReductoresDocument3 paginiBitacora 4. Curva Tipo Azucares ReductoresJavier AnguianoÎncă nu există evaluări
- CINÉTICA ENZIMÁTICA Y FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMÁTICA InformeDocument10 paginiCINÉTICA ENZIMÁTICA Y FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMÁTICA InformePaula Michelle PolaniaÎncă nu există evaluări
- Laboratorio de Actividad EnzimáticaDocument17 paginiLaboratorio de Actividad EnzimáticaMariaHelenaÎncă nu există evaluări
- ENTREVISTADocument2 paginiENTREVISTADante LlerenaÎncă nu există evaluări
- 02.7 GRA. Met Analisis Riesg (26022020)Document3 pagini02.7 GRA. Met Analisis Riesg (26022020)Dante LlerenaÎncă nu există evaluări
- Contaminación Atmosférica-Niveles Máximos Permisibles de Emisión de Los Equipos de Combustión de Calentamiento Indirecto y Su MediciónDocument18 paginiContaminación Atmosférica-Niveles Máximos Permisibles de Emisión de Los Equipos de Combustión de Calentamiento Indirecto y Su MediciónDante LlerenaÎncă nu există evaluări
- What IfDocument1 paginăWhat IfDante LlerenaÎncă nu există evaluări
- Fisio Xeral Tema 2Document3 paginiFisio Xeral Tema 2Ale MedinaÎncă nu există evaluări
- LaplaceDocument8 paginiLaplaceanon-377340% (1)
- Desintegración RadiactivaDocument1 paginăDesintegración RadiactivaDante LlerenaÎncă nu există evaluări
- Desintegración RadiactivaDocument1 paginăDesintegración RadiactivaDante LlerenaÎncă nu există evaluări
- Concentracion de SustratoDocument1 paginăConcentracion de SustratoDante LlerenaÎncă nu există evaluări
- Rosa de VientosDocument2 paginiRosa de VientosDante LlerenaÎncă nu există evaluări
- Hoja de CustodiaDocument3 paginiHoja de CustodiaDante LlerenaÎncă nu există evaluări
- Manual de Interfaz Arduino PDFDocument39 paginiManual de Interfaz Arduino PDFDante LlerenaÎncă nu există evaluări
- P13 MicroDocument5 paginiP13 MicroDante LlerenaÎncă nu există evaluări
- p11 DantDocument7 paginip11 DantDante LlerenaÎncă nu există evaluări
- Perspectivas Del IPNDocument9 paginiPerspectivas Del IPNDante LlerenaÎncă nu există evaluări
- Arrastre-De-Vapor Dante Llerena OlivaresDocument15 paginiArrastre-De-Vapor Dante Llerena OlivaresDante LlerenaÎncă nu există evaluări
- Ley Difusion GasesDocument3 paginiLey Difusion Gasesopulento22100% (1)
- Desintegración RadiactivaDocument1 paginăDesintegración RadiactivaDante LlerenaÎncă nu există evaluări
- MetabolismoProteinas - Jacqueline VelascoDocument6 paginiMetabolismoProteinas - Jacqueline VelascoADRIANA ZUBIA FLORESÎncă nu există evaluări
- Metabolismo de Proteínas - T10Document27 paginiMetabolismo de Proteínas - T10Eric JavierÎncă nu există evaluări
- Sintesis de NbutiloDocument6 paginiSintesis de NbutiloJose murciaÎncă nu există evaluări
- Previo 4 - Obtencion de Colorantes Del Tipo de Las FtaleinasDocument11 paginiPrevio 4 - Obtencion de Colorantes Del Tipo de Las FtaleinasIrving Saldaña RomoÎncă nu există evaluări
- Trabajo de Investigación - Compostaje DomésticoDocument4 paginiTrabajo de Investigación - Compostaje DomésticoLaura LopezÎncă nu există evaluări
- Ejemplos de NitrilosDocument5 paginiEjemplos de NitrilosMarianÎncă nu există evaluări
- Práctica 3 Reacción1 Diels Alder JCEDocument5 paginiPráctica 3 Reacción1 Diels Alder JCEGeraldÎncă nu există evaluări
- Una Voz en La Fuga CósmicaDocument8 paginiUna Voz en La Fuga CósmicaAndrey RodriguezÎncă nu există evaluări
- GLUTATIONDocument11 paginiGLUTATIONTina AmayaÎncă nu există evaluări
- Practica 5 (Inmunologia)Document6 paginiPractica 5 (Inmunologia)Oshiro CayoÎncă nu există evaluări
- INFORME10 J Peoducción de Piruvato Durante La GlucólisisDocument6 paginiINFORME10 J Peoducción de Piruvato Durante La GlucólisisAna Valentina Espitia BaqueroÎncă nu există evaluări
- La FosfinaDocument9 paginiLa FosfinaJuan Gabriel Rojas SuarezÎncă nu există evaluări
- Tipos de Tuberias para Conduccion de Agua PotableDocument5 paginiTipos de Tuberias para Conduccion de Agua PotableDiego GomezÎncă nu există evaluări
- GUIA6-La Respiracion en Los Seres VivosDocument11 paginiGUIA6-La Respiracion en Los Seres VivosMaria Elena SaraviaÎncă nu există evaluări
- 2da Clase NEURONA Ultimo - PPT Ultimo Plus 2018Document39 pagini2da Clase NEURONA Ultimo - PPT Ultimo Plus 2018hpamela91Încă nu există evaluări
- Guia 5. Propiedades Quimicas de Los Carbohidratos - BQ1Document6 paginiGuia 5. Propiedades Quimicas de Los Carbohidratos - BQ1Laura AriasÎncă nu există evaluări
- US - ESPA - MONAT BOTANIC BAKUCHIOL - Infosheet - 112020 - V2Document2 paginiUS - ESPA - MONAT BOTANIC BAKUCHIOL - Infosheet - 112020 - V2chandra PearlÎncă nu există evaluări
- Que Son Los LípidosDocument3 paginiQue Son Los LípidosdomeÎncă nu există evaluări
- Actividad 9 - Integración Metabólica 1Document21 paginiActividad 9 - Integración Metabólica 1Tomas VillanuevaÎncă nu există evaluări
- CATÁLISISDocument20 paginiCATÁLISISsonia_fuenla_cloe31Încă nu există evaluări
- Práctica 10 Laboratorio de Química Orgánica 1Document3 paginiPráctica 10 Laboratorio de Química Orgánica 1CarlosArturoCruzCervantesÎncă nu există evaluări
- Enzimas Bacterianas Microbiologia 1Document22 paginiEnzimas Bacterianas Microbiologia 1Bismarck Sernaque CordovaÎncă nu există evaluări
- 209491Document92 pagini209491Mauricio Castañón100% (1)
- Analisis Bromatologico de Aceites y GrasasDocument6 paginiAnalisis Bromatologico de Aceites y GrasaslorenaÎncă nu există evaluări
- Semilla de AguacateDocument8 paginiSemilla de AguacateCesar MontañezÎncă nu există evaluări
- Semana 4 EnzimasDocument65 paginiSemana 4 EnzimasYassimÎncă nu există evaluări
- Reglamento Etiquetado PDFDocument12 paginiReglamento Etiquetado PDFDiego PantojaÎncă nu există evaluări
- Preguntas para EnviarDocument6 paginiPreguntas para EnviarJohanS.AcebedoÎncă nu există evaluări
- Diels-Alder RepDocument2 paginiDiels-Alder RepCrash TinocoÎncă nu există evaluări
- Cuestionario de Moleculares de La Herencia ANGEL GONZALEZDocument3 paginiCuestionario de Moleculares de La Herencia ANGEL GONZALEZDavid VelascoÎncă nu există evaluări