Documente Academic
Documente Profesional
Documente Cultură
Spectres D'émission de L'atome D'hydrogène Et de L'ion Hydro PDF
Încărcat de
AlaaEddineBoukhrisTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Spectres D'émission de L'atome D'hydrogène Et de L'ion Hydro PDF
Încărcat de
AlaaEddineBoukhrisDrepturi de autor:
Formate disponibile
Chimie
Spectres dmission de latome dhydrogne et de lion
hydrognode Li2+
Exercice III-2
Exercice III-2 : Spectres de l'atome d'hydrogne et de l'ion Li2+.
Enonc
1- Exprimer le nombre d'onde 1/ d'mission d'un atome d'hydrogne en fonction des nergies Ei et
Ej des niveaux entre lesquels s'effectue une transition.
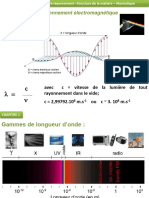
2- Calculer le nombre d'onde en cm-1 ainsi que les longueur d'onde en nm pour les raies extrmes de
chacune des deux premires sries (Lyman nj = 1, Balmer nj = 2).
3- Indiquer sur un axe gradu en longueurs d'onde, les domaines concerns pour chacune des sries,
leur position par rapport au visible (compris environ entre 400 nm et 750 nm).
4- Quelle est l'nergie du niveau le plus bas de l'ion Li2+ ?
5- Comparer le nombre d'onde de la raie situe le plus loin vers l'UV ( < 400 nm) dans le spectre
pour H et Li2+.
Page 1 Claude ANIES EduKlub S.A.
Tous droits de lauteur des uvres rservs. Sauf autorisation, la reproduction ainsi que toute utilisation des uvres autre que la
consultation individuelle et prive sont interdites.
Chimie
Spectres dmission de latome dhydrogne et de lion
hydrognode Li2+
Exercice III-2
Correction :
1- Le nombre donde est donn par la formule de Ritz qui se dduit des niveaux nergtiques de
lion hydrognode (lcart nergtique entre 2 niveaux est gal lnergie du photon mis ou
absorb) :
1 1 1
= R Ry 2 2 cf. cours : Atome d'Hydrogne et ion Hydrognode.
n nj
i
2- Pour la srie de Lyman, le niveau nergtique de retour est n = 1 ; les raies extrmes sont donc :
nj = 1 et ni = 2 pour la raie de plus faible nergie
et nj = 1 et ni = infini (niveau dionisation) pour la raie la plus nergtique
On en dduit que : 1/ = 0,822.105 cm-1 ;
Soit = 121,6 nm (raie la plus faible nergtiquement) ;
Et 1/ = 1,0962.105 cm-1 ;
Soit = 91,2 nm (raie la plus nergtique) ;
Pour la srie de Balmer, le niveau nergtique de retour est n = 2 ; les raies extrmes sont donc :
nj = 2 et ni = 3 pour la raie de plus faible nergie
et nj = 2 et ni = infini (niveau dionisation) pour la raie la plus nergtique
On en dduit que : 1/ = 1,5225.105 cm-1 ;
Soit = 656,8 nm (raie la plus faible nergtiquement) ;
et 1/ = 2,7405.105 cm-1 ;
Soit = 364,9 nm (raie la plus nergtique).
3- Pour la srie de Lyman, les raies sont mises dans l'UV lointain ; pour la srie de Balmer, elles
sont mises dans le visible.
4- Lnergie dnergie du niveau fondamental de lion hydrognode vaut :
2
Z
E fond = R Ry Li = - 122,4 eV (avec ZLi = 3 et n = 1).
n
5- On compare les nombres d'onde de la raie situe le plus loin vers l'UV, cest--dire des raies les
plus nergtiques (niveau dionisation) pour lhydrogne et Li2+. On a :
H: = 91,2 nm (1/ = 1,5225.105 cm-1) ;
Li2+ : = 10,1 nm (1/ = 9,8656.105 cm-1).
Page 2 Claude ANIES EduKlub S.A.
Tous droits de lauteur des uvres rservs. Sauf autorisation, la reproduction ainsi que toute utilisation des uvres autre que la
consultation individuelle et prive sont interdites.
S-ar putea să vă placă și
- Exercices de Physique Nucléaire et de la MatièreDe la EverandExercices de Physique Nucléaire et de la MatièreÎncă nu există evaluări
- Exercices d'Ondes, d'Optique et d'ÉlectromagnétismeDe la EverandExercices d'Ondes, d'Optique et d'ÉlectromagnétismeÎncă nu există evaluări
- PoteauDocument6 paginiPoteauAlaaEddineBoukhrisÎncă nu există evaluări
- Série N°3 - 2023 2024Document2 paginiSérie N°3 - 2023 2024ra kaÎncă nu există evaluări
- Fiche 2Document3 paginiFiche 2kbskevine8Încă nu există evaluări
- TD2 222Document2 paginiTD2 222Dô FlamîîngoÎncă nu există evaluări
- TD-2 AtomistiqueDocument3 paginiTD-2 AtomistiqueChaka TraoreÎncă nu există evaluări
- Excitation Et Ionisation de L'atome D'hydrogène PDFDocument2 paginiExcitation Et Ionisation de L'atome D'hydrogène PDFAlaaEddineBoukhrisÎncă nu există evaluări
- BCPST 1 - 2023 - Atomistique CHP IiDocument14 paginiBCPST 1 - 2023 - Atomistique CHP IiZie adama DiarrassoubaÎncă nu există evaluări
- Serie-1-2022-23 (1)Document8 paginiSerie-1-2022-23 (1)mariem OuriÎncă nu există evaluări
- TD2 (1)Document6 paginiTD2 (1)mlebguiraÎncă nu există evaluări
- Td-N-2-Chimie1-1-Aero 2015Document2 paginiTd-N-2-Chimie1-1-Aero 2015fasla100% (1)
- CH. II. Notions sur le LASER. LPA 2022Document31 paginiCH. II. Notions sur le LASER. LPA 2022sihamarbaz14Încă nu există evaluări
- 1 - Structure Électronique de L'atomeDocument11 pagini1 - Structure Électronique de L'atomeTaki EddineÎncă nu există evaluări
- Chapitre 4Document14 paginiChapitre 4Fleur MajkÎncă nu există evaluări
- Fiche TD Chim 1 - Atome de Bohr. M. OuaguedDocument2 paginiFiche TD Chim 1 - Atome de Bohr. M. OuaguedMehda RouÎncă nu există evaluări
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014)Document5 paginiDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014)AliMchirguiÎncă nu există evaluări
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2011-2012) MR BARHOUMIDocument4 paginiDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2011-2012) MR BARHOUMIMohamed SaidiÎncă nu există evaluări
- Cours Niveaux D Énergie 2022-23Document3 paginiCours Niveaux D Énergie 2022-23Moussa CISSEÎncă nu există evaluări
- Chimie1 - Chapitre 2Document6 paginiChimie1 - Chapitre 2inc onnueÎncă nu există evaluări
- Exercices Atome Et Mecanique de NewtonDocument4 paginiExercices Atome Et Mecanique de NewtonHAMADA1972Încă nu există evaluări
- PolycopiE Du Cours J Delaire Classification Periodique (2006-2007)Document11 paginiPolycopiE Du Cours J Delaire Classification Periodique (2006-2007)kamisnv2017Încă nu există evaluări
- Serie_2_2023-2024_SMDocument2 paginiSerie_2_2023-2024_SMcrbyounes123Încă nu există evaluări
- electrochimie[1]Document32 paginielectrochimie[1]hadil.23sd56Încă nu există evaluări
- Chap 1 TD Pour EtudiantsDocument4 paginiChap 1 TD Pour EtudiantsOnanda BouliÎncă nu există evaluări
- Fiche de TD N°4Document1 paginăFiche de TD N°4Madani Houssam .Încă nu există evaluări
- Struicture Model Atomique-1Document14 paginiStruicture Model Atomique-1Rostom KLÎncă nu există evaluări
- Chap 5 EtdexpDocument10 paginiChap 5 Etdexpfarid nanoÎncă nu există evaluări
- 2.le Spectre D'atome D'hydrogeneDocument7 pagini2.le Spectre D'atome D'hydrogeneMétatron Games100% (1)
- TD3 Structure - 12 - 13Document7 paginiTD3 Structure - 12 - 13sidi mohamed el amine nekkal100% (1)
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR FKIRI FAOUZIDocument4 paginiDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR FKIRI FAOUZIMohamed SaidiÎncă nu există evaluări
- PMC Chapitre 3 2021Document9 paginiPMC Chapitre 3 2021Tsirilalaina RamahandrisoaÎncă nu există evaluări
- Biophysique 2 RésuméComplet Morad Jari 1Document19 paginiBiophysique 2 RésuméComplet Morad Jari 1Ouu SsaamaÎncă nu există evaluări
- TD 3 Et 4 Chimie 1Document2 paginiTD 3 Et 4 Chimie 1bach nalÎncă nu există evaluări
- Devoir nc2b04Document2 paginiDevoir nc2b04Amadou Makhtar SeckÎncă nu există evaluări
- Spectres AtomiquesDocument35 paginiSpectres AtomiquesFarouk MessaoudÎncă nu există evaluări
- Chapitre III Structure Électronique de L'atome Partie 1Document11 paginiChapitre III Structure Électronique de L'atome Partie 1djafar.mokraneÎncă nu există evaluări
- Chimie 1 Chap3 (2) - 1Document8 paginiChimie 1 Chap3 (2) - 1Zehnouni AbderezakÎncă nu există evaluări
- Chapitre II Modèles Classiques de L'atome IMP 21 Oct 2021 ReduitDocument10 paginiChapitre II Modèles Classiques de L'atome IMP 21 Oct 2021 ReduitMonxef BlrÎncă nu există evaluări
- AutomatismeDocument7 paginiAutomatismeRzq BHÎncă nu există evaluări
- Chapitre 2Document59 paginiChapitre 2faye0% (1)
- Chimie StructuraleDocument28 paginiChimie Structuraleriadh01netÎncă nu există evaluări
- Structure de La Matière 2 PartieDocument19 paginiStructure de La Matière 2 PartiesafaÎncă nu există evaluări
- CC2 Chimie 1 2021-2022 - CorrDocument4 paginiCC2 Chimie 1 2021-2022 - Corrfleberre.balacÎncă nu există evaluări
- 2018-2019 Ie1Document2 pagini2018-2019 Ie1Eugene FoucherÎncă nu există evaluări
- Serie 2 AtomiqueDocument3 paginiSerie 2 AtomiqueAsma TmlghÎncă nu există evaluări
- Chapitre II Modele Classique de L - Atome TirDocument70 paginiChapitre II Modele Classique de L - Atome TirMonxef BlrÎncă nu există evaluări
- Chapitre 3 Spectroscopie AtomiqueDocument17 paginiChapitre 3 Spectroscopie AtomiqueZahiri MohanadÎncă nu există evaluări
- TE Atome Molécules Cours Chap3 2018 2019 PDFDocument13 paginiTE Atome Molécules Cours Chap3 2018 2019 PDFTabbaraÎncă nu există evaluări
- Chapitre IV Structure Électronique Des AtomesDocument14 paginiChapitre IV Structure Électronique Des Atomesشبكة العاب العرب / Arab Games NetworkÎncă nu există evaluări
- Cours 3Document26 paginiCours 3calvin gastaudÎncă nu există evaluări
- Chap1 SeriecDocument33 paginiChap1 SeriecsextansÎncă nu există evaluări
- Atmol PDFDocument9 paginiAtmol PDFfaslaÎncă nu există evaluări
- Leçon 6 Classification Quantitative Des Couples Oydant-RéducteurDocument4 paginiLeçon 6 Classification Quantitative Des Couples Oydant-RéducteurN'golo Ismaël CoulibalyÎncă nu există evaluări
- 5.atome de Bohr (DR - Boudiaf)Document16 pagini5.atome de Bohr (DR - Boudiaf)Neou Phors SoporsÎncă nu există evaluări
- TD1 AtomistiqueDocument2 paginiTD1 Atomistiquehayat KIRATEÎncă nu există evaluări
- Chapitre 3 Le Modèle Ondulatoire de L'atome Notion D'orbitaleDocument31 paginiChapitre 3 Le Modèle Ondulatoire de L'atome Notion D'orbitaleazeÎncă nu există evaluări
- C111 - Cours (Atomistique) (Chapitre 2)Document5 paginiC111 - Cours (Atomistique) (Chapitre 2)younescheldi119Încă nu există evaluări
- Niveaux D'énergie de L'atome - SunudaaraDocument6 paginiNiveaux D'énergie de L'atome - SunudaaraEder bienvenu Anago obaÎncă nu există evaluări
- E03T079A HistoriqueDocument1 paginăE03T079A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T083A HistoriqueDocument1 paginăE03T083A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T075A HistoriqueDocument1 paginăE03T075A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03t086a HistoriqueDocument1 paginăE03t086a HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T047A HistoriqueDocument1 paginăE03T047A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T022A HistoriqueDocument1 paginăE02T022A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T037A HistoriqueDocument1 paginăE02T037A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T039A HistoriqueDocument1 paginăE02T039A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T018A HistoriqueDocument1 paginăE02T018A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T062A HistoriqueDocument1 paginăE03T062A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T023A HistoriqueDocument1 paginăE02T023A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02t028a HistoriqueDocument1 paginăE02t028a HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T016A HistoriqueDocument1 paginăE02T016A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T007A HistDocument1 paginăE02T007A HistAlaaEddineBoukhrisÎncă nu există evaluări
- E02T011A HistoriqueDocument1 paginăE02T011A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T010A HistoriqueDocument1 paginăE02T010A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E01T033A HistoriqueDocument1 paginăE01T033A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T012A HistoriqueDocument1 paginăE02T012A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T003A HistoriqueDocument1 paginăE02T003A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T004A HistoriqueDocument1 paginăE02T004A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T005A HistoriqueDocument1 paginăE02T005A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- Fondation SuperficielleDocument4 paginiFondation SuperficielleAlaaEddineBoukhrisÎncă nu există evaluări
- E02T041A HistoriqueDocument1 paginăE02T041A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T004A HistoriqueDocument1 paginăE02T004A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02D106000A HistoriqueDocument1 paginăE02D106000A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E01I052A HistoriqueDocument1 paginăE01I052A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T038A HistoriqueDocument1 paginăE03T038A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E02T008A HistoriqueDocument1 paginăE02T008A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări
- E03T001A HistoriqueDocument1 paginăE03T001A HistoriqueAlaaEddineBoukhrisÎncă nu există evaluări

























![electrochimie[1]](https://imgv2-1-f.scribdassets.com/img/document/720456576/149x198/1ccb5c716c/1712362064?v=1)