Documente Academic
Documente Profesional
Documente Cultură
Destilación
Încărcat de
Jeniffer GonzálezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Destilación
Încărcat de
Jeniffer GonzálezDrepturi de autor:
Formate disponibile
INSTITUTO POLITCNICO NACIONAL
Escuela Superior de Ingeniera
Qumica e Industrias Extractivas
Departamento de Ingeniera Qumica Industrial
Academia de Operaciones Unitarias
Laboratorio de Introduccin a los Procesos de Separacin
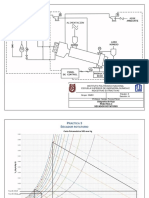
Prctica
Destilacin diferencial de una mezcla binaria
Gonzlez Alva Jeniffer Jocelyn
Equipo 3
Grupo: 3IM64 Semestre: 17-2
Cd. de Mxico a 31 de marzo de 2017
Laboratorio de Introduccin a los procesos de separacin
OBJETIVOS
Que el alumno al termino de las sesiones correspondientes al estudio de este equipo experimental
sea capaz de:
1. Comprender los conceptos fundamentales de esta operacin de separacin.
2. Explicar el funcionamiento del equipo de destilacin diferencial de una mezcla binaria ideal.
3. Llevar a cabo la destilacin de una mezcla binaria, en el destilador diferencial a presin
constante, comparando los resultados experimentales con los tericos calculados a partir de
la ecuacin de Rayleigh, observando as el rendimiento de destilacin por este mtodo.
INTRODUCCION
La destilacin continua es un proceso ininterrumpido en el cual se verifica la produccin de un flujo
continuo. El lquido o material orgnico que va a ser destilado puede ser introducido continuamente
en el alambique o cargado de una sola vez sin interrumpir la recogida del destilado.
Los mtodos de destilacin fraccionaria o continua son meramente descriptivos de los varios
procesos que ocurren, pudiendo ser todos incluidos en un nico sistema de destilacin.
Los sistemas profesionales de destilacin continua tienen aplicaciones evidentes en la produccin a
gran escala de alcohol con un elevado grado alcohlico, poseyendo un potencial ilimitado para
producir cualquier bebida alcohlica. El destilador aficionado puede probar a utilizar el alambique
charentais, una unidad completamente funcional y dotada de un bonito diseo. El Arrastre de Vapor
es un sistema de destilacin con mltiples propsitos debido a su versatilidad, pudiendo ser
utilizado para destilar bebidas espirituosas, aceites esenciales, extractos de plantas medicinales,
perfumes, agua de rosas, entre otros.
La destilacin es un mtodo que utiliza el principio de etapas de equilibrio para lograr la separacin
de una solucin. La facilidad de la separacin puede determinarse mediante el concepto de
volatilidad relativa, que se define como la relacin entre la composicin del componente A en el
vapor y en el lquido dividida en la relacin de la composicin de otro componente de referencia en
la fase vapor y el lquido.
Prctica Destilacin diferencial 2
Laboratorio de Introduccin a los procesos de separacin
Cuando el valor numrico de la volatilidad relativa es mayor a 1, la separacin es factible. Hay que
tener en cuenta que este parmetro es un valor que vara con la concentracin, aunque para
sistemas binarios que puedan ser modelados con la ley de Raoult la variacin es muy poca a
presin constante.
Es la operacin de separar, mediante calor, los diferentes componentes lquidos de una mezcla.
Una forma de destilacin, conocida desde la antigedad, es la obtencin
de alcohol aplicando calor a una mezcla fermentada.
El aparato utilizado para la destilacin es el alambique, que consta de un recipiente donde se
almacena la mezcla, a la que se le aplica calor, un condensador donde se enfran los vapores
generados, llevndolos de nuevo al estado lquido y un recipiente donde se almacena este lquido
concentrado.
En la industria qumica se utiliza la destilacin para la separacin de mezclas simples o complejas.
Una forma de clasificar la destilacin puede ser la de que sea discontinua o continua.
La destilacin discontinua se realiza introduciendo la mezcla en una caldera, donde se le
aplica calor y los vapores condensados se almacenan en un recipiente. La operacin de llenado de
la caldera con la mezcla hace que el proceso se realice en lotes. Un ejemplo sera la destilacin,
mediante alambique, del bagazo de la uva para la obtencin del orujo.
La destilacin continua, tambin llamada fraccionada, se basa en la alimentacin regulable y en
continuo de la mezcla a separar, introducindola en una columna o torre de destilacin, donde se
separan los componentes de una mezcla de forma continua en las distintas fracciones, saliendo por
la parte superior o cabeza la fraccin ms ligera o de menor punto de ebullicin, por el fondo la
fraccin ms pesada y a diferentes alturas de la columna, las distintas fracciones que se quieren
obtener dependiendo de su punto de ebullicin.
Un ejemplo de destilacin continua, fraccionada, sera la destilacin atmosfrica del petrleo.
En una instalacin de destilacin continua las composiciones de los productos separados
permanecen constantes en cada seccin de la columna, para lo cual se utilizan unas corrientes que
se denominan reflujos, que son recirculaciones de las propias extracciones, y aprovechando las
Prctica Destilacin diferencial 3
Laboratorio de Introduccin a los procesos de separacin
evaporaciones y condensaciones sucesivas de las extracciones, obteniendo productos destilados
de caractersticas definidas previamente.
TABLA DE DATOS EXPERIMENTALES.
SOLUCIONES z (cm) T(C) Vol. (lts) (g/cm3) %w Xmol
ALIMENTACION 38.6 20 32 0.960 21 0.13
DESTILADO 12 36 27.1 0.945 28 0.1794
RESIDUO 4 20 10.6 0.993 4 0.0229
CONDENSADOR 26.5 - - - - -
TABLA DE TEMPERATURAS.
Tinicial 20C
Tfinal 87C
TABLA DE EQUIPOS.
TANQUES DIAMETRO (cm). LONGITUD (cm).
ALIMENTACION 56 73
DESTILADO 31.5 58.5
RESIDUO 31.5 58.1
CONDENSADOR 38.5 -
Prctica Destilacin diferencial 4
Laboratorio de Introduccin a los procesos de separacin
1. Balance de materia
=+
= +
0.960 10003 1
= 32 ( 3
)( )( ) = .
1 1000
0.945 10003 1
= 27.1 ( ) ( ) ( ) = .
3 1 1000
0.993 10003 1
= 10.6 ( 3
)( )( ) = .
1 1000
Sustituyendo
29.76 = 25.704 + 10.5258
29.76 = 36.2298
0.21
= 32 = 0.13
0.21 (1 0.21)
+
32 18
0.28
= 32 = 0.1794
0.28 (1 0.28)
32 + 18
0.04
= 32 = 0.0229
0.04 (1 0.04)
32 + 18
Prctica Destilacin diferencial 5
Laboratorio de Introduccin a los procesos de separacin
= +
30.72(0.13) = .
25.6095(0.1794) + 10.52(0.0229) = .
Sustituyendo
3.9936 = 4.8352
2. Aplicando la ec. (14), obtener la relacin (D/F), y compararlo con el resultado de la ec.
(12)
= . . ()
25.6095 10.5258
= . = 1 = .
30.72 30.72
= . . ()
25.6095 0.13 0.0229
= . = = .
30.72 0.1794 0.0229
3. Relacin (F/W)
Aplicando la ecuacin anterior, se calcula la relacin F/W con las concentraciones de
equilibrio obtenidas a partir del diagrama de puntos de ebullicin con ayuda de las
temperaturas inicial y final de la destilacin. Considerar como un valor promedio entre
estas temperaturas
1 1
= . (10)
1
A B C
METANOL 8.0724 1574.99 238.8
AGUA 7.96681 1669.21 228.0
Prctica Destilacin diferencial 6
Laboratorio de Introduccin a los procesos de separacin
De la ecuacin de Antoine
B
log P A
C T
P=mmHg T=C
Para metanol:
1574.99
Log(1320.72) = 8.0724 -
230.00 + T
= 88.077
Para agua:
1669.21
Log(1320.72) = 7.96681-
228.00 + T
= 116.451
Pabs=Patm+Pman
Patm=585mmHg
Pman=1Kg/cm2=mmHg
Pabs=585+735.72= 1320.72 mmHg
T PA PB XA YA
88.077 1320.72 488.597 1.000 1.000
90 1414.35 525.856 0.8946 0.9580
95 1683.75 633.976 0.6541 0.8338
100 1993.9 759.983 0.4544 0.6860
105 2349.29 906.088 0.2873 0.5110
110 2754.71 1074.68 0.1464 0.3043
Prctica Destilacin diferencial 7
Laboratorio de Introduccin a los procesos de separacin
115 3215.23 1268.31 0.0269 0.0654
116.451 3359.94 1329.57 0.00 0.00
T vs XA, XB
120
115
110
105
Temperatura
100
XA
95 XB
90
85
80
-0.1 0.1 0.3 0.5 0.7 0.9 1.1
XA, XB
Entrando con 100 C se lee en el diagrama las composiciones de la mezcla binaria.
X=0.4544
Y=0.686
(1 )
=
(1 )
0.686(1 0.4544)
= = 2.6231
0.4544(1 0.686)
Sustituyendo
1 1
=
1
Prctica Destilacin diferencial 8
Laboratorio de Introduccin a los procesos de separacin
30.72 42.621 0.13 1 0.0229 2.6231
= 2.9185 = = 1.4137
10.5258 0.0229 1 0.13
Prctica Destilacin diferencial 9
S-ar putea să vă placă și
- Proceso de Elaboración de LevadurasDocument7 paginiProceso de Elaboración de LevadurasJeniffer GonzálezÎncă nu există evaluări
- Practica 5 TermoparDocument3 paginiPractica 5 TermoparJeniffer GonzálezÎncă nu există evaluări
- Practica 3 Diagrama y GraficaDocument2 paginiPractica 3 Diagrama y GraficaJeniffer GonzálezÎncă nu există evaluări
- Evaporador de Simple EfectoDocument4 paginiEvaporador de Simple EfectoJeniffer GonzálezÎncă nu există evaluări
- Historia y Evolución Del CoachingDocument28 paginiHistoria y Evolución Del CoachingJeniffer GonzálezÎncă nu există evaluări
- Transferencia de Calor. Práctica 1Document6 paginiTransferencia de Calor. Práctica 1Jeniffer GonzálezÎncă nu există evaluări
- Diagrama DescriptivoDocument1 paginăDiagrama DescriptivoJeniffer GonzálezÎncă nu există evaluări
- Practica Reflujo TotalDocument15 paginiPractica Reflujo TotalJeniffer GonzálezÎncă nu există evaluări
- Destilacion DiferencialDocument14 paginiDestilacion DiferencialJeniffer GonzálezÎncă nu există evaluări
- El Sutra Del LotoDocument9 paginiEl Sutra Del LotoAnalia Rosa BaiedÎncă nu există evaluări
- El Imperio Inca en Su Momento de Máxima ExpansiónDocument14 paginiEl Imperio Inca en Su Momento de Máxima Expansiónlina mejiaÎncă nu există evaluări
- BOE Convocatoria para La Rehabilitación Del Título de Marqués de CelaDocument2 paginiBOE Convocatoria para La Rehabilitación Del Título de Marqués de Celadanone1245Încă nu există evaluări
- Alteraciones Agudas de Las Transaminasas y ColestasisDocument13 paginiAlteraciones Agudas de Las Transaminasas y ColestasisAdrian CrespoÎncă nu există evaluări
- Cartilla de Junio 2do C de TecnologiaDocument12 paginiCartilla de Junio 2do C de Tecnologiamarina barriosÎncă nu există evaluări
- Manual: GasesDocument50 paginiManual: GasesRubén Mamani100% (1)
- Plus PotosiDocument59 paginiPlus Potosiedwin segoviaÎncă nu există evaluări
- Intubacion NasotraquialDocument99 paginiIntubacion NasotraquialJose Antonio Dominguez GalvanÎncă nu există evaluări
- Recombinación en PlantasDocument16 paginiRecombinación en Plantasruthp_40% (1)
- Prueba de Planos y Mapas 1ºDocument3 paginiPrueba de Planos y Mapas 1ºDaniela Castillo Saavedra100% (2)
- TIBITOCDocument12 paginiTIBITOCJimmyAlbertCardenasVargas0% (1)
- Soy Sontone - Memorias de Una Vida en AislamientoDocument144 paginiSoy Sontone - Memorias de Una Vida en AislamientoDavid Roca BasadreÎncă nu există evaluări
- Cantos A La Santisima Virgen MariaDocument5 paginiCantos A La Santisima Virgen MariakarenmvcÎncă nu există evaluări
- Resumen Tarea 4 Unidad3Document3 paginiResumen Tarea 4 Unidad3Saudy MezaÎncă nu există evaluări
- Lab 3 - CONSTRUCCION DEL VECTORÍMETRODocument4 paginiLab 3 - CONSTRUCCION DEL VECTORÍMETRORuth Maldonado100% (2)
- Lista de Verificación Crianza de PollosDocument1 paginăLista de Verificación Crianza de PollosTanya RubíÎncă nu există evaluări
- Sri CiuDocument372 paginiSri CiuAnonymous BUSFqHpÎncă nu există evaluări
- Escorrentía Acida en La MineríaDocument2 paginiEscorrentía Acida en La MineríaAngelJuniorVialetÎncă nu există evaluări
- Contrato de ArrendamientoDocument7 paginiContrato de Arrendamientotecnologicodelnorte plazaoasis100% (2)
- Auxiliar de Servicios GeneralesDocument2 paginiAuxiliar de Servicios GeneralesNihumar TimaureÎncă nu există evaluări
- Piratas - Bucaneros - Filibusteros - Corsarios en América-OkDocument325 paginiPiratas - Bucaneros - Filibusteros - Corsarios en América-OkFrancisco Javier ParedesÎncă nu există evaluări
- Análisis Por Métodos Espectroscópicos y Estudio Del Proceso de Envejecimiento de Aceites Esenciales de Cítricos PDFDocument321 paginiAnálisis Por Métodos Espectroscópicos y Estudio Del Proceso de Envejecimiento de Aceites Esenciales de Cítricos PDFMario MatuteÎncă nu există evaluări
- Cuestionarios Álgebra Geometría y TrigonometriaDocument37 paginiCuestionarios Álgebra Geometría y TrigonometriaWilmarMendozaÎncă nu există evaluări
- Plano de Jumbo DetallesDocument23 paginiPlano de Jumbo DetallesPedro Espinoza Huahuacondori100% (1)
- Levantamiento Observaciones EstructurasDocument8 paginiLevantamiento Observaciones EstructurasJosef Walter SosaÎncă nu există evaluări
- Examen Parcial Ciencias SocialesDocument4 paginiExamen Parcial Ciencias SocialesEnrique Najera GonzalezÎncă nu există evaluări
- Programacion Flota Nacional 17-04-2019Document54 paginiProgramacion Flota Nacional 17-04-2019Claudio Felipe Hernández BrunaÎncă nu există evaluări
- Ficha Tecnica Punzon de Marcar y CentrarDocument2 paginiFicha Tecnica Punzon de Marcar y Centrarvalentina alamosÎncă nu există evaluări
- Teorema de ParsevalDocument4 paginiTeorema de ParsevalNuñez Davila Edu100% (1)
- Érase Una Vez Una Hipótesis. VicencioDocument23 paginiÉrase Una Vez Una Hipótesis. VicencioAnonymous Nlno3ig100% (1)
- Recupera tu mente, reconquista tu vidaDe la EverandRecupera tu mente, reconquista tu vidaEvaluare: 5 din 5 stele5/5 (9)
- El poder del optimismo: Herramientas para vivir de forma más positivaDe la EverandEl poder del optimismo: Herramientas para vivir de forma más positivaEvaluare: 5 din 5 stele5/5 (16)
- Psicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaDe la EverandPsicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaEvaluare: 4.5 din 5 stele4.5/5 (766)
- Tus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadDe la EverandTus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadEvaluare: 4.5 din 5 stele4.5/5 (1834)
- DMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteDe la EverandDMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteEvaluare: 4.5 din 5 stele4.5/5 (19)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe la EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaEvaluare: 5 din 5 stele5/5 (203)
- Yo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)De la EverandYo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)Evaluare: 5 din 5 stele5/5 (9)
- Cómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaDe la EverandCómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaEvaluare: 5 din 5 stele5/5 (1875)
- Cómo Conversar Con Cualquier Persona: Mejora tus habilidades sociales, desarrolla tu carisma, domina las conversaciones triviales y conviértete en una persona sociable para hacer verdaderos amigos y construir relaciones significativas.De la EverandCómo Conversar Con Cualquier Persona: Mejora tus habilidades sociales, desarrolla tu carisma, domina las conversaciones triviales y conviértete en una persona sociable para hacer verdaderos amigos y construir relaciones significativas.Evaluare: 5 din 5 stele5/5 (54)
- Resetea tu mente. Descubre de lo que eres capazDe la EverandResetea tu mente. Descubre de lo que eres capazEvaluare: 5 din 5 stele5/5 (196)
- Homo antecessor: El nacimiento de una especieDe la EverandHomo antecessor: El nacimiento de una especieEvaluare: 5 din 5 stele5/5 (1)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe la EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceEvaluare: 5 din 5 stele5/5 (8)
- Las 6 necesidades de cada niño: Empoderar a padres e hijos a través de la ciencia de la conexiónDe la EverandLas 6 necesidades de cada niño: Empoderar a padres e hijos a través de la ciencia de la conexiónEvaluare: 4.5 din 5 stele4.5/5 (6)
- La violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaDe la EverandLa violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaEvaluare: 4 din 5 stele4/5 (2)
- La madre emocionalmente ausente: Como reconocer y sanar los efectos invisibles del abandono emocional infantilDe la EverandLa madre emocionalmente ausente: Como reconocer y sanar los efectos invisibles del abandono emocional infantilÎncă nu există evaluări