Documente Academic
Documente Profesional
Documente Cultură
Viscosita Gas
Încărcat de
antonio_delloste0 evaluări0% au considerat acest document util (0 voturi)
242 vizualizări6 pagini.
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest document.
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
242 vizualizări6 paginiViscosita Gas
Încărcat de
antonio_delloste.
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 6
Viscosit dei Gas
A) Alcuni valori di Viscosit di Gas
Viscosit di alcuni Gas (G = centipoise)
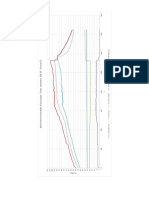
La viscosit pu essere ricavata con il nomogramma di Figura 1
Gas X Y Gas X Y
Acetico Acido 7,7 14,3 Freon-11 10,6 15,1
Acetone 8,9 13,0 Freon-12 11,1 16,0
Acqua 8,0 16,0 Freon-21 10,8 15,3
Acetilene 9,8 14,9 Freon-22 10,1 17,0
Ammoniaca 8,4 16,0 Freon-113 11,3 14,0
Aria 11,0 20,0 Idrogeno 11,2 12,4
Argon 10,5 22,4 3H2 + N2 11,2 17,2
Azoto 10,6 20,0 Idrogeno Bromuro 8,8 20,9
Benzene 8,5 13,2 Idrogeno Cloruro 8,8 18,7
Bromo 8,9 19,2 Idrogeno Cianuro 9,8 14,9
Butene 9,2 13,7 Idrogeno Ioduro 9,0 21,3
Butilene 8,9 13,0 Idrogeno Solfuro 8,6 18,0
Carbonio Biossido 9,5 18,7 Iodio 9,0 18,4
Carbonio Disolfuro 8,0 16,0 Mercurio 5,3 22,9
Carbonio Monossido 11,0 20,0 Metano 9,9 15,5
Cianogeno 9,2 15,2 Metil Alcol 8,5 15,6
Cicloesano 9,2 12,0 Nitrosile Cloruro 8,0 17,6
Cloro 9,0 18,4 Ossido Nitrico 10,9 20,5
Cloroformio 8,9 15,7 Ossido Nitroso 8,8 19,0
Elio 10,9 20,5 Ossigeno 11,0 21,3
Etano 9,1 14,5 Pentano 7,0 12,8
Esano (n) 8,6 11,8 Propano 9,7 12,9
Etil Acetato 8,5 13,2 Propil Alcol 8,4 13,4
Etil Alcol 9,2 14,2 Propilene 9,0 13,8
EtilCloruro 8,5 15,6 Solfuro Diossido 9,6 17,0
EtilEtere 8,9 13,0 Toluene 8,6 12,4
Etilene 9,5 15,1 2,3,3-TriMetilButano 9,5 10,5
Fluoro 7,3 23,8 Xeno 9,3 23,0
Perry J.H. Chemical Engineers Handbook 3d/4th/5th edition
McGraw-Hill Book Company, Inc.,New York, 1950/1963/1973
B) Metodi di Predizione
La viscosit di un Gas puro alla pressione di 1 ATA pu essere calcolata con
la seguente formula:
G = [1,286.MG1/2.PC2/3.TR]/[104] centipoise
G = Viscosit Gas centipoise
MG = Peso Molecolare Gas Kg/Kmole
PC = Pressione Critica Gas ATA
TR = Temperatura Ridotta Gas = T/TC Adimensionale
T = Temperatura Gas K
TC = Temperatura Critica Gas K
Una altra valutazione della viscosit di un Gas puro alla pressione di 1 ATA
pu essere cos ottenuta:
G = [33,3.(MG.TC)(1/2)].G /[VC2/3.104] centipoise
. .
G = [1,058.TR(0,645)]-0,261/[(1,9.TR)0,9 Log1,9 Tr]
(formula applicabile per TR > 0,3)
G = Viscosit Gas centipoise
MG = Peso Molecolare Gas Kg/Kmole
TC = Temperatura Critica Gas K
VC = Volume Critico Gas dm3/Kmole
TR = Temperatura Ridotta Gas = T/TC Adimensionale
T = Temperatura Gas K
Questa formula presenta una deviazione del 3% media e del 15% max
Una ulteriore valutazione della viscosit di un Gas puro o di una Miscela di
Gas pu essere ottenuta utilizzando il diagramma generalizzato di Fig.2
riportato da Hougen & Watson-Chemical Process Principles John Wiley & Sons
da cui noto il Valore della Viscosit Critica, Pressione Critica e
temperatura Critica pu essere ricavato il valore della viscosit a qualsiasi
altra pressione e temperatura.
G = c.R centipoise
G = Viscosit Gas centipoise
R = Viscosit Ridotta Gas (Hougen & Watson) Adimensionale
C = Viscosit Critica centipoise
PC = Pressione Critica Gas ATA
TC = Temperatura Critica Gas K
PR = Pressione Ridotta Gas = P/PC Adimensionale
P = Pressione Gas ATA
TR = Temperatura Ridotta Gas = T/TC Adimensionale
T = Temperatura Gas K
Il metodo di Hougen & Watson consente inoltre di estrapolare un valore di
viscosit noto ad una pressione e temperatura a qualsiasi altra pressione e
temperatura.
C) Variazione della viscosit con la Temperatura
Se noto un valore di viscosit G1 alla temperatura T1,si pu
conoscere un secondo valore G2 alla temperatura T2,usando la
seguente formula:
G2 = G1.[T2/T1)3/2.(T1+1,47.TB)]/[T2+1,47.TB)]
G = Viscosit Gas centipoise
T = Temperatura Gas K
TB = Temperatura normale di ebollizione K
La metodologia di Hougen & Watson riportata al punto B consente il
calcolo della viscosit a qualsiasi temperatura.
Il metodo di Hougen & Watson consente inoltre di estrapolare un
valore di viscosit noto ad una pressione e temperatura a
qualsiasi altra pressione e temperatura.
D) Variazione della viscosit con la Pressione
La metodologia di Hougen & Watson riportata al punto B consente il
calcolo della viscosit a qualsiasi Pressione.
Il metodo di Hougen & Watson consente inoltre di estrapolare un
valore di viscosit noto ad una pressione e temperatura a
qualsiasi altra pressione e temperatura.
E) Miscele di Gas
GM = [YiMi1/2Gi]/[YiMi1/2]
dove:
Yi = frazione molare del Componente i
Gi = viscosit del componente i
sommatoria = [Y1.M1(1/2). G1+...+YN.MN1/2.GN)]/[Y1.M1(1/2)+...+YN.MN1/2]
Questa formula accurata al 2-3% con leccezione di miscele
contenenti idrogeno per le quali lapprossimazione pu raggiungere
il 10% per bassi contenuti di idrogeno ed il 25% per contenuti di
idrogeno pari al 25%.
Una ulteriore valutazione della viscosit di una Miscela di Gas
pu essere ottenuta utilizzando il diagramma generalizzato di
Fig.2 riportato da Hougen & Watson Chemical Process Principles
John Wiley & Sons da cui noto il Valore della Viscosit Critica,
Pressione Critica e temperatura Critica dei componenti la miscela
di gas pu essere ricavato il valore della viscosit della miscela
di Gas a qualsiasi altra pressione e temperatura.
GM = cM.RM centipoise
GM = Viscosit Miscela Gas centipoise
RM = Viscosit PseudoRidotta Gas(Hougen & Watson ) Adimensionale
CM = Viscosit PseudoCritica Miscela Gas centipoise
PCM = Pressione PseudoCritica Miscela Gas ATA
TCM = Temperatura PseudoCritica Miscela Gas K
PRM = Pressione PseudoRidotta Gas = P/PCM Adimensionale
P = Pressione Miscela Gas ATA
TRM = Temperatura PseudoRidotta Gas = T/TCM Adimensionale
T = Temperatura Miscela Gas K
TCM = [YiTCi]
PCM = [YiPCi]
dove: Yi = frazione molare del Componente i
TCi = Temperatura Critica del componente i
= sommatoria = [Y1.TC1+...+YN. YN.TCN]
PCi = Temperatura Critica del componente i
= sommatoria = [Y1.PC1+...+YN.PCN]
Il metodo di Hougen & Watson consente inoltre di estrapolare un
valore di viscosit noto ad una pressione e temperatura a
qualsiasi altra pressione e temperatura.
Figura 1
Costanti Critiche
Temperatura(Tc) Pressione(Pc) Conducibilit(Kc) Viscosit(c)
Tc Pc Kc c
SOSTANZA (C) (Ata) (Kcal/mhC) (cp)
Acetone 229,5 48,5 0,0596 0,0286
Acetilene 36,0 63,7 0,0506 0,0236
Acido Cloridrico 51,4 84,4 0,0387 0,0356
Acido Cianidrico 183,5 51,6 0,0604 0,0319
Acqua 374,0 225,6 0,1302 0,0497
Aria -140,5 38,5 0,0246 0,0194
Ammoniaca 132,0 115,3 0,0909 0,0311
Anidride Carbonica 31,0 75,4 0,0363 0,0344
Anidride solforosa 157,0 80,4 0,0354 0,0414
Argo -122,0 49,7 0,0202 0,0264
Azoto -147,0 34,6 0,0234 0,0181
Benzene 288,5 50,2 0,0635 0,0314
n-Butano 153,0 37,2 0,0566 0,0239
Ossido di Carbonio -139,0 36,2 0,0271 0,0189
Cloroformio 263,0 55,6 0,0335 0,0408
Cicloesano 281,0 41,8 0,0750 0,0286
Etano 32,0 49,8 0,0432 0,0211
Etilacetato 251,2 39,0 0,0644 0,0303
Etilcloruro 187,0 53,8 0,0563 0,0347
Etiletere 193,8 36,7 0,0627 0,0269
Etilene 9,9 52,2 0,0411 0,0214
Elio -268,1 2,3 0,0131 0,0026
n-Esano 234,5 31,0 0,0673 0,0247
Idrogeno -240,0 13,2 0,0545 0,0035
Isobutano 135,0 37,2 0,0566 0,0239
Isopentano 188,0 34,0 0,0607 0,0239
Isopropanolo 235,0 54,7 0,0732 0,0297
Kripto -63,0 55,9 0,0137 0,0397
Metano -82,0 47,4 0,0424 0,0161
Metanolo 240,0 81,3 0,0923 0,0375
Metilcloruro 143,1 68,0 0,0405 0,0339
Neon -228,7 26,8 0,0185 0,0158
Ossido Azoto (NO) -94,0 67,1 0,0348 0,0256
Ossigeno -119,0 51,4 0,0296 0,0253
Protossido Azoto (N2O) 36,5 74,0 0,0394 0,0331
n-Pentano 196,5 34,5 0,0619 0,0239
Propano 96,5 43,4 0,0510 0,0228
Propilene 91,5 46,9 0,0472 0,0231
Toluene 321,0 41,5 0,0680 0,0306
Xeno 16,6 60,2 0,0119 0,0492
FIGURA 2
Bibliografia: Petr. Ref. Vol. 32, Giugno 1953, pag. 127
BIBLIOGRAFIA
Perry. Chemical Engineers Handbook
Gallant. Phisical Properties of Hydrocarbons
Reid, Prausnitz, Sherwood. The Properties of Gases and Liquids
Tredici. Impianti Chimici I
Hougen & Watson. Chemical Process PrinciplesJohn Wiley & Sons
S-ar putea să vă placă și
- SOLUZIONI COMPITO A CHIMICA 16-01-2012 (Univaq - Rossi)Document9 paginiSOLUZIONI COMPITO A CHIMICA 16-01-2012 (Univaq - Rossi)Aldo NardiÎncă nu există evaluări
- Chimica - Redox e BiochimicaDocument12 paginiChimica - Redox e BiochimicaPaolo D'AlessandroÎncă nu există evaluări
- Conducibilita Termica GasDocument4 paginiConducibilita Termica GasFerruccio RossiÎncă nu există evaluări
- TOC eDocument7 paginiTOC euffaaa1985Încă nu există evaluări
- Cap07 Tabella Entalpia-2 PDFDocument2 paginiCap07 Tabella Entalpia-2 PDFpippo2378793Încă nu există evaluări
- Codici G e M ISODocument2 paginiCodici G e M ISOCIAOOOOÎncă nu există evaluări
- Manuale Tecnico Stufe 5 Marzo 07Document45 paginiManuale Tecnico Stufe 5 Marzo 07MarinoÎncă nu există evaluări
- Dati Uni 11300 - Ehs TDM PlusDocument47 paginiDati Uni 11300 - Ehs TDM PlusGuidolol0% (1)
- MappeDocument13 paginiMappenet_phantomÎncă nu există evaluări
- Qubix Guida Alla Videosorveglianza IpDocument40 paginiQubix Guida Alla Videosorveglianza IpAlberto AlbergamoÎncă nu există evaluări
- Impianti Meccanici CompletoDocument78 paginiImpianti Meccanici CompletoMichele AssirelliÎncă nu există evaluări
- Diagrammi HeislerDocument26 paginiDiagrammi HeislerGiulio Milani100% (1)
- DATI UNI 11300 - EHS TDM Plus Senza Climate HubDocument6 paginiDATI UNI 11300 - EHS TDM Plus Senza Climate HubGuidololÎncă nu există evaluări
- Caratteristiche Biomassa LegnosaDocument30 paginiCaratteristiche Biomassa LegnosaMarco BertiÎncă nu există evaluări
- Econcept 15 A - 25 A - 35 A 06.2Document44 paginiEconcept 15 A - 25 A - 35 A 06.2Cristian CatarosÎncă nu există evaluări
- Dispensa Di Chimica Analitica StrumentaleDocument132 paginiDispensa Di Chimica Analitica StrumentalePinoÎncă nu există evaluări
- POTENZIOMETRIADocument71 paginiPOTENZIOMETRIAAniello LangellaÎncă nu există evaluări
- Tabelle Leghe AlDocument4 paginiTabelle Leghe AlEric Cocks100% (1)
- Diagrammi Di Flusso - Simboli e Attributi Nello Schema P&IDDocument5 paginiDiagrammi Di Flusso - Simboli e Attributi Nello Schema P&IDpasqualeÎncă nu există evaluări
- Encclopedia Degli Idrocarburi - Alchilazione - Cap 4 - 3Document12 paginiEncclopedia Degli Idrocarburi - Alchilazione - Cap 4 - 3MasterPie1950Încă nu există evaluări
- BIASI - Radiatori in Ghisa LBTDocument1 paginăBIASI - Radiatori in Ghisa LBTSerena D'angeloÎncă nu există evaluări
- Diagramma Di MollierDocument3 paginiDiagramma Di Mollierwilliam50% (2)
- Consumo Di AcsDocument18 paginiConsumo Di AcsLuca SonnoÎncă nu există evaluări
- Libretto Cerastar ZWE 24-28-4 HADocument40 paginiLibretto Cerastar ZWE 24-28-4 HAFrancescoÎncă nu există evaluări
- Impianti Meccanici Dispense Dimensionamento PDFDocument202 paginiImpianti Meccanici Dispense Dimensionamento PDFAnonymous kTLYjoBqÎncă nu există evaluări
- Esercizi RedoxDocument2 paginiEsercizi RedoxevaÎncă nu există evaluări
- Libri Primo Anno IngDocument1 paginăLibri Primo Anno IngFabio PolimiÎncă nu există evaluări
- Eserciziario - Compito 2a ParteDocument2 paginiEserciziario - Compito 2a ParteVincenzoABrunoÎncă nu există evaluări
- Linee Guida ElaboratiDocument5 paginiLinee Guida ElaboratiEmanuele PanzettaÎncă nu există evaluări
- Tariffe Professionali v1.1Document4 paginiTariffe Professionali v1.1Roberto TrunfioÎncă nu există evaluări
- Esempio Di Calcolo - Tettoia in LegnoDocument26 paginiEsempio Di Calcolo - Tettoia in LegnoAle85toÎncă nu există evaluări
- PallinometroDocument12 paginiPallinometrobipla BiplaÎncă nu există evaluări
- Norme Sulla Protezione Catodica Ad Anodi Sacrificali (Correnti Vaganti)Document9 paginiNorme Sulla Protezione Catodica Ad Anodi Sacrificali (Correnti Vaganti)Fabrizio BocchettiÎncă nu există evaluări
- Viscosita Gas PDFDocument6 paginiViscosita Gas PDFBonifacioPalmieriÎncă nu există evaluări
- Viscosità Dei Gas Tabella 1 - Process Engineering ManualDocument7 paginiViscosità Dei Gas Tabella 1 - Process Engineering ManualFabioSalaÎncă nu există evaluări
- Termodinamica CombustioneDocument31 paginiTermodinamica CombustioneStefano ValerioÎncă nu există evaluări
- Richiami TermodinamicaDocument16 paginiRichiami TermodinamicaRei HoxhaÎncă nu există evaluări
- ChimicaDocument75 paginiChimicandemanouÎncă nu există evaluări
- Viscosita LiquidiDocument9 paginiViscosita LiquidifabrcadÎncă nu există evaluări
- Dati Fisica TecnicaDocument42 paginiDati Fisica Tecnicaglicinedelcosmo22Încă nu există evaluări
- Imv RHRGDocument10 paginiImv RHRGlittlecheersÎncă nu există evaluări
- La Legge Di StevinoDocument4 paginiLa Legge Di StevinoSofia PeroloÎncă nu există evaluări
- EsempioDocument5 paginiEsempioDavide MartiniccaÎncă nu există evaluări
- Manuale vb188Document6 paginiManuale vb188theswingineerÎncă nu există evaluări
- CP Gas CombustiDocument6 paginiCP Gas CombustiFerruccio RossiÎncă nu există evaluări
- 061 066 TolleranzeDocument6 pagini061 066 TolleranzeiceschelÎncă nu există evaluări
- Esercitazione - Combustibili - 1 (Modalità Compatibilità) PDFDocument29 paginiEsercitazione - Combustibili - 1 (Modalità Compatibilità) PDFGianluca SantagataÎncă nu există evaluări
- Tut CfaDocument42 paginiTut CfaGustavoCiaccoÎncă nu există evaluări
- Practica 2 Termodinamica Del Equilibrio QuimicoDocument6 paginiPractica 2 Termodinamica Del Equilibrio QuimicoDiego SeCe100% (1)
- Relazione Costante Di TempoDocument7 paginiRelazione Costante Di TempoSimone Di NittoÎncă nu există evaluări
- Relazione Costante Di TempoDocument7 paginiRelazione Costante Di TempoSimone Di NittoÎncă nu există evaluări
- Perchè CP Medio in Camera Combustione - (Vedi Parte Gialla)Document2 paginiPerchè CP Medio in Camera Combustione - (Vedi Parte Gialla)DavideÎncă nu există evaluări
- BTU Calculater 1Document3 paginiBTU Calculater 1Михаил ПолковниковÎncă nu există evaluări
- Lo Stato GassosoDocument22 paginiLo Stato GassosoChi PuòessereÎncă nu există evaluări
- Parametri Geometrici e Statici Per Sezioni Piane ComuniDocument22 paginiParametri Geometrici e Statici Per Sezioni Piane Comunic_passerino6572Încă nu există evaluări
- Calcinazione DolomiteDocument13 paginiCalcinazione DolomiteLucaÎncă nu există evaluări
- Densita LiquidiDocument6 paginiDensita LiquidiPaolo BianchiÎncă nu există evaluări
- Microgenus 23 MffiDocument17 paginiMicrogenus 23 MffiAndrea ButtafavaÎncă nu există evaluări
- CineticaDocument4 paginiCineticaRoberto SchimmentiÎncă nu există evaluări
- Determinare Il Tipo Di Vapore Prodotto Dai Seguenti DatiDocument2 paginiDeterminare Il Tipo Di Vapore Prodotto Dai Seguenti DatiMiriam IzzilloÎncă nu există evaluări
- F1 Bnim0001 173254221Document1 paginăF1 Bnim0001 173254221antonio_dellosteÎncă nu există evaluări
- INSGEG01Document206 paginiINSGEG01antonio_dellosteÎncă nu există evaluări
- Modalità Di Pagamento Del Servizio Di PrevenzioneDocument1 paginăModalità Di Pagamento Del Servizio Di Prevenzioneantonio_dellosteÎncă nu există evaluări
- 5-Faccini Atex BisDocument34 pagini5-Faccini Atex Bisantonio_dellosteÎncă nu există evaluări
- Bio3-04 12Document33 paginiBio3-04 12antonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 173279276Document1 paginăA F1 Bnim0001 173279276antonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172952776Document1 paginăA F1 Bnim0001 172952776antonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172636825Document1 paginăA F1 Bnim0001 172636825antonio_dellosteÎncă nu există evaluări
- Cattedre Orario Esterne - Organico Di Diritto Scuola Sec. Ii GradoDocument55 paginiCattedre Orario Esterne - Organico Di Diritto Scuola Sec. Ii Gradoantonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172986552Document1 paginăA F1 Bnim0001 172986552antonio_dellosteÎncă nu există evaluări
- VI-Technical Description E-53-Rev001ger-itaDocument19 paginiVI-Technical Description E-53-Rev001ger-itaantonio_dellosteÎncă nu există evaluări
- Specifica-Tecnica-Cabina Primaria StandardDocument67 paginiSpecifica-Tecnica-Cabina Primaria Standardantonio_delloste100% (4)
- ADocument3 paginiAantonio_dellosteÎncă nu există evaluări
- ADocument3 paginiAantonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172834129Document1 paginăA F1 Bnim0001 172834129antonio_dellosteÎncă nu există evaluări
- Bnim0001 172821608Document1 paginăBnim0001 172821608antonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172798623Document1 paginăA F1 Bnim0001 172798623antonio_dellosteÎncă nu există evaluări
- Assevearzione Ai Fini Della Sicurezza AntincendioDocument3 paginiAssevearzione Ai Fini Della Sicurezza Antincendioantonio_dellosteÎncă nu există evaluări
- A F1 Bnim0001 172727463Document1 paginăA F1 Bnim0001 172727463antonio_dellosteÎncă nu există evaluări
- Linee Guida Di Orientamento Prevenzione e Contrasto Dei Fenomeni Di Bullismo e CyberbullismoDocument16 paginiLinee Guida Di Orientamento Prevenzione e Contrasto Dei Fenomeni Di Bullismo e Cyberbullismogiovanna balconiÎncă nu există evaluări
- Modalità Di Pagamento Del Servizio Di PrevenzioneDocument1 paginăModalità Di Pagamento Del Servizio Di Prevenzioneantonio_dellosteÎncă nu există evaluări
- Convocazione Dipartimenti SecondariaDocument1 paginăConvocazione Dipartimenti Secondariaantonio_dellosteÎncă nu există evaluări
- MANUALE AGM - 2 - Ita PDFDocument15 paginiMANUALE AGM - 2 - Ita PDFalessandroleonardiÎncă nu există evaluări
- M - Pi - AOODRCA.REGISTRO UFFICIALE (U) .0013516.13-04-2021Document1 paginăM - Pi - AOODRCA.REGISTRO UFFICIALE (U) .0013516.13-04-2021antonio_dellosteÎncă nu există evaluări
- Modalità Di Presentazione Delle PraticheDocument2 paginiModalità Di Presentazione Delle Praticheantonio_dellosteÎncă nu există evaluări
- Segnalazione Certificata Di Inizio AttivitàDocument3 paginiSegnalazione Certificata Di Inizio Attivitàantonio_dellosteÎncă nu există evaluări
- Collegamento Autostradale Di Connessione Tra Le Citta' Di Brescia E MilanoDocument60 paginiCollegamento Autostradale Di Connessione Tra Le Citta' Di Brescia E Milanoantonio_dellosteÎncă nu există evaluări
- Dichiarazione Di Non Aggravio Del Rischio IncendioDocument2 paginiDichiarazione Di Non Aggravio Del Rischio Incendioantonio_dellosteÎncă nu există evaluări
- All 3-LineaMTDocument41 paginiAll 3-LineaMTantonio_dellosteÎncă nu există evaluări
- Bio3-04 12Document33 paginiBio3-04 12antonio_dellosteÎncă nu există evaluări
- 1010 Haertha Nitrurazione Al Plasma PDFDocument2 pagini1010 Haertha Nitrurazione Al Plasma PDFiceschelÎncă nu există evaluări
- Curve Caratteristiche PompeDocument18 paginiCurve Caratteristiche PompeTommasoDominato100% (1)
- Scambiatori 4Document26 paginiScambiatori 4Alessio O'ConnellÎncă nu există evaluări
- Uni 8290Document3 paginiUni 8290Antonio SpagnoloÎncă nu există evaluări
- La Cronistoria Di Ato e Aca Sullo Scandalo Dell'acqua AvvelenataDocument45 paginiLa Cronistoria Di Ato e Aca Sullo Scandalo Dell'acqua AvvelenataPrimaDaNoi.itÎncă nu există evaluări