Documente Academic
Documente Profesional
Documente Cultură
Bitacora 3
Încărcat de
Dani CrTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Bitacora 3
Încărcat de
Dani CrDrepturi de autor:
Formate disponibile
Bitcora
PRECIPITACIN, SEPARACIN Y PUNTO ISOELCTRICO DE PROTEINAS
OBJETIVO
Analiza el efecto que produce la modificacin de factores fisicoqumicos sobre la solubilidad de las
protenas y determinar el punto isoelctrico de la insulina, basndose en sus propiedades de
solubilidad a diferentes valores de ph.
INTRODUCCION
La multiplicidad de grupos cidos y bsicos de una protena hace que su solubilidad dependa de las
concentraciones de las sales disueltas, la constante dielctrica del disolvente, pH y temperatura.
Algunas protenas precipitan en condiciones en que otras an no estn bastante solubles. Este
efecto debe usarse como base para la purificacin proteica.
Efecto de la solubilidad de una protena.
La solubilidad de una protena en solucin acuosa es sensible a las concentraciones de sales
disueltas. La concentracin salina se puede expresar en trminos de fuerza inica, esta ltima se
define como:
La solubilidad de una protena a una determinada fuerza inica vara con las clases de iones en
solucin. El orden de eficacia de los distintos iones en cuanto a su influencia sobre la solubilidad
proteica es bastante similar para las diferentes protenas y parece deberse en primer trmino al
tamao y la hidratacin del in.
La solubilidad de una protena a baja fuerza inica se incrementa por lo general con la
concentracin salina. La explicacin del fenmeno salting in (incremento dela solubilidad por
sales), es que a medida que se incrementa la concentracin salina de la solucin proteica, los
contraiones adicionales recubren con mayor eficacia las numerosas cargas inicas de la molcula
de protena. Con lo que se incrementa la solubilidad de la protena. A fuerzas inicas elevadas se
reduce la solubilidad de las protenas, como la mayora de las sustancias. Este efecto conocido
como Salting out (reduccin de solubilidad por sales) es por la competencia por las molculas que
interactan entre los iones salinos agregados y los otros solutos disueltos.
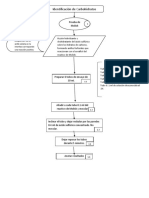
Diagrama de flujo de los procedimientos:
Bitcora
I. Colocar 6 ml de clara de huevo y 6 Agitar y filtrar durante
Biuret ml de sulfato de amonio. 15 min.
Suspender el precipitado en 2 Tomar 1 ml de el filtrado Tomar otra muestra,
ml de H2O y hacer reaccion de anterior y hacer reaccion de hacer la misma reaccin
biuret. biuret. y agregar sulfato de
amonio slido.
II Tubo 1
Filtrar 15 min y al
filtado volver a hacer la Efecto de ph y Aadir clara de huevo a un
misma reaccin. disolventes. tubo de ensaye +1 ml de HCL+
etanol 3ml.
Tubo 3
Tubo 2
Aadir clara de hevo+ 1 ml de
Aadir clara de huevo + 1 ml de hidroxido
regulador de acetatos+ 3ml de
de sodio+ 3 ml de etanol.
etanol.
Tubo1: Clara de huevo+.25 de cloruro de
III mercurio
Precipitacin por metales Tubo 2 :clara de huevo+.25 denitrato de plata.
pesados. Tubo 3: clara de huevo +.25 de acetato de
plomo
Tubo 4:clara de huevo+.25 de cloruro de
IV
bario. Preparar 5 tubos
Punto isoelctrico de la
Tubo 5: clara de huevo +.25 de cloruro de como se indica en la
Insulina.
sodio tabla.
Bitcora
Bibliografa consultada:
S-ar putea să vă placă și
- Precipitación ProteinasDocument4 paginiPrecipitación ProteinasvaleÎncă nu există evaluări
- BQ02 Laboratorio IDocument4 paginiBQ02 Laboratorio IMarlon Sneyder Vera CamargoÎncă nu există evaluări
- AlbuminaDocument5 paginiAlbuminarossy tello0% (3)
- Reporte 5 Bioquimica Precipitacion de ProteinasDocument10 paginiReporte 5 Bioquimica Precipitacion de ProteinasMaria Barreras100% (1)
- Bioquimica Final 3 ParcialDocument13 paginiBioquimica Final 3 ParcialRaquel MorrugaresÎncă nu există evaluări
- Bitacora 3Document6 paginiBitacora 3Yeshua CastañedaÎncă nu există evaluări
- Determinación Cuantitativa de ProteínasDocument13 paginiDeterminación Cuantitativa de ProteínasRaquel MorrugaresÎncă nu există evaluări
- Practicaproteinas 4Document3 paginiPracticaproteinas 4Lina María López RodríguezÎncă nu există evaluări
- Informe 4Document6 paginiInforme 4AngelaÎncă nu există evaluări
- Analisis de Proteinas de La Clara de HuevoDocument9 paginiAnalisis de Proteinas de La Clara de HuevoChiqui Lulu50% (2)
- Protocolo de BiomoléculasDocument2 paginiProtocolo de BiomoléculasPamela Tais Arroyo VargasÎncă nu există evaluări
- Informe Propiedades Fisicoquimicas de Las ProteinasDocument7 paginiInforme Propiedades Fisicoquimicas de Las ProteinasJose HernandezÎncă nu există evaluări
- Practica 1. Determinacion de Carbohidratos. BioquimicaDocument6 paginiPractica 1. Determinacion de Carbohidratos. BioquimicaDali MuñozÎncă nu există evaluări
- 4° Informe - Proteínas y AminoácidosDocument14 pagini4° Informe - Proteínas y AminoácidosMaira liset Arista mamaniÎncă nu există evaluări
- Práctica 5Document10 paginiPráctica 5Anais Lucero Zambrano PortillaÎncă nu există evaluări
- Determinación de Proteínas CrudaDocument4 paginiDeterminación de Proteínas CrudaRuth IbarrsÎncă nu există evaluări
- Informe Practica 3 Laboratorio de BioquimicaDocument15 paginiInforme Practica 3 Laboratorio de Bioquimicamirian puertasÎncă nu există evaluări
- Desnaturalizacion de ProteinasDocument12 paginiDesnaturalizacion de ProteinasMayra Vásquez100% (1)
- Reacción AmilasaDocument1 paginăReacción Amilasaarianaqc04Încă nu există evaluări
- Informe - ProteinasDocument8 paginiInforme - ProteinasCintia Azucena Villanueva EstacioÎncă nu există evaluări
- Practicas de Bioquimica Quimica - 5 - 11Document13 paginiPracticas de Bioquimica Quimica - 5 - 11FREILEN BRAYAN HUANCA CUSIÎncă nu există evaluări
- Informe Bioquimica 1.Document11 paginiInforme Bioquimica 1.chelsy lozanoÎncă nu există evaluări
- Practica #04 Reconocimiento de Actividad Enzimatica Lab MicrobiologiaDocument9 paginiPractica #04 Reconocimiento de Actividad Enzimatica Lab MicrobiologiaAna Fernanda JáureguiÎncă nu există evaluări
- Informe N°04 - Proteínas - IDocument8 paginiInforme N°04 - Proteínas - IDenisse Aracely Usecca CondoriÎncă nu există evaluări
- Práctica 4. Precipitación de Proteínas LAB. BIOQUIMICADocument6 paginiPráctica 4. Precipitación de Proteínas LAB. BIOQUIMICAFernanda Araiza100% (1)
- Informe 2Document11 paginiInforme 2Pedro SanchesÎncă nu există evaluări
- PRACTICA 3 ProteínasDocument3 paginiPRACTICA 3 ProteínasAna Carolina LozanoÎncă nu există evaluări
- PRACTICA 3 ProteinasDocument3 paginiPRACTICA 3 Proteinasmaria fernanda borja ballesterosÎncă nu există evaluări
- INF MetabolismoDocument7 paginiINF MetabolismoIsabela ForeroÎncă nu există evaluări
- JP-Semana 3 - Reconocimiento de Carbohidratos y LipidosDocument6 paginiJP-Semana 3 - Reconocimiento de Carbohidratos y LipidosMilagros ContrerasÎncă nu există evaluări
- p6. Cinética EnzimáticaDocument4 paginip6. Cinética EnzimáticaNORA PILAR NINAJA MAMANIÎncă nu există evaluări
- GUIADocument17 paginiGUIAJulian DavidÎncă nu există evaluări
- Práctica N°08 de AlbúminaDocument20 paginiPráctica N°08 de AlbúminaFrancisco LazoÎncă nu există evaluări
- Pract 06 Biol EmvzDocument3 paginiPract 06 Biol EmvzElmer AlaniaÎncă nu există evaluări
- Practica N 4Document5 paginiPractica N 4Narro Chigne A. HugoÎncă nu există evaluări
- Diagrama de Flujo Práctica 3Document3 paginiDiagrama de Flujo Práctica 3Diana CarranzaÎncă nu există evaluări
- Diagrama de Flujo Práctica 3Document3 paginiDiagrama de Flujo Práctica 3Diana CarranzaÎncă nu există evaluări
- Informe Biologia de ProteinasDocument12 paginiInforme Biologia de ProteinaswiliansÎncă nu există evaluări
- Accion EnzimaticaDocument14 paginiAccion Enzimaticainter celÎncă nu există evaluări
- Oxidación Con Reactivo de FehlingDocument1 paginăOxidación Con Reactivo de Fehlingfarid garcia (superfarid666)Încă nu există evaluări
- Laboratorio N°7 - ProteínasDocument4 paginiLaboratorio N°7 - ProteínaseleazarÎncă nu există evaluări
- Propiedades Fisicoquimicas de Las ProteinasDocument13 paginiPropiedades Fisicoquimicas de Las ProteinasLaura MejiaÎncă nu există evaluări
- Informe #2 BioquímicaDocument20 paginiInforme #2 Bioquímicadeivy alvarezÎncă nu există evaluări
- Ensayo de ProteinasDocument6 paginiEnsayo de ProteinasLucía YánezÎncă nu există evaluări
- Mapa 6Document1 paginăMapa 6Isaias PerdomoÎncă nu există evaluări
- Lab N°03-BiologiaDocument14 paginiLab N°03-BiologiaALBERTO ROMERO0% (2)
- ProteínasDocument8 paginiProteínasSelena FigueroaÎncă nu există evaluări
- Desnaturalización de La AlbúminaDocument16 paginiDesnaturalización de La AlbúminaClaudia Montoya Salazar100% (1)
- Informe Práctica 2 BioquímicaDocument6 paginiInforme Práctica 2 BioquímicaJUAN DANIEL RUELAS HUAMANÎncă nu există evaluări
- UntitledDocument18 paginiUntitledjosecarlosÎncă nu există evaluări
- Bioquimica 5Document7 paginiBioquimica 5HARACELY CARDENAS NIHUAÎncă nu există evaluări
- Informe TP1 - ProteínasDocument5 paginiInforme TP1 - ProteínasLibrería InfinityÎncă nu există evaluări
- Informe de Lab 4Document9 paginiInforme de Lab 4sergio limaÎncă nu există evaluări
- Sem3 Bio Sala1Document10 paginiSem3 Bio Sala1Jose carlosÎncă nu există evaluări
- PROTEÍNASDocument8 paginiPROTEÍNASAlexander Posso RestrepoÎncă nu există evaluări
- Práctica - EnzimasDocument21 paginiPráctica - EnzimasJHON ANDY SILVESTRE MAZGOÎncă nu există evaluări
- Caracterizacion y Cuantificacion de ProteinasDocument8 paginiCaracterizacion y Cuantificacion de ProteinasHP TecnologyÎncă nu există evaluări
- Conclusiones IIIDocument31 paginiConclusiones IIIbrayan jordi rodriguez guizado0% (1)
- SEMINARIO 2.analisis Cuantitativo Por Cromatografia en Capa Fina. LA CHIDADocument22 paginiSEMINARIO 2.analisis Cuantitativo Por Cromatografia en Capa Fina. LA CHIDADani CrÎncă nu există evaluări
- Diagrama 7Document1 paginăDiagrama 7Dani CrÎncă nu există evaluări
- Tincion Tinta China y R.congoDocument3 paginiTincion Tinta China y R.congoDani Cr0% (1)
- Farmacología Gnereal y Quimioterapia Práctica 4Document1 paginăFarmacología Gnereal y Quimioterapia Práctica 4Dani CrÎncă nu există evaluări
- Diagrama 8Document4 paginiDiagrama 8Dani CrÎncă nu există evaluări
- SEMINARIO 2.analisis Cuantitativo Por Cromatografia en Capa Fina.Document22 paginiSEMINARIO 2.analisis Cuantitativo Por Cromatografia en Capa Fina.Dani CrÎncă nu există evaluări
- PRÁCTICA NO 3 MétodosDocument3 paginiPRÁCTICA NO 3 MétodosDani CrÎncă nu există evaluări
- Cromatografía PDFDocument55 paginiCromatografía PDFDani CrÎncă nu există evaluări
- Práctica 7 FisioDocument8 paginiPráctica 7 FisioDani CrÎncă nu există evaluări
- SISTEMA DE SALUD EN MEXICO Con Mi ParteDocument28 paginiSISTEMA DE SALUD EN MEXICO Con Mi ParteDani CrÎncă nu există evaluări
- HPLCDocument26 paginiHPLCDani CrÎncă nu există evaluări
- Práctica 10 EspirometriaDocument3 paginiPráctica 10 EspirometriaDani CrÎncă nu există evaluări
- TermoquímicaDocument8 paginiTermoquímicaDani CrÎncă nu există evaluări
- Práctica 9 Síntesis 2,3-Difenilquinoxalina Qfi 2019 - 1Document26 paginiPráctica 9 Síntesis 2,3-Difenilquinoxalina Qfi 2019 - 1Dani CrÎncă nu există evaluări
- Seminario 4. Hormonas Tiroideas.Document29 paginiSeminario 4. Hormonas Tiroideas.Dani CrÎncă nu există evaluări
- Seminario 9Document21 paginiSeminario 9Dani CrÎncă nu există evaluări
- Sistema Nervioso AutonomoDocument16 paginiSistema Nervioso AutonomoDani CrÎncă nu există evaluări
- Arco ReflejoDocument10 paginiArco ReflejoDani CrÎncă nu există evaluări
- Práctica 9 Fisiología CelularDocument15 paginiPráctica 9 Fisiología CelularDani CrÎncă nu există evaluări
- Intro Practica 9 de FisiologíaDocument2 paginiIntro Practica 9 de FisiologíaDani CrÎncă nu există evaluări
- Ensayo MomoDocument4 paginiEnsayo MomoDani CrÎncă nu există evaluări
- Fundamento de La Re - CristalizaciónDocument4 paginiFundamento de La Re - CristalizaciónDani CrÎncă nu există evaluări
- 1 Marco Teórico: 1.1 Difusión Molecular en GasesDocument21 pagini1 Marco Teórico: 1.1 Difusión Molecular en GasesChristian PÎncă nu există evaluări
- PM751.14 Procedimiento General para La Inspeccion Por Radiografia (OK)Document17 paginiPM751.14 Procedimiento General para La Inspeccion Por Radiografia (OK)Muñoz EstebanÎncă nu există evaluări
- Extracción de La Nicotina Del TabacoDocument10 paginiExtracción de La Nicotina Del TabacoJean Phol Callalli TorresÎncă nu există evaluări
- Evaluacion Ciencias 6° BasicoDocument5 paginiEvaluacion Ciencias 6° Basicorodrigood27Încă nu există evaluări
- Hoja de Seguridad Hilti CP 637Document8 paginiHoja de Seguridad Hilti CP 637Marcelo San MartinÎncă nu există evaluări
- Practica#5 CualitativaDocument7 paginiPractica#5 CualitativaSelene CuacésÎncă nu există evaluări
- Concreto Armado (Rch11 2015)Document112 paginiConcreto Armado (Rch11 2015)Nash RodriguezÎncă nu există evaluări
- Reporte Fisicoquímica 3 1Document10 paginiReporte Fisicoquímica 3 1tenoch lopezÎncă nu există evaluări
- Marco Teórico FernandoDocument6 paginiMarco Teórico FernandoFernando Vergara RÎncă nu există evaluări
- Indicaciones Proyecto EstructurasDocument8 paginiIndicaciones Proyecto EstructurasJuan Camilo AcevedoÎncă nu există evaluări
- Componente de Cadena de Frio Mariano MelgarDocument41 paginiComponente de Cadena de Frio Mariano MelgarYubet Caceres100% (2)
- Identificación e Conectores y Adaptadores HidráulicosDocument5 paginiIdentificación e Conectores y Adaptadores HidráulicosJoel FernandoÎncă nu există evaluări
- Guía Peruana para Medición de CO2 en Oficinas y AulasDocument66 paginiGuía Peruana para Medición de CO2 en Oficinas y AulasElmer Ramos CruzÎncă nu există evaluări
- Diferencias Entre Suelos Cohesivos y GranularesDocument10 paginiDiferencias Entre Suelos Cohesivos y GranularesFernando Jimenez0% (1)
- DinámicaDocument36 paginiDinámicaRoy SantosÎncă nu există evaluări
- La Biblia de Los CristalesDocument200 paginiLa Biblia de Los CristalesTatiana Trejo87% (136)
- El Mucílago de NopalDocument4 paginiEl Mucílago de NopalstingraycorvetteÎncă nu există evaluări
- Ciclo Del FosforoDocument11 paginiCiclo Del FosforoYarisel Shosha MuñozÎncă nu există evaluări
- Practica 1-20201Document4 paginiPractica 1-20201Anonymous gh6mTPQsHÎncă nu există evaluări
- Tarea SolucionesDocument3 paginiTarea SolucionesFran J LpÎncă nu există evaluări
- Contenido de HumedadDocument11 paginiContenido de HumedadkatmarÎncă nu există evaluări
- ImgDocument5 paginiImgEdna FélixÎncă nu există evaluări
- Practica-Instrumental 1-1Document12 paginiPractica-Instrumental 1-1Cristian PintaÎncă nu există evaluări
- Desviacion de ParticulasDocument1 paginăDesviacion de ParticulasHumberto D. ParrillaÎncă nu există evaluări
- Ensayo de Concreto PrecomprimidoDocument20 paginiEnsayo de Concreto PrecomprimidoruthsuarezÎncă nu există evaluări
- Experimento SpallazaniDocument2 paginiExperimento SpallazaniJesus LopezÎncă nu există evaluări
- FORMALIZACIONDocument3 paginiFORMALIZACIONMARIOÎncă nu există evaluări
- Plan de Clase (Cs. Naturales) SecundariaDocument30 paginiPlan de Clase (Cs. Naturales) SecundariaDaniel Jhony Chambi RojasÎncă nu există evaluări
- Articulo IncubadoraDocument4 paginiArticulo IncubadoraDaniel LissaÎncă nu există evaluări
- Visita A CemexDocument12 paginiVisita A Cemexxxeennttee100% (3)