Documente Academic
Documente Profesional
Documente Cultură
Valoracion de Nahco3 Bicarbonato de Sodio
Încărcat de
Andy PhyTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Valoracion de Nahco3 Bicarbonato de Sodio
Încărcat de
Andy PhyDrepturi de autor:
Formate disponibile
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Fecha: 03/ 03/ 18
FACULTAD DE ESTUDIOS SUPERIORES ZARAGOZA
Valoración de Bicarbonato de sodio Lote:
AFM I Grupo: Modulo: Caducidad:
LAB L-402 2453
Objetivo:
Analizar la concentración de bicarbonato de sodio mediante una titulación Ácido-Base.
Objetivos Particulares:
-Analizar el porcentaje de pureza de una solución problema de bicarbonato de sodio.
-Obtener cálculos aproximados al contenido estipulado en FEUM, 2008, no menos del 99% y
no más del 100.5%.
-Practica de titulación volumétrica.
Reacción Química
Reacción de estandarización:
Reacción de valoración:
Metodología y Cálculos teóricos :
(Cálculos teóricos)
Estandarización:
Se preparó una disolución de ácido clorhídrico (HCl) 0.1 N. Se tomaron 2.22 ml de HCl con
una pipeta graduada 1 en 100 y se diluyeron en 250 ml de agua destilada.
Masa= (0.1 Eq L-1) (0.25L) (36.46 g Eq-1)
Masa= 0.9212 g de HCl ---> V= m/d = 0.9212g/1.12g mL -1
Volumen = 0.8136 mL
Ajuste de pureza 0.8136mL – 36.5%
X --- 100% x= 2.22 ml de HCl
Elaboro Reviso Aprobó
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Fecha: 03/ 03/ 18
FACULTAD DE ESTUDIOS SUPERIORES ZARAGOZA
Valoración de Bicarbonato de sodio Lote:
AFM I Grupo: Modulo: Caducidad:
LAB L-402 2453
Preparación para la estandarización con trometamina
Valoración: se realizaron tres pesadas de 0.1831 g de trometamina las cuales se vertieron
En matraz Erlenmeyer de 125 ml con 2 gotas de indicador rojo de metilo y 15 ml de agua
destilada.
Masa= (0.1 Eq L-1) (0.015L) (122.12 g Eq-1)
Masa = 0.1831 g de trometamina
A Cada muestras se le agrego dos gotas de indicador purpura bromo cresol y se tituló con
la disolución de ácido clorhídrico (HCl 0.1N) previamente preparada hasta el vire color
amarillo pálido. Obteniendo así la concentración experimental de HCl la cual fue de 0.1060
N.
Valoración:
Se realizaron tres pesadas de muestra problema de bicarbonato de sodio (NaHCO3) cada
una de 0.1357 g y se vertieron en matraz Erlenmeyer de 125ml con dos gotas de indicador
rojo de metilo y 15 ml de agua destilada, cada muestra se tituló con la disolución de HCl
previamente estandarizada hasta el vire color amarillo, asegurando el cambio mediante
calentamiento y agitación por un corto periodo de tiempo.
Masa= (0.1060 N) (0.015L) (84.01g Eq-1)
Masa = 0.1335g de bicarbonato de sodio
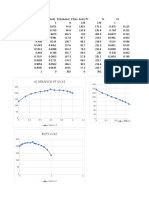
Tablas con los resultados obtenidos (numeradas y con título)
Tabla 1. Estandarización de HCl
Matraz Masa de trometamina Gasto de HCl Normalidad
1 0.1840 14.3 0.1053
2 0.1834 13.9 0.1080
3 0.1843 14.4 0.1048
Normalidad promedio 0.1060
Desviación estándar 0.00172
Coeficiente de variación 1.6234%
Elaboro Reviso Aprobó
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Fecha: 03/ 03/ 18
FACULTAD DE ESTUDIOS SUPERIORES ZARAGOZA
Valoración de Bicarbonato de sodio Lote:
AFM I Grupo: Modulo: Caducidad:
LAB L-402 2453
Cálculos
Análisis de Resultados
Como se observó en los resultados reportados la concentración promedio que se obtuvo en la
estandarización fue muy cercana a la esperada, obteniéndose un Cv= 0.7344% y en la valoración
se obtuvo un porcentaje de pureza del 99.45%, este valor se encuentra por debajo del reportado
en la literatura, esto debido a la variación del manejo de la bureta al ser difícil observar de
inmediato el punto de equilibrio, así como los errores que se tuvieron al pesar los reactivos.
Conclusión
Se cumplió con el objetivo ya que se logró obtener de manera satisfactoria la concentración de
una solución y posteriormente se pudo conocer el % de pureza de una solución problema. Con
base al porcentaje de pureza obtenido y con un coeficiente de variación menor al 1% se reporta
que la solución problema no cumple las especificaciones de Farmacopea de los Estados Unidos
Mexicanos.
También se puede concluir que a partir de una titulación ácido-base no solo se puede conocer la
concentración de una muestra problema si no también su pureza, y con los debidos cuidados de
pesadas y al ser cuidadoso con el uso de la bureta, se pueden obtener resultados óptimos.
Bibliografía
Elaboro Reviso Aprobó
S-ar putea să vă placă și
- Valoración Bicarbonato de Sodio Con HCLDocument3 paginiValoración Bicarbonato de Sodio Con HCLFranciscoVelasco83% (6)
- Bicarbonato de Sodio InyectableDocument5 paginiBicarbonato de Sodio Inyectableloganloganloganlogan100% (2)
- Determinación de Pureza de Bicarbonato de Sodio. REVISADODocument5 paginiDeterminación de Pureza de Bicarbonato de Sodio. REVISADOBrenVigueras100% (4)
- 001 Pureza en Bicarbonato de Sodio CorregidoDocument13 pagini001 Pureza en Bicarbonato de Sodio CorregidoEdgar Gabriel BravoÎncă nu există evaluări
- Bicarbonato de SodioDocument17 paginiBicarbonato de SodioErick Ramone100% (1)
- Bicarbonato de Sodio AFMP1Document8 paginiBicarbonato de Sodio AFMP1Pao MoralesÎncă nu există evaluări
- Extraccion Identificacion de Carbohidratos en Plantas y AnimalesDocument8 paginiExtraccion Identificacion de Carbohidratos en Plantas y AnimalesAndy PhyÎncă nu există evaluări
- MetronidazolDocument5 paginiMetronidazolAndy PhyÎncă nu există evaluări
- Anteproyecto 6 de Gluconato de CalcioDocument17 paginiAnteproyecto 6 de Gluconato de CalcioErick RamoneÎncă nu există evaluări
- Análisis lípidos yema huevoDocument9 paginiAnálisis lípidos yema huevoRicardoVelascoPeraltaÎncă nu există evaluări
- Actividades: Destilación Por Arrastre de Vapor de Agua. Separación Del Aceite Esencial de Canela e Identificación Del CinamaldehidoDocument12 paginiActividades: Destilación Por Arrastre de Vapor de Agua. Separación Del Aceite Esencial de Canela e Identificación Del CinamaldehidoAlan YañezÎncă nu există evaluări
- Bicarbonato de Sodio Solucion Inyectable v1.1Document5 paginiBicarbonato de Sodio Solucion Inyectable v1.1Vero Sandoval100% (1)
- Buffer acetato pH5Document13 paginiBuffer acetato pH5Nayeli Díaz100% (1)
- % de Contenido Del SulfametoxazolDocument13 pagini% de Contenido Del SulfametoxazolEsme Hernández0% (1)
- Acido Acetilsalicilico Por Retroceso 2Document4 paginiAcido Acetilsalicilico Por Retroceso 2Diana Rodriguez50% (4)
- Determinacion de MetronidazolDocument12 paginiDeterminacion de MetronidazolIvan Monroy100% (6)
- Valoracion Potenciometrica Del Acido CitricoDocument9 paginiValoracion Potenciometrica Del Acido CitricoBeatriz Mora SantiagoÎncă nu există evaluări
- Titulación de Sulfato de MagnesioDocument4 paginiTitulación de Sulfato de MagnesioPau Pérez100% (1)
- Acido CitricoDocument7 paginiAcido CitricoAndy PhyÎncă nu există evaluări
- Buffer AnteproyectoDocument18 paginiBuffer AnteproyectoHannya CruzÎncă nu există evaluări
- 1401.síntesis Del Ácido Antranílico.Document21 pagini1401.síntesis Del Ácido Antranílico.AFMP TeoriaÎncă nu există evaluări
- Anteproyecto Mezcla de AcidosDocument19 paginiAnteproyecto Mezcla de AcidosMaurilio HuÎncă nu există evaluări
- BenzoinaDocument16 paginiBenzoinaDiego MoralesÎncă nu există evaluări
- Determinación MgSO4 solución inyectable titulación EDTADocument10 paginiDeterminación MgSO4 solución inyectable titulación EDTAeduardo0% (1)
- PH de Mezcla de AcidosDocument6 paginiPH de Mezcla de AcidosDaniel PrepaÎncă nu există evaluări
- Valoración de Ácido Benzoico Con Hidróxido de SodioDocument3 paginiValoración de Ácido Benzoico Con Hidróxido de SodioFranciscoVelasco100% (2)
- INFORME Acido BenzoicoDocument6 paginiINFORME Acido BenzoicoReyna OregonÎncă nu există evaluări
- Gluconato de CalcioDocument6 paginiGluconato de CalciologanloganloganloganÎncă nu există evaluări
- Informe 2 Síntesis de P NitroacetanilidaDocument6 paginiInforme 2 Síntesis de P NitroacetanilidaNatalia Aroz OrtizÎncă nu există evaluări
- Reaccion de Shinoda y ShibataDocument2 paginiReaccion de Shinoda y ShibataNayely Arrieta García50% (2)
- Anteproyecto Ácido AntranilicoDocument16 paginiAnteproyecto Ácido AntranilicoDiana MoraÎncă nu există evaluări
- Titulaciones No AcuosasDocument24 paginiTitulaciones No Acuosas.:("*"BLacK BuLLeT"*"):.100% (2)
- MetronidazolDocument12 paginiMetronidazolkarla rosasÎncă nu există evaluări
- Sintesis de LuminolDocument3 paginiSintesis de LuminolDaniela Ibarra100% (1)
- ESTANDARIZACIONDocument5 paginiESTANDARIZACIONluceroÎncă nu există evaluări
- Informe - Curva Estándar de ProteínasDocument6 paginiInforme - Curva Estándar de ProteínasAndrade Ayala ValeriaÎncă nu există evaluări
- Análisis Cuantitativo de Analitos Con Base en Equilibrios de Formación de ComplejosDocument3 paginiAnálisis Cuantitativo de Analitos Con Base en Equilibrios de Formación de ComplejosGabriela Pietra Santa100% (1)
- Oxima de La Ciclohexanona SFMP1Document7 paginiOxima de La Ciclohexanona SFMP1Pao MoralesÎncă nu există evaluări
- Reporte Sintesis de BenzoinaDocument1 paginăReporte Sintesis de BenzoinaAnthonio Motha100% (1)
- Determinación de Cloruros en Vida Suero OralDocument16 paginiDeterminación de Cloruros en Vida Suero OralErick Ramone50% (2)
- Determinación de % Contenido Ácido Acético. ConductimetríaDocument21 paginiDeterminación de % Contenido Ácido Acético. ConductimetríaAndy RamosÎncă nu există evaluări
- Práctica 3: Valoraciones Complejométricas Por Retroceso.Document20 paginiPráctica 3: Valoraciones Complejométricas Por Retroceso.Enrique Delgado0% (1)
- Valoración Del Ácido Benzoico Con NaOHDocument5 paginiValoración Del Ácido Benzoico Con NaOHGilian SkalariÎncă nu există evaluări
- Análisis de MetronidazolDocument10 paginiAnálisis de MetronidazolAbimael969100% (1)
- Practica 1. Efecto Del Tamaño de Partícula y de Temperatura Sobre La Velocidad de La ReacciónDocument5 paginiPractica 1. Efecto Del Tamaño de Partícula y de Temperatura Sobre La Velocidad de La ReacciónPau Flurscheim100% (1)
- Síntesis de DibenzalacetonaDocument8 paginiSíntesis de DibenzalacetonaLalo AguerrilaÎncă nu există evaluări
- Informe Experimental Del Calor de Descomposición Del H2o2Document8 paginiInforme Experimental Del Calor de Descomposición Del H2o2Sheryl VegaÎncă nu există evaluări
- Determinacion Permanganometrica de H2o2 en Agua Oxigenada MedicinalDocument4 paginiDeterminacion Permanganometrica de H2o2 en Agua Oxigenada MedicinalErika Itzel C A100% (2)
- Determinacion de Metronidazol PDFDocument12 paginiDeterminacion de Metronidazol PDFMiguel Adrian GaonaÎncă nu există evaluări
- MEZCLA DE ÁCIDOSDocument8 paginiMEZCLA DE ÁCIDOSGeraldiine RamirezÎncă nu există evaluări
- Determinación Cloruros en Suero FisiológicoDocument3 paginiDeterminación Cloruros en Suero Fisiológicoroberto cch0% (1)
- Informe Punto Isosbestico.Document13 paginiInforme Punto Isosbestico.Jesus Gerardo Lopez ColmanÎncă nu există evaluări
- Practica 5 Extraccion y Analisis de Lipidos en La Yema de HuevoDocument8 paginiPractica 5 Extraccion y Analisis de Lipidos en La Yema de HuevoUriel Calderon Aragon100% (1)
- P9 AQ Determinación Mezcla Alcalina PDFDocument2 paginiP9 AQ Determinación Mezcla Alcalina PDFAdRiiiÎncă nu există evaluări
- Informe 2Document9 paginiInforme 2apoxapoxes2001Încă nu există evaluări
- Agua Oxigenada 3 %Document10 paginiAgua Oxigenada 3 %Jesus VillanuevaÎncă nu există evaluări
- 2° Informe de Analitica CDocument9 pagini2° Informe de Analitica CGERSON MARTIN CUCHO FERNANDEZÎncă nu există evaluări
- Determinación de Cloruros.Document6 paginiDeterminación de Cloruros.Andy PhyÎncă nu există evaluări
- Valoracion de Nahco3 Bicarbonato de SodioDocument3 paginiValoracion de Nahco3 Bicarbonato de SodioAndy Phy67% (3)
- MetronidazolDocument5 paginiMetronidazolAndy PhyÎncă nu există evaluări
- Usos de Los Microorganismos en La Elaboración de AlimentosDocument2 paginiUsos de Los Microorganismos en La Elaboración de AlimentosAndy PhyÎncă nu există evaluări
- Función renal y creatininaDocument2 paginiFunción renal y creatininaAndy PhyÎncă nu există evaluări
- RESORCINOLDocument4 paginiRESORCINOLAndy PhyÎncă nu există evaluări
- Vias de Degradación Oxidación y FotolisisDocument2 paginiVias de Degradación Oxidación y FotolisisAndy PhyÎncă nu există evaluări
- Vitaminas y Minerales en Los Alimentos BromatologíaDocument3 paginiVitaminas y Minerales en Los Alimentos BromatologíaAndy PhyÎncă nu există evaluări
- Prueba de Sulfatos y ClorurosDocument4 paginiPrueba de Sulfatos y ClorurosAndy PhyÎncă nu există evaluări
- Formas Farmacéuticas Orales, Polvos, Grageas y TabletasDocument7 paginiFormas Farmacéuticas Orales, Polvos, Grageas y TabletasAndy PhyÎncă nu există evaluări
- Pruebas Bioquimicas Informe Equipo 6Document13 paginiPruebas Bioquimicas Informe Equipo 6Andy PhyÎncă nu există evaluări
- Examen Practico MicrobilogiaDocument5 paginiExamen Practico MicrobilogiaAndy PhyÎncă nu există evaluări
- Acido CitricoDocument7 paginiAcido CitricoAndy PhyÎncă nu există evaluări
- Florometría RivoflabinaDocument4 paginiFlorometría RivoflabinaAndy PhyÎncă nu există evaluări
- Curva estándar y cálculos de concentración de albúmina y globulinasDocument3 paginiCurva estándar y cálculos de concentración de albúmina y globulinasAndy PhyÎncă nu există evaluări
- Calor de Descomposición Del H2O2Document5 paginiCalor de Descomposición Del H2O2Andy Phy100% (1)
- Cinética enzimática de la invertasaDocument8 paginiCinética enzimática de la invertasaAndy Phy100% (1)
- Osmosis y Dialisis Reporte 3Document6 paginiOsmosis y Dialisis Reporte 3Andy Phy0% (1)
- Sintesis de AcetanilidaDocument2 paginiSintesis de AcetanilidaAndy PhyÎncă nu există evaluări
- Monografia SulfatiazolDocument12 paginiMonografia SulfatiazolAndy PhyÎncă nu există evaluări
- Estructura CelularDocument8 paginiEstructura CelularAndy PhyÎncă nu există evaluări
- Cinética enzimática de la invertasaDocument8 paginiCinética enzimática de la invertasaAndy Phy100% (1)
- Extraccion Identificacion de Carbohidratos en Plantas y AnimalesDocument8 paginiExtraccion Identificacion de Carbohidratos en Plantas y AnimalesAndy PhyÎncă nu există evaluări
- Análisis y Determinación de Las Curvas Características de BombasDocument20 paginiAnálisis y Determinación de Las Curvas Características de BombasAndy PhyÎncă nu există evaluări
- Extraccion Identificacion de Carbohidratos en Plantas y AnimalesDocument8 paginiExtraccion Identificacion de Carbohidratos en Plantas y AnimalesAndy PhyÎncă nu există evaluări
- Informe Calor de Disolucion Na2CO3Document6 paginiInforme Calor de Disolucion Na2CO3Andy Phy100% (1)
- Modelos AtomicosDocument13 paginiModelos AtomicosAndy PhyÎncă nu există evaluări
- Practica de Calibracion Fes ZaragozaDocument9 paginiPractica de Calibracion Fes ZaragozaAndy PhyÎncă nu există evaluări
- Practica de Calibracion Fes ZaragozaDocument9 paginiPractica de Calibracion Fes ZaragozaAndy PhyÎncă nu există evaluări
- Practica 6Document5 paginiPractica 6Luis Alvarado100% (1)
- ConclusionDocument2 paginiConclusionElizabeth Yataco Pacheco100% (1)
- PL 03 - Soluciones (Guia Unmsm Laboratorio Quimica)Document2 paginiPL 03 - Soluciones (Guia Unmsm Laboratorio Quimica)CARLOS ENRIQUE TARAZONA VALVERDEÎncă nu există evaluări
- Materia PrimaDocument1 paginăMateria PrimaAlex OwenÎncă nu există evaluări
- Equilibrio químicoDocument20 paginiEquilibrio químicoKevin Jefferson BalladaresÎncă nu există evaluări
- Valoraciones potenciométricas: Estandarización de soluciones y aplicacionesDocument6 paginiValoraciones potenciométricas: Estandarización de soluciones y aplicacionesharold diazÎncă nu există evaluări
- 1ejercicio de MolaridadDocument1 pagină1ejercicio de MolaridadJorge MéndezÎncă nu există evaluări
- Guaifenesina, Solución OralDocument1 paginăGuaifenesina, Solución OralGeidy Tatiana Caro ParraÎncă nu există evaluări
- YONY FARIDTH MEDINA QUIRA - Segunda EvaluaciónDocument1 paginăYONY FARIDTH MEDINA QUIRA - Segunda EvaluaciónMayerlihd Hoyos DoradoÎncă nu există evaluări
- Equilibrios Acido-Base y Equilibrios de SolubilidadDocument39 paginiEquilibrios Acido-Base y Equilibrios de SolubilidadBella Ramirez AvilaÎncă nu există evaluări
- GUIA Laboratorio Analítica Práctica 4 I - 2020Document12 paginiGUIA Laboratorio Analítica Práctica 4 I - 2020Nancy Tola FloresÎncă nu există evaluări
- 2do Parcial Unidad Temática #8 Agua para La Industria Complemento de Cálculos Procesos Industriales Iq-415 Ii Pac 2020Document18 pagini2do Parcial Unidad Temática #8 Agua para La Industria Complemento de Cálculos Procesos Industriales Iq-415 Ii Pac 2020Rigo OsorioÎncă nu există evaluări
- Ejercicio 3Document13 paginiEjercicio 3Javier Ramirez DiazÎncă nu există evaluări
- DurezaDocument8 paginiDurezaDANIELA HERNANDEZ ALEMANÎncă nu există evaluări
- Acido Base - PreguntasDocument7 paginiAcido Base - PreguntasOscar Cruellas GrauÎncă nu există evaluări
- Determinación cuantitativa de ácido bórico en solución oftálmicaDocument14 paginiDeterminación cuantitativa de ácido bórico en solución oftálmicaCésar CastelánÎncă nu există evaluări
- Investigación CienciasDocument17 paginiInvestigación CienciasAnne McKyntireÎncă nu există evaluări
- Estandarizacion y PotenciometriaDocument13 paginiEstandarizacion y Potenciometriavictor andresÎncă nu există evaluări
- Solidos - 2012Document2 paginiSolidos - 2012Luis VacaÎncă nu există evaluări
- Práctica 07. Reacciones Reversibles. Introducción Al Equilibrio Químico. Ley de Acción de MasasDocument4 paginiPráctica 07. Reacciones Reversibles. Introducción Al Equilibrio Químico. Ley de Acción de MasasChristopher MorenoÎncă nu există evaluări
- OxisalesDocument12 paginiOxisalesNancy EstradaÎncă nu există evaluări
- Examen 4 Unidad I Metodo Ponchon SavaritDocument33 paginiExamen 4 Unidad I Metodo Ponchon SavaritKarel GerardoÎncă nu există evaluări
- PROBLEMASDocument6 paginiPROBLEMASJuan Carlos Castillo ZamoraÎncă nu există evaluări
- Equilibrio Iónico 3Document25 paginiEquilibrio Iónico 3marcosdysse09gmail.com ysseÎncă nu există evaluări
- Asignacion #2 CMIDocument7 paginiAsignacion #2 CMIKadir MuñozÎncă nu există evaluări
- UNIDAD #3 Reacciones Ácido BaseDocument35 paginiUNIDAD #3 Reacciones Ácido BaseValentinaÎncă nu există evaluări
- Cálculo de concentraciones de disoluciones en unidades físicasDocument17 paginiCálculo de concentraciones de disoluciones en unidades físicasJENNY LAZAROÎncă nu există evaluări
- Práctica de Laboractorio - Titulación Ácido - Base y EstequiometríaDocument10 paginiPráctica de Laboractorio - Titulación Ácido - Base y EstequiometríastephanysuazoÎncă nu există evaluări
- Memoria de CalculosDocument9 paginiMemoria de CalculosLeo Anthony Campos OlivasÎncă nu există evaluări
- Preparación y estandarización de disolucionesDocument50 paginiPreparación y estandarización de disolucionesEmerson Wilgen Apaza LopezÎncă nu există evaluări