Documente Academic
Documente Profesional
Documente Cultură
Preparación de NaOH Medios No Electroquimicos
Încărcat de
Ivan Ivenian0 evaluări0% au considerat acest document util (0 voturi)
28 vizualizări2 paginiLa preparación del hidróxido de sodio a través de la caustificación del carbonato sódico implica hacer reaccionar una disolución de carbonato de sodio con lechada de cal para producir una disolución de hidróxido de sodio. El proceso químico simple ocurre a unos 100°C y produce precipitados de carbonato de calcio y una disolución concentrada de hidróxido de sodio. La suspensión resultante se filtra y lava, y el carbonato de calcio lavado se utiliza como materia prima en la industria del vid
Descriere originală:
Preparación Del Hidróxido de Sodio Por Caustificación de Carbonato
Titlu original
Preparación de NaOH Medios no electroquimicos
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentLa preparación del hidróxido de sodio a través de la caustificación del carbonato sódico implica hacer reaccionar una disolución de carbonato de sodio con lechada de cal para producir una disolución de hidróxido de sodio. El proceso químico simple ocurre a unos 100°C y produce precipitados de carbonato de calcio y una disolución concentrada de hidróxido de sodio. La suspensión resultante se filtra y lava, y el carbonato de calcio lavado se utiliza como materia prima en la industria del vid
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
28 vizualizări2 paginiPreparación de NaOH Medios No Electroquimicos
Încărcat de
Ivan IvenianLa preparación del hidróxido de sodio a través de la caustificación del carbonato sódico implica hacer reaccionar una disolución de carbonato de sodio con lechada de cal para producir una disolución de hidróxido de sodio. El proceso químico simple ocurre a unos 100°C y produce precipitados de carbonato de calcio y una disolución concentrada de hidróxido de sodio. La suspensión resultante se filtra y lava, y el carbonato de calcio lavado se utiliza como materia prima en la industria del vid
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 2
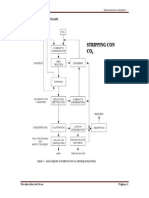
Preparación del hidróxido de sodio por caustificación de carbonato
Como la sosa cáustica es más difícil de transportar que el carbonato sódico,
frecuentemente, las fábricas se surten del carbonato y por caustificación de su disolución
obtienen la lejía de sosa cáustica in situ.El hidróxido de sodio, en su mayoría, se sintetiza
por el método de caustificación, es decir, juntando otro hidróxido con un compuesto de
sodio.
La caustificación consiste en hacer reaccionar disolución de CO3Na2 y lechada de cal
Ca(OH)2
El proceso de caustificación produce una disolución de cocción para el digestor a partir de
productos químicos inorgánicos reciclados generados en la caldera de recuperación y el
horno de cal. El proceso implica una reacción química muy simple seguida de etapas de
proceso que utilizan varios tipos de equipos de separación sólidos líquidos
Se opera a unos 100 °C para facilitar la velocidad de la transformación y la filtrabilidad del
precipitado.
Como existen dos fases sólidas (el Ca(OH)2 de la lechada y el CO3Ca precipitado)el
equilibrio está regido por:
Como los productos de solubilidad son:
Resulta:
Que escrita en la forma
indica que si se lleva a ordenadas la concentración de OH- en el líquido en equilibrio (y
esta concentración será la de la sosa cáustica al final) y a abcisas el cociente OH-/ (que
mide el grado de conversión del carbonato en hidróxido, o sea, el rendimiento de la
operación), se obtiene una hipérbola; es decir, si se quiere un alto rendimiento, las
concentraciones deben ser bajas.
Por tanto, el punto óptimo de esta transformación dependerá de los costes de adquisición
del CO3Na2 (que obligan a un rendimiento tanto más alto cuanto más altos sean) y del
coste de la evaporación de la disolución final para concentrarla.
Se suele trabajar con disoluciones de 12% de CO3Na2; el rendimiento de conversión es de
0,9 después de media hora de contacto. Por otra parte, las concentraciones elevadas de
CO3Na2 dan lugar a la formación de sales dobles insolubles, que determinan pérdidas de
reactivos.
La suspensión resultante se filtra y lava. El líquido de lavado se incorpora al ciclo siguiente
para disolver el CO3Na2. El CO3Ca lavado retiene un 1,5% de sosa; se utiliza como materia
prima en vidriería y también para producir por calcinación el CaO necesario para la
caustificación. Para ello hay que utilizar hornos —rotatorios, o de fluidización— capaces
de trabajar con un producto tan pulverizado
S-ar putea să vă placă și
- Metodos de SeparaciónDocument6 paginiMetodos de SeparaciónMarcelineAkumaPhantomhiveÎncă nu există evaluări
- Proceso de Elaboración de Acido NítricoDocument6 paginiProceso de Elaboración de Acido NítricoErik Arias CoronelÎncă nu există evaluări
- Obtención de CO2Document5 paginiObtención de CO2esc_21laqm6365Încă nu există evaluări
- Sintesis de UREADocument7 paginiSintesis de UREAJose Luis Cedeño CevallosÎncă nu există evaluări
- Fenol, Cloruro de Calcio y Sulfato de AluminioDocument26 paginiFenol, Cloruro de Calcio y Sulfato de AluminioCristian de los Rios100% (2)
- Proceso de Obtención de La Urea y AmoniacoDocument9 paginiProceso de Obtención de La Urea y AmoniacoDavid Briceño Gonzalez100% (1)
- Catalizadores en La UreaDocument19 paginiCatalizadores en La UreaLizeth AstudilloÎncă nu există evaluări
- Procesos de Desulfuracion TrabajoDocument12 paginiProcesos de Desulfuracion TrabajoKeilys GilÎncă nu există evaluări
- UREA de Grado AutomotrízDocument8 paginiUREA de Grado AutomotrízIrvingÎncă nu există evaluări
- Proceso de Elaboración de FertilizantesDocument3 paginiProceso de Elaboración de FertilizantesVeronica Ayala CarhuatoctoÎncă nu există evaluări
- Diagrama de Produccion de AmoniacoDocument8 paginiDiagrama de Produccion de AmoniacoSoraya Ochoa VillamizarÎncă nu există evaluări
- Operaciones Unitarias IDocument18 paginiOperaciones Unitarias IEvens CruzÎncă nu există evaluări
- Producción de UREADocument10 paginiProducción de UREARaul Roque YujraÎncă nu există evaluări
- Urea NweaaaasDocument9 paginiUrea NweaaaasMagaly Gutierrez VelaÎncă nu există evaluări
- Proceso de Producción de AmoníacoDocument5 paginiProceso de Producción de AmoníacoOmarRomarioMartinesÎncă nu există evaluări
- Ejercicio Reklaitis 3.33Document2 paginiEjercicio Reklaitis 3.33AngeloÎncă nu există evaluări
- Tecnologias de Obtencion de La Urea Y SYNGASDocument19 paginiTecnologias de Obtencion de La Urea Y SYNGASRocio Mamani CastroÎncă nu există evaluări
- 2014 Integracion IV - Práctico 6 - Producción de Sustancias Químicas A Partir Del Carbón de HullaDocument8 pagini2014 Integracion IV - Práctico 6 - Producción de Sustancias Químicas A Partir Del Carbón de HullaEzequiel KrumrickÎncă nu există evaluări
- Sintesis Del Carbonato SodicoDocument5 paginiSintesis Del Carbonato SodicoJorgeMartinÎncă nu există evaluări
- Proceso de Producción de AmoníacoDocument4 paginiProceso de Producción de AmoníacoFer JahrefÎncă nu există evaluări
- Recuperacion de AzufreDocument11 paginiRecuperacion de AzufreClaudia SaavedraÎncă nu există evaluări
- ExcerciseDocument34 paginiExcerciseOscarRealpe100% (2)
- Carbonato de Sodio, Sales de Sodio y Hidoxido de SodioDocument12 paginiCarbonato de Sodio, Sales de Sodio y Hidoxido de SodioMAYRA HURTADO MARCANOÎncă nu există evaluări
- Tecnologías de Obtención de La Urea Y SYNGASDocument19 paginiTecnologías de Obtención de La Urea Y SYNGASmtdescargaÎncă nu există evaluări
- Procesos de Produccion Del AmoniacoDocument5 paginiProcesos de Produccion Del AmoniacoJezz JuÎncă nu există evaluări
- Proceso de Producción de AmoníacoDocument4 paginiProceso de Producción de AmoníacoDiego SuarezÎncă nu există evaluări
- Clor-Alcali-IpqDocument15 paginiClor-Alcali-IpqCésar Antonio Wong JuradoÎncă nu există evaluări
- Obtención Del AmoniacoDocument5 paginiObtención Del AmoniacoPatricia Atia50% (2)
- Elaboración de Fertilizantes NitrogenadosDocument4 paginiElaboración de Fertilizantes NitrogenadosOscar Eduardo Cobo NarváezÎncă nu există evaluări
- Procesos Desarrollados en Las Plantas de Amoniaco y UreaDocument8 paginiProcesos Desarrollados en Las Plantas de Amoniaco y UreaDairoAndresTrillosPuentes100% (1)
- AmoniacoDocument4 paginiAmoniacoMarco Salazar CortésÎncă nu există evaluări
- Problemas Propuestos 2021 - 2022Document4 paginiProblemas Propuestos 2021 - 2022LauraBuitragoCortésÎncă nu există evaluări
- Balances MarmotaDocument3 paginiBalances Marmotayhon manuelÎncă nu există evaluări
- Proceso Haber BoschDocument5 paginiProceso Haber BoschKarla HerediaÎncă nu există evaluări
- Procesos Leblanc y SolvayDocument14 paginiProcesos Leblanc y SolvayGersonGarcíaSánchezÎncă nu există evaluări
- Obtencion de UreaDocument11 paginiObtencion de UreaOmar Jesus Monasterios LaimeÎncă nu există evaluări
- Colectores de Dioxido de Azufre, PresentaciónDocument30 paginiColectores de Dioxido de Azufre, PresentaciónALICIAÎncă nu există evaluări
- CARBONATO DE SODIOtrabajo Terminado de ProcesosDocument10 paginiCARBONATO DE SODIOtrabajo Terminado de ProcesosAdali Reyes JulcaÎncă nu există evaluări
- Produccion Industrial de Urea Textos Cientificos PDFDocument23 paginiProduccion Industrial de Urea Textos Cientificos PDFLuis Coronado100% (1)
- La Síntesis de Urea A Nivel Industrial Se Realiza A Partir de AmoníacoDocument6 paginiLa Síntesis de Urea A Nivel Industrial Se Realiza A Partir de AmoníacoluisanamontÎncă nu există evaluări
- Descripcion de La Obtencion de NH4Document3 paginiDescripcion de La Obtencion de NH4acte90Încă nu există evaluări
- Metodo de Obtencion de Acido SulfuricoDocument3 paginiMetodo de Obtencion de Acido SulfuricoArmando PerezÎncă nu există evaluări
- Recuperación de RenioDocument5 paginiRecuperación de RenioPablo JimenesÎncă nu există evaluări
- UreaDocument5 paginiUreajacerÎncă nu există evaluări
- Síntesis de Fertilizantes-UreaDocument13 paginiSíntesis de Fertilizantes-UreasamanthaÎncă nu există evaluări
- Proceso de Producción de AmoníacoDocument15 paginiProceso de Producción de AmoníacocitlaliÎncă nu există evaluări
- Acid SuccinicDocument3 paginiAcid SuccinicHector Millan FrancoÎncă nu există evaluări
- Trabajo de InvestigacionDocument13 paginiTrabajo de InvestigacionTania OrellanaÎncă nu există evaluări
- Método SolvayDocument3 paginiMétodo SolvayEmmaColladoArredondo100% (1)
- Amoniaco y UreaDocument14 paginiAmoniaco y UreaelelefanterozadoÎncă nu există evaluări
- Balance de materia orientado a procesosDe la EverandBalance de materia orientado a procesosÎncă nu există evaluări
- Reutilización de aguas residuales en la industria azucarera y AlcoholeraDe la EverandReutilización de aguas residuales en la industria azucarera y AlcoholeraÎncă nu există evaluări
- El Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaDe la EverandEl Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaÎncă nu există evaluări
- Manual técnico de refrigerantesDe la EverandManual técnico de refrigerantesEvaluare: 4 din 5 stele4/5 (4)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe la EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSEvaluare: 4.5 din 5 stele4.5/5 (7)
- Práctica de Operaciones de Separación Sol-Liq PDFDocument8 paginiPráctica de Operaciones de Separación Sol-Liq PDFIvan IvenianÎncă nu există evaluări
- Camara de RefrigeracionDocument10 paginiCamara de RefrigeracionIvan IvenianÎncă nu există evaluări
- INforme Cinetica QuimicaDocument3 paginiINforme Cinetica QuimicaIvan IvenianÎncă nu există evaluări
- Disolucion de BoraxDocument2 paginiDisolucion de BoraxIvan IvenianÎncă nu există evaluări
- Informe CatalisisProcesos de Obtención de Ácido SulfúricoDocument6 paginiInforme CatalisisProcesos de Obtención de Ácido SulfúricoIvan IvenianÎncă nu există evaluări
- Informe CatalisisProcesos de Obtención de Ácido SulfúricoDocument6 paginiInforme CatalisisProcesos de Obtención de Ácido SulfúricoIvan IvenianÎncă nu există evaluări
- Fosforo GasolinaDocument3 paginiFosforo GasolinaIvan IvenianÎncă nu există evaluări
- Planta de Acido Sulfurico en Eucaliptus EnviarDocument3 paginiPlanta de Acido Sulfurico en Eucaliptus EnviarIvan IvenianÎncă nu există evaluări
- Comic Del AguaDocument9 paginiComic Del AguaIvan Ivenian91% (11)
- CascadaDocument1 paginăCascadaIvan IvenianÎncă nu există evaluări
- Termodinámica de Disolución de BoraxDocument3 paginiTermodinámica de Disolución de BoraxIvan IvenianÎncă nu există evaluări
- Produccion de Jugo de ToronjaDocument2 paginiProduccion de Jugo de ToronjaIvan IvenianÎncă nu există evaluări
- Pilas GalvanicasDocument2 paginiPilas GalvanicasIvan IvenianÎncă nu există evaluări
- Celda de DiafragmaDocument2 paginiCelda de DiafragmaIvan IvenianÎncă nu există evaluări
- Indice de Neutralización Y Saponificación de Un Aceite LubricanteDocument1 paginăIndice de Neutralización Y Saponificación de Un Aceite LubricanteIvan IvenianÎncă nu există evaluări
- Informe 5Document5 paginiInforme 5Ivan Ivenian100% (1)
- Informe 6Document6 paginiInforme 6Ivan Ivenian0% (1)
- Rendimiento BombaDocument6 paginiRendimiento BombaIvan IvenianÎncă nu există evaluări
- Obtención Del NaOHDocument6 paginiObtención Del NaOHIvan Ivenian100% (1)
- Ecuaciones Adimensionales y de SemejanzaDocument2 paginiEcuaciones Adimensionales y de SemejanzaIvan IvenianÎncă nu există evaluări
- Celda de MercurioDocument1 paginăCelda de MercurioIvan IvenianÎncă nu există evaluări
- Analisis Instrumental PolarimetriaDocument1 paginăAnalisis Instrumental PolarimetriaIvan Ivenian100% (1)
- CUESTIONARIO ElectroquimicaDocument2 paginiCUESTIONARIO ElectroquimicaIvan IvenianÎncă nu există evaluări