Documente Academic
Documente Profesional
Documente Cultură
Ggc-pr-001 Procedimiento para La Gestion de Eventos Adversos Laboratorio Clinico Hsat
Încărcat de
Ktalina BeltranTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Ggc-pr-001 Procedimiento para La Gestion de Eventos Adversos Laboratorio Clinico Hsat
Încărcat de
Ktalina BeltranDrepturi de autor:
Formate disponibile
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 1 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
HOSPITAL SAN ANTONIO DE TAME
PROCEDIMIENTO PARA LA IDENTIFICACION Y GESTION DE EVENTOS
ADVERSON E INCIDENTES
SUBPROCESO
LABORATORIO CLINICO
E.S.E. DEPARTAMENTAL MORENO Y CLAVIJO ARAUCA
HOSPITAL SAN ANTONIO DE TAME
TAME – ARAUCA
2018
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 2 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
1. OBJETIVO
El presente procedimiento establece las directrices para la gestión de Incidentes y
eventos adversos en el laboratorio clínico del Hospital San Antonio de Tame que hace
parte de la E.S.E. Departamental Moreno y Clavijo.
2. ALCANCE
Este procedimiento se aplica desde que se identifica y registra el Incidente o Evento
Adverso hasta el cierre del plan de mejoramiento tendiente a mejorar la calidad de la
atención a los usuarios.
3. BASE LEGAL
o Resolución 1446 de 2008
o Anexo Técnico de la Resolución 1446 de 2008.
o GUIA DE BUENAS PRACTICAS DE SEGURIDAD DEL PACIENTE EMITIDA POR
MIN SALUD
4. TÉRMINOS Y DEFINICIONES
Evento Adverso
Entendemos como eventos adversos las lesiones o complicaciones involuntarias que
ocurren durante la atención en salud, las cuales son mas atribuibles a esta que a la
enfermedad subyacente y que pueden conducir a la muerte, la incapacidad o al deterioro
en el estado de sa.lud del paciente, a la demora del alta, a la Prolongación del tiempo de
estancia hospitalizado y al incremento de los costos de no-calidad. Por extensión, también
aplicamos este concepto a situaciones relacionadas con procesos no asistenciales que
potencialmente pueden incidir en la ocurrencia de las situaciones arriba mencionadas”.
(Anexo Técnico, Resolución 1446 de 2006).
Evento adverso evitable
Lesión o daño no intencional causado por la intervención asistencial ejecutada con error,
no por la patología de base.
Evento adverso no evitable o Complicación o Reacción Adversa: Aquellos eventos
adversos que no se pueden prevenir. (Anexo Técnico, Resolución 1446 de 2006). Lesión
o daño no intencional causado por la intervención asistencial ejecutada sin error, no por la
patología de base. Ocurre cuando, por ejemplo, se administra un medicamento o se aplica
una tecnología en dosis y forma adecuada, para la patología adecuada.
Incidente o Casi Evento Adverso
Se trata de situaciones en las cuales la intervención asistencial se ejecuta con error, por
acción o por omisión; pero como resultado del azar, o de una barrera de seguridad o de
una intervención oportuna, no se presenta un daño en el paciente.
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 3 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
Acción Insegura
Conducta que ocurre durante el proceso de atención en salud, usualmente por acción u
omisión de integrantes del equipo humano. En la ocurrencia de un evento adverso o
incidente pueden estar involucradas una o varias acciones inseguras:
Las acciones inseguras tienen dos características esenciales:
La atención se aparte de los límites de una práctica segura.
La desviación tiene al menos el potencial directo o indirecto de causar un incidente
o evento adverso para el paciente.
Son ejemplos de acciones inseguras:
No monitorizar, observar o actuar.
Tomar una decisión incorrecta.
No buscar ayuda cuando se necesita.
Contexto Clínico
Condición clínica del paciente en el momento en que se ejecutó la acción insegura
(hemorragia severa, hipotensión progresiva). Ésta información es crucial para entender
las circunstancias del momento en que ocurrió el incidente o el evento adverso.
Factor Contributivo
Condiciones que facilitaron o predispusieron a una acción insegura, por ejemplo:
Paciente muy angustiado, situación que le impide entender instrucciones.
Ausencia de protocolos
Falta de comunicación o experiencia
Mala comunicación entre los miembros del equipo asistencial.
Carga de trabajo inusualmente alta o personal insuficiente para prestar el servicio.
Acción correctiva: Acción tomada para eliminar la causa de un evento adverso o no
conformidad detectada u otra situación indeseable, con el fin de evitar que vuelva a
ocurrir.
Metodología para el análisis de causas: Métodos para detectar la(s) causa(s) raíz de
un evento adverso o no conformidad y de esta forma establecer acciones eficaces para
eliminar dichas causas.
Gestión del riesgo
Es la existencia de procesos de control y seguimiento a los principales riesgos en la
prestación de servicios. (Anexo Técnico 1 de la Resolución 1043 de 2006).
Protocolo de Londres
Es una metodología para la investigación y análisis de riesgos, incidentes y eventos
adversos. El propósito de esta metodología es facilitar la investigación clara y objetiva de
los incidentes clínicos y de los eventos adversos, lo cual implica ir mucho más allá de
simplemente identificar la falla o de establecer quién tuvo la culpa.
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 4 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
5. CONDICIONES DE OPERACIÓN / POLÍTICA DE OPERACIÓN
Todo evento adverso que se presente en el laboratorio clínico del Hospital San
Antonio de Tame debe ser registrado y analizado dado que son oportunidades para
hacer nuestros procesos más seguros y mejorar la calidad de la atención a nuestros
usuarios. Por lo anterior toda persona que detecte la ocurrencia de un incidente o de
un evento adverso debe registrarlo en el formato “GGC-FO-013 Reporte de Incidentes
y Eventos Adversos” e informar al comité de seguridad del paciente de la institución
para que se analice y se establezca el plan de mejoramiento pertinente.
Toda la información que se recolecte y procese en la gestión de eventos adversos es
de tipo confidencial.
Una vez que se ha registrado la ocurrencia del evento adverso en el formato “GGC-
FO-013 Reporte de Incidentes y Eventos Adversos”, se prosigue con la investigación y
análisis del evento adverso. Toda la información referente al incidente o evento
adverso a investigar desde la selección del equipo investigador hasta el cierre del plan
de mejora debe quedar registrada en el “GGC-F0-014 Formato de Análisis de
Incidentes y Eventos Adversos”.
Para la investigación y análisis de los eventos adversos en la organización se utilizará
el Protocolo de Londres.
PASOS PARA APLICAR EL PROTOCOLO DE LONDRES:
1. Identificación y decisión de investigar: Es obvio que el proceso de investigación
y análisis de un incidente supone un paso previo: haberlo identificado. Detrás de la
identificación está el inmenso campo del reporte de los errores y eventos
adversos, el cual, como se ha discutido en otros documentos, solo ocurre en
instituciones que promueven activamente una cultura en la que se puede hablar
libremente de las fallas, sin miedo al castigo, en donde no se sanciona el error
pero si el ocultamiento. Una vez identificado el incidente la institución debe decidir
si inicia o no el proceso. En términos generales, esta determinación se toma
teniendo en cuenta la gravedad del incidente y el potencial aprendizaje
organizacional. Independientemente de los criterios que se utilicen, toda
organización debe hacer explícito los motivos y las circunstancias por las que se
inicia una investigación.
En la institución la decisión de investigar y analizar el evento adverso queda
registrada en el “Reporte de Incidentes y Eventos Adversos”.
2. Selección del equipo investigador: Hay que reconocer que un proceso complejo
como este requiere, además de conocimiento y experiencia en investigación de
incidentes, conocimiento y experiencia clínica específica. Para el caso del
hospital/Centro de Salud el grupo de Investigación de los Eventos Adversos está
integrado por: Director o Coordinador de la Sede, Médico y Enfermero,
Responsable de Seguridad de Paciente toda la entidad, adicional un miembro de
la unidad asistencial donde ocurrió el incidente o el evento adverso. Es importante
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 5 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
que por lo menos uno de los integrantes conozca y aplique metodologías sobre
investigación de eventos adversos.
3. Obtención y organización de información: Todos los hechos, conocimiento y
elementos físicos involucrados deben recolectarse tan pronto como sea posible.
Estos incluyen como mínimo:
*Historia clínica completa
*Protocolos y procedimientos relacionados con incidente o con el evento adverso.
*Declaraciones y observaciones inmediatas.
*Entrevistas con los involucrados
* Evidencia física (planos del piso, listas de turnos, hojas de vida de los equipos
involucrados, etc.).
* Otros aspectos relevantes tales como índice de rotación del personal y
disponibilidad de personal bien adiestrado.
Las declaraciones y observaciones inmediatas son muy valiosas siempre y cuando
se orienten a obtener el tipo de información que se desea tener, para evitar que
sean resúmenes incompletos de la historia clínica. Las declaraciones deben ser
narraciones espontáneas de la percepción individual acerca de lo ocurrido, de la
secuencia de actividades que antecedieron el incidente o el evento adverso, de la
interpretación acerca de cómo esos actividades participaron en el incidente o
evento y de aquellas circunstancias y dificultades que los involucrados enfrentaron
–por ejemplo, equipo defectuoso- y no están descritas en la historia clínica. Las
observaciones referentes a supervisión o soporte insuficiente o inadecuado es
mejor reservarlas para las entrevistas. Esta información debe recolectarse lo más
pronto posible después de ocurrido el incidente o el evento adverso.
Una de las mejores formas de obtener información de las personas involucradas
en incidentes clínicos o eventos adversos son las entrevistas personales. El
equipo investigador decide a quién entrevistar y es responsable de llevarlas a cabo
lo más pronto posible.
El propósito de la es tranquilizar al entrevistado y obtener de él un análisis y unas
conclusiones lo más cercanas a la realidad de los acontecimientos. A continuación
se enuncia de manera esquemática el protocolo que debe seguirse en toda
entrevista que se conduzca durante un proceso de investigación:
Lugar: Privado y relajado, lejos del sitio donde ocurrió el incidente.
El entrevistado puede estar acompañado por quien desee.
Explique el propósito: Explique al entrevistado el motivo de la entrevista. Evite el
estilo confrontacional y los juicios de valor.
Garantícele que lo que diga no va a ser objeto de represalias y va a mantenerse
bajo estricta confidencialidad.
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 6 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
Establezca la cronología del incidente: Identifique el papel del entrevistado en el
incidente o evento adverso y registre el límite de su participación.
Establezca con su ayuda la secuencia de hechos que llevaron al incidente, tal
como él la vivió.
Compare esta información con la secuencia general que se conoce hasta el
momento.
Identifique las acciones inseguras: Explique al entrevistado el significado del
término acción insegura e ilustre el concepto con un ejemplo diferente al caso que
se investiga.
Invite al entrevistado a identificar acciones inseguras relevantes para el caso, sin
preocuparse por si alguien es o no culpable.
Cuando hay protocolos es relativamente fácil identificar no adherencia a
recomendaciones específicas. Recuerde que en la práctica diaria es aceptable
algún grado de variación.
Identifique los factores contributivos: Explique al entrevistado el significado del
término factor los factores contributivos e incentive su identificación sistemática
mediante contributivos ejemplos ilustrativos. Cuando el entrevistado identifica un
factor contributivo pregúntele si es específico para la situación actual o si se trata
de un problema general de la unidad asistencial.
Cierre: Permita que el entrevistado haga todas las preguntas que tenga. Las
entrevistas deben durar entre 20 y 30 minutos.
4. Precise la cronología del incidente o del Evento Adverso a investigar: Las
entrevistas, las declaraciones y las observaciones de quienes participaron de
alguna manera en el incidente, junto a la historia clínica, deben ser suficientes
para establecer qué y cuándo ocurrió.
5. El equipo investigador tiene la responsabilidad de identificar cualquier discrepancia
entre las fuentes. Es útil familiarizarse con alguna de las siguientes metodologías
para precisar las cronología:
Narración: Tanto las entrevistas como la historia clínica proporcionan una
cronología narrativa de lo ocurrido que permite entender cómo se sucedieron los
hechos y cuál fue el papel y las dificultades enfrentadas por los involucrados. Para
el caso de las sedes de la ESE Departamental Moreno y Clavijo, ésta será la
metodología a utilizar.
Diagrama: Los movimientos de personas, materiales, documentos e información
pueden representarse mediante un dibujo esquemático.
Puede ser útil ilustrar la secuencia de hechos como deberían haber ocurrido de
acuerdo con las políticas, protocolos y procedimientos, y compararla con la que
verdaderamente ocurrió cuando se presentó el incidente o el evento adverso.
6. Identifique las acciones inseguras: Una vez identificada la secuencia de
situaciones que condujeron al incidente clínico o al evento adverso, el equipo
investigador debe puntualizar las acciones inseguras. Es probable que algunas se
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 7 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
hayan identificado durante las entrevistas o como producto de la revisión de la
historia clínica. Sin embargo, es útil organizar una reunión con todo el personal
involucrado en el incidente para que entre todos intenten identificar las principales
acciones inseguras. La gente que de alguna manera participó en el incidente o en
el evento adverso usualmente es capaz de identificar el motivo por el cual ocurrió.
El facilitador debe asegurarse de que las acciones inseguras sean conductas
específicas –por acción o por omisión- en lugar de observaciones generales
acerca de la calidad de atención. Es fácil encontrarse con afirmaciones tales como
“mala comunicación” o “trabajo en equipo deficiente”, las cuales pueden ser
características reales del equipo, pero que corresponden a factores contributivos
más que a acciones inseguras. Aunque en la práctica las acciones inseguras y los
factores contributivos se mezclan, es aconsejable no explorar estos últimos hasta
que la lista de las primeras este completa.
La metodología del protocolo de Londres recomienda realizar análisis a las cinco
(5) primeras acciones inseguras más recurrentes en la aparición del evento
adverso objeto de análisis. Por esto en el formato de análisis de incidentes y
eventos adversos se deben identificar mínimo 5 acciones inseguras e identificar
los factores contributivos para cada una de ellas.
7. Identifique los factores contributivos: El paso siguiente es identificar las
condiciones asociadas con cada acción insegura. Cuando se ha identificado un
gran número de acciones inseguras es bueno seleccionar las más importantes y
proceder a analizarlas una a una, dado que cada una tiene su propio conjunto de
factores contributivos. Es posible que cada acción insegura esté asociada a
varios factores contributivos. Por ejemplo:
*Desmotivación (individuo), falta de supervisión (equipo de trabajo) y política de
entrenamiento inadecuada (organización y gerencia). La siguiente tabla muestra
los factores contributivos de las acciones inseguras y su fuente u origen:
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 8 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
Para priorizar los factores contributivos que causaron las condiciones inseguras se
recomienda utilizar la metodología denominada “Espina de Pescado o Diagrama Causa
Efecto”, los resultados de éste análisis se consignan en el gráfico de espina de pescado
que hace parte del formato “GGC-FO-014 análisis de eventos adversos e incidentes” y
luego se registran en el ítem 3 del formato los factores contributivos priorizados. A
continuación se explica cómo se aplica la metodología:
DIAGRAMA CAUSA EFECTO O ESPINA DE PESCADO APLICADO AL ANÁLSIS DE
FACTORES CONTRIBUTIVOS PARA LA OCURRENCIA DE UN EVENTO ADVERSO
a. Ubique en cada espina de pescado los factores contributivos de acuerdo a su origen
(Paciente, Tarea y Tecnología, Individuo que realice la actividad, Equipo humano de
trabajo, Ambiente, Organización y Gerencia, Contexto Institucional):
b. Anote los factores contributivos (causas) que ocasionaron la acción insegura (no
siempre se tienen factores contributivos de los diferentes orígenes):
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 9 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
c. Seleccione los factores contributivos que más impacto tuvieron para que se presentara
la acción insegura y sobre los cuales se centrará el plan de mejoramiento, es decir las
barreras para la seguridad del paciente que implementará la institución:
8. Recomendaciones y plan de acción: La etapa de investigación y análisis termina
con la identificación de los factores contributivos de cada acción insegura. El paso
siguiente es hacer una serie de recomendaciones cuyo propósito es mejorar las
debilidades identificadas. El plan de acción se registra al final del “formato de
análisis de incidentes y eventos adversos” y debe incluir la siguiente información:
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 10 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
*Lista de acciones para enfrentar cada factor contributivo identificado por el equipo
investigador.
*Asignar un responsable de implementar las acciones.
* Definir tiempo de implementación de las acciones.
* Hacer seguimiento a la ejecución del plan.
*Cierre formal cuando la implementación se haya efectuado.
* Fijar fecha de seguimiento para evaluar la efectividad del plan de acción.
El equipo investigador debe ser realista en cuanto a las recomendaciones que
propone con el fin de que se traduzcan en mejoramientos comprobables por toda
la organización. Cuando se plantean es aconsejable tener en cuenta su
complejidad, los recursos que requieren y el nivel de control del que dependen.
En ese orden de ideas se debe categorizar cada recomendación de acuerdo con el
nivel de control del que depende: individual / grupal, local (equipo), departamento /
dirección / organización / autoridad gubernamental y asignar personas con el
estatus administrativo y gerencial adecuado para garantizar su ejecución. De esta
manera se promueve la cultura de seguridad, pues la gente al ver que el proceso
efectivamente conduce a mejoramientos entiende su importancia y se apropia de
él.
6. DESCRIPCIÓN DE ACTIVIDADES
ACTIVIDAD DOCUMENTO /
RESPONSABLE OBSERVACIONES
REGISTRO
Identificar y
Todo el personal
registrar el “GGC-FO-013
asistencial, es
Incidente o el Reporte Eventos En caso de presentarse un Incidente o
responsable de
Evento Adverso Adversos e Evento Adverso, éste debe registrarse en
registrar todo evento
Incidentes”. el formato creado para tal fin.
adverso o incidente
que se presente.
Radicar el Una vez se haya registrado el incidente o
registro del “GGC-FO-013 el evento adverso, éste debe informarse
Responsable de
evento adverso Reporte Eventos a: Líder del servicio o proceso y al
Seguridad del
Adversos e Responsable de Seguridad del Paciente o
Paciente, Asesor
Incidentes”. al Asesor Garantía de Calidad, para
Garantía de Calidad
asignación de consecutivo de control y
trazabilidad.
Definir si se Líder del Servicio o “GGC-FO-013 El Responsable de Seguridad del Paciente
investiga y proceso, Responsable Reporte Eventos o el Asesor Garantía de Calidad de
analiza el de Seguridad del Adversos e acuerdo a la gravedad del incidente o
incidente o el Paciente, Asesor Incidentes”. evento adverso y al potencial aprendizaje
evento adverso? Garantía de Calidad organizacional decide si se investiga o no.
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 11 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
ACTIVIDAD DOCUMENTO /
RESPONSABLE OBSERVACIONES
REGISTRO
La decisión de investigar o no, debe
registrarse en el formato “GGC-FO-013
Reporte Eventos Adversos e Incidentes”.
Si se decide no investigar:
“GGC-FO-013
Definir El responsable del Reporte Eventos El responsable del servicio o proceso
tratamiento al servicio o proceso Adversos e donde ocurrió el incidente define el
incidente donde ocurrió el Incidentes”. tratamiento o corrección a realizar y hace
presentado. incidente. seguimiento a la correcta ejecución.
Si se decide Investigar:
Director / Coordinador De acuerdo al evento adverso o incidente
Definir equipo “Formato de
de Sede, junto con el que se haya decidido investigar el
que investigará y Análisis de
Líder del servicio o Director / Coordinador de Sede, junto con
analizará el Incidentes y
proceso donde ocurrió el Líder del servicio o proceso donde
evento adverso o Eventos
el evento adverso o ocurrió el evento adverso o incidente,
el incidente. Adversos”
incidente. definen quien integrará dicho equipo.
“GGC-FO-014 Analizar la secuencia de situaciones para
Precisar la Formato de establecer exactamente qué y cuándo
cronología del Análisis de ocurrió y registrar el punto 1 del “GGC-
Equipo Investigador
evento adverso o Incidentes y FO-014 Formato de Análisis de Incidentes
incidente Eventos y Eventos Adversos”, donde se describe el
Adversos” evento / incidente ocurrido.
“GGC-FO-014
Identificar las conductas por acción u
Formato de
Identificar las omisión (acciones inseguras) que
Análisis de
acciones Equipo Investigador presentó el personal de salud, en el
Incidentes y
inseguras momento en que sucedió el evento
Eventos
adverso o el incidente.
Adversos”
“GGC-FO-014
Formato de Identificar para cada acción insegura, los
Identificar los
Análisis de factores que contribuyeron a que dicha
factores Equipo Investigador
Incidentes y acción insegura ocasionara el evento
contributivos
Eventos adverso o incidente.
Adversos”
Establecer el plan de mejora, definiendo
“GGC-FO-014
Definir plan de actividades a ejecutar, responsables,
Líder del servicio o Formato de
mejora para los fechas.
proceso donde se Análisis de
factores
presentó el evento Incidentes y
contributivos Una vez elaborado se envía al Asesor
adverso o incidente. Eventos
identificados Garantía de Calidad
Adversos”
Una vez se reciba el “GGC-FO-014
Formato de Análisis de Incidentes y
Eventos Adversos”, el Asesor Garantía de
Revisar y “GGC-FO-014
Asesor Garantía de la la Calidad o el Responsable de Seguridad
proponer ajustes Formato de
Calidad, del Paciente de la Entidad lo revisan y
al plan de Análisis de
Responsable de proponen ajustes al plan de mejoramiento
mejoramiento en Incidentes y
Seguridad del Paciente en caso de ser necesario y lo devuelven al
caso de ser Eventos
de la Entidad. líder del proceso donde ocurrió el evento
necesario Adversos”
adverso o incidente para que lo presente a
Director/ Coordinador de Sede para su
Visto Bueno.
Revisar y dar Director / Coordinador “GGC-FO-014 El Directo / Coordinador de Sede revisa el
Visto Bueno o de Sede Formato de Plan de Mejoramiento propuesto, en caso
proponer ajustes Análisis de de estar de acuerdo con el mismo le da su
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 12 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
ACTIVIDAD DOCUMENTO /
RESPONSABLE OBSERVACIONES
REGISTRO
Visto Bueno, para que se ejecute. Si para
ejecutar el plan se requiere de la Gestión
de la Gerencia, se deberá enviar el Plan a
Subgerencia en salud para que lo haga
llegar a Gerencia y se analice y defina si
se ejecuta lo allí contenido o proponen
otras actividades que igual actúen sobre
Incidentes y las causas que ocasionaron el evento
al plan de
Eventos adverso, para evitar que vuelva a
mejoramiento
Adversos” presentarse y se afecte la seguridad del
usuario. Una vez aprobado por Gerencia
(cuando se requiera), el Subgerente
informa al Director / Coordinador de Sede,
para que éste a su vez lo transmita al líder
del servicio o proceso donde ocurrió el
evento adverso para que inicie la ejecución
de las acciones contenidas en el plan.
El Asesor Garantía de Calidad o
“GGC-FO-014
responsable de Seguridad del Paciente de
Realizar Asesor Garantía de Formato de
la Entidad, realiza seguimiento al
seguimiento y Calidad o responsable Análisis de
cumplimiento de las actividades y
cierre del plan de de Seguridad del Incidentes y
planteadas y establezca la eficacia o no
mejora Paciente de la Entidad. Eventos
del plan de mejora ejecutado y procede a
Adversos”
su cierre.
Mensualmente en el Comité Integrado de
Gestión el Asesor Garantía de Calidad
informa sobre los eventos adversos que se
han presentado en las sedes, los planes
de mejora implementados y el avance en
la ejecución de los mismos y las
situaciones en donde no se hayan
Informe planes Asesor Garantía de
ejecutado las acciones del plan de
de mejora Calidad o responsable
Informe mejoramiento.
derivados de de Seguridad del
eventos adversos Paciente de la Entidad.
Así mismo en conjunto con el responsable
de Seguridad del Paciente de la entidad,
deberán llevar propuestas para gestionar
los eventos adversos que se presentan
con mayor frecuencia en todas las sedes o
de mayor impacto negativo en seguridad
del paciente.
LISTADO DE POSIBLES EVENTOS ADVERSOS EN LOS DIFERENTES SERVICIOS
OFERTADOS.
LABORATORIO CLINICO
Extravasaciones, hematomas y/o equimosis luego de toma de muestra sanguínea
Lipotimias.
Múltiples punciones.
Procesar muestras con reactivos vencidos.
Falta de oportunidad para la remisión de muestras a laboratorios de referencia.
Inoportunidad en la entrega de resultados.
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 13 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
Pérdida de muestras por caída de un tubo o ruptura del mismo.
Necesidad de repetición de una prueba de laboratorio por deficiencias en la información
suministrada al paciente (orinas contaminadas, falsos positivos por falta de ayuno en glicemias
o perfiles lipídicos, etc.)
Falla en la trascripción de un reporte.
Fallar en la identificación de las muestras.
Coagulación de muestra sanguínea por error en la selección del tubo o mala calidad del mismo
Inoportunidad en la atención por falta de reactivos, insumos o daño de equipos
Resultados intercambiados entre pacientes.
Resultados de exámenes no solicitados.
7. REGISTROS QUE SE GENERAN
o “GGC-FO-013 Reporte de Eventos Adversos e Incidentes”
o “ GGC-FO-014 Análisis de Eventos Adversos e Incidentes”
8. DOCUMENTOS DE REFERENCIA
o Pautas de Auditoría para el Mejoramiento de la Calidad en la Atención de Salud de
2007. (Ministerio de la Protección Social).
o Protocolo de Londres. Traducción con modificaciones por los doctores Julio
Portecarrero y Sergio H. Luengas del Centro de Gestión Hospitalaria del
documentoSystem Analysis of clinical incidents: the London protocol. Autores:
Sally Taylor – Adams y Charles Vincent (Clinical Safety Research Unit, Imperial
College London, UK).
APROBACIÓN Y CONTROL DE CAMBIOS DEL DOCUMENTO
ELABORÓ REVISÓ APROBÓ
FIRMA:
NOMBRE: DIANA CAROLINA MEDINA MUR
CARGO: COORDINADORA LAB CLINICO
FECHA: 11/2016
ELABORÓ REVISÓ APROBÓ
FIRMA:
NOMBRE: DIANA CAROLINA MEDINA MUR
CARGO: COORDINADORA LAB CLINICO
FECHA: 11/2016
ELABORADO POR: REVISADO POR: APROBADO POR:
SISTEMA INTEGRADO DE GESTIÓN CODIGO: GGC-PR-001 LAB
EDICION: Versión 01
MANUAL DE LABORATORIO CLINICO FECHA: 2016
PROCEDIMIENTO PARA LA IDENTIFICACION Y PAGINA: Página 14 de 14
GESTION DE EVENTOS ADVERSOS E INCIDENTES VIGENCIA: 2016 - 2018
VERSIÓN FECHA DESCRIPCIÓN DEL CAMBIO
01 Abril 2018 Emisión del Documento
02
02
ELABORADO POR: REVISADO POR: APROBADO POR:
S-ar putea să vă placă și
- Guia de Seguridad II Del Paciente VII Semestre Pascual HerreraDocument15 paginiGuia de Seguridad II Del Paciente VII Semestre Pascual Herrerapaascual100% (1)
- PROTOCOLO DE EVENTOS ADVERSOS - ActulaizadoDocument23 paginiPROTOCOLO DE EVENTOS ADVERSOS - ActulaizadoDiana Isabel Soriano Arreaga100% (2)
- Manual Seguridad Del PacienteDocument14 paginiManual Seguridad Del PacientePIEDAD GONZALEZ100% (1)
- Diagramas de VennDocument10 paginiDiagramas de VennSulma Hernandez100% (1)
- Pa Gas PG 01 PR 01 Procedi Gestion de Reporte de Evento AdversoDocument15 paginiPa Gas PG 01 PR 01 Procedi Gestion de Reporte de Evento AdversoRigoberto PeñaÎncă nu există evaluări
- 2 - Manual de Manejo de Evento Adverso Ante, Durante y Después de La Toma de MuestraDocument17 pagini2 - Manual de Manejo de Evento Adverso Ante, Durante y Después de La Toma de MuestraMARIA ALEJANDRA OTALORA SANABRIAÎncă nu există evaluări
- Protocolo de Notificacion de Eventos Relacionados Con La Seguridad Del Paciente. CS 1 2020Document14 paginiProtocolo de Notificacion de Eventos Relacionados Con La Seguridad Del Paciente. CS 1 2020José Miguel Reinosa IbarraÎncă nu există evaluări
- Manual Seguridad Paciente LaEstanciaDocument34 paginiManual Seguridad Paciente LaEstanciaEnmanuel ValeroÎncă nu există evaluări
- Ac-G-04 Programa de Seguridad Del PacienteDocument10 paginiAc-G-04 Programa de Seguridad Del PacienteKatherineÎncă nu există evaluări
- PDP-02 PROCEDIMIENTO PARA EL MANEJO DE EVENTO ADVERSO Rv.0Document15 paginiPDP-02 PROCEDIMIENTO PARA EL MANEJO DE EVENTO ADVERSO Rv.0Ema CotesÎncă nu există evaluări
- Practica - Segura - Notificacion - de - Eventos - Adversos 8Document3 paginiPractica - Segura - Notificacion - de - Eventos - Adversos 8Nico MurilloÎncă nu există evaluări
- Politica Seguridad Paciente PDFDocument10 paginiPolitica Seguridad Paciente PDFAngelica Mayerli PENA PENAÎncă nu există evaluări
- Evento AdversoDocument16 paginiEvento AdversoMarcela100% (2)
- Protocolo de Seguridad Del PacienteDocument12 paginiProtocolo de Seguridad Del PacienteKarina PaolaÎncă nu există evaluări
- Seuridad Del Paciente PDFDocument234 paginiSeuridad Del Paciente PDFkaro_526100% (1)
- Global Trigger ToolsDocument21 paginiGlobal Trigger ToolsDanielaGarciaÎncă nu există evaluări
- Trabajo Eventos Adversos Revision 1Document14 paginiTrabajo Eventos Adversos Revision 1YULIMEY CORTESÎncă nu există evaluări
- Plan de Seguridad Del PacienteDocument8 paginiPlan de Seguridad Del PacienteshaomiriverosquispeÎncă nu există evaluări
- PC03. Procedimiento para La Medición Reporte Análisis y Gestión de Eventos Adversos V 2Document13 paginiPC03. Procedimiento para La Medición Reporte Análisis y Gestión de Eventos Adversos V 2pradabertha47Încă nu există evaluări
- GCL 2.2 Ed. 4 Prevencion de CaidasDocument18 paginiGCL 2.2 Ed. 4 Prevencion de CaidasSilent princessÎncă nu există evaluări
- Protocolo de Manejo de Reacciones Adversas Antes Durante y Despues.Document12 paginiProtocolo de Manejo de Reacciones Adversas Antes Durante y Despues.Pedro L. TuiranÎncă nu există evaluări
- Pausa QuirurgicaDocument5 paginiPausa QuirurgicaSolÎncă nu există evaluări
- Procedimiento para Seguridad en El PacienteDocument10 paginiProcedimiento para Seguridad en El PacienteFanny MorantesÎncă nu există evaluări
- GCL 2.3 - Programa de Vigilancia de Eventos Adversos Asociados A La Atención PDFDocument13 paginiGCL 2.3 - Programa de Vigilancia de Eventos Adversos Asociados A La Atención PDFNicole Constanza Reyes HidalgoÎncă nu există evaluări
- Sistemas de Registro y NotificacionDocument17 paginiSistemas de Registro y Notificacionesteban quitoÎncă nu există evaluări
- Presentacion Proframa de Tecnovigilancia 2022Document35 paginiPresentacion Proframa de Tecnovigilancia 2022iansamuelmontealegreÎncă nu există evaluări
- Clase 3 Eventos Adversos Error y Nueve AccionesDocument22 paginiClase 3 Eventos Adversos Error y Nueve AccionesRankaÎncă nu există evaluări
- Instrumentos Incidentes Eventos AdversosDocument16 paginiInstrumentos Incidentes Eventos AdversosUsagui MoonÎncă nu există evaluări
- Procedimento Control de Eventos Adversos 2021Document6 paginiProcedimento Control de Eventos Adversos 2021Mario Fernando Villota EsparzaÎncă nu există evaluări
- Pds-p-01 Procedimiento para El Manejo de Eventos AdversosDocument17 paginiPds-p-01 Procedimiento para El Manejo de Eventos AdversosNelsy Rojas QuesadaÎncă nu există evaluări
- Guia de Reporte de Eventos AdversosDocument11 paginiGuia de Reporte de Eventos AdversosAdriana BaenaÎncă nu există evaluări
- 1.protocolo de Seguridad Del PacienteDocument6 pagini1.protocolo de Seguridad Del PacienteMaria Elena Aguirre RamirezÎncă nu există evaluări
- Seguridad Del PacienteDocument19 paginiSeguridad Del PacienteSalvador CeronÎncă nu există evaluări
- 4.-Plan y Programas de Seguridad Del Paciente PDFDocument20 pagini4.-Plan y Programas de Seguridad Del Paciente PDFMaximiliano Villasana LahmannÎncă nu există evaluări
- Segurida Del Pte en El Contexto GeneralDocument5 paginiSegurida Del Pte en El Contexto GeneralSandra SanchezÎncă nu există evaluări
- Marco Conceptual de La Habilitación - Seguridad Del Paciente - Practicas Seguras en El SUHDocument9 paginiMarco Conceptual de La Habilitación - Seguridad Del Paciente - Practicas Seguras en El SUHdianacarolinarodriguezuribeÎncă nu există evaluări
- Acciones Esenciales PDFDocument6 paginiAcciones Esenciales PDFDaniela LaraÎncă nu există evaluări
- Gestión Del Evento AdversoDocument20 paginiGestión Del Evento AdversoCarlos Mario Miranda Sanchez100% (1)
- Seguridad Del PacienteDocument11 paginiSeguridad Del PacienteVALENTINA VASQUEZ ARTEAGAÎncă nu există evaluări
- Eventos Adversos y TecnovigilanciaDocument59 paginiEventos Adversos y TecnovigilanciaValezca Chavarria100% (1)
- Proceso de Notificación, Análisis y AprendizajeDocument15 paginiProceso de Notificación, Análisis y Aprendizajeoddrex87Încă nu există evaluări
- Seguridad Al PacienteDocument6 paginiSeguridad Al PacienteFernanda Cadena0% (1)
- Definiciones Clinicas EditadoDocument4 paginiDefiniciones Clinicas Editadobrandon martin aguilar becerraÎncă nu există evaluări
- Conceptoa - AdaraDocument5 paginiConceptoa - AdaraGALILEA TRUJILLOÎncă nu există evaluări
- Campañas ClinicasDocument6 paginiCampañas ClinicasMaty BustoÎncă nu există evaluări
- Programa Paciente Seguro PDFDocument23 paginiPrograma Paciente Seguro PDFjairo españaÎncă nu există evaluări
- Admin MedDocument51 paginiAdmin MedJose Fernández100% (1)
- Acta Primer Trimestre 2021Document3 paginiActa Primer Trimestre 2021FernandaGuapucalÎncă nu există evaluări
- Taller de EmergenciasDocument3 paginiTaller de EmergenciasNestor PetroloÎncă nu există evaluări
- Evento AdversoDocument7 paginiEvento Adversoluisa fernanda sanabria ariasÎncă nu există evaluări
- Guia de Auditoria ConcurrenteDocument9 paginiGuia de Auditoria ConcurrenteAmaury FernandezÎncă nu există evaluări
- Calidad y Seguridad Del PacienteDocument20 paginiCalidad y Seguridad Del PacienteAyala Nuñez MiriamÎncă nu există evaluări
- Acciones EsencialesDocument7 paginiAcciones EsencialesReynaldo GuzmanÎncă nu există evaluări
- Evento Adverso - Reporte y AnalisisDocument71 paginiEvento Adverso - Reporte y AnalisisMarlon Manjarres MindiolaÎncă nu există evaluări
- Clase 4 Modulo 2Document12 paginiClase 4 Modulo 2Jorge Lorke Castillo CortezÎncă nu există evaluări
- Evento AdversoDocument13 paginiEvento AdversoHaide RamosÎncă nu există evaluări
- Boletin Seguridad en El Paciente 12 - 2022 PDFDocument2 paginiBoletin Seguridad en El Paciente 12 - 2022 PDFLina TobarÎncă nu există evaluări
- OudiDocument46 paginiOudiAldito AC100% (1)
- Seguridad Del Paciente. SINTESISDocument8 paginiSeguridad Del Paciente. SINTESISKarina GarcíaÎncă nu există evaluări
- Valoración inicial del paciente en urgencias o emergencias sanitarias. SANT0208De la EverandValoración inicial del paciente en urgencias o emergencias sanitarias. SANT0208Încă nu există evaluări
- Guía-Temario formación en servicio de vigilancia privada en centros hospitalariosDe la EverandGuía-Temario formación en servicio de vigilancia privada en centros hospitalariosÎncă nu există evaluări
- Costos de SaludDocument11 paginiCostos de SaludKtalina BeltranÎncă nu există evaluări
- Manual de Atencion Al UsuarioDocument26 paginiManual de Atencion Al UsuarioKtalina Beltran100% (1)
- Punto de EquilibrioDocument24 paginiPunto de EquilibrioKtalina BeltranÎncă nu există evaluări
- Procedimiento de Transporte de Hemocomponentes en ColombiaDocument13 paginiProcedimiento de Transporte de Hemocomponentes en ColombiaKtalina BeltranÎncă nu există evaluări
- Cs M TB 01 Caracteriz Banco de Sangre v2Document10 paginiCs M TB 01 Caracteriz Banco de Sangre v2Ktalina BeltranÎncă nu există evaluări
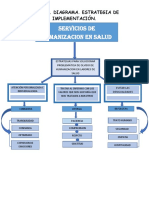
- AA3 EV01 Diagrama Estrategia de ImplementacionDocument1 paginăAA3 EV01 Diagrama Estrategia de ImplementacionKtalina Beltran100% (1)
- AA3 EV01 Diagrama Estrategia de ImplementacionDocument1 paginăAA3 EV01 Diagrama Estrategia de ImplementacionKtalina Beltran100% (1)
- Anti-H Lectin SpanishDocument2 paginiAnti-H Lectin SpanishKtalina BeltranÎncă nu există evaluări
- Balance GeneralDocument1 paginăBalance GeneralKtalina BeltranÎncă nu există evaluări
- APTr 1.3 APDs Procedimiento Trazabilidad UMT V2 2016Document10 paginiAPTr 1.3 APDs Procedimiento Trazabilidad UMT V2 2016Ktalina BeltranÎncă nu există evaluări
- New Guia Nutri MXDocument7 paginiNew Guia Nutri MXKtalina BeltranÎncă nu există evaluări
- Directorio Bancos Sangre Colombia 2021Document12 paginiDirectorio Bancos Sangre Colombia 2021Ktalina BeltranÎncă nu există evaluări
- Manual Del Servicio Al Cliente2.Document30 paginiManual Del Servicio Al Cliente2.Ktalina BeltranÎncă nu există evaluări
- Resolución 132 de 2006Document18 paginiResolución 132 de 2006Ktalina BeltranÎncă nu există evaluări
- Ciencias Auxiliares de La ArchivisticaDocument7 paginiCiencias Auxiliares de La ArchivisticaAnonymous Vq1TGrÎncă nu există evaluări
- Platon ArmoniaDocument16 paginiPlaton ArmoniaAna María Dávila GarcíaÎncă nu există evaluări
- Conv 1 05 Formato de Curriculum VitaeDocument7 paginiConv 1 05 Formato de Curriculum VitaeJhonny GutierrezÎncă nu există evaluări
- IV-4g-Mate - Máximo Común - SesiónDocument3 paginiIV-4g-Mate - Máximo Común - SesiónRosa Cusco DelgadoÎncă nu există evaluări
- CABA Manual Práctico de Diseño Universal - Basado en La Ley 962Document80 paginiCABA Manual Práctico de Diseño Universal - Basado en La Ley 962Gustavo VázquezÎncă nu există evaluări
- Experiencia de Aprendizaje N - 3Document6 paginiExperiencia de Aprendizaje N - 3박민서Încă nu există evaluări
- Formato de Entrevista Semiestructurada Al Experto en Terapia Familiar ALEXISDocument4 paginiFormato de Entrevista Semiestructurada Al Experto en Terapia Familiar ALEXISSuly CastilloÎncă nu există evaluări
- Números RacionalesDocument3 paginiNúmeros RacionalesEstrella Abigail Rodriguez PerezÎncă nu există evaluări
- Plan de Evaluación 1Document2 paginiPlan de Evaluación 1Pame ArlethÎncă nu există evaluări
- Resumen Del Programa para Embajadas y Organismos InternacionalesDocument4 paginiResumen Del Programa para Embajadas y Organismos InternacionalesRichar UviedaÎncă nu există evaluări
- Guia Grado 6° JunioDocument12 paginiGuia Grado 6° JunioDiana carmonaÎncă nu există evaluări
- Psicologia Uno Dos TresDocument2 paginiPsicologia Uno Dos TresMarcelYoshiraÎncă nu există evaluări
- Diseño Del Red: Figuras LiterariasDocument16 paginiDiseño Del Red: Figuras LiterariasAdriana BallesterosÎncă nu există evaluări
- Vidal, Marciano - Moral de Opcion Fundamental y de ActitudesDocument115 paginiVidal, Marciano - Moral de Opcion Fundamental y de ActitudesJuan Jo100% (1)
- Guía de Autoaprendizaje # 3 (1) Desarrollo EvolutivoDocument10 paginiGuía de Autoaprendizaje # 3 (1) Desarrollo EvolutivoRitamariaMeylanÎncă nu există evaluări
- Planeación Ignirida LozanoDocument43 paginiPlaneación Ignirida LozanoJackeline Ariza UsecheÎncă nu există evaluări
- Educacion para La Igualdad, GrupalDocument5 paginiEducacion para La Igualdad, GrupalBRYAN STEVEN SORIANO DAVILAÎncă nu există evaluări
- Platon - El BanqueteDocument102 paginiPlaton - El BanqueteCar Armar ArmarÎncă nu există evaluări
- Prestacion Servicio Social UnadistaDocument7 paginiPrestacion Servicio Social UnadistaFernanda RubioÎncă nu există evaluări
- Proceso AdministrativoDocument4 paginiProceso AdministrativoKerlis MendozaÎncă nu există evaluări
- Empresa Sistema AbiertoDocument12 paginiEmpresa Sistema AbiertoJhony PinedaÎncă nu există evaluări
- .... ProgramasAsignaturas Titulacion 5102 AsigUMA 50994 PDFDocument5 pagini.... ProgramasAsignaturas Titulacion 5102 AsigUMA 50994 PDFFrancisco MorenoÎncă nu există evaluări
- La Cohesion y El Rendimiento en Deportes de EquipoDocument7 paginiLa Cohesion y El Rendimiento en Deportes de EquipoAlejandra AnzeÎncă nu există evaluări
- ANEXO Actividad.Document6 paginiANEXO Actividad.Julio Ernesto TrinidadÎncă nu există evaluări
- Sesion 3 - Diseño OrganizacionalDocument38 paginiSesion 3 - Diseño Organizacionallincol huaman lopezÎncă nu există evaluări
- Maestría - Proyecto de InvestigaciónDocument29 paginiMaestría - Proyecto de Investigaciónsamuel100% (1)
- Jean PiagetDocument19 paginiJean PiagetCarlos Andres Yerovi PerezÎncă nu există evaluări
- El Resumen - DiapositivaDocument12 paginiEl Resumen - DiapositivaThebioscityÎncă nu există evaluări
- Ficha 3 MatemáticasDocument6 paginiFicha 3 MatemáticasdavidÎncă nu există evaluări