Documente Academic
Documente Profesional
Documente Cultură
Segundo Examen Parcial de Quimica
Încărcat de
Wiliams Pineda0 evaluări0% au considerat acest document util (0 voturi)
272 vizualizări2 paginiEste documento presenta un examen de química sobre la tabla periódica y los conceptos fundamentales asociados con ella, incluidos los enlaces químicos, la estructura atómica y las propiedades de los elementos. El examen consta de 15 preguntas de selección múltiple sobre temas como la clasificación de los elementos, las propiedades de los grupos y períodos, y los tipos de enlaces químicos. También incluye ejercicios para identificar elementos en una sopa de letras y representar las estruct
Descriere originală:
parcial
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentEste documento presenta un examen de química sobre la tabla periódica y los conceptos fundamentales asociados con ella, incluidos los enlaces químicos, la estructura atómica y las propiedades de los elementos. El examen consta de 15 preguntas de selección múltiple sobre temas como la clasificación de los elementos, las propiedades de los grupos y períodos, y los tipos de enlaces químicos. También incluye ejercicios para identificar elementos en una sopa de letras y representar las estruct
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
272 vizualizări2 paginiSegundo Examen Parcial de Quimica
Încărcat de
Wiliams PinedaEste documento presenta un examen de química sobre la tabla periódica y los conceptos fundamentales asociados con ella, incluidos los enlaces químicos, la estructura atómica y las propiedades de los elementos. El examen consta de 15 preguntas de selección múltiple sobre temas como la clasificación de los elementos, las propiedades de los grupos y períodos, y los tipos de enlaces químicos. También incluye ejercicios para identificar elementos en una sopa de letras y representar las estruct
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 2
COLEGIO DE BACHILLERES DE TABASCO, Plantel #23
Villa El Triunfo, Balancán, Tabasco.
SEGUNDO PARCIAL DE QUÍMICA I
Nombre: ___________________________________ Grupo: ______ Turno: ___________
Profesora: Q. F. B. Anabell Durán Pliego
I. Coloca en el paréntesis la letra que indique la respuesta correcta.
1. Los elementos en la clasificación periódica se agrupan en orden creciente de su: ( )
a) masa atómica b) masa molecular c) número atómico d) peso atómico
2. Los elementos de una familia tienen propiedades químicas semejantes, y generalmente el número del
grupo nos da a conocer el número de electrones que el elemento posee en su último nivel; éstos se
conocen con el nombre de: ( )
a) Isótopos b) niveles de energía c) periodo químico d) electrones de valencia
3. Los elementos del grupo IA se caracterizan por tener en su último nivel: ( )
a) 7 electrones b) 1 electrón c) 2 electrones d) 8 electrones
4. La tabla periódica en su forma actual ha sido dividida en: ( )
a) 4 regiones o bloques s, p, d, f
b) b) 7 regiones o bloques J, K, L, M, N, O, P
c) 3 regiones o bloques s, p, d
d) 2 regiones o bloques s, p
5. Si tenemos un elemento que pertenece al grupo II A y al periodo 3 debe tener la siguiente
configuración electrónica:
( )
a) 1s2 2s2 2p6 3s1 3p1 b) 1s2 2s2 2p5 3s2
c) 1s2 2s2 2p6 3s2 d) 1s2 2s1 2p5 3s2
6. Conjunto de elementos que presentan a su electrón diferencial en el mismo subnivel de energía, se
conoce con el nombre de: ( )
a) Periodo b) bloque c) clase d) grupo
7. Es la herramienta más útil para un químico: ( )
a) Bloque b) Periodo c) Tabla periódica d) Grupo
8. Es la distancia comprendida entre el centro del núcleo y el nivel externo de un átomo: ( )
a) electronegatividad b) radio atómico c) afinidad electrónica d) radio iónico
9. Es la representación ordenada de los elementos que permite visualizar y predecir cómo varían sus
propiedades físicas y químicas: ( )
a) tabla periódica b) bloque c) periodo d) grupo
10. Son los elementos más electronegativos: ( )
a) K, Sr, Bi b) Ca, Mg, Be c) Fr, Cs, Ba d) F, O, Cl
11. Tipo de enlace que resulta de la unión de dos átomos mediante la compartición de un par de
electrones:
………………………………………………………………………………………………………………( )
a) iónico b) covalente c) metálico d) puente de hidrógeno
12. Enlace en donde se tienen cationes ordenados que comparten cargas sumergidas en un mar de
electrones: …..………………………………………………………………………………………….. ( )
a) puente de hidrógeno b) covalente polar c) metálico d) iónico
13. ¿Cómo se llama la capacidad que tiene un átomo o conjunto de átomos para unirse a otro átomo o
conjunto de átomos y formar un compuesto? ………………………………………………………..( )
a) Electronegatividad b) Potencial de ionización c) Enlace químico d) Diferencia de potencial
14. La regla del octeto de Lewis expresa que: ……………………………………………………………( )
a) Al unirse dos átomos lo hacen en proporción de uno a ocho.
b) Un átomo siempre pierde 8 electrones.
c) Los átomos al reaccionar entre sí tienden a completar la estructura del gas noble más próximo en la
tabla periódica.
COLEGIO DE BACHILLERES DE TABASCO, Plantel #23
Villa El Triunfo, Balancán, Tabasco.
SEGUNDO PARCIAL DE QUÍMICA I
Nombre: ___________________________________ Grupo: ______ Turno: ___________
Profesora: Q. F. B. Anabell Durán Pliego
15. Para que se forme un enlace iónico, se requiere la presencia de: (
)
a) dos metales b) hidrógeno c) un metal y un no metal d) oxígeno
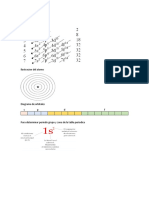
II. Localiza nueve de los elementos químicos en la siguiente sopa de letras, escribe el nombre y el símbolo de
los elementos localizados:
NOMBRE Símbolo
1.
2.
3.
4.
5.
6.
7.
8.
9.
III. Contesta las siguientes preguntas:
1. ¿Qué es enlace químico?
2. ¿Cuáles son los electrones de valencia?
3. Indica en el siguiente esquema cuál es la fórmula condensada, semidesarrollada y desarrollada,
respectivamente:
IV. Realizar la estructura
de lewis de los
siguientes elementos
(Mg y Li), realizando
cada paso como lo
hicimos en clase:
PASO 1: Símbolo y Número atómico (Z)
PASO 2: Configuración electrónica
PASO 3: Resaltar los electrones ubicados en el último nivel de energía o conocidos como electrones de valencia
PASO 4: Representación gráfica de la estructura de Lewis
S-ar putea să vă placă și
- Examen CIENCIAS Bloque 2 TelesecundariaDocument3 paginiExamen CIENCIAS Bloque 2 TelesecundariaBelgica Beltran MoralesÎncă nu există evaluări
- Ejercicios de Enlaces Quimicos ResueltosDocument4 paginiEjercicios de Enlaces Quimicos ResueltosLeidy Johana Cely RojasÎncă nu există evaluări
- Taller - Nomenclatura - Quimica - Inorganica y Tipos de Reacciones PDFDocument6 paginiTaller - Nomenclatura - Quimica - Inorganica y Tipos de Reacciones PDFThePigmanDarkÎncă nu există evaluări
- ¿Cómo Comprobar Las Leyes de Los Gases?Document4 pagini¿Cómo Comprobar Las Leyes de Los Gases?Fredy Alexander CastroÎncă nu există evaluări
- Guía de Factor Unitario y TemperaturaDocument2 paginiGuía de Factor Unitario y Temperaturalesly virginia castilloÎncă nu există evaluări
- Quimica para Curso para Examen de Admisión de Facultad de Ciencias QuímicasDocument33 paginiQuimica para Curso para Examen de Admisión de Facultad de Ciencias QuímicasHector Aguilar LopezÎncă nu există evaluări
- Remedial ExamenDocument8 paginiRemedial ExamenAnonymous k76mSIuNÎncă nu există evaluări
- Práctica 1 Célula VegetalDocument8 paginiPráctica 1 Célula VegetalPablo CruzÎncă nu există evaluări
- Evaluación Formativa-Modelos Atómicos ProcesoDocument5 paginiEvaluación Formativa-Modelos Atómicos ProcesoYerti Letelier100% (1)
- Temario Quimica GeneralDocument2 paginiTemario Quimica GeneralHUBERT RODRIGUEZ OREÎncă nu există evaluări
- 2 - Ejercicios - Masa Atomica - IsotoposDocument2 pagini2 - Ejercicios - Masa Atomica - IsotoposTatiana CainÎncă nu există evaluări
- El AtomoDocument2 paginiEl AtomoJOSE CARLOS VARGAS CALLISAYAÎncă nu există evaluări
- S - 4 Ejercicios Semana 3 (2Document6 paginiS - 4 Ejercicios Semana 3 (2López BlasÎncă nu există evaluări
- Taller Fuerzas IntermolecularesDocument9 paginiTaller Fuerzas IntermolecularesDina Judith CarpÎncă nu există evaluări
- Enlace Covalente EjerciciosDocument2 paginiEnlace Covalente EjerciciosRaul Anyosa LujanÎncă nu există evaluări
- 2.QUIM Segunda DE SEGUNDODocument4 pagini2.QUIM Segunda DE SEGUNDOAndrea Catuto100% (1)
- Unidad III Química IDocument8 paginiUnidad III Química IGracielaÎncă nu există evaluări
- Clase Geometria MolecularDocument65 paginiClase Geometria MoleculartortillasdemaizÎncă nu există evaluări
- Configuración ElectrónicaDocument25 paginiConfiguración ElectrónicaC & H CONSTRUCTORESÎncă nu există evaluări
- Guia #1 Reforzamiento de QuimicaDocument2 paginiGuia #1 Reforzamiento de QuimicaAly Aravena100% (1)
- Ejercicios de ElectromagnetismoDocument7 paginiEjercicios de ElectromagnetismojoseÎncă nu există evaluări
- Actividades Repaso Unidad 2Document4 paginiActividades Repaso Unidad 2Carolina100% (1)
- Ejercicios de Tabla PeriodicaDocument3 paginiEjercicios de Tabla PeriodicaAlcides Hermoza MejiaÎncă nu există evaluări
- Química IDocument10 paginiQuímica ICesaro LoquendoÎncă nu există evaluări
- Práctica #6Document5 paginiPráctica #6ANGELA CECILIA MATIENZO FLORESÎncă nu există evaluări
- Mitosis Lenin IsabelaDocument7 paginiMitosis Lenin IsabelaIsabela Chapoñan Casas100% (1)
- Estructura de LewisDocument10 paginiEstructura de Lewismaggy26Încă nu există evaluări
- 2do Parcial Quimica-I 2023-1Document3 pagini2do Parcial Quimica-I 2023-1Jimena Ramírez OsornoÎncă nu există evaluări
- TP N 2 Sistemas Materiales 1Document1 paginăTP N 2 Sistemas Materiales 1valkiriaaÎncă nu există evaluări
- Evaluacion de QuimicaDocument4 paginiEvaluacion de Quimicamprm2579Încă nu există evaluări
- 05 Sistema Peri DicoDocument7 pagini05 Sistema Peri Dicomiruiz12113281100% (1)
- Atmomos PDFDocument2 paginiAtmomos PDFVianis AriasÎncă nu există evaluări
- Taller Estados de Oxidacion 8° AbDocument11 paginiTaller Estados de Oxidacion 8° Abedgar dario badillo maciasÎncă nu există evaluări
- Prueba de Quimica MayoDocument3 paginiPrueba de Quimica MayonataliacolegioÎncă nu există evaluări
- Práctica. Radio Iónico y Especies IsoelectrónicasDocument5 paginiPráctica. Radio Iónico y Especies IsoelectrónicasAlessandro VillafuerteÎncă nu există evaluări
- Tema-Tabla Periodica de Los Elementos QuimicosDocument3 paginiTema-Tabla Periodica de Los Elementos QuimicosAlfredo FernandezÎncă nu există evaluări
- Evaluacion - Enlace-Ionico 2 (Recuperado Automáticamente) (2305843009215748719)Document1 paginăEvaluacion - Enlace-Ionico 2 (Recuperado Automáticamente) (2305843009215748719)Nury Lizarazo Albarracin100% (1)
- Cinetica Química PDFDocument5 paginiCinetica Química PDFHector Tineo100% (1)
- HadronesDocument4 paginiHadronesLuisão Almache CabreraÎncă nu există evaluări
- Ejercicios Formulación de Compuestos InorgánicosDocument12 paginiEjercicios Formulación de Compuestos InorgánicosTelmo Bastidas PrietoÎncă nu există evaluări
- Antecedentes de La Tabla Periódica ActualDocument4 paginiAntecedentes de La Tabla Periódica ActualSteffany AguilarÎncă nu există evaluări
- 2do Examen Parcial - La Materia y Sus Interacciones RespuestasDocument2 pagini2do Examen Parcial - La Materia y Sus Interacciones RespuestasFernando LeónÎncă nu există evaluări
- Guia TP Alquenos y Alquinos - Parte 1docxDocument2 paginiGuia TP Alquenos y Alquinos - Parte 1docxIngrid Dahiana Medina Maidana100% (1)
- Cantidad de Sustancia. El Mol (Resumen)Document13 paginiCantidad de Sustancia. El Mol (Resumen)lazaroclaudiaÎncă nu există evaluări
- Guia N 1 Balanceo de Ecuaciones QuimicasDocument4 paginiGuia N 1 Balanceo de Ecuaciones QuimicasCristian GonzálezÎncă nu există evaluări
- Examen de Recuperacion 11Document2 paginiExamen de Recuperacion 11freddymondragon100% (1)
- Banco de Preguntas T de Los GasesDocument18 paginiBanco de Preguntas T de Los GasesCésar HJ0% (1)
- Estructuras de Lewuis Con Cargas Formales.Document6 paginiEstructuras de Lewuis Con Cargas Formales.Zyanya MendozaÎncă nu există evaluări
- Trabajo 4Document10 paginiTrabajo 4RogerÎncă nu există evaluări
- Monohibridismo y DihibridismoDocument5 paginiMonohibridismo y DihibridismoMadafaking ClipsÎncă nu există evaluări
- Ejercicio Numeros Cuanticos PDFDocument2 paginiEjercicio Numeros Cuanticos PDFMariza Martina Camones MaguiñaÎncă nu există evaluări
- Ejercicios de MolDocument1 paginăEjercicios de MolMEGAN SUMMERÎncă nu există evaluări
- Plan de Nivelacion de QuimicaDocument13 paginiPlan de Nivelacion de QuimicaLiliana Rey Osorio100% (1)
- Presentacion Enlace QuimicoDocument33 paginiPresentacion Enlace QuimicoTio InataÎncă nu există evaluări
- 01-Ejercicios - Configuración Electronica y Propiedades PeriodicasDocument11 pagini01-Ejercicios - Configuración Electronica y Propiedades PeriodicasqcomoÎncă nu există evaluări
- Taller Tabla Periodica y Termodinamica OctavoDocument2 paginiTaller Tabla Periodica y Termodinamica OctavoJuan Pablo JiménezÎncă nu există evaluări
- Taller de Estructura Atomica y Tabla PeriodicaDocument1 paginăTaller de Estructura Atomica y Tabla PeriodicaCHARLIE DANIEL AMAYA RODRIGUEZÎncă nu există evaluări
- Segundo Examen Parcial de QuimicaDocument2 paginiSegundo Examen Parcial de QuimicaWiliams PinedaÎncă nu există evaluări
- Pap 9°Document7 paginiPap 9°Quimica SebastianaÎncă nu există evaluări
- Cuadernillo-20210205 235822hkQCDocument3 paginiCuadernillo-20210205 235822hkQCrobert calloapazaÎncă nu există evaluări
- Cuadernillo de Repaso 1er Grado CuitlahuacDocument55 paginiCuadernillo de Repaso 1er Grado CuitlahuacWiliams Pineda100% (5)
- La DeserciónDocument1 paginăLa DeserciónWiliams PinedaÎncă nu există evaluări
- El OrnitorrincoDocument3 paginiEl OrnitorrincoWiliams PinedaÎncă nu există evaluări
- 1.formato de Guía de Estudio TelesecundariaDocument1 pagină1.formato de Guía de Estudio TelesecundariaWiliams PinedaÎncă nu există evaluări
- M16Document20 paginiM16Wiliams Pineda100% (6)
- Cancion de DespedidaDocument1 paginăCancion de DespedidaWiliams Pineda0% (1)
- Cancion de DespedidaDocument1 paginăCancion de DespedidaWiliams Pineda0% (1)
- Poema de DespedidaDocument3 paginiPoema de DespedidaWiliams PinedaÎncă nu există evaluări
- Alta Por Translado NuevoDocument1 paginăAlta Por Translado NuevoWiliams PinedaÎncă nu există evaluări
- Segundo Examen Parcial de QuimicaDocument2 paginiSegundo Examen Parcial de QuimicaWiliams PinedaÎncă nu există evaluări
- Mitos y Leyendas de MéxicoDocument6 paginiMitos y Leyendas de MéxicoWiliams PinedaÎncă nu există evaluări
- Encuesta de ConvivenciaDocument3 paginiEncuesta de ConvivenciaWiliams PinedaÎncă nu există evaluări
- Tercer Parcial de Química 1Document1 paginăTercer Parcial de Química 1Wiliams PinedaÎncă nu există evaluări
- Primer Parcial de Quimica 1Document2 paginiPrimer Parcial de Quimica 1Wiliams PinedaÎncă nu există evaluări
- TP 2 Uniones Químicas IónicasDocument2 paginiTP 2 Uniones Químicas IónicasPatricia LopezÎncă nu există evaluări
- Afinidad ElectrónicaDocument4 paginiAfinidad ElectrónicaGabino Garcia SorianoÎncă nu există evaluări
- Qui 5to SM Cap6Document22 paginiQui 5to SM Cap6Diego MurilloÎncă nu există evaluări
- Clase 3Document27 paginiClase 3Leonel Andrés Mendoza MalagónÎncă nu există evaluări
- Cuadro Comparativo-Tipos de HibridaciónDocument2 paginiCuadro Comparativo-Tipos de HibridaciónErick UscangaÎncă nu există evaluări
- Ficha N1-Enlace Quimico IDocument2 paginiFicha N1-Enlace Quimico ICecilia Fernanda SEMINARIO CASTILLOÎncă nu există evaluări
- Serie N4 Uniones QuímicasDocument4 paginiSerie N4 Uniones QuímicasMicaela CaceresÎncă nu există evaluări
- EQ Enlace Quimico PMEEDocument11 paginiEQ Enlace Quimico PMEESilvano Salvador ondo ndongÎncă nu există evaluări
- Tema 1 Geometría Molecular y Teorías de EnlaceDocument26 paginiTema 1 Geometría Molecular y Teorías de EnlaceAndreina MPÎncă nu există evaluări
- Anexo 2 - Tarea 2 EditadoDocument16 paginiAnexo 2 - Tarea 2 Editadoingrid yulieth carabali mina100% (1)
- Semana 07Document1 paginăSemana 07Fabian RodasÎncă nu există evaluări
- Enlaces Covalente, Iónico y MetálicoDocument7 paginiEnlaces Covalente, Iónico y MetálicoMaria Jose Fuentes DiazÎncă nu există evaluări
- Rubrica de Taller de InterpretacionDocument1 paginăRubrica de Taller de InterpretacionCamilo BonillaÎncă nu există evaluări
- QuímicaDocument31 paginiQuímicaFernando DanielÎncă nu există evaluări
- La Naturaleza Del Enlace QuimicoDocument11 paginiLa Naturaleza Del Enlace QuimicoinversionesyoselevÎncă nu există evaluări
- Estructura de LewisDocument8 paginiEstructura de LewisJuana Juana Juana0% (1)
- Configuración Electrónica e Hibridación de OrbitalesDocument29 paginiConfiguración Electrónica e Hibridación de OrbitalesVICTORIA ISABEL AYTA CRUZÎncă nu există evaluări
- Quimica 5Document7 paginiQuimica 5Eder Sanches CuevaÎncă nu există evaluări
- Clase 6.1 Volumetría Por Formación de Complejos - IDocument16 paginiClase 6.1 Volumetría Por Formación de Complejos - IBC NandoÎncă nu există evaluări
- El Enlace Químico y La Geometrí MolecularDocument10 paginiEl Enlace Químico y La Geometrí MolecularGina AyalaÎncă nu există evaluări
- Ejercicios - Estruc. Lewis-Cf-Resonancia - Geometría y PolaridadDocument8 paginiEjercicios - Estruc. Lewis-Cf-Resonancia - Geometría y PolaridadLUIS DAVID CAMPOS CHICHANDEÎncă nu există evaluări
- Estructura de LewisDocument7 paginiEstructura de LewisManuel Vazquez PerezÎncă nu există evaluări
- Deber QuimicaDocument13 paginiDeber QuimicaRami ParedesÎncă nu există evaluări
- ENLACE QUIMICO TercerasDocument40 paginiENLACE QUIMICO TercerasYaya LunaÎncă nu există evaluări
- Actividad A4. Cuadro SQA Sobre Orbitales HíbridosDocument1 paginăActividad A4. Cuadro SQA Sobre Orbitales HíbridosNAHOMY GARDEAÎncă nu există evaluări
- PamerDocument4 paginiPamerGael BeckerÎncă nu există evaluări
- Enlace CovalenteDocument4 paginiEnlace CovalenteJhosep Krow100% (1)
- Química U3Document6 paginiQuímica U3Nel AedoÎncă nu există evaluări
- EnlaceDocument5 paginiEnlaceKarina NeyraÎncă nu există evaluări
- Taller Enlace QuímicoDocument3 paginiTaller Enlace QuímicoConsultores Inversiones industriales y de serviciosÎncă nu există evaluări