Documente Academic
Documente Profesional
Documente Cultură
Informe 1 Espectrofotometría
Încărcat de
CATALINA GONZALEZ JORQUERA0 evaluări0% au considerat acest document util (0 voturi)
50 vizualizări3 paginiTitlu original
Informe 1 Espectrofotometría.docx
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
50 vizualizări3 paginiInforme 1 Espectrofotometría
Încărcat de
CATALINA GONZALEZ JORQUERADrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 3
Laboratorio de Bioquímica General para Nutrición QIM202N 2º Semestre de 2018
INFORME DE ANÁLISIS DE RESULTADOS
PRÁCTICO N°1
Nombre: Catalina González Jorquera Sección: 1 Fecha: 20/08/2018
1. Complete la Tabla 1. Incluya los cálculos para la determinación de la
concentración de Cu(NH3)4 +2 (1,5 puntos)
Tabla 1: Curva de calibrado para una solución amoniacal de cobre II
Tubo Volumen solución Volumen de Absorbancia Concentración
Patrón, complejo solución 610nm Cu(NH3)4 +2 (M)
amoniacal de cobre amoniacal (mL)
II (mL)
1 300 9700 0,029 0,0006
2 600 9400 0,078 0,0012
3 1000 9000 0,105 0,002
4 1500 8500 0,163 0,003
5 2000 8000 0,218 0,004
6 2500 7500 0,272 0,005
7 3000 7000 0,328 0,006
MP (3) -- -- 0,058
Cálculos:
Fórmula utilizada: V1 x C1= V2 x C2
Tubo (1) Tubo (2)
0,3 mL x 0,02M= 10 mL x C2 0,6 mL x 0,02M= 10 mL x C2
C2= 0,3 mL x 0,02M C2= 0,6 mL x 0,02M
10 mL 10 mL
C2= 6 x 10-4M C2= 1,2 x 10-3M
Tubo (3) Tubo (4)
1 mL x 0,02M= 10 mL x C2 1,5 mL x 0,02M= 10 mL x C2
C2= 1 mL x 0,02M C2= 1,5 mL x 0,02M
10 mL 10 mL
C2= 2 x 10-3M C2= 3 x 10-3M
Laboratorio de Bioquímica General para Nutrición QIM202N 2º Semestre de 2018
Tubo (5) Tubo (6)
2 mL x 0,02M= 10 mL x C2 2,5 mL x 0,02M= 10 mL x C2
C2= 2 mL x 0,02M C2= 2,5 mL x 0,02M
10 mL 10 mL
C2= 4 x 10-3M C2= 5 x 10-3M
Tubo (6) MP
3 mL x 0,02M= 10 mL x C2 10 mL Cu+2 x 0,1M= 50 mL x C2
C2= 3 mL x 0,02M C2= 3 mL x 0,1M
10 mL 10 mL
C2= 6 x 10-3M C2= 0,02M
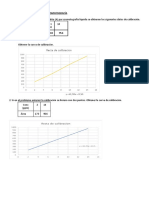
2. Construya su curva de calibrado empleando una calculadora gráfica o Excel.
Construya un Gráfico de Absorbancia v/s Concentración del complejo
amoniacal de cobre II. (1,5 puntos)
Curva de calibrado (1)
3. Obtenga la curva Absorbancia = m * Concentración + n (1,0 punto)
Especifique los valores de “m” y “n”
Absorbancia= 54,15 (m) * concentración + 0,0018 (n)
Laboratorio de Bioquímica General para Nutrición QIM202N 2º Semestre de 2018
4. Determine el coeficiente de extinción molar () (1,0 punto)
El coeficiente de extinción molar corresponde a la pendiente de la ecuación de la recta,
por lo tanto:
𝜀 = 54,15 M-1 cm-1
5. Determine la concentración de su muestra problema (1,0 punto)
Absorbancia= m x concentración
0,058= 54,15 x concentración
Concentración MP= 0,058
54,15
Concentración MP= 1,07 x 10-3
Concentración MP= 0,00107 M
S-ar putea să vă placă și
- Problemas resueltos de Hidráulica de CanalesDe la EverandProblemas resueltos de Hidráulica de CanalesEvaluare: 4.5 din 5 stele4.5/5 (7)
- Equilibrio químico: Determinación de la constante de equilibrio KeqDocument7 paginiEquilibrio químico: Determinación de la constante de equilibrio KeqPamela PupialesÎncă nu există evaluări
- Métodos Matriciales para ingenieros con MATLABDe la EverandMétodos Matriciales para ingenieros con MATLABEvaluare: 5 din 5 stele5/5 (1)
- Ejercicios AnaliticaIIDocument7 paginiEjercicios AnaliticaIIMauricio OrtegaÎncă nu există evaluări
- Adición Patrón (Tarea) Edward PDFDocument3 paginiAdición Patrón (Tarea) Edward PDFAndrea del Aguila0% (1)
- IDENTIFICACIÓN Y CUANTIFIFCACIÓN DE LA CONCENTRACIÓN DE UNA DISOLUCIÓN DE CuSO4.5H2O POR ESPECTROFOTOMETRÍA DE UV-Vis, MEDIANTE REGRESIÓN LINEAL SIMPLE (RLS), APLICANDO EL METODO DE ADICIÓN ESTANDARDocument6 paginiIDENTIFICACIÓN Y CUANTIFIFCACIÓN DE LA CONCENTRACIÓN DE UNA DISOLUCIÓN DE CuSO4.5H2O POR ESPECTROFOTOMETRÍA DE UV-Vis, MEDIANTE REGRESIÓN LINEAL SIMPLE (RLS), APLICANDO EL METODO DE ADICIÓN ESTANDARcarlos JR Simanca MadridÎncă nu există evaluări
- Universidad Autónoma Tomás Frías Facultad de Ciencias Puras Carrera de QuimicaDocument12 paginiUniversidad Autónoma Tomás Frías Facultad de Ciencias Puras Carrera de QuimicaCM Diana100% (1)
- Análisis Espectroscópico de Muestras QuímicasDocument7 paginiAnálisis Espectroscópico de Muestras Químicaswilfredoroman160% (2)
- Analisis Quimico Instrumental QMC208: Análisis Químico Instrumental - QMC 208 Primer Examen Parcial - G/01/2023Document14 paginiAnalisis Quimico Instrumental QMC208: Análisis Químico Instrumental - QMC 208 Primer Examen Parcial - G/01/2023Fernanda JaldinÎncă nu există evaluări
- Absorción Emisión Atómica - Ejercicios Resueltos y PropuestosDocument10 paginiAbsorción Emisión Atómica - Ejercicios Resueltos y Propuestoskelly roxana torres isuizaÎncă nu există evaluări
- Informe VoltametríaDocument8 paginiInforme VoltametríaEmanuel BarreraÎncă nu există evaluări
- Complejometría analíticaDocument6 paginiComplejometría analíticaPiter Ortega MuñozÎncă nu există evaluări
- Universidad Autónoma Tomás Frías Facultad de Ciencias Puras Carrera de QuimicaDocument13 paginiUniversidad Autónoma Tomás Frías Facultad de Ciencias Puras Carrera de QuimicaCM DianaÎncă nu există evaluări
- Problemas de Clase 5 y 6Document7 paginiProblemas de Clase 5 y 6Eduardo MaldonadoÎncă nu există evaluări
- Analisis Quimico Instrumental QMC208: Análisis Químico Instrumental - QMC 208 Primer Examen Parcial - G/01/2023Document12 paginiAnalisis Quimico Instrumental QMC208: Análisis Químico Instrumental - QMC 208 Primer Examen Parcial - G/01/2023Fernanda JaldinÎncă nu există evaluări
- Informe 4 CineticaDocument13 paginiInforme 4 CineticaBrenda MichelÎncă nu există evaluări
- Examen Analisis QuimicoDocument4 paginiExamen Analisis Quimicopisignatus123Încă nu există evaluări
- Sesion 3Document27 paginiSesion 3Rocio DelgadoÎncă nu există evaluări
- Soluciones Ejercicios Douglas Skoo1 (Recuperado Automáticamente)Document22 paginiSoluciones Ejercicios Douglas Skoo1 (Recuperado Automáticamente)Alexander CastroÎncă nu există evaluări
- Determinación de glucosa en sangreDocument20 paginiDeterminación de glucosa en sangreJimenaSanchezÎncă nu există evaluări
- 08 - 07 - Determinacion de Carbphidratos Por ColorimetriaDocument6 pagini08 - 07 - Determinacion de Carbphidratos Por ColorimetriaNatalia TorresÎncă nu există evaluări
- "Determinación Espectrofotométrica de Bismuto en Tabletas Utilizando Tiourea Mediante Curva de Calibración de Estándar Externo y Curva de Adición PatrónDocument9 pagini"Determinación Espectrofotométrica de Bismuto en Tabletas Utilizando Tiourea Mediante Curva de Calibración de Estándar Externo y Curva de Adición PatrónFernanda GómezÎncă nu există evaluări
- Diseño 1Document24 paginiDiseño 1Sergio Rivas Arancibia100% (1)
- Boletin 5Document4 paginiBoletin 5Ruben Fernandez100% (1)
- ADSORCIÓN ÁCIDO OXÁLICO CARBÓNDocument5 paginiADSORCIÓN ÁCIDO OXÁLICO CARBÓNBRENDA LINARESÎncă nu există evaluări
- Complexometria 1Document3 paginiComplexometria 1Jenny QuingaÎncă nu există evaluări
- Conductimetría - Informe 7Document6 paginiConductimetría - Informe 7sebas hernandezÎncă nu există evaluări
- Qan U3 A2e1 GoclDocument7 paginiQan U3 A2e1 Goclgonzalo castro lopezÎncă nu există evaluări
- Informe Ánalisis de Carbonatos y BicarbonatosDocument5 paginiInforme Ánalisis de Carbonatos y BicarbonatosNAYIBER GILÎncă nu există evaluări
- Informe 10. EspectrofotometríaDocument6 paginiInforme 10. EspectrofotometríaSharol Nathalia Garzon SerranoÎncă nu există evaluări
- Informe Laboratorio 3Document6 paginiInforme Laboratorio 3Fabrizzio Damian MaraviÎncă nu există evaluări
- Cromatografía de Gases GCDocument6 paginiCromatografía de Gases GCKiara Moreno CarrielÎncă nu există evaluări
- ANÁLISIS ESPECTROFOTOMETRICO DE SULFATO DE COBREDocument6 paginiANÁLISIS ESPECTROFOTOMETRICO DE SULFATO DE COBREvalentinaÎncă nu există evaluări
- 2 Espectroscopia Uv V Problema5Document13 pagini2 Espectroscopia Uv V Problema5margaritaÎncă nu există evaluări
- Cinetica InformeDocument17 paginiCinetica InformeAnonymous 90Q6rho6hPÎncă nu există evaluări
- ESPECTROFOTOMETRÍA VISIBLE, UV E IR EN ANÁLISIS QUÍMICO (ER-EQAN-1901-B1-002Document10 paginiESPECTROFOTOMETRÍA VISIBLE, UV E IR EN ANÁLISIS QUÍMICO (ER-EQAN-1901-B1-002Lalo MartiÎncă nu există evaluări
- Guia Ejercicios Analisis Instrumental N1-2022RDocument6 paginiGuia Ejercicios Analisis Instrumental N1-2022RChasconaÎncă nu există evaluări
- Ejercicios EspectroDocument5 paginiEjercicios EspectroJimenaSanchezÎncă nu există evaluări
- 5 PracticasDocument11 pagini5 PracticasGaliel SotomayorÎncă nu există evaluări
- Curva Estándar de Azúcares ReductoresDocument16 paginiCurva Estándar de Azúcares ReductoresAide DueñasÎncă nu există evaluări
- Lab 5 Cuantitativo ProteínasDocument7 paginiLab 5 Cuantitativo ProteínasJulieth Karina Yañez MenesesÎncă nu există evaluări
- Determinación de analitos por cromatografíaDocument5 paginiDeterminación de analitos por cromatografíakailÎncă nu există evaluări
- Curvas de calibración en bioquímicaDocument21 paginiCurvas de calibración en bioquímicaMayra RetamozoÎncă nu există evaluări
- Guía Analítica 1Document4 paginiGuía Analítica 1Francisca Ignacia Espinoza CastroÎncă nu există evaluări
- Practica 5 AnalisisDocument3 paginiPractica 5 AnalisisMyrthala SalasÎncă nu există evaluări
- Practica #9 Lab Fisica 2 Dilatacion Lineal de SolidosDocument17 paginiPractica #9 Lab Fisica 2 Dilatacion Lineal de SolidosMauricio Medrano MaciasÎncă nu există evaluări
- Determinación de benzoato de sodio en bebidas gaseosasDocument6 paginiDeterminación de benzoato de sodio en bebidas gaseosasAngélica JiménezÎncă nu există evaluări
- Análisis Aluminio AguaDocument12 paginiAnálisis Aluminio AguaIvan David Nisperuza RiveroÎncă nu există evaluări
- RESULTADOS Adicion EstandarDocument7 paginiRESULTADOS Adicion EstandarDaya RomeroÎncă nu există evaluări
- Analisis de Plata Por El Metodo de Volhard PDFDocument3 paginiAnalisis de Plata Por El Metodo de Volhard PDFNatalia Fuelantala100% (1)
- Dirigida 2 Instru 2Document7 paginiDirigida 2 Instru 2WILFREDO ROMAN PAUCARÎncă nu există evaluări
- Aguayogutierreznataliaabigail - 28842 - 838737 - Natalia Aguayo Inf 6-Equilibrio de AdsorcionDocument13 paginiAguayogutierreznataliaabigail - 28842 - 838737 - Natalia Aguayo Inf 6-Equilibrio de AdsorcionPatricia DiazÎncă nu există evaluări
- TP 2 AnalíticaDocument5 paginiTP 2 AnalíticaFranz ZÎncă nu există evaluări
- ANÁLISIS QUÍMICO A DISTANCIADocument12 paginiANÁLISIS QUÍMICO A DISTANCIAAmparo Delatorre100% (6)
- PRACTICA 4. DETERMINACION DE CR Con DifenilcarbazidaDocument16 paginiPRACTICA 4. DETERMINACION DE CR Con DifenilcarbazidaLaura PerdomoÎncă nu există evaluări
- Analisis Problemas EliseoDocument12 paginiAnalisis Problemas EliseoLimon C. UrielÎncă nu există evaluări
- Informes Bloque 2-Prácticas de Alimentos MDocument14 paginiInformes Bloque 2-Prácticas de Alimentos MMarcelaÎncă nu există evaluări
- Demanda Química de Oxígeno (Dqo) en Una Muestra de AguaDocument8 paginiDemanda Química de Oxígeno (Dqo) en Una Muestra de AguaLINA FERNANDA JURADO TORRESÎncă nu există evaluări
- PDF Problemas Espectrofotometria PDF - CompressDocument7 paginiPDF Problemas Espectrofotometria PDF - CompressKatia Agustina ZambranoÎncă nu există evaluări
- EduardoGonzalezCristinaHernandez_P4Document6 paginiEduardoGonzalezCristinaHernandez_P4cuernoferreo1Încă nu există evaluări
- Política de Alcohol en Chile. Evaluación de La Estrategia Nacional (2010-2020) Desde La Perspectiva de Actores ClaveDocument50 paginiPolítica de Alcohol en Chile. Evaluación de La Estrategia Nacional (2010-2020) Desde La Perspectiva de Actores ClaveCATALINA GONZALEZ JORQUERAÎncă nu există evaluări
- Clase Inferencia BioestadísticaDocument28 paginiClase Inferencia BioestadísticaCATALINA GONZALEZ JORQUERAÎncă nu există evaluări
- Introducción al método científico y la estadísticaDocument28 paginiIntroducción al método científico y la estadísticaCATALINA GONZALEZ JORQUERAÎncă nu există evaluări
- Informe 2 CarbohidratosDocument4 paginiInforme 2 CarbohidratosCATALINA GONZALEZ JORQUERAÎncă nu există evaluări
- Clasificacion de Residuos SolidosDocument25 paginiClasificacion de Residuos Solidosmirnael machicado castilloÎncă nu există evaluări
- SPC PemexDocument14 paginiSPC PemexDomingo DuertoÎncă nu există evaluări
- Balance de Masa 4Document27 paginiBalance de Masa 4Valeriita Marisol Basantes100% (1)
- Hojaseguridad Oxido ZincDocument5 paginiHojaseguridad Oxido ZincXuxek MartinezÎncă nu există evaluări
- Preguntas y Respuestas Taller Evaluación Segundo Corte LíneaDocument20 paginiPreguntas y Respuestas Taller Evaluación Segundo Corte LínealihgkpÎncă nu există evaluări
- Mod III-Unidad II-Mezcla de Aire-Vapor-Termodinámica IIDocument25 paginiMod III-Unidad II-Mezcla de Aire-Vapor-Termodinámica IIjose peñalbaÎncă nu există evaluări
- Control de Calidad Concreto de Alta ResistenciaDocument4 paginiControl de Calidad Concreto de Alta ResistenciaAntony MontenegroÎncă nu există evaluări
- Farmacología - Práctica N - 3 CorregidaDocument13 paginiFarmacología - Práctica N - 3 CorregidaErik Ortiz BlancoÎncă nu există evaluări
- Capítulo 07 Menor Distancia Problemas PDFDocument4 paginiCapítulo 07 Menor Distancia Problemas PDFJose ZizoldÎncă nu există evaluări
- Acidos VolatilesDocument5 paginiAcidos VolatilesPamee MancillaÎncă nu există evaluări
- Molgramostim (GM-CSF No Glicosilado)Document19 paginiMolgramostim (GM-CSF No Glicosilado)Enrique AdpiamÎncă nu există evaluări
- Resultados de Los Análisis de SuelosDocument7 paginiResultados de Los Análisis de SuelosRicardo LopezÎncă nu există evaluări
- Historia Del Vodka JosephDocument5 paginiHistoria Del Vodka JosephGuevara P. MiguelÎncă nu există evaluări
- Cloranfenicol ImgDocument20 paginiCloranfenicol ImgmartinÎncă nu există evaluări
- Alquimia InformacionDocument6 paginiAlquimia InformacionFederico Enriquez0% (1)
- Lab 2a (2012) - Fisiologia Del Sistema EndocrinoDocument18 paginiLab 2a (2012) - Fisiologia Del Sistema EndocrinoKarvezide0% (1)
- Agroempaques Practica 8Document7 paginiAgroempaques Practica 8Alexis Yairs Romero Munariz0% (1)
- Cómo prevenir y solucionar la cavitación en bombas hidráulicasDocument13 paginiCómo prevenir y solucionar la cavitación en bombas hidráulicasRicardo Anibal Arroyo FloresÎncă nu există evaluări
- BIOMECANICADocument59 paginiBIOMECANICAJorge CeballosÎncă nu există evaluări
- PRACTICA Plasticos.Document4 paginiPRACTICA Plasticos.Alejandro Diaz GarridoÎncă nu există evaluări
- Acción geológica de las aguas superficialesDocument42 paginiAcción geológica de las aguas superficialesJosué ZNÎncă nu există evaluări
- Tarea 1 - ModeloDocument4 paginiTarea 1 - ModeloerickÎncă nu există evaluări
- Absout Ficha TecnicaDocument2 paginiAbsout Ficha TecnicaFranco Quiñones100% (1)
- Diseño de Una Camara Frigorifica de Media Tonelada de Capacidad para La Congelacion de FresaDocument28 paginiDiseño de Una Camara Frigorifica de Media Tonelada de Capacidad para La Congelacion de FresaRicardo Rafael Rivera RamirezÎncă nu există evaluări
- Ecuación de cambio de estado y efecto creep en líneas de transmisiónDocument11 paginiEcuación de cambio de estado y efecto creep en líneas de transmisiónjeyson acostaÎncă nu există evaluări
- Lab 1 de Mediciones Hidrologicas Estacion MeteorologicaDocument36 paginiLab 1 de Mediciones Hidrologicas Estacion MeteorologicaMichaelIsiahRodriguezRiveraÎncă nu există evaluări
- Fórmula Taquígrafia y Fórmula SemidesarrolladaDocument5 paginiFórmula Taquígrafia y Fórmula SemidesarrolladaRUIZ AVILA ANGELICA SOFIAÎncă nu există evaluări
- Teoría Mezcla ConcretoDocument15 paginiTeoría Mezcla ConcretopawebaÎncă nu există evaluări
- Introducción A SeparadoresDocument1 paginăIntroducción A SeparadoresLeonardoÎncă nu există evaluări