Documente Academic
Documente Profesional
Documente Cultură
Determinacion de Proteinas Por Bradford
Încărcat de
brayan chavez oreTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Determinacion de Proteinas Por Bradford
Încărcat de
brayan chavez oreDrepturi de autor:
Formate disponibile
Laboratorio Enzimología
Práctica No. 2.- Determinación de proteínas mediante la técnica
de Bradford.
Universidad Autónoma de Ciudad Juárez.
Instituto de ciencias biomédicas.
Lic. Químico Farmacéutico Biólogo.
Introducción. proteínas con sulfato de cobre que absorbe la
La cuantificación de proteínas es una parte luz a una determinada longitud de onda, ente
esencial de cualquier trabajo de laboratorio que otros métodos (Santiago, S., 2005).
involucre extracción, purificación o análisis de Un método rápido y preciso para la estimación
proteínas. La cuantificación de proteínas es a de la concentración de las proteínas es un
veces necesaria para el aislamiento, separación ensayo originalmente descrito por Bradford,
y análisis por cromatografía o técnicas este método se basa en la unión de un tinte a la
inmunoquímicas y electroforéticas. proteína. Este método cuenta con un alto
Dependiendo de la precisión requerida y del coeficiente de extinción molar, lo que se traduce
porcentaje de pureza de la proteína de interés, en que la sustancia absorbe la luz de una forma
diferentes métodos serán apropiados para muy eficiente a la longitud de onda adecuada
determinar la concentración de la proteína (Walker, J., 2002).
(Hayworth, D., 2010). Debido a que las proteínas difieren en su
En general para la cuantificación de proteínas composición de aminoácidos cada una
se pueden emplear numerosos métodos. Es responde de manera diferente a cada tipo de
necesario decir que la selección del método método de cuantificación. Para lograr una alta
debe ser cuidadosa ya que en muchas eficiencia en la estimación de la concentración
ocasiones la presencia de sustancias que total de alguna proteína en muestras
interfieren genera un ruido al momento de la desconocidas es esencial incluir una curva de
cuantificación. Entre los distintos métodos se calibración la cual indicará en cierto margen de
pueden nombrar los siguientes: métodos correlación una concentración a partir de esta
espectrométricos, métodos químicos como la curva fabricada a partir de estándares de
técnica de Kjeldahl mediante el cual se concentraciones conocidas (Hayworth, D.,
determina el contenido de nitrógeno o el método 2010).
de Biuret que se basa en la reacción de las Objetivo.
Laboratorio Enzimología
Realizar y comprender el fundamento de una la curva de calibración se tomó de cada una 100
técnica de cuantificación de proteínas µL y se le adicionó 1 mL de reactivo de Bradford
(Bradford) y calcular la concentración de una y se incubo por 5 minutos a temperatura
muestra problema. ambiente, este último proceso se repitió solo
Metodología. que en lugar de los 100 µL de solución, se
Se inició el procedimiento con la realización de añadió esta cantidad de agua destilada, esto
una curva de calibración a concentraciones de para usar como blanco. Después se leyó en el
0.1, 0.2, 0.3, 0.4 mg/mL en 1 mL, esta curva fue espectrofotómetro a una absorbancia de 595
a partir de una solución con una concentración nm.
de 4 mg/mL. Una vez hechas las soluciones de
Resultados.
A continuación se muestra la tabla No. 1 en la cual se observan los resultados obtenidos, los cuales
incluyen la absorbancia dada en cada concentración de la muestra, así como su promedio.
En la gráfica No. 1 se muestra la curva de calibración con los promedios de absorbancia obtenidos por
cada equipo, además muestra el coeficiente de correlación y la ecuación de la recta con la cual se
obtuvo la concentración de la muestra problema.
Concentración (mg/mL) Equipo No. Equipo No. 2 Equipo No. 3 Equipo No. 4 Promedio
1
Absorbancia a 595 nm.
0.1 0.41 - - 0.19 0.3
0.2 1.019 0.971 0.386 0.53 0.7265
0.3 1.026 0.756 0.756 0.847 0.84625
0.4 1.444 0.987 0.833 1.002 1.0665
Tabla No. 1.- Resultados en absorbancia de la curva de calibración.
Gráfica No. 1.- Curva de calibración, ecuación de la recta, y coeficiente de correlación.
Laboratorio Enzimología
La ecuación obtenida de la gráfica No. 1 se De las tres formas cargadas del colorante se
despejó para obtener: encuentran las catiónicas que son de color rojo
𝑦 − 0.13 y verde las cuales absorben a una longitud de
𝑥=
2.4193 onda de 470 y 650 nm respectivamente. En
En esta ecuación se sustituye Y por la
contraste la forma anicónica es el azul, el cual
absorbancia de la muestra problema que en
se une a la proteína, este azul absorbe a 595
este caso fue:
nm, con lo cual se entiende que se cuantifica el
- Muestra problema No. 1 = 0.769.
azul de este colorante. El colorante aparece
- Muestra problema No. 2 = 0.212.
cuando se una a residuos de arginina y lisina en
Y se obtuvo una concentración de:
la proteína, esta unión es un enlace iónico o
- Concentración real de problema No. 1 =
salino, dado que la arginina y lisina son
0.264125 mg/mL.
aminoácidos cargados de forma positiva
- Concentración real de problema No. 2 =
(cationes) y el colorante está cargado de forma
0.03389 mg/mL.
negativa (anión).
Discusión.
Además Stephenson menciona que la
Los resultados de la curva de calibración
intensidad de absorción depende del contenido
muestran mucha variación, es por eso que se
de aminoácidos básicos y aromáticos. Las
decidió sacar un promedio y graficar a partir de
interferencias o no existen o son mínimas por
este. Los dos datos faltantes en la
cationes tanto sodio como potasio y
concentración de 0.1 de los equipos 2 y 3
carbohidratos como la sacarosa. Otras
reflejan la variación de los datos, estos
sustancias que interfieren en el ensayo son los
resultados pueden deberse a ciertos factores
agentes fuertemente alcalinos (fácilmente
sin embargo los demás datos demuestran que
solucionable con la utilización de buffers). Los
la mencionada variación no fue causada solo
únicos componentes encontrados que dan una
por algún factor si no que fueron varios factores
excesiva interferencia en el color del ensayo,
los que congeniaron para que estos resultados
son altas concentraciones de detergentes como
se dieran de esta manera.
el SDS, Triton X-100, etc.
Según Kruger, N. (2002) la reacción para el
Conclusión.
ensayo de Bradford se da entre el colorante
Se cumplió con los objetivos propuestos para la
Coomasie Blue g250 y la proteína. Menciona
práctica dado que se logró realizar la técnica de
también que diversos estudios dicen que el
cuantificación de Bradford y además mediante
colorante libre puede existir en 4 diferentes
la realización de este reporte se logró
formas iónicas cuyos pKa son 1.15, 1.82 y 12.4.
comprender el fundamento de esta técnica.
Laboratorio Enzimología
Además mediante los datos obtenidos en la • Walker, J. (2002). The protein
práctica se logró calcular la concentración de quantitation. The protein protocols
una muestra problema a partir de una curva de handbook. New Yersey: University of
Hertfordshire.
calibración. Debido a los resultados tan
• Kruger, N. (2002). Sample preparation
variables obtenidos se puede decir que la
for protein assays. Protein methods
manera en que se aplicó el método no es
overview. United Kingdon: University of
buena, pero dada la investigación bibliográfica
Oxford.
que indica que el método tiene un alto • Stephenson, F. (2008). Measuring
coeficiente de extinción lo cual es protein concentration by colorimetric
imprescindible para aumentar la sensibilidad en assay. Calculation for molecular biology
la medición de proteínas y que la unión and biotechnology.
colorante-proteína es un proceso muy rápido,
dos minutos, y el complejo permanece estable
durante un tiempo relativamente largo, una
hora, haciendo de este un proceso muy rápido,
y que no requiere un tiempo crítico para el
ensayo, además de que es un método muy
reproducible se puede llegar a la conclusión de
que el método de Bradford es un método muy
recomendable para la cuantificación de
proteínas, siempre y cuando se lleve de una
manera correcta.
Bibliografía.
• Hayworth, D. (2010). Assays methods.
Overview of protein assays methods.
U.S.: Thermo Scientific Pierce.
• Santiago, S. (2005). Separación y
determinación de proteínas.
Contribución a la determinación de la
fracción de metales traza ligados a las
proteínas similares a las metaloproteínas
en muestras de mejillón. España:
Universidad de Santiago de Compostela.
S-ar putea să vă placă și
- Determinacion de Proteinas Por BradfordDocument5 paginiDeterminacion de Proteinas Por Bradfordrizhy128100% (1)
- Microsoft Word - Taller 2. Evaluación de Datos AnalíticosDocument6 paginiMicrosoft Word - Taller 2. Evaluación de Datos AnalíticosYULI CRISTINA ZAMBRANO LEITONÎncă nu există evaluări
- Practica2 Bioquimica ExperimentalDocument8 paginiPractica2 Bioquimica Experimentalmelisa2000Încă nu există evaluări
- Curva de Calibración de GlucosaDocument5 paginiCurva de Calibración de GlucosaSergio Lym100% (6)
- Cuantificación de Proteínas Mediante el Método de BradfordDocument8 paginiCuantificación de Proteínas Mediante el Método de BradfordNestyÎncă nu există evaluări
- Informe 2-Análisis Instrumental - Montoya, Becerra-1Document10 paginiInforme 2-Análisis Instrumental - Montoya, Becerra-1andres felipe montoya bolañosÎncă nu există evaluări
- Cuantificacion de ProteinasDocument6 paginiCuantificacion de ProteinasEspinoza SilvaÎncă nu există evaluări
- Informe Bioquimica 3. Cuantificación de CaseinaDocument5 paginiInforme Bioquimica 3. Cuantificación de CaseinaANA MARIA ROMERO ARIASÎncă nu există evaluări
- Equipo 5. Curva EstandarDocument6 paginiEquipo 5. Curva EstandarSandin EugenioÎncă nu există evaluări
- Practica 6Document15 paginiPractica 6ANGELA ROCIO SAAVEDRA GALVISÎncă nu există evaluări
- CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO DE BRADFORDDocument6 paginiCUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO DE BRADFORDDANIELA MARÍA BARRERA MENDOZAÎncă nu există evaluări
- Comparacion de Los Metodos de Biuret y UV para La Identificacion de Albúmina en Clara de HuevoDocument12 paginiComparacion de Los Metodos de Biuret y UV para La Identificacion de Albúmina en Clara de HuevoJuan CalderonÎncă nu există evaluări
- DETERMINACIÓN DE PROTEÍNAS POR EL MÉTODO DE LOWRY ManceraMolinaBrenda 5QV2Document4 paginiDETERMINACIÓN DE PROTEÍNAS POR EL MÉTODO DE LOWRY ManceraMolinaBrenda 5QV2BrenDa Man Cera MolÎncă nu există evaluări
- Bioquímica Practica 4Document8 paginiBioquímica Practica 4Andres Fernando Silvestre SuarezÎncă nu există evaluări
- Extracción y cuantificación de proteínas mediante el método de BradfordDocument5 paginiExtracción y cuantificación de proteínas mediante el método de BradfordAlejandra Chavez MarinÎncă nu există evaluări
- Espectroscopia de Absorción AtómicaDocument3 paginiEspectroscopia de Absorción AtómicaAlexander Posso RestrepoÎncă nu există evaluări
- Guía de Laboratorio Práctico 2019Document45 paginiGuía de Laboratorio Práctico 2019Axel EguizabalÎncă nu există evaluări
- Informe Laboratoride Bioquímica 2Document9 paginiInforme Laboratoride Bioquímica 2ANA MARIA GONZALEZ BARRIOSÎncă nu există evaluări
- Informe: Determinación Cuantitativa de Proteinas Solubles Por El Método de BiuretDocument4 paginiInforme: Determinación Cuantitativa de Proteinas Solubles Por El Método de BiuretJeison Cardona67% (3)
- Bioquimica 4Document6 paginiBioquimica 4Crhiiztiian RojjazÎncă nu există evaluări
- Practica 5 BioquimicaDocument5 paginiPractica 5 BioquimicaSeidy AgamezÎncă nu există evaluări
- Reporte #2 Bioquimica FinalDocument13 paginiReporte #2 Bioquimica FinalJuan Emmanuel RamirezÎncă nu există evaluări
- Informe 1. EspectrofotometriaDocument6 paginiInforme 1. EspectrofotometriaAlexa LópezÎncă nu există evaluări
- Determinación de Proteínas Por El Método de Lowry y BradfordDocument13 paginiDeterminación de Proteínas Por El Método de Lowry y BradfordRafael Ochoa100% (1)
- Laboratorio Recuperativo Bio-005 - 2022Document6 paginiLaboratorio Recuperativo Bio-005 - 2022Jonathan Cisternas JametÎncă nu există evaluări
- 05 Determinacion Cuantitativa de ProteínasDocument8 pagini05 Determinacion Cuantitativa de ProteínasEdrian Fernando Rebollo GutiérrezÎncă nu există evaluări
- Determinacion de ProteinasDocument9 paginiDeterminacion de ProteinasYenifer Yuca GarciaÎncă nu există evaluări
- 2.laboratorio de BioquimicaDocument8 pagini2.laboratorio de BioquimicaMelissaÎncă nu există evaluări
- Practica#5 - Cuantificación de Proteínas y LípidosDocument11 paginiPractica#5 - Cuantificación de Proteínas y LípidosAgustin Pedraza GaleanaÎncă nu există evaluări
- Inf Práctica 6. Colorimetría FINALDocument6 paginiInf Práctica 6. Colorimetría FINALDaNiela GuevaraÎncă nu există evaluări
- Practica 2 Cuantificcion de ProteinasDocument4 paginiPractica 2 Cuantificcion de ProteinasGustavo LVÎncă nu există evaluări
- Métodos de Cuantificación de Proteínas-2Document10 paginiMétodos de Cuantificación de Proteínas-2Anonymous 7JbR482y100% (1)
- Borrador de ConclusionesDocument8 paginiBorrador de ConclusionesDaniel Alberto Bothia MartinezÎncă nu există evaluări
- Informe UV-visDocument7 paginiInforme UV-visManuela Ospina ArboledaÎncă nu există evaluări
- Determinación concentración proteína fotocolorimetríaDocument3 paginiDeterminación concentración proteína fotocolorimetríaJasmin ZoteloÎncă nu există evaluări
- Marcha Analitica Determinacion de Proteinas Por Metodo BradforDocument7 paginiMarcha Analitica Determinacion de Proteinas Por Metodo BradforRober ParedesÎncă nu există evaluări
- Determinación de proteínas por BradfordDocument8 paginiDeterminación de proteínas por BradfordCristian Tiburón ValdesÎncă nu există evaluări
- Cuestionario Práctica Cuantificación de ProeinasDocument6 paginiCuestionario Práctica Cuantificación de ProeinasGeorgina Camps ParadellÎncă nu există evaluări
- Adicion EstandarDocument7 paginiAdicion EstandarLuis Atencio0% (1)
- Cuaderno de LaboratorioDocument14 paginiCuaderno de LaboratorioValentina CastroÎncă nu există evaluări
- Informe de Curvas de CalibraciónDocument11 paginiInforme de Curvas de CalibraciónSara RodríguezÎncă nu există evaluări
- INFORME 4-Det. Cafeina en Gaseosas-FinalDocument9 paginiINFORME 4-Det. Cafeina en Gaseosas-FinalAngel Bryan Ñahuis OrtizÎncă nu există evaluări
- Informe de Laboratorio N°7 de Análisis Quimico e InstrumentalDocument6 paginiInforme de Laboratorio N°7 de Análisis Quimico e InstrumentalAngie Massiel Salvador de la cruzÎncă nu există evaluări
- Informe 1-1310 Bioquimica General (1) .Document10 paginiInforme 1-1310 Bioquimica General (1) .karenÎncă nu există evaluări
- Informe 3-Espectroscopia de Absorcion AtomicaDocument6 paginiInforme 3-Espectroscopia de Absorcion Atomicaleidy carolina peña ardilaÎncă nu există evaluări
- Cuantificación de proteínas en leche mediante el método de BradfordDocument7 paginiCuantificación de proteínas en leche mediante el método de BradfordPaola GamboaÎncă nu există evaluări
- Informe 3-Determinacion Del Calcio en La Leche Por Espectroscopia de Absorcion AtomicaDocument6 paginiInforme 3-Determinacion Del Calcio en La Leche Por Espectroscopia de Absorcion Atomicaleidy carolina peña ardilaÎncă nu există evaluări
- Guia 5 Extraccion y Cuantificacion de ProteinasDocument6 paginiGuia 5 Extraccion y Cuantificacion de ProteinasByron Calderón GonzálezÎncă nu există evaluări
- Fotocolorimetria 2023Document10 paginiFotocolorimetria 2023Débora OrtizÎncă nu există evaluări
- Se Connecter Activités Récentes Sur Le Site Signaler Un Abus Imprimer La Page Google Sites Google SitesDocument1 paginăSe Connecter Activités Récentes Sur Le Site Signaler Un Abus Imprimer La Page Google Sites Google SitesAndrés AnayaÎncă nu există evaluări
- BIURETDocument3 paginiBIURETBoris Cuesta VasquezÎncă nu există evaluări
- Cuantificación de ProteínasDocument2 paginiCuantificación de ProteínasValeria SaavedraÎncă nu există evaluări
- Analisis Instrumental Informe 2Document5 paginiAnalisis Instrumental Informe 2Valeria FajardoÎncă nu există evaluări
- Separación y Cuantificación de Proteínas PlasmáticasDocument7 paginiSeparación y Cuantificación de Proteínas PlasmáticasBrenda TapiaÎncă nu există evaluări
- Reporte 6Document12 paginiReporte 6JUAN DIEGO VALDEZ QUISPEÎncă nu există evaluări
- INF 2. Metodo KjeldahlDocument3 paginiINF 2. Metodo KjeldahlGABRIELA ANDREA VELEZ CERONÎncă nu există evaluări
- Informe de Laboratorio 1Document9 paginiInforme de Laboratorio 1Licht UmbraÎncă nu există evaluări
- Espectro IR Con BibliografiaDocument6 paginiEspectro IR Con Bibliografiabrayan chavez oreÎncă nu există evaluări
- Espectro IR Con BibliografiaDocument6 paginiEspectro IR Con Bibliografiabrayan chavez oreÎncă nu există evaluări
- Ejercicios Inge 1Document114 paginiEjercicios Inge 1brayan chavez oreÎncă nu există evaluări
- CuadroDocument2 paginiCuadrobrayan chavez oreÎncă nu există evaluări
- CuadroDocument2 paginiCuadrobrayan chavez oreÎncă nu există evaluări
- ExcelDocument6 paginiExcelbrayan chavez oreÎncă nu există evaluări
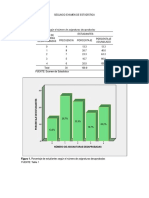
- Segundo Examen EstadisticaDocument4 paginiSegundo Examen Estadisticabrayan chavez oreÎncă nu există evaluări
- Tabla de IR 20785Document4 paginiTabla de IR 20785lacoalicionpetroleraÎncă nu există evaluări
- Segundo Examen EstadisticaDocument4 paginiSegundo Examen Estadisticabrayan chavez oreÎncă nu există evaluări
- Tabla de IR 20785Document3 paginiTabla de IR 20785brayan chavez oreÎncă nu există evaluări
- CuadroDocument2 paginiCuadrobrayan chavez oreÎncă nu există evaluări
- CuadroDocument2 paginiCuadrobrayan chavez oreÎncă nu există evaluări
- Libro1 (Autoguardado)Document3 paginiLibro1 (Autoguardado)brayan chavez oreÎncă nu există evaluări
- Imagen de PrincipiosDocument1 paginăImagen de Principiosbrayan chavez oreÎncă nu există evaluări
- Funciones de Ciencia CitasDocument2 paginiFunciones de Ciencia Citasbrayan chavez oreÎncă nu există evaluări
- CuestionarioDocument2 paginiCuestionariobrayan chavez oreÎncă nu există evaluări
- Viscosidad y tensión superficial del agua y alcoholDocument2 paginiViscosidad y tensión superficial del agua y alcoholbrayan chavez oreÎncă nu există evaluări
- Cactaceasdetacna Jos Pizarro ExcerptedDocument39 paginiCactaceasdetacna Jos Pizarro Excerptedbrayan chavez oreÎncă nu există evaluări
- 30501124Document6 pagini30501124brayan chavez oreÎncă nu există evaluări
- 30501124Document6 pagini30501124brayan chavez oreÎncă nu există evaluări
- Libro1 (Autoguardado)Document3 paginiLibro1 (Autoguardado)brayan chavez oreÎncă nu există evaluări
- EnsayoDocument2 paginiEnsayobrayan chavez oreÎncă nu există evaluări
- 30501124Document4 pagini30501124brayan chavez oreÎncă nu există evaluări
- Ejercicio - BernoulliDocument2 paginiEjercicio - Bernoullibrayan chavez oreÎncă nu există evaluări
- 30501124Document6 pagini30501124brayan chavez oreÎncă nu există evaluări
- Principios de La Ciencia 1 ConceptoDocument1 paginăPrincipios de La Ciencia 1 Conceptobrayan chavez oreÎncă nu există evaluări
- Principios de La Ciencia 1 ConceptoDocument1 paginăPrincipios de La Ciencia 1 Conceptobrayan chavez oreÎncă nu există evaluări
- Principios de La Ciencia 1 ConceptoDocument1 paginăPrincipios de La Ciencia 1 Conceptobrayan chavez oreÎncă nu există evaluări
- Costeo ABCDocument6 paginiCosteo ABCErnesto OrtizÎncă nu există evaluări
- ESTRATEGIAS COGNITIVAS Y CONDUCTUALES PARA EL MIEDO ESCÉNICODocument131 paginiESTRATEGIAS COGNITIVAS Y CONDUCTUALES PARA EL MIEDO ESCÉNICObergajoÎncă nu există evaluări
- Historia Del FaxDocument2 paginiHistoria Del FaxErick ZúñigaÎncă nu există evaluări
- Tarea S5Document6 paginiTarea S5Mondyx2001Încă nu există evaluări
- El Alma de EuropaDocument220 paginiEl Alma de Europamarcelo dellaÎncă nu există evaluări
- Agentes Naturales Responsables Del Biodeterioro en Estructuras Arqueologicas Del Parque Arqueológico de Choquequirao - CuscoDocument25 paginiAgentes Naturales Responsables Del Biodeterioro en Estructuras Arqueologicas Del Parque Arqueológico de Choquequirao - CuscoSergio Santiago Rafailo0% (1)
- Correlaciones SPT ensayoDocument16 paginiCorrelaciones SPT ensayoChris PillajoÎncă nu există evaluări
- Análisis Del Caso - Farmacias EstrellaDocument15 paginiAnálisis Del Caso - Farmacias Estrellahugo carrillo100% (2)
- Mapa Mental de La ManufacturaDocument1 paginăMapa Mental de La ManufacturaDennis Guzman GonzalesÎncă nu există evaluări
- Presupuesto Público UCSRDocument4 paginiPresupuesto Público UCSRNovahia AlvarezÎncă nu există evaluări
- 03 Costo-Hora-Hombre PDFDocument9 pagini03 Costo-Hora-Hombre PDFatreyu81116Încă nu există evaluări
- UAI Lenguaje 01 SolucionarioDocument8 paginiUAI Lenguaje 01 SolucionarioErik RaimanÎncă nu există evaluări
- Conceptos de Administracion 1 CnciDocument11 paginiConceptos de Administracion 1 CnciBertha adriana SosaÎncă nu există evaluări
- Factibilidad Farmacia ProyectoDocument56 paginiFactibilidad Farmacia ProyectoMaicol Beltran Mejia100% (2)
- Apunte de Cátedra - Metodos y TecnicasDocument97 paginiApunte de Cátedra - Metodos y TecnicasNestor SotomayorÎncă nu există evaluări
- Prueba PAC (1°GM, Periodo Entreguerras, 2°GM)Document12 paginiPrueba PAC (1°GM, Periodo Entreguerras, 2°GM)Claudia Olate Bello92% (12)
- Examen Muestra UNAMDocument34 paginiExamen Muestra UNAMMercedes Del Valle33% (3)
- Medicion y Comparacion-1Document29 paginiMedicion y Comparacion-1Mario EnriquezÎncă nu există evaluări
- Control de Arena en Pozos Petroleros PDFDocument54 paginiControl de Arena en Pozos Petroleros PDFlimberg_mayta100% (7)
- Proyecto CARGADORDocument22 paginiProyecto CARGADORVinicio TigseÎncă nu există evaluări
- Psicologia Industrial - Conflictos en Las OrganizacionesDocument45 paginiPsicologia Industrial - Conflictos en Las Organizacionesjuanromero1750% (1)
- Silabo Jcap Desarrollo EmpresarialDocument10 paginiSilabo Jcap Desarrollo EmpresarialAxel Angel Alvarez Venegas100% (1)
- Taller niños inclusiónDocument5 paginiTaller niños inclusiónGraciela GonzalezÎncă nu există evaluări
- Cuadernillo AlgebraDocument15 paginiCuadernillo AlgebraMate SauzalÎncă nu există evaluări
- Sustentabilidad Hidrica Tapachula 2030Document235 paginiSustentabilidad Hidrica Tapachula 2030Ángel CarriónÎncă nu există evaluări
- Parte+11+de+11+-+8+TIPOS+DE+MUJERES - La Guia Del Hombre para La Mente FemeninaDocument74 paginiParte+11+de+11+-+8+TIPOS+DE+MUJERES - La Guia Del Hombre para La Mente Femeninaenrique0jaja0risasÎncă nu există evaluări
- THEISSEN, Gerd (2002) - Defensa de Una Relación Renovada Entre Exégesis y HomiléticaDocument11 paginiTHEISSEN, Gerd (2002) - Defensa de Una Relación Renovada Entre Exégesis y HomiléticaBonzoR.BeltránÎncă nu există evaluări
- Avances Tecnologicos Edad ModernaDocument11 paginiAvances Tecnologicos Edad Modernaalex_adrian7Încă nu există evaluări
- Silabo-Mecánica de Suelos IiDocument10 paginiSilabo-Mecánica de Suelos Iimaxi dimitri steveÎncă nu există evaluări
- Libro de Oratoria - 3Document51 paginiLibro de Oratoria - 3Angel Trucu ShengÎncă nu există evaluări