Documente Academic
Documente Profesional
Documente Cultură
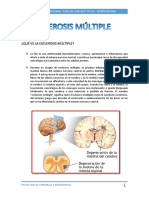
Esclerosis Múltiple
Încărcat de
Javiera Rayen Rivera LopezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Esclerosis Múltiple
Încărcat de
Javiera Rayen Rivera LopezDrepturi de autor:
Formate disponibile
ACTUALIZACIÓN
Esclerosis múltiple
O. Fernández, V.E. Fernández y M. Guerrero
Servicios de Neurología y Neurofisiología. Unidad de Gestión Clínica de Neurociencias. Hospital Universitario Regional y
Hospital Universitario Virgen de la Victoria. Málaga. España.
Palabras Clave: Resumen
- Esclerosis múltiple La esclerosis múltiple (EM) es la enfermedad neurológica crónica más frecuente en adultos jó-
- Incidencia venes. Su etiología es aún desconocida y la hipótesis patogénica más aceptada es la autoinmu-
- Prevalencia ne. Se caracteriza por episodios de disfunción neurológica diseminados en el espacio y el tiem-
po que originan una gran variedad de síntomas, según la zona del SNC afectada. El 90% de los
- Virus
pacientes de EM presentan un curso clínico caracterizado por la aparición de episodios o brotes
- Genética de disfunción neurológica más o menos reversibles, que se repiten cada cierto tiempo y que, a
- HLA medida que se repiten, van dejando secuelas funcionales neurológicas (forma en brotes o reci-
- Gemelos divante-remitente –RR o EMRR–). Tras 10 años, un 50% de los pacientes pasan del curso en bro-
tes a un curso progresivo (forma secundariamente progresiva –EMSP–). Un 10% de los pacien-
tes muestran un curso progresivo desde el comienzo (forma progresiva primaria –EMPP–). El
diagnóstico clínico de la EM se realiza tomando en consideración la existencia de criterios clíni-
cos de diseminación espacial (presencia de síntomas y signos que indiquen la existencia de dos
lesiones independientes en el SNC) y de dispersión temporal (2 o más episodios de disfunción
neurológica). En la actualidad, con la clínica y con la ayuda de los métodos de investigación pa-
raclínicos (LCR, potenciales evocados, resonancia magnética), es posible descartar con bastan-
te seguridad otras enfermedades y llegar a un diagnóstico de certeza de la EM en la mayoría de
los casos; además el diagnóstico se realiza cada vez de forma más precoz tras el comienzo de la
enfermedad.
Keywords: Abstract
- Multiple sclerosis Multiple sclerosis
- Incidence
Multiple sclerosis (MS) is the most frequent chronic neurologic disease affecting young adults. The
- Prevalence cause of MS is not known, but autoimmune mechanism is accepted as pathogenic hypothesis. It is
- Virus characterized by neurological dysfunction episodes spread over space and through time. As results,
- Genetic a wide variety of symptoms are observed depending on the area of central nervous systems affected.
In 90% of patients MS is clinically characterized by recurrent attacks and exacerbations of neurologic
- HLA
dysfunction leading to progressive physical disability [relapsing-remitting (RR) multiple sclerosis
- Twins (MS)]. After 10 years, 50% of patients evolve to a progressive course [secondary progressive (SP)
MS]. Primary progressive (PP) MS is observed in 10% of patients. Clinical diagnosis is supported on
clinical criteria for dissemination in space (presence of symptoms and signs denoting two
independent lesions in CNS) and in time (2 or more episodes of neurological dysfunction). Currently,
certainty diagnosis of MS is possible, in the majority of cases, by clinical symptomatology and
paraclinical diagnostic methods [cerebral spinal fluid (CSF), evoked potential, magnetic resonance
imaging]. Besides, earlier diagnosis after the onset of disease is achieved.
4610 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
Concepto y anatomía patológica A B
Las primeras descripciones anatomopatológicas de la escle-
rosis múltiple (EM) fueron hechas por Cruveilhier (1835) y
Carswell (1838); pero es Charcot en 1868 quien realiza la
correlación anatomoclínica y acuña el concepto de esclerosis
en placas, nombre con el que aún se conoce esta enfermedad
en la literatura francesa, y que hace referencia a los hallazgos
anatomopatológicos. Los autores ingleses le denominan es-
clerosis diseminada, aludiendo a la diseminación de las lesio-
nes en el sistema nervioso central (SNC) y los autores nor-
teamericanos la llaman EM, siendo esta última denominación
la más empleada en la literatura actual1,2.
La EM se caracteriza por su anatomía patológica3, con-
sistente en la aparición de lesiones focales en la sustancia Fig. 1. Cortes de cerebro mostrando placas de desmielinización periventricula-
res (flechas). A. Corte de cerebro sin teñir (la placa se ve más oscura que la
blanca, denominadas placas, en las que lo más llamativo es la sustancia blanca circundante). B. Tinción con osmio (la mielina se tiñe en negro,
pérdida de mielina (desmielinización) con preservación re- las placas en blanco).
lativa de los axones, pues siempre está presente un grado
variable de destrucción axonal4,5. Estas lesiones suelen ser A B
múltiples y están distribuidas por todo el SNC; característi-
camente tienen disposición perivenular y se localizan más
frecuentemente en la sustancia blanca periventricular y sub-
pial. Las localizaciones preferentes de estas lesiones son en
nervio óptico, regiones periventriculares, tronco encefálico y
médula espinal. Su tamaño es variable, en general no mayor
de 1,5 cm de diámetro, con tendencia a coalescer, dando
como resultado placas de mayor tamaño. Pueden aparecer
placas en la sustancia gris, en general subpiales, pero son más
difíciles de identificar; las neuronas suelen estar respetadas
(fig. 1).
Se distinguen la lesión aguda, en la que el fenómeno pa-
Fig. 2. A. Placas de desmielinización en el cerebro, con distribución periventri-
tológico fundamental es la inflamación, y la lesión crónica, cular (flecha negra). B. Infiltrado perivenoso de células inflamatorias en el cen-
en la que destacan la desmielinización, la degeneración axo- tro de una placa de esclerosis múltiple.
nal y la gliosis. La lesión aguda presenta unos bordes mal
definidos, con un importante infiltrado inflamatorio, prefe-
rentemente de linfocitos T, linfocitos B, microglía activada y
macrófagos en los que aparecen restos de mielina en distintas
fases de digestión. Se produce, además, pérdida de oligoden-
drocitos, con degradación de las vainas de mielina, degenera- B
ción axonal en grado variable y posterior proliferación de
astrocitos (fig. 2).
Hay placas en las que ocurre un fenómeno de remielini-
zación parcial (placas sombreadas), demostrándose la exis-
tencia de oligodendrocitos o de sus prolongaciones y axones
* **
finamente mielinizados (fig. 3).
En la lesión crónica, existe poca actividad inflamatoria,
pero hay una importante pérdida de vainas de mielina y de
oligodendrocitos, mostrándose los axones desmielinizados,
en ocasiones degenerados o rotos, con formaciones de redes
de prolongaciones astrocitarias (fig. 4).
En la primera fase de la enfermedad habría lesiones foca-
les perivasculares inflamatorias y desmielinizantes. En la fase
más avanzada sigue habiendo estas lesiones, pero aparecen Fig. 3. Placa desmielinizada en cerebro (*) y parcialmente remielinizada o som-
breada (**)
lesiones difusas constituidas por nódulos microgliales, nódu-
los linfoides en la pía-aracnoides, lesiones en la sustancia
gris, desmielinización cortical y atrofia global (fig. 5). crónica de la microglía, alteración de la expresión de los ca-
Múltiples mecanismos contribuyen a la neurodegenera- nales iónicos en los axones desmielinizados, daño mitocon-
ción en esta fase progresiva: desgaste de los mecanismos de drial y acumulación de hierro6, además de la presencia de
compensación funcional, falta de soporte trófico, activación estructuras similares a los folículos celulares B de los gan-
Medicine. 2015;11(77):4610-21 4611
ENFERMEDADES DEL SISTEMA NERVIOSO (VIII)
A B glios linfáticos en las meninges de
pacientes en fase progresiva de la
enfermedad relacionada con lesiones
localizadas en la corteza cerebral y
con peor pronóstico7 (figs. 6 y 7).
Etiopatogenia
La predisposición hereditaria, com-
binada con el factor ambiental des-
conocido, induce la aparición de
Fig. 4. Placa desmielinizada en el cerebro. A. Axones rotos en el centro de una placa de desmielinización (fle- células T autorreactivas que, tras un
chas negras). B. Axones (color verde) desmielinizados (mielina de color rojo) total o parcialmente (puntas de periodo de latencia de 10-20 años,
flechas blancas) y uno de ellos roto (flecha blanca). Modificada de Trapp BD, et al5.
serán activadas por un factor sisté-
mico o local (infección vírica, puer-
perio, etc.) mediante un mecanismo
EMRR EMSP de mimetismo molecular (epítopos
compartidos por la mielina y los po-
sibles agentes infecciosos)8 o por
una estimulación a través de supe-
rantígenos víricos o bacterianos
(proteínas bacterianas o víricas que
son capaces de unirse a la molécula
HLA de la molécula presentadora
de antígenos fuera de la hendidura
de unión antigénica)9. Una vez
reactivadas, estas células T auto-
rreactivas se unen a la pared endo-
telial mediante la interacción de dos
Fig. 5. Anatomía patológica de la esclerosis múltiple: en la fase inicial de EMRR (esclerosis múltiple recidivante moléculas LFA-1 (antígeno asocia-
remitente) hay lesiones inflamatorias y desmielinizantes (en verde). En la fase más avanzada de EMSP (esclero-
sis múltiple secundariamente progresiva) sigue habiendo estas lesiones, pero aparecen lesiones difusas cons-
do a la función leucocitaria) y VLA-
tituidas por nódulos microgliales (en negro), nódulos linfoides en la pía-aracnoides (en azul claro), lesiones en 4 (antígeno muy tardío) pasan la
la sustancia gris (en azul), desmielinización cortical (en naranja) y atrofia global. Modificada de Kutzelnigg barrera hematoencefálica (BHE)
A. Brain 2005.
debido a la acción de enzimas del
tipo de la MMP-9 (metaloprotea-
sa-9). Gracias a la acción de quimiocinas, (citocinas qui-
Cerebro intacto mioatrayentes que son responsables del reclutamiento se-
lectivo de células inflamatorias), se reclutan otras células en
el proceso inflamatorio. Una vez en el SNC, el linfocito T
activado encontrará a una célula presentadora de antígeno
(macrófago o microglía), que expresa en su superficie el an-
EMRR en brote Fig. 6. En la fase de brotes tígeno responsable de la EM, que es desconocido, en el
(EMRR –esclerosis múlti-
contexto de una molécula HLA clase II y de las moléculas
ple recidivante remiten-
te–) la barrera hematoen- coestimuladoras.
cefálica (BHE) está Una vez constituido el complejo trimolecular (receptor
abierta y pasan células y de la célula T o RCT, el antígeno y la molécula HLA clase
elementos humorales. La
BHE se cierra en las remi- II), las células T, que son de fenotipo colaborador CD4 (Th1
EMRR en remisión siones. En la fase progre- y Th17) producen citocinas proinflamatorias (interferón J,
siva (EMSP –esclerosis factor de necrosis tumoral alfa –TNFD–, IL-1, IL-2, IL-12,
múltiple secundariamente
progresiva–) la BHE está
IL-17) y quimiocinas, que inducen proliferación clonal de
cerrada y pasan pocas células T y que atraen a los macrófagos y a la microglía, ac-
células y elementos hu- tivándolos, con lo que se pone en marcha la inflamación.
morales, produciéndose
una compartimentación
Linfocitos T colaboradores tipo 2 (Th2) liberan citocinas
EM progresiva antiinflamatorias (IL-4, IL-6, IL-10, TGF) que tienden a re-
de la inflamación entre
los vasos y el sistema ner- gular a la baja el estado proinflamatorio del sistema inmune,
vioso central (nódulos pero que además inducen la proliferación de células B y la
linfoides). Modificada de
Bradl M, Lassmann H. Se- consecuente elaboración de anticuerpos por éstas. El equili-
min Immunopathol 2009. brio entre las distintas citocinas y de sus concentraciones
4612 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
Entorno crónicamente Agregados linfocitarios Folículo ectópico Folículo ectópico con CG
trones heterogéneos, sugieren la
inflamado organizado existencia de diferentes mecanismos
Células
CD LT α1β2
plasmáticas
patogénicos: la desmielinización me-
Célula B diada por linfocitos T y, en grado
Célula T
variable, por anticuerpos (patrón I y
Vaso Célula B
sanguíneo Célula estromal del CG II); una oligodendropatía secundaria
leptomeníngeo
(dying-back) a la expresión anómala
Producción de LT α1β2 a causa Diferenciación de CDF Redes de CDF maduras Formación del CG de las proteínas mielínicas y con
de la infiltración de células T y B Producción de CXCL-13
apoptosis de los oligodendrocitos
(patrón III); y la pérdida gradual de
los oligodendrocitos combinada con
Infiltrado de células
inmunes intrameníngeas desmielinización (patrón IV)12-14.
Entre los mecanismos efectores
de desmielinización, están los meca-
Infiltrado de células
inmunes en materia Plexo Aracnoides nismos celulares y, entre éstos, desta-
blanca coroideo
Duramadre ca el ataque directo a los oligoden-
drocitos por los linfocitos T CD8
Ventrículos Piamadre
citotóxicos y los T JG que no tienen
Espacios de
Virchow-Robin restricción HLA.
circundantes a los Lo más probable es que, en pri-
vasos sanguíneos
de la piamadre Espacio mer lugar, intervengan las células T,
subaracnoideo con
Materia blanca Materia gris LCR iniciando el proceso inflamatorio y,
posteriormente, las células B (que en
Fig. 7. En la fase crónica de la esclerosis múltiple se originan nódulos linfoides en la pía-aracnoides, donde
probablemente ocurra una estimulación antigénica continuada. LCR: líquido cefalorraquídeo. Modificada de condiciones normales no pueden
Uccelli A, et al. TRENDS in Immunology 2005 y Franciotta D, et al. Lancet Neurol 2008 atravesar la BHE), y otros elementos
presentes en la sangre, como anti-
cuerpos y complemento, pasan a tra-
Células T autorreactivas contra
antígenos de mielina
vés de la BHE al SNC y participan
BHE en la respuesta inmunológica.
El sistema inmune innato es el
responsable de los mediadores mo-
Ag desconocido leculares del daño a los oligoden-
drocitos15. Entre los mecanismos
moleculares independientes de re-
ceptor está el estrés oxidativo, me-
diado esencialmente por óxido nítri-
CPA
Células T activadas co; la excitotoxicidad mediada por
Péptido de mielina glutamato; las proteasas-calpaina
y el sistema perforina/granzima.
Todos estos mecanismos pueden
Periferia causar la muerte celular. Los meca-
CPA en el SNC
nismos efectores moleculares de
SNC desmielinización también pueden
ser dependientes de receptor, me-
Fig. 8. Etiopatogenia de la esclerosis múltiple simplificada. Reconocimiento antigénico en la periferia, prolifera-
diados por receptores de muerte ce-
ción clonal, paso de la barrera hematoencefálica (BHE) y nuevo reconocimiento en el sistema nervioso central
(SNC), con producción de lesiones en mielina y axones como resultado. CPA: célula presentadora de antígenos. lular (miembros de la superfamilia
de receptores del TNF), el CD95/
Fas y el TNF-R1.
determina en gran medida el sentido de la reacción inmune La inflamación sería el mecanismo más inmediato, pero
de todo el proceso (fig. 8). no el único, de la desmielinización característica de la enfer-
Además, los linfocitos T supresores (CD8+) y T regulado- medad y de la pérdida axonal presente desde el inicio de la
res, así como los que expresan el receptor “asesino natural” enfermedad (figs. 9 y 10).
producen la disminución de la proliferación de los linfoci- La fisiopatología del cuadro clínico de la EM es conse-
tos T colaboradores (respuesta antiergotípica), así como inhi- cuencia de las lesiones patológicas observadas en el SNC. El
bición de su activación (respuesta antiidiotípica), contribuyen- proceso de desmielinización produce una alteración en la
do de este modo a la contrarregulación de la inflamación10,11. conducción saltatoria típica de las vías mielinizadas norma-
El modelo patogénico de la EM basado en la inmunidad les, lentificándose la conducción e incluso bloqueándose, lo
celular mediada por células T resulta el más aceptado en la que da lugar, cuando la alteración ocurre en una vía elocuen-
actualidad; no obstante, los datos inmunopatológicos de pa- te, a la aparición de los síntomas de la enfermedad. La remie-
Medicine. 2015;11(77):4610-21 4613
ENFERMEDADES DEL SISTEMA NERVIOSO (VIII)
CD inmadura
rrir a todo lo largo del neuroeje. Las
Procesamiento antigénico y CD madura
lesiones muestran predilección por
presentación en MHC clase II ciertas partes del SNC (periventricu-
lares, nervio y quiasma óptico, tronco
Célula T cerebral, pedúnculos cerebelosos,
TGFβ CD4 + naive
médula), dando lugar a debilidad, pa-
IFNγ
+ restesias, alteración de la visión, di-
IL12 IL6
Treg plopía, nistagmo, disartria, temblor
intencional, ataxia, alteración de la
IL4 sensibilidad profunda, disfunción
IL10 Th17 vesical, paraparesia, alteraciones
IFNγ
Th2
TNFα IL17 emocionales, deterioro intelectual y
Th1 otros síntomas. Se configuran com-
activada
plejos de síntomas y signos, más o
menos característicos, que sugerirán
Célula B CD8+ el diagnóstico de EM en la presencia
de evidencia clínica o paraclínica de
MMP diseminación en el espacio (más
BHE
de una lesión en el neuroeje) y en el
tiempo (más de un episodio de dis-
función neurológica)17.
Fig. 9. Etiopatogenia de la esclerosis múltiple: reconocimiento antigénico y reacciones celulares posteriores en
la periferia. BHE: barrera hematoencefálica; IFM: ifosfamida; IL: interleucina; MHC: complejo principal de histo-
compatibilidad; TGF: factor de crecimiento transformante; TNF: factor de necrosis tumoral.
Formas evolutivas
Periferia
El 90% de los pacientes de EM pre-
sentan un curso clínico caracteriza-
do por la aparición de episodios o
brotes de disfunción neurológica
más o menos reversibles, que se re-
piten cada cierto tiempo y que, a
medida que se repiten, van dejando
secuelas funcionales neurológicas
SNC
(forma en brotes o recidivante-remi-
tente –RR o EMRR–). Tras 10 años,
un 50% de los pacientes pasan del
curso en brotes a un curso progresi-
vo (forma secundariamente progre-
siva –EMSP–). Un 10% de los pa-
cientes muestran un curso progresivo
desde el comienzo (forma progresiva
primaria –EMPP–)18. Un número
Cels CD+ autorreactivas: iniciadoras del proceso autoinmune. Papel secundario en fase efectora reducido de pacientes puede presen-
(lisis neuronal por interacción TRAIL-TRAILR) tar, tras un curso progresivo, ocasio-
Fig. 10. Etiopatogenia de la esclerosis múltiple: paso de la barrera hematoencefálica y reacciones celulares
nales exacerbaciones (forma progre-
posteriores en la periferia en la fase aguda (a la izquierda) y en fases más avanzadas (en recuadro a la derecha siva recidivante –EMPR–) (fig. 11).
BHE: barrera hematoencefálica; IFM: ifosfamida; IL: interleucina; SNC: sistema nervioso central; TGF: factor de Ocasionalmente nos encontra-
crecimiento transformante; TNF: factor de necrosis tumoral.
mos que una persona sana a la que
por otros motivos se le realiza una
linización no suele llegar a formar vainas de mielina como las resonancia magnética (RM) presenta lesiones típicas de EM,
originales, siendo los internodos más cortos, y apareciendo a esto se denomina síndrome radiológico aislado (SRA o RIS
las disfunciones más crónicas16. del inglés Radiologically Isolated Syndrome). Sólo algunos de
ellos convertirán más tarde a EM.
Al primer episodio sugerente de enfermedad desmielini-
Manifestaciones clínicas zante se le denomina síndrome desmielinizante aislado (SDA
o CIS del inglés Clinically Isolated Syndrome) del nervio óptico
La característica clínica más llamativa de la EM es su gran (neuritis óptica desmielinizante), médula espinal (mielitis
variabilidad: los síntomas y signos están determinados por la transversa) o del tronco de encéfalo se incluyen actualmente
localización de las lesiones desmielinizantes que pueden ocu- como parte del espectro clínico de la EM debido al elevado
4614 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
las mujeres (60%) que los hombres (40 %) en una propor-
ción de 1,517.
Recurrente-
0
remitente
Síntomas y signos de comienzo
Primariamente
progresiva 0
El síntoma de comienzo más frecuente es la alteración de la
sensibilidad (45%), consistente en la aparición de sensacio-
Secundariamente
0 nes de pinchazos u hormigueo (parestesias) o acorchamiento
progresiva
de uno o más miembros, o del tronco, sugestivo de afectación
del haz espinotalámico y sensación de banda constrictiva en
Progresiva- 0 el tronco o los miembros, indicando afectación de los cordo-
recurrente
nes posteriores. En la exploración se aprecian diversas com-
binaciones de hipoestesia táctil, térmica y dolorosa o dismi-
Fig. 11. Formas clínicas evolutivas de la esclerosis múltiple. nución de la sensibilidad profunda, posicional y vibratoria,
así como signo de Romberg frecuentemente positivo.
La alteración motora es también muy frecuente (40%),
porcentaje (40-70% para el caso de neuritis óptica) de estos caracterizada por pérdida de fuerza en uno o más miembros,
síndromes que desarrollarán una EM clínicamente definida. arrastrando uno o los dos pies al caminar, presentando tor-
La EM sería una enfermedad, por tanto, que evoluciona peza y debilidad en una o las dos manos, o bien fatiga mar-
en dos fases, caracterizada la primera por la existencia de bro- cada tras pequeños esfuerzos. En la exploración se aprecian
tes de disfunción clínica y acompañada de mucha actividad en paresias o parálisis francas (paraplejía, hemiplejía), hiperre-
la RM. Tras un periodo de transición que ocurre tras años de flexia osteotendinosa, ausencia de reflejos cutáneos abdomi-
evolución, la enfermedad entra en una fase progresiva, con o nales y signo de Babinski con frecuencia bilateral.
sin brotes y en la que se detecta menos actividad en EM, pero Los síntomas producidos por la disfunción del tronco
se comprueba un creciente grado de atrofia cerebral. En estas cerebral, tales como disartria, diplopía, disfagia o vértigo, son
diferentes fases subyacen cambios inmunológicos y neuropa- algo menos frecuentes (25%). En la exploración, son típicas
tológicos que se han descrito previamente, pero que configu- de la EM la presencia de nistagmo horizontal, vertical, rota-
rarían una primera fase, en la que existen mecanismos com- torio o retráctil y de oftalmoplejía internuclear, que si se pre-
pensatorios, y una segunda fase en la que no existen estos senta en una persona joven y es bilateral es un hallazgo casi
mecanismos o los mismos se han agotado (fig. 12). patognomónico de EM. Otras alteraciones menos frecuentes
son la oscilopsia (movimiento de las imágenes) y ocasional-
mente la parálisis facial nuclear.
Edad de comienzo y sexo Las alteraciones visuales por afectación del nervio o quias-
ma óptico son también características, aunque algo más infre-
La enfermedad puede comenzar a cualquier edad, siendo cuentes como síntoma de comienzo (20%); lo más frecuente
rara antes de los 10 y después de los 60 años. Suele presen- es la presencia de un escotoma central con disminución mar-
tarse entre los 25-30 años, afectando con mayor frecuencia a cada de la agudeza visual, pero pueden presentarse todo tipo
de alteraciones campimétricas. Du-
rante el episodio agudo, el fondo de
EMRR EMSP ojo puede ser normal (neuritis retro-
EM: una enfermedad en dos fases bulbar) o bien presentar edema de
papila (papilitis); se aprecia una dis-
SDA minución del reflejo pupilar, o bien el
signo de Marcus-Gunn (al iluminar
el ojo sano, se produce una contrac-
SRA
ción pupilar bilateral, si se estimula
inmediatamente después el ojo afec-
to, la pupila de éste se dilata), indican-
do en ambos casos un déficit aferente.
Es frecuente que al cabo de unas se-
Fase compensatoria Fase no compensatoria
manas se aprecie una palidez de papi-
S. inmune adaptativo S. inmune innato (microglía) la de predominio en la región tempo-
BHE alterada Inflamación atrapada tras la BHE
Lesiones focales restringidas Folículos de células B
ral o difusa (atrofia óptica).
Alta capacidad de remielinización (80%) Inflamación global del SNC El cerebelo se afecta inicialmen-
Diferenciación CPO Baja capacidad de remielinización (20%) te con menor frecuencia (10-20%),
Diferenciación reducida de CPO
Desmielinización cortical pudiendo presentarse en forma de
Fig. 12. La esclerosis múltiple: una enfermedad en dos fases. Fase compensatoria (EMRR –esclerosis múltiple disartria cerebelosa (lenguaje escan-
recidivante remitente–) y fase no compensatoria (EMSP –esclerosis múltiple secundariamente progresiva–). dido), incoordinación motora de los
Medicine. 2015;11(77):4610-21 4615
ENFERMEDADES DEL SISTEMA NERVIOSO (VIII)
miembros o inestabilidad en la marcha. En la exploración se Trastornos afectivos
encuentran temblor intencional, dismetría, disdiadococinesia La alteración afectiva más frecuente es la depresión, que apa-
o ataxia de los miembros o del tronco, con inestabilidad en la rece en el 75% de los pacientes en algún momento de la
prueba de Romberg y en la marcha. enfermedad. Suele ser una depresión moderada y reactiva.
La afectación de los esfínteres, o la aparición de síntomas La euforia es rara, aunque se presenta ocasionalmente.
de deterioro mental, como manifestaciones iniciales aisladas,
son muy infrecuentes; cuando aparecen, crean una gran incer- Epilepsia
tidumbre diagnóstica, hasta que se presentan otros síntomas17. Las crisis epilépticas son más frecuentes en la EM (2-5%)
que en la población en general (0,5%), pudiendo presentarse
cualquier tipo de crisis, a excepción de las ausencias típicas.
Síntomas y signos en el curso de la enfermedad
Cuadros pseudotumorales
En el curso de la enfermedad suelen afectarse la mayoría de Muy ocasionalmente puede presentarse en la EM un curso
los sistemas funcionales neurológicos (piramidal, sensitivo, pseudotumoral tanto en la clínica como en la neuroimagen
cerebeloso, tronco cerebral, esfinteriano, visual, mental), (signo del “anillo abierto” en la RM).
siendo las alteraciones motoras (90%), sensitivas (77%) y ce-
rebelosas (75%) las más frecuentes, seguidas en orden decre- Síntomas paroxísticos
ciente por las alteraciones de tronco cerebral, esfinterianas, Al menos un 1% de los pacientes de EM sufre de neuralgia
mentales y visuales. Los casos evolucionados de EM mues- del trigémino a lo largo de su enfermedad. Otros síntomas
tran con mucha frecuencia una combinación de síntomas y paroxísticos (disartria, ataxia, parestesias, crisis tónicas, dolor,
signos que indican la afectación de varios sistemas neuroló- prurito, diplopía y acinesia, entre otros) son mucho menos
gicos, lo que facilita enormemente el diagnóstico; en particu- frecuentes.
lar cuando este cuadro se presenta en personas jóvenes y, más
aún, si son mujeres. Narcolepsia
Aparte de los síntomas y signos más frecuentes que se Parece existir una asociación significativa entre la EM y la
deben a la alteración de los distintos sistemas funcionales ci- narcolepsia, quizás debida a una base genética, ya que ambas
tados, existen alteraciones clínicas que se presentan con cier- se asocian con el antígeno HLA DR2.
ta frecuencia en la EM.
Movimientos anormales
Fatiga Aparte del temblor intencional de origen cerebeloso tan fre-
La existencia de una fatiga excesiva es un síntoma frecuente cuente, en la EM pueden presentarse de forma ocasional co-
(76%) en los pacientes de EM, muy exacerbada por el calor, rea, atetosis, coreoatetosis, balismo, mioclonías y distonías
lo que la diferencia de la fatiga en los sujetos sanos. focales.
Atrofia muscular Afectación del sistema nervioso periférico
A veces pueden presentarse signos de afectación de segunda Se han descrito casos anecdóticos de afectación coincidente
motoneurona en la EM (fasciculaciones y atrofia muscular) del SNC y sistema nervioso periférico en la EM, tanto pre-
que suelen ser reversibles. cediendo la enfermedad como en el curso de la misma.
Dolor Neuritis óptica
Es un síntoma infravalorado, pero hasta un 50% de los pa- La neuritis óptica retrobulbar ocurre con la misma distribu-
cientes pueden experimentar alguna de las siguientes expe- ción de edad y sexo que la EM. Está acompañada de dolor y
riencias dolorosas: neuralgia del trigémino, convulsiones tó- pérdida de visión, con recuperación posterior como regla en
nicas dolorosas, disestesias dolorosas paroxísticas en unos dos meses. La alteración visual empeora con el ejercicio
extremidades, signo de Lhermitte doloroso, sensaciones di- y el calor (fenómeno de Uthoff). Aproximadamente el
sestésicas “eléctricas” en tronco y en miembros inferiores y 40-70% de los pacientes con neuritis óptica desarrollarán
lumbalgia. clínica de EM en el futuro, el resto de los casos deben consi-
derarse como formas localizadas de enfermedad desmielini-
Signo de Lhermitte zante inflamatoria idiopática.
Es una sensación de calambre eléctrico que desciende por la
espalda a los miembros inferiores al flexionar el cuello, en Alteraciones esfinterianas
general de carácter desagradable (presente en el 20-40%). Los síntomas esfinterianos son raros al comienzo de la enfer-
Puede deberse a otras patologías pero su presencia aislada en medad, pero en el curso ésta, la mayoría de los pacientes (más
una persona joven, en ausencia de traumatismo previo, debe del 90%) presentan algún síntoma o signo de disfunción es-
hacer sospechar una EM. finteriana. El patrón urodinámico más frecuente es la hipe-
rreflexia del músculo detrusor de la vejiga, que suele asociar-
Trastornos cognitivos se con disinergia entre el músculo detrusor y el esfínter
Aparece deterioro neuropsicológico en el 40-70% de los pa- externo de la uretra. En este caso, el esfínter externo se con-
cientes con EM. trae de forma involuntaria y al mismo tiempo que el múscu-
4616 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
lo detrusor, apareciendo el titubeo o la retención de la mic- Investigaciones paraclínicas
ción, micción interrumpida, incontinencia por rebosamiento
y el vaciado vesical incompleto. La arreflexia del detrusor es Líquido cefalorraquídeo
muy rara.
El estreñimiento es relativamente frecuente, al contrario
El LCR de los pacientes con EM es de aspecto macroscó-
que la incontinencia fecal.
pico normal, transparente, incoloro y a presión normal. El
número de células es normal (hasta 4/microl) en el 60% de
Alteraciones sexuales
los pacientes, tratándose en su mayoría de linfocitos T. Las
Presentan alteraciones en la esfera sexual, tras varios años de
proteínas totales y la albúmina son normales o están ligera-
evolución de la enfermedad, aproximadamente el 70% de los
mente elevadas en el 40% y el 20-30% respectivamente.
pacientes, no sólo secundarias a lesiones neurológicas sino
Un hallazgo característico es la elevación relativa con res-
también a un fuerte componente psicológico y a la medica-
pecto a las demás proteínas, de las inmunoglobulinas (nor-
ción recibida. Los hombres refieren impotencia, dificultades
mal hasta el 11-12% de las proteínas totales), preferente-
en la eyaculación, disminución de la libido y sensación geni-
mente la IgG (normal hasta 4 mg/100 ml), implicando
tal disminuida. Los síntomas referidos por las mujeres son
síntesis intratecal. El índice IgG se considera normal por
disminución de la libido, anorgasmia, lubrificación vaginal
debajo de 0,66.
disminuida y sensación genital disminuida.
[IgG LCR/albúmina LCR]
Índice IgG =
[IgG suero/albúmina suero]
Frecuencia de los brotes Síntesis IgG = [(IgG L–[IgGS/369]) - (AlbL–AlbS/230) x
(IgGS/AlbS) x 0,43] x 5 (mg/24 horas)
La recurrencia de los brotes es variable, pero como media
puede considerarse una cifra de 0,9 al año en los pacientes en
Ligado a la elevación de IgG está el hallazgo de bandas
fase recurrente-remitente y de 0,30 si se considera a todos
aisladas en la región catódica de los análisis electroforéticos
los pacientes, independientemente del tipo de evolución. El
del LCR, denominadas bandas oligoclonales (BO), que son
intervalo entre los síntomas de comienzo y el siguiente brote
producidas por uno o más clonos celulares de células plasmá-
es muy variable; en el primer año recae un 30%; el segundo
ticas. Existen falsos positivos, pudiendo aparecer estas bandas
año el 20%; entre los 5 y 9 años siguientes el 20% y entre
en algunas otras enfermedades (panencefalitis esclerosante
10-30 años el 10%. La recurrencia precoz se asocia con mal
subaguda, infecciones víricas, infecciones crónicas del SNC,
pronóstico.
síndrome de Guillain-Barré, etc.) (fig. 13).
Los hallazgos característicos son: elevación discreta de
las células y de las proteínas totales en el 40% de los pacien-
Escalas de disfunción neurológica tes, elevación del porcentaje de gammaglobulinas en el 70%,
elevación de la IgG en el 80%, índice IgG elevado y presen-
La necesidad de establecer medidas objetivas de la evolución
cia de BO en algo más del 90%. Si se realizan todas estas
de los pacientes con EM ha llevado al desarrollo de diversas
determinaciones, se halla anormalidad en alguna de ellas en
escalas clínicas de valoración de la disfunción neurológica en
EM. Kurztke desarrolló una escala de disfunción neurológica
(EDSS –Expanded Disability Status Scale–)19 que puntúa la
disfunción de 0 (normal) a 10 (fallecido), con intervalos de
0,50 puntos.
Existe otra escala denominada Escala Funcional Com-
puesta de Esclerosis Múltiple (MSFC –Múltiple Sclerosis
Functional Composite Scale–)20. La puntuación en esta escala se
calcula sumando las puntuaciones Z que el paciente obtiene
en tres test estandarizados:
1. El T25W o tiempo para caminar 25 pasos (del inglés
Timed 25-foot walk), que mide el tiempo que tarda el pacien-
te en recorrer 7,5 metros y constituye una medida simple y
útil de la motilidad.
2. El 9HPT o test de los nueve palitos en su agujero (del
inglés Nine Hole Peg Test) que mide el tiempo para meter y
retirar 9 palitos de una caja con 9 agujeros que mide la des-
treza manual y es una útil medida cuantitativa de la función
de la extremidad superior. Fig. 13. Bandas oligoclo-
3. El PASAT-3 o test de 3 segundos de audición seriada nales (señaladas con fle-
en pasos (del inglés Paced Auditory Serial Addition Test) que chas) en el líquido cefa-
lorraquídeo (LCR) que no
consiste en una lista de números estandarizada y presentada están presentes en el
de forma seriada cada 3 segundos. suero. Suero LCR
Medicine. 2015;11(77):4610-21 4617
ENFERMEDADES DEL SISTEMA NERVIOSO (VIII)
A B vidad de la enfermedad en los ensayos clínicos y e) avanzar
en el conocimiento de la patogenia de la enfermedad, mos-
trando que la actividad detectada por RM antecede a los sín-
tomas clínicos y que la actividad captada por RM es de 5 a
20 veces más frecuente que los brotes clínicos (fig. 15).
Se han desarrollado diversos criterios diagnósticos de
RM (Paty, Fazekas, Barkhof) que incluyen la presencia de 3
P100 a 9 lesiones, 3-6 mm de diámetro y localización periven-
95 125 tricular, yuxtacortical o en fosa posterior y que al menos
25 (ms)
una de las lesiones capte gadolinio. Cuantas más variables
Fig. 14. Potenciales evocados visuales: A. Normal. B. Neuritis óptica desmielinizante.
estén presentes, mayor es la sensibilidad y la especificidad
y, por tanto, la probabilidad de que estemos ante un caso
casi el 100% de los casos. La detección de la síntesis intrate- de EM.
cal de inmunoglobulinas IgM ha sido asociada a un peor pro- La RM craneal convencional detecta lesiones en el 95%
nóstico de la EM. y la RM cervical en el 75% de los pacientes con EM. Se de-
La presencia de más de 50 células o de polimorfonuclea- tecta atrofia corticosubcortical en el 40-50% de los casos tras
res, más de 100 mg/100 ml de proteínas totales y la ausencia una media de 12 años.
de BO debe hacernos sospechar otras enfermedades.
Diagnóstico
Potenciales evocados
El diagnóstico clínico de la EM se realiza tomando en con-
Los potenciales evocados (PE) son potenciales eléctricos sideración la existencia de criterios clínicos de disemina-
generados en el SNC tras la estimulación de un órgano ción espacial (presencia de síntomas y signos que indiquen
sensitivo/sensorial periférico. Se utilizan para la valoración la existencia de dos lesiones independientes en el SNC) y
de la función en algunas vías nerviosas (visual –PEV–, acús- de dispersión temporal (2 o más episodios de disfunción
tica –PEAT–, somatosensitiva –PESS–, motora –PEM–). neurológica). En la actualidad, con la clínica y con la ayuda
Proporcionan una medida fiable de la desmielinización. de los métodos de investigación paraclínicos (LCR, PE,
Los PE se utilizan en el diagnóstico de EM para definir la RM), es posible descartar con bastante seguridad otras en-
afectación de vías sensitivas o motoras en presencia de sín- fermedades y llegar a un diagnóstico de certeza de la EM
tomas vagos, y para detectar lesiones que no han producido en la mayoría de los casos; además el diagnóstico se realiza
clínica alguna. Los PEV son los más útiles para establecer cada vez de forma más precoz tras el comienzo de la enfer-
el diagnóstico de EM, por su mayor sensibilidad (hasta un medad.
85% de pacientes con PEV patoló-
gicos presentan una EM confirma-
da por la evolución y por otras
pruebas diagnósticas), seguidos de
los PESS de los miembros inferio-
res (30-65%). Los menos sensibles
son los PEAT (15%). Los PE moto-
res (PEM) son poco sensibles
(20%), y lo más útil sería una escala
combinada de PE multimodales
(fig. 14).
T2
T2
T1
Resonancia magnética
La RM permite: a) descartar otras
enfermedades; b) demostrar lesiones
desmielinizantes no sospechadas clí-
nicamente; c) determinar en un solo
estudio los criterios de diseminación
espacial (presencia de más de una le-
sión) y temporal (el estudio ponde-
rado en T1 con gadolinio evidencia SE T1-Gd T1-Gd
lesiones agudas y el ponderado en
T2 evidencia preferentemente lesio- Fig. 15. Resonancia magnética (RM). Se señalan con flechas aspectos de interés en las diferentes secuencias:
nes crónicas); d) monitorizar la acti- T1 (agujeros negros), T2 y SE (lesiones desmielinizantes), T1-Gd (lesiones captantes de contraste).
4618 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
TABLA 1 Diagnóstico diferencial
Criterios diagnósticos de la esclerosis múltiple
Categoría Brotes Evidencia clínica Evidencia práctica LCR IgG/BO
Debe dudarse del diagnóstico: a) si
EM clínicamente definida EMCD A1 2 2 no existen alteraciones visuales ni
EMCD A2 2 1 y1
oculomotoras; b) si hay ausencia
EM definida con apoyo de laboratorio EMDAL B1 2 1 o1 +
completa de alteraciones sensitivas y
EMDAL B2 1 2
esfinterianas; c) si existe un curso
EMDAL B3 1 1y 1 +
progresivo en pacientes jóvenes; d) si
EM clínicamente probable EMCP C1 2 1
todos los hallazgos clínicos pueden
EMCP C2 1 2
explicarse por una lesión única; e) si
EMCP C3 1 1 y1
el LCR es normal o f) en presencia
EM probable con apoyo de laboratorio EMPAL D1 2 +
de elevaciones anormalmente altas
Adaptada de Poser CM, et21.
del número de células (en particular,
polimorfonucleares), o de las proteí-
Criterios diagnósticos nas totales, y en ausencia de BO o de
lesiones en la RM de cráneo y columna cervical.
El diagnóstico de la EM se basa en la concurrencia de dise- En el diagnóstico diferencial de la EM RR se incluyen
minación en el espacio (al menos dos lesiones de distinta numerosos procesos que causan lesiones múltiples en el
localización en el SNC) y en el tiempo (al menos dos episo- SNC y que pueden cursar con episodios separados temporal-
dios de disfunción neurológica separados en el tiempo). Otro mente. Para realizar el diagnóstico diferencial habrá que rea-
aspecto fundamental es el hecho de que los síntomas/signos lizar diversas pruebas complementarias opcionales, según la
no puedan ser explicados por otro proceso, esto es, el diag- sospecha clínica24.
nóstico sólo puede hacerse tras haber descartado todas las
enfermedades que puedan acompañarse de una clínica simi-
lar. Historia natural. Pronóstico y
Ha habido diferentes propuestas de criterios diagnósti- complicaciones
cos, pero los más utilizados, hasta hace poco tiempo, han sido
los establecidos por el comité presidido por Poser (1983)21 La expectativa de vida tras el diagnóstico de la EMRR es de
que contempla datos clínicos y paraclínicos y define con unos 35-40 años. Las causas de muerte más frecuente son las
exactitud los aspectos que desarrolla. infecciones, las enfermedades no relacionadas y el suicidio.
Los criterios diagnósticos de Poser21 permiten clasificar a
los pacientes en cuatro grados de certeza diagnóstica (definida
o probable por la clínica aislada y definida o probable con Formas malignas y benignas
apoyo de laboratorio) combinando criterios clínicos y utilizan-
do pruebas complementarias de imagen, estudios del líquido Existen casos de EM con evolución muy rápida, en particular
cefalorraquídeo, urodinámicos y neurofisiológicos. Estos cri- la forma aguda conocida como enfermedad de Marburg, de
terios permiten un diagnóstico muy certero, pero no permiten curso fulminante, monofásico y que ocasiona la muerte en
un diagnóstico temprano de la enfermedad (tabla 1). pocas semanas desde su inicio. El fallecimiento ocurre con
Ante las evidencias crecientes de la importancia del diag- afectación de las estructuras del tronco cerebral. Otras for-
nóstico temprano de la EM, un comité de expertos presidido mas, sin ser agudas, son de evolución rápida y maligna, pu-
por McDonald propuso unos nuevos criterios diagnósticos diendo considerarse como tales, aquellas que originan el fa-
en 2001, revisados en 2005 y 201022,23 basados sobre todo en llecimiento del paciente tras unos cinco años de evolución.
la diseminación en el espacio y el tiempo valorada mediante Se denominan formas benignas aquellas EMRR que per-
RM. Estos criterios permiten adelantar el diagnóstico de EM miten desarrollar una vida normal tras 10-15 años de evolu-
de forma significativa y definir de forma más precisa las for- ción (puntuación no superior a 3 en la escala EDSS al cabo
mas progresivas primarias (tablas 2, 3 y 4). de estos años) constituyen un 20-30% de los pacientes. Con
el tiempo, estas formas pueden llegar a ser eventualmente
TABLA 2 incapacitantes.
Criterios de McDonald 2010 de resonancia magnética para la
demostración de DIS (diseminación en el espacio)
DIS puede demostrarse por ≥1 lesión T2a en al menos 2 de 4 áreas del SNC TABLA 3
Periventricular Criterios de McDonald 2010 de resonancia magnética (RM) para la
demostración de DIT (diseminación en el tiempo)
Yuxtacortical
Infratentorial Se puede demostrar DIT por
Una nueva lesión en T2 y/o lesión(es) captante de gadolinio en una RM de
Médula espinalb seguimiento, con respecto a otra basal, sin considerar el momento de la basal
a
No es necesaria la existencia de lesiones captantes de gadolinio para DIS. bSi una persona Presencia simultánea de una lesión asintomática captante de gadolinio y otra no
tiene un síndrome de tronco o medular, las lesiones sintomáticas son excluidas de los captante en cualquier momento
criterios y no contribuyen al recuento lesional.
DIS: diseminación lesional en el espacio; SNC: sistema nervioso central. DIT: diseminación lesional en el tiempo; RM: resonancia magnética.
Medicine. 2015;11(77):4610-21 4619
ENFERMEDADES DEL SISTEMA NERVIOSO (VIII)
TABLA 4 Historia natural
Criterios de McDonald 2010 para el diagnóstico de la esclerosis múltiple
Presentación clínica Datos adicionales necesarios
para el diagnóstico de EM En la EM existe una fase preclínica, en la que es posible de-
a
≥ 2 brotes ; evidencia clínica Ninguno c tectar lesiones por RM sin que hayan existido nunca fenóme-
objetiva de 2 lesiones o nos clínicos. La EM habitualmente se manifiesta por la apa-
evidencia clínica objetiva de
1 lesión con evidencia rición de síntomas-signos neurológicos esporádicos, que
histórica razonable de un constituyen los brotes, que se encuentran separados por pe-
brote previob
≥ 2 brotesa; evidencia clínica Diseminación en el espacio, demostrada por: riodos variables de remisión. La recuperación de estos brotes
objetiva de 1 lesión
≥ 1 lesión T2 en al menos 2 de 4 regiones típicas de iniciales suele ser completa. Esta es la fase RR de la enferme-
EM del SNC (periventricular, yuxtacortical, dad que dura generalmente de 8 a 20 años. El 50% de estos
infratentorial, o médula espinal)d; o
Esperar un nuevo brote clínicoa implicando a un
pacientes con brotes, a los 10-15 años, pasarán a un estado de
lugar diferente del SNC disfunción neurológica progresiva que se denomina forma
Un brotea; evidencia clínica Diseminación en tiempo, demostrada por: secundariamente progresiva (SP). Es durante esta fase cuan-
objetiva de 2 lesiones
Presencia simultánea de lesiones captantes y no do se producen la mayoría de los déficits neurológicos que
captantes de gadolinio en cualquier momento; o
incapacitarán a los pacientes e interferirán con su vida habi-
Una nueva lesión enT2 y/o lesión(es) captante de
gadolinio en una RM de seguimiento, sin tener en tual.
cuenta el momento con respecto al estudio basal;
o Los pacientes con EM en forma RR presentan un grado
Esperar un segundo brote clínicoa de discapacidad neurológica secundario a los episodios de
Un brotea; evidencia clínica Diseminación en espacio y tiempo, demostrada por inflamación y de desmielinización. Las remisiones se corres-
objetiva de 1 lesión (síndrome ponden a su vez con la resolución de la inflamación, reorga-
clínico aislado) Para DIS:
≥1 lesión T2 en al menos 2 de 4 regiones típicas de nización de los canales de sodio en los axones desmieliniza-
EM del SNC (periventricular, yuxtacortical,
infratentorial, o médula espinal)d; o dos y la remielinización. Durante todo este periodo de brotes
Esperar un segundo brotea que afecte a otro lugar y remisiones, la pérdida axonal es continua pero permanece
distinto del SNC; y clínicamente oculta25,26.
Para DIT: El daño y la pérdida axonal se acumularía durante la fase
Presencia simultánea de lesiones asintomáticas RR y alcanzaría un punto crítico a partir del cual los meca-
captantes y no captantes de gadolinio; o
Un nueva lesión en T2 y/o lesión (es) captante de nismos neurales de reserva funcional se agotarían. Estudios
gadolinio en una RM de seguimiento, sin tener en recientes sugieren que este umbral se encuentra alrededor
cuenta el momento de la RM basal; o
del punto 3-4 de la escala EDSS de valoración de la discapa-
Esperar un segundo brote clínicoa
Progresión neurológica 1 año de progresión de la enfermedad
cidad. A partir de ese momento, el paciente entraría en la fase
insidiosa sugerente de EM (determinado retrospectivamente o SP donde la progresión rápida es bastante predecible. Este
(EMPP) prospectivamente) más 2 de 3 de los siguientes
criteriosd: fenómeno puede ser el resultado de la continua pérdida axo-
1. Evidencia de DIS en el cerebro, basada en ≥ 1 nal que en este periodo añade cada vez más discapacidad. La
lesión T2 en una región característica de EM pérdida axonal durante la fase progresiva puede ser multifac-
(periventricular, yuxtacortical, o infratentorial)
2. Evidencia de DIS en la médula espinal basada torial con escaso componente inflamatorio y degeneración
en ≥ 2 lesiones T2 en ésta de los axones desmielinizados de forma crónica (fig. 7).
3. LCR positivo (evidencia de bandas oligoclonales
por isoelectroenfoque y/o índice IgG elevado)
Si se cumplen los criterios y no hay una mejor explicación para la clínica, el diagnóstico es
de EM; si hay sospechas pero no se cumplen por completo los criterios, el diagnósticos es Factores pronósticos de la progresión
posible EM; si surge otro diagnóstico durante la evaluación que explica mejor la clínica,
entonces el diagnóstico es no EM.
a
Un brote (recaída, ataque, exacerbación) se define según informe el paciente u observado Son factores pronósticos clínicos favorables: comienzo a
objetivamente como un evento típico de un evento agudo inflamatorio desmielinizante en el
SNC; actual o por anamnesis, con duración de al menos 24 horas, en la ausencia de fiebre o edad temprana, sexo femenino, síntomas de comienzo visua-
infección.
Deber ser documentado por la exploración neurológica en ese momento, pero algunos les y sensitivos, intervalo de tiempo prolongado entre el pri-
eventos con síntomas y evolución característicos de EM, pero de los que no han sido
documentados, pueden aportar evidencia razonable de un episodio desmielinizante previo. mer y segundo brote, pocos brotes durante los dos primeros
Informes de síntomas paroxísticos (por anamnesis o actuales) deben, sin embargo, consistir años y EDSS baja a los 2-5 años. Son, por el contrario, fac-
en episodios múltiple que han ocurrido al menos 24 horas antes de hacer un diagnóstico
definitivo de EM, al menos debe corroborarse un brote por hallazgos en la exploración tores pronósticos desfavorables: comienzo por encima de 40
neurológica, potenciales evocados visuales en pacientes que refieren alteraciones visuales,
o una RM consistente con desmielinización en el área del SNC implicada en los síntomas años, sexo masculino, comienzo por síntomas motores y ce-
neurológicos obtenidos en la historia.
b
El diagnóstico clínico basado en hallazgos clínicos objetivos de 2 brotes es el más seguro.
rebelosos, recurrencia precoz tras el primer brote, elevado
Evidencia anamnéstica razonable de 1 brote anterior, en ausencia de documentación número de brotes durante los primeros años y EDSS alta a
objetiva de los hallazgos neurológicos, puede incluir episodios con síntomas y evolución
característicos de un episodio inflamatorio desmielinizante previo; sin embargo, al menos un los 2-5 años27,28.
brote debe ser apoyado por hallazgos objetivos.
c
No se requieren pruebas adicionales. Sin embargo, es deseable que el diagnóstico de EM
se haga con acceso a imágenes de acuerdo a estos criterios. Si las pruebas de imagen u
otras (por ejemplo el LCR) se realizan y son negativas, se debe ser extremadamente cauto
antes de hacer un diagnóstico de EM, debiendo considerarse diagnósticos alternativos. No
debe existir una mejor explicación para el cuadro clínico, y deben estar presentes
Conflicto de intereses
evidencias objetivas para apoyar al diagnóstico de EM.
d
No se requiere la presencia de lesiones captantes de gadolinio; las lesiones sintomáticas Los autores declaran no tener ningún conflicto de intereses.
son excluidas de consideración en sujetos con síndromes de tronco cerebral o médula
espinal.
DIS: diseminación en el espacio; DIT: diseminación en el tiempo; EM: esclerosis múltiple;
EMPP: esclerosis múltiple primariamente progresiva; IgG: inmunoglobulina G; LCR: líquido
cefalorraquídeo; RM: resonancia magnética; SNC: sistema nervioso central.
4620 Medicine. 2015;11(77):4610-21
ESCLEROSIS MÚLTIPLE
Bibliografía 14. Storch M, Lassmann H. Pathology and pathogenesis of demyelinating
diseases. Curr Opin Neurol. 1997;10(3):186-92.
15. Zipp F. Apoptosis in multiple sclerosis. Cell Tissue Res. 2000;301:163-71.
t Importante tt Muy importante 16. Smith KJ, McDonald WI. The pathophysiology of multiple sclerosis: the
mechanisms underlying the production of symptoms and the natural his-
✔ Metaanálisis ✔ Artículo de revisión ✔
tory of the disease. Phi T R Soc Lon Biol Sci. 1999;354:1649-73.
17. Matthews WB. Symptoms and signs of multiple sclerosis. En: Compston
✔ Ensayo clínico controlado ✔ Guía de práctica clínica A, Ebers G, Lassmann H, Mc Donald I, Matthews WB, Wekerle H, edi-
tors. Mc Alpine 's multiple sclerosis. 3nd ed. Edinburgh & London: Cur-
✔ Epidemiología chill Livingstone; 1998. p. 145-90.
18. Lublin FD, Reingold SC. Defining the clinical course of multiple sclero-
sis: results of an international survey. Neurology. 1996;46:906-11.
19. Kurtzke JF. Rating neurological impairment in multiple sclerosis: an ex-
1. Charcot JM. Histologie de la sclérose en plaques. Gaz Hôp (Pa-
panded disability status scale (EDSS). Neurology. 1983;33:1444-52.
ris).1868;41:554-66.
20. Fisher JS, Rudick RA, Cutter GR, Reingold SC, for the National MS
2. Noseworthy JJH, Lucchinetti CC, Rodríguez M, Weinshenker BG. Mul-
Society Clinical Outcomes Assessment Task Force. The multiple sclerosis
tiple sclerosis. N Engl J Med. 2000;343:938-52.
✔3. Lassmann H. Pathology of multiple sclerosis. En: Compston A, Ebers G,
functional composite measure (MSFC): an integrated approach to MS
clinical outcome assessment. Mult Scler. 1999;5:244-50.
Lassmann H, Mc Donald I, Matthews WB, Wekerle H, editors. Mc Alpi-
ne 's multiple sclerosis. 3nd ed. Edinburgh & London: Curchill Livingsto- ✔
21. Poser CM, Paty DW, Scheinberg L, McDonald Wl, Davis FA, Ebers GC,
et al. New diagnostic criteria for multiple sclerosis: Guidelines for re-
ne; 1998. p. 323-57.
search protocols. Ann Neurol. 1983;13:227-3l.
4. Ferguson B, Matyszak MK, Esiri MM, Perry VH. Axonal damage in acu-
te multiple sclerosis lesions. Brain. 1997;120:393-9. ✔
22. McDonald WI, Compston A, Edan G, Goodkin D, Hartung H, Lublin F,
et al. Recommended diagnostic criteria for multiple sclerosis: guidelines
5. tt Trapp BD, Peterson J, Ransohoff RM, Rudick R, Mörk S, Bö
L. Axonal transection in the lesion of multiple sclerosis. N Engl J
from the International Panel on the diagnosis of multiple sclerosis. Ann
Neurol. 2001;50:121-7.
Med. 1998;338:278-2.
✔ tt
6. Lassmann H, van Horssen J, Mahad D. Progressive multiple scle-
23. tt Polman CH, Reingold SC, Banwell B, Clanet M, Cohen JA,
Filippi M, et al. Diagnostic criteria for multiple sclerosis: 2010 revi-
rosis: pathology and pathogenesis. Nat Rev Neurol. 2012;8(11):647-56.
sions to the McDonald criteria. Ann Neurol. 2011;69:292-302.
7. Serafini B, Rosicarelli B, Magliozzi R, Stigliano E, Aloisi F. Detection of
ectopic B-cell follicles with germinal centers in the meninges of patients
24. tt Miller DH, Weinshenker BG, Filippi M, Banwell BL, Cohen
JA, Freedman MS, et al. Differential diagnosis of suspected multiple
with secondary progressive multiple sclerosis. Brain Pathol. 2004;14(2):
sclerosis: a consensus approach. Mult Scler. 2008;14:1157–74.
164-74.
25. Confavreux C, Vukusic S, Moreau T, Adeleine P. Relapses and progres-
8. Gran B, Hemmer B, Vergelli MM, McFarland HF, Martín RR. Molecular
sion of disability in multiple sclerosis. New Engl J Med. 2000;343:1430-8.
mimicry and multiple sclerosis: degenerate T-cell recognition and the
26. Weinshenker BG, Bass B, Rice GPA, Noseworthy J, Carriere W, Basker-
induction of autoimmunity. Ann Neurol. 1999:45:559-67.
ville J, et al. The natural history of multiple sclerosis : a geographically
9. Brocke S, Piercy C, Steinman L. Superantigens in demyelinating disease.
based study. Brain. 1989;112:133-46.
Springer Semin Immunopathol. 1996;18:51-6.
✔
10. Martino G, Hartung HP. Immunopathogenesis of multiple sclerosis: the
role of T cells. Current Opinion in Neurology. 1999;12:309-21.
27. Riise T, Gróning M, Femández O, Lauer K, Midgard R, Minderhoud JM,
et al. Early prognostic factors for disability in multiple sclerosis, a Euro-
pean multicenter study. Acta Neurol Scand. 1992;85:212-8.
11. Navikas V, Link H. Review: cytokines and the pathogenesis of multiple
28. Molyneux PD, Filippi M, Barkhof F, Gasperini C, Yousry TA, Truyen L,
sclerosis. J Neurosci Res. 1996;45:322-33.
et al. Correlation between monthly enhanced MRI lesion rate and chan-
12. Lucchinetti C, Brück W, Parisi J, Scheithauer B, Rodríguez M, Lassmann
ges in T2 lesion volume in multiple sclerosis. Ann Neurol. 1998;41:332-9.
H. Heterogeneity of multiple sclerosis lesions: implications for the patho-
genesis of demyelination. Ann Neurol. 2000;47:707-17.
13. Lucchinetti CF, Bruck W, Rodríguez M, Lassmann H. Distinct patterns
of multiple sclerosis pathology indicates heterogeneity on pathogenesis.
Brain Pathol. 1996;6(3):259-74.
Medicine. 2015;11(77):4610-21 4621
S-ar putea să vă placă și
- Neuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaDe la EverandNeuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaEvaluare: 4 din 5 stele4/5 (16)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De la EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Evaluare: 5 din 5 stele5/5 (9)
- Esclerosis Multiple TerminadoDocument16 paginiEsclerosis Multiple TerminadoRomina Callapani Montoya100% (1)
- Enfermedad DesmielinizanteDocument105 paginiEnfermedad DesmielinizanteUSMP FN ARCHIVOSÎncă nu există evaluări
- Propiedades de los derivados del cannabis en el AlzheimerDe la EverandPropiedades de los derivados del cannabis en el AlzheimerÎncă nu există evaluări
- Esclerosis Múltiple FinalDocument25 paginiEsclerosis Múltiple Finalm2rv110100% (1)
- Ejercicios Resueltos - Equivalencias LógicasDocument3 paginiEjercicios Resueltos - Equivalencias LógicasOscar Alarcon Flores100% (2)
- Apunte Pruebas SupraliminaresDocument13 paginiApunte Pruebas SupraliminaresJaviera Rayen Rivera LopezÎncă nu există evaluări
- Enfermedades sistémicas y del aparato locomotorDe la EverandEnfermedades sistémicas y del aparato locomotorÎncă nu există evaluări
- La Publicidad ActividadesDocument4 paginiLa Publicidad ActividadesKarla OrtizÎncă nu există evaluări
- El cannabis en patologías del sistema nervioso centralDe la EverandEl cannabis en patologías del sistema nervioso centralÎncă nu există evaluări
- Esclerosis MúltipleDocument53 paginiEsclerosis MúltipleWill Aguilar Mamani100% (1)
- Compendio Instrumentos de MediciónDocument316 paginiCompendio Instrumentos de MediciónCristopherAlejandroRamirezÎncă nu există evaluări
- Nmo 1Document12 paginiNmo 1Santiago Tijo CardonaÎncă nu există evaluări
- Apuntes EnfermedadesDocument15 paginiApuntes Enfermedadesfrancisca rojas rodriguezÎncă nu există evaluări
- Nuevo em DesmielinizanteDocument38 paginiNuevo em DesmielinizanteSebastian Rivero GonzalezÎncă nu există evaluări
- Esclerosis MultipleDocument9 paginiEsclerosis Multipleviviana zamoraÎncă nu există evaluări
- EMtodoDocument11 paginiEMtododanielÎncă nu există evaluări
- Esclerosis Múltiple: Formación Continuada Del Médico PrácticoDocument7 paginiEsclerosis Múltiple: Formación Continuada Del Médico Prácticowiseguy1977Încă nu există evaluări
- Dialnet EsclerosisMultiple 4018455 PDFDocument20 paginiDialnet EsclerosisMultiple 4018455 PDFholaÎncă nu există evaluări
- M28T5 Alteraciones Del Lóbulo Frontal y Enfermedades DesmielinizantesDocument13 paginiM28T5 Alteraciones Del Lóbulo Frontal y Enfermedades DesmielinizantessusanacastrodsÎncă nu există evaluări
- Esclerosis Multiple ResumenDocument9 paginiEsclerosis Multiple ResumenDaniela Calderón PurránÎncă nu există evaluări
- Monografia Esclerosis MultipleDocument17 paginiMonografia Esclerosis MultipleOmar Dguez JimenezÎncă nu există evaluări
- 2503 Presentación Electrónica Educativa 2449 1-10-20190426Document21 pagini2503 Presentación Electrónica Educativa 2449 1-10-20190426Yaqueli CubasÎncă nu există evaluări
- Enfermedades DesmielinizantesDocument7 paginiEnfermedades Desmielinizantesjani reyesÎncă nu există evaluări
- Enfermedades Desmielinizantes PDFDocument9 paginiEnfermedades Desmielinizantes PDFMarcos TeliasÎncă nu există evaluări
- Neuritis Optica en PerrosDocument13 paginiNeuritis Optica en Perrosmoreiro2Încă nu există evaluări
- Sindrome de FoixDocument6 paginiSindrome de FoixCons TanzaÎncă nu există evaluări
- Enfermedades DesmielinizantesDocument63 paginiEnfermedades DesmielinizantesMartha Alicia Valentin MotutoÎncă nu există evaluări
- Esclerosis MúltipleDocument14 paginiEsclerosis MúltipleElsa Moreno100% (1)
- Esclerosis Multiple MedicineDocument11 paginiEsclerosis Multiple MedicineYaqueli CubasÎncă nu există evaluări
- Neuropatía Periférica Grupo 5Document21 paginiNeuropatía Periférica Grupo 5camila meraÎncă nu există evaluări
- 3-s2.0-B978032335775300014X-main (1) - 25Document1 pagină3-s2.0-B978032335775300014X-main (1) - 25Anita SánchezÎncă nu există evaluări
- Esclerosis Multiple.Document32 paginiEsclerosis Multiple.MIZAIM MONSERRATH PERLA ROMERO CURIELÎncă nu există evaluări
- Tomo 5 29-33.en - EsDocument138 paginiTomo 5 29-33.en - EsMarcela HenaoÎncă nu există evaluări
- EF4 Enfermedades Desmielinizantes PDFDocument14 paginiEF4 Enfermedades Desmielinizantes PDFZuleima GómezÎncă nu există evaluări
- 9 - Esclerosis MúltipleDocument13 pagini9 - Esclerosis MúltipleErmilo José Echeverría OrtegónÎncă nu există evaluări
- 8 - Malformaciones Congenitas Del SNCDocument13 pagini8 - Malformaciones Congenitas Del SNCDaironny A. FlorianÎncă nu există evaluări
- Glial Cells As Therapeutic Targets in Progressive Multiple Sclerosis - En.esDocument15 paginiGlial Cells As Therapeutic Targets in Progressive Multiple Sclerosis - En.esJUAN ANDRES GUARDIAS GARZONÎncă nu există evaluări
- Esclerosis en PlacasDocument5 paginiEsclerosis en PlacasLuis LemusÎncă nu există evaluări
- Parcial NeurologiaDocument15 paginiParcial NeurologiaRUBEN ALEJANDRO MENDEZ RIVERAÎncă nu există evaluări
- Tema 9 Enfermedades DesmielinizantesDocument10 paginiTema 9 Enfermedades Desmielinizantesdags 88Încă nu există evaluări
- Dialnet EsclerosisMultipleDocument20 paginiDialnet EsclerosisMultipleDannae Cornejo LucayÎncă nu există evaluări
- ELA Con MeningiomaDocument5 paginiELA Con MeningiomaAnghel V. AriasÎncă nu există evaluări
- Dieta Mediterranea y Esclerosis MultipleDocument55 paginiDieta Mediterranea y Esclerosis MultipleMacayu CoroÎncă nu există evaluări
- Esclerosis Múltiple - RedpacientesDocument12 paginiEsclerosis Múltiple - Redpacientesdiegomc111Încă nu există evaluări
- Esclerosis Multiple WordDocument6 paginiEsclerosis Multiple Wordapi-3856002Încă nu există evaluări
- Consecuencias Generales de Las Lesiones CerebralesDocument36 paginiConsecuencias Generales de Las Lesiones CerebralesAnahí CoronadoÎncă nu există evaluări
- Esclerosis MultipleDocument17 paginiEsclerosis MultiplenanandrealinaresÎncă nu există evaluări
- 1 Esclerosis MultipleDocument9 pagini1 Esclerosis MultipleNicole PeñaÎncă nu există evaluări
- Esclerosis Multiple WikiDocument29 paginiEsclerosis Multiple WikiDeivis PerezÎncă nu există evaluări
- Tesis Caso Unico Evalucion Cognitiva emDocument31 paginiTesis Caso Unico Evalucion Cognitiva emGabina GomezÎncă nu există evaluări
- Lesion de La Medula Espinal FinalDocument42 paginiLesion de La Medula Espinal FinalJhenyÎncă nu există evaluări
- Trabajo de Patologia EspecializadaDocument54 paginiTrabajo de Patologia EspecializadaalfredoÎncă nu există evaluări
- TEMA 6. Enf. DesmielinizantesDocument5 paginiTEMA 6. Enf. Desmielinizanteslugmary avellanedaÎncă nu există evaluări
- Esclerosis MultipleDocument7 paginiEsclerosis MultipleCarlos CuzcoÎncă nu există evaluări
- Cancercol, Degeneración CerebelosaDocument3 paginiCancercol, Degeneración CerebelosajosefinaÎncă nu există evaluări
- Esclerosis MúltipleDocument10 paginiEsclerosis MúltipleTatiana MasseoÎncă nu există evaluări
- Meningitis Bacteriana AgudaDocument8 paginiMeningitis Bacteriana AgudaSabrina Yamila CamnasioÎncă nu există evaluări
- Alteraciones neuropsicológicas en las α-sinucleinopatíasDocument9 paginiAlteraciones neuropsicológicas en las α-sinucleinopatíasInternational Medical PublisherÎncă nu există evaluări
- Ejercicio y ElaDocument18 paginiEjercicio y ElaMODERADOR CDEFISÎncă nu există evaluări
- Bandas OligoclonalesDocument7 paginiBandas OligoclonalesFelix SaavedraÎncă nu există evaluări
- Diez Grandes Frases de Vincent Van GoghDocument2 paginiDiez Grandes Frases de Vincent Van GoghJaviera Rayen Rivera LopezÎncă nu există evaluări
- Ensayo MatrixDocument8 paginiEnsayo MatrixJaviera Rayen Rivera LopezÎncă nu există evaluări
- Planificacion de Unidad Artes Visuales 4 1Document6 paginiPlanificacion de Unidad Artes Visuales 4 1Javiera Rayen Rivera LopezÎncă nu există evaluări
- Capitulo 4.1 MatemáticaDocument9 paginiCapitulo 4.1 Matemática7 SPORTSÎncă nu există evaluări
- Propiedades de TPDocument2 paginiPropiedades de TP《FF》 IVO T15 montenegroÎncă nu există evaluări
- YesodDocument3 paginiYesodPatricia SoleraÎncă nu există evaluări
- CARTA PARA LIC Miguel Aleman InterjetDocument6 paginiCARTA PARA LIC Miguel Aleman Interjetsergio millanÎncă nu există evaluări
- Guía de Aprendizaje Unidad 4 - Ordenamientos, Autofiltros, Subtotales y CondicionalesDocument3 paginiGuía de Aprendizaje Unidad 4 - Ordenamientos, Autofiltros, Subtotales y CondicionalesJeannette LunaÎncă nu există evaluări
- OOTT DAM Persona Natural M2021Document54 paginiOOTT DAM Persona Natural M2021Sandra AlfaroÎncă nu există evaluări
- Triptico ProteinasDocument2 paginiTriptico ProteinasFrank GraterolÎncă nu există evaluări
- Presentacion Final Fundamentos DinamoDocument36 paginiPresentacion Final Fundamentos DinamoAdriánPechCerveraÎncă nu există evaluări
- TAREADocument5 paginiTAREACristopher Johnny LaurenteÎncă nu există evaluări
- Informe de Labotorio de MicrobiologíaDocument6 paginiInforme de Labotorio de MicrobiologíaBaurin Joseph ChavézÎncă nu există evaluări
- Formato Registro de Accidentes de Trabajo Y Enfermedades ProfesionalesDocument6 paginiFormato Registro de Accidentes de Trabajo Y Enfermedades Profesionalesjesion jair poveda mendozaÎncă nu există evaluări
- Tema 4Document11 paginiTema 4JOSE MOLINAÎncă nu există evaluări
- Ud3 AbafsmDocument30 paginiUd3 AbafsmAntonio Rocio Pradas E IbanezÎncă nu există evaluări
- Diccionario Garifuna Martinez-2000Document60 paginiDiccionario Garifuna Martinez-2000Ellie BurkeÎncă nu există evaluări
- Capitulo 3 Allen, Robert C Global Economic HistoryDocument27 paginiCapitulo 3 Allen, Robert C Global Economic HistorySantiago ArcilaÎncă nu există evaluări
- Presentacion Produccion de Semillas Artesanales Corregido 111116Document42 paginiPresentacion Produccion de Semillas Artesanales Corregido 111116joseÎncă nu există evaluări
- Libro 2 U1 Clasificación de Funciones RealesDocument18 paginiLibro 2 U1 Clasificación de Funciones RealesG&K FreshiesÎncă nu există evaluări
- Ejer Cici OsDocument24 paginiEjer Cici OsKaren GarayÎncă nu există evaluări
- LIBERACON DE FARMACOS y ALIMENTOS EN ABSORCION DE FARMACOSDocument109 paginiLIBERACON DE FARMACOS y ALIMENTOS EN ABSORCION DE FARMACOSRoxana Magaly Chavez PillacaÎncă nu există evaluări
- El Vale y Bonos Bancarios Donny ReyesDocument19 paginiEl Vale y Bonos Bancarios Donny ReyesRobertoReyesPerezÎncă nu există evaluări
- Momento 1 Construcción de Obras en ConcretoDocument23 paginiMomento 1 Construcción de Obras en ConcretoNelson Duban Tapia IngaÎncă nu există evaluări
- El PatinajeDocument2 paginiEl Patinajeerik lauraÎncă nu există evaluări
- BiologiaDocument21 paginiBiologiaBadr AbdounÎncă nu există evaluări
- Cuestionario de Productos FermentadosDocument6 paginiCuestionario de Productos Fermentadosjosseline adriana rivera revolloÎncă nu există evaluări
- Piano Metodo Basico 2Document25 paginiPiano Metodo Basico 2Anonymous PF8dywI0% (1)
- Caracteristicas Del Sistema de Tren de Rodaje Rodriguez AldairDocument2 paginiCaracteristicas Del Sistema de Tren de Rodaje Rodriguez AldairAldair RodriguezÎncă nu există evaluări
- Venezuela EstadosDocument3 paginiVenezuela EstadossmallviviÎncă nu există evaluări
- Guia de Corriente Alterna 2012Document6 paginiGuia de Corriente Alterna 2012RichardÎncă nu există evaluări