Documente Academic
Documente Profesional
Documente Cultură
Rodrigo Rafael Ricardo Paredes
Încărcat de
Jesus Chavez RodriguezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Rodrigo Rafael Ricardo Paredes
Încărcat de
Jesus Chavez RodriguezDrepturi de autor:
Formate disponibile
PRÁCTICA No.
VELOCIDAD DE REACCIÓN EN MICROESCALA
OBJETIVOS
Adaptación de una práctica convencional, elegida entre las que cumplen los requisitos de Reactores
Químicos, para su realización en microescala. Con esta adaptación se persiguen varios objetivos: a)
determinar la velocidad de una reacción, b) concienciación de los estudiantes en materia de
sostenibilidad por medio de la realización de esta práctica de laboratorio bajo los criterios de “Química
Verde” y “Trabajo en Microescala”, c) disminuir los costos económicos asociados al consumo de
reactivos, y d) disminuir la generación de residuos.
FUNDAMENTOS TEÓRICOS
La rapidez con la que se produce una transformación química es un aspecto muy importante. Tanto
desde el punto de vista del conocimiento del proceso como de su utilidad industrial, interesa conocer
la velocidad de la reacción y los factores que pueden modificarla.
Se define la velocidad de una reacción química como la cantidad de sustancia formada (si tomamos
como referencia un producto) o transformada (si tomamos como referencia un reactivo) por unidad
de tiempo.
La velocidad de reacción no es constante. Al principio, cuando la concentración de reactivos es mayor,
también es mayor la probabilidad de que se den choques entre las moléculas de reactivo, y la
velocidad es mayor. a medida que la reacción avanza, al ir disminuyendo la concentración de los
reactivos, disminuye la probabilidad de choques y con ella la velocidad de la reacción. La medida de
la velocidad de reacción implica la medida de la concentración de uno de los reactivos o productos a
lo largo del tiempo, esto es, para medir la velocidad de una reacción necesitamos medir, bien la
cantidad de reactivo que desaparece por unidad de tiempo, bien la cantidad de producto que aparece
por unidad de tiempo. La velocidad de reacción se mide en unidades de concentración/tiempo, esto
es, en moles/s.
El aumento de la concentración de los reactivos hace más probable el choque entre dos moléculas de
los reactivos, con lo que aumenta la probabilidad de que entre estos reactivos se de la reacción. En el
caso de reacciones en estado gaseoso la concentración de los reactivos se logra aumentando la
presión, con lo que disminuye el volumen.
La velocidad de una reacción depende generalmente de la temperatura, la presión y las
concentraciones de las especies involucradas en ella. También puede depender de la fase o fases en
las que ocurre la reacción.
PRE-REPORTE
1- Proponer las ecuaciones integradas de velocidad de reacción para un sistema de orden cero,
primer y segundo orden.
2- Investigar los métodos experimentales para determinar velocidades de reacción
3- Generar un diagrama de flujo de proceso de la producción de biodiesel catalizada por una
base.
MATERIALES Y REACTIVOS
Materiales Reactivos
Matraz aforado de 10 mL (3) Azul de metileno
Erlenmeyer 3 mL (5) 10 ml hidróxido de sodio (0.5 M)
Vaso de precipitados de 10 mL (5) 10 ml ácido ascórbico (0.5 M)
Magneto Metanol (2 mL)
Parrilla de calentamiento con agitación Agua destilada
magnética Aceite vegetal (10 mL)
Gafas protectoras
Embudo de separación
PROCEDIMIENTO EXPERIMENTAL
Experimento 1 (Decoloración de azul de metileno por descomposición catalítica de H 2O2):
Preparar una solución stock de 10 ml (65 mg/L) de azul de metileno. En 5 vasos de precipitados de 10
mL, agregar 1.0 ml de la solución anterior medidos con la microgeringa (insulina). Posteriormente
agregar 1.0 ml de la solución de NaOH y enseguida 0.3, 0.6, 0.8, 1.0 y 1.2 mL de la solución de ácido
ascórbico respectivamente. Dejar que se lleve a cabo la degradación del color y medir el tiempo
requerido (hasta que la solución se torne transparente). Colocar como fondo de las muestras una hoja
de papel blanco.
Experimento 2 (Reacción de transesterificación catalizada por NaOH):
Se añade el hidróxido de sodio a un Erlenmeyer de 25 ml que contiene 2 ml de metanol (> 99% de
pureza), y se agita vigorosamente hasta que se disuelva. Se calienta el aceite vegetal (10 mL) hasta
unos 40 ºC en un vaso de precipitados de 25 ml. Se agrega a la disolución metanólica de hidróxido
sódico, sin dejar de agitar. Al principio, la mezcla aparece turbia, pero pronto se aprecia que se separan
dos fases. Se sigue agitando durante 20 min. El contenido del Erlenmeyer se pasa a un embudo de
decantación de 50 ml, para separar la mezcla en dos fases. El glicerol se va al fondo, y el éster metílico
(bio-diésel) flota sobre él. Dejar en el embudo durante 1 hora. Separar las dos fases en dos vasos de
precipitados. Pesar las cantidades recogidas.
ANÁLISIS Y DISCUSIÓN DE RESULTADOS
Experimento 1:
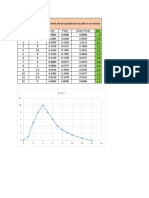
a) Llenar la tabla siguiente con la información correspondiente:
Azul de metileno NaOH Ácido ascórbico Tiempo
65 mg/L 0.5 M 0.5 M decoloración, s
1 mL 1 mL 0.10
1 mL 1 mL 0.15
1 mL 1 mL 0.20
1 mL 1 mL 0.25
1 mL 1 mL 0.30
a) Proponer el mecanismo de degradación de un colorante por descomposición de peróxido de
hidrógeno vía catálisis heterogénea.
b) Generar el gráfico de tiempo de degradación vs concentración de H 2O2 para ambos
colorantes.
c) Calcular la constante de velocidad de reacción en cada caso.
Experimento 2.
a) Proponer la reacción química de transesterificación entre un triglicérido (aceite vegetal) y
metanol, catalizados por hidróxido de sodio.
b) Determinar el porcentaje de rendimiento de la reacción
c) Para una conversión máxima en la reacción de transesterificación, ¿qué variable (s) deben
manipularse?
d) ¿En el caso particular de la síntesis realizada, qué efecto produciría un aumento o disminución
de la cantidad de catalizador utilizado?
e) Realizar un análisis por espectroscopía infrarroja del producto principal obtenido en el
experimento 1 (biodiesel).
f) Suponiendo el escalamiento del proceso de síntesis del biodiesel, explicar cuál sería el modo
de operación recomendable (reactor batch, CSTR, PFR o PBR)?
CONCLUSIONES
BIBLIOGRAFÍA
1. Smith, J. M., Ingeniería de la Cinética Química, 3ª. Edición, México, Compañía Editorial
Continental, 1991.
2. Levespiel, O., Chemical Reactor Engineering, 3ª. Edición, New York, Wiley, 1998.
3. H. Scott Fogler, Elements of Chemical Reaction Enginering, Fourth Edition, 2006, Prentice
Hall International Series
S-ar putea să vă placă și
- 008.cinética y Equilibrio QuímicoDocument9 pagini008.cinética y Equilibrio QuímicoluisÎncă nu există evaluări
- Equipo 1 - Reporte Practica 1Document8 paginiEquipo 1 - Reporte Practica 1Anayuri TrejoÎncă nu există evaluări
- 20-2019-Laboratorio 8Document3 pagini20-2019-Laboratorio 8Camila ContrerasÎncă nu există evaluări
- Informe 4 - Cinética QuímicaDocument14 paginiInforme 4 - Cinética QuímicaElizabeth HuamaniÎncă nu există evaluări
- 03 - Tablas Termodinamica - Van WylenDocument12 pagini03 - Tablas Termodinamica - Van WylenDiego Medrano Hidalgo100% (1)
- Ejercicios Quimica UndécimoDocument8 paginiEjercicios Quimica Undécimonaomy juanita vanegas garzonÎncă nu există evaluări
- FCQ3Document10 paginiFCQ3Ana MuñozÎncă nu există evaluări
- Informe 7 FisicoquimicaDocument11 paginiInforme 7 FisicoquimicaMichael Alexander Baltazar CondorÎncă nu există evaluări
- Práctica 2. Constante de Equilibrio KCDocument16 paginiPráctica 2. Constante de Equilibrio KCKaren AyalaÎncă nu există evaluări
- EstequiDocument11 paginiEstequiBriggitte RodríguezÎncă nu există evaluări
- Práctica 4. Velocidad de Una Reacción QuímicaDocument6 paginiPráctica 4. Velocidad de Una Reacción QuímicaBrayan GuttierrezÎncă nu există evaluări
- CyR - P4 - Velocidad de Reacción - A - MISCDocument10 paginiCyR - P4 - Velocidad de Reacción - A - MISCMaria Isabel SanchezÎncă nu există evaluări
- Prereporte Cinetica QuimicaDocument6 paginiPrereporte Cinetica QuimicaGabriel MoralesÎncă nu există evaluări
- Correccion. - Laboratorio Integral 2. - Práctica 14. - Reacción IónicaDocument17 paginiCorreccion. - Laboratorio Integral 2. - Práctica 14. - Reacción IónicaDavidHerreraÎncă nu există evaluări
- G8 - Cinética QuímicaDocument9 paginiG8 - Cinética QuímicaNeeiVidarteEspinoÎncă nu există evaluări
- Modulo 6 - 2020Document18 paginiModulo 6 - 2020Gisex Von LouzerÎncă nu există evaluări
- Trabajo Práctico #08, Velocidad de ReacciónDocument9 paginiTrabajo Práctico #08, Velocidad de ReacciónMauro GardinettiÎncă nu există evaluări
- Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoDocument9 paginiBalance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoANAHI ALVARADO TOLENETINOÎncă nu există evaluări
- Balance de Materia Con Reacción Química: Hidratación de Anhídrido AcéticoDocument9 paginiBalance de Materia Con Reacción Química: Hidratación de Anhídrido AcéticoFernando0% (1)
- Muñoz Ramírez S - Orta Pérez O - Ortíz Marín DM - PL1Document20 paginiMuñoz Ramírez S - Orta Pérez O - Ortíz Marín DM - PL1Osmyy OrtaÎncă nu există evaluări
- Practica 6 LabDocument7 paginiPractica 6 LabHnzÎncă nu există evaluări
- Practica 3 LIQDocument10 paginiPractica 3 LIQLuis Fernando Gomez GuzmanÎncă nu există evaluări
- Reporte Práctica 7Document3 paginiReporte Práctica 7cristo JiménezÎncă nu există evaluări
- Labs3 - Cinética QuímicaDocument4 paginiLabs3 - Cinética QuímicaCamila Helena Arevalo PeraltaÎncă nu există evaluări
- Metodo TitrimétricoDocument12 paginiMetodo Titrimétricoangelkgm2475% (4)
- Constante de EquilibrioDocument8 paginiConstante de EquilibrioMaggyBalcazarÎncă nu există evaluări
- Subtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Document9 paginiSubtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Adán Fonseca HernandezÎncă nu există evaluări
- Estequiometria de Las ReaccionesDocument3 paginiEstequiometria de Las ReaccionesLuis ZárateÎncă nu există evaluări
- Laboratorio de Equilibrio Quimico-2021-1Document12 paginiLaboratorio de Equilibrio Quimico-2021-1VICTOR ENRIQUE QUISPE SAMANEZÎncă nu există evaluări
- PRACTICA 11.2 CatalizadoresDocument6 paginiPRACTICA 11.2 CatalizadoresCari CarinaÎncă nu există evaluări
- 2da Guia de PreguntasDocument3 pagini2da Guia de PreguntasAna Sofía Molina OrtegaÎncă nu există evaluări
- Manual de FisicoquimicaDocument37 paginiManual de FisicoquimicaAriza CarmenÎncă nu există evaluări
- CINETICA QUIMICA MG - HCLDocument6 paginiCINETICA QUIMICA MG - HCLMinerosAguilarÎncă nu există evaluări
- ALIS Práctica de EstandarizaciónDocument11 paginiALIS Práctica de EstandarizaciónVivi Mar CSiÎncă nu există evaluări
- Equipo 6 - Práctica 5Document5 paginiEquipo 6 - Práctica 5Nazza ReyezÎncă nu există evaluări
- Orden de Reacción LaboratorioDocument12 paginiOrden de Reacción LaboratorioLuciaÎncă nu există evaluări
- Guia de Trabajo PracticoQUIMICADocument13 paginiGuia de Trabajo PracticoQUIMICAmarlon aliaga felipeÎncă nu există evaluări
- Informe 9-Cinetica QuímicaDocument6 paginiInforme 9-Cinetica QuímicaMari NarvaezÎncă nu există evaluări
- TERBUTILODocument5 paginiTERBUTILOjuanka0426Încă nu există evaluări
- Practica No. 2 Principio de Le ChatelierDocument4 paginiPractica No. 2 Principio de Le ChatelierAlfredo GarcíaÎncă nu există evaluări
- P-10 Calculos EstequiometricosDocument7 paginiP-10 Calculos Estequiometricosjose david de arco de avilaÎncă nu există evaluări
- Manual de Laboratorio de Quimica AnaliticaDocument7 paginiManual de Laboratorio de Quimica AnaliticaJESUS FRANCISCO DUARTEÎncă nu există evaluări
- Laboratorio de Quimica GeneralDocument8 paginiLaboratorio de Quimica GeneralGiovani Periche PachecoÎncă nu există evaluări
- Practica # 6. Degradación de Una Solución de MetilenoDocument5 paginiPractica # 6. Degradación de Una Solución de MetilenoPaula PechenéÎncă nu există evaluări
- 008.cinética y Equilibrio QuímicoDocument5 pagini008.cinética y Equilibrio QuímicoBoris Fabian Agaon BurbanoÎncă nu există evaluări
- Lab. Quimica2Document6 paginiLab. Quimica2Wilmer Castro RoblesÎncă nu există evaluări
- Quimica IIDocument24 paginiQuimica IIatila117Încă nu există evaluări
- Manual de Prácticas de Reactores QuímcosDocument35 paginiManual de Prácticas de Reactores QuímcosHéctor Alejandro Serrano Ortiz0% (1)
- Practica 4 CINETICADocument3 paginiPractica 4 CINETICALulú Olvera SalgadoÎncă nu există evaluări
- Manual de Prácticas. CqybDocument32 paginiManual de Prácticas. CqybjuansalvadorgarciaheÎncă nu există evaluări
- Practica N 7 Informe de LaboratorioDocument20 paginiPractica N 7 Informe de LaboratorioElizabethVargasÎncă nu există evaluări
- Practica 11Document20 paginiPractica 11Thania GarciaÎncă nu există evaluări
- p1 Ricardez Roman YazminDocument6 paginip1 Ricardez Roman YazminRicardez Román YazmínÎncă nu există evaluări
- Formato de Informe QADocument9 paginiFormato de Informe QAJuan Jurado CoboÎncă nu există evaluări
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDe la EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadÎncă nu există evaluări
- El cianuro en la minería. Efectos sobre las plantas acuaticasDe la EverandEl cianuro en la minería. Efectos sobre las plantas acuaticasÎncă nu există evaluări
- Introducción Liquido LiquidoDocument1 paginăIntroducción Liquido LiquidoJesus Chavez RodriguezÎncă nu există evaluări
- Ejercicio de Tarea de Ractores PFRDocument3 paginiEjercicio de Tarea de Ractores PFRJesus Chavez RodriguezÎncă nu există evaluări
- Gas NaturalDocument4 paginiGas NaturalJesus Chavez RodriguezÎncă nu există evaluări
- Tecnológico de Estudios Superiores de JocotitlánDocument6 paginiTecnológico de Estudios Superiores de JocotitlánJesus Chavez RodriguezÎncă nu există evaluări
- Practica de Naranja.Document8 paginiPractica de Naranja.Jesus Chavez RodriguezÎncă nu există evaluări
- CALCULOSDocument2 paginiCALCULOSJesus Chavez RodriguezÎncă nu există evaluări
- Ejercicios TraducidosDocument14 paginiEjercicios TraducidosJesus Chavez RodriguezÎncă nu există evaluări
- Columna de AbsorcionDocument4 paginiColumna de AbsorcionJesus Chavez RodriguezÎncă nu există evaluări
- Describir El Siguiente Diagrama de ProcesoDocument1 paginăDescribir El Siguiente Diagrama de ProcesoJesus Chavez RodriguezÎncă nu există evaluări
- Unidad III - No Idealidad en Reactores QuímicosDocument21 paginiUnidad III - No Idealidad en Reactores QuímicosJesus Chavez Rodriguez100% (3)
- Destilación Diferencial FLASHEOODocument4 paginiDestilación Diferencial FLASHEOOJulian Solo JulainÎncă nu există evaluări
- Encuesta de OpinionDocument3 paginiEncuesta de OpinionJesus Chavez RodriguezÎncă nu există evaluări
- Práctica No. 3 ReactoresDocument4 paginiPráctica No. 3 ReactoresJesus Chavez RodriguezÎncă nu există evaluări
- 1646488710.destilación DiferencialDocument1 pagină1646488710.destilación DiferencialJesus Chavez RodriguezÎncă nu există evaluări
- EjerciciosDocument7 paginiEjerciciosJesus Chavez RodriguezÎncă nu există evaluări
- Torre Absorcion Pag 15 PDFDocument56 paginiTorre Absorcion Pag 15 PDFomarlibardoÎncă nu există evaluări
- Muc ImexDocument4 paginiMuc ImexJesus Chavez RodriguezÎncă nu există evaluări
- Ejercicio 3Document2 paginiEjercicio 3Jesus Chavez RodriguezÎncă nu există evaluări
- Ejercicio 5 TareaDocument2 paginiEjercicio 5 TareaJesus Chavez RodriguezÎncă nu există evaluări
- Planteamiento Del ProblemaDocument1 paginăPlanteamiento Del ProblemaJesus Chavez RodriguezÎncă nu există evaluări
- Práctica No. 3 ReactoresDocument4 paginiPráctica No. 3 ReactoresJesus Chavez RodriguezÎncă nu există evaluări
- 13 SepDocument9 pagini13 SepJesus Chavez RodriguezÎncă nu există evaluări
- Destilación Diferencial FLASHEOODocument4 paginiDestilación Diferencial FLASHEOOJulian Solo JulainÎncă nu există evaluări
- 1646488710.destilación DiferencialDocument1 pagină1646488710.destilación DiferencialJesus Chavez RodriguezÎncă nu există evaluări
- Procesos de La Fabricacion de CerealDocument1 paginăProcesos de La Fabricacion de CerealJesus Chavez RodriguezÎncă nu există evaluări
- Reacciones DetergenteDocument6 paginiReacciones DetergenteJesus Chavez RodriguezÎncă nu există evaluări
- Conclusion EsDocument1 paginăConclusion EsJesus Chavez RodriguezÎncă nu există evaluări
- Documento CompletoDocument263 paginiDocumento CompletoAngie AyusawaÎncă nu există evaluări
- De PriesterDocument4 paginiDe PriesterJesus Chavez RodriguezÎncă nu există evaluări
- V e Covec y Riel Comun Hyundai PDFDocument109 paginiV e Covec y Riel Comun Hyundai PDFmanuelmanrique100% (2)
- Catalizadores y Catalisis HeterogeneaDocument36 paginiCatalizadores y Catalisis HeterogeneaMarlon Alarcon100% (3)
- Clase 11 (19-10-2022)Document26 paginiClase 11 (19-10-2022)Lucas RFÎncă nu există evaluări
- AlosterismoDocument12 paginiAlosterismoNatalia Santos100% (1)
- Practica 3. Tiempo de GelacionDocument4 paginiPractica 3. Tiempo de GelacionvillenaislaÎncă nu există evaluări
- Bolivia Ocupa El Quinto Lugar en Reservas de Shale GasDocument16 paginiBolivia Ocupa El Quinto Lugar en Reservas de Shale GasSoledad Apaza BaltazarÎncă nu există evaluări
- Taller de Repaso de EnzimasDocument8 paginiTaller de Repaso de EnzimasDani CardonaÎncă nu există evaluări
- Isoterma de AdsorciónDocument24 paginiIsoterma de AdsorciónFrancisco Lara100% (1)
- RotaxanosDocument8 paginiRotaxanosA Fernando CGÎncă nu există evaluări
- Plan Global Refinación PetroleoDocument15 paginiPlan Global Refinación PetroleoRodrigoMoreno100% (2)
- 303-42618-It-002 Retiro Juntas CiegasDocument20 pagini303-42618-It-002 Retiro Juntas CiegasJc JaÎncă nu există evaluări
- Trabajo Lechos EmpacadosDocument15 paginiTrabajo Lechos EmpacadosJessica Romero FontalvoÎncă nu există evaluări
- Taller ENZIMAS (1) - Yermyn SilvaDocument11 paginiTaller ENZIMAS (1) - Yermyn SilvaMichael ArangoÎncă nu există evaluări
- Jose Manuel GarciaDocument1 paginăJose Manuel Garciasaul parraÎncă nu există evaluări
- Dialnet Esterificacion 4902598 PDFDocument8 paginiDialnet Esterificacion 4902598 PDFBianca LeyvaÎncă nu există evaluări
- Cuadro Comparativo (Trabajo 2) EliaDocument4 paginiCuadro Comparativo (Trabajo 2) EliaJesús DelgadoÎncă nu există evaluări
- Guía 85Document8 paginiGuía 85Daniela AltamiranoÎncă nu există evaluări
- Estireno 1Document9 paginiEstireno 1GariTo GomezÎncă nu există evaluări
- Cap 8 Enzimas Cinetica HARPER Bioquimica Ilustrada 28a Ed-3Document13 paginiCap 8 Enzimas Cinetica HARPER Bioquimica Ilustrada 28a Ed-3Estela Beatríz Mora GarcíaÎncă nu există evaluări
- HIDROGENACIÓNDocument7 paginiHIDROGENACIÓNRuselÎncă nu există evaluări
- Planta de FCCDocument58 paginiPlanta de FCCAlvaro Choque AlmanzaÎncă nu există evaluări
- Curriculum Vitae Ing. GarciaDocument12 paginiCurriculum Vitae Ing. GarciaAlexis Morales PintoÎncă nu există evaluări
- Principales Características de Las Células VivasDocument3 paginiPrincipales Características de Las Células VivasJoos VillacisÎncă nu există evaluări
- Velocidad de Reacción y Equ Quimico (Nueva)Document25 paginiVelocidad de Reacción y Equ Quimico (Nueva)Luis SeijasÎncă nu există evaluări
- Sintesis de BiodieselDocument4 paginiSintesis de BiodieselAmparo PratticoÎncă nu există evaluări
- Solucionario Cap 1-Cap 2Document3 paginiSolucionario Cap 1-Cap 2davidlm22100% (1)
- Obtencion de Catalasa .. Esta SiDocument22 paginiObtencion de Catalasa .. Esta Sijuan100% (1)
- Tarea 8 CQC 2022-1Document5 paginiTarea 8 CQC 2022-1Miriam Hernández JaramilloÎncă nu există evaluări
- Goldbook IUPACDocument22 paginiGoldbook IUPACUlices Fdz0% (1)