Documente Academic
Documente Profesional
Documente Cultură
Qu Ica (Examen, Titular)
Încărcat de
Antonio Ruiz MartinezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Qu Ica (Examen, Titular)
Încărcat de
Antonio Ruiz MartinezDrepturi de autor:
Formate disponibile
QÚIMICA
UNIVERSIDADES DE ANDALUCÍA
CURSO 2017/2018
PRUEBA DE ACCESO PARA MAYORES DE 25 AÑOS
Instrucciones: a) Duración: El examen tendrá una duración de 1 hora y 30 minutos.
b) Elija y desarrolle uno de los dos problemas propuestos. Indique claramente el problema elegido.
c) El problema se calificará hasta un máximo de 4 puntos. En cada apartado se indica la puntuación máxima que
le corresponde.
d) Elija y desarrolle dos de las cuatro cuestiones teóricas propuestas. Indique claramente las cuestiones
elegidas.
e) Cada una de las dos cuestiones elegidas se calificará hasta un máximo de 3 puntos.
f) Puede utilizar calculadora no programable.
PROBLEMAS (a elegir uno)
Problema 1
En un recipiente de 5 L se introducen un mol de dióxido de azufre (SO2) y un mol de oxígeno (O2) y se
calienta a 1000 K, produciéndose trióxido de azufre (SO3). Cuando se alcanza el equilibrio quedan 0,15
moles de SO2 .
a) Escriba la correspondiente ecuación química ajustada. (hasta 1 punto)
b) Calcule los moles de O2 presentes en el equilibrio. (hasta 1 punto)
c) Calcule la presión parcial de SO3 en el equilibrio. (hasta 1 punto)
d) Calcule los valores de las constantes de equilibrio Kc y Kp. (hasta 1 punto)
Datos. R = 0,082 atm·L·K–1·mol–1.
Problema 2
a) Calcule la riqueza de una sosa cáustica comercial (expresada en % en masa de NaOH), sabiendo que
si se disuelven 0,5 g de la misma en 50 mL de agua, la disolución resultante necesita 20 mL de una
disolución de HCl de concentración 0,5 M para su completa neutralización. (hasta 1 punto)
b) ¿Cuál sería el pH de la disolución de NaOH antes de la neutralización?. (hasta 1 punto)
c) ¿Cómo prepararía 500 mL de una disolución 0.5 M de HCl si se dispone de una disolución 3 M de
HCl?. (hasta 1 punto)
d) ¿Cómo prepararía 1 L de la disolución 3 M de HCl a partir de HCl concentrado comercial que contiene
un 37% en masa de HCl y posee una densidad de 1,19 g/mL?. (hasta 1 punto)
Masas atómicas: Na= 23; Cl = 35,5; H = 1; O = 16.
CUESTIONES TEÓRICAS (a elegir dos)
Tema 1: Número atómico. Número másico. Isótopos.
Tema 2: Propiedades periódicas: Radio atómico y radio iónico, energía de ionización y afinidad
electrónica. Electronegatividad.
Tema 3: Isomería: concepto y clases.
Tema 4: Enlace iónico y enlace covalente: concepto y propiedades.
S-ar putea să vă placă și
- Economia Ejemplo PDFDocument4 paginiEconomia Ejemplo PDFAntonio Ruiz MartinezÎncă nu există evaluări
- CICLACIÓNDocument2 paginiCICLACIÓNAntonio Ruiz MartinezÎncă nu există evaluări
- PDFDocument8 paginiPDFAntonio Ruiz MartinezÎncă nu există evaluări
- Examenfisicacuantica I PDFDocument13 paginiExamenfisicacuantica I PDFAntonio Ruiz MartinezÎncă nu există evaluări
- Problemas de Ecuaciones Diferenciales. DepositosDocument2 paginiProblemas de Ecuaciones Diferenciales. DepositosAntonio Ruiz MartinezÎncă nu există evaluări
- Matematicas 1 Eso - Ejercicios Numeros Enteros Con SolucionesDocument22 paginiMatematicas 1 Eso - Ejercicios Numeros Enteros Con SolucionesOmar BritoÎncă nu există evaluări
- Tema 18. Operaciones Básicas. Mantenimiento y Preparación de Reactivos Yo Muestras para Espectrofotometría, Cromatografía de Gases, HPLC y Absorción Atómica, ICP, IR y RMNDocument3 paginiTema 18. Operaciones Básicas. Mantenimiento y Preparación de Reactivos Yo Muestras para Espectrofotometría, Cromatografía de Gases, HPLC y Absorción Atómica, ICP, IR y RMNAntonio Ruiz MartinezÎncă nu există evaluări
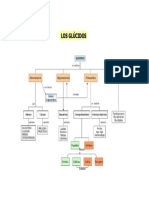
- Esquema GlucidosDocument1 paginăEsquema GlucidosAntonio Ruiz MartinezÎncă nu există evaluări
- Examen Parcial Ingeniería de Estructuras II Parte 1 - Revisión Del IntentoDocument5 paginiExamen Parcial Ingeniería de Estructuras II Parte 1 - Revisión Del Intentojosue geovanny villamar parralesÎncă nu există evaluări
- Diapositivas-Historia de La Ing CivilDocument15 paginiDiapositivas-Historia de La Ing CivilMayKol Rosas PomaÎncă nu există evaluări
- 3 - Conductividad Termica Del Hierro - UpdtDocument4 pagini3 - Conductividad Termica Del Hierro - UpdtMauro MalcaÎncă nu există evaluări
- 1.4.1. Elementos de Control y MandoDocument17 pagini1.4.1. Elementos de Control y MandoManuel Fabian Bacab EkÎncă nu există evaluări
- Metodos de Proteccion RadiologicaDocument26 paginiMetodos de Proteccion Radiologicakarlos0407Încă nu există evaluări
- Marcha Analítica de Separaciones de Los Cationes Del Quinto GrupoDocument13 paginiMarcha Analítica de Separaciones de Los Cationes Del Quinto GrupoJavier Carbajal Torrico33% (3)
- Formatos Oe en ExcellDocument22 paginiFormatos Oe en ExcellJorgeLuisMolinaMacavilcaÎncă nu există evaluări
- Aforo de TanquesDocument14 paginiAforo de TanquesSergio Dario Suarez RomeroÎncă nu există evaluări
- Ejercicios Capitulo 7 - VerticalDocument4 paginiEjercicios Capitulo 7 - VerticalCRISTIAN DAVID CRUZ ALFAROÎncă nu există evaluări
- Cañote Fisica 1 FIIS UNIDocument2 paginiCañote Fisica 1 FIIS UNIrianiÎncă nu există evaluări
- Cuestionario de Ciencias II Con Énfasis en FísicaDocument4 paginiCuestionario de Ciencias II Con Énfasis en FísicaLoupita SazsloÎncă nu există evaluări
- Informe Diseño Pavimento FlexibleDocument26 paginiInforme Diseño Pavimento Flexiblejair cantaro pabloÎncă nu există evaluări
- Martin Mora, Angel Campos - SueñonautaDocument38 paginiMartin Mora, Angel Campos - SueñonautaRay GamiÎncă nu există evaluări
- La Acción DramáticaDocument3 paginiLa Acción DramáticaMaxi HernandezÎncă nu există evaluări
- Cesar Soto Santos - Actividad Entregable - 2Document4 paginiCesar Soto Santos - Actividad Entregable - 2Alucart Cass100% (4)
- Tarea 2Document7 paginiTarea 2Kateryne RochaÎncă nu există evaluări
- CB 11-15 Matemáticas 5 C Pruebas EvalDocument20 paginiCB 11-15 Matemáticas 5 C Pruebas EvalSergio Mora OrtizÎncă nu există evaluări
- Vectores (Metodo Del Poligono 2)Document9 paginiVectores (Metodo Del Poligono 2)Josué Dassaev100% (1)
- Lab 05 Mec SolidosDocument24 paginiLab 05 Mec SolidosJhon Miranda VelasquezÎncă nu există evaluări
- Exoesqueleto NeckDocument16 paginiExoesqueleto NeckJUAN JOSEÎncă nu există evaluări
- Cap 09 Analisis y Diseño de PavimentosDocument104 paginiCap 09 Analisis y Diseño de PavimentosDiego Marquez AgueroÎncă nu există evaluări
- I Bimestre Geometría 1ro SecundariaDocument44 paginiI Bimestre Geometría 1ro SecundariaNicolns EstefannyÎncă nu există evaluări
- Documento 3Document2 paginiDocumento 3YesidCaballeroÎncă nu există evaluări
- Informe 5Document20 paginiInforme 5Mariana Estrella Callisaya ValenciaÎncă nu există evaluări
- Capitulo 5 Manuales de Mecanica de Pavimentos 2018Document111 paginiCapitulo 5 Manuales de Mecanica de Pavimentos 2018Fabio GarzonÎncă nu există evaluări
- Wa0024 PDFDocument358 paginiWa0024 PDFEylin Alexsandra Ramos CandiaÎncă nu există evaluări
- Actividad 3Document4 paginiActividad 3Alexander OrtizÎncă nu există evaluări
- Tarea 2 Ser Humano y Desarrollo SostenibleDocument8 paginiTarea 2 Ser Humano y Desarrollo Sosteniblejose mosquea100% (1)
- Concreto Vigas Teoria ElasticaDocument8 paginiConcreto Vigas Teoria ElasticaGladys VizcainoÎncă nu există evaluări
- NAT4 Saberes en Red ODDocument26 paginiNAT4 Saberes en Red ODDalina CostaÎncă nu există evaluări