Documente Academic
Documente Profesional
Documente Cultură
5 Lucia Pitarch
Încărcat de
Fernando RosalesDescriere originală:
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
5 Lucia Pitarch
Încărcat de
Fernando RosalesDrepturi de autor:
Formate disponibile
Implantación de la norma ISO
17025:2017 en un Sistema
Integrado de Gestión:
nuevos conceptos
JORNADAS DE REFERENCIA 2018 – Majadahonda 19 al 21 de junio
SESION: Modificación de norma ISO 17025. Nuevos proyectos de ENAC y los
Laboratorios Nacionales de Referencia (LNR).
Lucía B. Pitarch Mampel
Coordinadora General de Laboratorios de Sanidad Animal y
Responsable de los Sistemas Integrados de Gestión
MAPA - SGSHAT
REQUISITOS ISO/IEC 17.025:2005
4. REQUISITOS
5. REQUISITOS
RELATIVOS A LA
TÉCNICOS
GESTIÓN
4.2 Sistema de 4.3 Control de 5.1
4.1 Organización 5.2 Personal
gestión los documentos Generalidades
4.4 Revisión de 4.5 4.6 Compras de 5.3 Instalaciones
5.4 Métodos de
los pedidos, Subcontratación servicios y y cond.
ensayo
ofertas y contr. de ensayos suministros ambientales
4.9 Control de 5.6 Trazabilidad
4.7 Servicios al
4.8 Quejas trabajos de 5.5 Equipos de las
cliente
ensayo mediciones
5.8 Manipulación
4.11 Acciones 4.12 Acciones
4.10 Mejora 5.7 Muestreo de los ítems de
correctivas preventivas
ensayo
5.9
4.13 Control de 4.14 Auditorías 4.15 Revisión 5.10 Informe de
Aseguramiento
los registros internas por la Dirección los resultados
de la calidad
CGL – SANIDAD ANIMAL
REQUISITOS ISO/IEC 17.025:2017
5. REQUISITOS 6. REQUISITOS 8. REQUISITOS DEL
4. REQUISITOS 7. REQUISITOS DEL
RELATIVOS A LA RELATIVOS A LOS SISTEMA DE
GENERALES PROCESO
ESTRUCTURA RECURSOS GESTIÓN
7.1 Revisión
4.1 6.1
solicitudes, 7.2 Métodos 8.1 Opciones
Imparcialidad Generalidades
ofertas y contr.
4.2 7.4 Manipulación 8.2 Doc. Del sist. 8.3 Control de
6.2 Personal 7.3 Muestreo
Confidencialidad de ítems De gestión (A) los docs (A)
7.6 Evaluación 8.5 Acciones
6.3 Instalaciones 7.5 Registros 8,4 Control de
de la abordar riesgos y
y cond. Amb. técnicos registros (A)
incertidumbre oport. (A)
7.7 Aseg. de la
6.4 7.8 Informe de 8.7 Acciones
validez de los 8.6 Mejora (A)
Equipamiento resultados correctivas (A)
resultados
8.9 Revisiones
6.5 Trazabilidad 7.10 Trabajo no 8.8 Auditorías
7.9 Quejas por la Dirección
metrológica conforme internas (A)
(A)
7.11 Control de
6.6 Prod. Y serv.
los datos y gest.
Suministr. Ext.
información
CGL – SANIDAD ANIMAL
Transición a la ISO 17.025:2017
UNE-EN ISO/IEC 17025:2017 (30 noviembre 2017)
Los principales cambios que se han introducido son:
Enfoque a procesos. Concuerda con el resto de normas ISO recientemente
revisados, como es el caso de ISO 9001:2015.
Mayor uso de las tecnologías de la información. Se ve reforzado incluyendo
el uso de sistemas informáticos, registros electrónicos y producción tanto de
resultados como de informes en formato electrónico.
Pensamiento basado en el riesgo. Se reducen requisitos prescriptivos por
requisitos basados en el desempeño.
Además,
Mayor flexibilidad en los requisitos de procesos, procedimientos, información
documentada y responsabilidades organizacionales.
La revisión del alcance ha permitido que cubrir los ensayos, la calibración y
el muestreo vinculado con la calibración y las pruebas subsiguientes.
CGL – SANIDAD ANIMAL
ÍNDICE 1. Objeto y Campo de aplicación
2. Referencias normativas
3. Términos y definiciones
1. Objeto y Campo de aplicación
4. Contexto de la organización
2. Referencias normativas 5. Liderazgo
6. Planificación
3. Términos y definiciones 7. Apoyo
8. Operación
4. Requisitos generales
9. Evaluación de desempeño
5. Requisitos relativos a la Estructura 10. Mejora
6. Requisitos relativos a los Recursos 1. Alcance
2. Referencias normativas
7. Requisitos del Proceso 3. Términos y definiciones
4. Contexto de la organización
8. Requisitos del Sistema de Gestión
5. Liderazgo
6. Planificación
Anexo A Trazabilidad metrológica
7. Soporte
8. Operaciones
Anexo B Opciones de sistema de gestión
9. Evaluación del desempeño
10. Mejora
CGL – SANIDAD ANIMAL
PGSIG - LCV
❖ PGSIG-01: Elaboración de documentos
❖ PGSIG-02: Gestión de documentos
❖ PGSIG-03: Gestión de personal
❖ PGSIG-04: Identificación y evaluación de requisitos
legales y otros requisitos
❖ PGSIG-05: Objetivos y metas
❖ PGSIG-06: Aspectos ambientales y Desempeño
❖ PGSIG-07: Identificación y evaluación de riesgos
❖ PGSIG-08: Gestión de EPIs
❖ PGSIG-09: Gestión de incidentes, accidentes y
respuesta ante emergencias
❖ PGSIG-10: Gestión de muestras y ensayos
❖ PGSIG-11: Validación y evaluación de calidad de los
ensayos
❖ PGSIG-12: Ensayos de intercomparación
❖ PGSIG-13: Envío de material biológico
CGL – SANIDAD ANIMAL
PGSIG - LCV
❖ PGSIG-14: Gestión de control de equipos
❖ PGSIG-15: Planificación y Control operacional
❖ PGSIG-16: Gestión de residuos
❖ PGSIG-17: Gestión y control del área NBS3
❖ PGSIG-18: Contención primaria LBS3
❖ PGSIG-19: Contención primaria ABS3
❖ PGSIG-20: Contención secundaria LBS3
❖ PGSIG-21: Contención secundaria ABS3
❖ PGSIG-22: Gestión y control de sala limpia en
animalario
❖ PGSIG-23: Compras y subcontratación
❖ PGSIG-24: Gestión de reclamaciones
❖ PGSIG-25: mejora, Trabajos no conformes, no
conformidades y acciones preventivas
❖ PGSIG-26: Auditorías internas y revisión por la
dirección
❖ PGSIG-27: Gestión y control de la cuarentena
❖ PGSIG-28: Riesgos y oportunidades
CGL – SANIDAD ANIMAL
1. Objeto y Campo de aplicación
• Requisitos generales relativos a la competencia,
imparcialidad y operación coherente de los laboratorios
NUEVO • Aplicable a todos los laboratorios, con
independencia del nº de empleados
• No cubre el cumplimiento de los requisitos
reglamentarios y de seguridad en la actividad de los
laboratorios.
Esta norma requiere que el laboratorio planifique e NUEVO
implemente acciones para la gestión de riesgos y
oportunidades.
CGL – SANIDAD ANIMAL
2. Referencias normativas
Guía ISO/IEC 99 y la Norma ISO/IEC 17000 “Evaluación de la
conformidad – Vocabulario y principios generals”.
BASES DE DATOS TERMINOLÓGICAS – ISO e IEC
CGL – SANIDAD ANIMAL
3. Términos y definiciones
Los contenidos en los documentos de referencias normativas
• Imparcialidad: presencia de objetividad (no existen conflictos de
intereses o se resuelven sin afectar de forma adversa a las actividades
de laboratorio)
• Queja: expresión de insatisfacción que requiere una respuesta.
• Comparación interlaboratorios: organización, realización y
evaluación de mediciones o ensayos sobre el mismo ítem o ítems
similares por dos o más laboratorios de acuerdo con condiciones
predeterminadas.
• Comparación intralaboratorio: organización, realización y evaluación
de mediciones o ensayos sobre el mismo ítem o ítems similares, en el
mismo laboratorio de acuerdo con unas condiciones predeterminadas
• Ensayo de aptitud: evaluación del desempeño de los participantes con
respecto a criterios previamente establecidos mediante comparaciones
interlaboratorios.
CGL – SANIDAD ANIMAL
3. Términos y definiciones
• LABORATORIO: organismo que realiza una o más de las
siguientes actividades:
- Ensayos
- Calibración
- Muestreo (asociado con el subsiguiente ensayo o NUEVO
calibración)
• Regla de decisión: regla que describe cómo se toma en
cuenta la incertidumbre de medición cuando se declara la NUEVO
conformidad con un requisito especificado.
• Verificación: aportación de evidencia objetiva de que
un ítem dado satisface los requisitos especificados.
• Validación: verificación de que se cumplen los requisitos
especificados para un uso previsto.
CGL – SANIDAD ANIMAL
4. Requisitos generales
NUEVO
Los contenidos en los documentos de referencias normativas
• IMPARCIALIDAD: las actividades se deben realizar de manera imparcial y
estructurada (sin presiones comerciales, financieras,…).
- Concepto que debe aparecer en la política
- Debe identificarse y evaluar el riesgo de que se produzca:
- Riesgos de imparcialidad derivados de la propia actividad.
- Riesgos de imparcialidad derivados de las relaciones del
personal del laboratorio con partes interesadas.
- Riesgos de imparcialidad derivados de las relaciones del
personal del laboratorio entre si.
• CONFIDENCIALIDAD: evaluación del
desempeño de los participantes con respecto a
criterios previamente establecidos mediante
comparaciones interlaboratorios.
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
IDENTIFICACIÓN DE RIESGOS Y OPORTUNIDADES
FUENTE DE
SISTEMA DE OBSERVAC
FUENTE/FOCO ACTIVIDAD EFECTO IDENTIFICACIÓ DESCRIPCIÓN
EVALUACIÓN IONES
N
Riesgo 1 en realización de actividades diarias o con
la relación con las partes interesadas no se
considera riesgo significativo, ya que el personal
del LCV es funcionario/laboral o de medios propios
Derivada de la actividad
de la administración. Revisión del Sistema
del LCV (de ensayo y/o
Revisión del Sistema Riesgo 2 en realización de auditorías internas: No Reuniones de
IMPARCIALIDAD del auditorias) y derivadas de
Riesgo Reuniones de se considera riesgo significativo, el personal interno Dirección
personal del LCV las relaciones con las
Dirección escogido como equipo auditor cumple todos los Proceso de Auditoría
partes interesadas y/o
requisitos para ejercer dicha actividad.
entre el propio personal.
Riesgo 3 en las realizaciones entre el personal el
número no es elevado y la interrelación adecuada,
por tanto no hay tampoco un riesgo significativo
Acción: Supervisión y cumplimiento de requisitos.
Riesgo. No guardar la confidencialidad de los datos
con los que se trabaja.
Revisión del Sistema Seguimiento desde
Actividades diarias y Acción: Firma de documento de salvaguardia de
CONFIDENCIALIDAD Riesgo Reuniones de GC, control
puntuales en auditoria todo el personal con acceso a información
Dirección documentación
confidencial. Formación del personal de nuevo
ingreso.
CGL – SANIDAD ANIMAL
5. Requisitos generales a la estructura
• Laboratorio → entidad o parte definida de una entidad con MANUAL DE CALIDAD -
responsabilidades legales ORGANIZACIÓN
• Identificar personal de dirección que tiene la responsabilidad general
• Actividades que cumplen con esta norma definidas y documentadas
DECLARAR CONFORMIDAD CON EL DOCUMENTO DE TODAS LAS
ACTIVIDADES (no solo lo que incluyo en el Anexo técnico)
• Se incluyen actividades que se realizan en:
- Instalaciones permanentes
- Instalaciones temporales o móviles
- Instalaciones del cliente
CGL – SANIDAD ANIMAL
5. Requisitos generales a la estructura
• Definir la organización y estructura de gestión del laboratorio
• Responsabilidad, autoridad e interrelación de TODO el personal
que dirige, realiza o verifica trabajos que afectan a los resultados
• Procedimientos documentados (en la extensión necesaria)
• Personal técnico y de gestión con autoridad para:
implantación y mantenimiento del sistema, identificar
desviaciones, iniciar acciones, proporcionar recursos para
garantizar la validez de las actividades del laboratorio,
…………..
• Procesos de comunicación apropiados y planificación
de los cambios
Ahora NO especifica nombrar a un
responsable de calidad
CGL – SANIDAD ANIMAL
6. Requisitos relativos a los recursos
6.1 GENERALIDADES
6.2 PERSONAL
Concepto: PERFIL DE COMPETENCIA, cualificación para la competencia
para realizar las actividades,…..
SUPERVISAR QUE SE MANTIENE LA COMPENTECIA
(Ensayos de Aptitud, control de calidad,……)
AUTORIZACIÓN para cumplir requisitos de competencia (evidencias)….
No tanto hincapié en la eficacia de la formación
6.3 INSTALACIONES Y CONDICIONES AMBIENTALES
(registro de datos si aplica / control de acceso / separación de áreas)
CGL – SANIDAD ANIMAL
6. Requisitos relativos a los recursos
6.4 EQUIPAMIENTO
EQUIPOS
EQUIPAMIENTO (equipos, software, patrones, MR, reactivos, consumibles,…
6.5 TRAZABILIDAD METROLÓGICA
CALIBRACIÓN….externa…con quien?
- Instituto nacional de metrología
- Laboratorio Acreditado
- Laboratorios que yo evalúo y digo que son competentes (procedimiento de
calibración, de incertidumbre, de cualificación, resultados ensayos de
comparación, informe de auditoría,…)
MR: cumple 17043 ok / procede del LNR ok
6.6 PRODUCTOS Y SERVICIOS SUMINISTRADOS EXTERNAMENTE
PROVEEDORES / Subcontratación de ensayos
CGL – SANIDAD ANIMAL
7. Requisitos del proceso
NUEVO
7.1 REVISION DE SOLICITUDES, OFERTAS Y CONTRATOS
En caso de declaración de conformidad, se acuerda la regla de decisión a
adoptar.
Recoger en la sistemática los casos en los que el laboratorio mande el
contenedor primario de la muestra.
Cooperar con los clientes.
7.2 SELECCIÓN, VERIFICACIÓN Y VALIDACIÓN DE MÉTODOS
Características de desempeño de un método – parámetros de validación/verificación
Dejar claro cuándo el cambio de un método implica nueva verifiacion/validación
• Registros de:
- procedimiento de validación usado
- requisitos del método
- características del desempeño
NUEVO - resultados
- Declaración de su validez
CGL – SANIDAD ANIMAL
7. Requisitos del proceso
7.3 MUESTREO
7.4 MANIPULACIÓN DE LOS ITEMS DE ENSAYO O CALIBRACIÓN
gestión de las muestras a su llegada - custodia – almacenamiento
7.5 REGISTROS TÉCNICOS
que permitan repetir el ensayo de principio a fin / trazabilidad de los cambios
7.6 EVALUACIÓN DE LA INCERTIDUMBRE DE MEDICIÓN
Identificar contribuciones a la incertidumbre: ensayos / calibraciones
Indicar la incertidumbre en un resultado solo si es pertinente / si pide el cliente
7.7 ASEGURAMIENTO DE LA VALIDEZ DE LOS RESULTADOS
nuevo concepto: VALIDEZ DE LOS RESULTADOS – CALIDAD DE LOS…… NUEVO
7.7.1 ejemplos de las actividades a incluir……
7.7.2 Ensayo de aptitud/ensayos de intercomparación – SEGUIMIENTO DEL DESEMPEÑO
registro de EVALUACIÓN DE TENDENCIAS / detectar tendencias
CGL – SANIDAD ANIMAL
7. Requisitos del proceso
7.8 INFORME DE RESULTADOS
en papel o medios electrónicos / informes simplificados
7.8.2 Requisitos comunes
Identificación de la información suministrada por el cliente (con un descargo de
NUEVO responsabilidad si afecta a la validez de los resultados). NUEVO
Opiniones e interpretaciones (se incluyen en el informe y en la acreditación)
documentar la base sobre la cual se han emitido
7.9 QUEJAS
Disponible si me solicitan todo lo registrado / Comunicación de resultados al que
presenta la queja revisada y aprobada por personal no involucrado
NUEVO
7.10 TRABAJO NO CONFORME
Se adoptan medidas basadas en los niveles de riesgo establecidos
(impacto en el resultado – bajo/medio/alto) NUEVO
7.11 CONTROL DE DATOS Y GESTIÓN DE LA INFORMACIÓN
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
8.1 OPCIONES
NUEVO
Opción A
Se cumplen requisitos capítulos 4 a 7
Opción B
- Documentación del Sistema de Gestión
- Control de documentos del Sistema de Gestión
- Control de los registros
- Acciones para abordar riesgos y oportunidades
Opción A - Mejora
- Acciones correctivas
- Auditorías internas
- Revisiones por la dirección
Opción B
Cumplimiento ISO 9001 = cumplimiento con la “intención” de los
requisitos del capítulo 8
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
8.2 DOCUMENTACIÓN DEL SISTEMA DE GESTIÓN
Establecer, documentar y mantener políticas y objetivos NUEVO
NO especifica que debe haber un MANUAL (más flexible)
8.3 CONTROL DE DOCUMENTOS DEL SISTEMA DE GESTIÓN
8.4 CONTROL DE REGISTROS (7.5)
5 años…..periodo entre reevaluaciones
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
Poner la iamgen de control operacional de objetivos y metas
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
8.5 ACCIONES PARA ABORDAR RIESGOS Y OPORTUNIDADES NUEVO
• Considerar riesgos y oportunidades asociados con las
actividades del laboratorio para:
✓ asegurar que se consiguen los resultados previstos
✓ mejorar la posibilidad de conseguir propósitos y
objetivos
✓ prevenir o reducir impactos no deseados o
incumplimientos potenciales
✓ lograr la mejora
• Planificar acciones para abordar estos riesgos y oportunidades
• Integrar estas acciones en el Sistema de gestión y evaluar su
eficacia
• Acciones proporcionales al impacto potencial sobre la validez de
los resultados
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
8.5 ACCIONES PARA ABORDAR RIESGOS Y OPORTUNIDADES NUEVO
No es necesario utilizar métodos “formales” de gestión
de riesgos, ni un proceso documentado para dar
cumplimiento a este requisito
Abordar riesgos: identificar y evitar amenazas, asumir riesgos
buscando nuevas oportunidades, eliminar fuentes de riesgos,
cambiar la probabilidad de que se produzcan, eliminar o
disminuir las consecuencias, compartir el riesgo, mantener el
riesgo mediante decisiones informadas, ………………….
Abordar oportunidades: ampliación del alcance
de las actividades del laboratorio, nuevos clientes,
nuevas tecnologías, nuevos métodos, nuevas
matrices, ………………….
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
IDENTIFICACIÓN DE RIESGOS Y OPORTUNIDADES
FUENTE DE
SISTEMA DE OBSERVAC
FUENTE/FOCO ACTIVIDAD EFECTO IDENTIFICACIÓ DESCRIPCIÓN
EVALUACIÓN IONES
N
Riesgo. No poder llevar a cabo una actividad
por la ausencia del personal cualificado.
Reuniones de
AUSENCIA de Funciones de los Seguimiento desde
Dirección
PERSONAL CLAVE diferentes perfiles Riesgo Acción: Establecimiento de sustitutos GC, listado de
Seguimiento de
o relevante del personal del LCV asignados para cada persona del LCV dentro personal
GC
del perfil de su puesto de trabajo, con la
misma cualificación.
Oportunidad: Ampliar tratamiento de
resultados para abordar cuestiones
epidemiológicas, investigación de cepas
Técnica de (lengua azul en relación a nuevas actividades
NUEVAS secuenciación Oportunida Reuniones con de LR-UE, cepas de bacterias antibio Seguimiento desde
TECNOLOGÍAS (secuenciación d otros LNR / LR-UE resistencias). GC
masiva) Acción: cualificación del personal,
adquisición del conocimiento, equipos,
colaboración con otros LNR o LR-UE
RESIDUOS Generación de Oportunidad: Ampliar la segregación
Oportunida COSIG
PELIGROSOS: RESIDUOS diferenciada de residuos Objetivo 14C/18:
d Objetivos 2018
CDs y DVDs PELIGROSOS: Acción: Objetivos 2018
CGL – SANIDAD ANIMAL
8. Requisitos del sistema de gestión
8.6 MEJORA
Desaparecen las ACCIONES PREVENTIVAS
NUEVO
PLANIFICACIÓN Y SEGUIMIENTO DE ACCIONES DE MEJORA
8.7 ACCIONES CORRECTIVAS
No conformidad (7.10 Trabajo no conforme)
Actualizar riesgos y oportunidades durante la planificación
NUEVO
8.8 AUDITORIAS INTERNAS
8.9 REVISIONES POR LA DIRECCIÓN
Cambios en cuestiones internas y externas pertinentes al laboratorio
NUEVO Cumplimiento de objetivos
Resultados de la identificación de los riesgos
CGL – SANIDAD ANIMAL
• LNR
• LR-UE
• COSIG • DG SPA
• CBB • SG SHAT y SG ASCF
LCV • CEEA • DG PMA
• SG MPG y SG MPANOVV:
• LCSA
• CISA
Cuestiones • LAA
Internas • CNA
• RELAB
• TRAGSATEC
Cuestiones • TRANSPORTISTAS MUESTRAS
Externas
• Ayuntamiento del Municipio de Algete
• Canal de Isabel II
• CHT
• Empresas de las inmediaciones
• ENAC y AENOR
• Otras
1. Identificar las partes interesadas internas / externas
2. Evaluar sus necesidades y expectativas respecto a nosotros
3. Acciones a emprender por nuestra parte
4. Evaluación y seguimiento (RSD)
CGL – SANIDAD ANIMAL
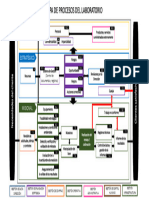
MAPA DE PROCESOS
CGL – SANIDAD ANIMAL
Lucía B. Pitarch Mampel
lpitarch@mapama.es
Muchas
gracias
¡¡¡¡¡¡¡¡A POR LA NUEVA ISO
17025:2017!!!!!!!
S-ar putea să vă placă și
- Requistos - Transición ISO-IEC 17025Document1 paginăRequistos - Transición ISO-IEC 17025Zenaida EncisoÎncă nu există evaluări
- Tabla Comparativa Entre La Segunda y Tercera Edicion de La ISO - IEC 17025Document4 paginiTabla Comparativa Entre La Segunda y Tercera Edicion de La ISO - IEC 17025Sandra Patricia Peñaherrera NavarreteÎncă nu există evaluări
- Resumen de La Norma Iso 17025 y Acreditacion MonitoreoDocument7 paginiResumen de La Norma Iso 17025 y Acreditacion MonitoreoJancarlos QPÎncă nu există evaluări
- Comparacion Sistema de Gestion de CalidadDocument6 paginiComparacion Sistema de Gestion de CalidadSara SánÎncă nu există evaluări
- Curso Normas Iso 17025 IIDocument62 paginiCurso Normas Iso 17025 IIErick BetancourtÎncă nu există evaluări
- Plantilla MAPA DE PROCESOSDocument1 paginăPlantilla MAPA DE PROCESOSEsperanza Del Carmen GamezÎncă nu există evaluări
- Mapa Conceptual Gestión de La Calidad: Norma ISO 9001-2008Document3 paginiMapa Conceptual Gestión de La Calidad: Norma ISO 9001-2008Mónica García carrilloÎncă nu există evaluări
- IEC/17025Document10 paginiIEC/17025RUBENS100% (1)
- Eje 2 - WikiDocument5 paginiEje 2 - WikiAngelica grillo trivoñpÎncă nu există evaluări
- Integralidad de Los Sistemas de Gestión OriginalDocument24 paginiIntegralidad de Los Sistemas de Gestión OriginalDaniel OlivaÎncă nu există evaluări
- Toaz - Info Iso 17025 PRDocument3 paginiToaz - Info Iso 17025 PRRafael CardenasÎncă nu există evaluări
- Plantilla MAPA DE PROCESOSDocument1 paginăPlantilla MAPA DE PROCESOSJoyce Briceida Torres SanchezÎncă nu există evaluări
- Diagram A en BlancoDocument2 paginiDiagram A en BlancoSandra Victoria Valdez RamírezÎncă nu există evaluări
- Requisitos para Las Normas de ReferenciaDocument6 paginiRequisitos para Las Normas de ReferenciaJoel RodriguezÎncă nu există evaluări
- Iso 17025:2017Document16 paginiIso 17025:2017Fernando100% (1)
- Estructura Norma ISO 9001 2015Document1 paginăEstructura Norma ISO 9001 2015sparrowomar85Încă nu există evaluări
- UNE 73401 Ed.95 - Garantía de La Calidad en Instalaciones NuclearesDocument22 paginiUNE 73401 Ed.95 - Garantía de La Calidad en Instalaciones Nuclearesrubenagudo7Încă nu există evaluări
- Mapa Mental RequisitosDocument1 paginăMapa Mental RequisitosPa NoliteÎncă nu există evaluări
- Cambios 17025 IsoDocument21 paginiCambios 17025 IsoNICOLASÎncă nu există evaluări
- Requisitos Normativos Tri-Norma.Document3 paginiRequisitos Normativos Tri-Norma.Alejandro Olivares100% (1)
- P. Cambios - Actualizacion17025 2017Document31 paginiP. Cambios - Actualizacion17025 2017Luis GutiÎncă nu există evaluări
- ISO 13485 EspañolDocument35 paginiISO 13485 EspañolMichelleAlvarezÎncă nu există evaluări
- NTC ISO 17025 Cambios Version 2017Document21 paginiNTC ISO 17025 Cambios Version 2017paulaandreapaezordoeÎncă nu există evaluări
- Implementa Un SGC de Forma Ágil Con Scrum - ASQ 11.05.20Document46 paginiImplementa Un SGC de Forma Ágil Con Scrum - ASQ 11.05.20Mn5ATUÎncă nu există evaluări
- Matriz de Sistemas Integrados de Gestión (Sig) de Correspondencia de Basc.2017, Iso 9001.2015, Iso 14001.2015, Iso 45001.2019, Iso 27001.2013, Iso 37001.2016Document3 paginiMatriz de Sistemas Integrados de Gestión (Sig) de Correspondencia de Basc.2017, Iso 9001.2015, Iso 14001.2015, Iso 45001.2019, Iso 27001.2013, Iso 37001.2016Wilian Atajo MamaniÎncă nu există evaluări
- SaeDocument20 paginiSaeSergioFernandoMendozaMendozaÎncă nu există evaluări
- CALIDADDocument57 paginiCALIDADGabriela Caba SardeÎncă nu există evaluări
- Sistema de Gestion de Calidad ISO 90012015Document117 paginiSistema de Gestion de Calidad ISO 90012015MassielAlcantaraÎncă nu există evaluări
- Manual de CalidadDocument58 paginiManual de Calidadnestor valladolidÎncă nu există evaluări
- Mapas ISO9001Document10 paginiMapas ISO9001Jeshuany CamposÎncă nu există evaluări
- A) MC-01 V11 Manual Del Sistema de Gestión de La CalidadDocument94 paginiA) MC-01 V11 Manual Del Sistema de Gestión de La CalidadCeline_1980Încă nu există evaluări
- Curso Formacion en Norma 15189 JUNIO PERUDocument238 paginiCurso Formacion en Norma 15189 JUNIO PERUedwin0% (1)
- 21PPL13-V1 Matriz Interrelacion HSEQDocument16 pagini21PPL13-V1 Matriz Interrelacion HSEQJack MorrizonÎncă nu există evaluări
- NTP Iso 17034Document53 paginiNTP Iso 17034Rmatos MayaÎncă nu există evaluări
- Iso 15189Document21 paginiIso 15189jose antonio tafur gonzalesÎncă nu există evaluări
- SMETA 6.1 BPG Spanish VersionDocument92 paginiSMETA 6.1 BPG Spanish VersionMarcelo del Valle100% (4)
- Contexto de La OrganizacionDocument13 paginiContexto de La OrganizacionMar Diaz100% (3)
- Introduccion A La Norma ISO9001-2015Document47 paginiIntroduccion A La Norma ISO9001-2015Melvin RiveraÎncă nu există evaluări
- Sistemas de Gestion Calidad-1Document21 paginiSistemas de Gestion Calidad-1Katherine FercorÎncă nu există evaluări
- Diagnostic oDocument146 paginiDiagnostic oErvin Omar Lizcano PrietoÎncă nu există evaluări
- ISO 9001 Auditor InternoDocument48 paginiISO 9001 Auditor InternoAdriana Parra100% (1)
- Mapa Conceptual Normas ISO 9001 2015Document1 paginăMapa Conceptual Normas ISO 9001 2015Angel HerreraÎncă nu există evaluări
- Comparacion Iso 9001 - Iso 14001 - Ohsa 18001Document1 paginăComparacion Iso 9001 - Iso 14001 - Ohsa 18001Francisco Vasquez AbarcaÎncă nu există evaluări
- 4.4 Sistema de Gestion de Los ProcesosDocument19 pagini4.4 Sistema de Gestion de Los ProcesosJUAN CAMILO RODRÍGUEZ GONZÁLEZÎncă nu există evaluări
- U3-1 Fiq - Norma Iso 9001Document9 paginiU3-1 Fiq - Norma Iso 9001miri-256Încă nu există evaluări
- Introduccion 17020Document27 paginiIntroduccion 17020maritzaÎncă nu există evaluări
- Matriz de Relacion de Iso&ntpDocument299 paginiMatriz de Relacion de Iso&ntpCarmenÎncă nu există evaluări
- 9 MejoraDocument11 pagini9 MejoraMiguel Marcelo Torres EcheverríaÎncă nu există evaluări
- Charla Introduccón A ISODocument13 paginiCharla Introduccón A ISOgabrielamcolaceÎncă nu există evaluări
- Actividad 3 Estructura NTC 17025 - 2017Document1 paginăActividad 3 Estructura NTC 17025 - 2017andrearojasÎncă nu există evaluări
- Core Tools PDFDocument72 paginiCore Tools PDFGuilherme AlcantaraÎncă nu există evaluări
- TALLER ISO 9001 - DEBE - Hoja1Document1 paginăTALLER ISO 9001 - DEBE - Hoja1LADY MARIAM PAGUAY CHOEZÎncă nu există evaluări
- Cambios - Transición de ISO 17025 2005 To 2017Document9 paginiCambios - Transición de ISO 17025 2005 To 2017jorge ZárateÎncă nu există evaluări
- FAI HSEQ 1 de 5Document19 paginiFAI HSEQ 1 de 5Juan Pablo Barrera VargasÎncă nu există evaluări
- Numerales Integrados de ISODocument3 paginiNumerales Integrados de ISOalvaro monteroÎncă nu există evaluări
- NCh-ISO - IEC 17025 - 2017 Laboratorio de Ensayo y Calibración. AnálisisDocument2 paginiNCh-ISO - IEC 17025 - 2017 Laboratorio de Ensayo y Calibración. AnálisisOscar Sanhueza100% (1)
- Ciclo PhvaDocument1 paginăCiclo PhvaGuaxxon92Încă nu există evaluări
- Arom-F032 Plan de Auditoria InternasDocument5 paginiArom-F032 Plan de Auditoria InternasEsthalyn Pablo Nuñez PradaÎncă nu există evaluări
- Anexo A Matriz de Correspondencia Entre SirDocument2 paginiAnexo A Matriz de Correspondencia Entre SirDanny DiazÎncă nu există evaluări
- Diseño Estructural PDFDocument2 paginiDiseño Estructural PDFFernando RosalesÎncă nu există evaluări
- PDFDocument2 paginiPDFFernando RosalesÎncă nu există evaluări
- Hoja RutaDocument6 paginiHoja RutaFernando RosalesÎncă nu există evaluări
- NMX-C-265-1984 Agregados para Concreto-Examen Petrogr-FicoDocument19 paginiNMX-C-265-1984 Agregados para Concreto-Examen Petrogr-FicoFernando RosalesÎncă nu există evaluări
- Crónicas de Una Muerte Anunciada - ResumenDocument3 paginiCrónicas de Una Muerte Anunciada - ResumenFernando RosalesÎncă nu există evaluări
- Planta Pamolsa-Ubicación 3 Consultorias FINAL REALDocument1 paginăPlanta Pamolsa-Ubicación 3 Consultorias FINAL REALFernando RosalesÎncă nu există evaluări
- ExpeDocument47 paginiExpeFernando RosalesÎncă nu există evaluări
- Outsourcing de TI en PerúDocument8 paginiOutsourcing de TI en PerúBakuryu MoleÎncă nu există evaluări
- Capitulo 10 Bovedas de Hormigon en Masa Hasta 40 Metros de LuzDocument16 paginiCapitulo 10 Bovedas de Hormigon en Masa Hasta 40 Metros de LuzRoberto AlvaradoÎncă nu există evaluări
- Gobierno Regional de Ica Gobierno Regional de Ica Gobierno Regional de Ica Gobierno Regional de IcaDocument143 paginiGobierno Regional de Ica Gobierno Regional de Ica Gobierno Regional de Ica Gobierno Regional de IcaKore Zitow Pa Laz WapazÎncă nu există evaluări
- Análisis e Ingeniería de RequerimientosDocument16 paginiAnálisis e Ingeniería de RequerimientosSteven RivadeneiraÎncă nu există evaluări
- Aplanadora, Rodillo, Tractor OrugasDocument33 paginiAplanadora, Rodillo, Tractor OrugasTanya YoungÎncă nu există evaluări
- Ficha Tecnica HidanteDocument6 paginiFicha Tecnica Hidantejasan33Încă nu există evaluări
- 15 Entrepisos MaderaDocument51 pagini15 Entrepisos MaderaFonchi Pterodactilo Volador100% (1)
- Procedimiento Manejo y Transporte Manual CargaDocument10 paginiProcedimiento Manejo y Transporte Manual CargaElkin BarriosÎncă nu există evaluări
- Las Competencias Clave de La Administración de La Cadena de SuministroDocument30 paginiLas Competencias Clave de La Administración de La Cadena de SuministroMario Obando CazorlaÎncă nu există evaluări
- Anuncios Emergencia PlaneadaDocument4 paginiAnuncios Emergencia PlaneadaLuis Angel Hernandez DiazÎncă nu există evaluări
- Proyecto MercadotecniaDocument12 paginiProyecto MercadotecniaCesar ChoyÎncă nu există evaluări
- Problemas de InventariosDocument5 paginiProblemas de InventariosJosue Candelario MuñozÎncă nu există evaluări
- Gerencia InformaticaDocument16 paginiGerencia InformaticaAnonymous 6Hynbb0IHTÎncă nu există evaluări
- El Circuito Paralelo y Nuestro Lienzo CanvasDocument5 paginiEl Circuito Paralelo y Nuestro Lienzo CanvasCiani Braham MARTINEZ RIVERAÎncă nu există evaluări
- Campanas Teka InstalacionDocument22 paginiCampanas Teka Instalacionred_oscura100% (1)
- Trabajo de InvestigacionDocument11 paginiTrabajo de InvestigacionAna Paula Gaitan100% (1)
- Manual de Instalacion Hule Piso Tachon de Caucho en RolloDocument2 paginiManual de Instalacion Hule Piso Tachon de Caucho en RolloGalicus Sucio Marvel ContestÎncă nu există evaluări
- Proyecto Life. Plan de Gestión de Residuos en Las Obras de Construcción y Demolición - ITeC - 2000Document89 paginiProyecto Life. Plan de Gestión de Residuos en Las Obras de Construcción y Demolición - ITeC - 2000ilobo24Încă nu există evaluări
- f44039120 Lista de Precios Mayo 2012Document1 paginăf44039120 Lista de Precios Mayo 2012andres silvestreÎncă nu există evaluări
- Instrumentos de Laboratorio de BiologíaDocument21 paginiInstrumentos de Laboratorio de BiologíaMariaElizabeth14Încă nu există evaluări
- Catalogo Ventilacion Industrial Curiel PDFDocument31 paginiCatalogo Ventilacion Industrial Curiel PDFMaría Alejandra Fernández ÁvilaÎncă nu există evaluări
- Formato Ficha TecnicaDocument2 paginiFormato Ficha Tecnicacedu126Încă nu există evaluări
- 03 Especificaciones IE El RecuerdoDocument493 pagini03 Especificaciones IE El Recuerdoanon_615179342100% (1)
- Catalogo GC Cocesa 2013 Interior BajaDocument168 paginiCatalogo GC Cocesa 2013 Interior BajaCristian CamposÎncă nu există evaluări
- Carga ProyectoDocument17 paginiCarga ProyectoFabian Roa EÎncă nu există evaluări
- Sistema de Gestion de La Seguridad de La InformacionDocument4 paginiSistema de Gestion de La Seguridad de La InformacionSaraÎncă nu există evaluări
- Orden Servicio TecnicoDocument2 paginiOrden Servicio Tecnicoaudicon201150% (4)
- TAREA 8 PCP 2 Ejercicios KrawjeskyDocument10 paginiTAREA 8 PCP 2 Ejercicios KrawjeskyGeordyn cuadra0% (1)
- Drenaje Subsuperficial o SubterraneoDocument12 paginiDrenaje Subsuperficial o SubterraneoJuan LlanoÎncă nu există evaluări
- Formato PNI-proceso de RemachadoDocument2 paginiFormato PNI-proceso de RemachadoAlex GonzalezÎncă nu există evaluări