Documente Academic
Documente Profesional
Documente Cultură
Fase 3 - Grupo - 212065A - 611 PDF
Încărcat de
jeisson castellanosTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Fase 3 - Grupo - 212065A - 611 PDF
Încărcat de
jeisson castellanosDrepturi de autor:
Formate disponibile
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
TAREA 2. PROPIEDADES DE LAS SUSTANCIAS PURAS Y PRIMERA LEY
DE LA TERMODINÁMICA
PRESENTADO POR
MARIA NIEVES ROSAS
LUISA FERNANDA MORALES VALERO
JEISSON ESNEIDER CASTELLANOS
JEISSON FABIAN PATIÑO
JENNY ALEJANDRA PICO MORA
PRESENTADO A
YURY MARLEN PERALTA
GRUPO
212065A_611
ABRIL DE 2019
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Paso 1
Cada estudiante debe dar solución individual a las 5 preguntas que se listan a continuación
y para ello se recomienda revisar las siguientes referencias bibliográficas que se
encuentran en el entorno de conocimiento.
NOMBRE ESTUDIANTE 1: MARIA NIEVES ROSAS
NOMBRE ESTUDIANTE 2: LUISA FERNANDA MORALES VALERO
Proceso adiabático: Proceso termodinámico en el que el sistema no
intercambia calor con su entorno.
Proceso isotérmico: Es un proceso mediante el cual la temperatura T
permanece constante.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Problema 1 Proceso isobárico: Proceso en el cual la presión P se mantiene
Procesos constante.
Proceso isocórico: Es aquel en donde el volumen especifico V
permanece constante.
Primera Ley de la termodinámica: Conocida también como el
principio de conservación de la energía, brinda unas bases para
estudiar las relaciones entre las diversas formas de interacción de
energía.
La energía no se puede crear ni destruir durante un proceso, solo
puede cambiar de forma.
Por lo tanto, cada cantidad de energía por pequeña que sea debe
justificarse durante un proceso.
La ley no hace referencia al valor de la energía total de un sistema
cerrado en un estado, solo establece que el cambio de energía total
durante un proceso adiabático debe ser igual al trabajo neto realizado.
Problema 2.
Balance de energía de un sistema: Principio de conservación de la
Que dice la ley energía: El cambio neto (incremento o disminución) en la energía total
primera de la del sistema durante un proceso es igual a la diferencia de la energía total
termodinámica: que entra y la energía total que sale del sistema durante el proceso.
(Energía total que entra al sistema) - (Energía total que sale del
sistema) = (Cambio en la energía total del sistema).
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Esta relacion es aplicable a cualquier tipo de sistema que experimenta
cualquier clase de proceso.
Para determinar el cambio de energia de un sistema durante un proceso,
sew requiere evaluar la energia del sistema al principio y al final del
proceso y encontrar su diferencia.
(Cambio de energia) = (Energia en el estado final) – (Energia en el
estado inicial).
El cambio en la energia total del sistema durante un proceso, e sla
suma de los cambios de sus energias interna, cinetica y potencial:
Liquido comprimido
En estas condiciones el agua existe en fase
liquida y se denomina liquido comprimido o
liquido sub-enfriado, lo que significa que NO
está a punto de evaporarse. Se transfiere calor
al agua hasta aumentar su temperatura y a
medida que aumenta la temperatura, el agua
líquida se expande un poco y por consiguiente
aumenta su volumen especifico. Debido a esta
expansión, el embolo sube. La presión en el
cilindro permanece constante en 1 atm durante
el proceso porque depende de la presión
barométrica externa y el peso del embolo que
son constantes. El agua sigue siendo liquido
comprimiendo ya que no ha iniciado a
comprimirse.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Problema 3
Líquido saturado
Conforme se transfiere más calor, la
temperatura aumenta hasta alcanzar 100°C.
Punto en el que el agua aún permanece
liquida, pero cualquier adición de calor hace
que se vaporice algo de agua, es decir, está a
punto de presentarse un cambio de proceso de
fase líquido a vapor.
Liquido saturado: Líquido que está a punto
de evaporarse.
Vapor saturado
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Conforme continua la trasferencia de
calor, el proceso de evaporación
continuara hasta evaporarse la última
gota de líquido. En ese punto el
cilindro está lleno de vapor, el cual se
halla en el borde de la fase liquida.
Cualquier cantidad de calor que pierda
este vapor hará que se condense.
Vapor saturado: Vapor que está a
punto de condensarse.
Vapor sobrecalentado
Una vez completado el proceso de cambio
de fase termina y se alcanza una región de
una sola fase (esta vez vapor). En este
punto, transferir más calor da como
aumento un resultado de temperatura y de
volumen especifico. En la imagen
notamos que el vapor es de 300°C, si se
transfiere algo de calor del vapor, la
temperatura descendería un poco pero no
habría condensación mientras la
temperatura permanezca arriba de 100°C
para (P=1 atm).
Vapor sobrecalentado: Vapor que no
está a punto de condensarse.
Calor específico
Energía requerida para elevar en un grado la temperatura de una unidad
de masa de una sustancia. Esta energía depende de cómo se ejecute el
Problema 4 proceso.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Calor especifico a volumen constante 𝑐𝑣 : Energia requerida para
elevar en un grado la temperatura de una unidad de masa de una
sustancia cuando el volumen se mantiene constante.
Calor especifico a presión constante𝑐𝑝 : La energía requerida para
hacer lo mismo cuando se mantiene constante la presión es el calor
especifico a presión constantes siempre mayor que el volumen constante
porque a presión constante se permite que el sistema se expanda y la
energía para este trabajo de expansión, también debe ser suministrada al
sistema.
El calor especifico de una sustancia cambia con la temperatura.
calor latente
Energía requerida por una cantidad de sustancia para cambiar de fase,
de sólido a líquido (calor de fusión) o de líquido a gaseoso (calor de
vaporización). Se debe tener en cuenta que esta energía en forma de calor
se invierte para el cambio de fase y no para un aumento de la
temperatura; por tanto, al cambiar de gaseoso a líquido y de líquido a
sólido se libera la misma cantidad de energía.
Entalpía:
La Entalpía es la cantidad de energía de un sistema termodinámico que
puede intercambiar con su entorno. Entalpía H es igual a U + Pv, donde
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
U es la energía interna, p es la presión y V es el volumen. H se mide en
julios.
H = U + Pv
Cuando un sistema pasa desde unas condiciones iniciales hasta otras
finales, se mide el cambio de entalpía (ΔH).
ΔH = Hf – Hi
Entalpia + ecuación de un gas ideal:
𝐻 = 𝑢 + 𝑃𝑣
} ℎ 0 𝑢 + 𝑅𝑇
𝑃𝑣 = 𝑅𝑇
Se deduce que la entalpia de un gas ideal es también solo una función de
la temperatura.
H=h (T)
Energía interna
Es una función de la temperatura solamente y no de la presión o del
volumen especifico
(U) magnitud que designa la energía almacenada por un sistema de
partículas. Es el resultado de la contribución de la energía cinética de las
moléculas o átomos que lo constituyen, de sus energías de rotación,
traslación y vibración, además de la energía potencial intermolecular
debido a las fuerzas de tipo gravitatorio, electromagnético y nuclear.
Tanto la energía interna como la entalpia de una sustancia, se puede
modificar mediante la trasferencia de energía en cualquier forma, con el
calor como una de las posibles formas de ellas.
Problema 5 A V constante: ΔU=Q
Expresión de la A P constante: Wsistema=−p⋅ΔV ó Wsistema=p⋅ΔV
primera ley
A T constante: ΔU=0
Proceso adiabático: Es aquel en el cual el sistema termodinámico no
intercambia calor con su entorno.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Proceso isotérmico: Es aquel proceso durante el cual la temperatura
permanece constante.
Proceso isobárico: Es aquel proceso durante el cual la presión se
mantiene constante.
Proceso isocórico: Es aquel proceso durante el cual el volumen
especifico se mantiene constante.
Que dice la ley primera de la termodinámica: Establece que la
energía no se puede crear ni destruir durante un proceso; solo puede
cambiar de forma. Por lo tanto toda cantidad de energía por
pequeña que sea, debe justificarse durante un proceso.
Balance de energía de un sistema: El principio de conservación de
energía se expresa: el cambio neto (incremento o disminución) en la
energía total del sistema durante un proceso es igual a la diferencia
entre la energía total que entra y la energía total que sale del sistema
durante el proceso.
Qué es liquido comprimido: Es un liquido que se encuentra lejos de
evaporarse por encontrarse a una temperatura que permite
mantenerse en su estado inicial.
Qué es liquido saturado: Es un liquido que esta a punto de evaporase
Qué es vapor saturado: Es un vapor que esta a punto de
condensarse.
Qué es vapor sobrecalentado: Es un vapor que no esta a punto de
condensarse y que no es saturado al encontrarse a una temperatura
muy lejana de su punto de condensación.
Qué es calor específico: Se define como la energía requerida para
elevar en un grado la temperatura de una unidad de masa de una
sustancia.
Qué es calor latente: Es la cantidad de calor por unidad de masa
necesaria para realizar el cambio de estado. Su unidad de medida
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
en el Sistema Internacional es el julio por kilogramo ( J/kg ) aunque
también se suele usar la caloría por gramo ( cal/g )
Qué es entalpía: Es una magnitud que define el flujo de energía
térmica en los procesos químicos efectuados a presión constante
cuando el único trabajo es de presión-volumen
Qué es energía interna: Es una caracterización macroscópica de la
energía microscópica de todas las partículas que lo componen. Un
sistema está formado por gran cantidad de partículas en
movimiento. Cada una de ellas posee energía cinética, potencial
gravitacional y potencial elástica. En definitiva, en el interior de un
sistema conviven distintos tipos de energía, asociadas a las
partículas microscópicas que los componen y que forman su energía
interna.
A V constante: ΔU=Q
A P constante: Wsistema=−p⋅ΔV
A T constante: ΔU=0
NOMBRE ESTUDIANTE 1: JEISSON ESNEIDER CASTELLANOS NIETO
Problema 1 Proceso adiabático: Es aquel en el cual el sistema termodinámico no
intercambia calor con su entorno.
Proceso isotérmico: Es aquel proceso durante el cual la temperatura
permanece constante.
Proceso isobárico: Es aquel proceso durante el cual la presión se
mantiene constante.
Proceso isocórico: Es aquel proceso durante el cual el volumen
especifico se mantiene constante.
Problema 2 Que dice la ley primera de la termodinámica: Establece que la
energía no se puede crear ni destruir durante un proceso; solo puede
cambiar de forma. Por lo tanto toda cantidad de energía por pequeña
que sea, debe justificarse durante un proceso.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Balance de energía de un sistema: El principio de conservación de
energía se expresa: el cambio neto (incremento o disminución) en la
energía total del sistema durante un proceso es igual a la diferencia
entre la energía total que entra y la energía total que sale del sistema
durante el proceso.
Problema 3 Qué es liquido comprimido: Es un liquido que se encuentra lejos de
evaporarse por encontrarse a una temperatura que permite mantenerse
en su estado inicial.
Qué es liquido saturado: Es un liquido que esta a punto de evaporase
Qué es vapor saturado: Es un vapor que esta a punto de condensarse.
Qué es vapor sobrecalentado: Es un vapor que no esta a punto de
condensarse y que no es saturado al encontrarse a una temperatura muy
lejana de su punto de condensación.
Problema 4 Qué es calor específico: Se define como la energía requerida para
elevar en un grado la temperatura de una unidad de masa de una
sustancia.
Qué es calor latente: Es la cantidad de calor por unidad de masa
necesaria para realizar el cambio de estado. Su unidad de medida en el
Sistema Internacional es el julio por kilogramo ( J/kg ) aunque también
se suele usar la caloría por gramo ( cal/g )
Qué es entalpía: Es una magnitud que define el flujo de energía
térmica en los procesos químicos efectuados a presión constante
cuando el único trabajo es de presión-volumen
Qué es energía interna: Es una caracterización macroscópica de la
energía microscópica de todas las partículas que lo componen. Un
sistema está formado por gran cantidad de partículas en movimiento.
Cada una de ellas posee energía cinética, potencial gravitacional y
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
potencial elástica. En definitiva, en el interior de un sistema conviven
distintos tipos de energía, asociadas a las partículas microscópicas que
los componen y que forman su energía interna.
Problema 5 A V constante: ΔU=Q
Expresión de la A P constante: Wsistema=−p⋅ΔV
primera ley
A T constante: ΔU=0
NOMBRE ESTUDIANTE 5: JEISON FABIAN PATIÑO
Problema 1 Proceso adiabático: Se le llama proceso adiabático cuando un sistema no
pierde ni gana calor, en otras palabras se considera proceso adiabático a
un sistema especial en el cual no se pierde ni tampoco se gana energía
calorífica. El término adiabático hace referencia a elementos que impiden
la transferencia de calor con el entorno. Un proceso adiabático que es
además reversible se conoce como proceso isentrópico.
Proceso isotérmico: El proceso isotérmico es el proceso de compresión
mediante el cual la temperatura se mantiene constante pero el volumen y
la presión varían. Se denomina proceso isotérmico al cambio de
temperatura reversible en un sistema termodinámico, siendo dicho cambio
de temperatura constante en todo el sistema.
Proceso isobárico: Proceso durante el cual la presión se mantiene
constante.
Proceso isocórico: Un proceso isocórico, también llamado proceso
isométrico o isovolumétrico es un proceso termodinámico en el cual el
volumen permanece constante; ΔV = 0. Esto implica que el proceso no
realiza trabajo.
Problema 2 Que dice la ley primera de la termodinámica: La energía no se puede
crear ni destruir durante un proceso; sólo puede cambiar de forma. Por lo
tanto, cada cantidad de energía por pequeña que sea debe justificarse
durante un proceso.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Balance de energía de un sistema: El principio de conservación de la
energía: se expresa como: el cambio neto (aumento o disminución) de la
energía total del sistema durante un proceso es igual a la diferencia entre
la energía total que entra y la energía total que sale del sistema durante el
proceso. Es decir,
Problema 3 Qué es líquido comprimido: El líquido comprimido (también llamado
subenfriado) es aquel que no está a punto de vaporizarse.
Qué es liquido saturado: Es aquel que está a punto de vaporizarse.
Cualquier adición de calor causará que alguna parte del líquido se
vaporice.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Qué es vapor saturado: El vapor saturado es aquel vapor que está apunto
de condensarse. Es decir cualquier pérdida de calor de este vapor causará
que alguna parte se condense.
Qué es vapor sobrecalentado: El vapor sobrecalentado es aquel vapor
que no está apunto de condensarse.
Problema 4 Qué es calor específico: Se define como la energía requerida para elevar
en un grado la temperatura de una unidad de masa de una sustancia.
Qué es calor latente: Es la cantidad de calor por unidad de masa necesaria
para realizar el cambio de estado. Su unidad de medida en el Sistema
Internacional es el julio por kilogramo ( J/kg ) aunque también se suele
usar la caloría por gramo ( cal/g )
Qué es entalpía: La Entalpía es la cantidad de energía de
un sistema termodinámico que puede intercambiar con su entorno.
Entalpía H es igual a U + Pv, donde U es la energía interna, p es la presión
y V es el volumen. H se mide en julios.
H = U + Pv
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Cuando un sistema pasa desde unas condiciones iniciales hasta otras
finales, se mide el cambio de entalpía (ΔH).
ΔH = Hf – Hi
Entalpia + ecuación de un gas ideal:
𝐻 = 𝑢 + 𝑃𝑣
} ℎ 0 𝑢 + 𝑅𝑇
𝑃𝑣 = 𝑅𝑇
Se deduce que la entalpia de un gas ideal es también solo una función de
la temperatura.
H=h (T)
Qué es energía interna: Es una caracterización macroscópica de la
energía microscópica de todas las partículas que lo componen. Un sistema
está formado por gran cantidad de partículas en movimiento. Cada una de
ellas posee energía cinética, potencial gravitacional y potencial elástica.
En definitiva, en el interior de un sistema conviven distintos tipos de
energía, asociadas a las partículas microscópicas que los componen y que
forman su energía interna.
Problema 5 A V constante: ΔU=Q
Expresión de la A P constante: Wsistema=−p⋅ΔV
primera ley
A T constante: ΔU=0
NOMBRE ESTUDIANTE 5: JENNY ALEJANDRA PICO MORA
Problema 1 Proceso adiabático: El término adiabático hace referencia a volúmenes
que impiden la transferencia de calor con el entorno. Una pared aislada se
aproxima bastante a un límite adiabático. Otro ejemplo es la temperatura
adiabática de llama, que es la temperatura que podría alcanzar una llama
si no hubiera pérdida de calor hacia el entorno. En climatización los
procesos de humectación (aporte de vapor de agua) son adiabáticos,
puesto que no hay transferencia de calor, a pesar que se consiga variar la
temperatura del aire y su humedad relativa. Se le llama proceso adiabático
cuando un sistema no pierde ni gana calor, en otras palabras se considera
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
proceso adiabático a un sistema especial en el cual no se pierde ni tampoco
se gana energía calorífica.
Proceso isotérmico: Se denomina proceso isotérmico o proceso isotermo
al cambio reversible en un sistema termodinámico, siendo dicho cambio a
temperatura constante en todo el sistema. También es el proceso es el
proceso de compresión mediante el cual la temperatura se mantiene
constante pero el volumen y la presión varían. Se denomina proceso
isotérmico al cambio de temperatura reversible en un sistema
termodinámico, siendo dicho cambio de temperatura constante en todo el
sistema.
Proceso isobárico: Un proceso isobárico es un proceso termodinámico
que ocurre a presión constante. La primera ley de la termodinámica, para
este caso, queda expresada como sigue: Donde: = Calor transferido. =
Energía interna. = Presión. = Volumen. En un diagrama P-V, un proceso
isobárico aparece como una línea horizontal. Proceso durante el cual la
presión se mantiene constante.
Proceso isocórico: Un proceso isocórico, también llamado proceso
isomen permanece constante; Esto implica que el proceso no
realiza trabajo presión-volumen, ya que éste se define como: donde P es
la presión el trabajo es cero pues no hay cambio de volumen En un
diagrama P-V, un proceso isocórico aparece como una línea
verticalétrico o isovolumétrico es un proceso termodinámico en el cual el
volumen Un proceso isocórico, también llamado proceso isométrico o
isovolumétrico es un proceso termodinámico en el cual el volumen
permanece constante; ΔV = 0. Esto implica que el proceso no realiza
trabajo.
Problema 2 Que dice la ley primera de la termodinámica: La energía no se puede
crear ni destruir durante un proceso; sólo puede cambiar de forma. Por lo
tanto, cada cantidad de energía por pequeña que sea debe justificarse
durante un proceso.
Balance de energía de un sistema: El principio de conservación de la
energía: se expresa como: el cambio neto (aumento o disminución) de la
energía total del sistema durante un proceso es igual a la diferencia entre
la energía total que entra y la energía total que sale del sistema durante el
proceso. Es decir,
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Problema 3 Qué es líquido comprimido: también llamado subenfriado es
aquel que no está a punto de vaporizarse. Son estados que se encuentran
en medio de los estados de líquido saturado y vapor saturado para una
temperatura y presión de saturación de una sustancia pura.
Qué es liquido saturado: Es aquel que está a punto de vaporizarse.
Cualquier adición de calor causará que alguna parte del líquido se
vaporice.
Qué es vapor saturado: El vapor saturado es aquel vapor que está apunto
de condensarse. Es decir cualquier pérdida de calor de este vapor causará
que alguna parte se condense.
Qué es vapor sobrecalentado: El vapor sobrecalentado es aquel vapor
que no está apunto de condensarse.
Problema 4 Qué es calor específico: Se define como la energía requerida para elevar
en un grado la temperatura de una unidad de masa de una sustancia.
Qué es calor latente: Es la cantidad de calor por unidad de masa necesaria
para realizar el cambio de estado. Su unidad de medida en el Sistema
Internacional es el julio por kilogramo ( J/kg ) aunque también se suele
usar la caloría por gramo ( cal/g )
Qué es entalpía: La Entalpía es la cantidad de energía de
un sistema termodinámico que puede intercambiar con su entorno.
Entalpía H es igual a U + Pv, donde U es la energía interna, p es la presión
y V es el volumen. H se mide en julios.H = U + Pv
Cuando un sistema pasa desde unas condiciones iniciales hasta otras
finales, se mide el cambio de entalpía (ΔH).ΔH = Hf – Hi
Se deduce que la entalpia de un gas ideal es también solo una función de
la temperatura. H=h (T)
Qué es energía interna: Es Un sistema está formado por gran cantidad
de partículas en movimiento. Cada una de ellas posee energía cinética,
potencial gravitacional y potencial elástica. En definitiva, en el interior de
un sistema conviven distintos tipos de energía, asociadas a las partículas
microscópicas que los componen y que forman su energía interna.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Problema 5 A V constante: ΔU=Q
Expresión de la A P constante: Wsistema=−p⋅ΔV
primera ley
A T constante: ΔU=0
Paso 2
1. Emplear tablas de vapor para encontrar las propiedades indicadas. Ingresar a
https://edoc.site/tablas-termodinamicas-cengel-pdf-free.html (apéndice 2)
NOMBRE ESTUDIANTE 2: LUISA FERNANDA MORALES VALERO
335Kpa
1. Un cilindro rígido contiene 6 Kg de líquido y 3 kg de vapor de agua a la
temperatura indicada, determine:
a. La calidad del sistema
𝑚𝑔 3 3
𝑥= = = = 0,33
𝑚𝑡 6 + 3 9
b. La Temperatura a la cual coexiste el equilibrio en °C
Como las dos fases coexisten en equilibrio, se tiene un vapor húmedo y la temperatura
debe ser la de saturación a la presión dada (335kPa), de la tabla de presiones para
agua saturada, interpolamos para el valor de presión dado y obtenemos:
𝑇1 − 𝑇0 138,86 − 136,27
𝑇 = 𝑇0 + (𝑃 − 𝑃0 ) = 136,27 + (335 − 325) = 137,31°𝐶
𝑃1 − 𝑃0 350 − 325
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
c. Volumen especifico m3/kg, energía interna kJ/kg y entalpía promedio en kJ/kg
Interpolamos los valores de volúmenes especifico, energía interna y entalpia, para liquido
y vapor saturado, a la presión dada:
Volumen especifico Energia interna Entalpia
Presión
Temp. Sat. liq sat vap sat liq sat evap vap sat liq sat evap vap sat
kPa °C m3/kg kJ/kg kJ/kg
325 136,27 0,001076 0,56199 572,84 1973,1 2445,9 573,19 2155,4 2727,6
335 137,31 0,001077 0,54688 577,26 1969,7 2486,9 577,62 2152,3 2729,4
350 138,86 0,001079 0,52422 583,89 1964,6 2548,5 584,26 2147,7 2732,0
d. Volumen de líquido, volumen de vapor y volumen total del recipiente en m3
𝑉𝑙 = 𝑚𝑙 ∗ 𝑣𝑙 = 6 ∗ 0,001077 = 0,006462 𝑚 3
𝑉𝑔 = 𝑚𝑔 ∗ 𝑣𝑔 = 3 ∗ 0,54688 = 1,64064 𝑚 3
𝑉 = 𝑉𝑙 + 𝑉𝑔 = 0,006462 + 1,64064 = 1,647102 𝑚 3
ESTUDIANTE 3 JEISSON ESNEIDER CASTELLANOS NIETO
340 kPa
Un cilindro rígido contiene 6 Kg de líquido y 3 kg de vapor de agua a la temperatura
indicada, determine:
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
a. La calidad del sistema
𝑚𝑣𝑎𝑝𝑜𝑟
𝑥=
𝑚𝑡𝑜𝑡𝑎𝑙
3
𝑥=
9
𝑥 = 0.33
b. La Temperatura a la cual coexiste el equilibrio en °C
Tenemos que la temperatura a 340 kPa corresponde a 280 ºF, por tal motivo
convertimos a ºC.
c. Volumen especifico m3/kg, energía interna kJ/kg y entalpía promedio en kJ/kg
0.0172 𝑓𝑡 3 0.0283 𝑚 3 1 𝑙𝑏𝑚 0.0004867 𝑚3
𝑣𝑓 = ∗ ∗ = = 0.00107
1 𝑙𝑏𝑚 1𝑓𝑡 3 0.4535 𝑘𝑔 0.4535 𝑘𝑔
8.6439 𝑓𝑡 3 0.0283 𝑚 3 1 𝑙𝑏𝑚 0.2446 𝑚3
𝑣𝑔 = ∗ ∗ = = 0.5394
1 𝑙𝑏𝑚 1𝑓𝑡 3 0.4535 𝑘𝑔 0.4535 𝑘𝑔
249.04 𝐵𝑡𝑢 1.055 𝑘𝐽 1 𝑙𝑏𝑚 262.73 𝑘𝐽
𝑢𝑓 = ∗ ∗ = = 579.33
1 𝑙𝑏𝑚 1𝐵𝑡𝑢 0.4535 𝑘𝑔 0.4535 𝑘𝑔
𝑘𝐽
𝑢𝑓 = 579.33 ∗ 6 𝑘𝑔
𝑘𝑔
𝑢𝑓 = 3475.98 𝑘𝐽
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
1095.2 𝐵𝑡𝑢 1.055 𝑘𝐽 1 𝑙𝑏𝑚 1155.43 𝑘𝐽
𝑢𝑔 = ∗ ∗ = = 2547.8
1 𝑙𝑏𝑚 1𝐵𝑡𝑢 0.4535 𝑘𝑔 0.4535 𝑘𝑔
𝑘𝐽
𝑢𝑔 = 2547.8 ∗ 3 𝑘𝑔
𝑘𝑔
𝑢𝑔 = 7643.4 𝑘𝐽
𝑢 = 𝑢𝑓 + 𝑢𝑔
𝑢 = 3475.98 + 7643.4
𝑢 = 11119.38 𝑘𝐽
249.2 𝐵𝑡𝑢 1.055 𝑘𝐽 1 𝑙𝑏𝑚 262.9 𝑘𝐽
ℎ𝑓 = ∗ ∗ = = 595.14
1 𝑙𝑏𝑚 1𝐵𝑡𝑢 0.4535 𝑘𝑔 0.4535 𝑘𝑔
𝑘𝐽
ℎ𝑓 = 595.14
𝑘𝑔
924.74 𝐵𝑡𝑢 1.055 𝑘𝐽 1 𝑙𝑏𝑚 975.6 𝑘𝐽
ℎ𝑓𝑔 = ∗ ∗ = = 2151.26
1 𝑙𝑏𝑚 1𝐵𝑡𝑢 0.4535 𝑘𝑔 0.4535 𝑘𝑔
𝑘𝐽
ℎ𝑓𝑔 = 2151.26
𝑘𝑔
ℎ𝑝𝑟𝑜𝑚 = ℎ𝑓 + 𝑥ℎ𝑓𝑔
ℎ𝑝𝑟𝑜𝑚 = 595.14 + (0.33)(2151.26)
𝑘𝐽
ℎ𝑝𝑟𝑜𝑚 = 1305.01
𝑘𝑔
d. Volumen de líquido, volumen de vapor y volumen total del recipiente en m 3
𝑚3
𝑣𝑓 = 0.00107 ∗ 6 𝑘𝑔
𝑘𝑔
𝑣𝑓 = 0.00643 𝑚 3
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑚3
𝑣𝑔 = 0.5394 ∗ 3 𝑘𝑔
𝑘𝑔
𝑣𝑔 = 1.6182 𝑚 3
𝑣 = 𝑣𝑓 + 𝑣𝑔
𝑣 = 0.00643 + 1.6182
𝑣 = 1.62463 𝑚 3
ESTUDIANTE 5 JEISSON FABIAN PATIÑO
350 kPa
TOMANDO LA TABLA DEL A5 del libro de cengen y dada una presión de 350Kpa
Un cilindro rígido contiene 6 Kg de líquido y 3 kg de vapor de agua a la temperatura
indicada, determine:
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
a. La calidad del sistema
𝑚𝑣𝑎𝑝𝑜𝑟
𝑥=
𝑚𝑡𝑜𝑡𝑎𝑙
𝑚𝑣𝑎𝑝𝑜𝑟
𝑥=
𝑚𝑙𝑖𝑞 + 𝑚𝑣𝑎𝑝𝑜𝑟
6
𝑥=
9
𝑥 = 0.6666
b. La Temperatura a la cual coexiste el equilibrio en °C
Para una presión de 350Kpa y X=0.6666 y basados en la tabla del apéndice A5 se
pueden observar los valores de la temperatura equivalente a 138.36ºC, también se
pueden calcular los valores entalpias, volúmenes específicos y energías internas en
fase líquido y gas
T=138.36ºC
c. Volumen especifico m3/kg, energía interna kJ/kg y entalpía promedio en kJ/kg
Con P=350 KPa.; X=0.6666; T=138.36ºC
𝑣𝑓 = 0.001079𝑚 3 /𝐾𝑔
𝑣𝑔 = 0.52422𝑚 3 /𝐾𝑔
𝑢𝑓 = 583,89𝑘𝐽/𝐾𝑔
𝑢𝑔 = 2548.5𝑘𝐽/𝐾𝑔
ℎ𝑓 = 584.26𝑘𝐽/𝐾𝑔
ℎ𝑔 = 2732.0𝑘𝐽/𝐾𝑔
𝑣 = 𝑣𝑓 + 𝑋 ∗ (𝑣𝑔 − 𝑣𝑓 )
𝑚3 𝑚3
𝑣 = 0.001079 𝑚 3 /𝐾𝑔 + 0.6666(0.52422 − 0.001079 )
𝐾𝑔 𝐾𝑔
𝑚3
𝑣 = 0.3498
𝐾𝑔
𝑢 = 𝑢𝑓 + 𝑋 ∗ (𝑢𝑔 − 𝑢𝑓 )
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑘𝐽 𝑘𝐽 𝑘𝐽
𝑢 = 583,89 + 0.6666(2548.5 − 583,89 )
𝐾𝑔 𝐾𝑔 𝐾𝑔
𝑘𝐽
𝑢 = 1893.49
𝐾𝑔
ℎ = ℎ𝑓 + 𝑋 ∗ (ℎ𝑔 − ℎ𝑓 )
ℎ = 584.26𝑘𝐽/𝐾𝑔 + 0.6666(2730.64𝑘𝐽/𝐾𝑔 − 584.26𝑘𝐽/𝐾𝑔
𝑘𝐽
ℎ = 2015.94
𝐾𝑔
d. Volumen de líquido, volumen de vapor y volumen total del recipiente en m 3
𝑀𝑙𝑖𝑞𝑖𝑑𝑜 = 6𝐾𝑔
𝑀𝑣𝑎𝑝𝑜𝑟 = 3𝐾𝑔
𝑉𝑙𝑖𝑞𝑢𝑖𝑑𝑜 = 𝑀𝑙𝑖𝑞𝑖𝑑𝑜 ∗ 𝑣𝑓
𝐾𝑔
𝑉𝑙𝑖𝑞𝑢𝑖𝑑𝑜 = 6𝐾𝑔 ∗ 0,001079
𝑚3
𝑉𝑙𝑖𝑞𝑢𝑖𝑑𝑜 = 6,474𝑥10−3 𝑚 3
𝑉𝑣𝑎𝑝𝑜𝑟 = 𝑀𝑣𝑎𝑝𝑜𝑟 ∗ 𝑣𝑔
𝑚3
𝑉𝑣𝑎𝑝𝑜𝑟 = 3𝐾𝑔 ∗ 0.52422
𝐾𝑔
𝑉𝑣𝑎𝑝𝑜𝑟 = 1.57266 𝑚 3
𝑉𝑡𝑜𝑡𝑎𝑙 = 𝑉𝑣𝑎𝑝𝑜𝑟 + 𝑉𝑙𝑖𝑞𝑢𝑖𝑑𝑜
𝑉𝑡𝑜𝑡𝑎𝑙 = 1.579094𝑚 3
Estudiante 5 JENNY ALEJANDRA PICO MORA
345 kPa
TOMANDO LA TABLA DEL A5 del libro de cengen y dada una presión de 345Kpa
Un cilindro rígido contiene 6 Kg de líquido y 3 kg de vapor de agua a la temperatura
indicada, determine:
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
a. La calidad del sistema
𝑚𝑣𝑎𝑝𝑜𝑟
𝑥=
𝑚𝑡𝑜𝑡𝑎𝑙
𝑚𝑣𝑎𝑝𝑜𝑟
𝑥=
𝑚𝑙𝑖𝑞 + 𝑚𝑣𝑎𝑝𝑜𝑟
6
𝑥=
9
𝑥 = 0.6666
b. La Temperatura a la cual coexiste el equilibrio en °C
Para una presión de 350Kpa y X=0.6666 y basados en la tabla del apéndice A5 se
pueden observar los valores de la temperatura equivalente a 138.36ºC, también se
pueden calcular los valores entalpias, volúmenes específicos y energías internas en
fase líquido y gas
T=138.36ºC
c. Volumen especifico m3/kg, energía interna kJ/kg y entalpía promedio en kJ/kg
Con P350= KPa.; X=0.6666; T=138.36ºC
𝑣𝑓 = 0.001079𝑚 3 /𝐾𝑔
𝑣𝑔 = 0.52422𝑚 3 /𝐾𝑔
𝑢𝑓 = 583,89𝑘𝐽/𝐾𝑔
𝑢𝑔 = 2548.5𝑘𝐽/𝐾𝑔
ℎ𝑓 = 584.26𝑘𝐽/𝐾𝑔
ℎ𝑔 = 2732.0𝑘𝐽/𝐾𝑔
𝑣 = 𝑣𝑓 + 𝑋 ∗ (𝑣𝑔 − 𝑣𝑓 )
𝑚3 𝑚3
𝑣 = 0.001079 𝑚 3 /𝐾𝑔 + 0.6666(0.52422 − 0.001079 )
𝐾𝑔 𝐾𝑔
𝑚3
𝑣 = 0.3498
𝐾𝑔
𝑢 = 𝑢𝑓 + 𝑋 ∗ (𝑢𝑔 − 𝑢𝑓 )
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑘𝐽 𝑘𝐽 𝑘𝐽
𝑢 = 583,89 + 0.6666(2548.5 − 583,89 )350
𝐾𝑔 𝐾𝑔 𝐾𝑔
𝑘𝐽
𝑢 = 1893.49
𝐾𝑔
ℎ = ℎ𝑓 + 𝑋 ∗ (ℎ𝑔 − ℎ𝑓 )
ℎ = 584.26𝑘𝐽/𝐾𝑔 + 0.6666(2730.64𝑘𝐽/𝐾𝑔 − 584.26𝑘𝐽/𝐾𝑔
𝑘𝐽
ℎ = 2015.94
𝐾𝑔
2. Cada estudiante debe seleccionar una condición para el H 2O. Llenar los espacios
argumentando su elección y mostrando los cálculos.
T P, h, kJ/kg X Descripción de
LUISA FERNANDA °C Kpa (entalpia) (calidad) la fase
MORALES VALERO
4000 0.3
Volumen especifico Energia interna Entalpia
Presión
Temp. Sat. liq sat vap sat liq sat evap vap sat liq sat evap vap sat
kPa °C m3/kg kJ/kg kJ/kg
4000 250,35 0,001252 0,049779 1082,4 1519,3 2601,7 1087,4 1713,5 2800,8
Para identificar si el agua está en la región de líquido comprimido, vapor sobrecalentado
o vapor húmedo, con el dato de presión y calidad calculamos volumen específico así:
𝒗 = 𝒙 ∗ 𝒗𝒇𝒈 + 𝒗𝒇 = 𝟎, 𝟑 ∗ (𝟎, 𝟎𝟒𝟗𝟕𝟕𝟗 − 𝟎, 𝟎𝟎𝟏𝟐𝟓𝟐) + 𝟎, 𝟎𝟎𝟏𝟐𝟓𝟐
= 𝟎, 𝟎𝟏𝟓𝟖𝟏𝟎𝟏 𝒎𝟑/𝒌𝒈
Resulta obvio que 𝒗𝒇 < 𝒗 < 𝒗𝒈 y que el agua está en la región de vapor húmedo, de
manera que la temperatura debe ser la de saturación a la presión especificada
Ahora calculamos la entalpia del vapor húmedo:
ℎ = ℎ𝑓 + 𝑥 ∗ ℎ𝑓𝑔 = 1087,4 + 0,3 ∗ (2800,8 − 1087,4) = 1601.42 𝑘𝑗/𝑘𝑔
ESTUDIANTE: JEISSON ESNEIDER CASTELLANOS NIETO
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
T °C P, h, kJ/kg X (calidad) Descripción
kPa (entalpia) de la fase
Estudiante 151.83 500 ℎ𝑝𝑟𝑜𝑚 0.5 La fase se
3 Jeisson = ℎ𝑓 + 𝑥ℎ𝑓𝑔 encuentra en
Esneider un punto
ℎ𝑝𝑟𝑜𝑚
Castellanos medio ya
= 640.09 que esta en
+ (0.5)(2108)
la mitad
ℎ𝑝𝑟𝑜𝑚 entre 1 y 0.
= 1694.09
ESTUDIANTE: JEISSON FABIAN PATIÑO
𝐾𝐽
ℎ = 𝟐𝟔𝟔𝟔
𝐾𝑔
𝑇 = 300º𝐶
𝑃 = 12.858 𝐾𝑝𝑎
𝐾𝐽
ℎ𝑓 = 1525.8
𝐾𝑔
𝐾𝐽
ℎ𝑓𝑔 = 1140.3
𝐾𝑔
ℎ = ℎ𝑓 + 𝑋 ∗ (ℎ𝑔 − ℎ𝑓 )
ℎ − ℎ𝑓
𝑋=
ℎ𝑓𝑔
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝐾𝐽 𝐾𝐽
2666 − 1525.8
𝐾𝑔 𝐾𝑔
𝑋=
𝐾𝐽
1140.3
𝐾𝑔
𝑋 = 0.999912
T P, h, kJ/kg X Descripción de
°C Kpa (entalpia) (calidad) la fase
Estudiante 5 330 12.858 2666 0.999912 Vapor Saturado
(jeisson Fabian
Patiño)
ESTUDIANTE: JENNY ALEJANDRA PICO MORA
𝐾𝐽
ℎ = 655.7
𝐾𝑔
𝑇 = 300º𝐶
𝑃 = 550 𝐾𝑝𝑎
𝐾𝐽
ℎ𝑓 = 1525.8
𝐾𝑔
𝐾𝐽
ℎ𝑓𝑔 = 1140.3
𝐾𝑔
ℎ = ℎ𝑓 + 𝑋 ∗ (ℎ𝑔 − ℎ𝑓 )
ℎ − ℎ𝑓
𝑋=
ℎ𝑓𝑔
𝐾𝐽 𝐾𝐽
2666 − 1525.8
𝐾𝑔 𝐾𝑔
𝑋=
𝐾𝐽
1140.3
𝐾𝑔
𝑋 = 0.999912
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
T P, h, kJ/kg X Descripción de la
°C Kpa (entalpia) (calidad) fase
Estudiante 550 655.7
5
2. Cada estudiante seleccionará un ejercicio y lo desarrollará correspondiente a la
temática de primera ley aplicado a sistemas cerrados. Deberá informar en el foro el
ejercicio seleccionado. Al final revisará y entenderá cómo solucionar todos los
ejercicios
LUISA FERNANDA MORALES VALERO
a. Un sistema cilindro pistón tiene una diferencia de energía interna de 5 KJ
cuando se comprime ingresando a él 500 J de trabajo. Determine el calor
que tuvo que intercambiar el sistema con los alrededores y el cambio de
volumen si la presión permanece constante y es de 3 atm.
Solución:
𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎 − 𝐸𝑠𝑎𝑙𝑖𝑑𝑎 = ∆𝐸
𝑊𝑒𝑛𝑡𝑟𝑎𝑑𝑎 − 𝑄𝑠𝑎𝑙𝑖𝑑𝑎 = ∆𝑈 → 𝑄𝑠𝑎𝑙𝑖𝑑𝑎 = 0,5 𝑘𝐽 − 5𝑘𝐽 = −4,5𝑘𝐽
2 𝑊𝑒𝑛𝑡𝑟𝑎𝑑𝑎
𝑊𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 0,5𝑘𝐽 = ∫ 𝑃𝑑𝑉 = 𝑃0 ∆𝑉 → ∆𝑉 =
1 𝑃0
0,5 𝑘𝐽 1𝑘𝑃𝑎 ∗ 𝑚 3 1𝑎𝑡𝑚
∆𝑉 = ∗ ∗ = 0,0016 𝑚 3
3𝑎𝑡𝑚 1𝑘𝑗 101,325 𝑘𝑃𝑎
3.
b. MARIA
Nombre del estudiante que desarrolla: Jeisson Esneider Castellanos
c. Se calientan 2kg de oxígeno, de 30 a 320 °C en un recipiente. Determine
la transferencia de calor que se requiere cuando eso se hace en un
proceso a) a volumen constante, b) isobárico.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Solución:
a) Para dar solución al ejercicio se utilizará la siguiente ecuación:
𝑄 = 𝑚 ∗ 𝑐𝑣 ∗ (𝑇2 − 𝑇1 )
Datos:
M= 2 kg T1= 30 °C T2= 320 °C Cv=?
Se busca a Cv en la tabla constantes de calores especificos
𝑘𝐽
𝑐𝑣 = 0.659
𝑘𝑔 ∗ 𝐾
Convertimos a T1 y T2 de °C a °K
T1= 303.15 °K T2= 593.15 °K
Ahora aplicamos los valores en la ecuación
𝑘𝐽
𝑄 = 2 𝑘𝑔 ∗ 0.659 ∗ (303.15 °𝐾 − 593.15 °𝐾)
𝑘𝑔 ∗ 𝐾
𝑄 = 382.22 𝑘𝐽
b) Para dar solución al ejercicio se utilizará la siguiente ecuación:
𝑄 = 𝑚 ∗ 𝑐𝑝 ∗ (𝑇2 − 𝑇1 )
Datos:
M= 2 kg T1= 30 °C T2= 320 °C Cp=?
Se busca a Cv en la tabla constantes de calores especificos
𝑘𝐽
𝑐𝑝 = 0.919
𝑘𝑔 ∗ 𝐾
Convertimos a T1 y T2 de °C a °K
T1= 303.15 °K T2= 593.15 °K
Ahora aplicamos los valores en la ecuación
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑘𝐽
𝑄 = 2 𝑘𝑔 ∗ 0.919 ∗ (303.15 °𝐾 − 593.15 °𝐾)
𝑘𝑔 ∗ 𝐾
𝑄 = 533.02 𝑘𝐽
NOMBRE DEL ESTUDIANTE QUE DESARROLLA: JENNY
ALEJANDRA PICO MORA
D) Un dispositivo cilindro-émbolo está inicialmente a 500 kPa y 27 °C y
tiene integrado un sistema de agitación que le transfiere 20kJ/kg de
energía en forma de trabajo. Durante este proceso se transfiere calor
para mantener constante la temperatura del aire, y al mismo tiempo se
triplica el volumen del gas. Calcule la cantidad requerida de
transferencia de calor, en kJ/kg.
∆𝑈 = 0 = 𝑄 + 𝑊
𝑑𝑜𝑛𝑑𝑒 𝑊 = 𝑊𝑒𝑗𝑒 − 𝑊𝑒𝑥𝑝𝑎𝑛𝑠𝑖ó𝑛 = 𝑊𝑒𝑗𝑒 − 𝑃1 𝑉1 ln 𝑣2/𝑣1
P1 = 500Kpa
T1 = 37º C + 273 = 310ºK
Energía = 40 KJ/Kg
T constante
V2 = 2 V1
Q=?
SOLUCIÓN :
Para resolver el ejercicio se procede a calcular la cantidad de
transferencia calor requerida de la siguiente manera :
ΔU = 0
ΔU = Q + W =0
W = P1 *V1 * Ln( V2/V1)
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
W= P1*V1 * Ln2
Q= 800 KJ/Kg .
Nombre del estudiante que desarrolla: Jeisson patiño
d. Gas ideal en un dispositivo cilindro-émbolo sufre un proceso de
compresión isotérmica que comienza con una presión inicial y un
volumen inicial de 200 kPa y 0.8 m3, respectivamente. Durante el
proceso, hay una transferencia de calor de 120 kJ del gas ideal al
entorno. Determine el volumen y la presión al final del proceso.
Solución:
𝑃1 = 200𝐾𝑝𝑎
𝑣1 = 0.8𝑚 3
𝑄 = −120𝐾𝐽
𝑃2 =?
𝑣2 =?
𝑣2
𝑄 = 𝑛𝑅𝑇𝑙𝑛( )
𝑣1
Ecuación de gases ideales es:
PV=nRT
Como es un proceso isotérmico se tiene la siguiente expresión
PV=k
nRT=K
𝑣2
𝑄 = 𝑘𝑙𝑛( )
𝑣1
𝑘 = 120 ∗ 0.8
𝑘 = 96𝐾𝐽
𝑣2
−120 = 96 ∗ ln( )
0.8
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑣2
−1.25 = 𝑙𝑛( )
0.8
𝑣2
0.2865 =
0.8
𝑣2 = 0.229𝑚 3
96𝐾𝐽
𝑃2 =
0.229𝑚 3
𝑃2 = 418.84𝐾𝑃𝑎
A continuación, se presentan dos ejercicios relacionados con aplicación de la primera ley
en sistemas abiertos. Para la resolución de los ejercicios, los estudiantes deberán
seleccionar un numeral y desarrollarlo de forma individual y deta 𝑄 =llada. Finalmente
se debe compilar las respuestas.
4. Cada estudiante selecciona un dispositivo y debe indicar la expresión general de
energía. Posteriormente escoger de forma grupal un solo equipo y cada uno dará
una característica o un ejemplo de su uso.
Nombre Ecuación de energía y supuestos
Dispositivo
estudiante
𝑊𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝑚̇ ̇ ∗ 𝑞𝑠𝑎𝑙𝑖𝑑𝑎 + 𝑚̇ (ℎ2 − ℎ1 )
LUISA Suposiciones:
FERNANDA Compresor Éste es un proceso de flujo estacionario puesto que no hay cambio
MORALES con el tiempo en ningún punto, por lo tanto ∆m=0 y ∆E=0.
VALERO El aire es un gas ideal porque está a temperatura alta y presión
baja en relación con sus valores de punto crítico.
Los cambios de energía cinética y potencial son cero.
Dispositivo
Compresor Su funcion es comprimir un fluido comprensible, por lo tanto:
seleccionado
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
𝑣2 << 𝑣1 → 𝑝2 >> 𝑝1
Nombre estudiante Dispositivo Ecuación de energía y supuestos
JEISSON FABIAN TURBINA Turbinas: La siguiente
PATIÑO expresión relaciona la potencia
producida con la energía que se
extrae del flujo y el caudal que
circula por el sistema:
𝑃 = 𝜂∗𝛾∗𝑄∗𝐻
Dónde:
- P es la potencia generada
- η es el rendimiento de la
turbina (valor entre 0 y 1)
- γ es el peso específico del
fluido (en este caso agua
con peso específico de
9800[N/m^3])
- Q es el caudal
- H es el Bernoulli extraído
desde el flujo
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
caracteristicas Turbina:
Funcionan como un mecanismo que
intercambian trabajo con el medio
externo tal que se le agregue a un
sistema por donde fluye un fluido, lo
cual por consiguiente, agrega energía a
las ecuaciones de balance de estas.
Para el caso de las turbinas, estas
representan una pérdida de energía,
que se traduce en el movimiento de una
hélice. Esto produce torque que puede
ser utilizado, entre otras cosas, para
generar electricidad. Existen varios
tipos de turbinas que varían según la
forma de la hélice y cómo interactúa
con el fluido. En el presente informe de
laboratorio se utilizará sólo una tipo
Pelton.
JEISSON ESNEIDER INTERCAMBIADOR DE
CASTELLANOS CALOR
Este es un proceso de intercambio de
calor entre dos fluidos sin ser
mezclado. Los intercambiadores no
tienen que ver comunmente con
interecciones de trabajo (W=0) y los
cambio de energia cinetica y potencial
son insignificantes (
) para cada
corriente de fluido.
MARIA NIEVES ROSAS DUCTO
JENNY ALEJANDRA TOBERA CARACTERISTICAS
PICO MORA Una tobera es un dispositivo que
convierte la energía térmica y de
presión de un fluido (conocida
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
como entalpía) en energía cinética.
Como tal, es utilizado
en turbomáquinas y otras máquinas,
como inyectores, surtidores,
propulsión a chorro, etc. El fluido sufre
un aumento de velocidad a medida que
la sección de la tobera va
disminuyendo, por lo que sufre
también una disminución de presión y
temperatura al conservarse la energía.
Existen diseños y tipos de tobera muy
usados en diferentes campos de la
ingeniería, como la de Laval, Rateau,
Curtis, etc.
2
𝑣
𝑚 (ℎ1 + 1) − 𝑚 (ℎ1
2
2
𝑣
+ 2) 𝑝𝑢𝑒𝑠𝑡𝑜 𝑞𝑢𝑒 𝑄
2
= 0, 𝑊 − 0 𝑦 ∆𝑐𝑝
≅0
𝑣22 − 𝑣12
ℎ2 − ℎ1 −
1
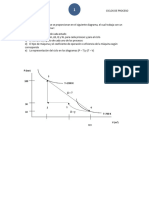
5. Una tobera (Figura A) entra vapor de agua a 400 °C y 800 kPa, con una velocidad de
10 m/s, y sale a 300 °C y 200 kPa. Para un área de entrada de 750 cm 2 , determine la
velocidad y el flujo volumétrico del vapor de agua en la salida de la tobera.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Una tobera es un dispositivo que incrementa la
velocidad de un fluido a expensas de la presión. Éste es
un proceso de flujo estacionario porque no hay cambio
con el tiempo en algún punto, por lo tanto ∆m=0; no
hay interacciones de trabajo y el cambio de energía
potencial es cero. Se observa que sólo hay una entrada
y una salida, por lo tanto mentrada=msalida
ESTUDIANTE N°2. LUISA FERNANDA MORALES VALERO
𝑚3 𝑘𝐽
𝑣1 = 0,38429 ; ℎ1 = 3267,7 ; 𝐴 = 750𝑐𝑚 2 = 0,075𝑚 2
𝑘𝑔 𝑘𝑔 1
𝑚3 𝑘𝐽
𝑣2 = 1,31623 ; ℎ2 = 3072,1
𝑘𝑔 𝑘𝑔
𝑚̇1 = 𝑚̇2
1 1 𝑣2
∗ 𝑄1 = ∗ 𝑄2 → 𝑄2 = ∗ (𝐴1 ∗ v1 )
𝑣1 𝑣2 𝑣1
1,31623
𝑄2 = ∗ (0,075 ∗ 10) = 2,6 𝑚 3 /𝑠
0,38429
1 1
𝑚̇ 1 = 𝑚̇2 = ∗ 𝑄2 = ∗ 2,6 = 1,98 𝑘𝑔/𝑠
𝑣2 1,31623
Asumiendo que el area de entrada es igual a la de salida
𝑄2 2,6 𝑚 3 /𝑠
v2 = = = 34,7 𝑚/𝑠
𝐴 0,075 𝑚 2
𝑚3 𝑘𝐽
𝑣1 = 0,38429 ; ℎ1 = 3267,7 ; 𝐴1 = 750𝑐𝑚 2 = 0,075𝑚 2
𝑘𝑔 𝑘𝑔
𝑚3 𝑘𝐽
𝑣2 = 1,31623 ; ℎ2 = 3072,1
𝑘𝑔 𝑘𝑔
𝑚̇1 = 𝑚̇2
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
1 1 𝑣2
∗ 𝑄1 = ∗ 𝑄2 → 𝑄2 = ∗ (𝐴1 ∗ v1 )
𝑣1 𝑣2 𝑣1
1,31623
𝑄2 = ∗ (0,075 ∗ 10) = 2,6 𝑚 3 /𝑠
0,38429
1 1
𝑚̇ 1 = 𝑚̇2 = ∗ 𝑄2 = ∗ 2,6 = 1,98 𝑘𝑔/𝑠
𝑣2 1,31623
Asumiendo que el area de entrada es igual a la de salida
𝑄2 2,6 𝑚 3 /𝑠
v2 = = = 34,7 𝑚/𝑠
𝐴 0,075 𝑚 2
Para hallar el flujo volumétrico del vapor de agua en la salida aplicamos la siguiente
ecuacion hallando el caudal primeramente:
𝑣2
𝑄2 = ∗ (𝐴1 ∗ V1 )
𝑣1
1,31623 𝑚 3 /𝑘𝑔
𝑄2 = ∗ (0,075 𝑚 2 ∗ 10 m/s) = 2,6 𝑚 3 /𝑠
0,38429 𝑚 3 /𝑘𝑔
Ahora aplicamos la siguiente ecuacion para determinar la masa que fluye por la salida de
la tobera.
1
𝑚̇2 = ∗ 𝑄2
𝑣2
1
𝑚= 3
∗ 2,6 𝑚 3 /𝑠 = 1,98 𝑘𝑔/𝑠
1,31623 𝑚 /𝑘𝑔
Ahora hallamos la velocidad de salida aplicando la siguiente ecuacion:
𝑄2
v2 =
𝐴
2,6 𝑚 3 /𝑠
V2 = = 34,7 𝑚/𝑠
0,075 𝑚 2
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Cada estudiante selecciona una condición, lo desarrolla y al final responden la pregunta
grupal ¿Cuál configuración tiene la mayor velocidad y por qué?
LUISA FERNANDA a. mientras pierde calor a una tasa de 55 kW
MORALES VALERO
Configuración de Argumentos:
mayor velocidad
Se analiza nuevamente, el dispositivo anterior, incluyendo la condición de pérdida de
calor hacia los alrededores,
El balance de energía para este sistema de flujo estacionario se puede expresar así:
𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎 = 𝐸𝑠𝑎𝑙𝑖𝑑𝑎
𝑊̇ = 0 𝑦 ∆𝐸𝑝𝑜𝑡𝑒𝑛𝑐𝑖𝑎𝑙 = 0
v12 v22
(ℎ1 + ) = 𝑞𝑠𝑎𝑙𝑖𝑑𝑎 + (ℎ2 + ) [𝑘𝐽/𝑘𝑔]
2 2
Despejando la velocidad de salida, reemplazando los valores para las condiciones 1 y 2 y
de acuerdo con las tablas de vapor:
1012 55 v22
(3267,7 + )= + (3072,1 + ) [𝑘𝐽/𝑘𝑔]
2 1,98 2
1012 55
v2 = √2 [(3267,7 + )− − 3072,1] = 20,9 𝑚/𝑠
2 1,98
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
NOMBRE ESTUDIANTE : b. mientras pierde calor a una tasa de 65 kW
MARIA NIEVES ROSAS
NOMBRE ESTUDIANTE : mientras pierde calor a una tasa de 35 Kw
JEISSON ESNEIDER
CASTELLANOS Solucion:
Datos: T1= 400 ºC T2= 300 ºC
P1= 800 kPa P2= 200 kPa
V1= 0,38429 m3/kg V2= 1,31623 m3/kg
h1= 3267,7 h2= 3071,1
A1=0,075 m2 A2= ?
Vel1= 10 m/s Vel2=?
m1=? m2= ?
Para hallar el flujo volumétrico del vapor de agua en la salida
aplicamos la siguiente ecuacion hallando el caudal primeramente:
𝑣2
𝑄2 = ∗ (𝐴1 ∗ V1 )
𝑣1
1,31623 𝑚 /𝑘𝑔3
𝑄2 = ∗ (0,075 𝑚 2 ∗ 10 m/s) = 2,6 𝑚 3 /𝑠
0,38429 𝑚 3 /𝑘𝑔
Ahora aplicamos la siguiente ecuacion para determinar la masa
que fluye por la salida de la tobera.
1
𝑚̇2 = ∗ 𝑄2
𝑣2
1
𝑚= ∗ 2,6 𝑚 3 /𝑠 = 1,98 𝑘𝑔/𝑠
1,31623 𝑚 3 /𝑘𝑔
Ahora hallamos la velocidad de salida aplicando la siguiente
ecuacion:
𝑄2
v2 =
𝐴
2,6 𝑚 3 /𝑠
V2 = = 34,7 𝑚/𝑠
0,075 𝑚 2
Tenemos que para determinar la V2 según la perdida de calor o
energia la siguiente ecuacion:
v12 v22
(ℎ1 + ) = 𝑞𝑠𝑎𝑙𝑖𝑑𝑎 + (ℎ2 + ) [𝑘𝐽/𝑘𝑔]
2 2
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
1012 35 v22
(3267,7 + )= + (3072,1 + ) [𝑘𝐽/𝑘𝑔]
2 1,98 2
Despejamos V2
1012 35
v2 = √2 [(3267,7 + )− − 3072,1]
2 1,98
v2 = √2(3317.7 − 17.7 − 3072,1)
v2 = √2(177.9)
v2 = √355.8
v2 = 18.86 𝑚/𝑠
Argumentos: Al perder energia o calor el vapor pierde presion y al
mismo tiempo pierde valocidad ya que la presion VS velocidad son
directamente proporcionales.
NOMBRE ESTUDIANTE : d. mientras pierde calor a una tasa de 10 kW
JEISSON FABIAN PATIÑO
̇ − 𝐸𝑠𝑎𝑙𝑖𝑑𝑎 = ∆̇ 𝐸̇𝑠𝑖𝑠𝑡𝑒𝑚𝑎
𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎
̇
𝐸𝑒𝑛𝑡𝑟𝑎𝑑𝑎 ̇
= 𝐸𝑠𝑎𝑙𝑖𝑑𝑎
2 2
𝑉𝑒𝑛𝑡 𝑉𝑠𝑎𝑙
𝑚̇ (ℎ𝑒𝑛𝑡 + ) = 𝑚̇ (ℎ𝑠𝑎𝑙 + ̇
) + 𝑄𝑠𝑎𝑙𝑖𝑑𝑎
2 2
𝑉12 𝑉22 𝑄̇𝑠𝑎𝑙𝑖𝑑𝑎
ℎ1 + = ℎ2 + +
2 2 𝑚̇
De las tablas A-6
𝑚3
𝑃𝑒𝑛𝑡 = 800𝑘𝑝𝑎 𝑉𝑒𝑛𝑡 = 0.38429 𝑘𝑔
}
𝑇𝑒𝑛𝑡 = 400°𝐶 ℎ𝑒𝑛𝑡 = 3267.7 𝑘𝐽/𝑘𝑔
𝑚3
𝑃𝑠𝑎𝑙 = 200𝑘𝑝𝑎 𝑉𝑠𝑎𝑙 = 1.31623
} 𝑘𝑔
𝑇𝑠𝑎𝑙 = 300°𝐶 ℎ𝑠𝑎𝑙𝑖𝑑𝑎 = 32072.1 𝑘𝐽/𝑘𝑔
La tasa de flujo de masa del vapor es
1 ̇ 1 𝑚
2 ) (10 ) = 2.082 𝑘𝑔/𝑠
𝑚= 𝐴𝑒𝑛𝑡 𝑣𝑒𝑛𝑡 = ( 0.08𝑚
𝑉𝑒𝑛𝑡 0.38429𝑚 3 /𝑠 𝑠
Sustituyendo
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
10𝑚 2 1
𝑘𝐽
𝑘𝐽 ( ) 𝑘𝑔
3267.7 + 𝑠 ( )
𝑘𝑔 2 𝑚2
1000 2
𝑠
𝑘𝐽 𝑘𝐽
𝑘𝐽 𝑉22 1 10
𝑘𝑔 𝑠
= 3072.1 + ( )+
𝑘𝑔 2 1000𝑚 2 𝑘𝑔
2 2.082
𝑠 𝑠
𝒗𝒔𝒂𝒍 = 𝟔𝟏𝟕. 𝟖𝟏𝟑 𝒎/𝒔
La tasa de flujo de volumen en la salida de la boquilla es
𝑘𝑔 𝑚3
̇
𝑉𝑠𝑎𝑙 = 𝑚̇ 𝑉𝑠𝑎𝑙 = (2.082 ) (1.31623 ) = 𝟐. 𝟕𝟒𝒎𝟑 /𝒔
𝑠 𝑘𝑔
Configuración de mayor Argumentos:
velocidad
Paso 3 (Actividad individual)
Este paso se debe solucionar de forma individual. El estudiante debe seleccionar un
numeral, indicarlo en el foro y responder la pregunta empleado un código en Excel. Al
final el moderador del grupo compilará todos los documentos Excel y lo subirá junto el
anexo-tarea 2 en el entorno de evaluación y seguimiento.
Pregunta:
La ecuación de Van der Walls es un modelo comúnmente usado para correlacionar el
comportamiento p-v-T de los gases. Esta ecuación contiene 2 constantes empíricas.
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Fuente: De Lucas, Antonio et al. (2004)Termotecnia básica para ingenieros químicos:
bases de termodinámica aplicada. Ed. Universidad de Castilla.
Empleando la información de la tabla 1.2, elabore en Excel un programa que permita
determinar la presión del Nitrógeno cuando se especifica un volumen molar y un rango
de temperatura especifico. Obtener una gráfica T vs P y comparar los resultados cuando
se tiene un modelo de gases ideales. (Observe que la constante de gases ideales debe tener
unidades de litros, atmosferas, kelvin y moles)
A Volumen 20 litros, 10 moles y evaluar T entre 300 y 340 K
B Volumen 15 litros, 8 moles y evaluar T entre 300 y 340 K
C Volumen 10 litros, 6 moles y evaluar T entre 300 y 340 K
D Volumen 5 litros, 4 moles y evaluar T entre 300 y 340 K
E Volumen 1 litro, 2 moles y evaluar T entre 300 y 340 K
El programa en Excel deberá reportar una tabla con datos de Presión y Temperatura para
ambos modelos, junto con el perfil como se muestra en el ejemplo que trabaja con el
metano. Se observa que el modelo de gases ideales presenta desfases frente al modelo de
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Van der Waals. Observe además que al modelo de gases ideales NO tiene en cuenta qué
tipo de sustancia es, mientras que el modelo trabajado sí.
LUISA FERNANDA MORALES VALERO
Interpolación:
Modelo gas real:
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
JEISSON CASTELLANOS
a b R
Element Volume
Mol L∙atm/(K∙m
o n (L)
2
𝑎𝑡𝑚 ∙ 𝑙𝑖𝑡𝑟𝑜 ∙ 𝑚𝑜𝑙 −1
𝑙𝑖𝑡𝑟𝑜2 ∙ 𝑚𝑜𝑙 −1 ol)
Nitrogen
1.39 0.0391 10 6 0.0821
o
Modelo de Van der Waals Modelo gases ideales
𝑅𝑇 𝑎
𝑃= − 2
𝑣 −𝑏 𝑣
P=(nRT/V)
T (˚K) P (atm) T (˚K) P (atm)
275 2.2515 275 13.5395
280 2.2927 280 13.7857
285 2.3339 285 14.0318
290 2.3751 290 14.2780
295 2.4163 295 14.5242
300 2.4575 300 14.7703
305 2.4987 305 15.0165
310 2.5399 310 15.2627
Modelo de Van der Waals VS Modelo gases ideales
20.0000
18.0000
16.0000
14.0000
12.0000
P
10.0000
8.0000
6.0000
4.0000
2.0000
0.0000
275 280 285 290 295 300 305 310
T (K)
Modelo de Van der Waals Modelo gases ideales
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
JEISSON PATIÑO
𝑏
𝑎 Volumen R
Elemento (𝑙𝑖𝑡𝑟𝑜 ∙ 𝑚𝑜𝑙 −1 )
2 Mol
2 −1 (litros) L∙atm/(K∙mol)
(𝑎𝑡𝑚 ∙ 𝑙𝑖𝑡𝑟𝑜 ∙ 𝑚𝑜𝑙 )
Nitrogeno 1.39 0.0391 5 4 0.08205746
Modelo por Ecuación de Van der Waals
𝑎
(𝑃 + ) (𝑣 − 𝑏) = 𝑅𝑇
𝑣2
R = 0,08205746 L∙atm/(K∙mol)
𝑅𝑇 𝑎
𝑃= − 2
𝑣 −𝑏 𝑣
Van der waals
T (K) P (atm)
300 19.440
305 19.779
310 20.118
315 20.457
320 20.795
325 21.134
330 21.473
335 21.812
340 22.151
Modelo gases ideales
PV=nRT
P=(nRT/V)
T (K) P (atm)
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
300 19.694
305 20.022
310 20.350
315 20.678
320 21.007
325 21.335
330 21.663
335 21.991
340 22.320
Modelo de Van der Waals y Gases Ideales
22.500
22.000
21.500
Presión (atm)
21.000
20.500
20.000
19.500
19.000
295 300 305 310 315 320 325 330 335 340 345
Temperatura (K)
Van der waals Modelo gases ideales
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
Figura B. Ejemplo del programa en Excel a desarrollar empleando el modelo de Benedict-
Webb-Rubin
Trabajo Colaborativo Unidad II
ECBTI
TERMODINÁMICA 212065
Semestre 2019 16-01
REFERENTES BIBLIOGRÁFICOS
Çengel, Y. A., & Boles, M. A. (2009). Propiedades de las sustancias puras. En Y.A.
Cengel (Ed. 6a), Termodinámica (p. 111-164). España: McGraw-Hill. Recuperado de
http://bibliotecavirtual.unad.edu.co:2077/lib/unadsp/detail.action?docID=10515088&p0
0=termodin%C3%A1mica.
Trabajo Colaborativo Unidad II
S-ar putea să vă placă și
- LF A252 Inf 2 SGR 3Document6 paginiLF A252 Inf 2 SGR 3Dayanna CristanchoÎncă nu există evaluări
- Taller Del MuaDocument2 paginiTaller Del MuaAndrés Felipe PerdomoÎncă nu există evaluări
- Diagramas de PourbaixDocument21 paginiDiagramas de PourbaixDiana Alvarez BugueñoÎncă nu există evaluări
- Podemos Definir Como Las Cargas Axiales Excentricas Como Las Fuerzas Que No Actuan Directamente en El Centroide Del ElementoDocument4 paginiPodemos Definir Como Las Cargas Axiales Excentricas Como Las Fuerzas Que No Actuan Directamente en El Centroide Del ElementoSTIVEN SANTIAGO TORRES VILLANUEVAÎncă nu există evaluări
- Programming Guide MX-13 Euro V MY2019 - Rev A - 3 - SpanishDocument101 paginiProgramming Guide MX-13 Euro V MY2019 - Rev A - 3 - SpanishAdan FloresÎncă nu există evaluări
- Campo Eléctrico 2º BachilleratoDocument5 paginiCampo Eléctrico 2º BachilleratoCharo VillamarizÎncă nu există evaluări
- HrdxftjcykvguliyñópDocument4 paginiHrdxftjcykvguliyñópCarlos AriasÎncă nu există evaluări
- Trabajo Final de AceroDocument45 paginiTrabajo Final de Aceroerick0zapataÎncă nu există evaluări
- Practica 4 Pruebas MecanicasDocument8 paginiPractica 4 Pruebas MecanicasPancho LópezÎncă nu există evaluări
- Laboratorio Virtual Caida LibreDocument6 paginiLaboratorio Virtual Caida Librejorge ortegaÎncă nu există evaluări
- Analisis Dimensional 1Document2 paginiAnalisis Dimensional 1Roxana Valladolid BranÎncă nu există evaluări
- Problemas de Procesos-Ds TBDocument7 paginiProblemas de Procesos-Ds TBCriis LeyvaÎncă nu există evaluări
- Enunciados GravitaciónDocument13 paginiEnunciados GravitaciónSara López-SerranoÎncă nu există evaluări
- Clase 1Document31 paginiClase 1DANIEL RAMIRO VEGA SANCHEZÎncă nu există evaluări
- Anexo 6 - Energía de FermiDocument6 paginiAnexo 6 - Energía de FermiWalter GarcíaÎncă nu există evaluări
- Informe 2 Lab I Subgrupo 1Document14 paginiInforme 2 Lab I Subgrupo 1EdwinLozanoÎncă nu există evaluări
- Smaart EspanolDocument118 paginiSmaart EspanolLuis FunkÎncă nu există evaluări
- Informe CalorimetroDocument8 paginiInforme CalorimetroValeria GallegosÎncă nu există evaluări
- Excel - Diseño de Pavimemto Rigido-ModeloDocument23 paginiExcel - Diseño de Pavimemto Rigido-ModeloMARGARITA DEL ROSARIO PADILLA LOZADAÎncă nu există evaluări
- Boletín 1Document4 paginiBoletín 1Trebor A ROÎncă nu există evaluări
- Equivalente Mecanico Del CalorDocument9 paginiEquivalente Mecanico Del CalorLen AbernathyÎncă nu există evaluări
- IClumodl CobedeDocument319 paginiIClumodl CobedeKenji DíazÎncă nu există evaluări
- Tarea N°1 PavimentosDocument55 paginiTarea N°1 PavimentosKiomi VelizÎncă nu există evaluări
- Resumen CGravDocument2 paginiResumen CGravJorgeÎncă nu există evaluări
- Zapata Concéntrica Carga AxialDocument38 paginiZapata Concéntrica Carga AxialCristian DiagamaÎncă nu există evaluări
- Sesión 03 - FluidosDocument30 paginiSesión 03 - FluidosJhordan Diaz CubasÎncă nu există evaluări
- Ley Logarítmica - Ley PotencialDocument13 paginiLey Logarítmica - Ley PotencialTINCO FERNÁNDEZ RANDY DUSTINÎncă nu există evaluări
- Elementos Estructurales Sometidos A Corte y TorsiónDocument22 paginiElementos Estructurales Sometidos A Corte y TorsiónJavier Cañizares100% (5)