Documente Academic
Documente Profesional
Documente Cultură
Laboratorio FIQUI 1
Încărcat de
fernando hectorDescriere originală:
Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Laboratorio FIQUI 1
Încărcat de
fernando hectorDrepturi de autor:
Formate disponibile
Laboratorio de Fisicoquímica / Gases
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 1
Laboratorio de Fisicoquímica / Gases
1. RESUMEN
El objetivo de esta práctica es determinar la densidad de los gases por el método de Víctor
Meyer y el coeficiente adiabático que está dado por la relación de las Capacidades
Caloríficas del aire a presiones por el método de Clément y Desormes. Ambos métodos se
trabajaron con una presión de 754.4 mmHg y 19.5 ºC de temperatura.
El método de Víctor Meyer se basa en determinar el volumen de una sustancia volátil de
masa conocida, midiendo el volumen de aire que es desplazado por ella en forma de vapor,
para determinar la densidad de la sustancia en cuestión. Se corrige la presión barométrica
(737.4 mmHg) que se usará para hallar el volumen desplazado a condiciones normales (13.9
mL), este a su vez se usa para determinar la densidad experimental al dividir m/V (6.29 g/L)
y la ecuación de Berthelot se usa para hallar la densidad teórica (5.66 g/L).
En el método de Clément y Desormes, el coeficiente adiabático hallado fue de 1.4 siendo
el teórico 1.40 para el aire habiendo un 0% de error. El fundamento del método de trabajo
se basa en una diferencia de alturas que son una consecuencia de cambios de presión y
volumen en un sistema adiabático. Es importante ser precisos en la medición de las
diferencia de alturas ya que de esto dependerá nuestro coeficiente adiabático hallado
experimentalmente.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 2
Laboratorio de Fisicoquímica / Gases
2. INTRODUCCIÓN
El conocimiento de gases es muy importante para la vida a partir de que vivimos inmersos
en un gas, el aire que forma la atmósfera, pocas veces reparamos en él. Otro tanto ocurre
con la mayoría de los gases que se nos presentan diariamente: el vapor de agua al cocinar,
el dióxido de carbono que se forma en la combustión o el butano que sale de la cocina,
normalmente no se ven y si uno se fija en ellos, al final se mezclan con el aire y
aparentemente desaparecen.
Los gases son distintos a los vapores a partir de que los vapores se condensan, para lo cual
solo requiere de la temperatura necesaria, mientras que para los gases, se licuan para lo cual
es necesario conseguir la presión y la temperatura critica de la sustancia, las cuales se
conocen por tablas teóricas. En el rubro de la ingeniería estos conceptos son de suma
importancia ya que en la aplicación del método de Víctor Mayer es posible un análisis con
muy poco porcentaje de error mientras que el Clement y Desormes contiene un gran
contenido en teoría por lo cual es aplicado en todas los centros de enseñanza de
fisicoquímica.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 3
Laboratorio de Fisicoquímica / Gases
3. PRINCIPIOS TEORICOS
GASES
Se denomina gas al estado de agregación de la materia en el que las sustancias no tienen
forma ni volumen propio, adoptando el de los recipientes que las contienen. Las moléculas
que constituyen un gas casi no son atraídas unas por otras, por lo que se mueven en el vacío
a gran velocidad y muy separadas unas de otras. El estudio de gases se clasifican como:
Gases ideales
Los primeros estudios fisicoquímicos realizados a partir del siglo XVII involucraron el
estudio de los gases, debido a que éstos responden en forma más dramática a cambios en el
ambiente que los líquidos y los sólidos. La mayoría de estos primeros estudios estuvieron
focalizados en las variaciones de presión, temperaturas y volumen de una determinada
porción de gas (relaciones P-V-T). La más simple es la Ley de Boyle –Mariotte, donde la
variable de estado que es constante es la temperatura, y en donde el la presión del gas es
inversamente proporcional al volumen del gas:
PV = cte
Análogamente, Gay-Lussac reportó la relación directa entre el volumen y la temperatura,
tomando como constante la variable de estado de la presión:
V/T = cte
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 4
Laboratorio de Fisicoquímica / Gases
Y la Ley Combinada es:
𝑃. 𝑉
= 𝑐𝑡𝑒
𝑇
Ahora podemos enunciar la ecuación de estado para un gas ideal, también conocida como
Ley de los Gases Ideales:
P.V = n.R.T
De esta ley se deducen las isotermas de un gas ideal:
Gases Reales
El modelo de gas ideal permite definir un marco de referencia para estudiar el
comportamiento de los gases. En algunas ocasiones, podremos modelarlos gases geológicos
utilizando Leyes Ideales; sin embargo, es de gran importancia tener una noción de las
desviaciones que sufren éstos bajo determinadas condiciones de temperatura, presión y
volumen. Los gases naturales o reales presentan las siguientes desviaciones del
comportamiento ideal:
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 5
Laboratorio de Fisicoquímica / Gases
- Para altas presiones: V real > V ideal
- Para moderadas presiones: V real < V ideal
- Para moderadas temperaturas: V real > V ideal
Estas desviaciones aparecen producto de la diferencia de volumen, por lo que definiremos
el factor de compresibilidad (Z), que corresponde a una medida de la no-idealidad en el
comportamiento de un gas:
𝑷𝑽
𝒁=
𝑹𝑻
Para un Gas Ideal, el factor de compresibilidad es unitario, mientras que para Gases Reales
es mayor o menor que 1. Ejemplos para el H2O, CO2 y O2 gaseosos:
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 6
Laboratorio de Fisicoquímica / Gases
DENSIDAD DE GASES
La densidad o densidad absoluta es la magnitud que expresa la relación entre la masa y
el volumen de un cuerpo.
𝑚 𝑃𝑀
𝜌= =
𝑉 𝑅´𝑇
CAPACIDAD CALORIFICA DE GASES
La capacidad calorífica de una sustancia es el calor necesario para elevar, en una unidad
termométrica, la temperatura de una unidad de masa de dicha sustancia. Existen 2 tipos de
capacidad calorífica: a presión constante y volumen constante y esto depende si es gas es
mono, di, o poliatómico. Mediante el método de Clement y Desormes en un sistema a presión
superior a la atmosférica se realiza una expansión adiabática y luego un calentamiento a
volumen constante; para un sistema de este tipo de cumple:
𝑪𝒑 𝒍𝒏𝑷𝟏 − 𝒍𝒏𝑷𝟎
=
𝑪𝒗 𝒍𝒏𝑷𝟏 − 𝒍𝒏𝑷𝟐
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 7
Laboratorio de Fisicoquímica / Gases
Y si el cambio de presión es pequeño, sabiendo que 𝑃=𝜌.g.h:
𝑪𝒑 𝒉𝟏
𝜸= =
𝑪𝒗 𝒉𝟏 − 𝒉𝟐
La capacidad calorífica de una sustancia tiene un valor mayor si se lleva acabo a presión
constante, que si es realizada a volumen constante. Toda vez que al aplicar presión constante
a una sustancia, ésta sufre un aumento en su volumen, lo que provoca una disminución en
su temperatura y, consecuentemente, necesitará más calor para elevarla.
A volumen constante, todo el calor suministrado a la sustancia pasa a aumentar la energía
cinética de las moléculas, por lo tanto la temperatura se incrementa con mayor facilidad. Es
evidente que mientras más alto sea el valor dela capacidad calorífica de una sustancia,
requiere mayor cantidad de calor para elevar su temperatura.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 8
Laboratorio de Fisicoquímica / Gases
4. DETALLES EXPERIMENTALES
MATERIALES
EQUIPO PARA EL MÉTODO DE VICTOR MEYER
Tubo de vaporización
Vaso precipitado
Cocinilla
Manguera
Bureta
Pera de decantación
Ampolla
Pinza
mechero
Reactivo: cloroformo
EQUIPO PARA EL MÉTODO DE CLEMENT Y DESORMES
Balón de gas
Manómetro
Inflador
Manguera
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 9
Laboratorio de Fisicoquímica / Gases
PROCEDIMIENTO
a) DETERMINACIÓN DE LA DENSIDAD DE GASES POR EL METODO DE
VICTOR MEYER
Primero instalamos el equipo (fig. 4-A), tener en cuenta que las adaptaciones de las
manguera con el tubo de vaporización este bien conectado, la pera y la bureta deben
de tener la misma distancia de agua.
llenamos agua en el vaso precipitado en la que introducimos el tubo de vaporización,
calentamos hasta llegar al punto de ebullición, esperamos unos 10 minutos.
mientras esperamos esos minutos pesamos una ampolla y lo calentamos para luego
introducirlo en un vasito que contiene cloroformo con el fin de que ese líquido
orgánico se introduzca por lo menos las 2/3 parte del volumen de la ampolla ; para
sellar la ampolla calentamos el capilar y lo doblamos. Esperamos que seque y lo
volvemos a pesar.
Luego de los 10 minutos de ebullición del agua cerramos el tubo de vaporización
vacío con el tapón lo más rápido posible y anotamos el volumen que descendió en
la bureta, luego sacamos el tapón y vemos como nuevamente regresa a su volumen
inicial.
Luego rompemos el capilar la ampolla e introducimos al tuvo cerrando lo más rápido
con el tapón (evitando alguna fuga) notamos que el volumen de la bureta desciende
lo cual debemos de acompañar el descenso con la pera haciendo que la distancia del
agua que contiene estos dos estén al mismo nivel. Cuando el líquido ya no desciende
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 10
Laboratorio de Fisicoquímica / Gases
este va a ascender la cual debemos de cerrar la llave de la bureta con el fin de que el
agua no descienda y anotamos el volumen indicado.
Luego de unos 15 minutos anotamos la temperatura de la pera.
b) DETERMINACIÓN DE LA CAPACIDAD CALORÍFICA (CP Y CV) POR EL
MÉTODO DE CLEMENT Y DESORMES.
Armamos el equipo como en la (fig. 4-B)
Todas las conexiones deben de estar bien unidas.
Para usar el inflador abrimos la seguridad para que así el gas pueda ingresar al balón
en la cual antes de iniciar debemos de tapar el tubo que se encuentra en la parte
externa del equipo para que el gas no se escape.
Inflamos hasta que la diferencia de alturas del manómetro tenga aproximadamente
10cm (h1), luego sacamos el dedo por un momento para después tapar en el momento
del primer cruce.
Esperamos que se estabilice durante 5 minutos y anotamos la altura (h2)
Este procedimiento se va a hacer con diferencias de alturas de 15,20 y 25cm.
Fig. 4-A (imagen izquierda) Equipo para la determinación de la densidad de
gases por el método de Victor Meyer.
Fig.4-B (imagen derecha) equipo para hallar la relación de capacidades
caloríficas por el método de Clement y Desormes.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 11
Laboratorio de Fisicoquímica / Gases
5. TABLA DE DATOS Y RESULTADO DE
EXPERIMENTACION
Condiciones de laboratorio
Tabla 1
Presión barométrica 754.4 mmHg
Humedad relativa 96 %
Temperatura 19.5°C
Determinación de la Densidad de Gases por el Método de Víctor Meyer
Tabla 2 (datos de la ampolla)
Masa de la ampolla Masa del
Masa de la ampolla
con cloroformo cloroformo
0.5584g 0.6364g 0.078g
Tabla 3 (volúmenes obtenidos en la bureta)
Volumen del
Volumen inicial Volumen
cloroformo Temperatura
de la bureta final de la
(volumen del proceso
(referencia) bureta
desplazado)
21.1mL 7.2mL 13.9mL 24 °C
Tabla 4 (datos obtenidos mediante el cálculo)
Presión barométrica corregida (P’) 𝟕𝟑𝟕. 𝟒 𝒎𝒎𝑯𝒈
Volumen corregido a CN 𝟏𝟐. 𝟒𝟎𝒎𝑳
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 12
Laboratorio de Fisicoquímica / Gases
𝐠
Densidad teórica del CHCl3 a CN 𝟓, 𝟔𝟔
𝐋
𝐠
Densidad experimental del CHCl3 a CN 𝟔. 𝟐𝟗
𝐋
Relación de Capacidades Caloríficas por el método de Clement y Desormes
Tabla 5
Diferencias de alturas 𝐡𝟏
h1 h2 𝛄=
iniciales aproximadas 𝐡𝟏 − 𝐡𝟐
10cm 10.8cm 3.6cm 1.5
15cm 14.6cm 3.8cm 1.4
20cm 21.6cm 5.4cm 1.3
25cm 23.5cm 6.7cm 1.4
6. CÁLCULO
Densidad de gases
a) Se necesita corregir la presión atmosférica o barométrica usando la siguiente formula,
ya que la humedad del ambiente afecta la presión atmosférica:
𝑃𝑏` = 𝑃𝑏 − 𝐹
Dónde:
𝑃𝑏 , 𝑃𝑏 `: Presión barométrica y presión barométrica corregida.
𝐹 : Presión de vapor del agua a temperatura ambiente.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 13
Laboratorio de Fisicoquímica / Gases
La presión de vapor del agua a 19.5 oC es 17.017 mmHg.
𝑃𝑏` = 754.4 𝑚𝑚𝐻𝑔 − 17.017 𝑚𝑚𝐻𝑔
𝑷𝒃` = 𝟕𝟑𝟕. 𝟒 𝒎𝒎𝑯𝒈
b) Corrija el volumen del aire desplazado a condiciones normales (CN), 0°C y 1 atm.
Ahora se necesita corregir el volumen de aire desplazado a condiciones normales, con
la ecuación de gases para una misma masa:
𝑷𝒃`. 𝑽𝒅𝒆𝒔𝒑𝒍𝒂𝒛𝒂𝒅𝒐 𝑷(𝑪𝑵). 𝑽(𝑪𝑵)
=
𝑻 𝒑𝒓𝒐𝒄𝒆𝒔𝒐 𝑻(𝑪𝑵)
Podemos hacer esto para cada volumen con su respectiva temperatura de proceso,
pero lo haremos con el volumen desplazado promedio y la temperatura del proceso
promedio. (V desplazado =13.9mL, T proceso = 24 oC=297 K)
737.4 𝑚𝑚𝐻𝑔 × 13.9 𝑚𝐿 760𝑚𝑚𝐻𝑔 × 𝑉(𝐶𝑁)
=
297𝐾 273𝐾
𝑽(𝑪𝑵) = 𝟏𝟐. 𝟒𝟎𝒎𝑳
c) Determine la densidad teórica del vapor a condiciones normales, usando la ecuación
de Berthelot.
9. 𝑇𝑐. 𝑃 6. 𝑇𝑐 2
𝑃. 𝑉 = 𝑛. 𝑇. 𝑅. [1 + (1 − )]
128. 𝑃𝑐. 𝑇 𝑇2
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 14
Laboratorio de Fisicoquímica / Gases
𝑚 9. 𝑇𝑐. 𝑃 6. 𝑇𝑐 2
𝑃. 𝑉 = ( ) . 𝑇. 𝑅. [1 + (1 − )]
𝑀 128. 𝑃𝑐. 𝑇 𝑇2
𝑚 9. 𝑇𝑐. 𝑃 6. 𝑇𝑐 2
𝑃. 𝑀 = ( ) . 𝑇. 𝑅. [1 + (1 − )]
𝑉 128. 𝑃𝑐. 𝑇 𝑇2
9. 𝑇𝑐. 𝑃 6. 𝑇𝑐 2
𝑃. 𝑀 = (ρ). 𝑇. 𝑅. [1 + (1 − )]
128. 𝑃𝑐. 𝑇 𝑇2
Despejando la densidad obtenemos:
𝑃. 𝑀
ρ=
9. 𝑇𝑐. 𝑃 6. 𝑇𝑐 2
𝑇. 𝑅. [1 + 128. 𝑃𝑐. 𝑇 (1 − )]
𝑇2
Dónde:
M: peso molecular de la muestra
m: masa de la muestra
R: Constante de los gases ideales
P, V, T: presión, volumen y temperatura del gas
Pc, Tc: presión y temperatura critica del gas
ρ: Densidad teórica del gas
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 15
Laboratorio de Fisicoquímica / Gases
Los vapores de sustancias que no son gases a temperaturas ordinarias suelen
encontrarse en este tipo. Hallando la densidad teórica a CN del vapor de la muestra
(cloroformo, CHCl3).
𝑔
1 𝑎𝑡𝑚 × 119.39
𝑃= 𝑚𝑜𝑙
𝑎𝑡𝑚 × 𝐿 9 × 536.4 𝐾 × 1 𝑎𝑡𝑚 6(536.4𝐾)2
273 𝐾 × 0.082 × [1 + (1 − )]
𝑚𝑜𝑙 × 𝑘 128 × 53.79 𝑎𝑡𝑚 × 273 𝐾 (273 𝐾)2
𝐠
𝛒 = 𝟓, 𝟔𝟔
𝐋
d) Determine la densidad experimental del vapor a CN, dividiendo la masa entre el
volumen corregido.
Como vamos a determinar la densidad experimental a condiciones normales tomamos
la masa y el volumen experimental corregido a C.N.
m
ρ=
V (C. N)
0,078g
ρ=
12.40mL
g
ρ = 6.29 × 10−3 .
mL
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 16
Laboratorio de Fisicoquímica / Gases
𝐠
𝛒 = 𝟔. 𝟐𝟗
𝐋
Determinamos el error experimental:
valor teórico − valor experimental
% error = x 100%
valor teórico
5,65 − 6.29
% error = | | x 100%
5,65
% 𝐞𝐫𝐫𝐨𝐫 = 𝟏𝟏. 𝟑𝟐 %
Relación de Capacidades Caloríficas
a) Determine la relación de capacidades caloríficas para cada altura inicial.
Cp 10.8 cm
γ= = 10.8cm−3.6 cm = 1,5
Cv
Cp 14.6 cm
γ= = 14.6cm−3,6 cm = 1,4
Cv
Cp 21.6 cm
γ= = 21.6cm−5.4 cm = 1,3
Cv
Cp 23.5 cm
γ= = 23.5cm−6.7 cm = 1,4
Cv
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 17
Laboratorio de Fisicoquímica / Gases
b) Determine 𝛾 promedio para el gas.
1.5+1.4+1.3+1.4
𝛾𝑝𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = = 1.4
4
c) A partir del valor promedio de γ, calcularemos las Cp y Cv experimentales.
Tenemos que:
Cp
𝛾𝑝𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = = 1.4
Cv
Sabemos también que:
Cp – Cv = R
Hemos llegado a 2 ecuaciones con 2 variables, es posible calcular el valor de cada
variable.
Cp =1.4 x Cv ………. (1)
Cp – Cv = R ………. (2)
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 18
Laboratorio de Fisicoquímica / Gases
(1) en (2)
cal
(1.4 x Cv) – Cv = 1.987 mol .K
cal
0.4 × Cv = 1.987 mol .K
𝐜𝐚𝐥
Cv = 4.968 𝐦𝐨𝐥 .𝐊
𝐜𝐚𝐥
Por ende, entonces: Cp = 6.955
𝐦𝐨𝐥 .𝐊
Hemos hallado la capacidad calorífica a presión constante por mol de aire y también
la capacidad calorífica a volumen constante por mol de aire. Estos son los valores
experimentales.
No olvidemos que la capacidad calorífica es el calor específico multiplicado por una
masa por lo tanto tiene unidades de calor/ temperatura y calor especifico tiene
unidades de calor/temperatura masa, entonces los Cp y Cv son calores específicos del
aire a presión y volumen contante.
Determinamos el error experimental:
valor real − valor experimental
% error = | | x 100%
valor real
Para 𝛾 su valor es aproximadamente 1,40 a la temperatura ambiental
1,40 − 1.40
% error = | | x 100% = 0 %
1,40
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 19
Laboratorio de Fisicoquímica / Gases
7. ANÁLISIS Y DISCUSIÓN DE RESULTADOS
El Método de Víctor Meyer es un mecanismo que nos permitió conocer ciertos resultados
como el volumen desplazado que se logró al medir en la bureta el volumen de aire que es
desplazado por el vapor de dicha muestra (cloroformo) a condiciones de presión y
temperaturas conocidas y la masa del cloroformo (0.078g) con los cuales se obtuvo la
densidad experimental (6.29 g/L), de esta forma se comparó con la densidad teórica
(5.66g/L) hallando el error de 11.32%.
Respecto al experimento relacionado a las capacidades caloríficas, pese a la simpleza del
método de Desormes, los resultados obtenidos experimentalmente con este método
corresponden muy bien a los datos teóricos (considerando al aire, que está compuesto en un
78% por Nitrógeno y 21 % de oxígeno, en estas condiciones como un gas ideal diatómico)
A diferentes medidas de alturas iniciales (15, 20, 25,30cm) como referencia se determinó
respectivas alturas posteriores, de tal manera que la relación Y se presentó prácticamente
constante para todos estos casos:
Cp
𝛾𝑝𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = = 1.4
Cv
El coeficiente adiabático teórico es de 1.4 hallando un error de 0%
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 20
Laboratorio de Fisicoquímica / Gases
8. CONCLUSIONES
Al efectuar varias veces el experimento de Clement y Desormes pudimos ver la
tendencia de un gas real a un valor aproximado al ideal para la relación calorífica.
La relación entre Cp y Cv, depende si el gas es mono, di o poliatómico, y dicha
relación es llamada coeficiente de dilatación adiabática ( γ).
El volumen descendió en la bureta invertida debido a la presión que el gas ejerce,
debe ir acompañado del descenso paralelo de la pera de decantación para así poder
obtener el volumen más exacto.
La ecuación de Berthelot suele usarse para los vapores de sustancias que no son
gases a temperaturas ordinarias, como por ejemplo la temperatura ambiental(19.5 oC
a 25 oC)
Los gases reales presentan desviación de la idealidad, expresada en el factor de
compresión Z, además existen diferentes ecuaciones de estado de los gases, una con
mayor exactitud que otras (Dieterici, Virial, Van Der Walls, etc.)
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 21
Laboratorio de Fisicoquímica / Gases
9. RECOMENDACIONES
Verificar que nuestro sistema no tenga ninguna fuga de gas.
Al volatilizar la sustancia problema, asegurarse de colocarlo rápido al tubo de
vaporización y taparlo bien para evitar pérdidas y errores.
Al finalizar el experimento de densidad de gases, destapar el tubo de vaporización y
luego abrir la llave de la bureta, para así no dañar el sistema.
Ser precisos en las mediciones de la diferencia de altura para evitar errores de
experimentación grandes.
10. BIBLIOGRAFÍA
Atkins P.W., “Fisicoquímica” , 2da ed. , Ed. Addison Wesley , Iberoamericana,
México, 1988
MARON Y PRUTTON, "Fundamentos de FISICOQUÍMICA", Editorial: Noriega –
Limusa, México, D.F., 1990 Páginas: 237-238,239-243, 245.252-253.
SHOEMAKER, DAVID P. y GARLAND, CARL W.Experimentos de
Fisicoquímica. 1ª edición en español – 1968 Editorial Hispanoamericano, Pág. 60-85.
Maron S., Lando J., “Fisicoquímica fundamental”, 1ra ed., Ed. Limusa , México,
1978.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 22
Laboratorio de Fisicoquímica / Gases
11. APÉNDICE
CUESTIONARIO
1. En qué consiste el método de Regnault para la determinación de los pesos moleculares
de las sustancias gaseosas.
Este método se usa para determinar los pesos moleculares de las sustancias gaseosas a la
temperatura ambiente y se realiza así: Un matraz de vidrio de unos 300 a 500 c.c. de
capacidad, provisto de llave, se evacúa y pesa, llenándolo a continuación con el gas cuyo
peso molecular se busca a una temperatura y presión, procediendo a pesarlo de nuevo. La
diferencia de pesos representa el del gas W en el matraz cuyo volumen se determina
llenándolo y pesándolo con agua o mercurio, cuyas densidades se conocen. Con los datos así
obtenidos, se deduce el peso molecular buscado mediante la ecuación:
𝜌𝑅𝑇
𝑀=
𝑃
En un trabajo preciso se usa un bulbo más grande para llenarlo y otro de contrapeso, y se
corrigen las mediciones reduciéndolas al vacío.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 23
Laboratorio de Fisicoquímica / Gases
2. Describe por lo menos dos métodos experimentales por la determinación de pesos
moleculares de gases.
Determinación experimental de masas moleculares de gases
En este método se busca determinar la masa molecular del gas y su densidad utilizando para
ello un experimento sencillo, realizando mediciones de volúmenes de masas conocidas del
gas a temperatura y presión constante. Utilizamos para las mediciones una probeta de un litro
graduada cada 10 ml, una balanza digital con una sensibilidad de 0.01 g y un encendedor
como fuente de butano.
Llenamos la probeta con agua y la colocamos invertida dentro de un recipiente con agua,
como se muestra en la figura. Es importante cuidar que no entre aire a la probeta al invertirla.
Se pesa entonces el encendedor antes de utilizar y una vez armado el dispositivo, se lo coloca
debajo de la probeta invertida dejando salir el gas dentro de la misma.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 24
Laboratorio de Fisicoquímica / Gases
Se mide el volumen de agua desplazada por el gas, teniendo cuidado de que el nivel de agua
de la probeta coincida con el del recipiente exterior, para asegurarnos que la presión dentro
de ella sea la misma que la atmosférica. Obtenemos así el dato de volumen del gas (Vgas).
Secamos bien el encendedor y lo volvemos a pesar, para que por diferencia podamos calcular
la masa de gas liberado dentro de la probeta (mgas).
Es importante también realizar varias mediciones de la masa del encendedor tanto antes de
sumergirlo en el recipiente como después de secarlo (antes de comenzar el experimento), de
modo de poder estimar el error de medición de mgas debido al agua que pudiera quedar
retenida dentro del encendedor.
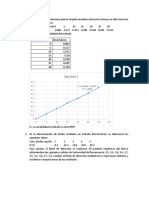
Luego de medir varios volúmenes de gas para varias masas del mismo, graficamos mgas vs
Vgas según:
Donde mgas es la diferencia de peso del encendedor lleno y luego de liberar el gas, Vgas el
volumen de agua desplazada por el butano, T es la temperatura ambiente en grados Kelvin,
R es la constante universal de los gases, Mgas la masa molecular del gas que se desea calcular
y P es la presión absoluta del gas, la cual debe corregirse del siguiente modo:
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 25
Laboratorio de Fisicoquímica / Gases
Siendo la presión de vapor del agua a la temperatura de trabajo, dato que se obtiene de tablas.
Determinación de masas moleculares por el método de Efusión de Gases
El montaje usado se muestra en la figura, consta de un tubo de efusión, cerrado en su parte
superior mediante un tapón atravesado por un conducto provisto de dos llaves, la primera de
las cuales permite la entrada de gas, y la segunda la salida de los mismos del tubo de efusión
hacia el tubo (provisto de una lámina de platino, con un pequeño orificio), o hacia el capilar,
según la disposición de la llave.
Entonces se disponen las llaves a y b en la posición 2 de la fig. 2 y el aire escapa a través del
orificio de la lámina de platino. Con un cronómetro se mide el tiempo necesario para que el
nivel del agua suba, desde la marca inferior A hasta la superior B, en el tubo de efusión.
3. Indique las características principales de una isoterma de gases reales.
Tienen una forma más compleja que las isotermas de un gas ideal (hipérbolas), ya que debe
dar cuenta de los cambios de fase que puede experimentar.
En la figura inferior se han representado las denominadas isotermas de Andrews. Dichas
isotermas fueron medidas experimentalmente, y representan la presión en función del
volumen a distintas temperaturas.La isoterma representada en rojo se denomina isoterma
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 26
Laboratorio de Fisicoquímica / Gases
crítica (y su temperatura, la temperatura crítica). Esta isoterma separa dos comportamientos:
cuando una sustancia se encuentra a una temperatura superior a su temperatura crítica,
siempre está en estado gaseoso, por muy alta que sea la presión. Por el contrario, cuando está
a una temperatura inferior a la crítica, puede estar en estado sólido, líquido o vapor (en la
gráfica se han representado solamente las zonas de líquido y vapor). Los puntos
representados con las letras A y B corresponden respectivamente a los estados denominados
vapor saturado y líquido saturado. Ambos están sobre una curva (representada en línea
punteada) denominada curva de saturación. Por debajo de ella, todos los estados son una
mezcla de líquido y vapor. En la figura también se observa que la zona de las isotermas que
se encuentra por debajo de la curva de saturación es una recta horizontal. Por tanto, cuando
el cambio de fase líquido - vapor se produce a presión constante, se produce también a
temperatura constante. Para que una sustancia cambie de fase, es necesario suministrarle o
extraerle una cierta cantidad de calor. Si el cambio de fase se produce a presión constante,
este calor no se traduce en un incremento de temperatura, y se denomina calor latente
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 27
Laboratorio de Fisicoquímica / Gases
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS 28
S-ar putea să vă placă și
- Ejercicios HidroDocument4 paginiEjercicios HidroAlvaro Barrera100% (6)
- Informe 12 Valoracion de Un Alcali Vs Un AcidoDocument6 paginiInforme 12 Valoracion de Un Alcali Vs Un AcidoCindy Villacis0% (2)
- Serie 2Document4 paginiSerie 2Andrea NeftaliÎncă nu există evaluări
- Lípidos y JabonesDocument15 paginiLípidos y Jabonesfernando hectorÎncă nu există evaluări
- Campos Magneticos RotatoriosDocument10 paginiCampos Magneticos RotatoriosasdjeÎncă nu există evaluări
- Descripcion y Funcionamiento AltDocument14 paginiDescripcion y Funcionamiento Altpfmex2011Încă nu există evaluări
- FileDocument33 paginiFileALEJANDRO PALOMINO FIGUEROA0% (1)
- Reporte 2-Daniel Chavez Micha - Grupo 6Document3 paginiReporte 2-Daniel Chavez Micha - Grupo 6DANIEL CHAVEZ MICHAÎncă nu există evaluări
- Equilibrio de Solubilidad, Ejercicios Resueltos2016Document19 paginiEquilibrio de Solubilidad, Ejercicios Resueltos2016holaÎncă nu există evaluări
- Presentacion Volumetria de Formacion de Complejos 1 PDFDocument29 paginiPresentacion Volumetria de Formacion de Complejos 1 PDFArielÎncă nu există evaluări
- Determinacion de Cloruros Por Los Metodos de Mohr Fajans y Volhard PDFDocument10 paginiDeterminacion de Cloruros Por Los Metodos de Mohr Fajans y Volhard PDFvaleriaÎncă nu există evaluări
- PRÁCTICA 14 ColorimetríaDocument6 paginiPRÁCTICA 14 ColorimetríaPablo SensoÎncă nu există evaluări
- Informe Uv Vis DicromatoDocument10 paginiInforme Uv Vis DicromatoOmar ArciaÎncă nu există evaluări
- Informe PotenciometriaDocument20 paginiInforme PotenciometriaJeison Palma ArzuagaÎncă nu există evaluări
- Informe Analítica #2 Hidrólisis de SalesDocument10 paginiInforme Analítica #2 Hidrólisis de SalesDavid GarciaÎncă nu există evaluări
- ArticuloDocument2 paginiArticuloDavid Mera Loboa100% (1)
- Lab 3 Análisis Cualitativo de AnionesDocument10 paginiLab 3 Análisis Cualitativo de AnionesRoger Ronaldo Montero CoronaciónÎncă nu există evaluări
- Cálculos Utilizados en Química AnaliticaDocument20 paginiCálculos Utilizados en Química AnaliticaGenaro IlacedoÎncă nu există evaluări
- Evaluacion de Datos Analiticos - 2018Document15 paginiEvaluacion de Datos Analiticos - 2018keila suarezÎncă nu există evaluări
- CA y MG en Leche (P.carmona)Document12 paginiCA y MG en Leche (P.carmona)Pablo C. VicencioÎncă nu există evaluări
- Demostracion de Las Leyes Fotometricas y Error Relativo de La ConcentracionDocument10 paginiDemostracion de Las Leyes Fotometricas y Error Relativo de La ConcentracionAraceliZavalaÎncă nu există evaluări
- Aplicaciones Acido-BaseDocument4 paginiAplicaciones Acido-BaseRosmeri DelgadoÎncă nu există evaluări
- Prueba de TollensDocument3 paginiPrueba de Tollenscristian lopezÎncă nu există evaluări
- YodometriaDocument8 paginiYodometriaSthefanía Elizabeth TisalemaÎncă nu există evaluări
- Experiment oDocument9 paginiExperiment ogiselxÎncă nu există evaluări
- Determinacion Del Peso Molecular de Un Vapor Condensable Por Los Metodos de Dumas y de Victor MeyerDocument11 paginiDeterminacion Del Peso Molecular de Un Vapor Condensable Por Los Metodos de Dumas y de Victor MeyerSEBASTIAN ALZATE ALZATEÎncă nu există evaluări
- Análisis Gravimétrico Por Volatilización: Determinación Del Contenido de Humedad de Una Muestra SólidaDocument9 paginiAnálisis Gravimétrico Por Volatilización: Determinación Del Contenido de Humedad de Una Muestra SólidaLuis David Mendoza PalaciosÎncă nu există evaluări
- Aplicaciones de La Titulación de Neutralización Acido-BaseDocument8 paginiAplicaciones de La Titulación de Neutralización Acido-BaseJosselyn Remache100% (1)
- Estudio de La Influencia de La Concentración Del Ion Hidronio en La Velocidad de Reacción Del Magnesio Con Los Ácidos HCL y H2so4 WuuuDocument17 paginiEstudio de La Influencia de La Concentración Del Ion Hidronio en La Velocidad de Reacción Del Magnesio Con Los Ácidos HCL y H2so4 WuuuwillaimÎncă nu există evaluări
- 5) Determinación de La Acidez Total Del VinagreDocument4 pagini5) Determinación de La Acidez Total Del VinagreJocelyn LópezÎncă nu există evaluări
- Naranja de Metilo Azul VictoriaDocument3 paginiNaranja de Metilo Azul VictoriaDaniel KStillo100% (1)
- Titulaciones ArgentométricasDocument4 paginiTitulaciones Argentométricasnata fallaÎncă nu există evaluări
- Practica Carbonilos y Nitrosilos Miriam M.Document6 paginiPractica Carbonilos y Nitrosilos Miriam M.Darwin MollinedoÎncă nu există evaluări
- Sulfato de Hexaacuacromo (III) y Potasio HexahidratadoDocument5 paginiSulfato de Hexaacuacromo (III) y Potasio HexahidratadoAnaly RodriguezÎncă nu există evaluări
- Aqi (L) 02 2021-I UnmsmDocument20 paginiAqi (L) 02 2021-I UnmsmPIERO LEONARDO TOMASTO CRISTOBALÎncă nu există evaluări
- Informe 5 ANALITICADocument11 paginiInforme 5 ANALITICAWalter Salazar SandiÎncă nu există evaluări
- Metodologia Determinación de Acidez Total Por PotenciometriaDocument4 paginiMetodologia Determinación de Acidez Total Por PotenciometriaEd José BuenoÎncă nu există evaluări
- Informe Analitica 3Document10 paginiInforme Analitica 3Gisell HuapayaÎncă nu există evaluări
- Practica N 6 Electroquimica UNMSMDocument20 paginiPractica N 6 Electroquimica UNMSMAnthony Ruiz ChavezÎncă nu există evaluări
- Practica 7 Determinación de Entalpías de Reacción y de SoluciónDocument13 paginiPractica 7 Determinación de Entalpías de Reacción y de SoluciónMariana SorianoÎncă nu există evaluări
- Practica de Laboratorio 7 Fisicoquimica IDocument13 paginiPractica de Laboratorio 7 Fisicoquimica Ieylen OviedoÎncă nu există evaluări
- Efecto Del Solvente en Espectroscopia Uv FINAL FinalDocument19 paginiEfecto Del Solvente en Espectroscopia Uv FINAL FinalValentina Jaramillo RiveraÎncă nu există evaluări
- Informe (Determinacion de Acidez)Document6 paginiInforme (Determinacion de Acidez)Juan Jose Vasquez SalazarÎncă nu există evaluări
- Practica No. 3 Titulacion PotenciometricDocument3 paginiPractica No. 3 Titulacion Potenciometricsussel badayÎncă nu există evaluări
- Reporte TitulacionDocument14 paginiReporte TitulacionFanny SantiÎncă nu există evaluări
- Cifras Significativas Angie Sa Udo PDFDocument6 paginiCifras Significativas Angie Sa Udo PDFmire3001Încă nu există evaluări
- Informe Capacidad Calorific A de Un SolidoDocument13 paginiInforme Capacidad Calorific A de Un SolidoAngélica María Castañeda RivasÎncă nu există evaluări
- PRACTICA Nº1 TDLDocument3 paginiPRACTICA Nº1 TDLAngela FernandezÎncă nu există evaluări
- Transposiciones y Efectos de Grupos VecinosDocument26 paginiTransposiciones y Efectos de Grupos VecinosDoloritasÎncă nu există evaluări
- INFORME Tecnicas CromatograficasDocument4 paginiINFORME Tecnicas CromatograficasAlejandra PlazasÎncă nu există evaluări
- Tema 3 Problemas 20 21 Acido BaseDocument4 paginiTema 3 Problemas 20 21 Acido BaseCHOLOSIMEONEÎncă nu există evaluări
- Quimica de Soluciones AcuosasDocument8 paginiQuimica de Soluciones AcuosasLuis Jose RodriguezÎncă nu există evaluări
- Equilibrio Químico 2Document10 paginiEquilibrio Químico 2Natasha ArcosÎncă nu există evaluări
- Ejercicio 1y 2 de CurvasDocument2 paginiEjercicio 1y 2 de CurvasNatasha VargasÎncă nu există evaluări
- Determinación Del PKa Del Azul de BromotimolDocument4 paginiDeterminación Del PKa Del Azul de BromotimoldanielÎncă nu există evaluări
- Informe Sales de DiazonioDocument2 paginiInforme Sales de DiazonioJUNIOR99-1100% (1)
- Titulación de HCL y NaOhDocument7 paginiTitulación de HCL y NaOhCiinThiia Lopez33% (3)
- Determinacion de Alcoholes y FenolesDocument5 paginiDeterminacion de Alcoholes y Fenolessara peresÎncă nu există evaluări
- 2 Prueba de SaponificacionDocument4 pagini2 Prueba de SaponificacionAlberto CristobalÎncă nu există evaluări
- Universidad Nacional Autónoma de Huanta: InformeDocument8 paginiUniversidad Nacional Autónoma de Huanta: InformeRutman TorresÎncă nu există evaluări
- LaboratorioDocument3 paginiLaboratorioBRIGITH STHEFANIA BENITES GARCIAÎncă nu există evaluări
- Marcha Sistematica de Cationes 1Document1 paginăMarcha Sistematica de Cationes 1Tahic PÎncă nu există evaluări
- SEMINARIODocument7 paginiSEMINARIOAlbert FernandezÎncă nu există evaluări
- Informe I - GASESDocument25 paginiInforme I - GASESSandra Nancy Ccama MamaniÎncă nu există evaluări
- Informe Laboratorio 1Document22 paginiInforme Laboratorio 1gabrielÎncă nu există evaluări
- Laboratorio FIQUI 13Document4 paginiLaboratorio FIQUI 13fernando hectorÎncă nu există evaluări
- TERMOQUIMICADocument24 paginiTERMOQUIMICAfernando hectorÎncă nu există evaluări
- WARDER - ProblemasDocument1 paginăWARDER - Problemasfernando hectorÎncă nu există evaluări
- Movimiento Rectilíneo Uniforme (MRU) y Sistema de ReferenciaDocument5 paginiMovimiento Rectilíneo Uniforme (MRU) y Sistema de ReferenciaLeidyÎncă nu există evaluări
- Dinámica - ResueltosDocument5 paginiDinámica - ResueltosWilder Montenegro100% (1)
- Informe 2 Concentración de MineralesDocument27 paginiInforme 2 Concentración de MineralesSebastián RiffoÎncă nu există evaluări
- Actividad 3 BiomecánicaDocument6 paginiActividad 3 BiomecánicaCarolina UrreaÎncă nu există evaluări
- Guia 1 Medicion de Resistencias 1Document12 paginiGuia 1 Medicion de Resistencias 1liÎncă nu există evaluări
- Diseño Hidraulico de Canal - CAIDA VERTICAL - v3Document9 paginiDiseño Hidraulico de Canal - CAIDA VERTICAL - v3Robert DeckerÎncă nu există evaluări
- Laboratorio TecnoDocument15 paginiLaboratorio TecnoEllis Vasquez MarquezÎncă nu există evaluări
- Valvulas Exp-Elec PDFDocument10 paginiValvulas Exp-Elec PDFjesus david franco barriosÎncă nu există evaluări
- Probl Inversores 1415Document4 paginiProbl Inversores 1415boris carballoÎncă nu există evaluări
- Introducción A La Termodinámica 2 2022Document34 paginiIntroducción A La Termodinámica 2 2022MILORT MARK EUDIS TABEL MEJIAÎncă nu există evaluări
- Tarea2 - Alexander MancipeDocument11 paginiTarea2 - Alexander MancipeSebastian Morales CuncanchunÎncă nu există evaluări
- Problemas (18) corriente-resistencia-Ohm-KirchhoffDocument3 paginiProblemas (18) corriente-resistencia-Ohm-KirchhoffPedro Valdeiglesias CarbajalÎncă nu există evaluări
- Laboratorio ReynoldsDocument10 paginiLaboratorio ReynoldsLeonardo Garcia EspitiaÎncă nu există evaluări
- Examen de Termodinamica. Virtual. Año 2021.Document2 paginiExamen de Termodinamica. Virtual. Año 2021.Miguel Angel R DominguezÎncă nu există evaluări
- Semana 02a PDFDocument14 paginiSemana 02a PDFdanielÎncă nu există evaluări
- Viscosidad D-45Document4 paginiViscosidad D-45daniel perniaÎncă nu există evaluări
- Reporte Práctica 2 Mecanica de FluidosDocument8 paginiReporte Práctica 2 Mecanica de FluidosJesús Kevin Zarate FloresÎncă nu există evaluări
- Elementos de Control de Circuitos ElectricosDocument30 paginiElementos de Control de Circuitos ElectricosDeivy Azaña Montañez100% (1)
- Ondas Estacionarias UMSSDocument12 paginiOndas Estacionarias UMSSAmador Arana100% (1)
- Anteproyecto Laboratorio de FisicaDocument9 paginiAnteproyecto Laboratorio de FisicaJAQUELINE CECILIA SANCHEZ VAZQUEZÎncă nu există evaluări
- Cuaderno de Informes S1Document13 paginiCuaderno de Informes S1Aron AFÎncă nu există evaluări
- Prácticas, U3. EA2024.Document3 paginiPrácticas, U3. EA2024.ANA PATRICIA ALEMAN DURONÎncă nu există evaluări
- INFORME 11 de Labo de Fisica 3Document23 paginiINFORME 11 de Labo de Fisica 3luis100% (2)
- Cliente Direccion Cruz de Vasquez, Altagracia Idalia C E Araujo No 1119 Bo LourdesDocument1 paginăCliente Direccion Cruz de Vasquez, Altagracia Idalia C E Araujo No 1119 Bo LourdesSamuel Granados MejíaÎncă nu există evaluări
- GuiaCompleta 71021017 2023Document20 paginiGuiaCompleta 71021017 2023Jorge HernandezÎncă nu există evaluări
- SEGUNDO Ranking Fisica II y TrigonometriaDocument5 paginiSEGUNDO Ranking Fisica II y Trigonometriavictor huayhua choqueticoÎncă nu există evaluări