Documente Academic
Documente Profesional
Documente Cultură
Laboratorio
Încărcat de
Anonymous kcTJSDyTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Laboratorio
Încărcat de
Anonymous kcTJSDyDrepturi de autor:
Formate disponibile
UNIVERSIDAD NACIONAL DE TRUJILLO
REDUCCIÓN DE O-NITRO ANILINA CON Fe Y HCl A
O-FENILENDIAMINA
OBJETIVOS:
Obtención de o-fenilendiamina a partir de la reducción de o-nitroanilina con
HCl y Fe.
Estudio y comparación de la reacción a temperaturas y tiempos diferentes,
obteniendo las variables óptimas ya mencionados, para el proceso de
reducción.
1. INTRODUCCIÓN:
La reducción de nitrocompuestos a aminas es un paso esencial en lo
que quizá sea la vía de síntesis más importante en la química aromática.
Los nitrocompuestos aromáticos tienen pocos usos directos; sin embargo, las
aminas aromáticas resultantes de la reducción de dichos nitrocompuestos se
pueden convertir en una amplia gama de productos con aplicaciones tan
diversas como: colorantes, productos farmacéuticos, materias primas para la
formación de diversos grupos funcionales [1].
Los nitrocompuestos pueden reducirse de dos maneras generales: por
hidrogenación catalítica, y por reducción química vía la transferencia de
hidrógeno proveniente de un donador adecuado. Al comparar la reducción
catalítica utilizando hidrógeno molecular con la reducción química vía
transferencia de donador de hidrógeno, esta última tiene varias ventajas
como el evitar el uso de gases inflamables y la mayor quimioselección que
puede obtenerse en las reacciones [2,5].
PROCESOS INDUSTRIALES ORGÁNICOS II 1
UNIVERSIDAD NACIONAL DE TRUJILLO
2. FUNDAMENTO TEÓRICO:
2.1. Hidrogenación:
La hidrogenación es un tipo de reacción química (redox) cuyo resultado
final visible es la adición de hidrógeno (H2) a otro compuesto. Los objetivos
habituales de esta reacción son compuestos orgánicos insaturados,
como alquenos, alquinos, cetonas, nitrilos, y aminas. La mayoría de las
hidrogenaciones se producen mediante la adición directa de hidrógeno
diatómico bajo presión y en presencia de un catalizador. Un ejemplo típico de
hidrogenación es la adición de hidrógeno a los dobles enlaces, convirtiendo
los alquenos en alcanos. La hidrogenación tiene importantes aplicaciones en
la industria farmacéutica, petroquímica y alimentaria [4].
2.1.1. Hidrógeno molecular:
El hidrógeno molecular (H2) es un gas con efectos antioxidantes muy
particulares y selectivos. Funciona principalmente al mejorar el estado redox
de la célula cuando es necesario [9].
El hidrógeno es la molécula más pequeña del universo y por esa razón tiene
gran biodisponibilidad. También es neutral, por lo que puede penetrar
fácilmente cualquier espacio de las membranas de su cuerpo [9].
El H2 solo es competitivo como reductor en hidrometalurgia (reducciones en
medio acuoso) en factorías donde la generación de H 2 por ejemplo para la
síntesis de amoniaco se realiza a muy bajo costo [10].
También se debe hacer una ligera mención a la producción de H 2 como gas
licuado pues es importante en criogenia y en el estudio de la
superconductividad dado que su punto de fusión está cercano al cero
absoluto (-259.2 ºC) [10].
APLICACIONES DEL HIDRÓGENO MOLECULAR
I. Reducción de nitrocompuestos.
Al igual que muchas otras sustancias orgánicas, los nitrocompuestos
pueden reducirse de dos maneras generales: (a) por hidrogenación catalítica
usando hidrógeno molecular, o (b) por reducción química, habitualmente con
un metal y un ácido [11].
La hidrogenación de un nitrocompuesto a amina procede suavemente
cuando se agita una solución del nitrocompuesto en alcohol con níquel o
platino finamente divididos en una atmósfera de hidrógeno. Por ejemplo [11].
PROCESOS INDUSTRIALES ORGÁNICOS II 2
UNIVERSIDAD NACIONAL DE TRUJILLO
Fig. Nº1: Reducción de o-Nitroacetanilida por
hidrogenación catalítica, Fuente: QUÍMICA
ORGÁNICA, Thornton-Neilson.
Este método no puede emplearse cuando la molécula contiene algún otro
grupo fácilmente hidrogenable, como un doble enlace carbono-carbono
[11].
II. Obtención de hidrácidos.
Los hidrácidos también llamados ácidos hidrácidos o hidruros no metálicos
son combinaciones binarias entre hidrógeno junto a los halógenos (F, Cl, Br, I)
exceptuando el At (Ástato) y con los anfígenos (S, Se, Te) exceptuando el O,
los primeros actúan con valencia (-1) y los segundos actúan con valencia (-2).
Estos compuestos presentan carácter ácido en disolución acuosa [12].
El ácido bromhídrico puede obtenerse de la mezcla directa de hidrógeno y
bromo en un reactor lleno con agua [13].
H2 (g) + Br2 (g) 2HBr (g)
[10]
A medida que se forma el HBr se va disolviendo en el agua; esta puede
arrastrarlo en las destilaciones, por lo que puede extraerse disoluciones con
diferentes concentraciones [13].
Las reacciones de terminación se hacen más importantes cuando menores son
las concentraciones de H2 y Br2 [10].
Con otros halógenos la reactividad desciende a lo largo del grupo, así pues, con
F es explosiva incluso a bajas temperaturas, con el Cl lenta en la oscuridad y
catalizada por la luz y con el I esta termodinámicamente poco favorecida [10].
H2 (g) + F2 (g) 2HF (g)
H2 (g) + Cl 2 (g) 2HCl (g)
H2 (g) + I 2 (g) 2HI (g)
PROCESOS INDUSTRIALES ORGÁNICOS II 3
UNIVERSIDAD NACIONAL DE TRUJILLO
III. Obtención de amoniaco.
El uso del H2 de forma comercial más importante está vinculado con la fijación
del nitrógeno, un conjunto de procesos por el cual, el N2 se capta de la
atmósfera y se transforma en amoniaco, que a su vez es reactivo de partida
para la síntesis de otros compuestos de interés comercial [10].
3H2 (g) + N2 (g) 3 NH3 (g)
[10]
IV. Obtención de metanol.
En la producción de metanol, uno de los compuestos que se obtienen en
mayor cantidad a escala de planta pues es importante en diversos usos como
aditivo en las gasolinas sin plomo, como precursor de otros compuestos
orgánicos (metanal, ácido acético...) y la síntesis de plásticos y fibras, la
reacción entre el H2 y el CO tiene lugar a altas presiones (25300 kPa) y
temperaturas (600 ºC)) con la presencia de catalizadores como el Al 2O3.
Modificando el catalizador se pueden conseguir reacciones más suaves (300
ºC, con un catalizador Cu/Zn) [10].
2H2 (g) + CO (g) CH3OH (g) ; ΔH = 149.7KJ
[10]
V. Reducción de enlaces dobles Carbono=Carbono.
Otro uso del H2 es la hidrogenación de compuestos orgánicos insaturados.
El H2 se utiliza como un agente reductor de los enlaces dobles del carbono C=C
formando aceites saturados y grasas [10].
Los ácidos grasos insaturados son hidrogenados con H2 utilizando metales
finamente divididos como Ni, Pd o Pt como catalizadores. La adición de H2 a los
dobles enlaces posibilita que aceites, que son líquidos a temperatura ambiente,
se conviertan en grasas sólidas lo que aumenta su valor comercial [10].
[10]
El mecanismo de adición al doble enlace pasa por la disociación homolítica
(radicales libre) del H2 sobre la superficie del catalizador [10].
PROCESOS INDUSTRIALES ORGÁNICOS II 4
UNIVERSIDAD NACIONAL DE TRUJILLO
2.1.2. Hidrógeno naciente:
Hidrógeno atómico (o hidrógeno naciente) consiste en
un átomo individual de hidrógeno , el cual no se encuentra junto a otro
átomo como en las moléculas normales de hidrógeno. La especie es
denominada H (atómico), en contraste con el usual H2 (dihidrógeno o
sólo 'hidrógeno') que comúnmente interviene en reacciones químicas
.Se dice que existe de forma transitoria, pero lo suficiente como para
afectar a las reacciones químicas. De acuerdo con esto, el hidrógeno
naciente está generalmente in situ, normalmente en reacciones
de zinc con un ácido, aluminio con sódico, o por electrólisis en
el cátodo. Siendo monoatómico, los átomos de hidrógeno son agentes
reductores mucho más reactivos y efectivos que el H2, pero de nuevo
la clave es si los átomos de H existen bajo las condiciones requeridas.
El concepto es más popular en ingeniería y en catálisis [4].
2.2. Métodos para obtención de aminocompuestos:
2.2.1. Reducción de nitrocompuestos:
Comprende la transformación (reducción) del grupo nitro (-NO2) en el
grupo amino (-NH2).
La reducción de compuestos aromáticos nitrados es el proceso de
mayor importancia industrial.
[H]
Ar-NO2 ----------> Ar-NH2
Implica la sustitución de los oxígenos del grupo nitro por átomos de
hidrógeno [3].
2.2.1.1. Reacción característica:
2.2.1.2. Agentes de proceso:
Sin el uso de reactores de alta presión (a presión
atmosférica) y sin el uso de catalizadores, los agentes
de reducción comunes son: Hierro y ácido, Zinc y álcali,
Sulfuro de sodio o polisulfuro de sodio, Sulfito ácido de
sodio, Hidrógeno electrolítico, Hidruros metálicos
Hidrógeno naciente- Preparado IN SITU.
Hidrógeno gaseoso (molecular) en presencia de un
metal (que actúa como catalizador) como Ni, Sn, Pt.
Hidrógeno producido por cracking de amoniaco [3].
PROCESOS INDUSTRIALES ORGÁNICOS II 5
UNIVERSIDAD NACIONAL DE TRUJILLO
2.2.1.3. Reducción de nitroderivados con metales en medio ácido:
Las reducciones metal-ácido son las más enérgicas y
únicamente dan como producto final las aminas [3].
2.2.1.3.1. Reducción con Fe y HCl:
2.2.1.3.2. Reducción con SnCl2 y HCl:
2.2.1.3.3. Reducción con Fe y CH3COOH:
Cuando hay que evitar la hidrólisis de grupos presentes
en el compuesto a reducir [3].
CH3COOH
2.2.1.4. Reducción de nitroderivados con metales en medio
jjjjjjjjjjjjjjjbásico:
2.2.1.4.1. Medio básico fuerte:
Se emplea zinc en solución alcalina (NaOH o KOH).
PROCESOS INDUSTRIALES ORGÁNICOS II 6
UNIVERSIDAD NACIONAL DE TRUJILLO
Se desean obtener productos de reducción diferentes a
la anilina [3].
Hidrazobenceno
2.2.1.4.2. Medio básico débil:
Se emplea zinc en polvo en solución acuosa de CaCl2.
El producto de la reducción del nitrobenceno es la
fenilhidroxilamina [3].
NO2 + Zn
2.2.2. Hidromonólisis:
Comprende la sustitución de grupos como el –SO3H, -OH, -Cl, por el
grupo –NH2 [3].
PROCESOS INDUSTRIALES ORGÁNICOS II 7
UNIVERSIDAD NACIONAL DE TRUJILLO
2.2.3. Reducción de nitrilos:
Comprende la transformación del grupo ciano (-CN) en el grupo amino
(- NH2) por acción de un agente reductor [3].
H2 / Ni
R-C≡N -------------> R-CH2-NH2
LiAlH4 / H2O
2.2.4. Hidrólisis de amidas N-sustituidas:
2.2.5. Por transposición intramolecular:
NH2-
CH3OH
3. MÉTODOS PARA CARACTERIZACION DE UN AMINODERIVADO:
Durante los dos últimos siglos, los químicos han desarrollado varias
formas de identificar compuestos y determinar sus estructuras. Algunas de
estas técnicas son antiguas, pero siguen siendo útiles; probar el punto de un
compuesto de fusión, por ejemplo, todavía es un paso clave en la
caracterización de la misma. Otras técnicas, como la resonancia magnética
nuclear (RMN), son más recientes y ahora se han vuelto indispensables [6].
3.1. PRUEBAS QUÍMICAS:
Dependiendo de su estructura, unos compuestos generalmente
reaccionan con algunos reactivos, pero no con otros. Un tipo particular de
compuesto llamado un aldehído, por ejemplo, reaccionará con una sustancia
química llamada reactivo de Jones mientras que otro tipo de compuesto
llamado una cetona no lo hará. En consecuencia, puede utilizar las pruebas
químicas, tales como la adición de reactivos o pruebas de solubilidad Jones,
para ayudarle a averiguar qué tipo de compuesto que tiene. Las pruebas
químicas son también muy útiles para la detección de la presencia o ausencia
de compuestos específicos en una mezcla [6].
Algunas de las pruebas químicas empleadas para la caracterización
de los aminocompuestos son:
PROCESOS INDUSTRIALES ORGÁNICOS II 8
UNIVERSIDAD NACIONAL DE TRUJILLO
3.1.1 CLORURO DE BENCENOSULFONILO (MÉTODO DE
HINSBERG PARA CARACTERIZAR AMINAS PRIMARIAS,
SECUNDARIAS Y TERCIARIAS)
A 0,3 ml o 300 mg de la muestra desconocida en un tubo de ensayo,
agregue 5 ml de solución de hidróxido de sodio al 10% y 0,4 ml de cloruro de
bencenosulfonilo. Se tapa el tubo de ensayo y se agita la mezcla muy
vigorosamente. Se prueba la solución para asegurarse de que sea alcalina.
Después de que haya reaccionado todo el cloruro de bencenosulfonilo, se
enfría la solución y se procede a separar el residuo, si está presente, de la
solución. Se prueba el residuo para la solubilidad en ácido clorhídrico al 10%.
Si no queda ningún residuo, entonces se trata la solución con ácido
clorhídrico al 10% y se observa si se forma un precipitado. Si todo el
compuesto original se disuelve en la base, no queda ningún residuo y la
acidificación produce un precipitado, la incógnita original es una amina
primaria [14].
Las aminas primarias reaccionan con el cloruro de bencenosulfonilo
en solución básica para formar la sal sódica de la sulfonamida, que
normalmente es soluble en solución básica, pero la sulfonamida precipita al
acidificarse. Si se forma un residuo y es insoluble en ácido, la incógnita
PROCESOS INDUSTRIALES ORGÁNICOS II 9
UNIVERSIDAD NACIONAL DE TRUJILLO
original es una amina secundaria. Las aminas secundarias experimentan una
reacción con cloruro de bencenosulfonilo para precipitar la sulfonamida, y la
acidificación no produce ningún cambio. Si está presente un residuo que es
soluble en ácido, indica que el residuo es la amina terciaria sin reaccionar.
Las aminas terciarias experimentan reacción con cloruro de bencenosulfonilo
para producir sales de sulfonato de amonio cuaternario, que producen
sulfonatos de sodio y aminas terciarias insolubles en agua en solución básica.
La acidificación de la mezcla de reacción da como resultado la formación de
ácidos sulfónicos y sales de aminas solubles en agua. Cualquier sólido que
se forme debe aislarse y clasificarse, y su punto de fusión debe compararse
con la amina original. Si la cantidad del sólido es suficiente, se puede guardar
y usar como un derivado para ese desconocido [14].
3.1.2 COPULACIÓN
Se agrega 2 ml de la solución fría de diazonio a una solución de 0,1 g
de 2-naftol en 2 ml de solución de hidróxido de sodio al 10% y 5 ml de agua.
La formación del colorante rojo anaranjado, con la evolución del gas solo al
calentarse indica que el compuesto original es una amina aromática primaria
[14].
PROCESOS INDUSTRIALES ORGÁNICOS II 10
UNIVERSIDAD NACIONAL DE TRUJILLO
3.1.3 REACCIÓN NITROSA DE LIEBENNANN
Se agrega 0,05 g de N-nitrosoamina, 0,05 g de fenol y 2 ml de ácido
sulfúrico concentrado a un tubo de ensayo y caliente suavemente durante 20
segundos. Se enfría la solución ligeramente. Debe desarrollarse un color
azul, que cambia a rojo cuando la solución se vierte en 20 ml de agua con
hielo. Se agrega un 10% de hidróxido de sodio hasta que la mezcla sea
alcalina y vuelva a producirse el color azul. La N-nitrosoamina libera ácido
nitroso en presencia de ácido sulfúrico. El ácido nitroso se somete a reacción
con fenol para producir el 4-nitrosofenol amarillo (quinona monoxime). El
color azul observado en esta reacción se debe al fenolindofenol formado a
partir de la reacción del 4-nitrosofenol (quinona monoxime) producido
inicialmente con el exceso de fenol. Esta reacción es característica de los
fenoles en los que una posición oriho o para no está sustituida. Para realizar
una prueba comparativa con el fin de verificar los colores, se puede realizar
el siguiente procedimiento. Agregando un cristal de nitrito de sodio a 2 ml de
ácido sulfúrico concentrado y agite hasta que se disuelva. Se añade 0,1 g de
fenol, y aparecerá un color azul. La solución se vierte en 20 ml de agua con
hielo y el color de la solución cambia a rojo. La adición de hidróxido de sodio
al 10%, hasta que la mezcla sea alcalina, da como resultado el retorno del
color azul [14].
PROCESOS INDUSTRIALES ORGÁNICOS II 11
UNIVERSIDAD NACIONAL DE TRUJILLO
3.2 PUNTO DE FUSIÓN:
Prueba de puntos de fusión es directa, y porque el punto de fusión es
una característica de un compuesto dado, puede servir como un medio de
identificación. Desafortunadamente, muchos compuestos tienen puntos de
fusión similares [6].
Particularmente del aminocompuesto en discusión (o-fenilendiamina), su
punto de fusión está en el rango de 100-103ºC, por lo tanto si se somete a
fusión el producto obtenido y se observa que empieza a fundirse entre el
intervalo de temperatura mencionado anteriormente, se puede determinar
que el compuesto incógnito es la o-fenilendiamina [6].
3.3 ESPECTROSCOPÍA INFRARROJA (IR):
Los compuestos orgánicos que absorben la luz infrarroja en longitudes
de onda determinadas por sus estructuras. Con la aprobación de la luz IR a
través de una muestra para ver qué longitudes de onda que absorbe, se
puede determinar qué tipo de compuesto que tiene sin utilizar pruebas
químicas. La espectroscopia de masas es otra técnica de gran alcance que
determina el peso molecular de un compuesto por ionizante entonces probar
cómo se comporta en un campo eléctrico y magnético [6].
En el caso del compuesto sintetizado, existen tres bandas que permiten esta
identificación:
El anillo bencénico, presenta una banda intensa en el rango
1500-1600 cm-1 .
La sustitución del anillo bencénico, en este caso orto, posee una
banda intensa entre el rango 800 – 700 cm-1 .
El grupo funcional amino posee una banda simétrica y asimétrica
en el rango 3400-3300 cm-1 ,además de bandas muy agudas en
1600 cm-1 y 1500 cm-1.
3.4 ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA
NUCLEAR:
La RMN es el más joven y más valioso de estas técnicas. Un
espectrómetro de RMN medidas que las frecuencias de las ondas de radio
son absorbidas por una muestra en presencia de un campo magnético
externo. A partir de esta información, se puede determinar la estructura de
PROCESOS INDUSTRIALES ORGÁNICOS II 12
UNIVERSIDAD NACIONAL DE TRUJILLO
un compuesto sin la necesidad de pruebas químicas y preparación de
derivados [6].
En el caso del compuesto sintetizado, de realizarse el espectro, debe
tener las siguientes bandas de absorción:
Se identifica el anillo bencénico por la presencia de bandas en el
rango de 100-160 ppm. Se suelen presentar como bandas
agrupadas.
Se identifica el grupo amino por la presencia de una banda en el
rango de 40-70 ppm.
Cabe recalcar que en este tipo de espectroscopía se suelen desplazar
los rangos, por lo que esta visión puede ser afectada.
UTILIDAD DE LA O-FENILENDIAMINA:
Es un compuesto orgánico con la fórmula C6H4(NH2)2. Su diamina
aromática es un importante precursor de muchos compuestos heterocíclicos.
Es isómero con m-fenilendiamina y p-fenilendiamina [7].
La o-fenilendiamina se condensa con cetonas y aldehídos para dar lugar a
una variedad de productos útiles. Las reacciones con ácidos carboxílicos y
sus derivados producen bencimidazoles. El herbicida benomil se prepara de
esta manera. Además, la quinoxalinediona se puede preparar por
condensación de o-fenilendiamina con oxalato de dimetilo. La condensación
con ésteres de xantato proporciona mercaptoimidazoles, que se utilizan
como antioxidantes en productos de caucho. El tratamiento con ácido nitroso
da benzotriazol, un inhibidor de la corrosión. La condensación de o-
fenilendiamina sustituida con varias dicetonas se usa en la preparación de
una variedad de productos farmacéuticos [7].
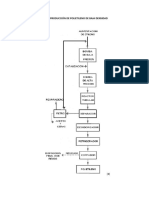
4. PRODUCTO SECUNDARIO: MAGNETITA Y SUS APLICACIONES:
La magnetita (o piedra imán) es un mineral de hierro constituido por
óxido ferroso-diférrico (Fe2+ Fe3+ 2O4) [8].
La magnetita es un mineral opaco de color negro grisáceo o negro hierro y
brillo metálico. Es frágil, tiene una dureza entre 5,5 y 6,5 en la escala de Mohs
y una densidad de 5,175 g/cm3. Es muy soluble en ácido clorhídrico
concentrado [8].
Junto con la hematita es una de las menas más importantes, al contener un
72 % de hierro2 (es el mineral con más contenido en hierro) [8].
Como material de construcción se usa como añadido natural de alta densidad
(4,65 hasta 4,80 kg/l) en hormigones, especialmente para protección
radiológica. Otra aplicación es en calderas industriales, dado que la magnetita
PROCESOS INDUSTRIALES ORGÁNICOS II 13
UNIVERSIDAD NACIONAL DE TRUJILLO
es un compuesto muy estable a altas temperaturas, si bien a temperaturas
bajas o en presencia de aire húmedo se oxide lentamente y forme óxido
férrico. Su estabilidad a elevadas temperaturas hace que sea un buen
protector del interior de los tubos de calderas. Por este motivo se hacen
tratamientos químicos en las calderas industriales con el fin de formar en el
interior de los tubos capas continuas de magnetita [8].
5. MATERIALES Y MÉTODOS:
6.1. Materia Prima
Se utilizó como materia prima 27.5 g de o-nitro anilina, proporcionado en
Laboratorio de Procesos.
6.2. Reactivos:
22.4 g de fierro, proporcionado en laboratorio.
289 mL de HCl 0.9596 N. adquirido en laboratorio. (reflujo)
166.2 mL de HCl 1.0030 N. adquirido en laboratorio.
1.0 g de NaOH, adquirido en laboratorio.
4 L de agua destilada.
Fenolftaleína, adquirido en laboratorio.
6.3. Equipos y Materiales:
Los equipos y materiales empleados, en general, a lo largo de todo el proceso
experimental, son:
1 balón de 300 mL con 2 bocas, Kymax.
1 condensador recto con 2 bocas esmeriladas, Pyrex.
2 cocinas eléctricas.
2 termómetros de mercurio, Boeco, de -10 a 360 ° C.
1 balanza electrónica, Sartorius, con una capacidad máxima de 410 g y + 0.01
g de precisión.
1 probeta de 100 mL, Pyrex.
4 vasos de precipitación (3 Pyrex, 1 Kyntel) de 250 mL
1 bureta, Pyrex, de 25 mL.
1 matraz Erlenmeyer, Pyrex, de 250 mL
1 embudo de 5 cm de diámetro con vástago de plástico.
1 fiola, Pyrex, de 100 mL.
1 pinza de metal.
1 espátula de metal.
1 piseta.
PROCESOS INDUSTRIALES ORGÁNICOS II 14
UNIVERSIDAD NACIONAL DE TRUJILLO
1 gotero de plástico de 5 mL.
3 varilla de vidrio, Pyrex, con punta paleta.
Soportes de metal.
2 pinzas de metal.
1 gotero de plástico de 5 mL.
1 tapón.
Los equipos y materiales que se emplearon para su específico procedimiento
experimental, son:
6.3.1. Para la preparación de solución de NaOH:
1 fiola, Pyrex, de 100 mL.
1 balanza electrónica, Sartorius, con una capacidad máxima de
410 g y + 0.01 g de precisión.
1 espátula de metal.
1 piseta.
6.3.2. Para la valoración de HCl:
1 bureta, Pyrex, de 25 mL.
1 soporte de metal.
1 pinza de metal.
1 matraz Erlenmeyer, Pyrex, de 250 mL.
1 embudo de 5 cm de diámetro con vástago de plástico.
1 gotero de plástico de 5 mL.
6.3.3. Para la reducción de o-nitro anilina con agitación:
1 balón de 300 mL con 3 bocas, Kymax.
3 cocinas eléctricas.
1 soporte de metal.
2 pinzas de metal.
1 tubo de seguridad de presión, Pyrex.
1 probeta de 100 mL, Pyrex.
2 termómetros de mercurio, Boeco, de -10 a 360 ° C.
3 varilla de vidrio, Pyrex, con punta paleta.
1 balanza electrónica, Sartorius, con una capacidad máxima de
410 g y + 0.01 g de precisión.
1 espátula de metal.
1 embudo de 5 cm de diámetro con vástago, Pyrex.
6.3.4. Para la reducción a reflujo de o-nitro anilina:
1 balón de 300 mL con 2 bocas esmerilada, Pyrex.
1 condensador recto con 2 bocas esmeriladas, Pyrex.
1 cocina eléctrica.
PROCESOS INDUSTRIALES ORGÁNICOS II 15
UNIVERSIDAD NACIONAL DE TRUJILLO
2 mangueras.
1 termómetro de mercurio Boeco de -10 a 360 °C.
1 balanza electrónica, Sartorius, con una capacidad máxima de
410 g y + 0.01 g de precisión.
1 soporte de metal.
2 pinzas de metal.
1 probeta de 100 mL, Pyrex.
1 espátula de metal.
1 tapón
Vaselina
6.3.5. Para la separación de productos:
1 cocina eléctrica.
1 rejilla de asbesto.
4 vasos de precipitación (3 Pyrex, 1 Kyntel) de 250 mL.
1 balanza electrónica, Sartorius, con una capacidad máxima de
410 g y + 0.01 g de precisión.
2 pinzas de metal.
1 embudo de 5 cm de diámetro con vástago, Pyrex.
15 papeles filtro de 12x12 cm2.
1 piseta.
6.4. Procedimiento experimental:
6.4.1. Para reducción de o-nitro anilina a 50, 70 y 90 oC a 1.5 horas:
Se instaló el balón de tres bocas en su respectivo soporte.
Se situó la cocina eléctrica debajo del balón.
Se colocó el termómetro en otra boquilla del balón.
Se pesó e introdujo 3.45 g de o-nitro anilina y 2.8 g de fierro, con
ayuda de una espátula de metal, en el balón.
Se agregó 55.4 mL de HCl 1.0030 N en el balón.
Se encendió la cocina eléctrica, iniciando el proceso de reducción
a la temperatura de 90ºC, con una agitación manual constante de
los reactivos.
Se apagó y retiró la cocina, después de que el proceso haya durado
1.5 h.
Simultáneamente, mientras se realizaba una agitación constante
en el balón, en dos vasos de precipitación Pyrex, se introdujo 3.45
g o-nitro anilina, 2.8 fierro y 55.4 mL HCl en cada vaso.
Se procedió a calentar los reactivos depositados en los vasos de
precipitación, poniéndolos en contacto con las otras dos cocinas
eléctricas.
PROCESOS INDUSTRIALES ORGÁNICOS II 16
UNIVERSIDAD NACIONAL DE TRUJILLO
Uno de los vasos se mantuvo con agitación constante a la
temperatura de 50 ºC, el segundo vaso de precipitación, se
mantuvo a 70 ºC.
Se apagó y retiro la cocina, después de haber transcurrido 1.5 h.
6.4.2. Para la reducción a reflujo de o-nitro anilina a 102°C con un
tiempo de 1.5, 2.5 y 3.5 h :
Se instaló el balón de dos bocas y el condensador en sus
respectivos soportes.
Se colocó las manguerillas en el condensador tipo recto; teniendo
en cuenta que el flujo de agua fría que va a recorrer por el
condensador debe estar en contracorriente respecto al flujo de
vapor.
Se colocó el termómetro en una de las boquillas del balón.
Se pesó e introdujo 3.45 g de o-nitro anilina y 2.8 g de fierro, con
ayuda de una espátula de metal, en el balón.
Se agregó 57.8 mL de HCl 0.9596 N de la misma manera que
agregamos los anteriores reactivos.
Se situó la cocina eléctrica debajo del balón.
Se encendió la cocina eléctrica, iniciando el proceso de reducción
a sus respectivas temperaturas, con una agitación manual
constante.
Se apagó y retiró la cocina, después de que el proceso haya durado
1.5 h y 2.5 y 3.5 h.
6.4.3. Para la separación de productos:
Se colocó el papel filtro en un embudo, asimismo éste en un vaso
de precipitación.
Se filtró en caliente, es decir, justo después de haber reteridado el
balón y los vasos de precipitación de la cocina eléctrica.
El proceso de filtración, se realizó tres veces por, ensayo, teniendo
en cuenta que la fenilendiamina es soluble en agua, mientras que
la magnetita, no lo es.
Debido a la filtración se logró separar la fase sólida (magnetita y
FeCl3) de la fase líquida (o-fenilendiamina y agua).
PROCESOS INDUSTRIALES ORGÁNICOS II 17
UNIVERSIDAD NACIONAL DE TRUJILLO
Posteriormente haciendo uso de una bandeja y de cubos de hielo
se procedió a cristalizar, la fase líquida, obteniendo así cristales de
o-fenilendiamina, en agua líquida.
Se logró cristalizar la o-fenilendiamina, para posteriormente volver
a filtrarla, separándola así del agua líquida, obteniendo una mejor
separación y purificación del producto.
7. RESULTADOS:
Reacción de reducción
NO2 NH2
NH2 NH2
2 Fe(s) 6 HCl (l) 2 FeCl3 (s) 2 H2O (l) (a)
o-nitroanilina Fierro Ácido clorhídrico o-fenilendiamina Tricloruro Agua
De fierro
PROCESOS INDUSTRIALES ORGÁNICOS II 18
UNIVERSIDAD NACIONAL DE TRUJILLO
Cuadro N°01: Obtención de o-fenilendiamina a partir de la reducción de
ssssssssssssssao-nitroanilina con Fe y HCl, variando la temperatura y tiempo de
aaaaaaaaaaaaaareacción:
Temperatura (°C) 50 70 90 102
tiempo (h) 1.5 1.5 1.5 1.5 2.5 3.5
o-nitroanilina (g) 3.45 3.45 3.45 3.45 3.45 3.45
Reactantes Fierro (g) 2.8 2.8 2.8 2.8 2.8 2.8
57.8 (0.9596 N)
55.4 (1.0030 N) 99.81 % de igualdad a la
HCl, (mL)
cantidad de HCl usada
anteriormente.
Productos
o-fenilendiamina (g) 0.0 0.14 1.82 0.4 0.41 0.45
principal
Producto
Magnetita (g) 3.79 1.65 2.25 0.2 0.8 0.76
secundario
Rendimientos o-fenilendiamina (%) 0.0 5.19 67.41 14.81 15.18 16.67
PROCESOS INDUSTRIALES ORGÁNICOS II 19
UNIVERSIDAD NACIONAL DE TRUJILLO
Gráfico 01: Temperatura vs rendimientos del producto principal
80
70
60
50
Rendimiento (%)
40
30
20
10
0
40 50 60 70 80 90 100 110
-10
Temperatura (ºC)
8. DISCUSIONES DE RESULTADOS:
Los resultados de la reacción de reducción de la o-nitroanilina en
presencia de Fe y HCl para la obtención de o-fenilendiamina, trabajando
a las temperaturas de 50, 70, 90 y 102 oC con un tiempo de 1.5 horas,
muestran que, cuando la reacción es llevada a cabo a 50 oC no es posible
obtener el producto deseado (o-fenilendiamina), en cambio se obtiene
únicamente productos secundarios como la magnetita; cuando se trabaja
a 70 oC la cantidad de producto obtenido es muy pequeña (0.14 g) en
comparación con el valor teórico que debería obtenerse(2.7g), teniendo
un bajo rendimiento de la reacción (5.19 %). Trabajando la reacción a 90
oC se consiguió la mayor cantidad de producto principal, siendo más
cercano al valor teórico establecido, esta cantidad es de 1.82 g de o-
fenilendiamina, con un rendimiento de 67.41 %.
Según la teoría, al trabajar a 102 oC, la cual es la temperatura de reflujo
para nuestra reacción, se debió tener los mejores rendimientos a
comparación de los experimentos anteriores, trabajados a menores
temperaturas, sin embargo, eso no fue del todo cierto, ya que, no se
obtuvo un rendimiento tan alto como el logrado al trabajar a 90 oC,
teniendo rendimientos de 14.81, 15.18 y 16.67% a 1.5, 2.5 y 3.5 horas,
respectivamente; sin embargo, se pudo notar que al incremento del
tiempo de reacción, el rendimiento va aumentando gradualmente.
PROCESOS INDUSTRIALES ORGÁNICOS II 20
UNIVERSIDAD NACIONAL DE TRUJILLO
9. CONCLUSIONES:
Se llega a la conclusión que, conforme se eleva la temperatura de la reacción
de reducción de o-nitroanilina con Fe y HCl a o-fenilendiamina, el rendimiento
aumenta gradualmente, pese a ello se demostró que, al pasar los 90oC, la
producción de magnetita es la que aumenta y la producción de o-
fenilendiamina disminuye, por ello se establece que la temperatura óptima de
reacción es a 90oC.
Al realizar las reacciones de reducción a reflujo, se demostró que existen
casos como el estudiado en el presente informe, que no cumplen con lo
establecido teóricamente, puesto que la temperatura de reflujo (102ºC) no
fue la más óptima para la reacción dada, pero al realizarla con diferentes
tiempos (1.5, 2.5 y 3.5 horas), se pudo verificar que, conforme aumenta el
tiempo de reacción, el rendimiento presenta un mayor incremento, por lo cual
se logra establecer que el tiempo óptimo para la reacción es de 3.5 horas.
10. RECOMENDACIONES:
Al momento de armar el equipo que se ha de utilizar en laboratorio, se debe
revisa que no existan fugas en el sistema.
En el transcurso de la reacción a reflujo, utilizar un correcto sistema de
refrigeración, para poder evitar la fuga de los vapores y así se logren
condensar.
Filtrar en caliente, aproximadamente, unas tres veces el producto obtenido
para obtener una mejor purificación de nuestro producto principal eliminado
en el filtrador la magnetita, la cual es una impureza.
Se puede realizar filtración al vacío para acelerar los procesos de purificación
por filtrado, debido a que el papel filtro suele quedar obstruido fácilmente por
partes sólidas.
PROCESOS INDUSTRIALES ORGÁNICOS II 21
UNIVERSIDAD NACIONAL DE TRUJILLO
11. REFERENCIAS BIBLIOGRÁFICAS:
1. Burke S.D., Danheiser R.L. Handbook of Reagents for Organic Synthesis Oxidizing
and Reducing Agents, Wiley, London, England, pp. 458-461, 1999.
2. Brieger G., Nestick T.J.Catalytic transfer hydrogenation. Chemí-calRevíews, 74.
pp. 567-580,1974
3. Entwistle, I. D.; Johnstone, R. A. W.; Povall, T. J., Reduction of nitro-compounds,
Journal of the Chemical Society, Perkin I, 443-444, 1977.
4. Mejía E. Aminación. [diapositivas] Perú: Slideshare; 2013. 136 diapositivas.
5. Rylander P.N. Hydrogenation Methods, Academic Press, New York, USA, pp. 365,
1985
6. Cusiritati. [Online].; 2012 [citado 2019 Marzo 01. Disponible en:
https://www.cusiritati.com/xBnwkMl3y/
7. Wikipedia. [Online].; 2017 [citado 2019 Febrero 04. Available from:
https://en.wikipedia.org/wiki/O-Phenylenediamine
8. Wikipedia. [Online].; 2015 [citado 2019 Febrero 04. Available from:
https://es.wikipedia.org/wiki/Magnetita
9. Dr.Mercola. Mercola Web site. [Online].; 2018 [citado13 Marzo 2019. Available
from: https://articulos.mercola.com/sitios/articulos/archivo/2018/10/21/beneficios-
del-hidrogeno-molecular.aspx.
10. Textos Científicos Web site. [Online].; 2006 [citado 2019 Marzo 11. Available from:
https://www.textoscientificos.com/quimica/hidrogeno/quimica-hidrogeno.
11. Thornton R, Neilson Boyd R. Química Orgánica. In Zugazagoitia Herranz R, Fiedler
P, editors. Química Orgánica. México: Fondo Educativo Interamericano, S.A. de
C.V.; 1985. p. 926-927.
12. Formulación Química formulación y nomenclatura online. Formulación Química
Web site. [Online].; 2018 [citado 2019 Marzo 13. Available from:
https://www.formulacionquimica.com/hidracidos/.
13. Bolívar G. lifeder Web site. [Online]. [citado 2019 Marzo 13. Available from:
https://www.lifeder.com/acido-bromhidrico/#Sintesis_de_halogenuros_de_alquilo.
14. SHRINER RL. The Systematic Identification of Organic Compounds. OCTAVA ed. New Jersey:
JOHN WILEY & SONS. INC.; 2004.
PROCESOS INDUSTRIALES ORGÁNICOS II 22
UNIVERSIDAD NACIONAL DE TRUJILLO
ANEXOS
PROCEDIMIENTOS COMPLEMENTARIOS A NUESTRA REACCIÓN DE
REDUCCIÓN:
1. Preparación de la solución de NaOH (0.14 N):
Se pesó 0.5 g de NaOH.
Se coloca los gramos de NaOH pesados dentro de una fiola de
100ml.
Se disolvió el NaOH en agua destilada aforándose a 100ml.
𝑾
𝑵(𝑵𝒂𝑶𝑯) =
𝑴 .𝒗
N= Normalidad de la solución de NaOH
W= Peso del NaOH en gramos
M= Masa molar del NaOH en gramos/moles
V= Volumen de la solución de NaOH en Litros
2. Para la valoración de HCl:
Se llenó la bureta de 25 ml con la solución de NaOH.
Se coloca 2 mL de HCl con normalidad desconocida en el
matraz Erlenmeyer.
Se colocó 3 gotas de fenolftaleína al matraz.
Se tituló la solución de HCl para determinarse su normalidad
hasta tornarse un color grosella.
Ley de dilución
N (NaOH) .V (NaOH) = N (HCl) .V (HCl)
N= Normalidad
V= Volúmenes en Ml
Ecuación empleada para obtener el porcentaje de concentración del HCl
𝑴. 𝑵
%(𝑯𝑪𝒍) =
⍴ . 𝟏𝟎
N= Normalidad de la solución de HCl en moles/Litros
M= Masa molar del HCl en gramos/moles
⍴= Densidad de HCl en gramos/mililitros
PROCESOS INDUSTRIALES ORGÁNICOS II 23
UNIVERSIDAD NACIONAL DE TRUJILLO
CÁLCULO ADICIONAL PA OBTENER RENDIMIENTOS
Se tomó referencia el rendimiento teórico, de la reacción (a), en la cual se
obtuvo un mol de o-fenilendiamina, cuyo peso molar es de 108 g, como las
cantidades de reactantes lo trabajamos utilizando su 40ava parte, la cantidad
de producto de o-fenilendiamina teórica cuando la conversión es del 100 %
tomando en cuenta el factor escala (dividirlo entre 40) debe ser de 2.7 g.
Por lo tanto, el rendimiento se obtiene de la siguiente fórmula:
𝑮𝒓𝒂𝒎𝒐𝒔 𝒓𝒆𝒂𝒍𝒆𝒔 𝒐𝒃𝒕𝒆𝒏𝒊𝒅𝒐𝒔
𝑹𝒆𝒏𝒅𝒊𝒎𝒊𝒆𝒏𝒕𝒐 = 𝒙 𝟏𝟎𝟎 %
𝑮𝒓𝒂𝒎𝒐𝒔 𝒕𝒆ó𝒓𝒊𝒄𝒐𝒔
ESPECTROS INFRAROJOS DE LOS GRUPOS FUNCIONALES
Los siguientes espectros permiten distinguir las distintas bandas
representativas del compuesto sintetizado.
La primera imagen muestra las bandas representativas del grupo
amino y del benceno.
Fig. Nº2: Espectro IR de la anilina
La siguiente imagen muestra la banda aguda esperada en la
sustitución del anillo bencénico en posición orto, ubicada entre 800-700 cm-1.
PROCESOS INDUSTRIALES ORGÁNICOS II 24
UNIVERSIDAD NACIONAL DE TRUJILLO
Fig. Nº3: Espectro IR de o-xileno
ESPECTRO DE RESONANCIA MAGNÉTICA NUCLEAR
La tabla que se muestra a continuación, muestra las diferentes áreas
de absorción para distintos tipos de carbono.
Fig. Nº4: Rangos del Espectro de Resonancia Magnética Nuclear
PROCESOS INDUSTRIALES ORGÁNICOS II 25
UNIVERSIDAD NACIONAL DE TRUJILLO
OBSERVACIONES:
Durante los dos primeros ensayos, se utilizó la destilación como método
de purificación de productos al considerarse el producto como líquido. Sin
embargo, la literatura menciona un producto sólido, por lo que el método
elegido fue incorrecto y al ser los residuos de dichos ensayos (2.5 h y 2
h) desechados, se realizó nuevamente el ensayo pertinente.
Al realizar los ensayos fallidos nuevamente, se observó que al dejar
reposar la solución obtenido se formaban pequeños cristales de producto,
por lo que se procedió a practicar la cristalización como método de
purificación.
Al ser bastante la cristalización, se procedió a realizar baños de hielo para
acelerar este proceso.
Se resalta la importancia de realizar filtrados en caliente para poder
eliminar las impurezas insolubles (en este caso la magnetita) y obtener
una mayor cantidad de producto.
PROCESOS INDUSTRIALES ORGÁNICOS II 26
S-ar putea să vă placă și
- Síntesis de productos químicos derivados de la biomasa empleando catálisis heterogénea: heterociclos de la biomasaDe la EverandSíntesis de productos químicos derivados de la biomasa empleando catálisis heterogénea: heterociclos de la biomasaÎncă nu există evaluări
- Practica 2 Benzoína Equipo 2Document15 paginiPractica 2 Benzoína Equipo 2Josue CarmonaÎncă nu există evaluări
- Anhidrido Maleico y Ácido MaleicoDocument13 paginiAnhidrido Maleico y Ácido MaleicoBenjamin López ChacaltanaÎncă nu există evaluări
- Estudio de Mercados para El Producto Ácido BenzóicoDocument38 paginiEstudio de Mercados para El Producto Ácido BenzóicoSebastián Velez Bedoya100% (1)
- Proceso de Obtención Del Ácido Acético DiapositivasDocument15 paginiProceso de Obtención Del Ácido Acético DiapositivasCarlos Ramon Vidal TovarÎncă nu există evaluări
- Clase 9 Fabricación de AmoniacoDocument20 paginiClase 9 Fabricación de AmoniacoFernando Renzo Alzamora CastilloÎncă nu există evaluări
- Obtencion Del BiodieselDocument9 paginiObtencion Del BiodieselWendyCondorcetJimenezÎncă nu există evaluări
- Quimica TrabajoDocument10 paginiQuimica Trabajoantonio juniorÎncă nu există evaluări
- Informe Exp2 Sintesis Medina-SolisDocument5 paginiInforme Exp2 Sintesis Medina-SolisSimón MedinaÎncă nu există evaluări
- Cinetica de DesorcionDocument5 paginiCinetica de DesorcionWilmar Andres Rodas CastroÎncă nu există evaluări
- Produccion Acido LacticoDocument4 paginiProduccion Acido LacticoLiliana Yaneth MenaÎncă nu există evaluări
- Diagrama de Produccion de AmoniacoDocument8 paginiDiagrama de Produccion de AmoniacoSoraya Ochoa VillamizarÎncă nu există evaluări
- Síntesis de Cloruro de EtiloDocument3 paginiSíntesis de Cloruro de EtiloNathalia F. Nariño AparicioÎncă nu există evaluări
- Practica 2 - Equipo 3Document13 paginiPractica 2 - Equipo 3Hazzel GutierrezÎncă nu există evaluări
- Ácido Meta-CloroperoxibenzoicoDocument2 paginiÁcido Meta-CloroperoxibenzoicoJorge Alberto Estrada TorresÎncă nu există evaluări
- Difusion en Medio PorosoDocument41 paginiDifusion en Medio PorosoMónica Porras RojasÎncă nu există evaluări
- Extraccion de La TrimiristinaDocument4 paginiExtraccion de La TrimiristinaMaria Alejandra Olarte CortesÎncă nu există evaluări
- Acilacion de Aminas y Sales de Diazonio Wade (Editado)Document16 paginiAcilacion de Aminas y Sales de Diazonio Wade (Editado)JeffersonPalaciosÎncă nu există evaluări
- Practica 1 BenzhidrolDocument22 paginiPractica 1 Benzhidrolmauricio ortegaÎncă nu există evaluări
- Exámen de III Unidad P.U.M - Sanchez Alfaro NestorDocument10 paginiExámen de III Unidad P.U.M - Sanchez Alfaro NestorNestor SanchezÎncă nu există evaluări
- Obtencion NH3Document17 paginiObtencion NH3DIANA DELACRUZZÎncă nu există evaluări
- BalanceDocument4 paginiBalanceandres9410Încă nu există evaluări
- Práctica 1 Química Orgánica 2semestreDocument5 paginiPráctica 1 Química Orgánica 2semestreDiana Katherine0% (1)
- Sintesis de Acetato de NDocument11 paginiSintesis de Acetato de NlÎncă nu există evaluări
- Producción de Acido NítricoDocument27 paginiProducción de Acido NítricoVictor Godos ChumaceroÎncă nu există evaluări
- Destilacion Destructiva F-1.Document8 paginiDestilacion Destructiva F-1.victor nuñezÎncă nu există evaluări
- Informe IIIDocument27 paginiInforme IIIPaulina PavicichÎncă nu există evaluări
- Examen-3 Materiales Ingeniería-2020Document2 paginiExamen-3 Materiales Ingeniería-2020LUIS DAVID ZAVALETA GUTIERREZÎncă nu există evaluări
- DFP Acido SulfuricoDocument24 paginiDFP Acido SulfuricoKimberly AndradeÎncă nu există evaluări
- PatenteDocument11 paginiPatentePedro JuanÎncă nu există evaluări
- Practicas 9 y 10Document3 paginiPracticas 9 y 10yimmo0% (2)
- Actividad 14Document13 paginiActividad 14LauraRosas100% (1)
- Informe 7 CompletoDocument15 paginiInforme 7 CompletoAnton Valve0% (1)
- PermanganometriaDocument7 paginiPermanganometriaJennifer MacaÎncă nu există evaluări
- Laboratorio de Aldehidos y Cetonas TerminadoDocument20 paginiLaboratorio de Aldehidos y Cetonas TerminadoAnonymous 28dbytÎncă nu există evaluări
- HIDROTRATAMIENTODocument8 paginiHIDROTRATAMIENTOedwardÎncă nu există evaluări
- Hudroxido de Sodio2 (Recuperado Automáticamente)Document84 paginiHudroxido de Sodio2 (Recuperado Automáticamente)Miguel Angel MontoyaÎncă nu există evaluări
- Informe de Destilacion Metodo Aurea y FibonacciDocument6 paginiInforme de Destilacion Metodo Aurea y FibonacciSteve Anthony Cortez PrincipeÎncă nu există evaluări
- Procesos Cataliticos IndustrialesDocument16 paginiProcesos Cataliticos IndustrialesIsmael PgÎncă nu există evaluări
- Coloracion de PropilenoDocument90 paginiColoracion de PropilenoFidelAlcantaraÎncă nu există evaluări
- AminasDocument9 paginiAminasSabadoGrisÎncă nu există evaluări
- Sintesis Del Acido CinamicoDocument2 paginiSintesis Del Acido Cinamicobea_scÎncă nu există evaluări
- Produccion y Obtencion Del Carbonato de Sodio en El PeruDocument14 paginiProduccion y Obtencion Del Carbonato de Sodio en El PeruLucerito Peredo BerlangaÎncă nu există evaluări
- Informe 12 Contenido de Azufre (Pila)Document6 paginiInforme 12 Contenido de Azufre (Pila)Tatiana Pila FonsecaÎncă nu există evaluări
- Formacion de SulfonamidasDocument4 paginiFormacion de SulfonamidasPaty Avendaño0% (1)
- Terminado NitracionDocument19 paginiTerminado NitracionANDERSSONÎncă nu există evaluări
- Zeolitas en Catalis PDFDocument13 paginiZeolitas en Catalis PDFLuis Niño0% (1)
- Produccion de Acetato de EtiloDocument8 paginiProduccion de Acetato de EtiloDavid Alendez QuispitupaÎncă nu există evaluări
- Obtencion Del Meta Nitro AnalinaDocument1 paginăObtencion Del Meta Nitro AnalinaVeronica Patiño Arancibia100% (1)
- Lou II-Laboratorio 3Document10 paginiLou II-Laboratorio 3victor hugo capchaÎncă nu există evaluări
- Planta de FenolDocument10 paginiPlanta de FenolkatepiÎncă nu există evaluări
- Azocolorantes 2Document75 paginiAzocolorantes 2Abraham L Álvarez100% (1)
- BallanceproDocument5 paginiBallanceproJohhn MendozÎncă nu există evaluări
- Sintesis de La Urea y AmoniacoDocument42 paginiSintesis de La Urea y AmoniacoSuárez KmiloÎncă nu există evaluări
- Procesos Quimicos Industriales Tercer ExamenDocument3 paginiProcesos Quimicos Industriales Tercer ExamenCristhianw QcÎncă nu există evaluări
- Obtencion de Poliacrilonitrilo TeoríaDocument11 paginiObtencion de Poliacrilonitrilo Teoríaprofesora1962Încă nu există evaluări
- Química Inorgánica Del AguaDocument6 paginiQuímica Inorgánica Del AguaMayra A Ramirez TÎncă nu există evaluări
- Funcion Quimica Hidrogenadas HidrurosDocument25 paginiFuncion Quimica Hidrogenadas HidrurosFernando MuñozÎncă nu există evaluări
- HidrogenacionDocument19 paginiHidrogenacionAdali Reyes JulcaÎncă nu există evaluări
- HidrogenoDocument5 paginiHidrogenoRosa CuchoÎncă nu există evaluări
- Al CanosDocument9 paginiAl Canosgeysell arely0% (1)
- Tabla Reactivos OrgánicaDocument8 paginiTabla Reactivos Orgánicajrb7590Încă nu există evaluări
- Grasas y AceitesDocument47 paginiGrasas y AceitesrosbilitaÎncă nu există evaluări
- S15 - S27 - CP14A - Qu Mica Org Nica - Material 2018 PDFDocument16 paginiS15 - S27 - CP14A - Qu Mica Org Nica - Material 2018 PDFDiego R. Cuellar CamachoÎncă nu există evaluări
- Evaluacin HidrocarburosDocument4 paginiEvaluacin HidrocarburosjairoÎncă nu există evaluări
- Reacciones de Compuestos Organicos AlcanDocument17 paginiReacciones de Compuestos Organicos AlcanJuanManuelAmaroLuisÎncă nu există evaluări
- Reacciones de Oxidacion Reduccion en Sintesis Organica4Document157 paginiReacciones de Oxidacion Reduccion en Sintesis Organica4Jairo BermúdezÎncă nu există evaluări
- Metodos de Obtención de AlquenosDocument12 paginiMetodos de Obtención de Alquenoseskereman100% (1)
- Modificadortes de Viscosidad - en.Es-CopiarDocument35 paginiModificadortes de Viscosidad - en.Es-CopiarJorge ZegarraÎncă nu există evaluări
- Perfil Obtencion de Hidrogeno A Partir de La Produccion de EtanolDocument9 paginiPerfil Obtencion de Hidrogeno A Partir de La Produccion de EtanolAnthony Pinto100% (1)
- Deber de Quimica - Semana 6Document8 paginiDeber de Quimica - Semana 6Victor DefazÎncă nu există evaluări
- Reacciones de AlquenosDocument18 paginiReacciones de AlquenosRoger ManzanarezÎncă nu există evaluări
- Trabajo Procesamiendo HidrocarburosDocument35 paginiTrabajo Procesamiendo Hidrocarburosluis machucaÎncă nu există evaluări
- Previo ObtenciondeAlquinos (Acetileno)Document12 paginiPrevio ObtenciondeAlquinos (Acetileno)Jimmy Daniel Balderas ContrerasÎncă nu există evaluări
- Actividad 10. Modelos de Reacciones ResueltaDocument2 paginiActividad 10. Modelos de Reacciones ResueltaCruz Martínez Jesúa SimríÎncă nu există evaluări
- Hidrogenizacion de Aceites y EnvasesDocument25 paginiHidrogenizacion de Aceites y EnvasesPaulo Da Cruz BravoÎncă nu există evaluări
- Tuxtla Gutiérrez Chiapas Marzo 2013Document122 paginiTuxtla Gutiérrez Chiapas Marzo 2013Lisandra Alvarez DiazÎncă nu există evaluări
- TAREA No.1 - B) - LIPIDOSDocument7 paginiTAREA No.1 - B) - LIPIDOSOz HdzÎncă nu există evaluări
- Estudio Comparativo de Las Propiedades Superficiales de Agregados Metálicos Soportados en AlúminaDocument178 paginiEstudio Comparativo de Las Propiedades Superficiales de Agregados Metálicos Soportados en AlúminaAngel Maroto ValienteÎncă nu există evaluări
- Cap-2 - 2 (Reacciones de Hidrocarburos) Def PDFDocument112 paginiCap-2 - 2 (Reacciones de Hidrocarburos) Def PDFAF'Tracks ™Încă nu există evaluări
- Presentacion TECNOLOGÍA DE GRASAS Y ACEITESDocument6 paginiPresentacion TECNOLOGÍA DE GRASAS Y ACEITESBen HarperÎncă nu există evaluări
- Reacciones Alcanos - Enos - InosDocument22 paginiReacciones Alcanos - Enos - InosGuillermo CúmezÎncă nu există evaluări
- AlquinosDocument46 paginiAlquinosCristina Tapia RamírezÎncă nu există evaluări
- 1.-Generalidades en Catálisis.Document65 pagini1.-Generalidades en Catálisis.Lucia PortugalÎncă nu există evaluări
- HalogenaciónDocument6 paginiHalogenaciónGisell QuijadaÎncă nu există evaluări
- Unidad 3 Hidrocarburos IIDocument22 paginiUnidad 3 Hidrocarburos IIGustavo ChoqueÎncă nu există evaluări
- Tarea 1 - Hidrocarburos AlifáticosDocument18 paginiTarea 1 - Hidrocarburos AlifáticosPeñaranda PaolaÎncă nu există evaluări
- Manual Lab Mod Mol Chem ComputeDocument86 paginiManual Lab Mod Mol Chem ComputeJudith FSÎncă nu există evaluări
- Aromaticidad TautomeriaDocument11 paginiAromaticidad TautomeriaceabymmbtÎncă nu există evaluări
- Anexo 1 Harold PaezDocument20 paginiAnexo 1 Harold PaezHarold Paez CastiblancoÎncă nu există evaluări