Documente Academic
Documente Profesional
Documente Cultură
Pie Diabetico
Încărcat de
Mirko PejerreyDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Pie Diabetico
Încărcat de
Mirko PejerreyDrepturi de autor:
Formate disponibile
FACULTAD DE CIENCIAS DE LA SALUD
ESCUELA DE MEDICINA HUMANA
CURSO : PATOLOGÍA
TEMA : PIE DIABÉTICO
ALUMNOS : CORTÉZ CUBAS KARELL LIZZETH
FERNÁNDEZ CAMPOS PAOLA
MONTEZA LÓPEZ EDINSON
PEJERREY PEJERREY MIRKO
SUÁREZ GÓMEZ AUGUSTO
TEZÉN ADANAQUE SAYURI
PROFESOR : DR. LIDO ZAMBRANO ACUÑA
SABADO, 11 DE MAYO DEL 2019
I. INTRODUCCIÓN
La Diabetes Mellitus ocupa el primer lugar entre las enfermedades crónicas
degenerativas, siendo el pie diabético una de las complicaciones más
frecuente e importante en estos pacientes, el cual se desarrollara con la
presencia de una ulcera en el pie o en la pierna durante el trascurso de su
enfermedad lo que le puede llevar a una amputación por muerte tisular del
mismo.
El pie diabético engloba un conjunto de síndromes en los que la presencia
de isquemia, neuropatía e infección van a generar lesiones tisulares o
úlceras debido a pequeños traumatismos, produciendo una importante
morbilidad que puede llegar a amputaciones; la mayoría de estos pacientes
presentan además enfermedad arterial periférica.
La neuropatía es una complicación microvascular que produce pérdida de
sensibilidad en el pie produciendo deformidades, presión anormal, heridas
y úlceras; estas últimas pueden ser prevenibles con una adecuada
estrategia que comprenda cribado, clasificación del riesgo y medidas
efectivas de prevención y tratamiento.
Del punto de vista histopatológico, en el pie diabético se encuentra la
presencia de respuesta inflamatoria como componente esencial de los
mecanismos de defensa ante la infección siendo hallada de manera de
infiltrado inflamatorio de predominio neutrofílico, con eosinófilos; así como
en el proceso de la cicatrización se aprecia ulceración y aspecto necrótico
de la epidermis y dermis.
Su alta incidencia, frecuente multicentricidad, la respuesta inflamatoria en
su génesis y la orientación diagnóstica y terapéutica, siguen siendo motivos
para su investigación. Por consiguiente el presente trabajo tiene como
finalidad dar a conocer acerca del pie diabético y sus complicaciones
desde un punto histopatológico, respuesta inmunológica y variantes
histológicas.
II. OBJETIVO GENERAL
- Conocer e identificar el pie diabético desde un punto de vista
histopatológico.
III. OBJETIVOS SECUNDARIOS
- Demostrar la incidencia de pie diabético en pacientes con diabetes
mellitus y las complicaciones clínicas consecuentes.
- Describir la histopatología observada en el pie diabético.
- Describir el cuadro clínico de pie diabético desde un punto
histopatológico
- Identificar la respuesta inmunitaria en el pie diabético.
- Conocer sobre los exámenes auxiliares para el diagnóstico de pie
diabético.
INCIDENCIAS DE PIE DIABETICO
El pie diabético es una complicación grave de la diabetes mellitus. Definimos pie
diabético como el conjunto de síndromes en los que la existencia de neuropatía,
isquemia e infección provocan alteraciones tisulares o úlceras secundarias a
microtraumatismos, ocasionando una importante morbilidad que puede devenir en
amputaciones.
Según la Organización Mundial de la Salud, El pie diabético se define como la
ulceración, infección y/o gangrena de los tejidos del pie, asociada a neuropatía
diabética y diferentes grados de compromiso vascular periférico, siendo el resultado de
la interacción de diferentes factores metabólicos
Las lesiones asociadas al síndrome de pie diabético se consideran la causa más
frecuente de hospitalización; además, son responsables de un mayor número de
ingresos hospitalarios, si se comparan con otras complicaciones de la diabetes. los
pacientes hospitalizados con diabetes tienen 28 veces más probabilidades de ser
amputados.
La tercera parte de los diabéticos que son amputados de un miembro sufren una
amputación contralateral en los tres años siguientes.
El pie diabético es entendido como una epidemia creciente, si tenemos en cuenta que
alrededor del 25 % de las personas con diabetes se verá afectado por una úlcera de
pie en su vida, con mayor frecuencia de presentación entre los 45 y 65 años.
El 35 % de los pacientes con úlceras del pie diabético (UPD) suelen evolucionar a
lesiones complejas (Wagner 3 o 4) y a su vez, el 40 % de ellas desarrollan gangrena
del pie.
Hasta el 85 % de las amputaciones sufridas por diabéticos se vieron precedidas de
una úlcera de pie
A partir de los diez años de evolución de la enfermedad, el 50 % de los diabéticos
tienen manifestaciones clínicas evidentes de enfermedad arterial periférica,
alcanzando su presencia a la totalidad de la población diabética más allá de los 25
años
Del total de infecciones:
40 % desarrolla una infección leve (celulitis o eritema de piel < 2 cm).
30 %, moderada (celulitis > 2 cm o compromiso de TCS, tendón, músculo,
hueso).
y el restante 30 %, severa (celulitis > 2 cm o compromiso de TCS, tendón,
músculo, hueso, a lo cual se le añade el compromiso sistémico y las
alteraciones metabólicas).
Un 70-90 % de los casos son causados por cocos gram positivos; los
gérmenes gram negativos y anaerobios se encuentran en las fases más
avanzadas.
La infección aumenta considerablemente el riesgo de amputación, ya que entre el 25 y
el 50 % conducen a una amputación menor, y entre un 10 y un 40 % a una amputación
mayor.
La combinación de infección e isquemia es peligrosa y puede causar rápida pérdida de
tejido
FISIOPATOLOGIA DESDE EL PUNTO PATOLOGICO:
INFECCIÓN:
El desarrollo de infecciones en el Pie Diabético
es multifactorial.
A la predisposición de los enfermos diabéticos
a desarrollar úlceras de causa neuropáticas y a
la propia macroangiopática, se asocia, como
consecuencia de las
alteraciones metabólicas, la alteración de la
flora microbiana "fisiológica" de origen
endógeno y el descenso en la eficacia de los
mecanismos de resistencia a la infección.
La ubicación más prevalente de las úlceras son las zonas de callosidades,
secundarias a la presión plantar en la zona1.
a. Alteraciones de la flora microbiana:
La neuropatía autonómica condiciona una pérdida de las funciones
vasomotoras y del reflejo de sudoración a nivel del pie. Como consecuencia
directa, provoca la sequedad de la piel y la aparición de grietas que, asociadas
a la disminución del flujo sanguíneo en los capilares nutritivos, secundaria a la
apertura de los shunts arterio-venosos, hacen que el pie en la DM constituya
un potencial e importante punto de inicio de infecciones. La flora implicada en
las infecciones del PD es la habitual de la superficie cutánea en otras
localizaciones: Staphylococcus y streptococcus2.
En zonas húmedas se promueve el crecimiento fúngico y bacteriano, tanto en
densidad como en variedad2.
b. Disminución de los mecanismos de defensa:
La neuropatía sensorial, que afecta a la sensibilidad nociceptiva y térmica,
implica que lesiones mínimas pasen inadvertidas al afectarse especialmente la
sensibilidad al dolor desencadenado por la presión, lo que es sustrato para la
aparición de necrosis de decúbito que, por lo general, afectan a un pie
previamente deformado2.
Las fibras C sensoriales forman parte de una red que participa en la respuesta
nociceptiva y neuroinflamatoria. Su estimulación produce la liberación de
sustancias con acción neuroquinina como son la sustancia P, la serotonina y el
péptido relacionado con el gen de la calcitonina (CGRP) 2.
Todo ello condiciona la liberación de histamina por las células cebadas,
provocando un incremento en la permeabilidad del endotelio capilar y la
vasodilatación2.
La importante afectación de estas fibras en los enfermos diabéticos da lugar a
una disminución de los signos de infección y de la respuesta inflamatoria vital
inherente al control de las infecciones2.
c. Alteración de la respuesta inflamatoria:
Se han descrito múltiples defectos en la respuesta inmune en la DM, que
contribuyen al desarrollo y control de las infecciones2.
Estas disfunciones alterándose fenómenos como la diapédesis, la adherencia
leucocitaria, la quimiotaxis y la capacidad destructiva de los
polimorfonucleares, defectos que se agravan cuando son concomitantes a un
control incorrecto de la glucemia2.
La respuesta inflamatoria es un componente esencial tanto en los mecanismos
de defensa ante la infección, como en el proceso de la cicatrización2.
Fisiológicamente2, el proceso inflamatorio y de cicatrización de las heridas
puede describirse con arreglo a tres fases:
1. Fase de aumento del aporte sanguíneo en la zona lesionada.
2. Fase de acumulación de exudado hiperproteico, participado por
leucocitos para la destrucción bacteriana.
3. Fase de formación de tejido colágeno fibroso.
Así, una disminución del aporte sanguíneo, que en ausencia de complicaciones
puede ser suficiente para mantener la viabilidad de la piel intacta, no lo es para
conseguir la cicatrización incluso de pequeñas heridas, con lo que éstas
evolucionan hacia la necrosis y la infección2.
El crecimiento de gérmenes anaerobios está favorecido en estos tejidos
isquémicos, sobre todo si es concomitante con la presencia de gérmenes
aerobios. Además de la posibilidad de la aparición de gangrena gaseosa por
clostridio, en la DM puede desarrollarse una miositis por anaerobios no
clostridiales, que generalmente es de mal pronóstico en cuanto a la viabilidad
del segmento afectado2.
La denervación de los vasos sanguíneos por la neuropatía autonómica puede
provocar una disminución de la respuesta vascular a la inflamación y a otros
estímulos2.
En este sentido, se ha demostrado un aumento de la vasoconstricción en
respuesta a catecolaminas, lo que puede ser un obstáculo adicional para el
desarrollo de los mecanismos autorreguladores locales2.
Todo ello puede aumentar el desarrollo de las infecciones, y en este sentido
existen evidencias de que la vasoconstricción local producida por la inyección
de noradrenalina aumenta la agresividad bacteriana2.
El ya mencionado engrosamiento del endotelio capilar puede contribuir a alterar
la fase de migración leucocitaria a la zona lesionada y de formación de líquido
hiperproteico, fase que cursa con un proceso inicial de transporte a la zona
inflamada, seguido de la migración al intersticio tisular a través de las paredes
del capilar e identificación o reconocimiento del espécimen a fagocitar, y que
concluye con la fagocitosis, la destrucción y la digestión del material
fagocitado2.
En el contexto de este proceso, existen evidencias de que varias de estas
fases se hallan alteradas en la DM2.
En primer término, existe una disminución de la adherencia de los leucocitos al
endotelio capilar, circunstancia que probablemente tenga una repercusión
clínica, ya que enfermos con trastornos genéticos capaces de afectar a la
capacidad de adherencia de los leucocitos cursan con un incremento del riesgo
para las infecciones bacterianas2.
En segundo término, en la DM parecen existir alteraciones en las propiedades
reológicas de los leucocitos que afectarían a la diapédesis, proceso en el que
es fundamental la glucólisis2.
Tras atravesar el endotelio capilar, la progresión celular es una función
mediatizada por gradientes químicos2.
La quimiotaxis se ha encontrado alterada en algunos enfermos diabéticos,
hecho al parecer determinado genéticamente, pues se observa en familiares
diabéticos de primer grado. Además, las anomalías en la quimiotaxis no se han
podido demostrar a partir de células de personas no diabéticas y cuyo plasma
se ha colocado en un medio hiperglucémico2.
La capacidad de los polimorfonucleares de fagocitar y destruir las bacterias
está reducida en la DM, alteración que puede corregirse totalmente pero sin
llegar a normalizarse con el correcto control metabólico2.
El mecanismo consiste probablemente en una reducción en la generación de
factores bactericidas derivados del oxígeno. La producción de estas sustancias
depende del metabolismo de la glucosa mediante la vía de la pentosa fosfato,
que está directamente conectada con el metabolismo hidrocarbonado de la
célula2.
Un componente muy importante de la respuesta celular es la intervención de
los monocitos con función fagocítica. Se ha demostrado que la alteración de la
misma modifica de forma relevante la actividad fibroblástica en animales de
experimentación, y que los monocitos tienen reducida su actividad metabólica
en la DM2.
Los cambios que implica esta respuesta inflamatoria son esenciales en la fase
previa de formación del tejido colágeno fibroso2.
El déficit de insulina va asociado a disminución de granulocitos y de
fibroblastos; a un mayor grado de edema y a una disminución de estructuras
capilares. Estos hechos sugieren que es la falta de insulina más que la propia
hiperglicemia la responsable del déficit de crecimiento capilar2.
En el enfermo diabético también se han evidenciado alteraciones en la
formación del tejido de granulación, si bien no son exclusivas de la DM,
afectando igualmente a enfermos con niveles plasmáticos elevados de urea de
forma crónica y en situaciones de malnutrición2.
Se interpreta que el efecto del déficit de insulina en el proceso de curación de
las heridas se debe a cambios que se producen en las primeras fases y con
posterioridad al inicio de la lesión, como lo demostraría el hecho de que la
administración precoz de insulina recupera la capacidad de producir tejido de
granulación2.
Se ha postulado, finalmente, que determinadas citoquinas, como el factor de
crecimiento plaquetario PDGF pueden influir en la mala evolución de las
heridas en la DM. Este hecho se ha demostrado en modelos animales en los
que, con posterioridad a una diabetes experimental, se ha observado una
respuesta negativa al incremento esperado de este factor2.
Figura 1. Histología de un nervio periférico con fibras mielinizadas. (A) Histología
normal. Cada axón normal [an] está rodeada de una vaina de mielina [color negro] y
en su interior hay microtúbulos [cortados]. Se observa también un vaso capilar del
endoneuro, con su endotelio, membrana basal y pericito. (B) El mismo nervio periférico
afectado por neuropatía diabética. Coexisten axones normales [an], axones destruidos
[ad], axones en proceso de regeneración inicial [arg] y mielina en proceso de
regeneración [amrg]. Es posible observar también la reducción del diámetro del
capilar del endoneuro, y la reduplicación (engrosamiento por superposición de
láminas) de su membrana basal3.
Factores inflamatorio-inmunológicos y neuropatía
Las neuropatías diabéticas de fisiopatología predominantemente inflamatorio-
autoinmune no sólo se limitan a la radículo-plexopatía lumbosacra, sino que también
incluyen a la radículo-plexopatía cervical, a la radiculopatía torácica, y a las
neuropatías craneales. En efecto, la 2 muestra la pérdida axonal y la infiltración
leucocitaria que ocurre en este tipo de neuropatías4.
Figura 2. Mecanismos inflamatorio-inmunológicos en algunas neuropatías
diabéticas. [A] Figura semiesquemática de la histología normal de un nervio periférico
con fibras mielinizadas. Se observan cuatro fascículos conteniendo axones
mielinizados. En el borde de cada fascículo hay una arteriola del endoneuro (aen). En
el tejido conectivo entre los fascículos hay una arteriola (a) y varias células adiposas
(adip). [B]Neuropatía Diabética de Fisiopatología predominantemente Inflamatorio-
inmunológica (radículo-plexopatías lumbosacra y cervical, radiculopatía torácica, y
neuropatía craneal). Se observa una casi total pérdida axonal y la infiltración
inflamatoria de las arteriolas del endoneuro con abundantes leucocitos4 [dibujo basado
en 4, Tracy JA, 2008)].
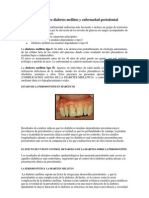
Figura 3.
Imágenes superiores: superior izquierda, vista plantar del pie donde se observa úlcera
sobre cabeza de 3.ermetatarsiano, con importante
er
enrojecimiento perilesional y 3. dedo necrótico. La úlcera
quedó expuesta tras la deslaminación de la hiperqueratosis
circundante, hecho típico en las lesiones neuropáticas.
Superior derecha, vista dorsal del pie donde se aprecia
enrojecimiento de medio pie y necrosis del 3.er dedo2.
Imágenes inferiores: inferior izquierda se observa congestión
y dilatación de los vasos sanguíneos así como tejido de
granulación; también se aprecia ulceración y aspecto
necrótico de la epidermis y dermis. Inferior derecha se
observa un intenso infiltrado inflamatorio de predominio
neutrofílico, con eosinófilos, que afecta al tejido óseo2.
HISTOPATOLOGÍA DEL PIE DIABETICO
A la angiopatía diabética se le ha descrito generalmente como “enfermedad de
pequeños vasos”. Goldenberg y cols. Publicaron, en 1959, un artículo que popularizó
el concepto de una enfermedad oclusiva arteriolar histológicamente única, que
producía isquemia a pesar de un flujo arterial adecuado. Esta teoría ha sido directa o
indirectamente refutada por otros estudios. El
único concepto válido en la actualidad de
“enfermedad de pequeños vasos” en diabéticos
es que la propensión a la afectación
aterosclerosa que predomina en las arterias
infrageniculares y es casi ausente en el
segmento aortoilíaco.
Lesión cutánea típica de la microangiopatía diabética en primer dedo del pie
Desde el punto de vista histológico la aterosclerosis del diabético es indistinguible de
la del no diabético. En los diabéticos se encuentran tanto la aterosclerosis de la íntima,
como la calcinosis de la túnica media, llamada también arteriosclerosis o calcinosis de
Mönkeberg. No se produce una estenosis anatómica típica, sino más bien una
estenosis funcional al disminuir la distensibilidad vascular e impedir la expansión
sistólica completa del vaso.
EXÁMENES AUXILIARES
1. De Patología Clínica
Glucemia basal en plasma venoso (GBP): Es el método recomendado para
el diagnóstico de diabetes y la realización de estudios poblacionales. Es un
test preciso, de bajo coste, reproducible y de fácil aplicación. La medición de
glucosa en plasma es aproximadamente un 11% mayor que la glucosa
medida en sangre total en situación de ayuno o basal. En los estados no
basales (postprandiales), ambas determinaciones son prácticamente iguales.
Empleando únicamente la GBP no se diagnostica al 30% de la población
diabética (diabetes desconocida).Esta cifra es superior si se trata de población
anciana y mayor aún si es del sexo femenino.5
Glucosa postprandial en plasma/suero venoso: Se define como glucosa
postprandial a los niveles de glucosa en sangre a las dos horas de la ingesta
de un alimento.6
Prueba de tolerancia oral a la glucosa (PTOG): Consiste en la
determinación de la glucemia en plasma venoso a las dos horas de una
ingesta de 75 gr de glucosa anhidra en adultos.
Para la realización de la PTOG la persona debe ingerir 75 gramos de glucosa
anhidra diluidos en 300 ml de agua con o sin sabor, a temperatura ambiente,
en un período no mayor de cinco minutos. Además debe reunir las siguientes
condiciones: 6
Ayuno de ocho a 14 horas (se puede tomar agua).
Evitar restricciones en la dieta durante los tres días previos (seguir
dieta habitual, la noche anterior se debe consumir 30-50 gramos de
hidratos de carbono).
Evitar cambios en la actividad física habitual durante los tres días
previos.
Durante la prueba debe mantenerse en reposo y sin fumar.
Es preferible que no tenga una infección u otra enfermedad
intercurrente. De lo contrario, debe quedar consignada en el informe de
la prueba.
Debe interrumpir el consumo de medicamentos que pudieran alterar los
valores de la glucemia mínimo 12 horas previas a la realización de la
prueba. De lo contrario, deben quedar consignados en el informe de la
prueba.
La PTOG no se debe practicar en personas con VIH positivo que estén
recibiendo inhibidores de proteasas por el alto número de resultados de
glucemia falsamente positivos.
Se recomienda utilizar la prueba de TTOG en los siguientes casos:
Cuando exista fuerte sospecha de diabetes (complicaciones
microvasculares, síntomas, resultados contradictorios o dudosos, etc.) y
existan glucemias basales normales.5
En pacientes con glucemias basales alteradas (GBA) (110-125 mg/dl)
repetidas, para comprobar el diagnóstico de diabetes, o con TAG, sobre
todo en población mayor y del sexo femenino.5
Orina completa: Evalúa la presencia de glucosuria, cuerpos cetónicos,
albuminuria (proteinuria) y leucocituria.5
2. De Imágenes
Radiografía simple de pie: Se debe realizar de forma comparativa, en
posiciones frontales y oblicuas, con el propósito de evidenciar presencia de
osteomielitis, infección productora de gas en tejidos blandos y calcificación de
las arterias del pie.1
CONCLUSIONES
- La incidencia de pie diabético en pacientes con diabetes mellitus se
considera la causa más frecuente de hospitalización si se comparan con
otras complicaciones de la diabetes. En estos pacientes hospitalizados
tienen 28 veces más probabilidades de ser amputados.
- La histología encontrada en el pie diabético se caracteriza por la
presencia de aterosclerosis de la íntima, así como la calcinosis de la
túnica media, llamada también arteriosclerosis o calcinosis de
Mönkeberg.
- El cuadro clínico del pie diabético desde el punto de vista histopatológico
se caracteriza por la presencia de ulceración y aspecto necrótico en
epidermis y dermis
- La respuesta inmunitaria que sobresale en pie diabético es el intenso
infiltrado inflamatorio de predominio neutrofílico, con eosinófilos, que
muchas veces afecta al tejido óseo.
- Los exámenes auxiliares constan de pruebas de glucemia, glucosa y
tolerancia para el diagnóstico de diabetes; para la observación de daños
en el pie, una radiografía simple de pie.
REFERENCIAS BIBLIOGRÁFICAS
1. ETIOPATOGENIA DE PIE DIABÉTICO, CAPITULO III. Blanes JI. Lluch I.
Morillas C. Nogueira JM. Hernández A.
2. FISIOPATOLOGÍA, CAPITULO II. Blanes JI. Lluch I. Morillas C. Nogueira JM.
Hernández A.
3. Tracy JA, Engelstad JK, Dyck PJB. Microvasculitis in diabetic lumbosacral
radiculoplexus neuroipathy. J Clin Neuromuscul Dis 2009; 11 (1): 44-8.
4. Tracy JA, Dick PJB. The spectrum of diabetic neuropathies. Phys Med Rehabil
Clin N Am 2008; 19 (1): 1-26. Doi:10.1016/j.pmr.2007.10.010.
5. Guía de Práctica Clínica para el Diagnóstico, Tratamiento y Control de la
Diabetes Mellitus Tipo 2 en el Primer Nivel de Atención. MINSA, Lima - Perú
2016. [Internet]. Disponible en: http://bvs.minsa.gob.pe/local/MINSA/3466.pdf.
6. Guía de Práctica Clínica sobre Diabetes tipo 2. MINSA, Lima - Perú 2017.
[Internet]. Disponible en: http://www.guiasalud.es/egpc/diabetes
7. Del Castillo R, Fernandez J, Del Castillo F. guía de práctica clínica del pie
diabético. Archivos de medicina. 2014 Vol. 10 (2).
8. García A. El pie diabético en cifras. Apuntes de una epidemia.
Rev.Med.Electrón. 2016 38 ( 4 ): 514-516.
9. Arango Montes G. Pie Diabético. [Internet]. 2014. Disponible en:
http://www.facmed.unam.mx/deptos/familiar/af8(3)/pie-diabetico.html
S-ar putea să vă placă și
- Taller Infecciones de Piel y Partes Blandas (Autoguardado)Document17 paginiTaller Infecciones de Piel y Partes Blandas (Autoguardado)Sara Ruiz ChantaÎncă nu există evaluări
- Herbitas-Dossier Pie DiabeticoDocument40 paginiHerbitas-Dossier Pie DiabeticoMARLONÎncă nu există evaluări
- Conjuntivitis alérgicas: Diagnóstico y tratamientoDe la EverandConjuntivitis alérgicas: Diagnóstico y tratamientoÎncă nu există evaluări
- Pie DiabeticoDocument31 paginiPie DiabeticoErika fragosoÎncă nu există evaluări
- Pie DiabeticoDocument25 paginiPie Diabeticoclaulsk100% (1)
- Mi TemaDocument7 paginiMi TemaEvelynÎncă nu există evaluări
- Pie DiabeticoDocument9 paginiPie DiabeticoFreddy TorresÎncă nu există evaluări
- Monografia Pie DiabeticoDocument14 paginiMonografia Pie DiabeticoLuigi Paolo Zapata Delgado0% (1)
- Pie Diabetico PDFDocument9 paginiPie Diabetico PDFMaría Fernanda Azócar NavarreteÎncă nu există evaluări
- Monografia Redaccion de TextosDocument11 paginiMonografia Redaccion de TextosJose Eduardo Becerra BazanÎncă nu există evaluări
- Justificación e ImportanciaDocument11 paginiJustificación e ImportanciaTirza RodriguezÎncă nu există evaluări
- Tutoria de InmunoDocument10 paginiTutoria de InmunoBelen MercadoÎncă nu există evaluări
- Pie DiabéticoDocument2 paginiPie DiabéticoosnelÎncă nu există evaluări
- .Trashed 1666752425 Articulo4Document8 pagini.Trashed 1666752425 Articulo4Hannia JiménezÎncă nu există evaluări
- Sensibilidad y Resistencia Bacteriana en Pacientes Con Diagnósticode Pie DiabéticoDocument11 paginiSensibilidad y Resistencia Bacteriana en Pacientes Con Diagnósticode Pie DiabéticoEdgar José Acosta GarcíaÎncă nu există evaluări
- Enfermedades PeriodontalesDocument17 paginiEnfermedades PeriodontalesYesenia Jopia OrellanaÎncă nu există evaluări
- Resumen de La Diabetes PeriodonciaDocument13 paginiResumen de La Diabetes Periodonciamastershackers11Încă nu există evaluări
- Manifestaciones Clinicas Pie DiabeticoDocument4 paginiManifestaciones Clinicas Pie DiabeticoHugo Jair Paz CabreraÎncă nu există evaluări
- Glomerulonefritis SecundariasDocument9 paginiGlomerulonefritis SecundariasJavier Apolinario Vargas100% (1)
- Pae Artritis ReumatoideDocument15 paginiPae Artritis ReumatoideVictor M. Ramírez SánchezÎncă nu există evaluări
- Complicaciones de La DiabetesDocument49 paginiComplicaciones de La DiabetesAiÎncă nu există evaluări
- Tareas 2º ParcialDocument3 paginiTareas 2º Parcialalejandro rivasÎncă nu există evaluări
- 6 Tesis Pie Diabético Ultima OkDocument32 pagini6 Tesis Pie Diabético Ultima OksimonÎncă nu există evaluări
- Sepsis CALLAODocument24 paginiSepsis CALLAOChristian Mendez UtcaniÎncă nu există evaluări
- Infecciones en El Paciente Inmunocomprometido (III) - Diabetes MellitusDocument10 paginiInfecciones en El Paciente Inmunocomprometido (III) - Diabetes MellitusDiego OssesÎncă nu există evaluări
- Abordaje Multidisciplinario Pie DiabeticoDocument20 paginiAbordaje Multidisciplinario Pie DiabeticoAnika VillaverdeÎncă nu există evaluări
- Pie Diabético.Document7 paginiPie Diabético.Laura GaliciaÎncă nu există evaluări
- 6ta TareaDocument27 pagini6ta TareamauricioÎncă nu există evaluări
- Pie DiabéticoDocument53 paginiPie DiabéticoVICTOR HERNANDEZÎncă nu există evaluări
- Complicaciones Post-Quirúrgicas en Pacientes Con Diabetes Mellitus Tipo 2Document6 paginiComplicaciones Post-Quirúrgicas en Pacientes Con Diabetes Mellitus Tipo 2David RodriguezÎncă nu există evaluări
- Tesis Final Pie Diabetico 001Document35 paginiTesis Final Pie Diabetico 001Doris Lorana Robinson Gallardo100% (2)
- Pie DiabeticoDocument14 paginiPie DiabeticoSteveFunky Velásquez PereiraÎncă nu există evaluări
- MonografiaDocument11 paginiMonografiaroxanaÎncă nu există evaluări
- 36a. Pie Diabético 1Document9 pagini36a. Pie Diabético 1Javiera Paz Guerrero CassanelloÎncă nu există evaluări
- El Pie Diabético. Medicina Integral. Garrido Calvo. 2003Document10 paginiEl Pie Diabético. Medicina Integral. Garrido Calvo. 2003Jose Fernando DiezÎncă nu există evaluări
- Dra. Ireiba Alvarez (Revisado)Document15 paginiDra. Ireiba Alvarez (Revisado)EDUCYAR OCVÎncă nu există evaluări
- Osteomielitis, Salmonelosis, Erisipela y CelulitisDocument44 paginiOsteomielitis, Salmonelosis, Erisipela y CelulitisCristian MuñozÎncă nu există evaluări
- Celulitis Imagenes y TratamientoDocument3 paginiCelulitis Imagenes y TratamientoRaimundo PazÎncă nu există evaluări
- Fisiopatología de Ulceras en DiabéticosDocument7 paginiFisiopatología de Ulceras en DiabéticosKro NaranjoÎncă nu există evaluări
- Infección de Piel y Tejidos Blandos (IPTBDocument31 paginiInfección de Piel y Tejidos Blandos (IPTBSofia MorenoÎncă nu există evaluări
- Taller Pie DiabéticoDocument19 paginiTaller Pie DiabéticoCENTRO DE SALUD CUNCHIBAMBAÎncă nu există evaluări
- SepsisDocument44 paginiSepsiselbamendezÎncă nu există evaluări
- Pie DiabéticoDocument2 paginiPie DiabéticoLisanny GomezÎncă nu există evaluări
- Pie DiabéticoDocument2 paginiPie DiabéticoClaudia ReyesÎncă nu există evaluări
- Sepsis y Shock Séptico - 2010 - Medicine - Programa de Formación Médica Continuada Acreditado PDFDocument11 paginiSepsis y Shock Séptico - 2010 - Medicine - Programa de Formación Médica Continuada Acreditado PDFDustin Raul Lazo BedoyaÎncă nu există evaluări
- Pie DiabeticoDocument14 paginiPie DiabeticoBeatriz Cano100% (3)
- Marco TeóricoDocument9 paginiMarco TeóricoCristian Alejandro Mendoza VillafañaÎncă nu există evaluări
- INTRODUCCIÓN Infeccion UrinariaDocument4 paginiINTRODUCCIÓN Infeccion UrinariaAlex Pedraza PeñaÎncă nu există evaluări
- PIE DIABÉTICO Modificado 23-2-2021Document47 paginiPIE DIABÉTICO Modificado 23-2-2021María José FuentesÎncă nu există evaluări
- Fascitis NecrozanteDocument5 paginiFascitis NecrozanteLeonardo BayonaÎncă nu există evaluări
- Pie DiabeticoDocument11 paginiPie DiabeticoCookie Wen Ale LaraÎncă nu există evaluări
- Resumen Dermatomiositis JuvenilDocument7 paginiResumen Dermatomiositis JuvenilAlejandro Hernández CompanioniÎncă nu există evaluări
- Volmer-Thole2016 (1) .En - EsDocument11 paginiVolmer-Thole2016 (1) .En - EsisaccalejandrohernandezjimenesÎncă nu există evaluări
- Pie Diabético 2Document3 paginiPie Diabético 2Keisha Daniela Baltazar TrejoÎncă nu există evaluări
- Fiore - Enfermedad Periodontal y Su Calsificacion PDFDocument9 paginiFiore - Enfermedad Periodontal y Su Calsificacion PDFFiorella MoffaÎncă nu există evaluări
- Pie Diabetico ..Imprimir PDFDocument3 paginiPie Diabetico ..Imprimir PDFDaniela SalinasÎncă nu există evaluări
- Pae Artritis ReumatoideDocument16 paginiPae Artritis ReumatoideVictor M. Ramírez SánchezÎncă nu există evaluări
- Objecion DownDocument58 paginiObjecion DownMartin PastorÎncă nu există evaluări
- Hipertrofia Ventricular Derecha y Ekg de PericarditisDocument19 paginiHipertrofia Ventricular Derecha y Ekg de PericarditisMirko PejerreyÎncă nu există evaluări
- Hemibloqueo Anterior IzquierdoDocument7 paginiHemibloqueo Anterior IzquierdoMirko PejerreyÎncă nu există evaluări
- FisiopatologiaDocument88 paginiFisiopatologiaMirko PejerreyÎncă nu există evaluări
- Estructura Del Espermatozoide MaduroDocument1 paginăEstructura Del Espermatozoide MaduroMirko PejerreyÎncă nu există evaluări
- Md. Programa Medicina 2019-2020Document106 paginiMd. Programa Medicina 2019-2020JoseLainezÎncă nu există evaluări
- 14 - AftasDocument10 pagini14 - AftasRo HaroÎncă nu există evaluări
- CAPITULO II Car. GasticoDocument67 paginiCAPITULO II Car. GasticoCaren MárquezÎncă nu există evaluări
- BazoDocument8 paginiBazoErick Patiño GraterolÎncă nu există evaluări
- Paralisis Facial de La CaraDocument22 paginiParalisis Facial de La CaraLein AyaÎncă nu există evaluări
- Banco de Preguntas Esqueleto AxialDocument15 paginiBanco de Preguntas Esqueleto AxialAlexis HernandezÎncă nu există evaluări
- Articulo 1Document13 paginiArticulo 1Ali ChaconÎncă nu există evaluări
- 3cirugiaep3 1Document560 pagini3cirugiaep3 1Marcelo Perez100% (1)
- Anticonvulsivantes PediatriaDocument118 paginiAnticonvulsivantes PediatriaSantiago LópezÎncă nu există evaluări
- Seguro de Vida - MetlifeDocument2 paginiSeguro de Vida - Metlifericardo100% (1)
- Eje Hipotálamo, Hipófisis, Ovario, ÚteroDocument66 paginiEje Hipotálamo, Hipófisis, Ovario, ÚteroLuis Enrique Calderon Almazan100% (2)
- Infectologia - PreguntasDocument3 paginiInfectologia - PreguntasLuz Estefany Huaman MachacaÎncă nu există evaluări
- Cefaleas en Pediatria - Dra - Aldao PDFDocument48 paginiCefaleas en Pediatria - Dra - Aldao PDFboorsi1971Încă nu există evaluări
- DisfagiaDocument6 paginiDisfagiaLaura CastilloÎncă nu există evaluări
- AminoglucosidosDocument39 paginiAminoglucosidosjmoÎncă nu există evaluări
- Coagulación Sanguínea y Anticoagulantes Fibrinolíticos y AntiplaquetariosDocument48 paginiCoagulación Sanguínea y Anticoagulantes Fibrinolíticos y AntiplaquetariosjennyÎncă nu există evaluări
- Patologías Frecuentes de La PielDocument40 paginiPatologías Frecuentes de La PielPaola Vilchez chancaÎncă nu există evaluări
- Insuficiencia CardiacaDocument11 paginiInsuficiencia CardiacaDelkiÎncă nu există evaluări
- Vademecum Dospu 2017Document35 paginiVademecum Dospu 2017Erik OblitasÎncă nu există evaluări
- Farmacos Moduladores de La AcDocument35 paginiFarmacos Moduladores de La AcVilma Brizaida Charalla100% (1)
- Antecedentes PediatricosDocument15 paginiAntecedentes PediatricosIngrid CisnerosÎncă nu există evaluări
- Deformidades Del Pie - TraumaDocument56 paginiDeformidades Del Pie - TraumabboyhelyÎncă nu există evaluări
- Insuficiencia Renal AgudaDocument6 paginiInsuficiencia Renal AgudaAna Cristina García Estrada100% (1)
- Arañas VenenosasDocument35 paginiArañas VenenosasEvy VanegasÎncă nu există evaluări
- Botiquin NaturalDocument34 paginiBotiquin NaturalliliaÎncă nu există evaluări
- Resumen Farma de Muy MedicoDocument24 paginiResumen Farma de Muy MedicoTrebos SCÎncă nu există evaluări
- Edema Agudo de PulmonDocument33 paginiEdema Agudo de PulmonROCIO ZUÑIGAÎncă nu există evaluări
- Onco ResumenDocument17 paginiOnco ResumenElisabeth Ortega ReyÎncă nu există evaluări
- Casos Clinicos Neurologia PDFDocument101 paginiCasos Clinicos Neurologia PDFDennis Sanga100% (2)
- Síndrome Del Ojo RojoDocument26 paginiSíndrome Del Ojo RojoMoises A Vigil GÎncă nu există evaluări