Documente Academic
Documente Profesional
Documente Cultură
Atomo
Încărcat de
Ruben MuñozDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Atomo
Încărcat de
Ruben MuñozDrepturi de autor:
Formate disponibile
El átomo es la unidad constituyente más pequeña de la materia que tiene las
propiedades de un elemento químico.1 Cada sólido, líquido, gas y plasma se compone
de átomos neutros o ionizados. Los átomos son muy pequeños; los tamaños típicos son
alrededor de 100 pm (diez mil millonésima parte de un metro).2 No obstante, los
átomos no tienen límites bien definidos y hay diferentes formas de definir su
tamaño que dan valores diferentes pero cercanos. Los átomos son lo suficientemente
pequeños para que la física clásica dé resultados notablemente incorrectos. A
través del desarrollo de la física, los modelos atómicos han incorporado principios
cuánticos para explicar y predecir mejor su comportamiento. El término proviene del
latín atŏmus, calco del griego ἄτομον (átomon) < ἄτομος, unión de α (a, que
significa «sin»), y τόμος (tómos, «sección»), que literalmente es «que no se puede
cortar, indivisible»,3 y fue el nombre que se dice les dio Demócrito de Abdera,
discípulo de Leucipo de Mileto, a las partículas que él concebía como las de menor
tamaño posible.4
Cada átomo se compone de un núcleo y uno o más electrones unidos al núcleo. El
núcleo está compuesto de uno o más protones y típicamente un número similar de
neutrones. Los protones y los neutrones son llamados nucleones. Más del 99,94 % de
la masa del átomo está en el núcleo. Los protones tienen una carga eléctrica
positiva, los electrones tienen una carga eléctrica negativa y los neutrones tienen
ambas cargas eléctricas, haciéndolos neutros. Si el número de protones y electrones
son iguales, ese átomo es eléctricamente neutro. Si un átomo tiene más o menos
electrones que protones, entonces tiene una carga global negativa o positiva,
respectivamente, y se denomina ion (anión si es negativa y catión si es positiva).
Los electrones de un átomo son atraídos por los protones en un núcleo atómico por
la fuerza electromagnética. Los protones y los neutrones en el núcleo son atraídos
el uno al otro por una fuerza diferente, la fuerza nuclear, que es generalmente más
fuerte que la fuerza electromagnética que repele los protones cargados
positivamente entre sí. Bajo ciertas circunstancias, más acentuado cuanto mayor
número de protones tenga el átomo, la fuerza electromagnética repelente se vuelve
más fuerte que la fuerza nuclear y los nucleones pueden ser expulsados o desechados
del núcleo, dejando tras de sí un elemento diferente: desintegración nuclear que
resulta en transmutación nuclear.
El número de protones en el núcleo define a qué elemento químico pertenece el
átomo: por ejemplo, todos los átomos de cobre contienen 29 protones. El número de
neutrones define el isótopo del elemento.5 El número de electrones influye en las
propiedades magnéticas de un átomo. Los átomos pueden unirse a otro u otros átomos
por enlaces químicos (en los cuales se comparten los electrones de dichos átomos)
para formar compuestos químicos tales como moléculas y redes cristalinas. La
capacidad de los átomos de asociarse y disociarse es responsable de la mayor parte
de los cambios físicos observados en la naturaleza y es el tema de la disciplina de
la química.
También existe la antimateria, la cual está compuesta también por átomos pero con
las cargas invertidas;6 los protones tienen carga negativa y se denominan
antiprotones, y los electrones tienen una carga positiva y se denominan positrones.
Es muchísimo menos frecuente en la naturaleza. Al entrar en contacto con la
respectiva partícula (como los protones con los antiprotones y los electrones con
los positrones) ambas se aniquilan generando un estallido de energía de rayos gamma
y otras partículas.
No toda la materia del universo está compuesta de átomos; de hecho, solo el 5% o
menos del universo está compuesto por estos. La materia oscura, que constituye
según algunas estimaciones más del 20% del universo, no se compone de átomos, sino
de partículas de un tipo actualmente desconocido. También cabe destacar la energía
oscura, la cual es un componente que está distribuido por todo el universo,
ocupando aproximadamente más del 70% de este.
S-ar putea să vă placă și
- Solucion Discurso NarrativoDocument5 paginiSolucion Discurso NarrativoRuben MuñozÎncă nu există evaluări
- Mapa ConceptualDocument1 paginăMapa ConceptualRuben MuñozÎncă nu există evaluări
- Participación en Los Nodos VirtualesDocument1 paginăParticipación en Los Nodos VirtualesRuben MuñozÎncă nu există evaluări
- Solución Al TrabajoDocument2 paginiSolución Al TrabajoRuben MuñozÎncă nu există evaluări
- Investigacion Accion Participativa Wiki....Document3 paginiInvestigacion Accion Participativa Wiki....Ruben MuñozÎncă nu există evaluări
- Capital en Economía Wiki...Document3 paginiCapital en Economía Wiki...Ruben MuñozÎncă nu există evaluări
- Sociedad Comunista Wiki...Document4 paginiSociedad Comunista Wiki...Ruben MuñozÎncă nu există evaluări
- Literatura Medieval Wiki....Document5 paginiLiteratura Medieval Wiki....Ruben MuñozÎncă nu există evaluări
- Texto en Linea Sobre Aplicación de Administración de EmpresasDocument1 paginăTexto en Linea Sobre Aplicación de Administración de EmpresasRuben MuñozÎncă nu există evaluări
- Lecturas para El TrabajoDocument3 paginiLecturas para El TrabajoRuben MuñozÎncă nu există evaluări
- Encuentro en Skype 2019Document3 paginiEncuentro en Skype 2019Ruben MuñozÎncă nu există evaluări
- Horarios SkypeDocument2 paginiHorarios SkypeRuben MuñozÎncă nu există evaluări
- Presentación Del Curso Cátedra UnadistaDocument5 paginiPresentación Del Curso Cátedra Unadistahogar huellas del ayerÎncă nu există evaluări
- René Descartes Wiki....Document5 paginiRené Descartes Wiki....Ruben MuñozÎncă nu există evaluări
- Tutorial Afectación Del Tipo de Cambio en Las Importaciones y en Las ExportacionesDocument8 paginiTutorial Afectación Del Tipo de Cambio en Las Importaciones y en Las ExportacioneskasanchezÎncă nu există evaluări
- Marketing de ContenidosDocument2 paginiMarketing de ContenidosRuben MuñozÎncă nu există evaluări
- Gobierno Local Wiki....Document4 paginiGobierno Local Wiki....Ruben MuñozÎncă nu există evaluări
- Formato de Autoevaluaciontarea2Document1 paginăFormato de Autoevaluaciontarea2Ruben MuñozÎncă nu există evaluări
- Marketing MultinivelDocument4 paginiMarketing MultinivelRuben MuñozÎncă nu există evaluări
- Manual Usuario Office365 EstudiantesDocument15 paginiManual Usuario Office365 EstudiantesALVARO PEREZ SEVERICHEÎncă nu există evaluări
- PosTarea RubenMuñozMenesesDocument3 paginiPosTarea RubenMuñozMenesesRuben MuñozÎncă nu există evaluări
- Marketing ViralDocument4 paginiMarketing ViralRuben MuñozÎncă nu există evaluări
- SimuladorFase 5Document58 paginiSimuladorFase 5Asesorias PipeÎncă nu există evaluări
- Para Revision Del ProfeDocument4 paginiPara Revision Del ProfeRuben MuñozÎncă nu există evaluări
- MicrodiseñoDocument6 paginiMicrodiseñoFaiber Julian Mora DussanÎncă nu există evaluări
- Dimensiones Políticas y Culturales en El Conflicto Colombiano PDFDocument14 paginiDimensiones Políticas y Culturales en El Conflicto Colombiano PDFDick EmanuelssonÎncă nu există evaluări
- 2 Web Conferencia Metodologiadeinvestigacion FINALDocument30 pagini2 Web Conferencia Metodologiadeinvestigacion FINALALEXANDRAÎncă nu există evaluări
- Instructivo Registro Fotografico Reconocimiento FacialDocument13 paginiInstructivo Registro Fotografico Reconocimiento FacialRuben MuñozÎncă nu există evaluări
- Datos Interesantes Sobre Las Teorías AdministrativasDocument6 paginiDatos Interesantes Sobre Las Teorías AdministrativasRuben MuñozÎncă nu există evaluări
- ReflexiónDocument1 paginăReflexiónRuben MuñozÎncă nu există evaluări
- Ensayo CNCDocument15 paginiEnsayo CNCSally Ortega100% (2)
- Arquitectura Bioclimatica AmericaDocument28 paginiArquitectura Bioclimatica AmericaJunior BarrenoÎncă nu există evaluări
- Actualizar TocomSat DUO HD MiniDocument23 paginiActualizar TocomSat DUO HD MiniDamian Delferro50% (2)
- Mi Colegio Una Parte Del Ecosistema UrbanoDocument8 paginiMi Colegio Una Parte Del Ecosistema UrbanoAndre MenesesÎncă nu există evaluări
- LQOI Práctica 8.1Document3 paginiLQOI Práctica 8.1Alex CarreñoÎncă nu există evaluări
- Direcciones y Ang. Horiz.Document10 paginiDirecciones y Ang. Horiz.LUIS CARLOS BURBANO CASTILLOÎncă nu există evaluări
- Anhidrido Acetico - MsdsDocument9 paginiAnhidrido Acetico - MsdsVíctor Julio Daza MÎncă nu există evaluări
- Prevencion de EmergenciasDocument18 paginiPrevencion de EmergenciasAdbleidys GutierrezÎncă nu există evaluări
- Embrague Seco DobleDocument1 paginăEmbrague Seco Dobleadiraii ordoezÎncă nu există evaluări
- Memoria de Calculo de Pavimento RigidoDocument15 paginiMemoria de Calculo de Pavimento RigidoMayrenee RodriguezÎncă nu există evaluări
- Plan Negocio 2004-2009 Pdvsa OrienteDocument49 paginiPlan Negocio 2004-2009 Pdvsa Orienter3n1Încă nu există evaluări
- Agrimac Motocultor Diesel Catalogo Agria HispaniaDocument12 paginiAgrimac Motocultor Diesel Catalogo Agria HispaniaborioÎncă nu există evaluări
- Serie 04Document3 paginiSerie 04gastonÎncă nu există evaluări
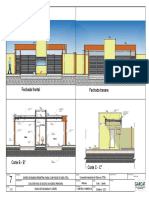
- Fachada Frontal Fachada TraseraDocument1 paginăFachada Frontal Fachada TraseraGabriel Rodrigo Cano TapiaÎncă nu există evaluări
- Anexo Rovira - SPDocument12 paginiAnexo Rovira - SPAngel Bures AmatÎncă nu există evaluări
- Clase 15 Carga Excéntrica PDFDocument30 paginiClase 15 Carga Excéntrica PDFAlvaro AlataÎncă nu există evaluări
- 957956893.ventiladores IndustrialesDocument15 pagini957956893.ventiladores IndustrialeswilmerÎncă nu există evaluări
- Comparacion de Pisos Epóxicos y Piso PulidoDocument1 paginăComparacion de Pisos Epóxicos y Piso PulidoserviincaÎncă nu există evaluări
- Diseño de VigasDocument14 paginiDiseño de VigasJose ChuquimiaÎncă nu există evaluări
- Tema2blaplaneacion 110626134012 Phpapp01Document5 paginiTema2blaplaneacion 110626134012 Phpapp01Carlos Alexander Suarez RodriguezÎncă nu există evaluări
- Utencilios para Una CarniceriaDocument6 paginiUtencilios para Una CarniceriaCamila Valencia BohorquezÎncă nu există evaluări
- ACOTADODocument26 paginiACOTADOSaul VargasÎncă nu există evaluări
- Instalación y Configuración IISDocument8 paginiInstalación y Configuración IISSofia Kari Vargas KamiyaÎncă nu există evaluări
- Canal, Vertedero, TunelDocument50 paginiCanal, Vertedero, TunelJhon Anderzo Diaz Garcia100% (1)
- Taller Energía y PotenciaDocument3 paginiTaller Energía y PotenciaRaúl Avila0% (7)
- Investigación Unidad 2Document6 paginiInvestigación Unidad 2Itzel López EugenioÎncă nu există evaluări
- Modelo para ProyectoDocument54 paginiModelo para ProyectoDiego PomaÎncă nu există evaluări
- HOPSA - Manual de Techos N°3 PDFDocument18 paginiHOPSA - Manual de Techos N°3 PDFLuis LopezÎncă nu există evaluări
- Analisador de RedesDocument4 paginiAnalisador de RedesJorge FrancoÎncă nu există evaluări
- Buscar Mi Dispositivo - Cómo Localizar Un Teléfono Firefox OS Perdido o RobadoDocument2 paginiBuscar Mi Dispositivo - Cómo Localizar Un Teléfono Firefox OS Perdido o RobadoperexwiÎncă nu există evaluări