Documente Academic
Documente Profesional
Documente Cultură
Metabolismo Afectado
Încărcat de
Fernando Hdz0 evaluări0% au considerat acest document util (0 voturi)
13 vizualizări3 paginiMetabolismo afectado
Titlu original
Metabolismo afectado
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentMetabolismo afectado
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
13 vizualizări3 paginiMetabolismo Afectado
Încărcat de
Fernando HdzMetabolismo afectado
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 3
En este trabajo, los macrófagos humanos se infectaron con diferentes cepas
virulentas de M. tuberculosis y se investigaron los efectos del tiempo de infección.
Usando múltiples métodos de análisis estadístico, los resultados experimentales
mostraron que las concentraciones de muchos metabolitos intracelulares
cambiaron significativamente. El cambio anormal de estos metabolitos estaba
estrechamente relacionado con una variedad de vías metabólicas y funciones
fisiológicas. Se sugiere que el metabolismo de los macrófagos humanos se
desordenó después de infectarse con cepas de M. tuberculosis, y los mecanismos
de acción virulentos de M. tuberculosis podrían revelarse en cierta medida. Hubo
veintidós metabolitos diferenciales que pueden identificarse como biomarcadores
potenciales. Curiosamente, estos metabolitos tuvieron una regularidad y una
tendencia a la variación similares después de infectarse con diferentes cepas de
M. tuberculosis en diferentes períodos de tiempo, ya sea en grupos virulentos
(BCG y Ra) o grupos virulentos. (Rv y B36). Se utilizó otro método para verificar y
certificar este resultado; Se analizaron los metabolitos completos con áreas de
pico relativas utilizando MetaboAnalyst 2.0 después de normalizarse con ribitol
(estándar interno). Después del análisis de grupo sin supervisión (Figura 5a) y del
análisis PLS-DA supervisado (Figura 5b), se obtuvieron veinticuatro metabolitos (el
valor VIP total de los componentes principales de cada metabolito estaba por
encima de 1.0) como metabolitos diferenciales. Este resultado fue bastante
encajado con el resultado antes mencionado. El análisis de la ruta del
metabolismo mostró que estos metabolitos diferenciales se relacionaban
principalmente con el metabolismo de los aminoácidos y la biosíntesis (como la
alanina, aspartato, glutamato, valina, leucina, etc.), el metabolismo anabólico del
glutatión (GSH), el metabolismo de los carbohidratos (como la galactosa, fructosa,
sacarosa, etc.), metabolismo de los ácidos grasos, metabolismo de los
esfingolípidos, metabolismo del piruvato y glioxilato, y metabolismo del
dicarboxilato. Muchas vías de metabolismo y biosíntesis se vieron afectadas
después de la infección por cepas de M. tuberculosis, como el metabolismo de los
aminoácidos, el metabolismo de los carbohidratos y el metabolismo de los
fosfolípidos. Finalmente, estas rutas de metabolismo y biosíntesis afectaron el
ciclo del ácido tricarboxílico (TAC, que no solo es la ruta final del metabolismo de
tres nutrientes principales, sino que también es un importante centro asociado de
metabolismo de carbohidratos, ácidos grasos y aminoácidos), y luego causa la
Anomalías del metabolismo energético.
El ácido glutámico, la 5-oxoprolina y el ácido aspártico tuvieron la misma dirección
de perturbación (regulación hacia arriba o hacia abajo) en los grupos infectados
por diferentes virulentos. Estos tres metabolitos son sustratos muy importantes
involucrados en el metabolismo anabólico de GSH (las líneas de puntos en la
Figura 6). Se propone que el metabolismo anabólico GSH fue afectado en estas
condiciones. GSH es un componente importante de la defensa celular contra la
virulencia del oxígeno (Ung y Av-Gay 2006). Las concentraciones de estos
metabolitos aumentaron después de infectarse por M. tuberculosis durante un día.
Se indica que los macrófagos inducen la producción de GSH para proteger a los
macrófagos contra el efecto virulento de los intermediarios reactivos del oxígeno
(ROI) y los intermediarios reactivos del nitrógeno (RNI) (Venketaraman et al. 2005;
Millman et al. 2008; Zahrt and Deretic 2002). En nuestro trabajo, las
concentraciones de los tres metabolitos mencionados anteriormente disminuyeron
después de la infección durante tres días y más. Se indica que la ruta del
metabolismo anabólico de GSH se destruyó, por lo que se agotó el GSH y
disminuyó la inmunidad de los macrófagos. Las concentraciones de otros
aminoácidos, como la prolina, treonina, hidroxiprolina, glicina, beta-alanina, etc.,
disminuyeron, lo que resultó directa o indirectamente del metabolismo anabólico
de GSH (Figura 6).
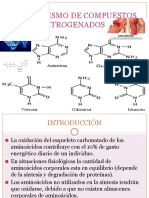
Figure 6. Putative metabolic pathways of human macrophages infected by M. Tuberculosis. For
clarity, arrows indicate the direction of the reaction assumed in the model. Red marks indicated
the reactions that were significantly elevated relative to those of the controls. Blue marks show
significantly inhibited reactions. Amaranth marks show insignificantly inhibited reactions. PEP,
phosphoenolpyruvate; AA, Amino acids; Amino acids were abbreviated using the standard three-
letter convention. (Figure available in color online.)
La perturbación de varios metabolitos diferenciales, como el fosfoglicérido, el ácido
fosfórico, el glicerol, la fosforiletanolamina, el ácido esteárico, el ácido palmitínico y
el ácido oxálico, sugirieron que el metabolismo de los ácidos grasos, el
metabolismo de los glicerofosfolípidos, el metabolismo de los esfingolípidos y el
metabolismo del inositolfosfito se vieron afectados. Estas vías metabólicas se
relacionaron con la biosíntesis y el metabolismo de los lípidos. Muchos estudios
han demostrado que las grandes cantidades de lípidos en la envoltura celular de
M. tuberculosis tienen funciones importantes en los virulentos (Barry 2001;
Mendelson et al. 2005). Algunos de estos lípidos sirven como ligandos clave
cuando las micobacterias ingresan a las células huésped a través de varios
receptores de superficie y pueden afectar fuertemente la señalización de la célula
huésped y la secreción de las citoquinas inflamatorias (Neyrolles y Guilhot 2011).
Al mismo tiempo, las células T activan los macrófagos a través del interferón
gamma (IFN-c), una citoquina de tipo TH1 para proteger contra la tuberculosis
como respuesta inmune (Rocha-Ramirez et al. 2008). Las concentraciones de los
lípidos anteriores (o esos metabolitos). relacionado con la biosíntesis y el
metabolismo de los lípidos) disminuyó en cierta medida en el grupo virulento. Se
indica que las vías biosintéticas de los lípidos se pueden inhibir y las vías
metabólicas de los lípidos se pueden reforzar. Se sugirió que la actividad o
expresión de enzimas en la biosíntesis de lípidos se puede suprimir para que
disminuyan las composiciones y cantidades de lípidos. Eventualmente conduciría
a restringir las citoquinas diferenciales (o quimiocinas) de la respuesta inmune de
macrófagos a la infección micobacteriana (Manca et al. 2004). Las
concentraciones de galactosa, glucosa y maltosa en los grupos virulentos
mostraron una tendencia alcista. Se sugirió que varias vías metabólicas de
carbohidratos, como el metabolismo de la galactosa, el metabolismo de la fructosa
y la manosa, el metabolismo del almidón y la sacarosa, etc., se vieron afectadas
después de la infección por M. tuberculosis, y se puede promover la biosíntesis de
los polisacáridos. Los polisacáridos son una de las sustancias inmunomoduladoras
importantes. Algunos de ellos pueden unirse a receptores de superficie comunes e
inducir respuestas inmunomoduladoras en macrófagos para aumentar la
producción de especies reactivas de oxígeno (ROS) y óxido nítrico (NO) y
aumentar la secreción de citoquinas y quimioquinas (Bai et al. 2012). Por otro
lado, algunas partes de los carbohidratos pueden introducirse en los macrófagos
durante la infección por M. tuberculosis, como los polisacáridos en la capa más
externa de M. tuberculosis, que pueden bloquear la fagocitosis de los macrófagos.
S-ar putea să vă placă și
- Plan de Campaña Semana de Vacunacion de Las AmericasDocument4 paginiPlan de Campaña Semana de Vacunacion de Las AmericasDiogo Ramos Peñaloza79% (14)
- Universidad Autónoma de Nuevo León Facultad de Ciencias QuímicasDocument21 paginiUniversidad Autónoma de Nuevo León Facultad de Ciencias QuímicasFernando HdzÎncă nu există evaluări
- Mapa Mental DOGMA BIOLOGIA MOLECULARDocument1 paginăMapa Mental DOGMA BIOLOGIA MOLECULARJennyfer Sanchez Calle0% (1)
- Tatuajes en La SociedadDocument5 paginiTatuajes en La SociedadFernando HdzÎncă nu există evaluări
- Cóctel Nieve RosaDocument1 paginăCóctel Nieve RosaFernando HdzÎncă nu există evaluări
- Ciclo de Born HaberDocument3 paginiCiclo de Born HaberFernando HdzÎncă nu există evaluări
- AditivosDocument12 paginiAditivosFernando HdzÎncă nu există evaluări
- NeurotransmisoresDocument25 paginiNeurotransmisoresFernando HdzÎncă nu există evaluări
- 1.-La Evolución de La Educacion de Enf en México PDFDocument11 pagini1.-La Evolución de La Educacion de Enf en México PDFFernando HdzÎncă nu există evaluări
- 1.-La Evolución de La Educacion de Enf en México PDFDocument11 pagini1.-La Evolución de La Educacion de Enf en México PDFFernando HdzÎncă nu există evaluări
- 1610Document113 pagini1610FlorezÎncă nu există evaluări
- Metabolismo de Compuestos NitrogenadosDocument53 paginiMetabolismo de Compuestos NitrogenadosIsai GonzalezÎncă nu există evaluări
- Corrección Anabolismo (EvAU Madrid)Document7 paginiCorrección Anabolismo (EvAU Madrid)Susa Garzón GuereñaÎncă nu există evaluări
- Vi Características Ultraestructurales y Morfología de Los Virus.Document6 paginiVi Características Ultraestructurales y Morfología de Los Virus.LUIS DAVID PEREZ MERCADOÎncă nu există evaluări
- Temas Selectos de InmunologíaDocument31 paginiTemas Selectos de Inmunología.:("*"BLacK BuLLeT"*"):.100% (2)
- Sol y MalezasDocument7 paginiSol y MalezasJorge Perez BernalÎncă nu există evaluări
- Guía4 Respiración CelularDocument7 paginiGuía4 Respiración CelularignaciaÎncă nu există evaluări
- Silabos Biologia MolecularDocument17 paginiSilabos Biologia MolecularFio CabezudoÎncă nu există evaluări
- Topico 2 Fisiología BlancoDocument51 paginiTopico 2 Fisiología BlancoAnny ViviescaÎncă nu există evaluări
- Materiales, Introduccion y Marco TeoricoDocument5 paginiMateriales, Introduccion y Marco TeoricoDiego VHÎncă nu există evaluări
- Catabolismo y AnabolismoDocument27 paginiCatabolismo y AnabolismoJeimy Orantes100% (1)
- 9 BioenergeticaATPGlucolisis PDFDocument50 pagini9 BioenergeticaATPGlucolisis PDFGise HinostrozaÎncă nu există evaluări
- BioquimicaDocument3 paginiBioquimicaKatherine Arrieta AngelÎncă nu există evaluări
- Célula IDocument26 paginiCélula ILizeth Nataly OréÎncă nu există evaluări
- Glucolípidos y EsteroidesDocument2 paginiGlucolípidos y EsteroidesAmy Álvarez RomeroÎncă nu există evaluări
- La Célula y Sus PartesDocument6 paginiLa Célula y Sus PartesPlutarco LithzÎncă nu există evaluări
- Disciplina: Morfofisiología Humana Unidad Curricular: Morfofisiología Humana I Trimestre: Primero CursoDocument20 paginiDisciplina: Morfofisiología Humana Unidad Curricular: Morfofisiología Humana I Trimestre: Primero CursoPAOLAÎncă nu există evaluări
- San Miguel de Brasil - ENI Sala Situacional - 2023Document22 paginiSan Miguel de Brasil - ENI Sala Situacional - 2023San Miguel de Brasil Centro de SaludÎncă nu există evaluări
- Control Genico en Celulas Pro y EucariotasDocument40 paginiControl Genico en Celulas Pro y EucariotasEvelyn ManchayÎncă nu există evaluări
- Luis Alaya - Tesis PDFDocument61 paginiLuis Alaya - Tesis PDFJose Fernando SNÎncă nu există evaluări
- Bacterias y VirusDocument58 paginiBacterias y Virusceeesaar100% (1)
- Biotecnología MicrobianaDocument81 paginiBiotecnología MicrobianaMaría CadenaÎncă nu există evaluări
- Grupo SanguineoDocument19 paginiGrupo SanguineoIvan E. GómezÎncă nu există evaluări
- Examen - 2do. Parcial - BiocelDocument5 paginiExamen - 2do. Parcial - BiocelSarah SánchezÎncă nu există evaluări
- 4BIOLOGIADocument95 pagini4BIOLOGIACamila FernandezÎncă nu există evaluări
- Exposición MaquetaDocument2 paginiExposición MaquetaSONIA MARIA PRADA AMANDIÎncă nu există evaluări
- Bioquimica Metabolismo CarbohidratosDocument46 paginiBioquimica Metabolismo CarbohidratosBristan Maraza PedemonteÎncă nu există evaluări
- MitocondriaDocument3 paginiMitocondriajhonatanÎncă nu există evaluări