Documente Academic
Documente Profesional
Documente Cultură
Cinetica Tiosulfato Clorhídrico
Încărcat de
cristian camposDescriere originală:
Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Cinetica Tiosulfato Clorhídrico
Încărcat de
cristian camposDrepturi de autor:
Formate disponibile
QUÍMICA PRÁCTICA: CINÉTICA QUÍMICA
La cinética estudia la rapidez con la que se produce una reacción espontánea. Son muchos
los factores que influyen en la velocidad de reacción. Con esta práctica, se pretende que el alumno
determina la influencia de la concentración y de la temperatura sobre la velocidad de una reacción.
La reacción elegida -por la facilidad a la hora de determinar cuándo termina la reacción- es la de
tiosulfato de sodio disuelto (Na2S2O3(aq)) con ácido clorhídrico diluido, HCl(aq) .
1. OBJETIVO DE LA PRÁCTICA
2. REVISIÓN BIBLIOGRÁFICA.(en hoja aparte)
a) Encuentra la ecuación química que se produce en la reacción entre tiosulfato de sodio en
disolución con una disolución de ácido clorhídrico. Ajústala.
b) Busca el significado de: velocidad de reacción; constante cinética; ley de acción de masas; orden
de reacción; Energía de activación; Ecuación de Arrhenius
c) Recuerda aquí la definición de mol, masa molar y las expresiones de concentración en masa y
molaridad de una disolución.
d) Busca las masas atómicas relativas de azufre, oxígeno, sodio, cloro, hidrógeno.
3. HIPÓTESIS
Antes de realizar la práctica, escribe aquí qué crees que pasará a la velocidad de la reacción
cuando , sin variar la temperatura, aumenta la concentración de reactivos:
Idem cuando manteniendo constante la concentración de los reactivos, la temperatura aumenta.;:
4. EXPERIMENTACIÓN
4.1. OBTENCIÓN DE DATOS.
Sobre la mesa encontrarás disolución de tiosulfato de sodio de 40 g/L, disolución de ácido
clorhídrico 2M, dos probetas -una de 100 mL y otra de 10 mL, un vaso, un cronómetro, agua
destilada, un papel donde se ha dibujado una cruz y una placa eléctrica para calentar.
En la reacción química entre el tiosulfato de sodio (Na₂S₂O₃) y el acido
clorhídrico (HCl) se produce azufre coloidal (S) que enturbia la reacción .Puede
determinarse la velocidad de reacción estableciendo el tiempo requerido para que
la solución alcance cierto grado de turbidez. En nuestro caso tomamos el
momento en el cual una cruz negra dibujada debajo del recipiente en el que se
produce la reacción deja de ser visible cuando se la observa a través de la misma.
1ª EXPERIENCIA: INFLUENCIA DE LA CONCENTRACIÓN
El procedimiento es el siguiente:
1º. Con ayuda de la probeta de 100 mL, se toman 50 ml de disolución de tiosulfato sódico y se
añaden al vaso.
2º. Se añaden 6 ml de acido clorhídrico con una pipeta y, al mismo tiempo, se pone en marcha el
crónometro.
3º. Se agita suavemente el vaso a intervalos regulares de tiempo y se coloca sobre el papel con la
cruz ya marcada.
4º. Se mira la cruz marcada a través de la disolución y cuando se deje de ver se para el cronómetro
anotando el tiempo transcurrido para la reacción.
Esta experiencia la repetimos tres veces pero tomando cantidades cada vez menores de tiosulfato
sódico y diluyendo con agua destilada (H2O). Completa la tabla 1:
TABLA 1
V1= Volumen V2 =volumen V3= volumen volumen de Tiempo
total Temperatura
Na2S2O3 de agua (tiosulfato+agua)
HCl (mL) tardado
Ensayo 1 50 mL 0 mL 50 mL 6
Ensayo 2 40 mL 10 mL 50 mL 6
Ensayo 3 30 mL 20 mL 50 mL 6
Ensayo 4 20 mL 30 mL 50 mL 6
4.2. TRATAMIENTO DE LOS DATOS OBTENIDOS
La ecuación de la velocidad de esta reacción vendrá dada por:
m n
r =k [Na 2 S2 O 3 ] [HCl]
No obstante, la concentración de ácido clorhídrico va a ser mantenida constante a lo largo de toda la
experimentación, por lo que la vamos a incluir en la constante cinética. En definitiva, para nuestro
trabajo, en el que sólo hemos variado la concentración de tiosulfato de sodio, tenemos:
m
r =k 1 [Na2 S2 O3 ]
a) Cálculo de la velocidad de la reacción.
Cuánto menos tiempo tarda en desaparecer la cruz, más rápida es la reacción. Existe una
proporcionalidad inversa entre tiempo y velocidad de reacción. Tomaremos, entonces, como medida
de la velocidad de la reacción la inversa del tiempo tardado en cada ensayo, en segundos.
TABLA 2
tiempo tardado (s) velocidad de reacción (s-1)
ensayo 1
ensayo 2
ensayo 3
ensayo 4
b) Cálculo de la concentración, expresada como molaridad, del tiosulfato sódico en disolución.
Con ayuda de la tabla 3 calcularemos la concentración de tiosulfato [Na 2S2O3] expresada como
molaridad.
TABLA 3.
cem V1 (L) masa Na2S2O3 , g cantidad química V3 (L) [Na2S2O3], mol/L
Na2S2O3 , mol
ensayo 1 0,05
ensayo 2 0,05
40 g/L
ensayo 3 0,05
ensayo 4 0,05
c) Cálculo de la constante cinética y del orden parcial de reacción respecto al tiosulfato sódico
Para hacer los cálculos indicados, tomaremos logaritmos neperianos en la expresión de la velocidad
de reacción ln r=ln k +m . ln [ Na S O ]
1 2 2 3
Hallaremos los logaritmos neperianos con ayuda de la tabla 4:
TABLA 4
r ln r : (eje Y) [Na2S2O3] ln [Na2S2O3]: (eje X)
ensayo 1
ensayo 2
ensayo 3
ensayo 4
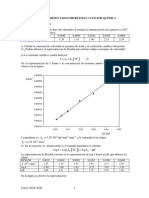
Al representar, en abcisas, el neperiano de la concentración y, en ordenadas, el neperiano de la
velocidad de la reacción, nos debe salir -si todo está bien hecho- una línea recta. De la ordenada en
el origen hallaremos el logaritmo neperiano de la constante cinética; de la pendiente, el orden de
reacción respecto al tiosulfato de sodio. El ajuste por mínimos cuadrados permite encontrar la recta
que mejor ajusta los datos. La ecuación de la recta viene dada por
∑ x.y −̄x . ̄y
σy n
y− ̄y =CC σ ( x−̄x ) con CC=
x σx . σ y
donde x y y son los valores medios de x e y , respectivamente, n el número de péndulos
utilizados, σx y σy son las desviaciones típicas de x e y .
x = ln [Na2S2O3] y = ln r x.y
ensayo 1
ensayo 2
ensayo 3
ensayo 4
x= y= Σ( x.y )
=
n
σx = σy =
CC = _________ ; ln r = ________ . ln [Na2S2O3] + ________
5.1. NUEVA OBTENCIÓN DE DATOS.
2ª EXPERIENCIA: INFLUENCIA DE LA TEMPERATURA
En esta segunda parte, repetimos la experiencia sin modificar la concentración de los reactivos, y
solo variando la temperatura de la reacción. Gracias a un calefactor eléctrico, calentaremos agua
hasta unos 80ºC, aproximadamente, e iremos tomando las cantidades que se indican a continuación.
TABLA 5
V1 = V2=volumen V3=volumen V4= volumen volumen de Temperatura Tiempo
volumen agua caliente agua fría total HCl (mL) tardado
Na2S2O3 (tiosulfato+agua)
ensayo 1 20 mL 30 mL 0 mL 50 mL 6 mL
ensayo 2 20 mL 20 mL 10 mL 50 mL 6 mL
ensayo 3 20 mL 10 mL 20 mL 50 mL 6 mL
*
ensayo 4 20 mL 0 mL 30 mL 50 mL 6 mL
* Este ensayo es el ensayo 4 de la tabla I (se puede repetir para comprobar o utilizar el valor
previamente hallado)
5.2. TRATAMIENTO DE LOS DATOS OBTENIDOS
Seguimos trabajando con la ecuación cinética.
m
r =k 1 [Na2 S2 O3 ]
En esta nueva experimentación, la concentración de tiosulfato es siempre la misma. La variación de
la velocidad de la reacción se debe a que la constante cinética depende de la temperatura de acuerdo
con la ecuación de Arrhenius: −E a
k 1=A . e RT
siendo Ea la energía de activación, R la constante de los gases expresada en términos de energía y T
la temperatura absoluta.
a) Cálculo de la velocidad de la reacción.
Cuánto menos tiempo tarda en desaparecer la cruz, más rápida es la reacción. Existe una
proporcionalidad inversa entre tiempo y velocidad de reacción. Tomaremos, entonces, como medida
de la velocidad de la reacción la inversa del tiempo tardado en cada ensayo, en segundos.
TABLA 6
tiempo tardado (s) velocidad de reacción (s-1)
ensayo 1
ensayo 2
ensayo 3
ensayo 4
b) Cálculo de la concentración, expresada como molaridad, del tiosulfato sódico en disolución.
Con ayuda de la tabla 5 calcularemos la concentración de tiosulfato [Na 2S2O3] expresada como
molaridad. TABLA 7.
cem V1 (L) masa Na2S2O3 , g cantidad química V4 (L) [Na2S2O3], mol/L
Na2S2O3 , mol
ensayos
40 g/L 20 mL 0,05
1,2,3,4
c) Cálculo de la constante cinética
Conocidas las velocidades de reacción, la concentración de tiosulfato de sodio y el orden de
reacción, se calculan las diferencias constantes cinéticas. r =k [Na S O ]m
1 2 2 3
TABLA 8
r [Na2S2O3]m Temperatura k1
ensayo 1
ensayo 2
ensayo 3
ensayo 4
d) Cálculo de la energía de activación, Ea, y del factor de partición, A
Al representar, en abcisas, la inversa de la temperatura absoluta (1/T) y, en ordenadas, el neperiano
de la constante cinética, ln k1, nos debe salir -si todo está bien hecho- una línea recta.
−Ea Ea
ln k1 =ln A −
k 1=A . e RT RT
De la ordenada en el origen hallaremos el logaritmo neperiano de A; de la pendiente (-Ea/R) se
podrá sacar la energía de activación. El ajuste por mínimos cuadrados permite encontrar la recta que
mejor ajusta los datos. La ecuación de la recta viene dada por
σy
∑ x.y −̄x . ̄y
y− ̄y =CC σ ( x−̄x ) con n
x CC=
σx . σ y
donde x y y son los valores medios de x e y , respectivamente, n el número de péndulos
utilizados, σx y σy son las desviaciones típicas de x e y .
x = 1/T y = ln k1 x.y
ensayo 1
ensayo 2
ensayo 3
ensayo 4
x= y= Σ( x.y )
=
n
σx = σy =
CC = _________ ; ln k1 = ________ .1/T + ________
S-ar putea să vă placă și
- Informe de Laboratorio - Cinética QuímicaDocument28 paginiInforme de Laboratorio - Cinética QuímicaSTEPHANIE MILAGROS AVILA ALANYAÎncă nu există evaluări
- Cinética de La Reacción de Oxidación Del Ion Yoduro Por Ion PersulfatoDocument10 paginiCinética de La Reacción de Oxidación Del Ion Yoduro Por Ion PersulfatoninnaesolfenÎncă nu există evaluări
- Guia 02 Soluciones BufferDocument6 paginiGuia 02 Soluciones Bufferalanys amado0% (1)
- Cinetica de Descomposicion Del TiosulftoDocument9 paginiCinetica de Descomposicion Del TiosulftobeatrizÎncă nu există evaluări
- EjerciciosDocument9 paginiEjerciciosDENNIS - CONDORIÎncă nu există evaluări
- Comp1 Dismutacion Correccion EZP ZN - NH3Document3 paginiComp1 Dismutacion Correccion EZP ZN - NH3Rafael GonzálezÎncă nu există evaluări
- Practica Nro.02 Analisis InstrumentalDocument30 paginiPractica Nro.02 Analisis InstrumentalSeili Espinoza CarrilloÎncă nu există evaluări
- Informe 3 Quimica LabDocument7 paginiInforme 3 Quimica LabJuanÎncă nu există evaluări
- ProblemasdeLeydeCoulomb Martes 20 de FebreroDocument1 paginăProblemasdeLeydeCoulomb Martes 20 de Febreroeduc2008100% (1)
- ColigatDocument47 paginiColigatTakshivana Navarro Flores100% (1)
- Actividad 2 Tabla PeriodicaDocument6 paginiActividad 2 Tabla PeriodicaestefaniaÎncă nu există evaluări
- Acido Base Prueba de Nivel 2Document6 paginiAcido Base Prueba de Nivel 2Juancho JuarezÎncă nu există evaluări
- Enlace QuímicoDocument12 paginiEnlace QuímicoAbigail AC100% (1)
- Tema 6, Tema 7 Alquinos SN1 y SN2 20 Mayo 2020Document17 paginiTema 6, Tema 7 Alquinos SN1 y SN2 20 Mayo 2020Alan YañezÎncă nu există evaluări
- Examenes Quimica AnaliticaDocument37 paginiExamenes Quimica AnaliticaHarold Cesar Gabriel HerreraÎncă nu există evaluări
- Guía N°3 de Ejercicios (Reactivo Limitante, Reactivo en Exceso, Calculo de Productos y Rendimiento)Document2 paginiGuía N°3 de Ejercicios (Reactivo Limitante, Reactivo en Exceso, Calculo de Productos y Rendimiento)Constanza ArancibiaÎncă nu există evaluări
- Prueba Disoluciones Unidades de Concentración II 2° Medio Fila BDocument2 paginiPrueba Disoluciones Unidades de Concentración II 2° Medio Fila BDaniela Andrea Aros BarriosÎncă nu există evaluări
- Guia de Ejercicios Soluciones y Propiedades ColigativasDocument4 paginiGuia de Ejercicios Soluciones y Propiedades Coligativasmartin muñoz0% (1)
- Demanda de Oxígeno PDFDocument4 paginiDemanda de Oxígeno PDFLu UrdialesÎncă nu există evaluări
- Química Analítica CualitativaDocument65 paginiQuímica Analítica Cualitativa1394203031Încă nu există evaluări
- Taller 11 ReaccionesDocument5 paginiTaller 11 ReaccionesJaime Cervantes HernandezÎncă nu există evaluări
- Solucion Leccion 6Document15 paginiSolucion Leccion 6DanielÎncă nu există evaluări
- Hidrolisis Del Cristal VioletaDocument8 paginiHidrolisis Del Cristal VioletaJosep LopezÎncă nu există evaluări
- SensibilidadDocument11 paginiSensibilidadRoxii WojtuñÎncă nu există evaluări
- Tema 5 - EquilibrioDocument30 paginiTema 5 - Equilibrioandres guerreroÎncă nu există evaluări
- Informe Sulfato de Tetramin Cobre IIDocument6 paginiInforme Sulfato de Tetramin Cobre IIJuan VillavicencioÎncă nu există evaluări
- Complejos de Cobre IIDocument6 paginiComplejos de Cobre IIRodrigo Iriarte GomezÎncă nu există evaluări
- Primera Evaluacion de Quimica InorganicaDocument2 paginiPrimera Evaluacion de Quimica InorganicaJoselyne PerezÎncă nu există evaluări
- Tarea Cinética Enzimática IIIPAC-2020 PDFDocument11 paginiTarea Cinética Enzimática IIIPAC-2020 PDFKatherine SusethÎncă nu există evaluări
- Informe 1..Document3 paginiInforme 1..julian realpeÎncă nu există evaluări
- P5 Marcha de Cationes Del Grupo IIDocument18 paginiP5 Marcha de Cationes Del Grupo IIFabio Tello ChapoñanÎncă nu există evaluări
- Análisis Retrosintético-5Document8 paginiAnálisis Retrosintético-5Luisa CausilÎncă nu există evaluări
- Exercicis Disolucions Ahikar Nadal 2019Document4 paginiExercicis Disolucions Ahikar Nadal 2019FattyÎncă nu există evaluări
- Evaluación Ácido Carboxílicos PDFDocument4 paginiEvaluación Ácido Carboxílicos PDFDiana MuñozÎncă nu există evaluări
- Taller Cinetica QuimicaDocument6 paginiTaller Cinetica Quimicaapi-241769574Încă nu există evaluări
- Fijas de QuimicaDocument5 paginiFijas de QuimicaGonzalo Humberto Quispe HuaranccaÎncă nu există evaluări
- PRACTICA 1 ElectrolitosDocument9 paginiPRACTICA 1 ElectrolitosSaúl RodríguezÎncă nu există evaluări
- Informe Final - Celdas ElectroquímicasDocument6 paginiInforme Final - Celdas ElectroquímicasNICOLH DAYANA ENRIQUEZ ROCHA100% (1)
- Informe #6Document6 paginiInforme #6Limey JuniorÎncă nu există evaluări
- Parcial 1 QuimicaorgDocument21 paginiParcial 1 QuimicaorgDebbie Fernandez0% (2)
- Inorganica 4Document6 paginiInorganica 4emilyÎncă nu există evaluări
- Seminario 1 QFDocument5 paginiSeminario 1 QFSimsmaniaco InserteApellidoÎncă nu există evaluări
- Práctica 6 - Titulación Por Retroseso, Factores de DiluciónDocument5 paginiPráctica 6 - Titulación Por Retroseso, Factores de Diluciónalbina vargasÎncă nu există evaluări
- Guia de Ejercicios 530024 2TDocument8 paginiGuia de Ejercicios 530024 2TJerico JosuéÎncă nu există evaluări
- Práctica Velocidad DelDocument4 paginiPráctica Velocidad DelLuis Alfonso del Río CovarrubiasÎncă nu există evaluări
- Práctica #1Document5 paginiPráctica #1Cristina Cardona BermudezÎncă nu există evaluări
- GUIA Laboratorio CineticaDocument2 paginiGUIA Laboratorio CineticamorrantiaoÎncă nu există evaluări
- Informe de Laboratorio - Cinetica QuimicaDocument5 paginiInforme de Laboratorio - Cinetica QuimicaEliana Duette100% (1)
- Informe 4 Miranda Bravo Diego Mendez y Martin BelmarDocument10 paginiInforme 4 Miranda Bravo Diego Mendez y Martin BelmarMartín Aníbal BelmarÎncă nu există evaluări
- Trabajo Práctico #9 Cinética QuímicaDocument11 paginiTrabajo Práctico #9 Cinética QuímicaPau ZalazarÎncă nu există evaluări
- Manual Practicas - CinéticaDocument24 paginiManual Practicas - CinéticaFernando GonzalezÎncă nu există evaluări
- Hidrolisis Acida de Acetato de EtiloDocument14 paginiHidrolisis Acida de Acetato de Etilokarina huayhuaÎncă nu există evaluări
- TP CineticaDocument5 paginiTP CineticaAixa RafaelaÎncă nu există evaluări
- Yodinacion CetonaDocument6 paginiYodinacion CetonaemerengiÎncă nu există evaluări
- Yodinación de La AcetonaDocument6 paginiYodinación de La AcetonaALEXIS CAMILO ARCOS CATUCHEÎncă nu există evaluări
- 2oxidacion Del Yoduro Con PersulfatoDocument30 pagini2oxidacion Del Yoduro Con PersulfatoJuniorRomeroÎncă nu există evaluări
- Manual de Prácticas - Cinética QuímicaDocument24 paginiManual de Prácticas - Cinética QuímicaRicardo Alfonso Trujillo SantillanaÎncă nu există evaluări
- Quimica-Semana 06 MD3N5Document13 paginiQuimica-Semana 06 MD3N5Piero TorresÎncă nu există evaluări
- Prã Ctica 02 Cinã Tica Quã MicaDocument5 paginiPrã Ctica 02 Cinã Tica Quã MicaPaul Elvis Murillo CaceresÎncă nu există evaluări
- Práctica 02 Cinética QuímicaDocument5 paginiPráctica 02 Cinética QuímicaJordy Castillon Manosalva100% (1)
- Campos Delgado Cristhian 3ER PRACAL - IX - PRACTICAS PRE-PROFESIONALESDocument3 paginiCampos Delgado Cristhian 3ER PRACAL - IX - PRACTICAS PRE-PROFESIONALEScristian camposÎncă nu există evaluări
- Clasificacion de RAM Segun OMS Casos ClinicosDocument10 paginiClasificacion de RAM Segun OMS Casos Clinicoscristian camposÎncă nu există evaluări
- Toxicolo 7 TrabajoDocument2 paginiToxicolo 7 Trabajocristian camposÎncă nu există evaluări
- Introducción: XVI Encuentro de Economía PúblicaDocument29 paginiIntroducción: XVI Encuentro de Economía Públicacristian camposÎncă nu există evaluări
- Ejemplos de RamsDocument12 paginiEjemplos de Ramscristian camposÎncă nu există evaluări
- Administración Es Arte o CienciaDocument1 paginăAdministración Es Arte o Cienciacristian camposÎncă nu există evaluări
- Esquema de Proyecto de Tesis - Ep FB - NH 2021 IIDocument7 paginiEsquema de Proyecto de Tesis - Ep FB - NH 2021 IIcristian camposÎncă nu există evaluări
- Tranquilizantes Mayores y Menores IDocument14 paginiTranquilizantes Mayores y Menores Icristian camposÎncă nu există evaluări
- Trabajo AdrenérgicosDocument13 paginiTrabajo Adrenérgicoscristian camposÎncă nu există evaluări
- TOXICOLOGÍA MEDIO AMBIENTAL - pdf-1-2Document2 paginiTOXICOLOGÍA MEDIO AMBIENTAL - pdf-1-2cristian camposÎncă nu există evaluări
- ManualDocument78 paginiManualcristian camposÎncă nu există evaluări
- Interacciones Medicamentosas - UapDocument18 paginiInteracciones Medicamentosas - Uapcristian camposÎncă nu există evaluări
- Problemas Programación LinealDocument3 paginiProblemas Programación LinealThaliaVillegasÎncă nu există evaluări
- Tarea de Dibujo 2Document11 paginiTarea de Dibujo 2Jesus Alfredo Vasquez LucasÎncă nu există evaluări
- Problemas Resueltos de Física 1Document16 paginiProblemas Resueltos de Física 1Amanda CohenÎncă nu există evaluări
- Laboratorio FIQUI 1Document28 paginiLaboratorio FIQUI 1fernando hectorÎncă nu există evaluări
- 1-Defnición de Los TrabajosDocument23 pagini1-Defnición de Los Trabajospablo puñalÎncă nu există evaluări
- Laguna TragaderoDocument3 paginiLaguna TragaderoAlex HuamaniÎncă nu există evaluări
- Ficha Tecnica Trituradora RS150Document6 paginiFicha Tecnica Trituradora RS150Mario CastilloÎncă nu există evaluări
- Desmi Rotan PDFDocument16 paginiDesmi Rotan PDFDiego Alejandro HerreraÎncă nu există evaluări
- Tipos de TablerosDocument51 paginiTipos de TablerosRaul HERNÁNDEZÎncă nu există evaluări
- ACFrOgB0Tg R4 Em7Uwvej0PoLjxTuUteImnPHiCCFGl36eBSD7ejbMMumJsAvk1hhp0nxcvzg2yHZnLTzBho3pCIc0unQMHQqy6NXqtiEL o9PPLABMbg NT ZtQ4AWWZFfwOf5cpGmQHpbyr1Document5 paginiACFrOgB0Tg R4 Em7Uwvej0PoLjxTuUteImnPHiCCFGl36eBSD7ejbMMumJsAvk1hhp0nxcvzg2yHZnLTzBho3pCIc0unQMHQqy6NXqtiEL o9PPLABMbg NT ZtQ4AWWZFfwOf5cpGmQHpbyr1SEBASTIAN RODRIGO CHAVEZ RAMOSÎncă nu există evaluări
- Practica 01 ResueltaDocument15 paginiPractica 01 ResueltaSilvio Ramon MateoÎncă nu există evaluări
- Reporte Diario 22-08Document3 paginiReporte Diario 22-08Hugo Juan Justo ApazaÎncă nu există evaluări
- Moran Ortiz Amador: Total $1,612.49Document2 paginiMoran Ortiz Amador: Total $1,612.49David RicardoÎncă nu există evaluări
- Catalogo Bormas Viking 3 LegrandDocument35 paginiCatalogo Bormas Viking 3 LegrandJefferson Andrade PereiraÎncă nu există evaluări
- FTIR ASTM E2412 ViernesDocument7 paginiFTIR ASTM E2412 Viernesjimy.taipe.pÎncă nu există evaluări
- Prelectio 2Document1 paginăPrelectio 2Alfonso García NietoÎncă nu există evaluări
- U-5.2 VIENTOS Consideraciones GeneralesDocument12 paginiU-5.2 VIENTOS Consideraciones GeneralesLeonardo BarreraÎncă nu există evaluări
- Manual CBMDocument80 paginiManual CBMAnibal RiosÎncă nu există evaluări
- Tarea - 3 - Modelado de Sistema Inalámbrico Con Nodos Sensor y ActuadorDocument34 paginiTarea - 3 - Modelado de Sistema Inalámbrico Con Nodos Sensor y ActuadorLuisÎncă nu există evaluări
- Los Hidrocarburos (Alcanos, Alquenos y Alquinos) Propiedades, Reacciones y Metodos de ObtencionDocument36 paginiLos Hidrocarburos (Alcanos, Alquenos y Alquinos) Propiedades, Reacciones y Metodos de ObtencionYonar Shmit Gallo QuispeÎncă nu există evaluări
- 1-Diapositivas de Mortero y Sello Asfaltico1Document67 pagini1-Diapositivas de Mortero y Sello Asfaltico1Huaquisto BrigÎncă nu există evaluări
- Taller # 2 Formulación de Modelos de Programacion LinealDocument1 paginăTaller # 2 Formulación de Modelos de Programacion LinealVictor GonzalezÎncă nu există evaluări
- Informe 7 Laboratorio de FisicaDocument8 paginiInforme 7 Laboratorio de Fisicaliana.runte393Încă nu există evaluări
- Ejer Cici OsDocument92 paginiEjer Cici OsGleny Fernandez Requejo67% (3)
- Tomo 2Document5 paginiTomo 2Mario FernandoÎncă nu există evaluări
- Anexo Registros de Medidores (1) - 1 PDFDocument12 paginiAnexo Registros de Medidores (1) - 1 PDFJef PeñÎncă nu există evaluări
- ETO090Document6 paginiETO090jorgedarioayub100% (1)
- PDF Materiales Inteligentes CompressDocument6 paginiPDF Materiales Inteligentes CompressAbel OrozcoÎncă nu există evaluări
- Epson Secuencia de ServicioDocument6 paginiEpson Secuencia de ServicioRoberto Pro BuzÎncă nu există evaluări