Documente Academic
Documente Profesional
Documente Cultură
Obtencion Del Amoniaco
Încărcat de
Andres R. AñezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Obtencion Del Amoniaco
Încărcat de
Andres R. AñezDrepturi de autor:
Formate disponibile
OBTENCION DEL AMONIACO
El amoníaco es un compuesto químico con la fórmula NH3. El amoníaco, en disolución acuosa
puede actuar como base, agregando un átomo de hidrógeno y transformándose en el catión
amonio NH4+.
CARACTERISTICAS:
• Gas incoloro
• Olor característico por lo nauseabundo y penetrante
• A temperatura ambiente se disuelve fácilmente en agua y se evapora con rapidez
Se produce de manera natural y a nivel industrial:
a) De manera natural: por bacterias que se encuentran en el suelo, y que degradan la
materia orgánica proveniente de desechos de animales, y plantas y animales muertos.
b) b) De manera industrial: Una cantidad de amoníaco similar a la producida
naturalmente es obtenida anualmente de manera industrial. La mayor parte del
amoníaco obtenido de esta manera se destina a la producción de fertilizantes. En
menor proporción, se utiliza en producción de productos de limpieza, refrigerantes,
alimentos, bebidas entre otros.
c) Obtención de amoníaco a nivel industrial. -El proceso mediante el cual se obtiene
amoníaco obtiene su nombre de los químicos que lo idearon: Fritz Haber y Carl
Bosch. Este proceso es el resultado de la combinación directa entre el nitrógeno
(proveniente de la atmósfera) y el hidrógeno (proveniente del gas natural), ambos en
estado gaseoso:
d) N2(g) + 3H2(g) → 2NH3(g)
Esta reacción ocurre con lentitud, dado que necesita gran cantidad de energía de activación,
como consecuencia de la estabilidad química del nitrógeno. Para acelerar la reacción se utiliza
un catalizador, y se aumenta la presión y la temperatura a la que esta ocurre.
De esta manera las moléculas gaseosas tienen mayor energía cinética, aumentando la
velocidad con que reaccionan. Además, al retirar el amoníaco a medida que se va formando, se
acelera aún más la producción del mismo.
La presión aplicada para mejorar el rendimiento de esta reacción puede llegar hasta las 900
atmósferas. Con esta presión, a una temperatura de 450 o 500 grados C, el rendimiento de la
reacción puede ser del 40%.
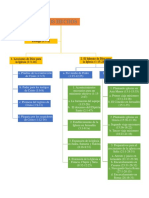
PROCESO DE PRODUCCION DEL AMONIACO. –
Desulfuración. -Antes del reformado tenemos que eliminar el S que contiene el gas
natural, dado que la empresa distribuidora le añade compuestos orgánicos de S para
olorizarlo.
R-SH + H2 RH + H2S hidrogenación
H2S + ZnO H2O + ZnS absorción
Reformado. -Una vez adecuado el gas natural se le somete a un reformado catalítico con
vapor de agua (craqueo- rupturas de las moléculas de CH4). El gas natural se mezcla con
vapor en la proporción (1 : 3,3)-(gas : vapor) y se conduce al proceso de reformado, el cual
se lleva a cabo en dos etapas:
Reformador primario.
Reformador secundario.
Purificación.-El proceso de obtención de NH3 requiere un gas de síntesis de gran
pureza, por ello se debe eliminar los gases CO y CO2.
Etapa de conversión.-Tras enfriar la mezcla se conduce a un convertidor donde el CO
se transforma en CO2 por reacción con vapor de agua,
CO + H2O ↔ CO2 + H2
esta reacción requiere de un catalizador que no se desactive con el CO.
Etapa de eliminación del CO2.-Seguidamente el CO2 se elimina en una torre con
varios lechos mediante absorción con K2CO3 a contracorriente, formándose
KHCO3 según
K2CO3 + CO2 + H2O 2KHCO3
este se hace pasar por dos torres a baja presión para desorber el CO2, el bicarbonato
pasa a carbón liberando CO2.
Etapa de metanización.-Las trazas de CO (0,2%) y CO2 (0,09%), que son
peligrosas para el catalizador del reactor de síntesis, se convierten en CH4:
CO + 3H2 CH4 + H2O
CO2 + H2 CH4 + 2H2O
Síntesis de amoníaco.-Así se obtiene un gas de síntesis con restos de CH4 y Ar
que actúan como inertes.
A continuación el gas se comprime a la presión de 200 atm. aproximadamente
(compresor centrífugo con turbina de vapor) y se lleva al reactor donde tiene
lugar la producción del amoníaco, sobre un lecho catalítico de Fe.
N2 (g) + 3 H2 (g) 2 NH3 (g)
En un solo paso por el reactor la reacción es muy incompleta con un rendimiento del
14-15%. Por tanto, el gas de síntesis que no ha reaccionado se recircula al reactor
pasando antes por dos operaciones,
extracción del amoníaco mediante una condensación.
eliminación de inertes mediante una purga, la acumulación de inertes es mala
para el proceso. El gas de purga se conduce a la unidad de recuperación
Ar para comercializarse
CH4 se utiliza como fuente de energía
N2 y H2 se introducen de nuevo en el bucle de síntesis
S-ar putea să vă placă și
- Sintesis Del MetanolDocument2 paginiSintesis Del MetanolJose Maria Herrera SaraviaÎncă nu există evaluări
- 4 60felderDocument1 pagină4 60felderDavid ZamoraÎncă nu există evaluări
- BalanceDocument8 paginiBalanceAlex Pascual ToapantaÎncă nu există evaluări
- Tarea 3-Equilibrio QuimicoDocument12 paginiTarea 3-Equilibrio QuimicoAnthonyÎncă nu există evaluări
- Comparación de Las Tecnologías para La Obtención Del SyngasDocument27 paginiComparación de Las Tecnologías para La Obtención Del SyngasfihioÎncă nu există evaluări
- Incertidumbre ASTM D - 524 - Pedro SaavedraDocument8 paginiIncertidumbre ASTM D - 524 - Pedro Saavedrapedro javier saavedra martinezÎncă nu există evaluări
- Práctica N°5Document8 paginiPráctica N°5RAMIRO BLANCOÎncă nu există evaluări
- Humidificación, SecadoDocument11 paginiHumidificación, SecadoAlvaro Pacheco0% (1)
- Ejercicio 1 RefrigeracionDocument6 paginiEjercicio 1 RefrigeracionBoris Camata ArroyoÎncă nu există evaluări
- Transporte y LmacenajeDocument8 paginiTransporte y Lmacenajeadolfo mier rivaÎncă nu există evaluări
- Instrumentacion T Lazos de Control Reactor IsotermicoDocument9 paginiInstrumentacion T Lazos de Control Reactor IsotermicoJorge Guanare100% (1)
- Ejercicio de Fraccionamiento de CrudoDocument12 paginiEjercicio de Fraccionamiento de CrudoBryan Keny CeronÎncă nu există evaluări
- Dr. Saúl Escalera GN en Bolivia Cátedra LibreDocument77 paginiDr. Saúl Escalera GN en Bolivia Cátedra LibreOswaldo CondarcoÎncă nu există evaluări
- Capitulo Iii - Simulación de Transporte de Fluidos en Flujo Estacionario para Poliductos y Oleoductos 2021Document32 paginiCapitulo Iii - Simulación de Transporte de Fluidos en Flujo Estacionario para Poliductos y Oleoductos 2021NeylaÎncă nu există evaluări
- Problemas RQ 10 - 11Document29 paginiProblemas RQ 10 - 11Carlos Camacho CaeroÎncă nu există evaluări
- DFP Acido SulfuricoDocument24 paginiDFP Acido SulfuricoKimberly AndradeÎncă nu există evaluări
- Cap 7 EndulzamientoDocument20 paginiCap 7 EndulzamientoRichard Caparicona MamaniÎncă nu există evaluări
- INFORMEDocument29 paginiINFORMEJhonny RodriguezÎncă nu există evaluări
- Balance de Materia y EnergiaDocument2 paginiBalance de Materia y EnergiaAndre Rojas100% (1)
- PROBLEMARIO TERMODINÁMICA 2. Mezclas Multicomponentes y FugacidadDocument3 paginiPROBLEMARIO TERMODINÁMICA 2. Mezclas Multicomponentes y FugacidadVíctor Hugo Castro TavaresÎncă nu există evaluări
- Proyecto Proceso Producción de AmoniacoDocument5 paginiProyecto Proceso Producción de AmoniacoyahuinzicÎncă nu există evaluări
- Otros ExamnesDocument9 paginiOtros ExamnesEliseo FloresÎncă nu există evaluări
- Cianuro de HidrogenoDocument15 paginiCianuro de HidrogenoerikÎncă nu există evaluări
- Tema 1 El Gas NaturalDocument40 paginiTema 1 El Gas NaturalrobertÎncă nu există evaluări
- Proceso GirbotolDocument7 paginiProceso GirbotolVirnia Patzi100% (2)
- Cap.5 Sistemas MulticomponenteDocument62 paginiCap.5 Sistemas MulticomponenteestefaniaÎncă nu există evaluări
- Obtencion de HidrogenoDocument22 paginiObtencion de HidrogenoHidrosouth SpaÎncă nu există evaluări
- Proyecto de TesisDocument15 paginiProyecto de TesisMarcoDulongJaraÎncă nu există evaluări
- Labo 6 Uni 2Document15 paginiLabo 6 Uni 2alexofigurinÎncă nu există evaluări
- Capitulo 3Document23 paginiCapitulo 3William BernalÎncă nu există evaluări
- CUESTIONARIO Práctica 4Document2 paginiCUESTIONARIO Práctica 4Jefte Martínez GarcíaÎncă nu există evaluări
- Guia - de - Ejercicios Cientifico - El - Estado - Gaseoso - IiDocument9 paginiGuia - de - Ejercicios Cientifico - El - Estado - Gaseoso - IiJoselo MamaniÎncă nu există evaluări
- Cuestionario de Lab de Operaciones Unitarias IIDocument19 paginiCuestionario de Lab de Operaciones Unitarias IIIsabel Cl50% (2)
- Ecuaciones Fases YassDocument17 paginiEcuaciones Fases YassSara Vera TorresÎncă nu există evaluări
- Presentacion Ley 767Document11 paginiPresentacion Ley 767RamiroUluriMamaniÎncă nu există evaluări
- Problemas de Difusión MolecularDocument2 paginiProblemas de Difusión MolecularAlexis John Soncco HanccoÎncă nu există evaluări
- Determinacion de La Cantidad de Agua en El Gas NaturalDocument4 paginiDeterminacion de La Cantidad de Agua en El Gas NaturalLuis Chino SarsuriÎncă nu există evaluări
- Proceso Fischer TropschDocument17 paginiProceso Fischer TropschHeidy LeonÎncă nu există evaluări
- Ingenieria Unidades de Deshidratacion de Gas NaturalDocument57 paginiIngenieria Unidades de Deshidratacion de Gas NaturalMauricio E Campo RÎncă nu există evaluări
- Diagrama TernarioDocument20 paginiDiagrama TernarioH Marquez R Graciela100% (1)
- Ecuaciones de HETPDocument4 paginiEcuaciones de HETPYeilis VelasquezÎncă nu există evaluări
- Dimetil Eter en BoliviaDocument6 paginiDimetil Eter en BoliviaFlores Toroya Paulino0% (1)
- Visita A Planta Separadora de Líquidos Carlos Villegas QuirogaDocument5 paginiVisita A Planta Separadora de Líquidos Carlos Villegas QuirogaJuan José Tirado BalcasÎncă nu există evaluări
- Proceso Urea 2000 PlisDocument4 paginiProceso Urea 2000 PlisDiana Sofía Revilla OrbegozoÎncă nu există evaluări
- Laboratorio Teorico, PasaporteDocument6 paginiLaboratorio Teorico, PasaporteJuan GudielÎncă nu există evaluări
- Informe de Endulzamiento Del Gas NaturalDocument27 paginiInforme de Endulzamiento Del Gas NaturalJhoss MateoÎncă nu există evaluări
- Capítulo 2 - Propiedades Termodinamicas de Los Gases y VaporesDocument56 paginiCapítulo 2 - Propiedades Termodinamicas de Los Gases y VaporesEdgar GutierrezÎncă nu există evaluări
- Sintesis Del MetanolDocument10 paginiSintesis Del MetanolSarita Marisol Aranda MauricioÎncă nu există evaluări
- Diseño y Simulacion Proyecto FinalDocument30 paginiDiseño y Simulacion Proyecto FinalL Roberto Bonilla EspinozaÎncă nu există evaluări
- Producción de Ácido Aspártico y Fenilalanina - Zucchi, Gabriel PabloDocument46 paginiProducción de Ácido Aspártico y Fenilalanina - Zucchi, Gabriel PabloGabriel ZucchiÎncă nu există evaluări
- Deshidratacion Del Gas Natural Con GlicolDocument3 paginiDeshidratacion Del Gas Natural Con GlicolTop ListÎncă nu există evaluări
- Ejercicio de ReaccionesDocument7 paginiEjercicio de ReaccionesGabriela MendezÎncă nu există evaluări
- Procesos Selexol y Girbotol 1Document10 paginiProcesos Selexol y Girbotol 1Andrea GarciaÎncă nu există evaluări
- Catalogo Orbis PDFDocument41 paginiCatalogo Orbis PDFJavier SeeberÎncă nu există evaluări
- Proceso de Producción de AmoníacoDocument15 paginiProceso de Producción de AmoníacocitlaliÎncă nu există evaluări
- AMONIACODocument2 paginiAMONIACOKatherine SalazarÎncă nu există evaluări
- DP Planta AmoniacoDocument17 paginiDP Planta AmoniacojluisvasquezcÎncă nu există evaluări
- Tema AmoniacoDocument31 paginiTema AmoniacoEdson EcosÎncă nu există evaluări
- Amoniaco AcidonitricoDocument15 paginiAmoniaco AcidonitricoDanny AndradeÎncă nu există evaluări
- Diagrama de Produccion de AmoniacoDocument8 paginiDiagrama de Produccion de AmoniacoSoraya Ochoa VillamizarÎncă nu există evaluări
- Arranque Con Inversor de GiroDocument4 paginiArranque Con Inversor de GiroAndres R. AñezÎncă nu există evaluări
- Presentación BEERDocument48 paginiPresentación BEERAndres R. AñezÎncă nu există evaluări
- Arranque Con Inversor de GiroDocument4 paginiArranque Con Inversor de GiroAndres R. AñezÎncă nu există evaluări
- Analisis de PestelDocument2 paginiAnalisis de PestelAndres R. AñezÎncă nu există evaluări
- DucalDocument51 paginiDucalAndres R. AñezÎncă nu există evaluări
- CROMATOGRAFIA de Capa FinaDocument9 paginiCROMATOGRAFIA de Capa FinaAndres R. AñezÎncă nu există evaluări
- Presentación BEERDocument48 paginiPresentación BEERAndres R. AñezÎncă nu există evaluări
- Tamiz Mezclado y MoliendaDocument12 paginiTamiz Mezclado y MoliendaAndres R. AñezÎncă nu există evaluări
- Aspectos de Seguridad en Los LaboratoriosDocument19 paginiAspectos de Seguridad en Los LaboratoriosAndres R. AñezÎncă nu există evaluări
- Desactivación de Reactivos QuímicosDocument30 paginiDesactivación de Reactivos QuímicosAndres R. AñezÎncă nu există evaluări
- Aspectos de Seguridad en Los LaboratoriosDocument19 paginiAspectos de Seguridad en Los LaboratoriosAndres R. AñezÎncă nu există evaluări
- Cromatografia de GasesDocument7 paginiCromatografia de GasesAndres R. AñezÎncă nu există evaluări
- Proyecto FinalDocument2 paginiProyecto FinalAndres R. AñezÎncă nu există evaluări
- ACS150 - Microconvertidor de FrecuenciaDocument1 paginăACS150 - Microconvertidor de FrecuenciaAndres R. AñezÎncă nu există evaluări
- PROYECTO FINAL-Panaderia Cuatro HermanosDocument25 paginiPROYECTO FINAL-Panaderia Cuatro HermanosAndres R. AñezÎncă nu există evaluări
- Planificacon de Las Politicas de InventarioDocument1 paginăPlanificacon de Las Politicas de InventarioAndres R. AñezÎncă nu există evaluări
- Proceso de Tratamiento de Agua - SaguapacDocument9 paginiProceso de Tratamiento de Agua - SaguapacAndres R. AñezÎncă nu există evaluări
- Proyecto de Estadistica UpsaDocument9 paginiProyecto de Estadistica UpsaAndres R. AñezÎncă nu există evaluări
- Sistema Gestion A La Calidad Proyecto FinalDocument30 paginiSistema Gestion A La Calidad Proyecto FinalAndres R. AñezÎncă nu există evaluări
- Residuos Toxicos Orgánicos e InorgánicosDocument6 paginiResiduos Toxicos Orgánicos e InorgánicosAndres R. AñezÎncă nu există evaluări
- Isa 5.5-1985Document50 paginiIsa 5.5-1985Andres R. Añez0% (1)
- BOROSCOPIODocument4 paginiBOROSCOPIOjulio vazques100% (1)
- MEDIDORES DE FLUJO y COMPUTADOR DE FLUJODocument12 paginiMEDIDORES DE FLUJO y COMPUTADOR DE FLUJOAndres R. AñezÎncă nu există evaluări
- Desactivación de Reactivos QuímicosDocument30 paginiDesactivación de Reactivos QuímicosAndres R. AñezÎncă nu există evaluări
- Unidad IDocument35 paginiUnidad IAndres R. AñezÎncă nu există evaluări
- Isa 5.5-1985Document50 paginiIsa 5.5-1985Andres R. Añez0% (1)
- Reactivos QuimicosDocument20 paginiReactivos QuimicosAndres R. Añez100% (1)
- Reactivos QuimicosDocument20 paginiReactivos QuimicosAndres R. Añez100% (1)
- Medidores de NivelDocument16 paginiMedidores de NivelAndres R. AñezÎncă nu există evaluări
- DISEÑO FINAL - Detallado 1 - 1584293590469Document6 paginiDISEÑO FINAL - Detallado 1 - 1584293590469Nicole Parada CabreraÎncă nu există evaluări
- Clase 4. Envejecimiento Activo y SaludableDocument22 paginiClase 4. Envejecimiento Activo y Saludablepatricio burgos cedeñoÎncă nu există evaluări
- Practica 13 Uroanalisis Grupo FDocument9 paginiPractica 13 Uroanalisis Grupo FYovani Salas VasquezÎncă nu există evaluări
- Parcial 2 - Unidad 3Document4 paginiParcial 2 - Unidad 3mercedes.fontaineÎncă nu există evaluări
- Permisos Trabajo de Especial PeligrosidadDocument25 paginiPermisos Trabajo de Especial PeligrosidadLUIS ALBERTO VENEGASÎncă nu există evaluări
- El Ascenso y Caida Final Del Rey Del Norte, Jeff PippengerDocument71 paginiEl Ascenso y Caida Final Del Rey Del Norte, Jeff PippengerHayber Jimenez100% (1)
- 1er Informe Texto H.schlierDocument2 pagini1er Informe Texto H.schlierBlas De Jesús Caba CornelioÎncă nu există evaluări
- Caso Clinicos Diabetes-15Document3 paginiCaso Clinicos Diabetes-15YomiraHuamaniSimonÎncă nu există evaluări
- Taller Analisis Vertival y HorizontalDocument1 paginăTaller Analisis Vertival y HorizontalZully Fontalvo100% (1)
- Introducción A La BiologíaDocument14 paginiIntroducción A La BiologíaenemeveÎncă nu există evaluări
- Clera 1683Document15 paginiClera 1683Dra PeñaÎncă nu există evaluări
- Igm I2022Document44 paginiIgm I2022Jairo CondoriÎncă nu există evaluări
- Esquema HechosDocument1 paginăEsquema HechosElíGómezÎncă nu există evaluări
- TEMA 4 BuenoDocument17 paginiTEMA 4 Buenojuan achaÎncă nu există evaluări
- PEC4 - Marta BattistellaDocument3 paginiPEC4 - Marta BattistellaKevin SarmientoÎncă nu există evaluări
- Enarm t1v RM Preguntas Enarm 13 WebDocument6 paginiEnarm t1v RM Preguntas Enarm 13 WebJulio César Valdivieso Aguirre100% (1)
- RFID FinalDocument23 paginiRFID FinalGro Gro100% (1)
- HISTOLOGIA 04 Sistema Linfatico y Organos LinfaticosDocument21 paginiHISTOLOGIA 04 Sistema Linfatico y Organos LinfaticosJose Miranda ChavezÎncă nu există evaluări
- PSC - U2 - A2 - More 04Document6 paginiPSC - U2 - A2 - More 04jose moreno100% (1)
- 0.4 The Moth & The Flame (The Wrath & The Dawn, #0.4) - Renée AhdiehDocument38 pagini0.4 The Moth & The Flame (The Wrath & The Dawn, #0.4) - Renée AhdiehDulceet LezamaÎncă nu există evaluări
- Las TIC en La Escuela Secundaria BonaerenseDocument165 paginiLas TIC en La Escuela Secundaria BonaerenseAdriana FavieriÎncă nu există evaluări
- Política InformáticaDocument11 paginiPolítica Informáticaanon_278407064100% (1)
- REVISTA OFICIAL - Porque Sois Fuertes-2Document59 paginiREVISTA OFICIAL - Porque Sois Fuertes-2David Delgado100% (1)
- Accidente Cantagallo 175-HDocument11 paginiAccidente Cantagallo 175-HJenifer Carolina Rojas RodríguezÎncă nu există evaluări
- Ampliacion de Plazo A La Orden de Servicio #484Document3 paginiAmpliacion de Plazo A La Orden de Servicio #484Susan Salazar VargasÎncă nu există evaluări
- Ciudad Lineal. Análisis ChingDocument3 paginiCiudad Lineal. Análisis ChingSuzettyParedesÎncă nu există evaluări
- ALCOHOLESDocument26 paginiALCOHOLESPaul Paz Cieza100% (3)
- INFORME 12 DE QUIMICA ORGANICA LLLDocument5 paginiINFORME 12 DE QUIMICA ORGANICA LLLGrace Castillo PerezÎncă nu există evaluări
- Test Creencias TipologicasDocument123 paginiTest Creencias TipologicasCamila Godoy Chávez100% (1)
- Conde LucanorDocument10 paginiConde LucanorCandela Garrido GarciaÎncă nu există evaluări
- 2 - Cuadernillo Integración Areal 2 - Profesorado de Historia - Prof. FloresDocument5 pagini2 - Cuadernillo Integración Areal 2 - Profesorado de Historia - Prof. FloresNatashaÎncă nu există evaluări