Documente Academic
Documente Profesional
Documente Cultură
7 Esterification
Încărcat de
sendibed0 evaluări0% au considerat acest document util (0 voturi)
88 vizualizări2 paginiTitlu original
7_esterification.doc
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOC, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOC, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
88 vizualizări2 pagini7 Esterification
Încărcat de
sendibedDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOC, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 2
Estérification
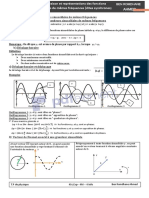
Exercice n° 1: On étudie expérimentalement la réaction d’estérification de l’acide éthanoïque par
l’éthanol. On
prépare dans un nA(mol)
ballon un
mélange
équimolaire
d’acide et
d’alcool. A une Fig
date t=0, ce 3
ballon est placé
dans un bain
marie porté à
80°C.
1°/ Ecrire 0,033
l’équation de la
réaction.
2°/En cours de
réaction, à
intervalles de téq
temps réguliers,
on a prélevé dans le mélange réactionnel de très petits échantillons de volume V connu, que l’on a
refroidit puis dosé avec une solution d’hydroxyde de sodium de concentration molaire C B =2mol.L-1
en présence de phénolphtaléine. On peut ainsi connaître l’évolution du nombre de mole n A de
l’acide éthanoïque dans le mélange réactionnel au cours du temps ce qui nous a permis de tracer
la courbe de nA = f(t) (Voir figure ci-dessus).
a- Représenter un schéma annoté du matériel utilisé au cours du dosage.
b- Comment peut-on détecter la fin du dosage ?
3°/ Déterminer:
a- La composition initiale du mélange.
b- La composition du mélange à l’équilibre.
4/ Donner les caractères de la réaction.
5/ Calculer le volume de base versée à l’équivalence lorsque le système a atteint son état
d’équilibre dynamique.
Exercice n :2 ( Bac 91 )
On prépare comme suit deux mélanges que l'on place dans deux ampoules A et B .
l'ampoule A contient : 0,30 mole d'un acide carboxylique R 1COOH et 0,30 mole d'un monoalcool
R2OH.
l'ampoule B contient : 0,60 mole du même acide et 0,30 mole du même alcool .
On scelle les ampoules et on les place dans une étuve à 800° C pendant un temps qui
permet d'atteindre les états d'équilibre dans les deux ampoules .
Ecrire l’équation de la réaction.
Si la réaction d'estérification était totale , combien obtiendrait-on de moles d'ester dans
chacune des deux ampoules ?
En est-il réellement ainsi ? justifier la réponse .
Dans quelle ampoule devrait-on avoir le plus d'ester ?
On dose à l'aide d'une solution de soude l'acide restant dans chacune des ampoules A et B
.
Le nombre de moles d'acide trouvé est respectivement nA = 0,10 et nB = 0,34 .Quelle est la
composition du mélange avant le dosage dans chaque ampoule ? En déduire la limite
d'estérification dans chaque cas en pourcentage d'alcool estérifié.
Exercice n :3
On réalise une réaction d’estérification en mélangeant à t=0 une masse m ac =12 g d’acide
éthanoïque et une masse mal= 12 g de propane-1-ol dans un Bécher auquel on ajoute quelques
gouttes d’acide sulfurique. Ce mélange est partagé d’une façon égale dans 10 tubes à essai. Les
tubes sont placés dans un bain marie de 80 °C
1- Montrer que le mélange initial d’acide et d’alcool est équimolaire. Calculer la composition
initiale dans chaque tube. On
donne MC = 12 g.mol-1 ; MO=16 nacide restant(10-3 mol)
g.mol MH= 1 g.mol .
-1 -1
2- Ecrire l’équation de la réaction.
3- Pour déterminer la composition )nac(
0
du mélange à une date t, on
dose l’acide restant par une
solution d’hydroxyde de sodium 1
M, l’indicateur coloré utilisé est la
phénolphtalèïne. Les résultats de
mesure sont traduits par le
graphe suivant :
a- Pourquoi a -t on chauffé le
mélange et quel est le rôle de
6,66
l’acide sulfurique ?
b- Comment peut-on connaître
expérimentalement le point
d’équivalence ? 2 t(min
c- Que représente la date t=160 )
min ? déterminer graphiquement 20
la quantité de matière d’acide
éthanoïque restant à la fin de la réaction. Déduire le nombre de mole d’ester formé.
d- Calculer le volume de soude Véq versé au cours du dosage à la date t=160 min.
Comparer les volumes V1 et V2 de soude versés respectivement aux dates t1 = 100 min
et t2 = 200 min au volume Véq.
e- Représenter sur le même graphe l’allure de la courbe représentant le nombre de mole
d’ester formé en fonction du temps nester = g(t).
S-ar putea să vă placă și
- Série 1Document4 paginiSérie 1Lamia ALACHAHER100% (1)
- Cours - Chimie ESTERIFICATION - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMIDocument2 paginiCours - Chimie ESTERIFICATION - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMIMohamed HamdeneÎncă nu există evaluări
- Applications de la spectrophotomérie en phytochimie: sciencesDe la EverandApplications de la spectrophotomérie en phytochimie: sciencesÎncă nu există evaluări
- Exercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFDocument5 paginiExercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFBouba KhedherÎncă nu există evaluări
- Chimie TD 3 Cinétique Chimique PDFDocument4 paginiChimie TD 3 Cinétique Chimique PDFOussama El BouadiÎncă nu există evaluări
- Amines - Acides CarboxyliquesDocument2 paginiAmines - Acides Carboxyliquesdiengsalla diengÎncă nu există evaluări
- AvancementDocument3 paginiAvancementbaatout oumaymaÎncă nu există evaluări
- Preparz Votre Baccalaureat Cinetique ChimiqueDocument4 paginiPreparz Votre Baccalaureat Cinetique ChimiquesdirianisÎncă nu există evaluări
- Bac Blanc 2 ts2 1Document5 paginiBac Blanc 2 ts2 1Amadou Makhtar SeckÎncă nu există evaluări
- Passage Der AcideDocument3 paginiPassage Der AcideBelgasem Assel100% (1)
- Série D'exercices N°7 - Chimie Série Physique Dipole RLC SCIENCE & MATH - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMI PDFDocument2 paginiSérie D'exercices N°7 - Chimie Série Physique Dipole RLC SCIENCE & MATH - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMI PDFAzizElheni100% (1)
- AFBF2021Document2 paginiAFBF2021Abdourahmane BaÎncă nu există evaluări
- C5 Sol Aqueuses WahabDiopDocument3 paginiC5 Sol Aqueuses WahabDiopGaye Bachir100% (1)
- 6-Acides CarboxyliquesDocument1 pagină6-Acides CarboxyliquesBen Slema AzizÎncă nu există evaluări
- TP 5 Quotient de ReactionDocument1 paginăTP 5 Quotient de Reactionparacetamol1000Încă nu există evaluări
- Les Acides Carboxyliques: L'idéal N'est Pas de Tout Faire, Mais de Bien Faire Ce Que L'on ConnaîtDocument4 paginiLes Acides Carboxyliques: L'idéal N'est Pas de Tout Faire, Mais de Bien Faire Ce Que L'on ConnaîtNjipnangÎncă nu există evaluări
- Alcools Amines Renf AT 22Document6 paginiAlcools Amines Renf AT 22Émile Michel FayeÎncă nu există evaluări
- Avancement D - Une RéactionDocument2 paginiAvancement D - Une RéactionchebbisÎncă nu există evaluări
- Les Equation BilanDocument3 paginiLes Equation Bilanآيكا الاميرÎncă nu există evaluări
- Renforcement PH - Acide Fort Et Tampon 2022Document5 paginiRenforcement PH - Acide Fort Et Tampon 2022GueyeÎncă nu există evaluări
- Alcools CoursDocument4 paginiAlcools CoursNEADJ100% (1)
- PhysiqueDocument3 paginiPhysiqueAbđė Ěł Łğđ100% (1)
- TD Alcools 2020 LSLL - Wahab DiopDocument2 paginiTD Alcools 2020 LSLL - Wahab DiopSeck MoustaphaÎncă nu există evaluări
- TD T5 PDFDocument2 paginiTD T5 PDFAbd Errezak ChahoubÎncă nu există evaluări
- Serie 1 E Et 2 E (Cinétique Chimique) PDFDocument9 paginiSerie 1 E Et 2 E (Cinétique Chimique) PDFbouaounÎncă nu există evaluări
- Conductim PDFDocument4 paginiConductim PDFMokhtarBensaidÎncă nu există evaluări
- TD Tampon 2013 lsll-WahabDiopDocument4 paginiTD Tampon 2013 lsll-WahabDiopFy EzahanaÎncă nu există evaluări
- Devoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Document3 paginiDevoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Moufida ZouaghiÎncă nu există evaluări
- TPC4Document2 paginiTPC4hhedfiÎncă nu există evaluări
- Serie TDDocument4 paginiSerie TDTaoufik Ez100% (1)
- Exercice IDocument15 paginiExercice IInes De Paul Feudjeu100% (1)
- Acides Bases PDFDocument8 paginiAcides Bases PDFHafidi AhmedÎncă nu există evaluări
- TSE ChimieDocument2 paginiTSE ChimieOumar TraoréÎncă nu există evaluări
- FICHE DE TP Eau de JavelDocument3 paginiFICHE DE TP Eau de JavelAbdelhamid ABDENNOURIÎncă nu există evaluări
- Al Canes 0607Document2 paginiAl Canes 0607PFEÎncă nu există evaluări
- TP Cinetique ChimiqueDocument1 paginăTP Cinetique ChimiqueAyoub GuerriÎncă nu există evaluări
- Chapitre 7, Transformations Spontanées Dans Les Piles Et Récupération de L'énergie, Activités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHIDDocument3 paginiChapitre 7, Transformations Spontanées Dans Les Piles Et Récupération de L'énergie, Activités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHIDaristide mabialaÎncă nu există evaluări
- TP2 ChimieDocument10 paginiTP2 ChimieHalima ZighÎncă nu există evaluări
- Caisse de Solidarite Du Groupe G3 Nioro Du RipDocument3 paginiCaisse de Solidarite Du Groupe G3 Nioro Du RipMohamed CoulibalyÎncă nu există evaluări
- TPCorrCeFe 4Document2 paginiTPCorrCeFe 4Amelie Pinchon100% (1)
- Correction TDDocument5 paginiCorrection TDBasmã AlilecheÎncă nu există evaluări
- Série D'exercices Conductance Et ConductivitéDocument2 paginiSérie D'exercices Conductance Et Conductivitéammoura youssefÎncă nu există evaluări
- Exercice 1: Dosage de L'iode: I-Préparation de La Solution de Thiosulfate de SodiumDocument4 paginiExercice 1: Dosage de L'iode: I-Préparation de La Solution de Thiosulfate de Sodiumkhaoula elhansaliÎncă nu există evaluări
- TD Acide CarboxyliqueDocument2 paginiTD Acide CarboxyliqueHamza Dicko100% (1)
- 08 09 Devoir N 01Document3 pagini08 09 Devoir N 01anon-280479100% (3)
- Acide Base Faible CoupleDocument5 paginiAcide Base Faible CoupleBicaba MarkissÎncă nu există evaluări
- TP Chimie #10C, Synhtèse D'esters, Correction, Terminale S, tstp10chcDocument10 paginiTP Chimie #10C, Synhtèse D'esters, Correction, Terminale S, tstp10chcZakaria ElhammoumiÎncă nu există evaluări
- 1cm3jftoi 866968Document2 pagini1cm3jftoi 866968bipÎncă nu există evaluări
- Chimie 03 2020-2021: Données: ρ (H O) = 1 Kg.L ; M = 40 g.molDocument1 paginăChimie 03 2020-2021: Données: ρ (H O) = 1 Kg.L ; M = 40 g.molRomaissa Loulhaci100% (1)
- Série D - Exercices #10 - Sciences Physiques Etats Physiques de La Matière - Concentrations Massique - Solubilité Et Molaire - 1ère AS (2010-2011) MR Adam BoualiDocument2 paginiSérie D - Exercices #10 - Sciences Physiques Etats Physiques de La Matière - Concentrations Massique - Solubilité Et Molaire - 1ère AS (2010-2011) MR Adam BoualiIhoucine FatnassiÎncă nu există evaluări
- Diagramme de FrostDocument19 paginiDiagramme de Frostmehdi100% (1)
- Fiche Defibac Reaction D EsterificationDocument2 paginiFiche Defibac Reaction D Esterificationali100% (1)
- Correction Dosage Javel PDFDocument1 paginăCorrection Dosage Javel PDFanon_115085036100% (2)
- ED Chimie Generale 2008Document4 paginiED Chimie Generale 2008Medoumar AlagudeÎncă nu există evaluări
- Chapitre C3 ConductimetrieDocument5 paginiChapitre C3 ConductimetrieLahcen Ben SalmÎncă nu există evaluări
- Auteur: ALLOH Yaovi Robert Professeur de Sciences Physiques Au TOGODocument28 paginiAuteur: ALLOH Yaovi Robert Professeur de Sciences Physiques Au TOGORodrigueWafoÎncă nu există evaluări
- TP Suivi EsterificationDocument2 paginiTP Suivi EsterificationMondher DhahriÎncă nu există evaluări
- Brochure de Chimie TSM Tse (1) - 1Document46 paginiBrochure de Chimie TSM Tse (1) - 1Elhadj BahÎncă nu există evaluări
- S12 (PH Des Solutions AqueusesDocument5 paginiS12 (PH Des Solutions AqueusesLotfi BoucharebÎncă nu există evaluări
- Ester Bac Serie 1 202324 1 - 231116 - 153830Document4 paginiEster Bac Serie 1 202324 1 - 231116 - 153830deissemmhidhi3Încă nu există evaluări
- Astuces 2 Oscillations Électriques Forcées-CopierDocument4 paginiAstuces 2 Oscillations Électriques Forcées-CopiersendibedÎncă nu există evaluări
- Astuces 2 Oscillations Électriques Forcées-CopierDocument4 paginiAstuces 2 Oscillations Électriques Forcées-CopiersendibedÎncă nu există evaluări
- TP Résonance D'intensite-CopierDocument2 paginiTP Résonance D'intensite-Copiersendibed100% (1)
- Cours - Sciences Physiques - Mouvement Trajectoire, La Vitesse - 1ère AS (2015-2016) MR Sdiri Anis PDFDocument3 paginiCours - Sciences Physiques - Mouvement Trajectoire, La Vitesse - 1ère AS (2015-2016) MR Sdiri Anis PDFsendibedÎncă nu există evaluări
- Programmes Officiels Enseignement SecondaireDocument32 paginiProgrammes Officiels Enseignement SecondairesendibedÎncă nu există evaluări
- Série D'exercices N°7 Lycée Pilote - Physique MOUVEMENT RECTILIGNE - 3ème Sciences Exp (2015-2016) MR MABROUKI SALAH PDFDocument7 paginiSérie D'exercices N°7 Lycée Pilote - Physique MOUVEMENT RECTILIGNE - 3ème Sciences Exp (2015-2016) MR MABROUKI SALAH PDFsendibedÎncă nu există evaluări
- T.P Construction de Fresnel-CopierDocument3 paginiT.P Construction de Fresnel-CopiersendibedÎncă nu există evaluări
- 5 AlcoolDocument3 pagini5 AlcoolsendibedÎncă nu există evaluări
- DR1 2triDocument2 paginiDR1 2trisendibedÎncă nu există evaluări
- Enoncés Des Exercices: Exercice 1Document4 paginiEnoncés Des Exercices: Exercice 1sendibedÎncă nu există evaluări
- Filtre Passe BandeDocument2 paginiFiltre Passe BandesendibedÎncă nu există evaluări
- Enoncés Des Exercices: Exercice 1Document4 paginiEnoncés Des Exercices: Exercice 1sendibedÎncă nu există evaluări
- RLC Forcé Suite 2Document3 paginiRLC Forcé Suite 2sendibedÎncă nu există evaluări
- Devoir de Synthese N°1Document2 paginiDevoir de Synthese N°1sendibedÎncă nu există evaluări
- DA2008Document171 paginiDA2008neculaitarabutaÎncă nu există evaluări
- c3 Les Acide Carboxyliques Et DerivesDocument12 paginic3 Les Acide Carboxyliques Et DerivesComan SakoÎncă nu există evaluări
- ChimieDocument32 paginiChimieanassÎncă nu există evaluări
- Les LipidesDocument32 paginiLes LipidesWã RdäÎncă nu există evaluări
- TD Sur Les Alcools Terminale CD 2023Document3 paginiTD Sur Les Alcools Terminale CD 2023Admi BraccÎncă nu există evaluări
- 7 EsterificationDocument2 pagini7 EsterificationsendibedÎncă nu există evaluări
- Chimie VerteDocument16 paginiChimie VerteimaneÎncă nu există evaluări
- Exercice Chimie 07Document2 paginiExercice Chimie 07Haouphouet armel KouadioÎncă nu există evaluări
- Fiche Defibac Reaction D EsterificationDocument2 paginiFiche Defibac Reaction D Esterificationali100% (1)
- Chimie-TP13-Saponification Et Proprietes Des SavonsDocument2 paginiChimie-TP13-Saponification Et Proprietes Des Savonstaki djÎncă nu există evaluări
- Reactions Chimie OrgaDocument47 paginiReactions Chimie OrgafluiddynamicÎncă nu există evaluări
- Lecon Exercice PC 1ere SDocument5 paginiLecon Exercice PC 1ere SKevin RajaonarivonyÎncă nu există evaluări
- Livre Final de Chimie P (C D)Document90 paginiLivre Final de Chimie P (C D)Valeria PeredaÎncă nu există evaluări
- Chimie Organique I - Readings PDFDocument79 paginiChimie Organique I - Readings PDFArouna DoloÎncă nu există evaluări
- Ocl 2004116 P 454Document3 paginiOcl 2004116 P 454Silvia CalabreseÎncă nu există evaluări
- Les Acides CarboxyliquesDocument6 paginiLes Acides CarboxyliquesLAHCEN OUTALBÎncă nu există evaluări
- 2011 Asie Exo1 Sujet ParfumFraise 6 5ptsDocument3 pagini2011 Asie Exo1 Sujet ParfumFraise 6 5ptsmaëlleÎncă nu există evaluări
- Chap 01 NomenclatureDocument9 paginiChap 01 NomenclatureAyoub DoumirÎncă nu există evaluări
- Cinetique - 111817 Exercice ImportantDocument6 paginiCinetique - 111817 Exercice Importantmohamed laghribÎncă nu există evaluări
- Magazine 17 Esterification PDFDocument5 paginiMagazine 17 Esterification PDFamal mansour0% (1)
- Devoir de Contrôle N°2 - Sciences Physiques - Bac Sciences Exp (2016-2017) MR Chebbi Rachid PDFDocument2 paginiDevoir de Contrôle N°2 - Sciences Physiques - Bac Sciences Exp (2016-2017) MR Chebbi Rachid PDFMayssa JouiniÎncă nu există evaluări
- Synthèse Chimie - Les Grandes Réactions ChimiquesDocument21 paginiSynthèse Chimie - Les Grandes Réactions ChimiquesAdrien StandaertÎncă nu există evaluări
- TD Chimie Organique NomDocument18 paginiTD Chimie Organique Nomemmanuel cerda adonaïÎncă nu există evaluări
- Biotech Des LipidesDocument10 paginiBiotech Des LipidesndassisamoradanelleÎncă nu există evaluări
- Questionnaires de Revision ChimieDocument3 paginiQuestionnaires de Revision ChimieMohamed Konate100% (1)
- MonoglicerideDocument18 paginiMonoglicerideInga JurjuÎncă nu există evaluări
- Série D'exercices N°2 - Chimie - Esterification - Hydrolyse - Bac Sciences Exp (2015-2016) MR Daghsni SahbiDocument4 paginiSérie D'exercices N°2 - Chimie - Esterification - Hydrolyse - Bac Sciences Exp (2015-2016) MR Daghsni SahbiAmine AlaoUii AlaouiÎncă nu există evaluări
- Les LipidesDocument25 paginiLes LipidesMamineTecDelmaÎncă nu există evaluări
- Sujet Bac STI Physique-Chimie Sujet I 2023Document3 paginiSujet Bac STI Physique-Chimie Sujet I 2023Toumany FofanaÎncă nu există evaluări
- CO1 TS2 2016 LSLL WahabdiopDocument4 paginiCO1 TS2 2016 LSLL WahabdiopMed BriniÎncă nu există evaluări