Documente Academic
Documente Profesional
Documente Cultură
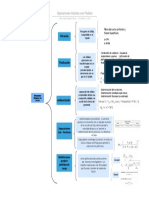
Exposición Conservación Materia y Energía
Încărcat de
Jose Gregorio Davila Hernandez0 evaluări0% au considerat acest document util (0 voturi)
7 vizualizări6 paginiTitlu original
Exposición Conservación Materia y Energía.pptx.docx
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
7 vizualizări6 paginiExposición Conservación Materia y Energía
Încărcat de
Jose Gregorio Davila HernandezDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 6
Principios Básicos de Conservación de Materia y Energía
La Ley de la Conservación de la Materia fue postulada en 1789 por
el químico francés Antoine Laurent Lavoisier, quien observó que los
productos obtenidos en una reacción química era n exactamente igual al
peso de los reactivos involucrados. Esta se ley se basa en el hecho de que
los átomos son partículas indivisibles en este tipo de reacciones; mientras
que en las reacciones nucleares los átomos se fragmentan, razón por la que
no se consideran reacciones químicas.
En las reacciones químicas se desprende energía, si son
exotérmicas, y se absorbe en el caso de ser endotérmicas. Los reactivos
de una reacción endotérmica, más una cierta cantidad de calor (energía) dan
los productos. Puede demostrarse que la energía de los productos es igual a
la suma de la energía que tenían los reactivos más el calor aportado.
Einstein demostró que la ley no es estrictamente cierta, según su
teoría el universo es un sistema dinámico en constante cambio y movimiento.
La materia y la energía son manifestaciones de la misma entidad física. En
determinadas condiciones, la masa puede transformarse en energía y
viceversa.
En las reacciones químicas la energía involucrada es baja, y los
cambios de masa por energía son despreciables. Por ello la ley de
conservación de la materia continúa siendo aplicable.
En fenómenos nucleares como la fisión nuclear (ruptura parcial de
núcleos atómicos) y fusión nuclear (unión de núcleos atómicos), están
involucradas grandes cantidades de energía y los cambios de masa son
apreciables y se pueden evaluar con la ecuación de Einstein
En el siglo XIX, Mayer estableció la ley de conservación de la energía,
‟la suma de energía cinética, potencial y térmica en un sistema aislado
permanece constante.”
Se pueden diferenciar tres tipos de sistemas:
o Un sistema aislado es aquel que no intercambia materia ni energía
con el medio que lo rodea.
o Un sistema cerrado intercambia solamente energía con el medio que
lo rodea.
o Un sistema abierto intercambia materia y energía.
En cualquier cambio físico o químico que tenga lugar en un sistema existe
una serie de propiedades que permanecen constantes. Básicamente, las
propiedades que se conservan son: la materia, la energía y la cantidad de
movimiento.
La conservación de cada una de estas propiedades dio lugar a una ley
fundamental. Así tenemos:
Para la conservación de la materia tenemos la Ley de conservación de
la masa, de Lavoisier.
Para la conservación de la energía tenemos el 1º y 2º principios de la
termodinámica:
o 1° Principio: la energía no se crea ni se destruye, se transforma.
o 2° Principio: el calor no fluye espontáneamente desde un
cuerpo frío a uno caliente si no hay trabajo por medio.
Para la conservación de la cantidad de movimiento tenemos la Ley de
Newton.
Estas leyes permiten establecer ecuaciones que nos permiten definir
"balances" a los sistemas. Un balance puede ser macroscópico o
microscópico. Decimos que un balance es macroscópico cuando lo
realizamos a sistemas en los que las variables intensivas no son función de
la posición para un momento dado. Un balance es microscópico los que
aplicamos a sistemas en los que las variables intensivas son función de la
posición en un momento dado. Consecuentemente, en los balances
microscópicos debemos considerar elementos diferenciales de volumen. Una
vez definido el balance, lo extenderemos a todo el volumen mediante la
correspondiente integral.
Fundamentos del balance de materia
En primer lugar, recordemos algunas definiciones necesarias para introducir
las operaciones o procesos unitarios.
Un sistema se puede entender como un conjunto de componentes que
actúan de manera conjunta a fin de cumplir con cierto(s) objetivo(s).
No necesariamente se limita a objetivos meramente físicos, sino que
puede aplicarse a fenómenos dinámicos abstractos pertenecientes a
otras áreas del conocimiento (economía, biología, antropología,...).
Un proceso se puede definir, según el diccionario, como una operación
o conjunto de operaciones que se suceden unos a otros de modo
relativamente fijo, y que producen un resultado final. Se puede hablar de
procesos biológicos, económicos, físicos, químicos, entre otros.
Cuando se estudia un sistema, o una porción de un sistema, es
imprescindible establecer la frontera del sistema. Dependiendo del proceso
(o procesos) a ser analizados, habrá que delimitar hasta donde una
unidad o parte pertenece o no al sistema objeto de estudio. Al
delimitar el objeto de estudio, es posible formular las estrategias de
análisis y resolución del problema planteado. Toda parte o componente que
no pertenece al sistema en estudio (que está fuera de la frontera del sistema)
se considera parte de los alrededores o del entorno.
Un sistema se considera abierto cuando se transfiere materia por la
frontera del sistema; es decir, que entra materia del entorno al sistema o
sale materia del sistema hacia el entorno, o ambas cosas.
Un sistema es cerrado cuando no tiene lugar una transferencia
semejante de materia, durante el intervalo de tiempo en el que se estudia el
sistema.
Los balances de materia se aplican a cualquier sistema al que se le
hayan definido sus fronteras, no importa si su naturaleza es física,
química o abstracta. Son una de las herramientas básicas de análisis
de los sistemas, así como también lo son: el balance de energía, las
relaciones físico-químicas entre algunas variables y las especificaciones
o restricciones en el funcionamiento del proceso.
Se podría traducir la ley de conservación de la masa, para este caso,
como sigue: El total de la masa que entra a un proceso o unidad es igual al
total de la masa que sale de esa unidad. Obsérvese que se hace
referencia a la masa y no a la cantidad de materia (medida en moles) ni
a cualquier otra relación física de los componentes (volumen, área,...)
Se entiende por variable de un proceso a una magnitud física que
caracteriza una operación de un proceso. Por ejemplo, las temperaturas,
presiones, volúmenes y velocidades de flujo son variables de un proceso.
Los diagramas de flujo son muy útiles al momento de analizar un
sistema. Estos diagramas permiten representar mediante rectángulos las
operaciones unitarias o procesos (e.g. reactores, condensadores,
columnas de destilación, separadores) y mediante flechas las corrientes (i.e.
flujos que circulan por tuberías) de los componentes que intervienen en
el sistema y que circulan entre las unidades de operación.
Clasificación de los procesos Basándose en la dependencia o no
respecto del tiempo, un proceso pueden clasificarse como:
o Proceso en estado estacionario, aquel cuyo estado (i.e. las
variables que intervienen en el mismo) no cambia en el tiempo
o sus variaciones son despreciables durante un intervalo de tiempo
suficientemente amplio.
o Proceso en régimen transitorio (estado no estacionario), aquel cuyo
estado varía en el tiempo, haciendo que los valores de las
variables involucradas presenten cambios significativos en su
dinámica. Basándose en la manera en que es diseñado para
llevar a cabo sus operaciones, un proceso puede ser clasificado
como: Proceso continuo, cuando las corrientes de entrada y
descarga fluyen de manera continua durante todo el proceso.
o Proceso por lotes o intermitente, cuando, por ejemplo, se cargan en un
recipiente las corrientes de alimentación al comienzo del proceso
solamente y, después de transcurrido cierto tiempo, se retira el
contenido del recipiente en parte o en su totalidad. Proceso
semicontinuo, cuando tiene características de los dos anteriores
Tipos de balance Hay dos tipos de balance que se pueden aplicar a un
sistema. El balance diferencial indica lo que ocurre en un sistema en un
momento determinado. Por lo general, este tipo de balance se aplica a los
sistemas continuos. Si el sistema está en régimen estacionario, un
balance diferencial dará en cualquier instante el mismo resultado (los
términos de acumulación son nulos). Si el sistema es transitorio, este
balance generará un conjunto de ecuaciones diferenciales respecto del
tiempo que habrá que resolver. El balance integral indica lo que le ocurre
a un sistema durante dos instantes determinados. Solo informa sobre
el comportamiento del sistema durante el intervalo comprendido entre
esos dos momentos. Generalmente, los balances integrales se aplican
a procesos tipo batch o por lotes, los cuales tienen condiciones de
inicio y finalización bien definidas. Matemáticamente, se obtendrá un
conjunto de ecuaciones integrales que deberá ser resuelto para los
límites de integración establecidos
Balances totales y por componentes
Para cada unidad de proceso o sistema se puede escribir un balance total y
varios balances por componente. En un balance total se considera la masa
total de cada corriente implicada en el proceso. En un balance por
componentes se considera solamente la masa del componente
analizado en cada una de las corrientes involucradas en el proceso.
RECIRCULACIÓN, PURGA Y DERIVACIÓN
El propósito general de la Recirculación en un proceso industrial es reducir el
consumo de materiales y energía por unidad de producto elaborado.
La Purga es necesaria en un proceso o en una etapa de éste para remover
una acumulación de algún componente, que de otra manera conduciría a un
incremento no deseado o inconveniente en su concentración.
El flujo de Derivación o de bypass es aquel que retirándose de una corriente
de proceso, se “salta” una o varias etapas de transformación, avanzando
directamente a un punto posterior, en donde se reúne con la porción de flujo
original si tratado.
Flujos de recirculación
o Recuperar energía
o Aumentar la calidad de un producto (lograr que salga más concentrado en
alguno de los componentes)
o Recuperar reactantes sin transformar
S-ar putea să vă placă și
- v8n8 A06Document9 paginiv8n8 A06Kerly Marylin Manrique BarrigaÎncă nu există evaluări
- v8n8 A06Document9 paginiv8n8 A06Kerly Marylin Manrique BarrigaÎncă nu există evaluări
- Módulo II. Sistemas de Producción y PronósticoDocument5 paginiMódulo II. Sistemas de Producción y PronósticoJose Gregorio Davila HernandezÎncă nu există evaluări
- UntitledDocument3 paginiUntitledJose Gregorio Davila HernandezÎncă nu există evaluări
- 1 Procesamiento de Materias Primas Hortofruticolas Orientados Hacia La Optimización, Conservación y Obtención de DerivadosDocument25 pagini1 Procesamiento de Materias Primas Hortofruticolas Orientados Hacia La Optimización, Conservación y Obtención de DerivadosJose Gregorio Davila HernandezÎncă nu există evaluări
- Sistema de Planificacion de La FabricacionDocument24 paginiSistema de Planificacion de La FabricacionxzpedroÎncă nu există evaluări
- Sistema de Planificacion de La FabricacionDocument24 paginiSistema de Planificacion de La FabricacionxzpedroÎncă nu există evaluări
- Módulo II. Sistemas de Producción y PronósticoDocument5 paginiMódulo II. Sistemas de Producción y PronósticoJose Gregorio Davila HernandezÎncă nu există evaluări
- Paper Modelo de Planeación de La Produccion PDFDocument9 paginiPaper Modelo de Planeación de La Produccion PDFDiana BlancoÎncă nu există evaluări
- MODULO II La Función de Producción, Pronosticos y Control ZLFDocument1 paginăMODULO II La Función de Producción, Pronosticos y Control ZLFJose Gregorio Davila HernandezÎncă nu există evaluări
- Determinación de Parámetros de Control de Calidad de Granos y SemillasDocument22 paginiDeterminación de Parámetros de Control de Calidad de Granos y SemillasJose Gregorio Davila HernandezÎncă nu există evaluări
- Ciencia, Docencia y Tecnología 0327-5566: Issn: Cdyt@uner - Edu.arDocument26 paginiCiencia, Docencia y Tecnología 0327-5566: Issn: Cdyt@uner - Edu.arJose Gregorio Davila HernandezÎncă nu există evaluări
- Romero Guia MichaelDocument47 paginiRomero Guia MichaelMarianela Diaz LloccllaÎncă nu există evaluări
- Granos y SemillasDocument17 paginiGranos y SemillasJose Gregorio Davila HernandezÎncă nu există evaluări
- MIP en SilosDocument118 paginiMIP en SilosWilmer PerezÎncă nu există evaluări
- Modulo I. El Método Del Camino CríticoDocument8 paginiModulo I. El Método Del Camino CríticoJose Gregorio Davila HernandezÎncă nu există evaluări
- Modulo I. Modelos Gráficos Planificación y ProducciónDocument8 paginiModulo I. Modelos Gráficos Planificación y ProducciónJose Gregorio Davila HernandezÎncă nu există evaluări
- 1 Modulo II. Metodos AnalíticosDocument15 pagini1 Modulo II. Metodos AnalíticosJose Gregorio Davila HernandezÎncă nu există evaluări
- Extrusión y PlagasDocument16 paginiExtrusión y PlagasJose Gregorio Davila HernandezÎncă nu există evaluări
- 353 1271 1 PB PDFDocument10 pagini353 1271 1 PB PDFRober ParedesÎncă nu există evaluări
- 1 Modulo II. Caracterización Desechos Gaseosos AgroindustrialesDocument10 pagini1 Modulo II. Caracterización Desechos Gaseosos AgroindustrialesJose Gregorio Davila HernandezÎncă nu există evaluări
- Cap3 10 PDFDocument129 paginiCap3 10 PDFNatanael ManriqueÎncă nu există evaluări
- Actividades A Realizar de Acuerdo Al Progra de La Materia Desechos AgroindustrialesDocument4 paginiActividades A Realizar de Acuerdo Al Progra de La Materia Desechos AgroindustrialesJose Gregorio Davila HernandezÎncă nu există evaluări
- DiagramaDocument1 paginăDiagramaJose Gregorio Davila HernandezÎncă nu există evaluări
- 1 Modulo II. Metodos AnalíticosDocument15 pagini1 Modulo II. Metodos AnalíticosJose Gregorio Davila HernandezÎncă nu există evaluări
- Agroindustria y EnergiaDocument114 paginiAgroindustria y EnergiaMIJAEL TEYRO TARAZONA MARRUJOÎncă nu există evaluări
- Lenguajes de Programacion PDFDocument120 paginiLenguajes de Programacion PDFleitohest100% (1)
- Carmen Fullana Belda y Elena Urquía GrandeDocument11 paginiCarmen Fullana Belda y Elena Urquía GrandeNORMA REYESÎncă nu există evaluări
- Lenguaje de Simulacion y SimuladoresDocument3 paginiLenguaje de Simulacion y SimuladoresJose Gregorio Davila HernandezÎncă nu există evaluări
- Toc 6634 01 01Document15 paginiToc 6634 01 01Jose Gregorio Davila HernandezÎncă nu există evaluări
- EXA RECU Corrección S1 P4 18 - 19Document6 paginiEXA RECU Corrección S1 P4 18 - 19Juan Juuzou SuzuyaÎncă nu există evaluări
- Fisica Primero 5tDocument8 paginiFisica Primero 5tJuan Carlos Rengel RomanÎncă nu există evaluări
- ESTABILIDADDocument19 paginiESTABILIDADLiler TantaleanÎncă nu există evaluări
- TrabajoDocument5 paginiTrabajoYomaly Nuñez JulcaÎncă nu există evaluări
- Calentamiento DieléctricoDocument4 paginiCalentamiento DieléctricoGeraldine Villa100% (1)
- Termocupla A BluetoothDocument38 paginiTermocupla A BluetoothC M CÎncă nu există evaluări
- EXTRAORDINARIA 2019 QUÍMICA 4º ESO ResueltoDocument7 paginiEXTRAORDINARIA 2019 QUÍMICA 4º ESO ResueltoCris CrisÎncă nu există evaluări
- Parcial EsDocument45 paginiParcial EsYeyson Ferney Sierra RodriguezÎncă nu există evaluări
- BobinasDocument8 paginiBobinasJhonathan GómezÎncă nu există evaluări
- Tarea 1.2 VictorEuceda 11211125Document10 paginiTarea 1.2 VictorEuceda 11211125Víctor EucedaÎncă nu există evaluări
- Corriente EléctricaDocument5 paginiCorriente EléctricajoseRÎncă nu există evaluări
- A-2 Introducción A La Energía Solar FotovoltaicaDocument40 paginiA-2 Introducción A La Energía Solar FotovoltaicaManuelÎncă nu există evaluări
- Fisica 3 PDFDocument7 paginiFisica 3 PDFGladys Maria Quiroz TorrealvaÎncă nu există evaluări
- Taller de Diodo SolucionDocument13 paginiTaller de Diodo SolucionIsaac Yamith Guzman PaterninaÎncă nu există evaluări
- Laboratorio Virtual Campos MagneticosDocument3 paginiLaboratorio Virtual Campos Magneticosmsdcm1Încă nu există evaluări
- Evaluacion SensorialDocument44 paginiEvaluacion SensorialEddy Paceñito100% (1)
- Cuadro Sinóptico Solidos y FluidosDocument1 paginăCuadro Sinóptico Solidos y Fluidoserika viviana vargas ferruchoÎncă nu există evaluări
- TRANSMISIÓN DE CALOR (Nivel Universitario)Document20 paginiTRANSMISIÓN DE CALOR (Nivel Universitario)Ricardo BilbaoÎncă nu există evaluări
- Guia No1 Mecanica Dinamica-2011Document3 paginiGuia No1 Mecanica Dinamica-2011Maix Alejandro Padilla Vergara100% (1)
- Corrientes ParasitasDocument3 paginiCorrientes ParasitasCristhian E. VilcaÎncă nu există evaluări
- Caída Libre y Tiro VerticalDocument17 paginiCaída Libre y Tiro VerticalJakelin Fernandez S.Încă nu există evaluări
- Laboratorio Vectores 1 PhetDocument7 paginiLaboratorio Vectores 1 PhetHarry PlonesÎncă nu există evaluări
- Tarea 2 Fundamentos de Circuitos Semiconductores y Senal AcDocument3 paginiTarea 2 Fundamentos de Circuitos Semiconductores y Senal AcLorainis Rangel RangelÎncă nu există evaluări
- S04 Practica Induccion e InductanciaDocument1 paginăS04 Practica Induccion e InductanciaCLAUDIA RUIZÎncă nu există evaluări
- Cuestiones y Problemas Del Tema 6: Equilibrio QuímicoDocument21 paginiCuestiones y Problemas Del Tema 6: Equilibrio QuímicoBlueStorsÎncă nu există evaluări
- Capitulo 5 Motores de Corriente ContinuaDocument13 paginiCapitulo 5 Motores de Corriente ContinuaKaren CárdenasÎncă nu există evaluări
- Tesis de GeofisicaDocument144 paginiTesis de GeofisicaJose Quiñonez Choquecota0% (1)
- Transferencia de Masa 1Document5 paginiTransferencia de Masa 1jose angel reyes0% (2)
- Informe de Lab Nro 3 Medicion de VelocidadDocument25 paginiInforme de Lab Nro 3 Medicion de VelocidadDevilSzexÎncă nu există evaluări
- 3G3HVDocument16 pagini3G3HVRafael Nogales GarciaÎncă nu există evaluări