Documente Academic
Documente Profesional
Documente Cultură
Cirugia Pediatrica PDF
Încărcat de
Eva Garcia MartinezTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Cirugia Pediatrica PDF
Încărcat de
Eva Garcia MartinezDrepturi de autor:
Formate disponibile
lOMoARcPSD|4513632
Cirugia Pediatrica
Cirugía Pediátrica (Universidad Miguel Hernández de Elche)
StuDocu no está patrocinado ni avalado por ningún colegio o universidad.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada: Ariadna Carme NavarroCIRUGÍA
Blasco PEDIÁTRICA 25/09/14
Profesor: Dr. Sánchez París CP-1
25/09/2014; 13:00 – 13:50
INTRODUCCIÓN A LA ASIGNATURA:
El examen de esta asignatura constará de 4 preguntas de desarrollo, entre las que puede haber casos
clínicos. Además el profesor informó de que las faltas de ortografía se penalizarían.
El 85% de las clases de esta asignatura serán impartidas por el Dr. Sánchez París:
ATRESIA DE ESÓFAGO OBSTRUCCIÓN DIGESTIVA BAJA:
ESTENOSIS HIPERTRÓFICA DE PÍLORO o ENFERMEDAD DE
INVAGINACIÓN INTESTINAL HIRSCHSPRUNG
OBSTRUCCIÓN DIGESTIVA ALTA: o MALFORMACIONES
o ATRESIA DUODENAL ANORECTALES
o PÁNCREAS ANULAR ONCOLOGÍA PEDIÁTRICA:
o ATRESIA YEYUNOILEAL o NEUROBLASTOMA
o MALROTACIÓN INTESTINAL o TUMOR DE WILMS
o ÍLEO MECONIAL o TERATOMAS
ATRESIAS DE ESÓFAGO
CONCEPTO
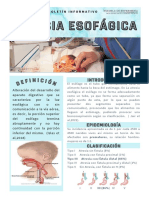
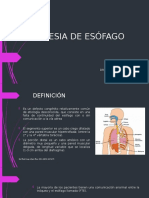
La ATRESIA ESOFÁGICA se define como la ausencia de continuidad del esófago
con el estómago, con o sin comunicación con la vía aérea.
EMBRIOLOGÍA
• Cuando el embrión tiene 4 semanas aparece en la parte ventral del intestino
anterior el divertículo respiratorio.
• Este divertículo se separa poco a poco de la porción dorsal del intestino anterior
por medio del tabique traqueoesofágico.
• El intestino anterior queda dividido en una porción ventral (el primordio
respiratorio) y una porción dorsal (el esófago).
ETIOPATOGENIA (no lo dió en clase, pero estaba en la comisión del año pasado)
Se cree que atresia esofágica (AE) y la fístula traqueoesofágica (FTE) se desarrollan por
separación anómala de las divisiones respiratoria y digestiva del intestino anterior
primitivo.
1/5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 25/09/14
EPIDEMIOLOGÍA
• 1 de cada 4000 recién nacidos vivos.
• Es más frecuente en varones.
• La mayoría son casos esporádicos.
• En < 1% son familiares sindrómicos (secuencia de Pierre-Robin, secuencia de
DiGeorge, síndrome de Holt-Oram,…)
• En el 6% se encuentran anomalías cromosómicas asociadas: trisomías 13, 18 y 21.
ANOMALÍAS ASOCIADAS (no hace falta saber los porcentajes)
• Malformaciones CARDÍACAS (35%): ¡Las más frecuentes!
▫ CIA (20%), CIV y Tetralogía de Fallot.
▫ Arco aórtico derecho (4%).
• Malformaciones GÉNITO-URINARIAS (24%):
▫ Criptorquidia, hidronefrosis, reflujo vesicoureteral, hipospadias (el meato
urinario se localiza en la cara inferior del pene), agenesia e hipoplasia renal.
• Malformaciones DIGESTIVAS (24%):
▫ Malformaciones anorectales, malrotación intestinal, atresia duodenal e
ileal, páncreas anular, estenosis hipertrófica de píloro.
Un ejemplo es el SÍNDROME V.A.C.T.E.R.L.:
• Defectos vertebrales (V).
• Atresia anal (A).
• Anomalías cardiacas (C).
• Fístula traqueoesofágica (T).
• Atresia de esófago (E).
• Displasia renal y radial (R).
• Deformidad de extremidades (L, limb (extremidad)).
Otro ejemplo es el SÍNDROME DE CHARGE:
• Coloboma (C)
• Alteración cardiaca (H, heart)
• Atresia de coanas (A)
• Retraso en el desarrollo (R)
• Hipoplasia genital (G)
• Deformidades de oído (E, ear)
CLASIFICACIÓN ANATÓMICA (LADD)
• TIPO I (A): Atresia esofágica (AE) sin
fístula (7-8%).
• TIPO II (B): AE con fístula al bolsón
proximal (1%).
• TIPO III (C): AE con fístula al bolsón
distal (85-90%, la más frecuente).
• TIPO IV (D): AE con fístula proximal y
distal.
• TIPO V (E): Fístula sin atresia tipo H.
• TIPO VI (F): Estenosis congénita del esófago.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 25/09/14
CLASIFICACIÓN PRONÓSTICA: Supervivencia de SPITZ (1992)
• GRUPO I: Peso al nacer > 1500 gr sin malformaciones cardiacas asociadas
(supervivencia del 97%).
• GRUPO II: Peso < 1500 gr SIN malformaciones cardíacas asociadas (59%).
• GRUPO III: Peso < 1500 gr CON malformaciones cardíacas asociadas (22%).
DIAGNÓSTICO:
• PRENATAL: a partir de la semana 18 de gestación
▫ POLIHIDRAMNIOS (el feto no traga líquido amniótico, por eso
aumenta).
▫ Burbuja gástrica pequeña o ausente (no pasa aire al estómago).
▫ Área anecoica en el 1/3 medio del cuello fetal (bolsa esofágica
proximal con extremo ciego).
• EN RECIÉN NACIDO:
▫ Síntomas poco después del nacimiento.
▫ SIALORREA (ante un RN con sialorrea sospechar siempre AE).
▫ Crisis de sofocación (cianosis) y atragantamiento.
▫ IMPOSIBILIDAD DE PASAR UNA SONDA NASOGÁSTRICA
HACIA EL ESTÓMAGO (hallazgo exploratorio principal en el RN).
▫ En el caso de FTE sin atresia (TIPO E) la presentación es TARDÍA con
episodios recurrentes de neumonía.
▫ Exploraciones complementarias
• Rx simple abdomen:
• Sonda enrollada en el bolsón proximal (signo de la
lazada).
• Presencia de aire en la cámara gástrica (fístula distal,
por el paso de aire desde las vías aéreas hacia el
estómago). Tipos III, IV y V.
• Ausencia de aire en el estómago en los casos de AE sin
fístula o con fístula al bolsón proximal. Tipos I y II.
• Entre el 50 y el 70% de los pacientes va a tener malformaciones
asociadas, por lo que también realizaremos:
• ECOGRAFÍA CARDÍACA: descartar arco aórtico
derecho (es importante, ya que la cirugía se realiza por el
lado derecho)
• ECOGRAFÍA RENAL (malformaciones renales)
• CARIOTIPO (trisomías 13, 18, 21)
• BRONCOSCOPIA: en los casos de AE con fístula al
bolsón proximal
3/5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 25/09/14
TRATAMIENTO: SIEMPRE QUIRÚRGICO
- Preoperatorio
• Sonda de aspiración con doble luz a débito continuo bajo aspiración suave del
bolsón.
• Colocación del paciente en posición semisentada (con la cabeza más alta que el
resto del cuerpo) para evitar que el ácido del estómago vaya hacia la fístula.
• Mantener la oxigenación. Evitar la colocación de CPAP nasal y de ventilación
con ambú (para evitar el paso de aire hacia el estómago).
• Iniciar antibioterapia iv.
• Se deberán tratar ANTES las lesiones cardiacas asociadas.
- Principios del tratamiento quirúrgico
• Se realizará la ligadura de la fístula traqueoesofágica y la anastomosis primaria
término-terminal del esófago cuando sea posible.
• Se suele realizar a los 2-3 meses del nacimiento.
• En niños prematuros o con complicaciones de cualquier naturaleza, la
anastomosis primaria se puede demorar mediante la colocación transitoria de
una sonda de gastrostomía y la realización de una ligadura de la fístula.
• Si la distancia entre los bolsones es > 3-4 cm, no se puede realizar una
reparación primaria, y habrá que interponer un fragmento de estomago, yeyuno
o colon.
- Técnica quirúrgica: ATE con fístula distal
1. Toracotomía posterolateral derecha (5ei).
2. Abordaje extrapleural.
3. Localización de la vena ázigos
4. Localización de la fístula, disección de la misma y cierre de la tráquea.
5. Disección del bolsón proximal.
6. Anastomosis termino-terminal del esófago.
7. Colocación de tubo endotorácico.
4/5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 25/09/14
- Tratamiento postoperatorio
• Se deja intubado al paciente, sobre todo si la anastomosis ha quedado a tensión.
• Debe evitarse la hiperextensión del cuello.
• Debe evitarse recolocar la SNG, en caso de que se salga, para no dañar la
anastomosis.
• Si todo va bien al 7º día postoperatorio se realiza el esofagograma para
comprobar la permeabilidad de la anastomosis y ver si hay o no hay contraste en
el mediastino. Si es todo normal se empezará a dar nutrición enteral por SNG.
COMPLICACIONES
• Tempranas:
▫ Fuga anastomótica (15%): la salida de saliva por el tubo endotorácico
nos indica esta complicación.
▫ Estenosis de la anastomosis (10-15%).
▫ Recidiva de la fístula (3-14%).
• Tardías:
▫ REFLUJO GASTRO-ESOFÁGICO (la más frecuente).
▫ Traqueomalacia (colapso de la tráquea durante la espiración por una
alteración del desarrollo de su cartílago, es más frágil).
▫ Alteración de la motilidad del esófago.
BIBLIOGRAFÍA:
-Apuntes de clase
-Comisión del año pasado
- PDF del profesor
*Las imágenes se pueden ver más grandes en el PDF.
5/5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada: Maite Marchena Rojas
Profesor: Óscar Sánchez París HGUA CP-2
Fecha y hora: 25/09/2014; 14:00-14:50
ESTENOSIS HIPERTROFICA DE PILORO
1.- Concepto:
La EHP es un estrechamiento a nivel del píloro consecuencia de una hipertrofia de su
musculatura que impedirá el paso del contenido gástrico hacia el duodeno, con la consiguiente
aparición de vómitos en el lactante.
2.- Epidemiología:
• CAUSA MÁS FRECUENTE DE VÓMITOS EN LA INFANCIA.
• 1-3 de cada 1000 recién nacidos vivos (RNV)
• Más frecuente en raza blanca.
• Más frecuente en varones (5:1)
• Primogénitos (no se sabe bien la razón)
• Típico de lactantes de entre 3-6 semanas de vida (más frecuente 20 días de vida). Es decir,
NO ES CONGÉNITO, no se da en neonatos, a diferencia de las atresias, ni tampoco se da en
niños mayores (>3-4 años)
3.- Fisiopatología:
Causa desconocida.
Componente genético:
Aumenta la incidencia si los padres han tenido EHP (x4 si ha sido la madre)
Asociado a:
o Atresia de esófago.
o Sdme de Roviralta (ictericia por déficit de glucoril-transferasa)
o Toma de eritromicina por parte de la madre, que pase al neonato a
través de la lactancia materna.
o Se ha visto en madres jóvenes.
4.- Histología:
Se produce una hipertrofia de la musculatura del píloro (no un aumento del número
de fibras) lo que produce un alargamiento y un estrechamiento del mismo.
Se observa una disminución de:
Células intersticiales de Cajal
Terminaciones nerviosas
Neurofilamentos
Actividad de la sintetasa de óxido nítrico
Página 1 de 5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
5.- Clínica:
Vómitos: son vómitos alimentarios violentos, EN PROYECTIL, y NO BILIOSOS (no han
pasado al intestino). Además pueden llegar a ser “en posos de café” (20%), si llega a
darse hemorragia digestiva alta por la gastritis producida.
Adelgazamiento. El niño presenta un llanto característico “llanto de hambre”.
Deshidratación, pudiendo aparecer oliguria con orina concentrada.
Alteraciones electrolíticas.
Hambre después del vómito.
Ictericia (2-5%): Sdme de Roviralta.
Estreñimiento (ya que no come).
Pérdida de peso.
6.- Exploración física:
Suele ser normal.
Deshidratación normalmente leve (10%).
Ondas peristálticas de lucha (no es frecuente verlas).
Se puede palpar la “oliva pilórica” (que es el píloro hipertrofiado) en el cuadrante
superior derecho. En la actualidad es difícil verla, antes se diagnostica por técnicas de
imagen como veremos a continuación.
Pérdida de peso cuando se demora el dx.
7.- Pruebas complementarias:
Gasometría venosa: alcalosis metabólica hipoclorémica hipopotasémica. Con los
vómitos se pierde H+, Cl- y Na+. La hipopotasemia es debida a la difusión del potasio al
interior de la célula y como respuesta a un hiperaldosteronismo secundario que
pretende compensar la hiponatremia.
Aciduria paradójica porque los riñones intentan conservar el Na+ a expensas de los
iones de H+.
Bioquímica:
o Hipoglucemia
o Hipocloremia <98 mEq/l
o Bicarbonato <29 mEq/l
o Hiponatremia
o Hipopotasemia
o Aumento de bilirrubina indirecta (déficit de glucoril-transferasa)
Página 2 de 5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
8.- Ecografía abdominal:
Prueba principal para el diagnóstico
Se realiza ante toda sospecha de EHP
Sensibilidad 99,5% y especificidad 100%
Si no resulta concluyente se repetirá al cabo de 24-48h
Hallazgos ecográficos: número PI (3,1416…)
o Espesor muscular o grosor del píloro > = 3mm
o Diámetro total del píloro > = 14mm*
o Longitud del píloro o canal pilórico > = 16 mm
o Pretérminos y bajo peso: espesor muscular/diámetro total del píloro > = 0,27
es diagnóstico
*en las diapos pone que el diámetro del píloro es >=11mm pero él en clase dijo lo
de la regla del 3,14 y dijo “bueno el 11 no se acerca exactamente pero bueno da
igual” vamos que no será tan importante, pero pensad que es 11 que es lo que
pone en las diapos…
Píloro “en donuts” o “en diana”
en la diapositiva 10 se ve la eco y las líneas que miden la longitud (izqda.) y el grosor o
espesor (drcha. La flecha pequeña) y el diámetro (drcha. La grande)
9.- Tránsito gastro-duodenal:
• Cada Vez más en desuso
• Solo Si ECO No concluyente o recidiva (ECO en recidiva no porque en ella no se
apreciarían cambios de un día para otro, saldría como la primera que se hizo para el dx).
• Conducto Pilórico alargado “signo De la cuerda”
• El Bulbo duodenal aparece en forma de paraguas abierto sobre el píloro hipertrofiado.
en la diapositiva número 12 se aprecia el signo de la cuerda (la imagen de arriba a la izqda.)
y el parecido con un paraguas abierto (imagen de abajo a la drcha.)
10.- Diagnóstico diferencial:
Reflujo gastroesofágico. Se considera fisiológico hasta los dos años de edad, además
los vómitos no son proyectivos.
Atresia de píloro. Los vómitos son no biliosos (no hay comunicación con el duodeno) y
se evidencia una única burbuja en la Rx simple de abdomen (no pasa aire hacia los
intestinos).
Atresia de duodeno. En este caso los vómitos son biliosos (debido al paso del
contenido duodenal hacia el estómago) y se evidencian dos burbujas en la Rx de
abdomen (una es la cámara gástrica y la otra se halla a nivek duodenal, proximal a la
atresia).
Página 3 de 5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Otras: mala técnica alimentaria, malrotación intestinal, alergia a las proteínas de la
leche de vaca, gastroenteritis, hiperplasia suprarrenal, insuficiencia suprarrenal,
errores innatos del metabolismo.
11.- Tratamiento preoperatorio:
NO es una cirugía urgente.
Es importante reponer las pérdidas mediante fluidoterapia iv a 150 ml/kg/día hasta
corrección de la alcalosis asociada a los vómitos, hasta que HCO3- < 30mEq/l (24-48h).
*cálculos basales ante cualquier paciente:
los 10 primeros kg: 100cc/kg/día
los 10 kg siguientes: 50cc/kg/día
a patir de 20kg: 20cc/kg/día
Ejemplo: neonato de 5kg: 500cc/24h; niño de 12kg: 1100cc/24h (10x100+2x50)
En el caso del tto de la EHP hemos comentado que la fluidoterapia es de 150ml/kg/24h ¿por
qué 150? Porque son los cálculos basales y a parte el paciente está deshidratado y con
alteraciones electrolíticas.
El grado de depleción condiciona el tiempo de rehidratación preoperatorio que puede
llegar a las 48h en los casos graves.
Es importante corregir las alteraciones electrolíticas del lactante ya que la alcalosis es
peligrosa cuando se acompaña de una complicación respiratoria (aumento de la pCO2)
que puede actuar deprimiendo el SNC (apnea).
Colocación de una SNG unas horas antes de la intervención. Actualmente hay
controversia respecto a esto, el profe dijo que en su hospital le colocan SNG antes de
meter al paciente en quirófano solo si vomita ya que puede haber demasiada
aspiración por la sonda y acentuar así la alcalosis (deshidratarlo más); una vez dentro
del quirófano, ya sí colocamos la sonda para descomprimir el estómago.
12.- Intervención quirúrgica:
Piloromiotomía extramucosa de Ramstedt: incisión longitudinal sobre la oliva pilórica.
El objetivo principal es eliminar la acción compresiva de la musculatura hipertrofiada
mediante la sección longitudinal, que respeta la mucosa.
*en la diapositiva 16 vemos el estómago, el bulbo duodenal, y entre ellos, de color
blanquito, la oliva pilórica.
*en la diapos 17 vemos la piloromiotomía: el cirujano coge la oliva pilórica entre los
dos dedos y hace una pequeña incisión para que el músculo que está debajo rompa y
la mucosa protruya. Si se vuelve a hipertrofiar, se vuelve a operar. Es la operación más
corta de la cirugía pediátrica, tarda 5 minutos.
Página 4 de 5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
13.- Complicaciones:
Perforación duodenal (si se realiza una incisión demasiado larga). Al profe lo que le
gusta hacer al terminar la es echar suero en el campo e inyectar aire en el estómago, y
si hay burbujeo es que se ha producido perforación.
Piloromiotomía incompleta (2%)
Vómitos persistentes (>7 días) por atonía gástrica o por edema. La musculatura
gástrica se relaja después de la distensión mantenida o por la cirugía, pero se recupera
en unas 48h.
Infección de la herida
Apnea postoperatoria (si no corriges la alcalosis metabólica)
RIP <1%
para acabar, en las diapos que os pasaré hay unas preguntas de MIR respecto a la EHP.
Leedlas, las respuestas son: pregunta 14, preg21, preg33,preg45, preg54 y
preg63
Bibliografía:
Apuntes tomados en clase
Diapositivas facilitadas por el profesor
Comisión del año pasado (gracias Alejandra García y Ariadna )
La primera comi de nuestro último año se la dedico a mis liantes e
indecisos médicos (L)
Página 5 de 5
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada: Marisa Peral Garrido
Profesor: Óscar Sánchez París (S. Qx pediátrica HGUA)
Curso: 6º Medicina CP-3
Fecha y hora: 02/10/14; 13:00h – 13:50h
INVAGINACIÓN INTESTINAL
Nota:
-El profesor ha recalcado que, como dijo el primer día de clase, debemos repasar la embriología del Langman. Para
este tema, da por sabida la “rotación intestinal”. Por si alguien no tiene el libro:
http://books.google.es/books?id=KEw1RjJQ6hEC&pg=PA231&lpg=PA231&dq=rotaci
%C3%B3n+intestinal+langman&source=bl&ots=7Z-vZ-wrgp&sig=Tl04J-uffHvba4g61fer1E1t_j8&hl=es&sa=X&ei=iPovVIf
0GYaWapLlgIAJ&ved=0CCEQ6AEwAA#v=onepage&q=rotaci%C3%B3n%20intestinal%20langman&f=false
-No hace falta saber los datos de los porcentajes ni las frecuencias que vayan apareciendo a lo largo del temario.
-He puesto en la comisión todas las imágenes que aparecen en la presentación del tema.
ETIOPATOGENIA
La invaginación intestinal (también llamada intususcepción) es la introducción de una porción del
intestino en sí mismo, es decir, la introducción de un segmento en la luz de otro segmento
adyacente. La porción proximal es arrastrada hacia el intestino distal por la actividad peristáltica. El
mesenterio del intestino proximal también es traccionado hasta el intestino distal,
comprometiéndolo, lo que produce obstrucción venosa y gangrena de la pared intestinal proximal.
El profesor comparó la disposición que adquiere un asa invaginada dentro de otra con un
telescopio reducido (ver primera imagen). En la segunda imagen se ve el colon con una zona
equimótica. El cirujano presiona el colon para que el asa vaya recuperando su forma normal.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
EPIDEMIOLOGÍA
Es la causa más frecuente de obstrucción intestinal y dolor abdominal en lactantes y en niños
preescolares (en los adultos es inusual). En escolares, la causa más frecuente de dolor abdominal
es la apendicitis. En la población general, la causa más frecuente de dolor abdominal es el
estreñimiento.
La invaginación intestinal se produce con mayor frecuencia durante el primer año de vida, sobre
todo entre los 5 - 10 meses de vida. Su incidencia es de 1,5-4 casos/ 1000 RNV. Es más frecuente
en varones. Sigue un patrón estacional (primavera, verano), debido a que es en estas épocas
cuando se producen picos de viriasis (algunos virus pueden ser la causa, como veremos más
adelante).
CLASIFICACIÓN
*Anatómica
• Ileocólica: es la más frecuente. Comienza cerca de la válvula ileocecal, con el íleon distal
traccionando hacia el colon proximal, es decir, el íleon terminal se introduce en el colon
ascendente. Esta forma se asocia con enfermedad celiaca.
• Ileoileal: esta forma puede ser autolimitada y revertir sin tratamiento.
• colocólica: muy poco frecuente.
*Etiológica
• Primaria (90%): <1-2 años de edad.
– Idiopática (etiología más frecuente).
– Hipertrofia de las placas de peyer por adenovirus y rotavirus. Es la segunda causa más frecuente,
después de la idiopática.
• Secundaria (5-10%): >2-3 años de edad.
– Divertículo de Meckel: es la causa secundaria más frecuente. Se produce una prolongación del
borde antimesentérico del íleon terminal.
– Duplicación intestinal.
– Pólipo intestinal.
– Linfoma: se puede descartar palpando la pared intestinal.
– Púrpura de Schonlein-Henoch.
CLÍNICA
El cuadro típico es el de un lactante que, súbitamente, empieza a llorar y encoger las piernas en
salvas cada 10-15 minutos (dolor abdominal cólico). Al encogerse, está intentando aumentar la
presión intraabdominal para vencer la invaginación y que el asa “salga” de ella. Después del ataque
se queda letárgico.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Las deposiciones son normales al principio pero,
posteriormente, son heces en “jalea de grosella” (rectorragia).
Éstas, adquieren un aspecto y color similar a la mermelada de
frambuesa. Se trata en realidad de la mucosa intestinal. La
presencia de heces en “jalea de grosella” (60%) da el
diagnóstico clínico (ver imagen).
Además, se producen vómitos (al principio alimentarios y
después biliosos). La tríada DOLOR + VÓMITO + SANGRADO
sólo se manifiesta en <25% de casos.
Otros síntomas frecuentes de invaginación intestinal incluyen: distensión abdominal, somnolencia,
respiración superficial, fiebre, infección respiratoria o intestinal previa.
EXAMEN FÍSICO
Durante la fase temprana los signos vitales son normales, es decir, la exploración física puede ser
normal. A la palpación, podemos encontrar la fosa iliaca derecha “vacía” (= signo de Dance. 13%)
o bien palpar una masa (en fosa derecha se localizaría una invaginación ileocólica, que es la más
frecuente) y/o una masa en hipocondrio derecho y colon transverso (= signo de la morcilla). Tacto
rectal: dedil normal o manchado de sangre. En las formas evolucionadas: deshidratación y
bacteriemia ocasionando taquicardia y fiebre. La bacteriemia se produce por el paso de bacterias
intestinales al torrente sanguíneo cuando hay mucha necrosis del tejido y puede progresar a sepsis
y ocasionar la muerte del paciente.
EXPLORACIONES COMPLEMENTARIAS
• Rx simple de abdomen: si es normal, es inespecífica. Es la primera prueba a realizar cuando
viene a urgencias un paciente con dolor abdominal (recordad que la primera causa de dolor
abdominal es el estreñimiento), aunque el diagnóstico de la invaginación intestinal lo da la
ecografía, como veremos a continuación. En la Rx simple de abdomen se puede observar
un patrón de obstrucción intestinal con asas de intestino dilatadas y niveles hidroaéreos
con ausencia de gas a nivel distal.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
• Ecografía abdominal: la lesión “en donut” se observa en los
cortes transversos y consiste en dos anillos de baja
ecogenicidad separados por un anillo hiperecoico. El “signo
del pseudoriñón” o imagen “en diana” o “en ojo de buey”
se observa en el corte longitudinal y aparecen como capas
hiperecoicas superpuestas (paredes edematosas de la
invaginación). Sensibilidad y especificidad del 100%. En la
imagen vemos la invaginación, dos paredes de intestino a
modo de “telescopio”.
TRATAMIENTO
• En primer lugar, estabilizar:
-Colocar SNG.
-ATB i.v. de amplio espectro (posible bacteriemia).
-Suero fisiológico 0,9% (20 cc/kg).
-AS con hemograma, bioquímica y coagulación.
-Gasometría venosa.
• Después, reducción de la invaginación. Se puede realizar mediantes dos procedimientos:
-Neumoenema: tras anestesiar al paciente, insuflar aire por el recto con una sonda rectal, con
control radioscópico. La tasa de éxito realizando esta modalidad es del 84% y la recurrencia del 7%.
La presión a la que insuflaremos será como máximo de 80-90 mmHg en lactantes menores y
110-120 mmHg en lactantes mayores. Si fuese necesario sobrepasar dichas presiones, no se
continúa insuflando aire. *Excepcionalmente, si vemos que falta muy poco para resolver la
invaginación, se puede correr el riesgo de seguir aumentando unos mmHg la presión.
Complicaciones: la principal es la perforación, de ahí la importancia de no sobrepasar los límites de
presión. Se puede producir perforación con neumoperitoneo masivo (0,5%) → evacuar el aire libre
con aguja del nº 18 y realizar laparotomía. Cuanto más grave esté el niño (tiempo de evolución de
la invaginación, necrosis, shock...), más complicaciones pueden producirse. En las imágenes
inferiores vemos el manómetro de presión con la sonda rectal, una sala de control fluoroscópico o
radioscópico y la monitorización continua de un paciente.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
En las imágenes siguientes vemos una “imagen de cobra” en la primera (imaginad una cobra con la
boca abierta donde señala la flecha), y la desaparición de la misma en la segunda (se ha resuelto la
invaginación tras realizar el neumoenema).Si se duda de si se ha resuelto o no, se comprueba con
una ecografía.
-Reducción hidrostática salina con control ecográfico: es la técnica de elección. Es sencilla, tiene
una tasa de éxito del 90%, no irradia y evita la perforación. Se realiza también con anestesia. Se
introduce por una sonda rectal suero fisiológico poco a poco pero, en este caso, no hay un límite
del volumen a introducir.
• Por último, tratamiento postreducción:
Se ingresa al paciente para observación. Se inicia tolerancia en 12-24h y si tolera se le da el alta
hospitalaria. No precisa revisión en consulta salvo que sea el tercer episodio, en cuyo caso habrá
que pensar un punto guía. Es decir, si recidiva una o dos veces, no es necesario un estudio, pero al
tercer episodio, hay que sospechar que, probablemente, la invaginación tenga una causa
secundaria (en este caso, en primer lugar habría que pensar en un divertículo de Meckel, ya que es
la causa más frecuente dentro de las secundarias). Es muy importante explicar a los padres del
paciente que, a pesar de haber tratado bien la invaginación intestinal, puede volver a producirse.
** Se puede realizar un tratamiento quirúrgico, de acuerdo con las siguientes indicaciones:
INDICACIONES ABSOLUTAS: si cuenta con alguna de las siguientes, directamente se realiza cirugía.
-Signos de perforación intestinal.
-Signos de shock.
-Fallo en la reducción con neumoenema o con presión hidrostática salina.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
INDICACIONES RELATIVAS:
-Edad >4años: por ser la edad a la que más frecuentemente se manifiestan tumores de intestino
delgado (por ej. linfomas), divertículo de Meckel... realizar cirugía permite descartar estas
patologías.
- >48h con síntomas.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Durante la cirugía, se aplican paños impregnados de suero fisiológico, para ver cómo responden las
asas intestinales: si se revitalizan, se mantienen; si no, se corta el segmento necrótico y se suturan
los cabos con anastomosis termino-terminal.
PRONÓSTICO
La tasa de recurrencia es de aproximadamente un 10% (8-12%). En los casos de invaginación
recurrente se volverá a repetir la reducción, ya que con poca frecuencia se encuentra un origen
específico. Se realiza cirugía en la primera recurrencia de un niño mayor, debido a una incidencia
mayor de tumores de intestino delgado en este grupo de edad, como hemos comentado en las
indicaciones relativas de la cirugía.
**Esta patología ha sido preguntada en el examen MIR. A continuación, se vieron en clase unas
preguntas que tratan sobre ella:
1. Una niña de 2 años se ha encontrado bien hasta hace aproximadamente 12h, momento en
que empezó con un cuadro de letargia, vómitos y episodio de llanto intermitente con un estado
de dolor visible. Coincidiendo con los episodios, retrae las piernas hacia el abdomen. En la
consulta emite una deposición de color rojo oscuro; el abdomen muestra plenitud y un discreto
dolor a la palpación. El diagnóstico más probable es:
1. Estenosis hipertrófica de píloro.
2. Apendicitis.
3. Infección urinaria.
4. Invaginación intestinal.
5. Enfermedad ulcerosa péptica.
2. La invaginación ileocecal:
1. Es una malformación congénita de la válvula ileocecal.
2. Es una obstrucción intestinal que aparece en la adolescencia.
3. Se diagnostica mediante la ecografía abdominal.
4. Debe ser tratada quirúrgicamente mediante laparoscopia.
5. Se presenta clínicamente mediante dolor abdominal, vómitos y hematemesis.
3. Un lactante de 6 meses que, estando previamente bien, comienza bruscamente con vómitos
asociados a episodios de llanto intenso, palidez y heces en “jarabe de grosella”, presenta como
diagnóstico más probable:
1. Gastroenteritis vírica.
2. Apendicitis aguda.
3. Cólicos del lactante.
4. Invaginación.
5. Diarrea secretora.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
4. Sobre la invaginación, ¿Cuál de las siguientes aseveraciones es verdadera?
1. La edad de presentación en la invaginación idiopática es mayor de 2 años.
2. La edad de presentación de la invaginación secundaria es entre los 3 y los 6 meses de edad.
3. Los adenovirus es la etiología más frecuente.
4. La tríada de dolor abdominal, vómitos y rectorragia aparece en el 30% de los casos.
5. El tratamiento de urgencia es quirúrgico.
*Se debe hacer tto sintomático de la viriasis, si la hay.
**La pregunta 4 es impugnable por dos motivos:
-La tríada aparece en menos del 25%.
-¿Qué se entiende por “urgencia” en la opción 5? La invaginación es una urgencia en sí misma pero
el tratamiento, de entrada, no es quirúrgico (la opción 5 en este caso sería falsa). Pero también se
puede referir a una urgencia entendida como complicación de la invaginación (por ejemplo, que el
paciente esté shockado...entonces la respuesta 5 sería correcta).
BIBLIOGRAFÍA
-Apuntes de clase.
-Diapositivas del Dr. Sánchez París.
-http://www.uptodate.com/contents/intussusception-in-children.
-http://www.pediaclic.org
-http://www.familiaysalud.es/nos-preocupa-que/dolor-abdominal-en-la-infancia.
-http://kidshealth.org/parent/en_espanol/medicos/intussusception_esp.html#
Dichoso el que olvida el porqué del viaje y, en la
estrella, en la flor, en el celaje... Deja su alma
prendida
(A. Machado)
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada Anto Pomares Varó
Profesor
Fecha y hora
Óscar Sánchez Paris
02/10/14; 14:00-14:50
CP-4
OBSTRUCCIÓN INTESTINAL NEONATAL
ALTA
1. INTRODUCCIÓN
En esta parte de la clase veremos las obstrucciones intestinales neonatales, que
podemos dividirlas en altas (tema de esta comisión) y bajas (objeto de otra clase).
La atresia yeyuno-ileal se da en un 50-60% de los casos
(es la más frecuente de todas y dentro de estas la
yeyunal). La siguiente por orden de frecuencia la
duodenal (30-40%) y por último, con menor frecuencia,
se da la atresia de colon (5%).
La clínica de la obstrucción neonatal alta consiste en
VÓMITOS BILIOSOS (MUY IMPORTANTE),
DISTENSIÓN ABDOMINAL MÍNIMA (porque la
obstrucción es alta y no hay muchas asas dilatadas. El
abdomen puede estar normal o incluso excavado) Y
MECONIO RETRASADO O INEXISTENTE (es
decir, puede haber meconio).
Página 1 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
2. ATRESIA DE DUODENO
A. GENERALIDADES
La atresia de duodeno (AD) es una enfermedad congénita que se da en 1 de cada 5000 –
10000 recién nacidos vivos (r.n.v.).
Un 30% de las atresias de duodeno se asocian a síndrome de Down (MIR).
Es posible hacer diagnóstico prenatal entre la 18ª y 20ª semana mediante:
Polihidramnios (17-50%) porque aunque puede deglutir el líquido amniótico,
este no pasa de cierto punto.
Ecografía prenatal: imagen típica de “doble burbuja” (aire en estómago y
primera porción del duodeno).
Descartar anomalías asociadas (50%) y hacer amniocentesis para poder realizar
el cariotipo (para descartar síndrome de Down).
IMPORTANTE quedarnos con que VÓMITOS BILIOSOS + SDME DE DOWN
probablemente sea una ATRESIA DUODENAL
B. EMBRIOLOGÍA
La atresia duodenal se produce por la no existencia de una apoptosis adecuada de las
células que forman el cordón fibroso del duodeno, el cual se debe recanalizar entre la
8ª y 10ª semana de gestación con lo cual falla la vacuolización del intestino anterior y se
produce la atresia.
C. ANOMALÍAS ASOCIADAS
Malformaciones cardiacas (20%)
Malrotación intestinal (20%)
Anomalías genito-urinarias (20%)
Atresia de esófago (20%)
Anomalías rectales (3%)
Asociación VACTERL
Esta última (asociación VACTERL) no se comentó en clase y tampoco está en el Power-
point. Sí que está en la comisión del año pasado. También dijo que no preguntaría
porcentajes.
D. CLASIFICACIÓN DE LA ATRESIA DUODENAL
La atresia duodenal se clasifica en tres tipos:
Tipo I: que a su vez que divide en Ia, Ib y Ic. Es la más frecuente, apareciendo
en el 92% de los casos. Se caracteriza por la presencia de una membrana
duodenal.
Tipo II: aparece en el 1% de los casos. Se caracteriza por la presencia de un
cordón fibrótico.
Tipo III: se da en el 7% de los casos, y se debe a un defecto del mesenterio.
Página 2 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
E. CLÍNICA
El 50% son prematuros con bajo peso (polihidramnios).
Vómitos biliosos (fundamental) en las primeras horas de vida en el 80% de los
casos (son postampulares). En el 20% restante los vómitos no son biliosos
puesto que son preampulares.
Deshidratación con alteraciones hidroelectrolíticas a causa de los vómitos.
Discreta distensión abdominal o abdomen excavado.
En un 25% de neonatos hay un fallo en la expulsión de meconio.
La clínica típica es la de un niño RN con muchos vómitos (más de 10) o vómitos
biliosos.
F. DIAGNÓSTICO
La radiografía simple de abdomen permite el diagnóstico de Estómago
atresia duodenal (sin necesidad de hacer más pruebas) ante la
presencia de doble burbuja sin aire distal.
Si hay dudas, como el paciente lleva una SNG, Duodeno
inyectas 15 cc de aire por ella y se formará
la imagen característica.
G. DIAGNÓSTICO DIFERENCIAL
Ante una clínica sugerente y una Rx simple de abdomen con:
“Imagen en doble burbuja SIN aire distal”:
atresia duodenal
“Imagen en doble burbuja CON aire distal”:
Membrana duodenal perforada
Páncreas anular
Malrotación intestinal
Vena porta preduodenal
H. TRATAMIENTO
• MÉDICO:
sonda nasogástrica
reponer pérdidas electrolíticas
ecocardio y eco renal
• QUIRÚRGICO: Duodenoduodenostomía de Kimura o en diamante. Se hace
una incisión transversa en el extremo proximal del duodeno y longitudinal en el
distal, cerrándose en forma de rombo o diamante. Se realiza esta técnica
Página 3 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
bypaseando la zona donde está la obstrucción para no llevarnos el Wirsung en
una anastomosis termino-terminal.
A veces, por dificultades para la aplicación de la técnica quirúrgica, se recurre a una
duodenoyeyunostomía.
3. PÁNCREAS ANULAR
A. EMBRIOLOGÍA
El esbozo pancreático ventral está formado por dos componentes que, en condiciones
normales se fusionan y experimentan una rotación alrededor del duodeno de manera que
se sitúan por debajo del esbozo pancreático dorsal.
En ocasiones la porción derecha del esbozo ventral emigra su camino normal, pero la
porción izquierda lo hace en sentido opuesto.
El duodeno es rodeado por tejido pancreático y se forma el páncreas anular alrededor
de la 2ª porción duodenal (compresión extrínseca del duodeno).
B. DIAGNÓSTICO
La clínica es la misma que en el caso de una atresia duodenal.
Respecto a las pruebas de imagen:
• Radiografía simple de abdomen: boble burbuja CON aire
distal
• Y como la anterior no es patognomónica, haremos diagnóstico
diferencial con otras entidades, permitiéndonos el diagnóstico
definitivo el tránsito gastrointestinal.
Página 4 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
a. Normal. b. Malrotación intestinal. c. Vólvulo intestinal (es una urgencia vital en cirugía
pediátrica) d. Atresia duodenal (que NO hay que hacer esta prueba) e. Páncreas anular.
Vemos la estenosis (flecha azul) y el ligamento de Treitz –unión duodenoyeyunal-
normoposicionado (flecha amarilla).
C. TRATAMIENTO
Siempre que sea posible haremos una duodenoduodenostomía láterolateral. Cuando
no se pueda, duodenoyeyunostomía.
4. ATRESIA YEYUNO-ILEAL1
A. GENERALIDADES
Es la causa más frecuente de obstrucción intestinal neonatal (1:1000 r.n.v). El 35% se
dan en prematuros.
• Etiopatogenia: Son de etiología vascular: trombosis de vasos mesentéricos
intraútero, hernia interna intraútero, perforación intestinal intraútero.
• El diagnóstico diferencial de la atresia ileal lo haremos con:
íleo meconial
síndrome del tapón meconial
malrotación intestinal
enfermedad de Hirschsprung.
• Estas atresias se asocian con:
defectos de la pared abdominal (gastrosquisis) (asas
intestinales fuera de la pared abdominal)
atresia biliar
atresia duodenal
atresia de colon
enfermedad de Hirschsprung (19 casos)
madre cocainómana (espasmo vascular en feto)
glomerulonefritis materna
Todas las atresias pueden cursar con otras atresias de localización inferior. En el
quirófano, para descartarlas, inyectamos suero con una sonda en el extremo distal y
vemos como se rellena.
1
Recuerda que aunque la describa aquí, la atresia ileal es una obstrucción baja.
Página 5 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
B. CLASIFICACIÓN DE ATRESIA YEYUNO-ILEAL
Tres tipos:
• Tipo I: presencia de membrana. Se da en un 20% casos.
• Tipo II: cordón fibrótico. Se da en un 30% casos.
• Tipo III: es la más frecuente, apareciendo en el 46% de los casos.
Tipo IIIa: defectos en la unión con el mesenterio.
Tipo IIIb: defecto típico en cáscara de manzana (apple peel) o en
árbol de navidad.
• Tipo IV: atresias múltiples en casi un 20%
C. CLÍNICA
• Polihidramnios
• En las primeras 24-48h de vida comienzan con vómitos biliosos, distensión
abdominal (más evidente cuanto más bajo sea el nivel de la obstrucción).
• Puede haber o no paso de meconio.
D. DIAGNÓSTICO
• Radiografía simple de abdomen:
o Atresia yeyunal: triple burbuja sin aire
distal
o Atresia ileal: múltiples asas dilatadas
• TGD/Enema opaco: Según sospechemos que sea obstrucción alta (yeyunal) o
baja (ileal), respectivamente. En el caso del enema opaco el diagnóstico
diferencial sería:
Página 6 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
(d). Normal. (a). Microcolon. (b). Microcolon corto. (c). Cambio de calibre
Esta imagen muestra un microcolon en un enema opaco. El
diagnóstico es de una atresia ileal.
E. TRATAMIENTO
Primero hay que descartar la existencia de otras atresias intestinales asociadas (20%).
El objetivo es resolver la atresia, conservando la mayor longitud de intestino (para
intentar evitar un síndrome de intestino corto), por lo que trataremos de hacer
anatomosis termino-terminal.
Si hay mucha discrepancia entre los cabos realizaremos una anastomosis termino-
oblicua o en boca de pez (incisión longitudinal en el borde antimesentérico asa distal,
para ampliar la apertura y evitar una estenosis futura de la sutura).
BIBLIOGRAFIA: Apuntes de clase, diapositivas del profesor, comisión año
2013/2014.
Página 7 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Nº Clase 7 Hora 14-14:50
CP Tema Obstrucción Intestinal alta (continuación). OI BAJA (inicio)
Profesor Óscar Sánchez París
20/10/14 Comisionado Raquel Revert Gil
OBSTRUCCIÓN INTESTINAL ALTA.
MALROTACIÓN INTESTINAL
1. EMBRIOLOGÍA
Durante la 3ª semana de gestación el intestino primitivo es una formación tubular
rectilínea que se divide en tres partes:
Intestino anterior (porción craneal)
Intestino posterior (porción caudal)
Intestino medio: es la que en un futuro se diferenciará desde el duodeno hasta el
colon transverso. Irrigada por la arteria mesentérica superior.
El intestino medio sufrirá las siguientes diferenciaciones:
1. Herniación: El intestino medio al crecer, deja de tener cabida en el
abdomen y se hernia en el saco vitelino, que se comunica con el resto del
intestino por el conducto onfalomesentérico. El eje es la arteria
mesentérica superior (AMS). El intestino medio formará dos asas:
o Intestino medio porción prearterial (asa duodenoyeyunal)
Conforme va creciendo el intestino medio fuera del abdomen, el
asa duodenoyeyunal sufre un proceso de rotación de 90º en
dirección contraria a las manecillas del reloj y posicionándose a la
derecha de la AMS (Fig. a y b).
Conforme crece el intestino y antes de que llegue la segunda fase
sufre otra rotación de 90º de tal forma que el asa duodenoyeyunal
se posiciona posterior al eje de la AMS (Fig. c)
o Intestino medio porción caudal o postarterial (asa cecocólica)
La rotación del asa cecocólica en esta primera fase corre de forma
paralela a la del asa duodenoyeyunal. La unión íleo-cecal empieza
inferior a la AMS y rota en un primer momento 90º situándose a la
izquierda de la AMS. Antes de retornar al abdomen rotará otros
90º (ventralmente a la AMS) (Fígs. a,b y c).
2. Retorno al abdomen:
o ASA DUODENOYEYUNAL. Es la primera que retorna al abdomen y
para esto sufre otro proceso de rotación de 90º alrededor de la
AMS. El resultado es una rotación de 270º alrededor del ejee de la
AMS con el asas duodenoyeyunal fijada en la cara posterior a la
izquierda de la AMS a nivel del ligamento de Treitz. (Fíg. d)
Página 1 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
20/10/10 [CIRUGÍA PEDIÁTRICA]
o ASA CECOCÓLICA. A la vez que retorna al abdomen sufre una
nueva rotación de 90º (total de 270º) lo que lo posiciona a la
derecha de la AMS. (Fíg. d)
Página 2 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 20/10/14
3. Fijación:
Página 3 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
20/10/10 [CIRUGÍA PEDIÁTRICA]
Desde la 12ª semana de gestación hasta después del nacimiento el colon y su
mesenterio se fijan a la pared posterior del abdomen. Este proceso de fijación
no es posible hasta que el proceso de rotación haya concluido. La fijación del
colon ascendente, descendente y del intestino delgado proporciona una
fijación estable y de base amplia para el mesenterio e intestino delgado, lo que
asegura que no sea posible un vólvulo.
2. GENERALIDADES
Incidencia: 0.5%.
El 60% de los pacientes que requieren cirugía son neonatos (40% en la 1ª semana).
La malrotación es un componente integral del onfalocele, gastrosquisis y de la hernia
diafragmática.
3. CLASIFICACIÓN
NO ROTACIÓN
ROTACIÓN
INVERSA
MALROTACIÓN
•Duodenal
•Cecocólica
*En negrita las 2 más importantes
1-No rotación
El intestino delgado (ID) está situado a la derecha y el grueso (IG) a la izquierda.
Los pacientes están asintomáticos.
2 -Malrotación
El ciego y parte del colon ascendente están situados en el epigastrio, a la izquierda de la AMS.
Bandas de Ladd
Página 4 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 20/10/14
Se extienden desde el ciego mal posicionado (que no termina de bajar). Se fijan a hipocondrio
derecho e hígado y debajo queda el duodeno.
4. CLÍNICA
• 30% Primera semana de vida
• 50% Antes del primer mes de vida
– Vómitos biliosos
– Abdomen excavado (no distendido)
– Vólvulo de intestino medio
• 10-18% > 1 año de edad
• Obstrucción duodenal parcial crónica. Se puede presentar a cualquier edad.
– Vómitos recurrentes
– Cuadro de malabsorcion
– Dolor abdominal crónico
• Bandas de Ladd
Se extienden desde el ciego mal posicionado (que no termina de bajar). Se fijan a
hipocondrio derecho e hígado y debajo queda el duodeno.
Vólvulo de I.Medio
Ocurre cuando el intestino delgado rota sobre el propio
mesenterio (AMS), resultando un compromiso vascular y
posible necrosis de todo el intestino medio si no se trata a
tiempo.
Es una emergencia vital que debuta con vómitos biliosos en un
paciente previamente asintomático, con rápido deterioro
general. Al principio no hay distensión abdominal porque es
una obstrucción alta. El paso de deposiciones es normal y
puede haber rectorragia por el compromiso de la mucosa. Si
sigue progresando el niño desarrolla hipotensión, fallo
respiratorio, acidosis y sepsis.
5. EXPLORACIONES COMPLEMENTARIAS
- Radiografía simple de abdomen: doble burbuja con aire distal. En caso de vólvulo: imagen en
“piel de naranja” o “sacacorchos”
- Tránsito gastrointestinal: Comprobación de la posición de la unión duodenoyeyunal: Es típico
del vólvulo que esta unión se encuentre a la derecha de la línea media por debajo del ombligo.
Las asas de intestino delgado proximales están a la derecha de la línea media.
OJO Aquí el profesor remarcó que no es necesario realizar una ECOGRAFÍA (que a quien lo
pusiera en el examen, se lo cargaba). Y señaló que la eco se realiza sólo para descartar un
píloro hipertrófico y una invaginación intestinal.
6. TRATAMIENTO
Intervención de Ladd.
Página 5 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
20/10/10 [CIRUGÍA PEDIÁTRICA]
Consiste en la desrotación quirúrgica de las asas volvuladas en el sentido de las agujas del
reloj. A continuación, se seccionan las bandas de Ladd y se ubica en la cavidad el intestino
delgado a la derecha, y el ciego y colon a la izquierda –posición de no rotación-. Además, se
realiza apendicectomía.
Puede recidivar.
OBSTRUCCIÓN INTESTINAL BAJA
ÍLEO MECONIAL
Se trata de una obstrucción intestinal intraluminal que ocurre en la época prenatal o neonatal
temprana nivel del íleon terminal producido por meconio espeso (el meconio es muy espeso y
no va a poder circular bien quedando impactado a nivel del íleo) que se adhiere a las paredes
del intestino.
• 1/3000 r.n.v
• 15% de los pacientes con fibrosis quísticas lo desarrollarán.
• 95% de los pacientes con íleo meconial simple desarrollaran fibrosis quística.
• Igual proporción de hombres y mujeres.
ÍILEO MECONIAL SIMPLE (66%):
o Vómitos biliosos
o Distensión abdominal
o Fallo en la expulsión de meconio
o Las asas intestinales dilatadas son visibles a la palpación
Página 6 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 20/10/14
ÍLEO MECONIAL COMPLICADO
• PERITONITIS MECONIAL
FISIOPATOLOGÍA
o Peritonitis química estéril
o Bloqueo del meconio (semana 20 de gestación) que produce distensión de asas y
necrosis de pared con posterior solución de continuidad.
o Perforación intestinal y salida de meconio en contacto con el peritoneo.
CAUSAS
• Atresia intestinal
• Invaginación intestinal
• Vólvulo intestinal
• Fibrosis quística
CLÍNICA
– Distensión abdominal
– Masa palpable
– Pared edematosa y eritematosa
– Sepsis
1. PRUEBAS COMPLEMENTARIAS:
• RX SIMPLE DE ABDOMEN
- SIMPLE: Se verán asas dilatadas (a más cantidad, más baja será la obstrucción) y
meconio con aire en íleo terminal-ciego. El aire se mezcla con el meconio, entonces se
Página 7 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
20/10/10 [CIRUGÍA PEDIÁTRICA]
ve a nivel del íleon terminal, sobre la fosa ilíaca derecha burbujas que es el aire que
rodean al meconio.
Con este patrón hacemos el diagnóstico diferencial con la atresia ileal: en la atresia
ileal no observaremos está imagen porque hay un stop a nivel íleo terminal y no puede
pasar aire, sin embargo en el íleo meconial aunque haya obstrucción va a poder pasar
algo de aire mezclándose con el meconio.
- P. MECONIAL: meconio calcificado en toda la cavidad (puede bajar hasta escroto). No
hay niveles hidroaéreos (el aire no puede pasar)
• ENEMA OPACO
- Gold standard para hacer el diagnostico diferencial de las
obstrucciones intestinales bajas.
- Se observa un microcolon (por desuso, el meconio no ha pasado
al resto del intestino por lo que no se ha utilizado) con restos de
meconio.
- En la imagen de la derecha veríamos el microcolon hasta que el
contraste llega al íleo terminal donde empieza a atenuarse
viéndose entonces como una especie de empedrado, que es lo
que se marca con las flechas.
2. TRATAMIENTO
ENEMA OPACO HIPEROSMOLAR (Gastrografin):
• Resuelve el 60% de los casos.
• Desimpacta el meconio por disolución con el líquido
atraido a la luz intestinal.
• Requiere rehidratación y cobertura antibiótica.
• ¡Peligro de perforación intestinal!
QUIRÚRGICO:
• Derivación ileal (ileostomía) para facilitar la limpieza del meconio con solución
hiperosmolar, suero salino o N-acetilcisteina.
Se realiza una derivación en T (es decir, se saca el íleon al exterior, y se une
el cabo distal al cabo proximal). Por la ileostomía se introduce o bien suero,
o bien N-acetilcisteina o gastrografín, y con esto se intenta que se disuelva
el meconio que quede. En cirugía todas las ostomías son de cabos
separados (se aboca un cabo fuera y el otro se cierra, o se abocan los dos
fuera), pero en este caso se realiza una anastomosis en T (el Íleo meconial
es la única situación donde está indicada la anastomosis en T), dejamos
los cabos unidos, de este modo nos aseguramos que el microcolon se
quede lo menos desfuncionalizado posible, ya que una parte del meconio
saldrá por la ileostomía, pero otra parte continuará el recorrido por el
colon, activando, de este modo, su funcionamiento.
3. DIAGNÓSTICO DIFERENCIAL
Síndrome del tapón meconial.
Atresia intestinal (ileal).
Atresia de colon.
Página 8 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 20/10/14
Síndrome del colon hipoplásico pequeño. Asociado a madres diabéticas (PREGUNTA MIR)
Enfermedad de Hirschsprung
Estenosis anal.
Sepsis neonatal.
Obstrucción funcional por prematuridad.
Drogas maternas (ejemplo: la cocaína produce una vasoconstricción a nivel del íleon)
Hipotiroidismo
SÍNDROME DEL TAPÓN MECONIAL
• Obstrucción temporal del intestino grueso, aliviada por la expulsión de tapones de
meconio sin complicaciones añadidas.
• Puede asociarse (14-20%) a otras anomalías como la enfermedad de Hirschsprung,
fibrosis quística y síndrome del hemicolon izquierdo pequeño.
• La motilidad anormal del colon hace que el meconio del hemicolon izquierdo y recto
formen un tapón que no puede evacuarse.
1. ETIOLOGÍA
Síndrome del colon izquierdo hipoplásico (Asociado a madres diabéticas).
Fibrosis quística
Enfermedad de Hirschsprung
Drogadicción materna
Prematuridad
Tratamiento con sulfato de magnesio de la preclampsia materna
2. CLÍNICA
• Distensión abdominal progresiva.
• Evacuación de meconio escaso o nada
• Vómito tardío
3. TRATAMIENTO
• Estimulación rectal
• Lavados con suero fisiológico templado a 10ml /kg cada 8 horas
• Realizar prueba de sudor, biopsia rectal y pruebas para descartar hipotiroidismo
BIBLIOGRAFÍA:
Apuntes de clase.
Diapositivas del profesor.
Comisiones de otros años (¡Gracias Miriam!)
“A los hombres les probaría cuán equivocados están, He aprendido que todo el mundo quiere vivir
al pensar que dejan de enamorarse cuando envejecen, en la cima de la montaña,
sin saber que envejecen cuando dejan de enamorarse. Sin saber que la verdadera felicidad está
A un niño le daría alas, en la forma de subir la escarpada.
pero le dejaría que él solo aprendiese a volar. He aprendido que cuando un recién nacido
A los viejos les enseñaría que la muerte aprieta con su pequeño puño,
no llega con la vejez sino con el olvido. por vez primera, el dedo de su padre,
Tantas cosas he aprendido de ustedes, los hombres lo tiene atrapado por siempre. “
Página 9 de 9
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Nº Clase 8 Hora 15:00-15:50 H
CP Tema Obstrucción intestinal BAJA neonatal
Profesor Dr. Óscar Sánchez París
20/10/14 Comisionado María Rodriguez Romero
OBSTRUCCION INTESTINAL BAJA:
ENFERMEDAD DE HIRSCHSPRUNG ó
HIPOGANGLIONISMO:
¿QUÉ ES?
Es una enfermedad que produce una obstrucción intestinal y dilatación o
hipertrofia de una sección del colon (megacolon). La enfermedad se
produce por una ausencia de células ganglionares (zona patológica),
por lo que no se produce peristaltismo, además la zona patológica no se
puede distender.
Se debe su nombre al Dr. Harald Hirschsprung, médico danés que en 1888
describió el caso de dos niños que habían fallecido con una gran distensión
abdominal.
La obstrucción intestinal se debe a que una parte del colon presenta una
inervación anómala, secundaria a una interrupción en la migración de los
neuroblastos dando lugar a una ausencia del SNP intramural (plexos de Meissner
y Auerbach) y una hiperplasia compensadora del SNP extramural (fibras
colinérgicas). Es decir, hay una ausencia de los plexos de Meissner y
Auerbach, y donde no hay células ganglionares los troncos nerviosos se
hipertrofian.
GENERALIDADES
Afecta a 1/3000-5000 recién nacidos vivos.
Es más frecuente en varones (80%) 4:1 cuando afecta a recto-sigma
(PREGUNTA MIR)
Cuando afecta a segmentos largos que pueden incluir a todo colon e incluso a
todo el intestino (es muy raro) es igual de frecuente tanto en niños como en
niñas.
La mayoría son esporádicos.
Hay una incidencia familiar de entre un 7-10%.
Anomalías asociadas:
- Trisomía 21 del 5%-15%. (la trisomía del 21 también se asocia a la
atresia duodenal) (PREGUNTA MIR)
- Neurocristopatías (enfermedades que Llevan a un fallo en la derivación
de los neuroblastos a partir de la cresta neural): Sdre. de Waardenburg
y el Sdre. de hipoventilación (Ordine).
- Atresia de colon.
- Síndrome del tapón meconial (14%).
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
ANOMALÍAS MÁS FRECUENTES
La mutación más frecuente asociada a la EH se encuentra en el brazo largo del
cromosoma 10 (protooncogen RET y el protooncogen EDNRB). El RET es
importante porque se asocia con los síndromes MEN IIa y IIb y con casos esporádicos
de Ca. medular de tiroides (PREGUNTA MIR) (por lo que a un niño diagnosticado de
Ca.medular de tiroides hay que descartar que no tenga una EH). Las mutaciones en RET
ocurren en cerca del 25% de los casos familiares y en 15% en los esporádicos.
EMBRIOLOGÍA
Los neuroblastos que derivan de la cresta neural aparecen en el esófago a las
cinco semanas de gestación, luego emigran a través del vago hasta el conducto anal
durante las semanas cinco a doce. Estas células se forman justo por fuera de la capa
circular y después quedan en medio de las capas musculares longitudinales. El plexo
submucoso se forma con neuroblastos que migran del plexo mientérico hacia la
submucosa y la mucosa a través de la capa muscular circular.
ANATOMÍA
CLASIFICACIÓN
Se clasifica por su localización:
Rectosigma 75%-80%.
Puede llegar hasta colon transverso17%.
Puede afectar a todo el colon 10%.
Y es muy raro, muy raro, que afecte a nivel yeyuno-ileal <5% (aganglionismo
total de todo el intestino, desde el recto hasta el yeyuno)
CLÍNICA
La mayoría dan clínica en el periodo neonatal, sin embargo hay niños con EH
que se diagnostican cuando son mayores (7-8 años) por estreñimiento crónico.
En el 90% de los niños hay una fallo en la expulsión de meconio en las
primeras 24-48h (este es el tiempo en el que se debe expulsar el meconio, si se
retrasa, debemos sospechar que algo raro pasa). Pero hay que tener en cuenta
que el que expulse meconio no descarta la EH ya que aproximadamente un 25%
va a expulsar meconio teniendo la enfermedad.
Vómitos biliosos
Página 2 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
Distensión abdominal
Estreñimiento (solo en más mayores, por lo que el profesor lo quitaría de la
patología neonatal)
Puede dar ENTEROCOLITIS entre un 10-15% (es la causa más importante de
morbi-mortalidad en la EH):
- El niño tiene una gran distensión abdominal
- Si se estimula con una sonda rectal el ano, solo con estimular sale las
heces de forma explosiva, mal olientes y de color grisáceo (el profesor
dijo que en el momento que estimulas, mejor apártate porque las heces
salen explosivas).
- Fiebre
- Afectación del estado general
- Puede dar lugar a un cuadro de sepsis e incluso acidosis metabólica
EXPLORACIONES COMPLEMENTARIAS
RX SIMPLE DE ABDOMEN:
- Se observa el colon muy distendido por toda la placa, y
habrá una zona donde no haya aire, esta es la zona de
transición. Niveles hidroaéreos.
ENEMA OPACO:
- El enema opaco identifica la zona de transición. (flecha)
- Cuando la zona de transición no se observa de forma muy
clara, hay un signo que nos hace sospechar que un niño
pueda tener EH, y es que se produzca un enlentecimiento
en la evacuación del bario o del contraste que le
hayamos puesto de más de 24h.
- Si con el enema sospechamos de una EH procederemos a
realizar una biopsia rectal.
- MUY IMPORTANTE: el enema opaco NO es la prueba
diagnóstica ya que en neonatos puede haber falsos
negativos, el diagnóstico siempre lo dará la biopsia.
- En la imagen de la derecha veríamos la zona de transición
marcada por la flecha: por debajo veríamos la zona
aganglíonica y por encima (distendida) la zona
ganglíonica.
BIÓPSIA RECTAL:
Se trata de la prueba “gold standard”: es la que nos va a dar el diagnóstico.
- Se puede hacer abierta, o con una pistola que se llama Pistola de Nobbet.
- Se hace a unos 2-3 cm proximal a la línea dentada o pectínea, donde va a
coger mucosa, submucosa y muscular, hay que coger las tres capas para que
sirva la muestra (esto se hace en la cuna del niño, no hace falta anestesiar ni
nada, no duele, o eso dicen).
Página 3 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
- En la biopsia se observa:
Ausencia de células ganglionares en los plexos mienterico y
submucoso.
Presencia de troncos nerviosos hipertrofiados en el espacio
normalmente ocupado por las células ganglionares.
Por inmunohistoquímica veríamos que hay un aumento de la
actividad de la acetilcolinesterasa en la lámina propia y en la
muscular y esto se debe a la hipertrofia de los troncos nerviosos.
MANOMETRÍA ANO-RECTAL:
No se suele hacer ya que los niños pequeños son muy poco colaboradores, pero
debemos saber que con la manometría se puede llegar al diagnóstico.
- Diagnóstico hasta el 85% de los casos.
- En pacientes sanos, la insuflación de un balón rectal distiende el recto y le
causa relajación del esfínter anal interno.
- En los pacientes con EH, la curva de presión del canal anal y el recto distal
muestra contracciones rítmicas multisegmentarias y falta de relajación del
esfínter interno, no se puede distender ya que no hay fibras parasimpáticas.
TRATAMIENTO
1. Tras confirmar el diagnóstico se tratará al paciente mediante técnicas
de descompresión (“NURSING”) utilizando sondas rectales
(estimulando el recto a unos 5cm pasando la zona de transición, ya
que como sabemos el 80% son a nivel recto sigma) y haciendo
lavados con suero fisiológico templado a 10cc/kg (3 veces al día)
con el fin de que disminuya la distensión y facilitar la evacuación de
materia fecal para evitar la enterocolitis hasta que se haga el
procedimiento definitivo a los 2-3meses de edad. (Antiguamente se
hacía una colostomía, y cuando el niño tuviese 2 o 3 meses, y pesase 10kg, se
hacía el procedimiento definitivo, hoy en día se intenta, siempre que se pueda,
hacer todo el procedimiento en un tiempo).
2. ANTIBIÓTICOS (vancomicina, metronidazol)
3. TRATAMIENTO QUIRÚRGICO:
El objetivo es resecar la zona agangliónica que es la que causa la obstrucción
intestinal funcional (descenso abdomino-perineal de intestino sano y resección
de segmento agangliónico)
Hoy en día la mayoría se operan en el periodo neonatal sin realizar
previamente una colonostomía de descarga, aunque hay ocasiones en las que
sí que debe realizarse una colostomía: (“colostomía en cañón de escopeta”)
Página 4 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
- Cuando falla el “nursing”. Si vemos que con el “nursing” no
conseguimos sacar todo el meconio, el niño empeora, empieza con
vómitos y distensión, debemos realizar la colostomía
- Prematuros y de bajo peso
- Colostomía en zona de transverso o sigma (en zona gangliónica)
- Ileostomía (en los EH largos que afectan a todo el colon)
Hay veces que a simple vista se ve una zona más estrecha que otra, entonces
saben que ahí está la zona de transición y es en esa zona donde realizan la
colostomía, con la zona más dilatada. Pero muchas veces no es así de fácil, y no
se ve a simple vista, entonces lo que hacen es coger biopsias intraoperatorias
desde abajo, y se las mandas al anatomopatólogo, el cual va diciendo si hay
células o no, hasta que te diga que sí hay células y es ahí donde debes hacer la
colostomía, ya que donde no hay células es la zona patológica. (a simple vista lo
hacen en momentos de urgencia, pero siempre que se pueda debe de hacerse
con biopsias intraoperatorias).
No tiene incontinencia porque la musculatura anal está bien.
Complicaciones de la cirugía
- Enterocolitis: 25% (morbi-mortalidad) Puede aparecer antes de la
operación, en el postoperatorio inmediato o años después de la intervención.
- Estrechamiento
- Infección de la herida
- Fuga de la anastomosis
- Obstrucción intestinal
DIAGNÓSTICO DIFERENCIAL
• Mecánicas:
– Atresia ileal.
– Atresia de colon.
– Malformaciones anorectales.
– Ileo meconial.
– Síndrome del tapón meconial.
• Funcionales:
– Prematuridad.
– Hipotiroidismo.
– Sepsis.
– Alteraciones hidoelectrolíticas.
Síndrome de colon izquierdo hipoplásico
Página 5 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
OBSTRUCCION INTESTINAL BAJA
NEONATAL
MALFORMACION ANORRECTAL
1. MALFORMACIÓN ANORRECTAL
EPIDEMIOLOGÍA
o 1/5000 recién nacidos vivos.
o Es más frecuente en niños (60:40).
IMPORTANTE
MALFORMACIONES ASOCIADAS
o VACTERL: -EcoLumbar
- Anomalías vertebrales: hemivertebra, escoliosis, disrafismo espinal,
-Ecocardíaca
médula anclada (25%).
- Anomalías cardiacas: Tetralogía de Fallot, CIV (15%). -Eco renal
- Anomalías genitourinarias (60%). Las más frecuentes son atresia renal y
reflujo vesicoureteral. Para
o Anomalías gastrointestinales (20%). descartar los
o Anomalías cromosómicas (10%). problemas
más graves
o Anomalías del SNC (5%).
CLASIFICACIÓN DE PEÑA EN NIÑAS
Peña es un cirujano pediátrico mejicano que revolucionó el tratamiento de las
malformaciones anorrectales. El profesor dijo que esta clasificación ya no se usa.
I. FÍSTULA RECTOPERINEAL O ANO
ANTERIOR
- El recto está en su posición normal dentro del esfínter,
excepto en su porción inferior que se encuentra
localizado anteriormente. El recto y la vagina están bien
Página 6 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
separados. Es decir, el recto sí que tiene ano, pero tiene ano en forma de fístula, no es
un ano normal, no está en la posición normal, por eso se dice ano anterior, ya que el
ano aboca anterior al esfínter. Se explora con el niña en decúbito supino y las piernas
abiertas. Se observa que el ano está más cerca de la vagina (más anterior).
-Si no se repara puede dar clínica de estreñimiento. Son de buen pronóstico. Se tratan
con dilataciones hasta hacer una anorrectoplastia definitiva. El profesor dijo que solo
se hace colostomía si hay estreñimiento (no se expulsa meconio) o distensión (*IMP, en
el resto de fístulas la colostomía se hace siempre), es decir, si con dilataciones no
puede controlarse.
II. FÍSTULA RECTO VESTIBULAR
- Es el defecto más frecuente en niñas. Y de buen pronóstico.
- Si se inspecciona el vestíbulo podemos ver un orificio uretral normal, una vagina
normal, y un tercer espacio que es la fístula retrovestibular, es decir, el recto aboca al
vestíbulo (en la niña normal, en el vestíbulo desembocan solo la vagina y el tracto
urinario).
III. CLOACA
-Repaso: la cloaca es la zona del embrión en formación
donde termina el aparato reproductor, urinario y el
digestivo anterior. En el feto normal se separan
posteriormente por tabiques, pero en este caso dicha
separación no ocurre.
- Las niñas con cloaca no tienen ni uno, ni dos, ni tres
orificios, sino que solo tienen un orificio, es decir
tienen un canal común en el que vacían el recto, el tracto
urinario y la vagina.
- Son las de peor pronóstico (las más graves y las de
peor tratamiento).
- Se operan al cabo del año. Y antes de operar debes
hacer una endoscopia para ver exactamente a qué nivel está
la salida del aparato reproductor, la salida del aparato
digestivo y del urinario.
- Las malformaciones cloacales con canales más cortos
(menores de 3cm) son menos complejas (el abordaje es en
decúbito prono y la cirugía es más simple), mientras que las
Página 7 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
que presentan canales más largos exigirán una reparación quirúrgica más compleja (en
decúbito supino).
DIAGNOSTICO Y TRATAMIENTO
CLASIFICACIÓN DE PEÑA EN NIÑOS
perineal
I. FÍSTULA RECTOPERINEAL
- Igual que ocurre en las niñas: el recto está en su posición
normal dentro del esfínter, excepto en su porción inferior que se
encuentra localizado anteriormente.
- Se puede manejar con dilataciones (con el objetivo de evitar una
colostomía) hasta que se realice una ARPSP definitiva.
II. FÍSTULA RECTOURETRAL
Página 8 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
- La fístula más frecuente en niños es la rectouretral, y dentro de esta hay dos tipos, la
que aboca a la uretra bulbar y la que aboca a la uretra prostática. Dentro de la fístula
rectouretral la más frecuente es la bulbar.
II.1. FÍSTULA RECTOURETRAL BULBAR
-El complejo muscular anorrectal aparece bien desarrollado. Sacro
bien formado, un surco prominente en la línea media y una fosita anal
bien marcada.
-El diagnóstico en esta fístula se haría detectando meconio en la
orina, es decir, hay que pedir una analítica de orina para ver si tiene
meconio o no.
-Tiene mejor pronóstico que la prostática, a efectos de incontinencia.
II.2. FÍSTULA RECTOURETRAL PROSTÁTICA
-Tiene musculatura mal desarrollada, sacro anormal y periné
plano con un surco en la línea media deficiente y una fosita anal
sutil.
-Peor pronóstico funcional que la anterior.
Para saber si un paciente va a tener una buena
continencia o no hay que fijarse en los glúteos:
-Si los glúteos están bien marcados y tenemos como una
insinuación de dónde debería estar en ano, van a ser de buen
pronóstico.
-Si no se marca el pliegue interglúteo (glúteos planos), no se ve surco ni se insinúa
donde debería de estar el ano, la malformación será más alta y serán de mal
pronóstico.
FÍSTULA BULBAR FÍSTULA
(buen pronóstico) PROSTÁTICA (mal
pronóstico)
III. FÍSTULA RECTOVESICAL
-Aparece en un 10%. Tiene un complejo muscular
anorrectal mal desarrollado, así como un sacro anormal.
Página 9 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
DIAGNÓSTICO Y TRATAMIENTO
distancia de la bolsa rectal al margen anal).
INVERTOGRAMA
Es una radiografía con el niño invertido y en posición lateral, de forma que al elevar
la pelvis la burbuja de aire intestinal vaya al fondo de saco rectal y podamos verla en
la radiografía. En el recién nacido debe realizarse pasadas varias horas, al menos 18-
24hs, para que haya aire deglutido suficiente. Se
coloca un objeto radioopaco en la zona donde
debería de estar el ano (por ejemplo una moneda), y
se mide la distancia entre este y la bolsa rectal,
llena de aire. Si la bolsa rectal la vemos por debajo
del sacro tendrá mejor pronóstico que si la vemos
por encima de éste, ya que en el primer caso con una
anorectoplastia sagital posterior podemos llegar al
defecto. Sin embargo, si la bolsa rectal está por
encima del sacro, aparte de una anorectoplastia
sagital posterior también tendremos que abordarlo
vía abdominal.
Tratamiento quirúrgico:
Página 10 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CIRUGÍA PEDIÁTRICA 9 20 de octubre de 2014
o Colostomía sigmoidea de cabos separados. Esta técnica se utiliza en todos los
casos, excepto en la fístula perianal que se hacen dilataciones, tanto en niñas como
en niños. Es sigmoidea y de cabos separados para conseguir lo siguiente:
- Si en vez de hacerlo en el sigma lo hacemos en el colon ascendente,
después va a costar mucho poder bajar el resto de intestino, por eso se
hace en el sigma, para que cuando hagamos la cirugía definitiva sea más
fácil poder traerte el intestino.
- Y es de cabos separados porque no
queremos que pasen más heces al
aparato urinario, ya que la fístula
conecta la vía urinaria con la vía
rectal.
Por tanto, con esta técnica se consigue:
- Evitar la distensión abdominal.
- Evitar el paso de material fecal por la
fístula.
- Realizar colostograma distal previo a
la reparación definitiva.
o Después de la colostomía, a los dos o tres meses (4-8 semanas según el
esquema) se realiza la operación definitiva que es una anorectoplastia por
vía sagital posterior (Peña).
BIBLIOGRAFÍA
- Apuntes de clase
- Diapositivas del profesor(Adjuntadas a esta comisión)
- Comisiones de años anteriores
Quiero agradecer al comité de promo y prensa por su duro trabajo durante todo un año, chicos lo
conseguimos salio genial, el istacnem fue todo un éxito y todo no hubiera sido posible sin vosotros
Tambien felicitar al resto de organizadores, os lo currasteis un montón, me alegro de haber participado
en esto con tod@s vosotr@s.
Por último decir que este año seguro que es inolvidable y que merece la pena vivirlo sin agobios y
disfrutar de lo que nos queda
Muchas gracias chupipandi porque se q puedo contar con vosotras
Página 11 de 11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada: ANDREA ROMERO VALERO
Profesor: ÓSCAR SÁNCHEZ PARÍS CP-9
Fecha y hora: 23/10/2014 15:00-15:50h
NEUROBLASTOMA
(CIRUGÍA ONCOLÓGICA I)
El profesor advirtió de que la mayoría de las preguntas del examen caen de cirugía oncológica
CONCEPTO Y EPIDEMIOLOGÍA
El neuroblastoma es un tumor que deriva del tejido simpático. Siendo el tumor sólido
extracraneal más frecuente en edad infantil (5-10%). Representa el cuarto en
frecuencia de las neoplasias infantiles, después de las leucemias, los tumores del SNC y
los linfomas.
El 95% de los neuroblastomas se presentan en niños menores de 5 años, teniendo dos
picos de incidencia: < 1 año y 2-4 años. Es más frecuente en niños.
ETIOLOGÍA
• Síndrome alcohólico fetal.
• Tratamiento materno con difenilhidantoína.
• Síndrome de Beckwith-Wiedemann:
o Macroglosia
o Macrocefalia
o Hipoglucemia neonatal
o Onfalocele
o Hemihipertrofia corporal (puede tener una pierna 3 veces más
grande que la otra).
o Tumor de Wilms (se explicará en la próxima comisión).
o Neuroblastoma
• Enfermedad de Hirschsprung
• Neurofibromatosis tipo I
• Formas familiares con herencia autosómica dominante: alteración en el brazo
corto del cromosoma 1.
LOCALIZACIÓN
El neuroblastoma puede originarse a lo largo de toda la cadena simpática, aunque:
• El 70% en abdomen: dentro de este porcentaje, un 50% asientan en glándula
suprarrenal. Es la localización más frecuente en niños mayores (no lactantes).
• El 20% en mediastino posterior, siendo la localización más frecuente en
lactantes.
• En pelvis: 4% en el órgano de Zunkerland (bifurcación aorta abdominal).
Página 1 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
CLÍNICA
Dentro de la clínica se distinguen distintos síntomas según qué los origine:
1. Síntomas relacionados con el tumor primitivo:
• Lactante: masa abdominal o torácica asintomática que se descubre en
un examen rutinario del pediatra o los padres cuando lo bañan.
• Niño: puede presentar un síndrome de malestar maligno con palidez,
anemia, dolor en extremidades y febrícula. DxD con tumor de Wilms: BEG
• En tumores paraespinales: se pueden dar cuadros de compresión
medular por invasión del canal a través de los agujeros de conjunción.
Puede llegar a dar una paraplejia completa si no se diagnostican y tratan
a tiempo.
• En tumores mediastínicos o cervicales: puede provocar Síndrome de
Claude-Bernard-Horner por afectación del ganglio estrellado (causando
ptosis palpebral, miosis y anhidrosis).
2. Síntomas provocados por el síndrome paraneoplásico:
• Síndrome opsocerebelomioclónico: 2-4% de los pacientes con NB.
Provoca irritabilidad continua, movimientos incontrolados de los ojos en
todas direcciones (opsoclonus) y, en ocasiones, ataxia cerebelosa y/o
mioclonías. Sin embargo, suele ser un factor de buen pronóstico.
• Diarrea acuosa intratable: se produce debido a la liberación de VIP por
parte del tumor. Suele desaparecer al resecarlo.
• HTA, rubor facial y sudoración: debido a la eliminación de
catecolaminas o bien mediado por la renina ya que los vasos renales
pueden verse afectados por la infiltración tumoral.
3. Síntomas relacionados con las metástasis: (vía hematógena o linfática).
• Están presentes en el diagnóstico hasta en un 70%.
• Los lugares más frecuentes son: médula ósea, hígado y piel.
- Hígado: su afectación masiva es más frecuente en lactantes
(estadío 4S) y produce gran distensión abdominal.
- Médula ósea: produce dolor óseo en la deambulación en niños
mayores e irritabilidad en lactantes.
Pueden producirse metástasis óseas en los huesos de la región
periorbitaria y retrobulbar causando ptosis y equimosis
periorbitaria (hematoma en anteojos).
- Piel: las metástasis subcutáneas también son propias del estadío
4S y se presentan en forma de nódulos múltiples, duros, no
dolorosos, a veces de color azulado.
Hígado Hueso Piel
Página 2 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
DIAGNÓSTICO
Los criterios diagnósticos son muy estrictos:
Diagnóstico anatomo-patológico del tumor primario mediante biopsia,
independientemente del aumento de las catecolaminas o sus metabolitos en
orina.
Aspirado o biopsia de médula ósea positiva* para células tumorales con
aumento de catecolaminas o sus metabolitos en orina. Se deberán realizar 2
aspirados y 2 biopsias de médula ósea para asegurarnos (es un criterio del
protocolo).
La determinación de catecolaminas en orina sirve tanto para el diagnóstico
como para el posterior seguimiento del paciente y su sensibilidad y
especificidad es cercana al 90-95%.
*A pesar de tener una biopsia del tumor primario siempre se ha de realizar el estudio
de médula ósea ya que es crucial para estadiar el tumor y descartar posibles
metástasis.
ESTUDIO DE EXTENSIÓN
1. Ecografía abdominal: sirve para ver las características y
de qué órgano depende, valorar el resto del abdomen
(metástasis hepáticas, etc.) y ganglios linfáticos.
2. TAC o RMN: (con contraste). Es imprescindible para
definir los límites del tumor, su volumen y relación con
estructuras vecinas de cara a la cirugía. En caso de
tumores paraespinales es de elección la RMN. Se
pueden observar calcificaciones en un 85%.
3. Radiografía de tórax, en caso de metástasis pulmonares
(en este tumor es raro).
4. Gammagrafía con I 123-MIBG: detecta el tumor
primario y las metástasis. Si no existe captación se
realizaría con Tc 99.
ANATOMÍA PATOLÓGICA (NO ENTRA)
El NB forma parte del grupo de tumores de células azules, redondas, pequeñas típicas del niño.
Hay 3 patrones histopatológicos clásicos que reflejan un espectro de maduración y diferenciación:
• Neuroblastoma típico: compuesto por células pequeñas, de tamaño uniforme, con
núcleo denso hipercromático y escaso citoplasma. La presencia de prolongaciones
neuríticas es patognomónica, las pseudorrosetas de Homer- Wright son otro hallazgo
frecuente.
- Indiferenciado
- Moderadamente diferenciado
- Diferenciado
• En el otro extremo, el ganglioneuroma es un tumor completamente diferenciado,
compuesto de células ganglionares maduras,estroma y células de Schwann.
- En maduración
- Maduro
• El ganglioneuroblastoma es un tumor heterogéneo que presenta características de
ambos tumores en diferente proporción.
- Difuso
- Nodular (peor pronóstico).
Página 3 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
FACTORES DE RIESGO
Localización anatómica: Abdomen más agresivo que los localizados en tórax,
cuello o pelvis.
Edad: <18 meses (mejor pronóstico).
Estadio (basado en los hallazgos quirúrgicos).
BIOLOGÍA MOLECULAR:
o La NMA (amplificación del gen N-myc) se da en un 20% en los NM en
fase avanzada. Es independiente de la edad y estadio al diagnóstico. Se
asocia a mal pronóstico por rapida progresión tumoral.
o Las células tumorales producen cantidades variables de ADN: índice de
ADN. Para las células normales, el volumen de ADN es diploide (2n
cromosomas). Los llamados NB hiperdiploides o casi-triploides. (ADN >
1) tienen mejor pronóstico ya que son más sensibles a la QT.
Triploides: buen pronóstico.
Tetraploides: mal pronóstico
o Deleccion del brazo corto del cromosoma 1. Mal pronóstico
o Indice mitosis-karrioresis. Consiste en estimar el número de células en
mitosis-karrioresis en relación con el total de células tumorales. MK alto
> 200 cel MK/5000 cel. tumorales o >4% células MK (mal pronóstico).
ESTADIFICACIÓN (INSS) LO PREGUNTA EN 1 DE CADA 2 EXÁMENES
Los estadíos I al III son post-quirúrgicos (los da la AP de la pieza)
1. ESTADÍO I: tumor localizado con escisión macroscópica completan, con
enfermedad residual microscópica o sin ella. Ganglios linfáticos ipsilaterales
microscópicamente negativos para el tumor.
2. ESTADÍO II: tumor localizado con escisión macroscópica incompleta:
a. IIA: ganglios linfáticos ipsilaterales representativos negativos.
b. IIB: puede tener escisión macroscópica completa pero ganglios
linfáticos positivos.
3. ESTADÍO III: tumor irresecable unilateral, infiltrante más allá de la línea media
(viene determinada por la columna vertebral) o tumor unilateral localizado con
ganglios contralaterales positivos, o tumor en línea media con extensión
bilateral por infiltración o afectación de ganglios.
4. ESTADÍO IV: todo tumor primario con diseminación a ganglios linfáticos
distantes, huesos, médula ósea, hígado, piel u otros órganos con excepción de
lo definido para el estadío 4S. Es el más frecuente.
ESTADÍO 4S: (LA GRAN EXCEPCIÓN)
Estuvimos con esto más de 30 minutos por dudas, siéntete superdotado si lo pillas rápido
Menores de 18 meses (en guías anteriores 12 meses). Lactantes. Es más
frecuente en recién nacidos y lactantes menores de 2 meses.
Tumor primario localizado 1, 2A o 2B
Diseminación limitada a piel, hígado y médula ósea.
Afectación medular <10% de células nucleadas totales identificadas como
malignas (por los métodos antes especificados por el protocolo). Si es mayor
del 10% se consideraría un Estadío IV.
Muy buen pronóstico (como se verá puede remitir espontáneamente).
Página 4 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Resumen de la estadificación de los Neuroblastomas y localización de metástasis.
CLASIFICACIÓN POR RIESGO
European Neuroblastoma-International Society Pediatric Oncology (SIOPEN)
BAJO RIESGO:
o Estadío I, II de cualquier edad sin NMA.
o Estadío 4S sin NMA.
RIESGO INTERMEDIO:
o Estadío III de cualquier edad sin NMA
o Estadío IV < 1 año sin NMA
RIESGO ALTO:
o Estadío IV > 1 año
o Cualquier estadío con NMA.
TRATAMIENTO
En general, los neuroblastomas se tratan mediante quimioterapia, cirugía, radioterapia
e inmunoterapia.
Objetivos de la cirugía:
Establecer el diagnóstico, estadiando el tumor por la AP de la pieza.
Suministrar tejido para estudios biológicos (NMA, etc.).
1. TRATAMIENTO EN GRUPO DE BAJO RIESGO
a. Únicamente cirugía.
b. En caso de compresión medular sintomática la administración de
quimioterapia y dexametasona puede evitar la cirugía descompresiva y
la radioterapia en algunos casos, siendo la laminotomía necesaria sólo
en pacientes con deterioro neurológico muy rápido.
c. Estadio 4S: El tumor tiene capacidad de regresión espontánea. Pero en
algunos casos presentan un comportamiento inicial muy agresivo que
puede conducir al fallecimiento del paciente.
i. Quimioterapia en caso de riesgo de muerte por insuficiencia
hepática o respiratoria hasta conseguir detener a los pacientes
con riesgo de muerte porinsuficiencia hepática o respiratoria
hasta conseguir detener la progresión rápida de la enfermedad y
estabilizar al paciente.
ii. El resto son vigilados.
Página 5 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
2. TRATAMIENTO EN GRUPO DE RIESGO INTERMEDIO
a. Existe una cierta controversia acerca de dar o no quimioterapia previa a
la cirugía.
b. Tendencia actual: biopsia al diagnóstico, quimioterapia de inducción y
cirugía, con posterior quimioterapia de mantenimiento.
i. La QT convierte los neuroblastomas irresecables a resecables en
un 70-90% de los casos y reduce el riesgo de complicaciones
quirúrgicas.
QT QX QT
3. TRATAMIENTO EN GRUPO DE ALTO RIESGO
a. Es el grupo de riesgo mayoritario.
b. Se realiza siempre quimioterapia de inducción (ciclofosfamida,
vincristina, etopósido y platino), seguido de cirugía, radioterapia con
trasplante autólogo de médula ósea y tratamiento de la enfermedad
residual mínima.
c. La tasa de respuesta oscila entre 60-80% pero la mayoría recaen.
QT QX RT Tto Enf. residual
¬ Agentes diferenciadores: inducen la diferenciación del neuroblastoma y
producen apoptosis.
¬ Anticuerpos monoclonales contra gangliósidos que son antígenos de
superficie de membrana presentes en todas las células de NG y el sistema
nervioso.
¬ 131 I-METAYODOBENCILGUANIDINA: se administra a altas dosis para el
tratamiento del neuroblastoma avanzado. Es captada de forma activa por la
membrana celular de los tumores de la cresta neural y sus metástasis. Se
utiliza sólo o en combinación con Topotecán o Cisplatino para el tratamiento
de las recaídas o en tumores refractarios.
Clínica +
FR
MANEJO PACIENTE CON NEUROBLASTOMA
ECO + BX o PAAF Catecolaminas TTO
RMN/TC (1º o m.o.) (orina 24h) (QX±QT)
Estadiaje Pronóstico
(otros TTOs)
Bibliografía: Apuntes de clase. Diapositivas del profesor (sólo pide lo que hay en ellas). Comisión 2013
Por acompañarme a quemar más de un chino y cerves...You Brooks ;)
Página 6 de 6
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionado: Andrea Torregrosa García
Profesor: Óscar Sánchez París
Curso: 6º Medicina CP - 10
Fecha y hora: 23-10-2014; 16:00 – 16:50
Oncología Pediátrica
TUMORES RENALES
TUMOR DE WILMS (NEFROBLASTOMA).
El tumor de Wilms es el tumor renal más frecuente en la infancia (80%) y es el
segundo tumor abdominal maligno con mayor prevalencia.
La edad de presentación oscila entre 1 y 5 años (mostrando una frecuencia máxima
entre los 3-4 años, siendo rara su aparición en mayores de 7 años).
Suele ser unilateral en un 93%, aunque puede presentarse de forma bilateral (7%).
Destacar, que en el caso de que el nefroblastoma sea bilateral y sindrómico la edad de
presentación es menor.
1. Anomalías asociadas. (El profesor recalcó que era importante saberlo).
El tumor de Wilms en el 90% es esporádico sin otras anomalías asociadas. No obstante
es importante conocer con qué patologías está relacionado para poder hacer un buen
diagnóstico del mismo.
- El 5% está asociado a anomalías genitourinarias como: criptorquidia, hipospadias y
alteraciones de la fusión renal como “riñón en herradura”.
Por tanto, ante cualquier paciente que diagnostiquemos algunas de estas patologías será
fundamental realizar una ecografía renal para descartar tumor de Wilms.
- Existe la forma familiar o hereditaria (1-2%), con una edad de inicio anterior y
frecuencia elevada a la bilateralidad.
- Menos del 1% se asocia a síndromes específicos, que a su vez pueden estar
relacionados a hipercrecimiento o no.
o Síndromes con Hipercrecimiento:
Síndrome de Becwith-Wiedemann (SBW): onfalocele, macroglosia,
macrosomía, hipoglucemia neonatal, hemihipertrofia corporal. Con un riesgo
de desarrollar tumor de Wilms del 4-10%.
Hemihipertrofia aislada (Ej: niño que acude a consulta con una masa
abdominal y una pierna más grande que la otra, sospechar nefroblastoma).
Página 1 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Síndrome de Perlam: polihidramnios, sobrecrecimiento fetal, macrocefalia,
macrosomía neonatal, visceromegalia y rasgos faciales dismórficos.
Presentan un mayor riesgo de tumor de Wilms en una edad temprana.
Síndrome de Sotos: patología autosómica dominante que se caracteriza por
un crecimiento de la frente acompañado de retraso en el desarrollo.
o Síndromes no asociados a hipercrecimiento (suele caer en el MIR):
Síndrome de WAGR: Wilms, aniridia (hipoplasia del iris), malformación
genitourinaria y retraso mental.
En este enfermedad lo que ocurre es una delección del cromosoma 11p13.
En él se encuentra TW1 (gen supresor de tumor del tumor de Wilms), es por
ello por lo que tienen riesgo aumentado de nefroblastoma.
Síndrome de Denys-Drash: pseudohermafroditismo masculino y
enfermedad renal (glomerulonefritis o síndrome nefrótico) con tumor de
Wilms. Se debe a mutaciones puntuales en el gen TW1.
Síndrome de Bloom: trastorno raro autosómico recesivo.
2. Screening.
Se debe realizar detención sistemática con ecografía renal seriada cada 3 o 4 meses a
niños con:
- Aniridia.
- Hemihipertrofia.
- Síndrome de Becwith-Wiedemann.
Aunque se ha demostrado que realizar el diagnóstico en estadios más bajos no aumenta
la supervivencia, sí será importante a la hora del tratamiento, sobre todo quirúrgico.
3. Anatomía patológica.
- Macroscópica: lo más importante a este nivel (y que hay que saber según el
profesor) es que el tumor de Wilms presenta una PSEUDOCÁPSULA, la presencia de
ésta es fundamental para realizar un diagnóstico diferencial con otros tumores renales.
Afecta al parénquima renal normal adyacente. Son tumores blandos y fiables con áreas
necróticas y hemorrágicas , y sobre todo con alto riesgo de rotura de la
pseudocápusla intraoperatoria (esto es importante, ya que la simple rotura durante la
operación cambiará el estadio de I a III).
- Microscópica: se basa en observar si tienen presente los tres componentes de
un riñón normal o no: blastema, epitelio y estroma.
Si es trifásico: tiene los tres componentes. Tiene buen pronóstico.
Si es difásico: tiene dos componentes. Si epitelio + estroma: menos agresivo. Si
blastema + estroma : más agresivo pero responde bien a quimioterapia.
Página 2 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Si es monofásico: tiene solo uno de los componentes. El pronóstico dependerá de cual
sea el tejido predominante. Lo importante es saber que si el tejido predominante del
tumor es el epitelial o el estromal el pronóstico es bueno, pero si es de predominio
blastematoso el pronóstico es peor.
Pero lo más importante de todo, es si el tumor presenta ANAPLASIA ya que implica
mal pronóstico pues ofrecen una mayor resistencia a quimioterapia.
La anaplasia se caracteriza por la presencia de tres anomalías:
- Agrandamiento del núcleo hasta 3 o 4 veces.
- Hipercromasia de los núcleos agrandados.
- Figuras mitóticas anormales.
A su vez puede ser focal (presencia de 1 o 2 focos aislados, bien delimitados) o difusa.
Es más frecuente en pacientes mayores de 5 años (13%) y pocas veces se observan en
pacientes menores de 2 años al diagnóstico (2%).
4. Clínica.
- Masa abdominal ASINTOMÁTICA (es el signo más frecuente ya que aparece
en el 75% de los casos). Suele estar situada en un flanco, redondeada, de
consistencia elástica, que NO suele superar la línea media (diagnóstico
diferencial con el neuroblastoma). Cabe destacar, que los pacientes afectos del
tumor de Wilms, en general, son algo mayores que los afectos por
neuroblastoma, por lo que en general los primeros parecen menos enfermos
(recordad que en el neuroblastoma los niños afectados estaban muy malitos
“síndrome de malestar maligno”).
La mayoría no presentan dolor, sólo si tienen un traumatismo, debido al
sangrado.
- Hipertensión arterial en el 60%. Aparece por compresión de la arteria renal por
el tumor y producción de renina.
- Hematuria macro- o microscópica en el 30%.
- Hemorragia intratumoral tras sufrir un traumatismo, y como hemos dicho en
este caso presentarán dolor.
5. Exploración física. (El profesor dijo que lo preguntó hace dos años y sólo
aprobó a 10 personas, ¡ojo!).
- Buen estado general.
- Masa anterior que puede tener contacto lumbar. Es firme, no carácter indurado
ni está fijo.
- Posible HTA.
- Hepatomegalia por obstrucción de la vena hepática derecha.
- Varicocele por extensión del tumor a la vena renal. Recordad que el varicocele
clásico por una dilatación de las venas del cordón espermático en hombres,
Página 3 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
ocurría en niños prepuberales (10-11 años) por lo que si nos viene un niño de 2-
3 años con varicocele ¡debemos sospechar el tumor de Wilms! POSIBLE CASO
CLÍNICO.
6. Diagnóstico diferencial.
- Neuroblastoma.
- Fiebre: descartar ITU (pielonefrosis complicada, pielonefritis pseudotumoral
xantogranulomatosa).
- Enfermedad poliquística renal.
- Nefroma mesoblástico (importante PSEUDOCÁPSULA).
- Linfoma de Burkitt.
- Otros: adenocarcinoma de células claras tipo adulto, sarcoma de células claras y tumor
rabdoide.
7. Evaluación y estadificación preoperatoria.
1) Ecografía abdominal: tumor muy voluminoso, > de 8 cm. Bien delimitado de
estructura heterogénea.
2) Laboratorio: Catecolaminas negativas (diagnóstico diferencial con
neuroblastoma), hipercalcemia (diagnóstico diferencial con tumor rabdoide) y
estudio de coagulación (enfermedad de Von Willebrand adquirido).
3) TAC ABDOMINAL CON CONTRASTE (IMPORTANTE): masa sólida y
heterogénea. Lo realizamos para evaluar la extensión abdominal: extensión a
vena cava (4%), o renal (presencia de trombos, adenopatías retroperitoneales,
metástasis hepáticas y evaluación del riñón contralateral.
4) TAC de tórax: descartar metástasis pulmonares (PULMÓN METÁSTASIS
MÁS FRECUENTE, diferencia con neuroblastoma que da metástasis más
frecuentemente en médula ósea).
Como veis, no se realizará BIOPSIA del tumor por el alto riesgo de rotura de la
pseudocápsula.
8. Estadiaje
En el estadiaje valoraremos: los hallazgos quirúrgicos, hallazgos histopatológicos,
extensión a cápsula, enfermedad residual, afectación vascular y compromiso ganglionar.
Estadiaje postquirúrgico:
o ESTADIO I: tumor limitado al riñón y resecado totalmente. Cápsula intacta y el
tumor no se rompió antes de extirparlo. NO hay tumor residual.
o ESTADIO II: más allá del riñón pero resecado totalmente. Los vasos
extrarrenales pueden contener trombo mural o bien estar infiltrados por el tumor.
Página 4 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
o ESTADIO III: resección incompleta con residuos tumorales macro o
microscópicos; ruptura tumoral pre- o intraoperatoria. Tumor en ganglios
abdominales. Biopsia.
o ESTADIO IV: metástasis hematógenas a pulmón, hígado, hueso o encéfalo.
Metástasis ganglionares extraabdominales.
o ESTADIO V: tumores bilaterales en el momento del diagnóstico.
9. Clasificación histopronóstica (dijo que no hacía falta sabérsela para el
examen, saber la importancia de la anaplasia para el pronóstico).
- BAJO RIESGO: TW de predominio epitelial, TW de predominio estromal, TW mixto,
Tw regresivo, TW con anaplasia focal.
- RIESGO INTERMEDIO: nefrona xenoblástico, TW quístico parcialmente
diferenciado, TW 100% necrótico.
- ALTO RIESGO (histología desfavorable): TW anaplasia difusa, TW de predominio
blastematoso, tumor rabdoide, sarcoma de células claras.
10. Tratamiento.
El tratamiento del tumor de Wilms siempre seguirá el siguiente esquema:
1º Pre-quimioterapia inicial + 2º Nefroureterectomía ampliada + 3º Tratamiento postQx
según grupo de riesgo.
1) Pre-QUIMIOTERAPIA para reducción del tamaño tumoral, pues como hemos
dicho es un tumor muy voluminoso. La pauta es 4 semanas de vincristina y
actinomicina D.
Página 5 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
2) CIRUGÍA:
- Incisión transversa supraumbilical (transperitoneal).
- Exploración locorregional. Apreciar los límites del tumor y las adherencias
peritumorales.
- Ligadura primero de la arterial renal y después de la vena renal.
- Ligadura del uréter a nivel de la vejiga (debemos intentar seccionar lo más
abajo posible el uréter).
- NEFROURETERECTOMÍA AMPLIADA (se denomina ampliada ya que se
extirpa el máximo de grasa perirrenal y las posibles adherencias).
- MUESTREO SELECTIVO DE LOS GANGLIOS SOSPECHOSOS (sobre
todo aquellos de >1 cm), como componente esencial de la estadificación del
tumor.
3) El tratamiento postquirúrgico dependerá del tipo histológico y de la extensión
locorregional. Todo ello se basa en la existencia de protocolos como el SIOP 01.
(esto es lo que dio en clase, pero amplio un poco más por si acaso).
BAJO RIESGO: CIRUGÍA, no necesita QT post-cirugía.
RIESGO INTERMEDIO:
- ESTADIO I: daremos QT durante 4 SEMANAS (Vincristina y
dactinomicina). Igual que el tratamiento Preoperatorio.
- ESTADIO II: daremos lo mismo pero asociando una antraciclina y
prolongando el ciclo a 27 SEMANAS
- ESTADIO III y IV: QT con tres fármacos durante 27 SEMANAS + RT
locorregional.
ALTO RIESGO: QT con los tres fármacos anteriores a la vez durante 9 MESES
- 1 AÑO + fármaco de segunda línea (ifosfamida, etopósido o carboplatino) +
RT a dosis superiores a las que se daba en los tumores de riesgo intermedio.
4) En tumores de Wilms BILATERALES (5% de los niños se presenta con
tumores de Wilms bilaterales y sincrónicos).
El tratamiento de se basa en quimioterapia preoperatoria, seguido de cirugía. En
este caso se realizara una NEFRECTOMÍA PARCIAL ya que si no
provocaríamos una insuficiencia renal.
Además, hay que realizar un seguimiento más prolongado, pues se ha visto en
este tipo recaídas tardías después de más de cuatro del tratamiento en .
5) Factores de riesgo para la recidiva tumoral.
- Derrame tumoral.
- Histología desfavorable.
- Extirpación incompleta del tumor.
- Ausencia de cualquier muestra ganglionar.
La tasa de supervivencia a los 2 años después de la recidiva tumoral fue del 43%
Página 6 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Lo más importante es la RESECCIÓN COMPLETA Y CUIDADOSA DEL
TUMOR.
11. Supervivencia.
La supervivencia por lo general es muy buena, aunque siempre debemos tener en cuenta
que la presencia de anaplasia empeora el pronóstico.
o Tumor de Wilms con histología favorable. Supervivencia a los 5 años.
- Estadio I/II >90%
- Estadio III 80-85%
- Estadio IV 60-80%
- Estadio V (bilateral) 70-80%
o Tumor de Wilms con histología desfavorable. ANAPLASIA. Supervivencia a los
5 años de tratamiento del 60%.
NEFROBLASTOMA QUÍSTICO PARCIALMENTE DIFERIDO.
El nefroblastoma quístico parcialmente diferido es un tumor con renal con excelente
pronóstico. Se presenta en niños < a 1.5 años de edad.
Se caracteriza por la presencia de QUISTES CON SEPTOS en su interior, como
podemos observar en la ecografía renal, que será la forma de diagnóstico.
En cuanto al tratamiento, realizaremos sólo nefrectomía.
NEFROMA MESOBLÁSTICO o TUMOR DE BOLANDE.
Es el tumor renal más frecuente de la edad neonatal, < 6 meses de vida, alcanzando un
pico en los primeros 3 meses. (Así un niño menor de 6 meses no va a tener un tumor de
Wilms, sospechar este tipo). Predomina en varones.
Como todos los tumores que hemos visto en la clase, aparece típicamente como una
masa abdominal palpable con un comportamiento usualmente benigno, que raramente
produce metástasis.
Por último, el tratamiento de elección también será la nefrectomía.
BIBLIOGRAFÍA: -Apuntes del profesor.
-Diapositivas del profesor de este año (están muy bien).
- Apuntes de clase.
- Algunas páginas de internet para contrastar.
Página 7 de 7
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionada: Paloma Ruiz Torregrosa
Profesor: Francisco Ivorra CP 11
28-10-14; 14:00 – 14:50
ATRESIA DE LA VIA BILIAR (AVB)
1. ANATOMÍA ÁRBOL BILIAR:
2. DEFINICIÓN:
Es una patología congénita, que cursa como una colangiopatía obstructiva neonatal
(a diferencia de los quistes de colédoco), consecuencia de un proceso inflamatorio
destructivo idiopático que puede afectar tanto a los conductos biliares
intrahepáticos como extrahepáticos, que acaba provocando fibrosis, y obstrucción
de la vía. Su principal manifestación es la ictericia.
3. EPIDEMIOLOGÍA
- Afecta a 1 de cada 10.000 -15.000 nacidos vivos
- Predomina en el sexo femenino 4:1.
- Niños asiáticos.
- No es hereditario (aunque se ha descrito en gemelares con idéntico HLA; pero no
hay patrón genético).
- Es la causa principal de enfermedad hepática crónica en niños.
- Es la causa más frecuente de trasplante de hígado en niños.
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
4. FENOTIPOS CLÍNICOS:
Aislada. Es la más frecuente, supone 70-80 % de los casos. La ictericia y la acolia
aparecen durante las primeras 2 semanas de vida, sin otras anomalías asociadas.
Asociada a otras alteraciones extrahepáticas: poliesplenia, anomalías de la vena
porta, malrotación, situs inversus y cardiopatía congénita. Representa el 15-30 % de
los casos.
5. ETIOPATOGENIA:
La etipoatogenia es desconocida pero se relaciona con:
- Viriasis prenatal
- Factores genéticos
- Factores inmunológicos
- Enfermedad inflamatoria progresiva
6. CLASIFICACIÓN:
El tipo de atresia se clasifica según el lugar donde se encuentra la obstrucción:
Atresia tipo I: Obliteración del colédoco, con libre tránsito por los
conductos proximales.
Atresia tipo II: Obstrucción del conducto hepático, pero a nivel del hilio hepático hay
dilatación quística de los conductos.
IIa: Libre tránsito por los conductos
cístico y colédoco.
IIb: Obliteración de ambas estructuras.
Página 2 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Atresia tipo III (90%): No se identifican conductos hepáticos o hilio dilatado o con libre
tránsito.
La diferencia entre el tipo IIb y el III es que en el tipo IIb hay una dilatación muy
importante de los conductos hepáticos, y en el III apenas están dilatados.
7. MANIFESTACIONES CLÍNICAS:
Hepatomegalia (signo más precoz, pero es inespecífico).
Ictericia: a partir de las 2 semanas de vida y perdura más de 15 o 20 días. (OJO
al nacer es NORMAL que un niño esté ictérico pero si a las 2 semanas perdura
SOSPECHAR esta patología) Es la principal manifestación!!!
Hipocolia o acolia.
Coluria.
Otros síntomas o signos de insuficiencia hepática (edema, circulación colateral
y otros síntomas y signos de hipertensión portal…)
8. DIAGNÓSTICO DIFERENCIAL
Habrá que realizarlo con cualquier causa de ictericia en el periodo neonatal (hemolisis
por incompatiblididad Rh….)
Entre las causas quirúrgicas tenemos:
- Atresia de vías biliares
- Hipoplasia de vías biliares o Síndrome de Alagille (conductos biliares malformados y
estrechos): por lo general las heces no son acólicas sino hipo cólicas o la acolia es
intermitente.
Página 3 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
- Quiste del colédoco: no es muy frecuente la acolia aunque puede verse, en el 60%
de los pacientes existe la clásica triada de ictericia, dolor abdominal y tumor
palpable.
- Perforación espontánea de las vías biliares.
- Tapón de bilis impactado.
- Síndrome de bilis espesa.
- Estenosis de los conductos biliares.
- Alteraciones analíticas
9. DIAGNÓSTICO:
9.1 Alteraciones analíticas:
- Hiperbilirrubinemia a expensas de la bilirrubina directa (hígado funciona
correctamente pero no puede expulsar la bilis)
- Aumento de las transaminasas.
- Elevación de la gammaglutamiltranspeptidasa (GGT).
- Elevación fosfatasa alcalina.
9.2 Pruebas de imagen:
- Ecografía hepatobiliar:
Es la primera prueba que se realiza ya que es barata, rápida, inocua y de gran
utilidad ya que permite diferenciar la atresia de vías biliares de otras causas de
colestasis como quiste de colédoco, litiasis, etc. Puede dar el diagnóstico, pero
al ser una intervención tan complicada requiere el apoyo de la RMN.
Signos ecográficos:
La ausencia o hipoplasia de la vesícula biliar y la falta de contractilidad de
ésta.
El signo de la cuerda (cordón fibroso a nivel de porta hepatis).
Ecografía Doppler: permite evaluar signos de hipertensión portal,
malformaciones vasculares.
Cintigrafía Hepática (Se usa pero cada vez menos)
Gammagrafía hepatobiliar con derivados del IDA (HIDA Scan): hay captación
Página 4 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
hepática del fármaco sin excreción biliar, la presencia de isótopos en el tracto
gastrointestinal excluye el diagnostico de AVB.
RNM y conlangioRMN: es una RMN que mediante un software específico que
reconoce la densidad de la bilis, reconstruye el árbol biliar de forma
tridimensional. * Con la Ecografía y la colangioRMN es suficiente para el
diagnóstico.
9.3 Biopsia hepática: Permite el diagnóstico definitivo en un 97-98% de los casos; se
observa:
- Proliferación de los conductos biliares.
- Fibrosis portal.
- Estasis biliar en los canalículos biliar.
- Transformación gigantocelular.
*Cada vez se utiliza menos, por el avance de las
pruebas diagnósticas no invasivas.
10. TRATAMIENTO QUIRÚRGICO:
Su objetivo es restablecer el flujo biliar y evitar el desarrollo de cirrosis biliar y fallo
hepático secundario.
Se emplea la portoenteroanastomosis en Y de Roux (se sube un asa de intestino
delgado y se anastomosa por encima de la obstrucción) descrita por Kasai en 1959.
Los mejores resultados se obtienen antes de los 2 meses de vida.
Antes y después del tratamiento quirúrgico, estos pacientes requieren un manejo
médico multidisciplinario (fluidoterapia, antibioterapia, etc).
En los casos en que fracasa (la principal causa de fracaso es la estenosis) la
hepatoportoenterostomía (es una cirugía muy compleja y con una tasa de fracaso de
hasta un 60%), el trasplante hepático es el tratamiento de elección (de progenitor en la
mayoría de los casos).
Página 5 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
11. COMPLICACIONES:
La principal complicación asociada a la corrección quirúrgica son los cuadros de
colangitis que pueden empeorar la disfunción hepática basal. Prevención con
Antibióticoterapia: Cefalosporinas o quinolona. Otra complicación, aunque menos
frecuente, es el desarrollo de carcinoma hepatocelular (pero es muy poco frecuente).
12. CONCLUSIONES:
La AVB es la causa más frecuente de ictericia neonatal obstructiva extrahepática y
la causa más frecuente de trasplante hepático pediátrico de forma aislada.
En todo niño con ictericia que sobrepase los 14 días de vida debe investigarse la
presencia de bilirrubina directa en sangre y pensar en primer lugar en la atresia de
vías biliares.
QUISTES DE COLÉDOCO
1. DEFINICIÓN:
Son lesiones quísticas únicas o múltiples que pueden afectar tanto a la vía biliar
intrínseca (VBI) como a la vía biliar extrínseca (VBE).
2. EPIDEMIOLOGÍA:
- Se da en 1/100.000-150.000 nacidos.
- Es más frecuente en mujeres (4:1)
- 1/3 de ellos se diagnostica en la edad adulta.
- Tiene un potencial de malignización (a diferencia de la atresia), que aumenta
conforme pasa el tiempo: siendo del 0,7% en menores de 10 años y del 14,3% en
mayores de 20 años.
3. FISIOPATOLOGÍA:
Se ha observado que existe una anomalía de la unión pancreático-biliar con unión
anormalmente alta del colédoco con el Wirsung y con un canal común mayor de 2 cm.
En las series pediátricas esto se ha observado en un 95-100% de los casos, mientras
que en las series en adultos en un 55-95% de los casos.
Página 6 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Hay una serie de teorías a las que el profesor no dio importancia:
- Teoría de Yotsuyanagi (1936): Vacuolización desigual del árbol biliar en periodo
embrionario precoz.
- Teoría de Babbit (1973): Cambios degenerativos inflamatorios por exposición
persistente al jugo pancreático. Es la teoría que más importancia tiene.
- Teoría de Kusonoki (1988): Inervación autonómica inadecuada del árbol biliar
distal.
El mecanismo fisiopatológico que se comentó en clase es el siguiente: tanto el
conducto común colédoco-Wirsung mayor de 2 cm como la disfunción del esfínter de
Oddi va a favorecer un reflujo de líquido pancreático, que producirá reacción
inflamatoria y erosión de la mucosa de la vía biliar y finalmente dilatación.
3. ANATOMÍA PATOLÓGICA:
- Macroscópicamente se observa la pared muy engrosada.
- Microscópicamente se observa tejido conectivo denso con escasas fibras
musculares, hiperplasia o metaplasia epitelial y eventualmente carcinoma.
4. CLÍNICA:
En niños (triada clásica): Bilirrubina elevada, ictericia, prurito, masa abdominal,
dolor abdominal, retraso en el desarrollo.
En adultos (mas inespecífica y variada): dolor epigástrico/hipocondrio derecho
crónico intermitente, colangitis recurrente, masa abdominal.
5. COMPLICACIONES:
Litiasis secundaria: primera manifestación en el 80% de los casos.
Ictericia obstructiva fluctuante.
Colangitis: por sobrecrecimiento bacteriano por éstasis biliar agravado por
litiasis intracanalicular; es más común en adultos.
Pancreatitis de repetición: en un 30% de los casos.
Cirrosis biliar: se ha observado en un 10% de las series pediátricas y en un 15%
de las series en adultos.
Riesgo de Carcinoma: se ha demostrado clínicamente y experimentalmente que
es 20 veces superior al de la población normal en adultos.
Página 7 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
6. DIAGNOSTICO:
Sospecha diagnóstica: Dilatación vías biliares a cualquier nivel con ausencia de
obstrucción biliar.
Pruebas complementarias a realizar:
o Ecografía: es el primer examen que se realiza, muy útil para seleccionar
pacientes.
o ERCP (colangio-pancreatografía retrograda endoscópica): se usa más en
adultos.
o Colangio-RMN: la que más se utiliza tras la ecografía en niños. Tiene una
excelente correlación con ERCP.
o TAC: útil sobretodo en intrahepáticos, que actualmente se ven con la
colangio-RMN, por lo que se usa poco.
7. CLASIFICACIÓN DE TODANI: (posible pregunta de EXAMEN)
Tipo I (50-85%): la más frecuente. La porción
más distal del colédoco suele ser normal.
o Ia: dilatación saciforme y afecta a todo o casi
todo el hepatocolédoco.
o Ib: dilatación saciforme y afecta a una parte del hepatocolédoco
o Ic: dilatación fusiforme de toda la VBE.
Tipo II: divertículo de colédoco (el más infrecuente).
Tipo III: dilatación de la porción terminal intraduodenal de la vía biliar. También
llamado coledococele. Es el único que podemos tratar de manera expectante.
Página 8 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Tipo IV:
o IVa: dilatación multiple de VBI/VBE. Es el
segundo en frecuencia.
o IVb: dilatación múltiple de la VBE.
Tipo V: dilatación única o múltiple de la VBI.
También llamada Enfermedad de Caroli.
8. TRATAMIENTO
En general, para los quistes extrahepáticos se utilizará resección y reconstrucción de la
vía biliar utilizando derivaciones biliodigestivas. No se realizan anastomosis
quistoentéricas, aunque técnicamente sería el camino sencillo, ya que hay riesgo de
malignización. En cuanto a los quistes intrahepáticos, se debe valorar la hepatopatía vs
transplante, en función de la extensión de la afectación.
Tratamiento quirúrgico según tipo:
Tipo I y II Resección de vesícula y formación
quística + derivación biliar
hepáticoyeyunal
Tipo III (coledococele) - Si asintomático: no se realiza
resección profiláctica (bajo índice de
malignización)
- Si clínica: resección transduodenal
+ colédoco-duodeno anastomosis.
Tipo IV Resección vía biliar + anastomosis
proximal bilioyeyunal (puede ser
intrahepática).
Tipo V Resección hepática
Página 9 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
9. ENFERMEDAD DE CAROLI: (posible pregunta de EXAMEN)
9.1. Concepto:
Es una dilatación quística única o múltiple de la VBI, que se corresponde al tipo V de la
clasificación de Todani. Se piensa que se produce por una malformación embrionaria
de la placa ductal. Su localización puede ser uni o bilobar. Es raro que aparezca después
de los 50 años, pero puede aparecer a cualquier edad. Su posibilidad de malignización
es del 7%.
9.2. Clasificación:
Tipo 1: Es la Enfermedad de Caroli y se presenta de manera aislada.
Tipo 2: Es el Síndrome de Caroli y se presenta asociada a fibrosis hepática,
quistes renales y de colédoco entre otros. Presenta un patrón de herencia AR.
9.3. Clínica:
Cursa con dolor abdominal recurrente, prurito, colangitis de repetición, hipertensión
portal en el tipo 2.
9.4. Diagnóstico:
- Eco
- Colangio-RMN: De elección
- TAC
- RMN
- CPRE
9.5. Tratamiento:
- Tratamiento médico en los episodios colangíticos
- Tratamiento definitivo: -Hepatectomía (si afectación parcial)
-Transplante hepático (si afectación de ambos lobulos).
Bibliografía:
- Documento Word Dr. Ivorra.
- Apuntes contrastados (Gracias Elisa, Alba y Ana ).
- Comisiones años anteriores.
Página 10 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionado: Pablo Salces Ortiz
Profesor: Dr. F Ivorra CP-12
28/10/2014; 15:00-15:50
DEFECTOS CONGÉNITOS DE LA PARED
ABDOMINAL
ÍNDICE:
1. Formas de presentación.
2. Onfalocele
3. Gastrosquisis.
4. Epidemiología.
5. Etiología.
6. Malformaciones asociadas.
7. Diferencias entre Onfalocele y Gastrosquisis.
8. Diagnóstico.
9. Clasificación Onfalocele.
10. Clasificación Gastrosquisis.
11. Tratamiento quirúrgico.
12. Hernia umbilical.
13. Hernia inguinal.
Pongo en letra más pequeña aclaraciones dichas en clase, que no están en los esquemas del profesor
1. Formas de presentación.
Las formas de presentación de los defectos congénitos de la pared abdominal
son muy variadas, asociadas a múltiples patologías. Pueden presentarse aisladamente o
bien formar parte de un síndrome complejo. Pueden afectar a uno o más componentes
de la pared, como la piel, músculo, aponeurosis…
Las entidades más importantes por su frecuencia y repercusiones son: (en ellas se
va a centrar la clase y son las más importantes.) Onfalocele, Gastrosquisis, Hernia umbilical
y Hernia inguinal (estas dos últimas son las más frecuentes).
Aunque también existen Otras entidades menos frecuentes tales como:
1. Ombligo cutáneo: Es un defecto de cicatrización de la piel a nivel del ombligo, sin la
presencia de orificio herniario. Es un defecto únicamente estético, sin trascendencia
clínica.
2. Diastasis de la musculatura de los rectos anteriores: Consiste en una separación
anormal de ambos bordes mediales de los músculos rectos. No produce molestias y no
precisa tratamiento, puesto que irá regresando con el crecimiento. También es muy frecuente
en adultos, por ejemplo en las mujeres durante el embarazo, suele mejorar.
Página 1 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
29/10/14 [CIRUGÍA PEDIÁTRICA]
3. Hernia epigástrica: Defecto de cierre de la fascia a nivel de la línea alba, por encima
del orificio umbilical. No curan espontáneamente, por lo que la corrección quirúrgica es
necesaria a partir de los 2 ó 3 años de vida.
4. Onfalitis: Consiste en una infección recurrente del fondo del ombligo. Hay que dar
tratamiento antibiótico.
5. Granuloma umbilical: Granuloma azulado que aparece en el fondo del ombligo. Sin
transcendencia clínica.
6. El Síndrome de Prune-Belly: Es conocido como el Síndrome del abdomen en
“ciruela-pasa”, que se caracteriza por:
Ausencia, deficiencia o hipoplasia congénita de la musculatura de la pared
abdominal. El contenido abdominal se mantiene solo con la piel.
Anomalías en el tracto urinario como vejiga hipotónica (megavejiga), uréteres y
uretra prostática dilatados.
Criptorquidia bilateral.
Se trata de un síndrome complejo con manifestaciones clínicas diversas según el
grado de afectación de los elementos afectados.
El tratamiento debe ser individualizado en cada paciente. Lo importante en este
síndrome es que asocia alteraciones más graves que la pared abdominal. Por tanto, lo primero es tratar
anomalías cardíacas o renales si las hay. A continuación la pared abdominal, si es posible se intenta diferir
la cirugía pues consiste en poner una malla que con el crecimiento y desarrollo del niño puede requerir
reintervenciones.
2. Onfalocele
Consiste en una herniación de cualquiera de las vísceras abdominales a través de
un defecto umbilical. El contenido está cubierto por una membrana, que en su parte
interna está recubierta de peritoneo y la parte externa de membranas amnióticas con una
delgada capa entre ellas de gelatina de Wharton.
3. Gastrosquisis.
En este caso el defecto de la pared es pequeño y solo se hernia el intestino
delgado,y se produce a través de los músculos rectos abdominales, lateral y a la derecha
del ombligo. No existe membrana que recubra el defecto de la pared abdominal (sin
saco). (Diferencia con el onfalocele)
En ambas existe una salida del contenido abdominal hacia fuera, pero es
importante conocer las diferencias entre ambas.
Página 2 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 29/10/14
4. Epidemiología
En el onfalocele: Aparece en 1/7000 nacidos vivos. La mortalidad asociada está
entre el 30% y 70% (debido a las múltiples malformaciones asociadas).
En la gastrosquisis: Aparece en 1/5000 nacidos vivos. La mortalidad es del 20%,
el pronóstico es mejor, ya que no suele asociar ningún otro problema. Si solo tuviéramos en
cuenta el orificio y el contenido que protruye es más grave la gastrosquisis, pero no hay que olvidar que
en Onfalocele se producen más malformaciones asociadas, y afectan al pronóstico.
5. Etiología
El onfalocele se produce por un defecto en el cierre de los pliegues laterales del
abdomen y un defecto en el retorno del intestino medio a la cavidad abdominal que
normalmente se presenta hacia la décima semana de vida intrauterina.
La gastrosquisis se produce por una ruptura tardía de la membrana amniótica, lo
que hace que no se encuentre recubrimiento sobre el contenido herniado. En la
gastrosquisis, al nacimiento, aparece compromiso inflamatorio del intestino que se
encuentra por fuera de la cavidad abdominal. Lo que marca el pronóstico es el grado de
compromiso inflamatorio intestinal y de necrosis.
6. Malformaciones asociadas.
El onfalocele se asocia a:
Sdr. de Beckwith-Wiedemann.
Cardiopatías congénitas. (la más importante y que más determina el pronóstico).
Trisomía 13, 18 y 21.
Defectos de la línea media superior con hernia diafragmática y
cardiopatía.
Pentalogía de Cantrell.
Defectos espinales, malformación anorectal con extrofia vesical
(complejo de O.E.I.S)
Todas estas malformaciones asociadas es lo que determina la mortalidad y
morbilidad de estos pacientes.
La gastrosquisis se asocia a malrotación intestinal, atresia intestinal y
criptorquidia. Estas malformaciones no se asocian a mal pronóstico, por lo que en esta
patología la mortalidad es menor.
Página 3 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
29/10/14 [CIRUGÍA PEDIÁTRICA]
7. Diferencias entre Onfalocele y Gastrosquisis. (importante)
ONFALOCELE GASTROSQUISIS
Localización del defecto Anillo umbilical Lateral al cordón
Tamaño del defecto 4-10 cm. < 4cm.
Localización del cordón Sobre el saco Sobre la piel
Posición del hígado Puede estar herniado In situ
Apariencia del intestino Normal (porque el anillo es Edematoso o necrosado
grande y por la presencia de
la membrana)
Cavidad abdominal Pequeña Casi normal
Malrotación intestinal Presente Presente
Atresia intestinal Raro Común
Isquemia del mesenterio Raro (porque no hay Común
compromiso de los vasos)
Anomalías asociadas 40-80 % Raro
Peritonitis asociada Raro 18%
Malabsorción Ausente Frecuente
Prematuridad 10-20% (baja) 50-60% (alta)
Edad materna >20 años <20 años
Pronóstico de sobrevida Con cardiopatía: 20% 70-90%
Sin cardiopatía: 70%
Podemos relacionar varios datos, el mayor tamaño del defecto en el onfalocele, hace que se pueda herniar
mayor contenido abdominal, el hígado puede estar herniado o no. Un menor tamaño en la gastrosquisis,
facilita que se pueda estrangular y así encontramos una apariencia del intestino edematoso o incluso
gangrenado, isquemia del mesenterio es común, peritonitis asociada más frecuente, malabsorción por
afectación del intestino delgado. El profesor ha comentado que este cuadro a salido otros años y que por
eso este año no toca (cada uno que decida si se lo estudia)
8. Diagnóstico.
Es importante realizar un diagnóstico prenatal; en casos de gastrosquisis o de
onfalocele gigante se recomienda realizar una cesárea programada, dejando que el feto
llegue a término, para evitar el traumatismo del parto vaginal.
Si falla el diagnóstico prenatal, entonces el diagnóstico se realizará tras el
nacimiento del niño, mediante la simple exploración del recién nacido.
También es importante en estos casos, la cirugía intraútero, aunque en alicante todavía no se hace, sí que
hay algunos centros en España en los que se está empezando a hacer. (Comisión 2012).
Página 4 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 29/10/14
9. Clasificación del onfalocele.
Hace referencia al tamaño del anillo:
1. Pequeño: El diámetro del defecto es menor de 4cm.
2. Mediano: El diámetro del defecto es de 4 a 7 cm.
3. Gigante: El defecto es mayor de 7 cm o igual al diámetro biparietal.
Existe otra clasificación que tiene en cuenta la integridad o no del saco.
10. Clasificación de la gastrosquisis.
Hace referencia al grado de peritonitis, al estado del intestino que protruye:
1. Tipo I: Peritonitis leve con intestino normal.
2. Tipo II: Peritonitis severa. Exudado.
3. Tipo III: Compromiso intestinal con atresia, necrosis o perforación.
4. Tipo IV: Necrosis intestinal severa.
11. Tratamiento quirúrgico.
Por supuesto el tratamiento fundamental en ambas patologías es el tratamiento
quirúrgico, y el objetivo fundamental es en la medida de lo posible realizar un cierre
primario. (Conseguir cerrar el defecto y devolver las asas al interior)
Debemos de tener siempre en cuenta que el tratamiento debe ser individualizado
en cada caso.
A veces no es posible reintroducir todas las vísceras en un solo tiempo, por el
aumento de la presión abdominal, lo que produciría un Sdr. compartimental abdominal.
La presión intra-abdominal siempre hay que medirla y ésto se puede hacer mediante la
colocación de una sonda en la vejiga, y nunca deberá ser mayor de 12cm H2O; en el caso
de que sobrepase los 12cm H2O no se pueden reintroducir las asas. Lo que se haría sería colocar las
vísceras en una bolsa estéril que se sutura a la pared abdominal e ir reintroduciendo las vísceras poco a
poco, para evitar aumentos de la presión intra-abdominal bruscos.
Respecto al tratamiento preoperatorio, siempre es importante intentar llevar al
paciente a quirófano en las mejores condiciones posibles, sirve para cualquier patología que requiera
tratamiento quirúrgico.l
Mantener la oxigenación, evitar la colocación de CPAP nasal (aunque a veces es
inevitable), para así evitar el aumento de presión abdominal, pues no introduce aire de forma
selectiva y puede pasar al ap. digestivo.
Administración generosa de líquidos endovenosos.
Prevención de la hipotermia.
Se introduce el contenido del defecto en una bolsa estéril.
Sonda gástrica para descomprimir el intestino y el estómago.
Administrar antibióticos
Administrar bloqueadores de H2 (para evitar la hipersecreción ácida).
Página 5 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
29/10/14 [CIRUGÍA PEDIÁTRICA]
Respecto al tratamiento quirúrgico, para cerrar el orificio, debemos tener
precaución con el uso de mallas sintéticas puesto que éstas se adhieren al intestino y
promueven la aparición de fístulas. Y en casos de intestino no viable se realizará la
resección intestinal oportuna; hacer anastomosis y reintroducir el intestino sano en la
cavidad abdominal.
Esquema sobre el manejo quirúrgico.
El tamaño menor del defecto en la gastrosquisis permite normalmente hacer un cierre primario, que
seguirá su manejo según haya hipertensión abdominal o no. La escleroterapia del saco permite diferir la
intervención, hasta un cierre definitivo posterior.
12. Hernia umbilical.
Es una protuberancia (abultamiento hacia fuera) del revestimiento abdominal, o
de una porción de los órganos abdominales a través del área alrededor del ombligo.
1. Epidemiología
Aparece en 1 de cada 6 nacidos vivos (muy frecuente). Es más frecuente en el
sexo femenino y en prematuros. Es 9 veces más común entre los individuos de raza
negra, probablemente debido a una ausencia o debilidad de la fascia umbilical. El 75%
de los lactantes por debajo de 1500 gramos tiene una hernia umbilical a los 3 meses de
vida. A veces acompaña a procesos como el ddr. de Down, hipotiroidismo, síndromes
metabólicos como la mucopolisacaridosis o el sdr. exonfalomacroglosia.
Página 6 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
[CIRUGÍA PEDIÁTRICA] 29/10/14
2. Etiopatogenia.
Durante la vida intrauterina, la pared abdominal está abierta por el ombligo para
permitir el desarrollo del intestino; aproximadamente, en la décima semana de
gestación, éste regresa a la cavidad abdominal y se cierra progresivamente el orificio.
Cuando falla este mecanismo y persiste el orificio aparece la hernia umbilical.
3. Presentación.
Por lo general, las hernias umbilicales son asintomáticas. La valoración de la
hernia umbilical no se debe hacer por el volumen que protruye sino por el diámetro del
orificio herniario. (Importante)
La gran mayoría de las hernias umbilicales no están relacionadas con ninguna
afección patológica; sin embargo, pueden estar asociadas a enfermedades raras como la
enfermedad de almacenamiento de mucopolisacáridos, el sdr de Beckwith-Wiedemann,
el Sdr. de Down y otros.
4. Tratamiento
Las hernias pequeñas (menos de 1cm) usualmente se cierran espontáneamente a
los 3-4 años de edad sin tratamiento alguno.
La utilización de fajas, esparadrapos, monedas y, en general, mecanismos
externos de compresión están totalmente contraindicados.
A pesar de esto en un pequeño porcentaje de casos (<1%) sí que existe
indicación quirúrgica y, es cuando hay complicaciones, tales como:
Incarceración: (el 5.1% de niños con hernia umbilical se incarceran)
Estrangulación
Se deben sospechar estas complicaciones ante dolores abdominales en un bebé
con una hernia umbilical o si aparece sensibilidad en la zona herniaria, se inflama o se
decolora, y particularmente, si se desarrollan signos de peritonitis o de shock.
También se considera indicación quirúrgica aquellos casos en los que persistan
hernias umbilicales pasados los 3 años si son de gran tamaño, y a los 5 años si son de
menos de 1cm de diámetro (aunque el profesor dijo que su experiencia personal le dice que aún así
éstas también acaban cerrando por sí solas.)
13. Hernia inguinal.
La hernia inguinal infantil corresponde a la persistencia del conducto peritoneo-
vaginal en el niño o del conducto de Nück en la niña.
En los niños las hernias van a ser casi siempre indirectas. El profesor indicó que las
hernias indirectas son aquellas externas a los vasos epigástricos, mientras que las hernias directas son
Página 7 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
29/10/14 [CIRUGÍA PEDIÁTRICA]
internas a los vasos epigástricos.
1. Manifestaciones clínicas
El síntoma más evidente es la aparición de un bulto en la zona de la ingle. Puede
aumentar de tamaño en distintos momentos y desaparecer en otros. Puede ser
muy voluminoso, incluso llegar al escroto.
Es raro que sea causa de molestias para el niño y que este se queje por ese motivo.
2. Tratamiento
Es siempre quirúrgico (porque a diferencia de la hernia umbilical no desaparece),
pero se suele diferir (fundamentalmente por comodidad en cuanto a la anestesia). El tratamiento
consiste en la sección y ligadura del saco herniario en el orificio inguinal profundo tras
un acceso inguinal directo a través de una incisión corta en el pliegue abdominal
inferior. En los adultos se puede realizar herniorrafias (el cierre del defecto suele generar mucha
tensión) o hernioplastias (se coloca generalmente una malla para disminuir la tensión). En los niños no
hacen falta ninguna de estas técnicas.
3. Complicaciones
Son raras:
- Estrangulación: El intestino no puede volver al abdomen, se inflama y provoca
vómitos y otros síntomas de obstrucción intestinal. Para que esto ocurra, deben pasar
varias horas, el profesor comentó que cuando llega una hernia incarcerada si han pasado más de
seis horas se mete directamente a quirófano, pero si es más reciente se puede intentar reducir.
- Si la hernia inguinal sucede en una niña, a veces, arrastra consigo uno de los
ovarios, que puede percibirse como una almendra en el interior del conducto
inguinal.
En ambos casos debe operarse de urgencia.
BIBLIOGRAFÍA:
- Esquemas del profesor.
- Comisión 2013.
- Apuntes de clase.
Página 8 de 8
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionado: Helena Sánchez Hortal
Profesor: Francisco Miguel Ivorra Muñoz
Curso: 6º Medicina CP-13
Fecha y hora: 03-11-14; 15:00 – 15:50
APENDICITIS AGUDA, LINFADENITIS MESENTÉRICA Y
DIVERTÍCULO DE MECKEL
1. APENDICITIS AGUDA
1.1. RESEÑA HISTÓRICA
En 1521 el italiano Caprio describió el apéndice como órgano por primera vez.
En 1773, a finales del S. XVIII, Amyand realiza la primera apendicectomía en
ausencia de anestesia, asepsia y antisepsia (puesto que todavía no existía).
En 1889, finales del S. XIX, John B. Murphy dijo: “tenemos el convencimiento que
dentro de pocos años todos los casos diagnósticados como peritiflitis
(Inflamación del peritoneo que rodea el ciego, término que actualmente no se
usa, en ocasiones se emplea en pacientes oncológicos) se operarán
inmediatamente, ligando el apéndice y extirpándolo si fuera posible”
Alex Simpson Smith, Cirujano, The hospital for Sick Children, Great Ormond
Street, London (1935): “El apéndice, un órgano vestigial de la anatomía, al
acecho en un pequeño rincón del abdomen, pone en peligro la vida de un niño,
más que cualquier otra emergencia quirúrgica”.
1.2. EPIDEMIOLOGÍA
Es la urgencia quirúrgica abdominal más frecuente.
Constituye el 60% de los cuadros de abdomen agudo quirúrgico en adultos, en
niños este porcentaje es todavía más elevado.
El 5-15% de la población padece este cuadro en algún momento de su vida.
No hay diferencias respecto al sexo.
Tiene en la actualidad todavía una mortalidad de 0.1% (de cada mil apendicitis,
una fallece) con una morbilidad del 10-40% (abcesos, sepsis, infecciones de
herida). Como vemos en la gráfica, la mortalidad ha disminuido mucho desde
principios de siglo hasta la actualidad, pero aun así sigue existiendo.
1/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
1.3. ETIOPATOGENIA
El mecanismo patogénico más aceptado es la obstrucción de la luz apendicular (lo que
condiciona un sobrecrecimiento bacteriano en el apéndice).
La causa más frecuente es la hiperplasia de los folículos linfoides submucosos (en
niños) y obstrucción por concreciones fecales: fecalitos (en adultos).
Existen otras causas raras: parásitos, cuerpos extraños, tumores (el tumor carcinoide
es el más frecuente), bridas, ingesta habitual de pipas, etc.
Además se ha postulado otro mecanismo patogénico: la ulceración en la mucosa
apendicular.
1.4. ESTADÍOS EVOLUTIVOS ANATOMOPATOLÓGICOS
Una vez instaurada, la apendicitis sigue un curso evolutivo progresivo, no se detiene.
Es importante el estadiaje anatomopatológico, puesto que dependiendo de él,
llevaremos a cabo distintos tipos de tratamiento. Los clasificamos en:
1. APENDICITIS CATARRAL: aspecto macroscópico normal con infiltrado
inflamatorio en submucosa. Al intervenir parece un apéndice normal, pero
siempre que se opera con sospecha de apendicitis se extirpa el apéndice, ya que
es menos iatrogénico hacer una apendicectomía blanca, que dejar un apéndice en
fase catarral que luego pasará a fase flemonosa, siendo más complicado.
2. APENDICITIS FLEMONOSA: se aprecia proliferación bacteriana en todas las
capas, con alteración microscópica en todo el espesor de la pared apendicular. El
apéndice tiene mayor tamaño pero no hay signos de pus, de necrosis ni de
perforación.
3. APENDICITIS PURULENTA: se observan microabscesos en el espesor de la pared,
con apéndice distendido, rígido y exudado purulento periapendicular, pero sin
perforación.
4. APENDICITIS GANGRENOSA: aparecen zonas de necrosis que provocan
perforación (por el compromiso vascular, la distensión de la apéndice hace que el
flujo sanguíneo no llegue bien a la pared). Es el episodio previo a la perforación y
la peritonitis.
A su vez, los estadíos evolutivos de la apendicitis aguda gangrenosa son:
Peritonitis local o circunscrita: la más frecuente, dando lugar a un plastrón
o abceso (dependiendo de si el proceso está limitado por una pared de nueva
formación). El resto del abdomen no tiene pus.
Peritonitis aguda o difusa: aparece en personas con defensas disminuidas:
ancianos, inmunodeprimidos, en niños y en casos de evolución ultrarápida.
En niños ( más frecuente cuanto más pequeño es el niño). El epiplón
está poco desarrollado y no envuelve bien al apéndice, siendo éste más
vulnerable de producir peritonitis difusa al romperse (el epliplon
2/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
presenta habilidad para atenuar la diseminación de la sepsis en la
peritonitis). Pueden llegar a drenarse incluso 2-3 L de pus entre las asas
intestinales (el abdomen está lleno de pus).
En casos de evolución ultrarápida al epiplón no le da tiempo a contener
la inflamación, ya que evoluciona rápidamente, pasando por todas las
fases en 2h siendo lo normal 7 días.
1.5. PRESENTACIÓN CLÍNICA
Es muy variable (tiene una de las manifestaciones clínicas más variables que existe).
El síntoma más constante es el dolor abdominal, que suele ser contínuo (no fluctúa, va
a más poco a poco), de carácter somático y de localización predominante en FID.
Hay anorexia (como dicen los libros clásicos “una apendicitis nunca come”). En la
anamnesis preguntar siempre ¿Tiene hambre? Un paciente con apéndice jamás tiene
hambre, (aunque le ofrezcas su comida favorita, el niño no la querrá).
También vómitos en las primeras horas, cuando empieza el dolor.
Típicamente, comienza con un dolor contínuo en epigastrio, el
paciente vomita un poco y al cabo de las horas, conforme va
evolucionando, el dolor se focaliza en la FID en el punto de
Mc.Burney (trazando una línea desde la espina ilíaca hasta el
ombligo, se localizaría cerca del ombligo a 2/3 de la línea).
Se presenta también con fiebre no muy elevada o febrícula.
Cuando hay enfermedad difusa sí que hay fiebre.
1.6. PRESENTACIÓN EN <2 AÑOS
En niños menores de dos años es un proceso muy infrecuente pero grave, debido a la
alta posibilidad de perforación por diagnóstico tardío.
En estas edades el cuadro suele ser atípico y no suele considerarse dada su baja
frecuencia, por lo que suele provocar el desarrollo de una peritonitis aguda difusa (por
el escaso desarrollo del epiplón, como ya hemos dicho antes).
Por encima de los dos años el diagnóstico y la presentación clínica suelen ser los
habituales.
1.7. EXPLORACIÓN FÍSICA
Dolor abdominal a la palpación del punto de Mc Burney. (A veces duele en este
punto, pero en ocasiones duele el punto ovárico, en ocasiones duele la fosa renal).
En apéndices retrocecales y de localización pélvica la palpación abdominal puede
ser normal. Es útil la maniobra del Psoas: colocamos la mano en FID a la vez que
levantamos pasivamente la pierna derecha, así al contraerse dicho músculo, se
comprime el apéndice y causa dolor.
3/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Si existe participación del peritoneo parietal (estadío avanzado) habrá signos de
irritación peritoneal: Blummberg+ (dolor a la descompresión en FID), Rousing+
(parecido al Blummberg pero presentando dolor en FID cuando presionamos FII).
Se aprecia claramente en la exploración, involuntariamente se contrae la
musculatura abdominal (defensa) y no presenta el vientre normal fácilmente
depresible.
1.8. DIAGNÓSTICO Y PRUEBAS COMPLEMENTARIAS
No hay ninguna técnica que nos dé el diagnóstico al 100%. El diagnóstico de certeza se
obtiene tras la cirugía.
LABORATORIO: Suele haber leucocitosis moderada con desviación izquierda y
elevación de la PCR (este último presenta un poco más de sensibilidad) y demás
reactantes de fase aguda. Pero OJO porque ¡una analítica normal no descarta una
apendicitis!
PRUEBAS DE IMAGEN:
a. Rx de abdomen y tórax suele ser inespecífica. Puede apreciarse borramiento
de la línea del psoas, asas dilatadas, obstrucción. La presencia de
apendicolitos es diagnóstica.
Utilización selectiva de ECO y TAC según las necesidades:
b. La ecografía es útil en personas delgadas y en manos expertas, porque es
operador dependiente. Como signos ecográficos sugestivos de apendicitis
tenemos:
- apéndice alargado, no compresible;
- apendicolito;
- diámetro mayor de 6 milímetros;
- masa si el plastrón está inflamado.
La eco tiene una S:83-90 %, E:95-99%, VPP:86%, VPN:94%; pero como hemos
dicho depende mucho de la habilidad del radiólogo. Se usa cuando hay duda
diagnóstica y el resultado siempre se debe correlacionar con la clínica.
c. TAC: es la prueba de imagen más útil (sobre todo en estadíos avanzados),
pero sólo debe utilizarse en casos de duda diagnóstica. Esta prueba consta de
una S: 99% , E:95%, VPP:93%, VPN: 99%. Existen estudios que se preguntan si
es excesivo el uso de las investigaciones radiológicas en caso de la apendicitis,
llegando a la conclusión de que NO existe correlación entre la indicación de
TAC y la severidad de la apendicitis. Como dato, saber que en los últimos 10
años ha habido un aumento de un 35% del uso del TAC. Con todo ello el
profesor pretende transmitirnos que tenemos que pedir un TAC cuando
realmente nos haga falta (mucha duda diagnóstica, casos graves,
postoperatorio)
SISTEMAS DE PUNTUACIÓN. ESCALA ALVARADO: si la puntuación al evaluar al
paciente es Score>= 7 habrá mayor probabilidad de apendicitis, pero no es una
indicación quirúrgica por si sola. El profesor comenta que nunca ha visto utilizar
4/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
esta escala y que no es específica (una gastroenteriris por ejemplo también daría
una puntuación mayor que 7). Ante todo tenemos que tener sentido común.
Criterios:
- Migración del dolor hacia FID – 1 punto
- Anorexia – 1 punto
- Nauseas o Vomitos – 1 punto
- M.e.g. y Decaimiento – 2 puntos
- Dolor a la descompresión – 1 punto
- Elevación de la temperatura >= 37,3º C – 1 punto
- Leucocitosis > 10.000 – 2 puntos
- Desviación a la izquierda > 75% Neutrofilia – 1 punto
Score >= 7 Mayor probabilidad de Apendicitis
RECOMENDACIONES
En el año 2014 el diagnóstico de la apendicitis aguda sigue siendo clínico. El TAC y
la Eco no se utilizan a diario, por lo que se suele intervenir quirúrgicamente con la
mera sospecha clínica.
Nunca debemos decidirlo en el primer contacto (a no ser que sea un abdomen
agudo). Dejaremos al paciente en observación y al cabo de unas 6-12 horas
realizamos la reevaluación. Este cambio evolutivo va a ser el que más valor tendrá
a la hora de decidir operar o no, ya que si es una apendicitis empeorará seguro y si
era otra causa puede que mejore. Si después de dejar al paciente en observación y
haberlo reevaluado seguimos teniendo dudas, realizaremos una ECO.
1.9. DIAGNÓSTICO DIFERENCIAL:
a. Linfadenitis mesentérica (en niños es lo más frecuente).
b. Gastroenteritis aguda (frecuentísimo, sobre todo si se presenta con diarrea,
aunque no se puede descartar apendicitis si hay diarrea).
c. Invaginación intestinal. Es el segundo cuadro de urgencia quirúrgica después
de la apendicitis.
d. Neumonía basal derecha (en niños clínicamente puede producir un cuadro casi
indistinguible de la apendicitis).
e. Diverticulitis por divertículo de Meckel.
f. En adultos se barajan otros diagnósticos diferenciales (colecistitis, diverticulitis,
tumores complicados…).
Como hemos comentado anteriormente en caso de duda diagnóstica es mejor
intervenir para extirpar un apéndice normal (apendicectomía blanca) que esperar a
que el cuadro evolucione y se produzca una peritonitis.
5/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
1.10. TRATAMIENTO: APENDICECTOMÍA
Sólo en casos seleccionados de plastrón con palpación de masa fija localizada y sin
abscesos se puede realizar tratamiento antibiótico (raro en niños) y a medio o
largo plazo plantear si se lleva a cabo o no apendicectomía de manera diferida. El
profesor no ve ventajas al tratamiento conservador.
La apendicectomía se realiza tanto por vía abierta como laparoscópica.
En niños muy pequeños habitualmente se utiliza la vía abierta.
La incisión más utilizada es la de Mc.Burney, pero en casos de peritonitis difusa se
debe utilizar un abordaje por línea media o pararrectal (se refiere al músculo recto
del abdomen) lavando bien todas las asas intestinales, y colocando un drenaje.
También se utiliza el abordaje laparoscópico, pero en los niños no tiene utilidad,
ya que resulta complicado maniobrar laparoscópicamente con un abdomen de
pequeñas dimensiones. Las dos indicaciones para el uso de laparoscopia son:
pacientes muy obesos y en mujeres en edad fértil con dudas diagnósticas de
apendicits vs patología ginecológica.
1.10. COMPLICACIONES POSTOPERATORIAS
Van a depender del estadío evolutivo en el que se opere el apéndice.
A. PRECOCES:
Infección de herida quirúrgica: es la complicación más frecuente y menos grave,
sobre todo en las apendicitis perforadas o gangrenosas.
Abscesos intraabdominales: si son pequeños (<3-5 cm) se pautan antibióticos para
ver si hay regresión. Si son grandes se pinchan y se drenan radiológicamente
(guiado con Eco o TAC) y si no remiten se vuelve a intervenir al paciente.
Íleo paralítico.
Fístula estercorácea: rara pero temible, el muñón del apéndice extirpado puede
fistulizar por encontrarse en estado necrótico, saliendo heces por el drenaje.
Suelen cerrarse solas.
B. TARDÍAS:
Eventración, hernias.
Obstrucción intestinal por adherencias (tras casi todas las intervenciones
quirúrgicas del abdomen se producen adherencias en mayor o menor medida).
2. LINFADENITIS MESENTÉRICA
2.1. DEFINICIÓN
Entidad benigna que se caracteriza por la inflamación de los ganglios mesentéricos
ileales. Puede ser crónica o aguda dependiendo del agente causal.
6/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
El cuadro agudo tiene una presentación clínica muy similar a la apendicitis aguda.
2.2. EPIDEMIOLOGÍA
Es muy frecuente, aunque la incidencia exacta es desconocida. Se dice que es
incluso más frecuente que la apendicitis aguda, pero que muchas veces no se
diagnostica.
Es muy común en niños y adolescentes menores de 15 años.
20% de los pacientes llevados a apendicectomía tienen hallazgo de adenitis.
Suele ser secundaria a una infección orofaringea por un adenovirus que
posteriormente invade los ganglios del mesenterio.
También puede ser secundaria a una infección gastrointestinal por Yersinia
enterocolítica (USA, Europa, Australia).
Por ello, ante un cuadro de dolor abdominal, es imprescindible preguntar en la
anamnesis si el niño ha estado aletargado anteriormente, si ha presentado mocos,
etc.
2.3. ETIOLOGÍA
Se han encontrado múltiples organismos en cultivos de nódulos linfáticos:
Streptococo Bhemolitico, Staphilococos, E. Coli, Stp. Viridans, Yersinias,
Mycobacterium TB, Salmonella, shiguella, Giardia lamblia.
Virus: Coxsackie (A,B), Rubeola, Adenovirus (1,2,3,5,7).
En el caso de adenovirus, el esputo contaminado en infecciones respiratorias es
ingerido y se absorbe después en el intestino, pasando de esta forma a los ganglios
mesentéricos.
En cuanto a Yersinia enterocolítica se admite la teoría de la transmisión fecal–oral.
2.4. HISTOLOGÍA
El patrón es el de una linfadenitis reactiva, que puede ser común a muchas causas,
mostrando un patrón histológico parecido con:
Dilatación de los senos: incremento del flujo de linfa.
Acumulación de neutrófilos.
Dilatación vascular.
Edema de la cápsula.
2.5. FISIOPATOLOGÍA
Los agentes microbianos acceden a los nódulos linfáticos a través de los vasos linfáticos
intestinales, donde se multiplicarán dependiendo de la virulencia del patógeno y
ocasionarán respuesta inflamatoria, y ocasionalmente, supuración. A continuación, el
mesenterio adyacente se edematiza, pero sin presentar exudado. Por último se forma
un nódulo linfático que muestra una hiperplasia inespecífica.
7/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
2.6. CLÍNICA (es lo que nos interesa saber de la linfadenitis, para el dd con apendicitis)
Progresión rápida o insidiosa, similar a la de la apendicitis aguda.
Antecedente de infección del tracto respiratorio alto o ingesta de cerdo
(Yersinia).
Dolor abdominal (FID) ó localización difusa.
Signo de Klein: el punto máximo de dolor se traslada desde FID hacia la línea
media cuando el paciente pasa de supino a decúbito lateral izquierdo. Es
importante saber que esto sucede en la linfadenitis y no en la apenticitis aguda
puesto que el mesenterio, a diferencia del apéndice, es móvil, y cae cuando el
paciente pasa a decúbito lateral izquierdo, trasladándose de esta forma el dolor.
Contractura voluntaria. Aunque no haya irritación peritoneal, el paciente presenta
defensa voluntaria ante la compresión, debido a que hay dolor. Por ello es tan
importante mantener distraido al niño durante la exploración y evitar que
contraiga voluntariamente para poder hacer el diagnóstico diferencial con
peritonitis.
Fiebre (>38–38.5°C), más elevada que en la apendicitis aguda.
Adenopatías cervicales (20%).
Nauseas, vómitos (preceden a dolor abdominal).
2.7. DIAGNÓSTICO
A) Laboratorio
Leucocitosis >10.000 en 50 % de los pacientes (sobre todo linfocitosis, a
diferencia de la apendicitis, donde hay neutrofilia)
Aunque menos frecuentemente se pueden realizar:
Analítica urinaria (descartar ITU’s).
Serología (usada para aislamiento de Y.Enterocolítica).
Coprocultivo en pacientes con diarrea.
Hemocultivo: si hay septicemia.
Aislamiento de germen en nódulos, sangre u otros fluidos para definir
tratamiento.
B) Eco abdominal
Se puede evidenciar edema de Ileon terminal, además, el engrosamiento mesentérico
puede ser indicio de enteritis regional. Rigidez focalizada al transductor. Se prefiere de
modo inicial, especialmente en niños con dolor abdominal leve.
C) TAC abdominal
Muestra nódulos linfáticos mesentéricos ensanchados, con o sin presencia de
8/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
engrosamiento de paredes del ileon. El Apéndice tiene aspecto normal.
2.8. DIAGNÓSTICO DIFERENCIAL
Sobre todo con la apendicitis.
Gastroenteritis aguda (GEA).
Enteritis.
Colecistitis.
Isquemia mesentérica crónica.
Patología ginecológica (Embarazo ectópico, salpingitis…).
Intestino irritable.
ITU’s (Pielonefritis).
2.9. TRATAMIENTO
Lo principal es identificar pacientes que requieran tratamiento quirúrgico
(habitualmente debido a duda diagnóstica).
Si el diagnóstico de linfadenitis aguda está claro trataremos con:
- Hidratación.
- Analgesia.
- Antibióticos si hay infección por Yersinia.
2.10. COMPLICACIONES
Las complicaciones son raras, pudiendo observar: repleción de volumen y desequilibrio
hidroelectrolítico, abscesos, peritonitis y septicemia.
El pronóstico es bueno, con recuperación completa sin tratamiento específico en la
mayoría de casos.
3. DIVERTÍCULO DE MECKEL
3.1. GENERALIDADES
Es la malformación congénita más prevalente del tracto gastrointestinal.
Se trata de un divertículo verdadero, ya que contiene todas las capas histológicas
de la pared intestinal.
Es un vestigio del conducto onfalomesentérico, resultado de la obliteración
incompleta de la parte proximal de dicho conducto.
Se localiza habitualmente a 60-100 cm de la válvula ileocecal.
9/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
En el 20 – 30% de los casos es asiento de tejido ectópico, generalmente de origen
gástrico, y menos frecuente pancreático. La secreción activa de HCl de la mucosa
gástrica ectópica daña la mucosa intestinal adyacente y ello es causa frecuente de
enterorragias, siendo su origen la mucosa adyacente ileal y no la ectópica.
3.2. EMBRIOLOGÍA
El conducto onfalomesentérico conecta el saco vitelino
con el tracto intestinal en las primeras semanas del
desarrollo embrionario, y normalmente se oblitera
entre la 5º y 7ºsemana de gestación. Su cierre
defectuoso conduce a distintas anomalías, incluyendo el
seno umbilical (A), fístula onfalomesentérica(B), cordón
fibroso (C), divertículo de Meckel (D) o quiste umbilical
(E).
3.3. CLÍNICA
Generalmente es asintomática (sobre todo cuando no es permeable), aunque en
ocasiones puede presentar complicaciones:
Hemorragia por ulceración de la mucosa ileal adyacente: puede presentarse
como sangre roja-fresca en heces (cuando el sangrado es agudo y el tránsito
intestinal rápido) o como melenas (si el tiempo de tránsito es más prolongado y la
sangre ha sufrido procesos digestivos).
Obstrucción intestinal por invaginación o vólvulo: Es una obstrucción adquirida
pero producida por una anomalía congénita. Las invaginaciones suelen
presentarse en niños mayores, no tanto en lactantes. Los vólvulos aparecen
cuando persiste una brida de conexión entre el divertículo y el ombligo que actúa
como eje para la rotación del intestino.
Diverticulitis: se puede infectar el divertículo por la translocación bacteriana al
igual que puede hacerlo cualquier otro divertículo. La clínica es la misma que la de
una apendicitis, por lo que hay que hacer con ella el diagnóstico diferencial. De
hecho, muchas apendicitis en blanco resultan ser divertículos de Meckel, por lo
que se recomienda ante su sospecha rastrear el ID hasta 60-100 cm de la válvula
íleo-cecal para descartarlo.
Secreción umbilical: es persistente en fistulas incompletas.
Es importante saber que en la edad pediátrica la complicación más frecuente es la
obstrucción, mientras que en adultos lo es la hemorragia digestiva.
La diverticulitis es un cuadro clínico indestinguible de la apendicitis aguda.
La presencia del divertículo en una hernia inguinal (hernia de Littré) es poco frecuente.
10/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
3.4. DIAGNÓSTICO
El diagnóstico preoperatorio es muy difícil, debido a la similitud con la apendicitis.
La TAC es la prueba más rentable en ante un divertículo complicado. Por tanto, sólo
podemos diagnosticarlo cuando iniciamos la cirugía. De hecho, cuando iniciamos una
apendicectomía y vemos que el apéndice no es causante del cuadro, debemos de
explorar los últimos 60 – 100 cm para descartar que la causa sea una diverticulitis de
Meckel.
En caso de hemorragia, se utiliza la gammagrafía con Tc-99, que es captado por las
células parietales de la mucosa gástrica ectópica en el divertículo. Sin embargo, es una
prueba que cuando es negativa no permite descartar la enfermedad, ya que también
puede deberse a mucosa pancreática u otras menos frecuentes que en este caso no
captan Tc-99.
3.5. TRATAMIENTO
Sólo existe indicación quirúrgica si hay complicaciones, en cuyo caso se realiza la
resección del divertículo si éste está inflamado, o la resección segmentaria del
intestino delgado adyacente en caso de sangrado o perforación de base (recordamos
que la mucosa que sangra es la adyacente enteroileal, y no la mucosa ectópica del
divertículo).
Con los hallazgos incidentales de divertículos asintomáticos en otras intervenciones
(apendicectomía), no está claro qué hacer, aunque el profesor recomienda no extirpar
el divertículo si no es necesario.
BIBLIOGRAFÍA:
11/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
- Apuntes de clase proporcionados por el profesor.
- Apuntes propios.
- Comisiones de años anteriores.
Gracias Ana, Jau
12/11
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Comisionado: Luca Schneller-Pavelescu Apetrei
Profesor: Francisco Ivorra CP-14 Y 15
Fecha y hora: 05/11/14; 14.00-15.30
SESIÓN CLÍNICA ABDOMEN AGUDO
1. DOLOR ABDOMINAL Y ABDOMEN AGUDO
El dolor abdominal es una de las consultas más frecuentes en Pediatría (incluso la más
frecuente) y según su evolución, distinguimos dos tipos:
▫ Agudo: Obliga a hacer un diagnóstico en urgencia. Tipos:
Quirúrgico:
Sdme. Peritoneal.
Sdme. Oclusivo.
Sdme. Perforativo.
Sdme. Hemorrágico.
Sdme. Torsión.
No quirúrgico.
▫ Crónico: más frecuentemente benigno (en referencia a sus
implicaciones quirúrgicas), cuando lleva más de 1-2 días:
Dolor abdominal recurrente.
Dolor abdominal en relación con la alimentación.
Un niño con dolor abdominal crónico puede presentar un dolor agudo en un momento
dado, por ejemplo, en un niño intolerante a la lactosa hay que tener cuidado cuando
presente una apendicitis y que no se pase.
2. TIPOS DE DOLOR SEGÚN SUS CARACTERÍSTICAS (se dio por sabido)
• Dolor visceral: difuso y mal localizado, expresado como quemazón o
incomodidad. Frecuentemente asociado a síntomas vegetativos. No se
encuentra postura antiálgica.
• Dolor somático: bien localizado y punzante. Produce quietud, originando una
posición antiálgica que intenta evitar cualquier movimiento.
• Dolor referido: el que se expresa en un lugar distinto al que se origina. El dolor
referido a escápula sugiere origen en la vía biliar, el percibido en el hombro
origen diafragmático, en genitales origen ureteral y gonadal y en región lumbar,
uterino.
3. CONCEPTO DE ABDOMEN AGUDO
“Cuadro clínico que involucra un conjunto de signos y síntomas dónde el dolor
abdominal está siempre presente y además se asocian otros fenómenos y otras
circunstancias de significación o gravedad (mal estado general, fiebre, hipotensión,
taquicardia, palidez, anemia,…).”
Página 1 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
En su gran mayoría los dolores abdominales agudos son secundarios a causas que no
revisten gravedad como pueden ser las transgresiones alimentarias, los cólicos
comunes, los cuadros febriles por infecciones leves, anginas, otitis, gastroenteritis
leves, etc. En otros casos pueden ser secundarios a enfermedades un poco más
complejas y delicadas como las Hepatitis, Neumonías de la base derecha del pulmón,
Infecciones urinarias, gastroenteritis moderadas y graves, traumatismos abdominales,
episodios convulsivos, cefaleas migrañosas, etc.
Por ello uno de los objetivos fundamentales al abordar el dolor abdominal en los
Servicios de Urgencia, es distinguir el dolor abdominal subsidiario de tratamiento
médico de aquellas patologías abdominales de evolución rápida, que necesitan para su
tratamiento una intervención quirúrgica de urgencia.
4. CLASIFICACIÓN SINDRÓMICA (CLASIFICACION DE CHRISMANN)
• Síndrome peritoneal (o inflamatorio): apendicitis, diverticulitis de Meckel,
peritonitis primaria y/o de cualquier otro origen…
• Síndrome oclusivo: invaginación intestinal, malrotación, tumores, hernia
estrangulada…
• Síndrome perforativo: enterocolitis necrotizante, traumatismo, apendicitis o
diverticulitis perforadas,…
• Síndrome hemorrágico: rotura esplénica, hepática, trauma…
• Síndrome de torsión o síndrome oclusivo vascular: ovárica, mesenterio…
4.1 Síndrome peritoneal
• Patogenia: irritación o inflamación del peritoneo.
• Causas: apendicitis aguda (la más frecuente), diverticulitis de Meckel,
peritonitis primaria (en neonatos).
• Síntomas: dolor abdominal, vómitos y fiebre.
• Exploración física: taquicardia,
dolor con defensa,
descompresión y percusión dolorosas.
4.2 Síndrome oclusivo (son las patologías vistas en las clases del Dr. Sánchez París)
• Patogenia: imposibilidad de tránsito del contenido intestinal. Puede ser alto,
medio o bajo, según la localización de la obstrucción. La obstrucción puede ser
paralítica o mecánica. La única obstrucción paralítica subsidiaria de tratamiento
quirúrgico es el megacolon agangliónico.
• Causas:
▫ Neonatos: megacolon agangliónico, malformaciones ano-rectales,
atresia intestinal, estenosis intestinal, hernia diafragmática, malrotación
intestinal.
▫ > 28 días: bridas, invaginación intestinal, malrotación, tumores, hernia
inguinal estrangulada.
• Síntomas: vómitos, dolor abdominal cólico y ausencia de expulsión de gas o
heces por recto.
Página 2 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
• Exploración física: abdomen distendido y doloroso, con posible defensa. Ruidos
hidroaéreos aumentados. Ampolla rectal vacía o con masas fecales. Puede
haber taquicardia y signos de deshidratación (por la formación de un gran
tercer espacio).
4.3 Síndrome perforativo
• Patogenia: irritación peritoneal al ponerse en contacto con jugo gástrico,
contenido intestinal o bilis.
• Causas:
▫ Neonato: enteritis necrotizante, perforación gástrica espontánea, úlcera
de estrés, iatrogenia.
▫ > 28 días: úlcera péptica, perforación traumática, úlcera de estrés,
iatrogenia.
• Síntomas: intenso dolor abdominal, fiebre y afectación del estado general. No
suele haber vómitos, porque el contenido intestinal pasa al peritoneo.
• Exploración física: taquicardia, abdomen en tabla, percusión dolorosa con
pérdida de la matidez en el área hepática y descompresión dolorosa.
• Pruebas complementarias: gas libre en la radiografía simple en bipedestación
(neumoperitoneo).
4.4 Síndrome hemorrágico
• Patogenia: irritación del peritoneo por la presencia de sangre libre en la cavidad
abdominal, típico de los traumatismos.
• Causas:
▫ Neonato: rotura hepática, esplénica o de glándula suprarrenal por
trauma obstétrico.
▫ > 28 días: rotura hepática, esplénica o renal de causa traumática, lesión
de vasos mesentéricos.
• Síntomas: palidez, sudoración, afectación del estado general y posible shock
hipovolémico.
• Exploración física: taquicardia, hipotensión arterial, signos externos de
traumatismo, dolor y defensa a la palpación con descompresión dolorosa.
• Pruebas complementarias: en un TAC podrá visualizarse sangre libre en la
cavidad peritoneal.
4.5 Síndrome de torsión o de oclusión vascular
• Patogenia: torsión de tumor u órgano pediculado, por ello es más frecuente en
niñas.
• Causas: torsión de quiste de ovario.
• Síntomas: dolor abdominal brusco e intenso y vómitos acompañado de gran
cortejo vegetativo (sudor, vómitos, mal estado general, inquietud,…).
• Exploración física: tumoración dolorosa en hipogastrio o fosa iliaca. Tacto
rectal: palpación de la masa.
Página 3 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
5. CAUSAS DE DOLOR ABDOMINAL NO QUIRÚRGICO
6. ETIOLOGÍA DEL DOLOR ABDOMINAL AGUDO
Recién Nacido: (no apendicitis)
Atresia intestinal.
Mal rotación.
Vólvulo intestinal.
Enfermedad de Hirschsprung.
Malformaciones ano rectales.
Ileo meconial.
Lactante: (no apendicitis)
Invaginación intestinal.
Gastroenteritis.
Hernia incarcerada.
Alergia a proteínas vacunas.
Obstrucción intestinal.
Patología renoureteral.
Preescolar, escolar y adolescente:
Patología intestinal:
Apendicitis.
Linfadenitis mesentérica.
Ileitis infecciosa.
Gastroenteritis.
Hernia incarcerada.
Púrpura de Schönlein-Henoch.
Otras:
Patología biliar: colecistitis.
Patología pancreática: pancreatitis.
Página 4 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Patología de órganos genitales.
Torsión testicular.
Quiste ovárico.
Patología urinaria.
Pielonefritis.
Cólico nefrítico.
Patología pulmonar: neumonía basal.
7. DIAGNÓSTICO
• Anamnesis.
• Síntomas acompañantes.
• Localización del dolor.
• Exploración física.
• Pruebas complementarias.
• Reevaluación clínica si el estado del paciente lo permite.
7.1 Anamnesis
• Edad y sexo: en niñas adolescentes es importante recoger los antecedentes
ginecológicos u obstétricos.
• Forma de presentación:
- Brusco en casos de perforación, invaginación o embarazo ectópico.
- Gradual en procesos inflamatorios como apendicitis o pancreatitis.
- Crónico en estreñimiento, EII, fibrosis quística o anemia de células
falciformes.
• Tiempo transcurrido: dolor abdominal severo de más de seis horas de duración
sugiere patología quirúrgica.
• Características:
- Dolor constante que se exacerba con los movimientos sugiere
peritonitis.
- Dolor cólico cuando hay afectación de vísceras huecas o situaciones que
aumentan el peristaltismo.
7.2 Síntomas acompañantes
• Vómitos: se asocian a patología quirúrgica, sobre todo si son persistentes, de
contenido bilioso o fecaloideo o si son posteriores al dolor. En niños pequeños,
la anorexia y náuseas tienen el mismo significado que los vómitos.
• Diarrea: junto con dolor abdominal cólico sugiere gastroenteritis. Puede darse
en apendicitis por irritación peritoneo visceral.
• Fiebre desde el inicio del cuadro sugiere origen infeccioso.
• Síntomas respiratorios: descartar neumonía de lóbulos inferiores.
• Síntomas genitourinarios.
• Síntomas ginecológicos.
7.3 Localización
• Hipocondrio derecho: En donde se localizan el hígado, la vesícula biliar, el
ángulo hepático del colon y profundamente el riñón derecho.
Página 5 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
• Epigastrio: En donde se localizan el estómago, el duodeno, el páncreas y plexo
solar.
• Hipocondrio izquierdo: en donde se localizan la cola del páncreas, el bazo, el
ángulo esplénico del colon y más profundamente el riñón izquierdo
• Flanco derecho: En donde se localizan el colon ascendente y asa delgadas
intestinales.
• Región umbilical: En donde se encuentran asas delgadas intestinales.
• Flanco izquierdo: En donde se encuentran el colon descendente y asas delgadas
intestinales.
• Fosa ilíaca derecha: En donde se ubican el ciego, el apéndice cecal y los anexos
derechos en la mujer.
• Hipogastrio: En donde se ubican el epiplón mayor, asas delgadas intestinales,
vejiga y el útero en la mujer.
• Fosa ilíaca izquierda: En donde se localiza el colon sigmoides y los anexos
izquierdos en la mujer.
7.4 Exploración física
• General: observar la actitud del paciente y la adopción de posturas antiálgicas.
Búsqueda de causas extraabdominales: infecciones ORL, neumonía, meningitis.
• Abdominal:
▫ Inspección.
▫ Auscultación.
▫ Percusión.
▫ Palpación: inicialmente superficial y comenzando por la zona más
alejada al punto de máximo dolor. Comprobar los orificios inguinales.
Realizar las maniobras más dolorosas en último lugar (Blumberg, psoas,
Murphy, etc).
▫ Tacto rectal: no de forma rutinaria, sólo en aquellos casos que pueden
ayudar al diagnóstico (fecaloma, sospecha de apendicitis retrovesical o
patología anexial).
▫ Maniobras activas: sentarse desde posición de tumbado, saltar o
levantar las piernas, se encuentran limitadas en caso de irritación
peritoneal.
▫ Genitales externos: exploración sistemática.
• En la primera evaluación del paciente se debe establecer la gravedad del
cuadro y su situación hemodinámica.
• El examen abdominal en recién nacidos y lactantes pequeños, en ocasiones es
tan engañoso que se puede estar en presencia de una peritonitis difusa y no
encontrar una sensibilidad importante.
7.5 Pruebas complementarias
• Analítica de sangre
- Hemograma: fórmula y recuento.
- Reactantes de fase aguda: se elevan en el dolor abdominal de causa
inflamatoria.
- Bioquímica y gasometría.
- Coagulación.
Página 6 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
• Análisis de orina: (sedimento) rutinario en el diagnóstico diferencial.
• Test de embarazo: En toda adolescente con actividad sexual. Descartar
embarazo antes de realizar pruebas radiológicas.
7.6 Pruebas complementarias radiológicas
• Radiografía simple: valoración de la distribución del aire intestinal y la
existencia de aire ectópico. Imágenes cálcicas (apendicolito, litiasis biliar o
renal, ganglios calcificados, tumores).
• Enema opaco: diagnóstico y tratamiento de la invaginación intestinal.
• Ecografía abdominal: es la prueba diagnóstica ideal, por su buena sensibilidad y
especificidad y ausencia de radiación, aunque es muy radiólogo dependiente.
• En caso de trauma y paciente inestable se puede realizar una ECO-fast.
• TAC: alta especificidad y sensibilidad para muchas patologías. Sólo se debe
realizar en casos seleccionados.
8. CONSIDERACIONES FINALES
• Tiempo evolución muy variable.
• Síntomas inespecíficos que en ocasiones confunden.
• Escaso rendimiento datos de laboratorio.
• Poco rendimiento estudios de imagen.
• Enfermos especiales.
9. CASOS CLÍNICOS
Caso clínico 1
Niña de 7 años que consulta por dolor abdominal de 24 horas de evolución.
Sin antecedentes médico-quirúrgicos de interés.
EA: paciente con dolor abdominal de 24 horas de evolución que comienza en
mesogastrio y ahora se focaliza en FID. Presenta diarrea, anorexia. No disuria.
Diagnóstico de sospecha
Diagnóstico diferencial
Tipos de dolor que tiene el paciente
Analgesia en el abdomen agudo
Prueba de imagen
Diagnóstico diferencial
Apendicitis.
Dolor abdominal inespecífico.
ITU.
Página 7 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
Neumonía base derecha.
Adenitis mesentérica.
GEA.
Exploración clínica
Afebril.
Dolor leve a la exploración abdominal, con predominio en FID.
No signos de irritación peritoneal.
Blumberg -. Rousing -. Maniobra de psoas -.
¿Qué pruebas solicitarías en este momento?
Hemograma: 15.000 leucocitos con 85% de granulocitos.
Radiografía de tórax y ECG sin alteraciones.
Radiografía simple de abdomen sin alteraciones.
Podría pedirse también un sedimento en orina.
¿Qué actitud tomamos?
Observación y dieta líquida.
Exploración clínica (2ª visita)
Persiste mismos hallazgos exploratorios.
Aparición de febrícula (37,8 ºC).
La madre nos refiere que desde la anterior visita ha realizado dos deposiciones
blandas y refiere disuria.
¿Solicitarías alguna prueba más en este momento?
Ecografía
Diagnóstico definitivo
Apendicitis aguda.
Caso clínico 2
Presentación clínica
Niño de 6 años de edad que acude por dolor abdominal de predominio en
mesogastrio, intenso, exacerbado con ingesta, refractario a antiinflamatorios
no esteroideos (AINES).
Se asocian vómitos incontables, distensión abdominal y evacuaciones
diarreicas abundantes y fétidas.
Exploración física
38 ºC de temperatura.
Aparenta malas condiciones generales, diaforético, facies álgida, en actitud
antiálgica, marcada distensión abdominal, ruidos hidroaéreos aumentados, no
signos de lucha, timpanizado y doloroso a la palpación superficial y profunda.
Página 8 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
¿Qué harías a continuación?
Primeras medidas
Ante la presencia de vómitos profusos se decide:
Sonda nasogástrica: 1000cc de contenido gástrico, aspecto bilioso no fétido.
Sonda vesical: Diuresis: 1200cc/12horas.
Canalización de vía venosa. Reposición hidroelectrolítica.
¿Que pruebas complemenetarias realizarías?
Laboratorio: leucocitosis 23.000.
Radiografía abdominal simple de pie: niveles hidroaéreos.
ECO abdominal: asas dilatadas.
Diagnósticos de sospecha
Obstrucción por vólvulo, por invaginación, por divertículo de Meckel invaginado,
apendicitis.
¿Qué actitud adoptarías?
Se decide intervención quirúrgica, objetivando una obstrucción intestinal por
Divertículo de Meckel inflamado. Se hubiese podido plantear la duda entre hacer un
TAC o pasar directamente a laparotomía diagnóstica. Se prefiere esta última por la
gravedad del cuadro.
Caso clínico 3
Presentación clínica
Escolar de siete años que consulta por dolor abdominal iniciado tres horas
antes, súbito, de intensidad progresiva, severo cuando llego a la consulta,
localizado en zona periumbilical e irradiado a cuadrante superior izquierdo.
Acompañado de fiebre alta no cuantificada.
Exploración física
39,5 ºC de temperatura oral.
Dolor abdominal en el momento del examen, grave y difuso con leve
distensión abdominal.
¿Que pruebas complemenetarias realizarías?
Hemograma: marcada leucocitosis con predominio de polimorfonucleares.
Sedimento urinario sin hallazgos patológicos.
Radiografía simple de abdomen y tórax.
Diagnóstico
Neumonía basal izquierda.
Página 9 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
lOMoARcPSD|4513632
10. CONCLUSIONES
El dolor abdominal continúa siendo un dilema diagnóstico y de tratamiento en
Pediatría.
Se ha descrito el concepto de dolor abdominal "reflejo“, para describir cuadros
clínicos extraabdominales que provocan dolor abdominal y abdomen agudo.
En la edad pediátrica la causa más frecuente de dolor abdominal reflejo es la
neumonía basal.
11. BIBLIOGRAFÍA
• Apuntes de clase.
• Apuntes del profesor.
Benidorm10, Santa Pola21, y las que queramos ;)
Página 10 de 10
Descargado por EviTa García Martinez (miel.5577@gmail.com)
S-ar putea să vă placă și
- PIELDocument99 paginiPIELJuan ArellanoÎncă nu există evaluări
- Atresia de EsofagoDocument17 paginiAtresia de EsofagoSara RōmanovÎncă nu există evaluări
- Malformaciones DigestivasDocument28 paginiMalformaciones DigestivasCata villaÎncă nu există evaluări
- Atresia EsofagicaDocument17 paginiAtresia EsofagicaRay Kevin Leyva GarciaÎncă nu există evaluări
- Atresia de EsofagoDocument79 paginiAtresia de EsofagoGianluca Corelli Bisso ValdezÎncă nu există evaluări
- Urgencias Quirurgicas en NeonatologiaDocument51 paginiUrgencias Quirurgicas en NeonatologiaIVANÎncă nu există evaluări
- Atresia EsofágicaDocument65 paginiAtresia EsofágicaLiz GonzalesÎncă nu există evaluări
- Fistula Traqueoesofagica FinalDocument47 paginiFistula Traqueoesofagica FinalRudy TtitoÎncă nu există evaluări
- Atresia Traqueo Esofagica CirugiaDocument20 paginiAtresia Traqueo Esofagica CirugiaNeuverys MateoÎncă nu există evaluări
- Protocol o Atresia Es of A GicaDocument21 paginiProtocol o Atresia Es of A GicaYe StÎncă nu există evaluări
- Defectos de La Pared AbdominalDocument37 paginiDefectos de La Pared AbdominalRodrigo SantibañezÎncă nu există evaluări
- Patologia Del Aparato DigestivoDocument15 paginiPatologia Del Aparato DigestivoMendoza CarlosÎncă nu există evaluări
- Libro DR Juan NamocDocument50 paginiLibro DR Juan NamocJavier Manuel Escobedo Calderón100% (1)
- Atresia EsofágicaDocument4 paginiAtresia EsofágicaMarvatÎncă nu există evaluări
- Gastrosquisis OnfaloceleDocument29 paginiGastrosquisis OnfaloceleJorge Paul HerreraÎncă nu există evaluări
- 2 Atresiay Estenosis - Esofagica - UMBDocument43 pagini2 Atresiay Estenosis - Esofagica - UMBJorge Antonio YzRzÎncă nu există evaluări
- Malformaciones Gi...Document36 paginiMalformaciones Gi...lulu caceresÎncă nu există evaluări
- Clase Trastornos EsofágicosDocument6 paginiClase Trastornos EsofágicosagustinalopfÎncă nu există evaluări
- Fistula y Atresia Gastro EsofagicaDocument39 paginiFistula y Atresia Gastro EsofagicaSARAY100% (1)
- Obstruccion Intestinal PDFDocument29 paginiObstruccion Intestinal PDFJean Aguilar MaldonadoÎncă nu există evaluări
- ClaseDocument144 paginiClaseJimmy PinoÎncă nu există evaluări
- Fistula TraqueoesofagicaDocument37 paginiFistula TraqueoesofagicaMichelle Gonzalez HaroÎncă nu există evaluări
- Clase 9 Cirugía PediatricaDocument40 paginiClase 9 Cirugía PediatricamedicinaandiaÎncă nu există evaluări
- Malformaciones DigestivasDocument57 paginiMalformaciones DigestivasDavid DiazÎncă nu există evaluări
- PATOLOGIA QUIRURGICA PediatriaDocument6 paginiPATOLOGIA QUIRURGICA PediatriaCeci LallanaÎncă nu există evaluări
- CirugiapediatricaDocument203 paginiCirugiapediatricaJUAN CARLOSÎncă nu există evaluări
- 2°-Examen-Cx GeneralDocument39 pagini2°-Examen-Cx GeneralBS3091Încă nu există evaluări
- Ilovepdf MergedDocument30 paginiIlovepdf MergedGissela izaÎncă nu există evaluări
- Atresia Esofagica - 20231107 - 232026 - 0000Document15 paginiAtresia Esofagica - 20231107 - 232026 - 0000Evelyn Aburto AguilarÎncă nu există evaluări
- Atresia Del EsofagoDocument35 paginiAtresia Del EsofagoJessicaALÎncă nu există evaluări
- Patologías Digestivas PediátricasDocument60 paginiPatologías Digestivas PediátricasGreysi Nayeli Martínez GirónÎncă nu există evaluări
- Fístula y AtresiaDocument31 paginiFístula y AtresiataracenaarellanomaquillajeÎncă nu există evaluări
- Malformaciones Anorectales 2019Document16 paginiMalformaciones Anorectales 2019Gustavo MartínezÎncă nu există evaluări
- RN QuirurgicoDocument13 paginiRN QuirurgicoPablo Espíndola MatéÎncă nu există evaluări
- Atresia EsofágicaDocument57 paginiAtresia EsofágicaDaniela Huechumpan anticanÎncă nu există evaluări
- Sexta ClaseDocument5 paginiSexta ClaseLuis Armando Santos AlvarezÎncă nu există evaluări
- Atresia EsofagicaDocument19 paginiAtresia EsofagicaDPEM01Încă nu există evaluări
- Onfalocele ARZUDocument14 paginiOnfalocele ARZUAlberto ZOÎncă nu există evaluări
- Atresia Del EsófagoDocument6 paginiAtresia Del EsófagoRestauradas Para ServirÎncă nu există evaluări
- CriptorquideaDocument57 paginiCriptorquideaSantiago LópezÎncă nu există evaluări
- Trabajo CX GeneralDocument3 paginiTrabajo CX GeneralIsabel GuzmánÎncă nu există evaluări
- Aganglionosis Congénita Del ColonDocument8 paginiAganglionosis Congénita Del ColonAnabel AldasÎncă nu există evaluări
- Atresia EsofagicaDocument25 paginiAtresia EsofagicaSebastian AjaÎncă nu există evaluări
- Atresia EsofágicaDocument4 paginiAtresia Esofágicapaola andreaÎncă nu există evaluări
- Atresia EsofágicaDocument3 paginiAtresia EsofágicaKaReN YañezÎncă nu există evaluări
- Atresia+y+Fistula+Traqueo EsofagicaDocument5 paginiAtresia+y+Fistula+Traqueo EsofagicaJesenia Chapoñan BancesÎncă nu există evaluări
- Atresia EsofágicaDocument3 paginiAtresia EsofágicaFernandoÎncă nu există evaluări
- Cirugia Pediatrica IiDocument58 paginiCirugia Pediatrica IiAaron VargasÎncă nu există evaluări
- Esofago QXDocument52 paginiEsofago QXKenai IlasÎncă nu există evaluări
- Obstruccion de Tubo Digestivo AltoDocument8 paginiObstruccion de Tubo Digestivo AltoAbigailÎncă nu există evaluări
- Onfalocele WordDocument11 paginiOnfalocele WordmariajoseÎncă nu există evaluări
- Recién Nacido Con Episodio de Atragantamiento y CianosisDocument42 paginiRecién Nacido Con Episodio de Atragantamiento y CianosisVicky Leyne Alcantara BecerraÎncă nu există evaluări
- Villamemo CirugíaDocument35 paginiVillamemo CirugíaMirko Espejo VargasÎncă nu există evaluări
- Herniainguinalumbilicalinguinoescrotal 160330221617Document37 paginiHerniainguinalumbilicalinguinoescrotal 160330221617gustavokeilholdÎncă nu există evaluări
- ONFALOCELE y GASTROSQUISISDocument4 paginiONFALOCELE y GASTROSQUISISKarina AmadorÎncă nu există evaluări
- Urgencias NeonatalesDocument64 paginiUrgencias Neonatalesmitchell erazoÎncă nu există evaluări
- Exposición Grupo 5 (2Document45 paginiExposición Grupo 5 (2ARIAN MILAGROS BARRIENTOS CHOCCAÎncă nu există evaluări
- 5° Patología de Pared Abdominal y Ano Rectal BenignaDocument153 pagini5° Patología de Pared Abdominal y Ano Rectal BenignaJOSE LUIS SALAZAR LEON100% (1)
- Apuntes en Atresia de EsofagoDocument6 paginiApuntes en Atresia de EsofagoValery MFÎncă nu există evaluări
- PROTOCOLO ERC en DialisisDocument65 paginiPROTOCOLO ERC en DialisisEva Garcia MartinezÎncă nu există evaluări
- Santos Manejo de La Via AereaDocument47 paginiSantos Manejo de La Via AereaEva Garcia MartinezÎncă nu există evaluări
- EXPERTO MANUAL de ANESTESIA PEDIATRICA - 9 - 3 PDFDocument517 paginiEXPERTO MANUAL de ANESTESIA PEDIATRICA - 9 - 3 PDFEva Garcia Martinez100% (2)
- Historia Clinica PediatricaDocument5 paginiHistoria Clinica PediatricaEva Garcia MartinezÎncă nu există evaluări
- DEXMEDETOMIDINA - PDF TIVA) PDFDocument13 paginiDEXMEDETOMIDINA - PDF TIVA) PDFEva Garcia MartinezÎncă nu există evaluări
- Criterios de Extubacion Ampliados PDFDocument247 paginiCriterios de Extubacion Ampliados PDFEva Garcia MartinezÎncă nu există evaluări
- Ventilacion Pulmonar Selectiva 2 PDFDocument31 paginiVentilacion Pulmonar Selectiva 2 PDFEva Garcia MartinezÎncă nu există evaluări
- Analgesia Durante El Trabajo deDocument13 paginiAnalgesia Durante El Trabajo deEva Garcia MartinezÎncă nu există evaluări
- Protocolo de NefrectomiaDocument11 paginiProtocolo de NefrectomiaEva Garcia Martinez100% (1)
- Guia Dosificacion 3 Edicion - PediatriaDocument1 paginăGuia Dosificacion 3 Edicion - PediatriaEva Garcia MartinezÎncă nu există evaluări
- Ensayo Sobre La AnsiedadDocument6 paginiEnsayo Sobre La AnsiedadVillegas Pérez America JazminÎncă nu există evaluări
- Sindrome Climaterico PDFDocument18 paginiSindrome Climaterico PDFPaula Martínez VazquezÎncă nu există evaluări
- OsteonecrosisDocument2 paginiOsteonecrosisvettel11Încă nu există evaluări
- Antidepresivos. Llanos MerínDocument4 paginiAntidepresivos. Llanos MerínEstíbaliz NavalicheÎncă nu există evaluări
- Clase 3 Colocación Sonda VesicalDocument24 paginiClase 3 Colocación Sonda VesicalDiego Licetti Valencia0% (1)
- Clave AzulDocument11 paginiClave AzulHeidy Montero LaraÎncă nu există evaluări
- Psicosis en La Segunda InfanciaDocument43 paginiPsicosis en La Segunda InfanciaJulio ArmendarizÎncă nu există evaluări
- Terapia Manual OrtopédicaDocument8 paginiTerapia Manual Ortopédicaanon_569746210100% (1)
- Diptico Alimentacion Por SondaDocument2 paginiDiptico Alimentacion Por SondaRosamaria Silva Henriquez100% (1)
- Casos Heridas 2015-10Document7 paginiCasos Heridas 2015-10mayraÎncă nu există evaluări
- Recomendaciones para La Atención de Intoxicaciones Por Opioides 2022Document4 paginiRecomendaciones para La Atención de Intoxicaciones Por Opioides 2022Carla CifuentesÎncă nu există evaluări
- Taller Sobre El Desarrolo Fisico y Cognitivo en La Edad Adulta TempranaDocument2 paginiTaller Sobre El Desarrolo Fisico y Cognitivo en La Edad Adulta Tempranaebanisteriaalian bodegaprincipalÎncă nu există evaluări
- Quiz Semana 3Document7 paginiQuiz Semana 3Alejo Correa RestrepoÎncă nu există evaluări
- Guia de Buenas Practicas en Enfermeria. Valoracion y Manejo de Ulceras Del Pie Diabetico. 2011Document119 paginiGuia de Buenas Practicas en Enfermeria. Valoracion y Manejo de Ulceras Del Pie Diabetico. 2011Lucinia EspinozaÎncă nu există evaluări
- AIEPI CapurroDocument60 paginiAIEPI CapurroGloriaflores100% (2)
- Glosario OrtopediaDocument14 paginiGlosario OrtopediaValentina GarciaÎncă nu există evaluări
- Desequilibrio HidroelectroliticoDocument46 paginiDesequilibrio Hidroelectroliticoipseg0% (1)
- Examen Preguntas y RespuestasDocument27 paginiExamen Preguntas y RespuestasanablllÎncă nu există evaluări
- Malformaciones Anorrectales. LibroDocument22 paginiMalformaciones Anorrectales. LibroSizy Elizabeth Mesa EscalonaÎncă nu există evaluări
- Cirugia HBP La FeDocument10 paginiCirugia HBP La FeGustavo UriondoÎncă nu există evaluări
- Folleto de CitologiaDocument8 paginiFolleto de CitologiaingridÎncă nu există evaluări
- Clasificación de AtlantaDocument1 paginăClasificación de AtlantaHumberto Gmz De SantiagoÎncă nu există evaluări
- Herramientas Savia SaludDocument4.321 paginiHerramientas Savia SaludPracticante San JuanÎncă nu există evaluări
- Cap 13 Enfermedad Mixta Del Tejido ConectivoDocument10 paginiCap 13 Enfermedad Mixta Del Tejido ConectivoAbygail RH100% (1)
- Patologia Genital MasculinoDocument12 paginiPatologia Genital MasculinoESTELA JORDAN LOPEZÎncă nu există evaluări
- Convocatoria 2018-2019Document10 paginiConvocatoria 2018-2019JoseLainezÎncă nu există evaluări
- El Amor No Es para Siempre Walter RisoDocument19 paginiEl Amor No Es para Siempre Walter RisoCarlos Andres Gomez ValenciaÎncă nu există evaluări
- Historia AntonioDocument2 paginiHistoria Antonioz9hz4vmqdqÎncă nu există evaluări
- Caso Centro de Neurorrehabilitación Infantil SanasaninDocument4 paginiCaso Centro de Neurorrehabilitación Infantil SanasaninLUCIANO NICOLA CLAVERIEÎncă nu există evaluări
- Capacitacion - EFE S y PFA - 14 - 08 - 2020Document5 paginiCapacitacion - EFE S y PFA - 14 - 08 - 2020Betty Garcia HernándezÎncă nu există evaluări