Documente Academic
Documente Profesional
Documente Cultură
Exam 204-B. Química
Încărcat de
BybyAna ArellanoDescriere originală:
Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Exam 204-B. Química
Încărcat de
BybyAna ArellanoDrepturi de autor:
Formate disponibile
INSTITUTO TECNOLÓGICO
SUPERIOR DE HUATUSCO
Tipo de Instrumento de Evaluación:
Opción: Primera Oportunidad ( X ) Segunda Oportunidad ( )
Tiempo de evaluación Asignatura: : QUÍMICA. AEC-1058 Tema: Unidad I.- Teoría cuántica y estructura atómica
Carrera INGENIERÍA EN SISTEMAS COMPUTACIONALES. Hoja: 1 de 2
Nombre del Alumno(a): Grupo: Fecha de aplicación: Calificación:
204-B 28 DE MARZO /2020
I.- Seleccione falso o verdadero según la pregunta (Valor 5% cada respuesta
1.- Se del Hablo del Átomo por primera vez 450 años A.C. con Demócrito y (verdadero)
John Daltón en 1812.
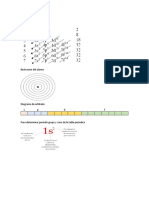
2.-El Átomo en química y física, es la unidad más pequeña de un elemento
(verdadero)
Químico que mantiene su identidad o sus propiedades y que no es posible dividir
mediante procesos químicos
3.-El Electrón es una partícula elemental cuya carga es positiva, en la ( falso )
mayoría de los casos, es el constituyente esencial de la corriente eléctrica.
4.- Valencia, Es la cantidad de electrones que puede ganar o perder ( verdadero )
un elemento en una combinación química.
5.-Los rayos catódicos son corrientes de electrones observados
( verdadero )
en tubos de vacío,es decir los tubos de cristal que se equipan por lo
menos con dos electrodos
6.- Un cátodo es un (electrodo negativo) ( verdadero )
7.- Un ánodo es un (electrodo negativo) ( falso
)
8.- La radioactividad es la emisión de energía por la desintegración
( verdadero )
de núcleos de átomos inestables. La energía emitida son partículas con carga
eléctrica u onda electromagnética
Elaboró: Vo.Bo.
M.C. GENARO TORRES ANTONIO
M.E. IRMA VALLEJO SARTORIUS
JEFE DE DIVISIÓN DE CIENCIAS BÁSICAS
INSTITUTO TECNOLÓGICO
SUPERIOR DE HUATUSCO
Tipo de Instrumento de Evaluación:
Opción: Primera Oportunidad ( X ) Segunda Oportunidad ( )
Tiempo de evaluación Asignatura: : QUÍMICA Tema: Unidad I.- Teoría cuántica y estructura atómica
AEC-1058
Carrera INGENIERÍA EN SISTEMAS COMPUTACIONALES. Hoja: 1 de 2
Nombre del Alumno(a): Grupo: Fecha de aplicación: Calificación:
204-B 28 DE MARZO /2020
II.- RELACIONA LA COLUMNA DE LA IZQUIERDA CON LA DE LA DERECHA Y ESCRIBE EN EL PARENTESIS,
El NUMERO QUE CORRESPONDA LA RESPUESTA CORRECTA. ( valor 5% c/u)
1.- Es imposible que dos electrones de un mismo átomo tengan los mismos valores en los ( 11 ) JOSEPH
cuatro números cuánticos: Principio de exclusión JOHN THOMSON
2.- Descubrió los protones y propuso un modelo atómico cuyas orbitas semejan el sistema ( 4 ) NIELS
planetario BOHR
3.- Establece que la emisión y absorción de energía es a través de paquetes de energía ( 6 )
denominados “cuantos”: CHADWICK
4.- Estableció que los electrones giran alrededor del núcleo y que cuando un electrón pasa de ( 2 )
una órbita interna a una externa la diferencia de energía se emite en forma de radiación. RUTHERFORD
Utilizando el modelo atómico para el átomo de hidrogeno.
5.- la función de Y² en el valor de la función de onda asociada con una partícula en movimiento ( 10 ) HUND
está relacionada con la probabilidad de encontrar a la partícula en el punto (x,y,z) en el instante
de tiempo t “ y velocidad. Por medio de modelos matemáticos.
6.- Descubrió los neutrones ( 9 ) ALBERT
EINSTEN
7.- Es imposible medir simultáneamente de forma precisa la posición y el momento lineal de una ( 3 ) MAX
partícula, como un electrón: Formulo el principio de incertidumbre PLANCK
8.- ¿De quién es el principio de construcción o del serrucho, Principio de mínima energía o ( 1 ) PAULI
principio de edificación progresiva?
9.- El efecto fotoeléctrico por quién fue .observado, y explica que la emisión de energía ( 7 )
sobre una placa metálica provoca la existencia de partículas llamadas fotones. HEISEMBERG
10.- La configuración electrónica más estable es la que se representa a través de espines ( 12 )
paralelos y es la regla de la máxima multiplicidad. SOMMERTIELD
11.- descubrió unas partículas con propiedades sorprendentes: prácticamente no tenían masa ( 5 )
y tenían carga eléctrica negativa. Las llamó Electrones (pudin de pasas.) SCHRODINGER
12.- Modifico la teoría atómica de Bohr y definió que los electrones podían ser circulares o ( 6 )
elípticas. Introdujo el número cuántico azimutal (l) AUFBAU
Biblliografia: Chang 2004. Química. - Brown, T. L. Y Le May, H. E. Química: La Ciencia Central Ed. Prentice-Hal
Elaboró: Vo.Bo.
M.C. GENARO TORRES ANTONIO
M.E. IRMA VALLEJO SARTORIUS
JEFE DE DIVISIÓN DE CIENCIAS BÁSICAS
S-ar putea să vă placă și
- Taller de Alcanos 2Document1 paginăTaller de Alcanos 2Nubia GutierrézÎncă nu există evaluări
- Taller de Enlace Quimico H H GDocument11 paginiTaller de Enlace Quimico H H GJULLY MARCELA PACHON HUERTASÎncă nu există evaluări
- Distribución ElectrónicaDocument30 paginiDistribución Electrónicapaul reyna100% (1)
- Tema 2 GlúcidosDocument54 paginiTema 2 GlúcidosVanessa Castillo PauliniÎncă nu există evaluări
- La GeografiaDocument4 paginiLa GeografiauserÎncă nu există evaluări
- Guia de Actividades 3. Compuestos Oxigenados PDFDocument6 paginiGuia de Actividades 3. Compuestos Oxigenados PDFenmanuel carrascoÎncă nu există evaluări
- Uniones QuímicasDocument15 paginiUniones QuímicasFelipe Alejandro JaraÎncă nu există evaluări
- ElectronegatividadDocument3 paginiElectronegatividadgdcs19Încă nu există evaluări
- 11 Quimica Del Carbono (2) IsomeriaDocument30 pagini11 Quimica Del Carbono (2) Isomeriajose sepulvedaÎncă nu există evaluări
- Taller 1 Resuelto PDFDocument14 paginiTaller 1 Resuelto PDFAngel HoyosÎncă nu există evaluări
- Seminario N°5 - Fuerzas Intermoleculares - Problemas ResueltosDocument9 paginiSeminario N°5 - Fuerzas Intermoleculares - Problemas ResueltosPatricio AlmadaÎncă nu există evaluări
- Quimica para Curso para Examen de Admisión de Facultad de Ciencias QuímicasDocument33 paginiQuimica para Curso para Examen de Admisión de Facultad de Ciencias QuímicasHector Aguilar LopezÎncă nu există evaluări
- Guia de Uniones QuimicasDocument2 paginiGuia de Uniones QuimicasMariel CáceresÎncă nu există evaluări
- Regla Del OctetoDocument27 paginiRegla Del Octetostigma subs ;;Încă nu există evaluări
- Temario BiologiaDocument3 paginiTemario BiologiaCésar Ortiz BravoÎncă nu există evaluări
- Enlace CovalenteDocument2 paginiEnlace CovalenteFrancisca OlivaresÎncă nu există evaluări
- 2 - Mini Cartilla - Alqueno Si PDFDocument3 pagini2 - Mini Cartilla - Alqueno Si PDFLizeth Condori100% (1)
- 1° - Química - I - Ii BimDocument57 pagini1° - Química - I - Ii BimSami Galicia Mendez100% (1)
- Plan de Mejora Grado 8°1 Ciencias Naturales Periodo DosDocument3 paginiPlan de Mejora Grado 8°1 Ciencias Naturales Periodo DosAnonymous oHIjyPgÎncă nu există evaluări
- Evaluacion de QuimicaDocument4 paginiEvaluacion de Quimicamprm2579Încă nu există evaluări
- Evaluación Formativa-Modelos Atómicos ProcesoDocument5 paginiEvaluación Formativa-Modelos Atómicos ProcesoYerti Letelier100% (1)
- Taller Compuestos Nitrogenados Grado Once Iete 2017Document2 paginiTaller Compuestos Nitrogenados Grado Once Iete 2017Diana Carolina Burbano Ruano50% (2)
- Actividades Repaso Unidad 2Document4 paginiActividades Repaso Unidad 2Carolina100% (1)
- GUÍA 1 Química 2do BGUDocument12 paginiGUÍA 1 Química 2do BGUbyit s5Încă nu există evaluări
- Cuestionario Enlace QuimicoDocument3 paginiCuestionario Enlace QuimicoCynthia100% (4)
- Planificacion CCNN 10mo 2do TrimestreDocument9 paginiPlanificacion CCNN 10mo 2do TrimestreMARIA DOLORES SALAZAR TOVAR100% (1)
- Guia QuimicaDocument20 paginiGuia Quimicali_t23Încă nu există evaluări
- Conversion PPM A ImecaDocument4 paginiConversion PPM A ImecaLOKI WOLF100% (1)
- GUIA 03 Al 07 de Abril BIOLOGIADocument15 paginiGUIA 03 Al 07 de Abril BIOLOGIAGladys AmaguayaÎncă nu există evaluări
- Guia de Aprendizaje Decimo-Enlace QuimicoDocument3 paginiGuia de Aprendizaje Decimo-Enlace QuimicoISABELA CORREDINÎncă nu există evaluări
- EXAMEN FINAL-2 (Con Respuestas)Document10 paginiEXAMEN FINAL-2 (Con Respuestas)Isabel de RoÎncă nu există evaluări
- CIRCULACIONDocument3 paginiCIRCULACIONwendy dayanna barrios caicedoÎncă nu există evaluări
- Guìa de Repaso Sistemas MaterialesDocument3 paginiGuìa de Repaso Sistemas Materialesbelenrosa73100% (3)
- Examen Mensual de Quimica 5toDocument2 paginiExamen Mensual de Quimica 5toJavier Rojas FranciaÎncă nu există evaluări
- Guía de Estudio Números Cuánticos y Configuración ElectrónicaDocument3 paginiGuía de Estudio Números Cuánticos y Configuración ElectrónicaFrancisco Alejandro Valenzuela Marquez100% (1)
- Diapositiva Modelos AtomicosDocument16 paginiDiapositiva Modelos AtomicosDaniel Salamanca100% (1)
- Guía Modelos AtómicosDocument2 paginiGuía Modelos AtómicosLisi Gómez100% (1)
- Cantidad de Sustancia. El Mol (Resumen)Document13 paginiCantidad de Sustancia. El Mol (Resumen)lazaroclaudiaÎncă nu există evaluări
- Guia de ActividadesDocument1 paginăGuia de ActividadesMaria GracielaÎncă nu există evaluări
- Biologia 3 Eso BiomoleculasDocument4 paginiBiologia 3 Eso BiomoleculaschamakitoÎncă nu există evaluări
- Trabajo NDocument4 paginiTrabajo NDiego CardozoÎncă nu există evaluări
- Proyecto Interdisciplinario 3ro Bgu GeneralDocument28 paginiProyecto Interdisciplinario 3ro Bgu GeneralFatima SornozaÎncă nu există evaluări
- Trabajo 4Document10 paginiTrabajo 4RogerÎncă nu există evaluări
- Electrostática Secundaria 8334Document44 paginiElectrostática Secundaria 8334Eduardo Robles OlivasÎncă nu există evaluări
- Guía 6. Enlace QuímicoDocument3 paginiGuía 6. Enlace QuímicoLuis JoséÎncă nu există evaluări
- Configuracion Electronica PDFDocument2 paginiConfiguracion Electronica PDFAlexandra ChavarroÎncă nu există evaluări
- Taller Nomenclatura de Alquenos, Alquinos y AromáticosDocument4 paginiTaller Nomenclatura de Alquenos, Alquinos y AromáticosneespinelÎncă nu există evaluări
- Tema de Numeros CuanticosDocument11 paginiTema de Numeros CuanticosZeta SeiÎncă nu există evaluări
- ACELERACIONDocument61 paginiACELERACIONClodomiro Jara QuispicusiÎncă nu există evaluări
- Introduccion A La Quimica, Materia, EnergiaDocument6 paginiIntroduccion A La Quimica, Materia, EnergiaAlex Alfaro TorresÎncă nu există evaluări
- Actividadessobreestructuracelular1 120318122717 Phpapp02Document6 paginiActividadessobreestructuracelular1 120318122717 Phpapp02ceceort50% (2)
- Quincena 7Document29 paginiQuincena 7william BarreraÎncă nu există evaluări
- Actividad. Ciencias N. Teoria Atomica ModernaDocument5 paginiActividad. Ciencias N. Teoria Atomica ModernaSebastián Garcia Mosquera100% (1)
- La Primer Ley de Mendel para Cuarto de SecundariaDocument7 paginiLa Primer Ley de Mendel para Cuarto de SecundariaJohanValleIngaÎncă nu există evaluări
- Estructura Atomica Energia CuanticaDocument24 paginiEstructura Atomica Energia Cuanticacarlos torresÎncă nu există evaluări
- Prueba El Atomo 1Document3 paginiPrueba El Atomo 1Johanna MuñozÎncă nu există evaluări
- 3° Evaluacion 2° CienciasDocument3 pagini3° Evaluacion 2° CienciasVIVIANA RIVERA VALENZUELAÎncă nu există evaluări
- 3° Evaluacion 2° CienciasDocument3 pagini3° Evaluacion 2° CienciasEncomiendas El SherpaÎncă nu există evaluări
- CUESTIONARIO PREVIO PRACTICA #2 Uriarte Ortiz Enrique YahirDocument3 paginiCUESTIONARIO PREVIO PRACTICA #2 Uriarte Ortiz Enrique YahirYayo UrÎncă nu există evaluări
- Registro de TareasDocument1 paginăRegistro de TareasBybyAna ArellanoÎncă nu există evaluări
- 7 de OctubreDocument5 pagini7 de OctubreBybyAna ArellanoÎncă nu există evaluări
- 4 de NoviembreDocument1 pagină4 de NoviembreBybyAna ArellanoÎncă nu există evaluări
- Encuesta para PadresDocument1 paginăEncuesta para PadresBybyAna ArellanoÎncă nu există evaluări
- Evaluacion EspañolDocument2 paginiEvaluacion EspañolBybyAna ArellanoÎncă nu există evaluări
- Examen 1roDocument14 paginiExamen 1roBybyAna ArellanoÎncă nu există evaluări
- Examen Del Primer TrimestreDocument21 paginiExamen Del Primer TrimestreBybyAna ArellanoÎncă nu există evaluări
- ESPANOLDocument26 paginiESPANOLBybyAna ArellanoÎncă nu există evaluări
- Rubrica TerceroDocument2 paginiRubrica TerceroBybyAna ArellanoÎncă nu există evaluări
- Unidad Ii Tabla Periodica.l.Document34 paginiUnidad Ii Tabla Periodica.l.BybyAna ArellanoÎncă nu există evaluări
- Rubrica de Evaluación La MayusculaDocument1 paginăRubrica de Evaluación La MayusculaBybyAna Arellano100% (3)
- Ficha Individual AcumulativaDocument4 paginiFicha Individual AcumulativaBybyAna ArellanoÎncă nu există evaluări
- CartaDocument1 paginăCartaBybyAna ArellanoÎncă nu există evaluări
- MATEMATICASDocument33 paginiMATEMATICASBybyAna ArellanoÎncă nu există evaluări
- Plan de IntervenciónDocument2 paginiPlan de IntervenciónBybyAna ArellanoÎncă nu există evaluări
- Rubrica de Evaluación Del Uso Del PuntoDocument1 paginăRubrica de Evaluación Del Uso Del PuntoBybyAna Arellano100% (1)
- Rubrica de Evaluación La MayusculaDocument1 paginăRubrica de Evaluación La MayusculaBybyAna Arellano100% (3)
- Caratula PlaneacionDocument1 paginăCaratula PlaneacionBybyAna ArellanoÎncă nu există evaluări
- Definición de PolinomioDocument2 paginiDefinición de PolinomioBybyAna ArellanoÎncă nu există evaluări
- Cómo Usar Correctamente El PuntoDocument5 paginiCómo Usar Correctamente El PuntoBybyAna ArellanoÎncă nu există evaluări
- 10 Cortometrajes para Educar en Valores A Los NiñosDocument3 pagini10 Cortometrajes para Educar en Valores A Los NiñosBybyAna ArellanoÎncă nu există evaluări
- DISCURSODocument2 paginiDISCURSOBybyAna ArellanoÎncă nu există evaluări
- Desarrollo Cuerpos Geométricos Primaria PDFDocument14 paginiDesarrollo Cuerpos Geométricos Primaria PDFBybyAna ArellanoÎncă nu există evaluări
- Mecanica de Materiales Investigacion Del TemarioDocument38 paginiMecanica de Materiales Investigacion Del TemarioEleazar SantiagoÎncă nu există evaluări
- Como Se Puede Ver Con Un Espejo Detras de Una EsquinaDocument2 paginiComo Se Puede Ver Con Un Espejo Detras de Una EsquinajÎncă nu există evaluări
- Ejercicios EBAUDocument4 paginiEjercicios EBAURaquel Martinez HernandezÎncă nu există evaluări
- Geometria EspacialDocument8 paginiGeometria Espacialkatherine letelierÎncă nu există evaluări
- Oa6 SeptimoDocument2 paginiOa6 Septimojose felipeÎncă nu există evaluări
- Iyc - #528 - Septiembre 2020 - PreviewDocument12 paginiIyc - #528 - Septiembre 2020 - PreviewJuve600% (1)
- SCIU-154 - Entregable 01 Fisica y QuimicaDocument6 paginiSCIU-154 - Entregable 01 Fisica y QuimicaTheUnicornAndTheDragonÎncă nu există evaluări
- Diagrama 2Document1 paginăDiagrama 2García Castillo Yajaira AdareliÎncă nu există evaluări
- Transportes III - Unidad 2 Clase 9Document26 paginiTransportes III - Unidad 2 Clase 9JIMÎncă nu există evaluări
- Fprodfiltres Spi - (Esv2) 1608Document4 paginiFprodfiltres Spi - (Esv2) 1608Juan Esteban SeguelÎncă nu există evaluări
- Tab 02 - Estallido, Colapso y TensiónDocument14 paginiTab 02 - Estallido, Colapso y Tensiónjackson labordeÎncă nu există evaluări
- Informe Pavimentos - FinalDocument65 paginiInforme Pavimentos - FinalPAOLA NINOSKA SANTA CRUZ CARRASCOÎncă nu există evaluări
- Informe3 M3 HuillcagarciarodrigoDocument7 paginiInforme3 M3 HuillcagarciarodrigoAlexis PerezÎncă nu există evaluări
- Libros de Texto Ies Gabriela Mistral 22 - 23 - Definitivo 2Document11 paginiLibros de Texto Ies Gabriela Mistral 22 - 23 - Definitivo 2xdÎncă nu există evaluări
- Documento Final. Tesis Sobrecapas.Document204 paginiDocumento Final. Tesis Sobrecapas.Ricardo ReyesÎncă nu există evaluări
- Actividad 4Document8 paginiActividad 4Raúl Núñez GonzálezÎncă nu există evaluări
- Guía de Trabajo No 4 - IParcial - 2023 - I BCHDocument3 paginiGuía de Trabajo No 4 - IParcial - 2023 - I BCHLauren HernándezÎncă nu există evaluări
- Examen Parcial Diplomado NanotecnologíaDocument4 paginiExamen Parcial Diplomado NanotecnologíaKathe MellizoÎncă nu există evaluări
- NC Ra2 201Document12 paginiNC Ra2 201javier vargasÎncă nu există evaluări
- Clase 6 Hormigón ArmadoDocument21 paginiClase 6 Hormigón ArmadoCarlos Arias MuñozÎncă nu există evaluări
- Sílabo Introducción A La Ciencias SocialesDocument24 paginiSílabo Introducción A La Ciencias SocialesVíctor ZamoraÎncă nu există evaluări
- MOLDEDocument14 paginiMOLDEGustavo García SánchezÎncă nu există evaluări
- ARTICULO CIENTIFICO JOSELO - en ProcesoDocument17 paginiARTICULO CIENTIFICO JOSELO - en ProcesoGabriel Panduro ContrerasÎncă nu există evaluări
- 2021-11-02 M2online Práctica FADUDocument51 pagini2021-11-02 M2online Práctica FADUNacho SchmittÎncă nu există evaluări
- Trabajo de SoldaduraDocument9 paginiTrabajo de SoldaduraLorena ValentinaÎncă nu există evaluări
- Ce Anejo 30 Mixtas Bases Diseño Generales y EdificacionDocument113 paginiCe Anejo 30 Mixtas Bases Diseño Generales y EdificacionElena Collazos GonzálezÎncă nu există evaluări
- Parcial 4 Algebra Lineal OficioDocument2 paginiParcial 4 Algebra Lineal OficioANA MARÍA. HERNÁNDEZ LÓPEZÎncă nu există evaluări
- Horario Programa Ingenieria Civil Por Ciclo Propedeuticos Sem B 2023Document7 paginiHorario Programa Ingenieria Civil Por Ciclo Propedeuticos Sem B 2023Juan MendezÎncă nu există evaluări
- Transferencia de CalorDocument4 paginiTransferencia de Caloroilkgas31Încă nu există evaluări
- Práctico 2 - Propiedades Sustancia PuraDocument2 paginiPráctico 2 - Propiedades Sustancia PuraBrayan SilveraÎncă nu există evaluări