Documente Academic
Documente Profesional
Documente Cultură
Lab1 Diagrama de Pourbaix
Încărcat de
Maria JoseDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Lab1 Diagrama de Pourbaix
Încărcat de
Maria JoseDrepturi de autor:
Formate disponibile
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Laboratorio n°1
Diagramas de Pourbaix
Profesores: Flavia Leiva
Pedro Muñoz
Ayudante: Evelyn Reyes
Integrantes: Felipe Cancino
María José Carrasco
Felipe Echeverría
Daniela Jara
Ariel Sanhueza
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Introducción
En la minería, para el tratamiento de minerales metálicos extraídos de los yacimientos, se
cuenta con una herramienta pionera en Chile, que lo llevó a posicionarse en el mundo
como una potencia minera, que es la hidrometalurgia. Esta rama metalúrgica permite la
extracción y recuperación de las especies metálicas mediante medios físico-químicos.
En general, el desarrollo de la hidrometalurgia se realiza en tres etapas físico-químicas
secuenciales: etapa de disolución selectiva de los metales desde los sólidos que los
contienen mediante una solución acuosa, conocida como lixiviación; etapa de
procesamiento y transformación de los metales disueltos en el medio acuoso de lixiviación
mediante agentes externos que permiten la purificación y/o concentración de estos
metales; etapa de recuperación selectiva de los metales disueltos en el medio acuoso
conocido como precipitación con el objetivo de obtener un metal de forma sólida.
El presente informe se abordarán conceptos para la primera etapa de disolución. Al tener
un metal interactuando con un medio en solución, es requerido conocer las regiones de
estabilidad termodinámica para tener una referencia del comportamiento de este en el
medio. Es por esto, que surgieron diagramas que relacionan tanto el potencial de voltaje y
el pH de la solución, variable que permiten establecer gráficamente la estabilidad del
metal, denominados diagramas de Pourbaix.
Pudiendo establecer un diagrama para cada metal deseado, se encarga en el presente
trabajo confeccionar los diagramas para los siguientes metales: Oro y Plata. A partir de
esto, se realizará un análisis en primera instancia de cada elemento que se obtiene al
interactuar el metal con la solución acuosa y su reacción química asociada, para tener las
ecuaciones necesarias para la construcción del diagrama, utilizando las ecuaciones de
Nerts y las constantes de equilibrio.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Marco teórico
Como se mencionó, la construcción del diagrama se hace a partir de la ecuación de
Nernst:
RT actividad reactivos
Eth =E +
0
nF
∗2.3 log (
actividad productos )
pH=−log ¿
−∆ G°
E0 =
nF
Dependiendo de los electrones y protones intercambiados, se pueden obtener 4 tipos de
soluciones para graficar posteriormente en el diagrama de Pourbaix.
Tomando una reacción de la forma:
−¿¿
aA +c H 2 O ↔bB+ m H +¿+n e ¿
Tipo 1. Reacción electroquímica con electrones y protones
RT
Eth =E 0+ ∗2.3 log ¿
nF
Tipo 2. Reacción electroquímica con electrones y sin protones
RT A a∗H 2 O c 0 RT Aa
Eth =E 0+
nF
∗2.3 log ( B
b
→ E th )
=E +
nF
∗2.3 log
B
b ( )
Tipo 3. Reacción química sin electrones y con protones
−∆ G ° RT
Eth = + ∗2.3 log ¿
nF nF
−∆ G ° A a∗H 2 Oc
Aa∗H 2 Oc 2.3 RT
−log
Bb ( )
0=−∆ G ° +2.3 RT∗ log
( (
Bb
+ m∗pH → pH= ) m)
Tipo 4. Reacción química sin electrones ni protones
A a∗H 2 Oc
0=−∆ G ° +2.3 RT∗log
Bb ( )
Para efectos del diagrama de Pourbaix no se considerarán las ecuaciones del tipo 4.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Desarrollo
Diagrama de Pourbaix
Definir en qué consiste un diagrama de Pourbaix, para qué sirve, qué contiene y
cómo se construye
El diagrama de Pourbaix es una representación gráfica de la termodinámica en sistemas
acuosos mediante el potencial y el pH y así predecir los estados más estables de un
metal. El equilibrio termodinámico del sistema se representa obteniendo todas las
reacciones electroquímicas que experimentan las especies mediante la constante de
equilibrio y la ecuación de Nernst.
Los sistemas Metal-Agua permiten comparar los efectos de las zonas de inmunidad,
corrosión y pasividad. Para la hidrometalurgia estos diagramas permiten conocer las
condiciones y las zonas que es posible lixiviar los minerales.
Diagrama del oro
Las especies iónicas y neutras que se encuentran estables a una temperatura ambiente
de 25°C y que actúan en la reacción son las siguientes:
Tabla 1 Parámetros termodinámicos del Oro
Especie n° de oxidación Estado Energía Libre de Gibbs [kJoule]
Au 0 sólida 0
Au2 O3 3 sólida 163.176
AuO2 4 sólida 200.83
+¿¿
Au 1 Acuosa 163.176
Au3+¿¿ 3 Acuosa 433.4624
H 3 Au O 3 3 Acuosa -258.5712
3−¿¿
H 3 Au O 3 3 Acuosa -191.6272
HAu O 32−¿¿ 3 Acuosa -115.4784
AuO33−¿¿ 3 Acuosa -24.2672
H2O - Líquida -237.232
+¿¿
H - Acuosa -
Las reacciones balanceadas se presentan en la tabla a continuación:
Tabla 2 Reacciones y especies para el Oro
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
N° reacción Especies involucradas Reacción
+ ¿¿
Au3+¿+3 H O ↔ H 3 Au O3+3 H
1 Au3+¿/ H Au O3 ¿
3 2 ¿
+¿ ¿
H 3 Au O3 /H 2 AuO3−¿ ¿ H 3 Au O 3 ↔ H 2 AuO3−¿+ H ¿
2
+¿ ¿
2−¿ ¿ 2−¿+ H ¿
H 2 Au O3−¿/ HAu O H 2 Au O 3−¿↔ HAu O
¿ ¿
3 3 3
+¿ ¿
3−¿¿ 3−¿+ H ¿
HAu O 32−¿/ Au O HAu O 32−¿↔ Au O
¿ ¿
4 3 3 3 3
−¿ ¿
3+ ¿¿ 3+ ¿+ 2e ¿
5 Au+¿/ Au Au+¿↔ Au
¿ ¿
−¿ ¿
+ ¿+ 2 e ¿
Au+¿/ H Au O3 ¿
Au+¿+ 3 H O ↔ H 3 Au O3 +3 H
6 3 2 ¿
−¿ ¿
−¿¿ +¿ +2e ¿
Au+¿/ H Au O3 +¿+ 3 H 2 O ↔ H 2 Au O3−¿+ 4 H ¿
7 2 ¿
Au
¿
−¿ ¿
2−¿¿ +¿ +2e ¿
+¿+ 3 H 2 O ↔ HAuO 32−¿+ 5 H
Au+¿/ HAuO ¿
¿
8 3
Au
¿
−¿¿
Au/ Au2 O 3 2 Au+3 H 2 O↔ Au2 O3+ 6 H +¿+6 e ¿
9
−¿¿
Au2 O3 /2 Au O2 Au2 O 3 + H 2 O ↔ 2 AuO 2 +2 H +¿+2 e ¿
10
+¿ ¿
11 2 Au3 +¿/ Au O ¿ 2 3
2 Au3 +¿+3 H O ↔ Au O + 6 H ¿
2 2 3
12 Au2 O3 / H 3 Au O3 Au2 O3 +3 H 2 O ↔2 H 3 Au O3
+¿ ¿
Au2 O 3 / H 2 Au O 3−¿¿ Au2 O 3 +3 H 2 O ↔2 H 2 Au O 3−¿+2 H ¿
13
+ ¿¿
Au2 O 3 / HAu O 32−¿¿ Au2 O 3 +3 H 2 O ↔2 HAu O 32−¿+4 H ¿
14
−¿ ¿
15 Au/ Au+¿ ¿ Au↔ Au+¿+e ¿
−¿¿
16 Au/ Au3 +¿¿ Au↔ Au3 +¿+3 e ¿
−¿¿
Au/H 3 AuO 3 Au+ 3 H 2 O↔ H 3 Au O 3+ 3 H +¿+3 e ¿
17
−¿ ¿
+ ¿+ 3e ¿
Au/H 2 AuO3−¿ ¿ Au+ 3 H 2 O↔ H 2 Au O 3−¿+4 H ¿
18
−¿ ¿
+¿+ 3 e ¿
19 Au/HAu O32−¿ ¿ Au+ 3 H 2 O↔ HAu O32−¿+5 H ¿
−¿ ¿
+ ¿+ e ¿
20 Au3+¿/ AuO ¿ 2
Au3+¿+2 H 2 O ↔ AuO2 +4 H ¿
−¿¿
21 H 3 Au O 3 / Au O 2 H 3 Au O 3 ↔ Au O 2 + H 2 O+ H +¿+e ¿
−¿¿
H 2 Au O 3−¿↔ AuO +H O +e
H 2 Au O 3−¿/ Au O ¿
¿
22 2 2 2
−¿ ¿
+ ¿↔ Au O2 + H 2 O+ e ¿
23 HAu O32−¿/ Au O ¿ 2
HAu O32−¿+H ¿
Para la construcción del Diagrama de Pourbaix se obtendrán las ecuaciones para pH y
potencial de las 23 reacciones presentadas en la tabla XX:
+ ¿¿
1. Au3+¿+3 H 2 O ↔ H 3 Au O3+3 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
nF∗E th=−∆ G °+ 2.3 RT∗log¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
La actividad de H 2 O es igual a 1.
Como no hay intercambio de electrones n=0.
0=−∆ G ° +2.3 RT∗log¿
pH=−∆ G° +2.3 RT∗log ¿ ¿
−∆ G°
pH= + log¿ ¿
3∗2.3 RT
Reemplazando:
∆ G °=∆ G° H 3 Au O3 −¿
kJ
∆ G °=19.66 [ ] mol
2.3∗8.31
2.3∗R∗T = ∗298.15=5.70
1000
∆G°
=3.45
2.3 RT
Finalmente,
1
pH=−3.45+ ∗log ¿
3
+ ¿¿
−¿+H ¿
2. H 3 Au O 3 ↔ H 2 AuO 3
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
nF∗E th=−∆ G °+ 2.3 RT∗log¿
Como no hay intercambio de electrones n=0.
pH=−∆ G° +2.3 RT∗log ¿ ¿
−∆ G °
pH= + log ¿
2.3 RT
Reemplazando:
∆ G °=∆ G° H 2
−¿
Au O3 −∆ G °H Au O3 =−191.63− (−258.57 ) ¿
3
kJ
∆ G °=66.94 [ ] mol
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
−∆ G ° −66.94
= =−11.73
2.3 RT 2.48
Finalmente,
pH=11.73+ log ¿
+¿ ¿
2−¿+ H ¿
3. H 2 Au O 3−¿↔ HAu O 3 ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
nF∗E th=−∆ G °+ 2.3 RT∗log¿
Como no hay intercambio de electrones n=0.
pH=−∆ G° +2.3 RT∗log ¿ ¿
−∆ G °
pH= + log ¿
2.3 RT
Reemplazando:
∆ G °=∆ G° HAuO 3
2−¿
−∆ G ° H −¿
Au O 3 =−115.48− (−191.63 )¿
¿
2
kJ
∆ G °=76.15 [ ]
mol
2.3∗8.31
2.3∗R∗T = ∗298.15=5.70
1000
∆ G ° 76.15
= =13.36
2.3 RT 5.70
Finalmente,
pH=−13.36+ log ¿
+¿ ¿
3−¿+ H ¿
4. HAu O2−¿↔ AuO 3 ¿
3
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
nF∗E th=−∆ G °+ 2.3 RT∗log¿
Como no hay intercambio de electrones n=0.
pH=−∆ G° +2.3 RT∗log ¿ ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
−∆ G °
pH= + log ¿
2.3 RT
Reemplazando:
∆ G °=∆ G° Au O 3−¿
−∆ G °HAuO ¿
3 2−¿
3
=−24.27− (−115.48) ¿
kJ
∆ G °=91.21 [ ] mol
−∆ G ° −91.21
= =−16.00
2.3 RT 2.48
Finalmente,
pH=16.00+ log¿
−¿ ¿
3+ ¿+ 2e ¿
5. Au+¿↔ Au ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° Au 3+ ¿
− ∆ G °Au +¿ ¿
=433.46−163.18 ¿
kJ
∆ G °=47.41 [ ] mol
2.3 RT=5.70
nF=2∗96.485=192.97
∆ G° 47.41
= =1.40
nF 192.97
2.3 RT
=0.03
nF
Finalmente,
Eth =−1.40+ 0.03∗log ¿
−¿ ¿
+ ¿+ 2 e ¿
6. Au+¿+ 3 H 2 O ↔ H 3 Au O3 +3 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
La actividad de H 2 O es igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° H 3 Au O3 −¿
kJ
∆ G °=289.95 [ ]
mol
−∆ G 0 −289.95 kJ
0
E=
nF
=
−192.97
=1.50
C [ ]
2.3 RT 5.70
= =−0.03
nF −192.97
Finalmente,
Eth =1.50−0.03∗log ¿
−¿ ¿
+¿ +2e ¿
O ↔ H 2 Au O3−¿+ 4 H
7. Au+¿+ 3 H
¿
2
¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° H 2
Au O3−¿ −¿¿
kJ
∆ G °=356.89 [ ]
mol
−∆ G 0 −356.89 kJ
0
E=
nF
=
192.97
=−1.85
C [ ]
2.3 RT 5.70
= =0.03
nF 192.97
Finalmente,
Eth =−1.85+ 0.03∗log ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
+¿ +2e
−¿ ¿
¿
Laboratorio de Procesos Metalúrgicos
O ↔ HAuO 32−¿+ 5 H
8. Au+¿+ 3 H
¿
2
¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° HAuO 2−¿
−¿¿
3
kJ
∆ G °=433.04 [ ] mol
−∆ G 0 −2∗433.04 kJ
0
E=
nF
=
−192.97
=2.24
C [ ]
2.3 RT 5.70
= =−0.03
nF −192.97
Finalmente,
Eth =2.24−0.03∗log ¿
−¿¿
+¿+6 e ¿
9. 2 Au+3 H 2 O↔ Au2 O3+ 6 H
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au , Au2 O 3 y H 2 O igual a 1.
−∆ G ° 6∗2.3 RT
Eth = − ∗pH
nF nF
Reemplazando:
∆ G °=∆ G° Au O −3∗∆ G ° H O=163.18−3∗(−237.23 )
2 3 2
kJ
∆ G °=874.87 [ ] mol
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
−¿¿
+¿+2 e ¿
10. Au2 O 3 + H 2 O ↔ 2 AuO 2 +2 H
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 , Au O 2 y H 2 O igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2∗2.3 RT
Eth = − ∗pH
nF nF
Reemplazando:
∆ G °=2∗∆ G ° AuO −( ∆ G ° Au O + ∆ G° H
2 2 3 2 O )=2∗200.83−(163.18+ (−237.23 ) )
kJ
∆ G °=475.72 [ ]
mol
−∆ G 0 −475.72 kJ
0
E=
nF
=
−192.97
=2.47
C [ ]
2.3 RT 5.70
= =−0.03
nF −192.97
Finalmente,
Eth =2.47−0.06∗pH
+¿ ¿
11.2 Au3 +¿+3 H 2 O ↔ Au 2 O3+ 6 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
nF∗E th =−∆ G °+ 2.3 RT∗log¿
∆ G °=2.3 RT∗¿
∆G°
=−2 log¿
2.3 RT
−∆ G °
pH= −2 log¿ ¿
2.3 RT
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Reemplazando:
∆ G °=∆ G° Au O −¿
2 3
kJ
∆ G °=7.947 [ ]
mol
∆G°
=1.394
2.3 RT
Finalmente,
pH=0.69−3 log ¿
12. Au2 O 3 +3 H 2 O ↔2 H 3 Au O 3
Utilizando la ecuación de Nernst (ecuación XX):
3
[ Au2 O3 ]∗[ H 2 O ]
Eth =
−∆ G ° 2.3 RT
nF
+
nF
∗log
[ H 3 Au O3 ] (
2
)
Con la actividad de Au2 O 3 y H 2 O igual a 1.
−∆ G ° 2.3 RT −2
Eth = + ∗log ( [ H 3 AuO 3 ] )
nF nF
−2
nF∗E th=−∆ G °+ 2.3 RT∗log ( [ H 3 AuO 3 ] )
∆ G °=−2∗2.3 RT∗log ( [ H 3 AuO3 ])
−∆ G °
=log ( [ H 3 AuO 3 ] )
2∗2.3 RT
Reemplazando:
∆ G °=2∗∆ G ° H 3 Au O3 −( 3∗∆G ° H O + ∆ G° Au O )=2∗(−258.57 )−(163.18+3∗(−237.23 ) )
2 2 3
kJ
∆ G °=31.38 [ ]
mol
−31.38
=log ( [ H 3 Au O 3 ] )
11.40
log ( [ H 3 Au O3 ] ) =2.75
+ ¿¿
−¿+2 H ¿
13. Au2 O 3 +3 H 2 O ↔2 HAu O 3
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
nF∗E th=−∆ G °+ 2.3 RT∗log¿
∆ G °=2.3 RT∗¿
∆G°
=−2 log¿
2.3 RT
−∆ G °
pH= −2 log¿ ¿
2.3 RT
Reemplazando:
∆ G °=2∗∆ G ° HAu O 3
−¿
− (3∗∆ G ° H O+ ∆ G ° Au O )=2∗( −191.627) −(3∗(−237.23 ) +163.77)¿
2 2 3
kJ
∆ G °=165.265 [ ]
mol
∆G°
=28.986
2.3 RT
Finalmente,
pH=−14.493+ log¿
+ ¿¿
2−¿+4 H ¿
14. Au2 O 3 +3 H 2 O ↔2 HAu O 3
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
nF∗E th =−∆ G °+ 2.3 RT∗log¿
∆ G °=2.3 RT∗¿
∆G°
=−2 log¿
2.3 RT
−∆ G °
pH= −2 log¿ ¿
2.3 RT
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Reemplazando:
∆ G °=2∗∆ G ° HAu O 2−¿
− ( 3∗∆ G ° H O +∆ G ° Au O )=2∗( −115.48 )−(3∗(−237.23 ) +163.77)¿
3 2 2 3
kJ
∆ G °=317.56 [ ] mol
∆G°
=55.70
2.3 RT
Finalmente,
pH=13.92+0.5 log ¿
−¿ ¿
15. Au↔ Au+¿+e ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con [ Au ] igual a 0
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° Au +¿
−∆ G ° Au =163.18−0 ¿
kJ
∆ G °=163.18 [ ] mol
2.3 RT=5.70
nF=1∗96.485=96.485
∆ G° 163.18
= =1.692
nF 96.4857
2.3 RT
=0.0591
nF
Finalmente,
Eth =1.629+ 0.0591∗log ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
−¿¿
Laboratorio de Procesos Metalúrgicos
16. Au↔ Au3 +¿+3 e ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au igual a 0.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT
Eth = − ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° kJ
3+ ¿
Au − ∆ G °Au =433.46 [ ]
mol
¿
∆ G° 433.46
= =1.50
nF 3∗96.49
2.3 RT 5.70
= =0.02
nF 289.46
Finalmente,
Eth =−1.50−0.02∗log ¿
−¿¿
+¿+3 e ¿
17. Au+ 3 H 2 O↔ H 3 Au O 3+ 3 H
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT 3∗2.3 RT
Eth = − ∗log ( [ H 3 Au O 3 ]) − ∗pH
nF nF nF
Reemplazando:
kJ
∆ G °=∆ G° H 3 Au O3 −3∗∆ G° H O =453.125
2 [ ]
mol
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
∆ G° 453.125
= =1.565
nF 3∗96.49
2.3 RT 5.70
= =0.02
nF 289.46
Finalmente,
Eth =2.06−0.02∗log ( [ H 2 Au O3 ] ) −0.0591∗pH
−¿ ¿
+ ¿+ 3e ¿
18. Au+ 3 H 2 O↔ H 2 Au O 3−¿+4 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT
Eth = − ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° kJ
−¿
H2 Au O3 −3∗∆ G °H O =520.07
2 [ ]
mol
¿
∆ G° 520.07
= =1.80
nF 3∗96.49
2.3 RT 5.70
= =0.02
nF 289.46
Finalmente,
Eth =−1.80−0.02∗log ¿
−¿ ¿
+¿+ 3 e ¿
19. Au+ 3 H 2 O↔ HAu O 32−¿+5 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de Au2 O 3 y H 2 O igual a 1.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT
Eth = − ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° kJ
HAuO3
2−¿
−3∗∆ G ° H O=596.218
2 [ ]
mol
¿
∆ G° 520.07
= =2.06
nF 3∗96.49
2.3 RT 5.70
= =0.02
nF 289.46
Finalmente,
Eth =2.06−0.02∗log ¿
−¿ ¿
+ ¿+ e ¿
20. Au3+¿+2 H 2 O ↔ AuO2 +4 H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O y Au O 2 igual a 1.
−∆ G ° 2.3 RT
Eth = + ¿
nF nF
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° Au O −¿ 2
kJ
∆ G °=241.83 [ ]
mol
∆ G° 241.83
= =2.50
nF 1∗96.49
2.3 RT 5.70
= =0.06
nF 96.49
Finalmente,
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Eth =−2.50−0.06∗log ¿
−¿¿
+¿+e ¿
21. H 3 Au O 3 ↔ Au O 2 + H 2 O+ H
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O y Au O 2 igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT 2.3 RT
Eth = + ∗log ( [ H 3 AuO 3 ] ) − ∗log ¿
nF nF nF
Reemplazando:
∆ G °=∆ G° Au O +∆ G ° H O−∆ G° H
2 2 3 AuO3 =200.83−237.23−(−258.571 )
kJ
∆ G °=222.169 [ ] mol
∆ G° 222.169
= =2.302
nF −1∗96.49
2.3 RT 5.70
= =0.06
nF 96.49
Finalmente,
Eth =2.03−0.06∗Ph−0.06∗log ¿
−¿¿
−¿↔ AuO 2+H 2 O +e ¿
22. H 2 Au O 3
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O y Au O 2 igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Reemplazando:
∆ G °=∆ G° Au O +∆ G ° H O−∆ G° H
2 2 2
−¿
Au O3 =200.83−237.23− ( 191.63 ) ¿
kJ
∆ G °=155.23 [ ]
mol
∆ G° 155.23
= =1.61
nF 1∗96.49
2.3 RT 5.70
= =0.06
nF 96.49
Finalmente,
Eth =−1.61+0.06∗log ¿
−¿ ¿
+ ¿↔ Au O2 + H 2 O+ e ¿
23. HAu O32−¿+H ¿
Utilizando la ecuación de Nernst (ecuación XX):
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Con la actividad de H 2 O y Au O 2 igual a 1.
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
−∆ G ° 2.3 RT
Eth = + ∗log ¿
nF nF
Reemplazando:
∆ G °=∆ G° Au O +∆ G ° H O−∆ G° HAuO
2 2
2−¿
=200.83−237.23−( −115.478 ) ¿
3
kJ
∆ G °=79.076 [ ]
mol
∆ G° 79.076
= =0.82
nF 1∗96.49
2.3 RT 5.70
= =0.06
nF 96.49
Finalmente,
Eth =0.82−0.06∗log ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Para realizar el diagrama de Pourbaix se graficarán las ecuaciones obtenidas
anteriormente:
1
1. pH=−3.45+ ∗log ¿
3
2. pH=11.73+ log ¿
3. pH=−13.36+ log ¿
4. pH=16.00+ log ¿
5. Eth =−1.40+ 0.03∗log¿
6. Eth =1.50−0.03∗log ¿
7. Eth =−1.85+ 0.03∗log ¿
8. Eth =2.24−0.03∗log ¿
9. Eth =1.511−0.06∗pH
10. Eth =2.47−0.06∗pH
11. pH=0.69−3 log ¿
12. log ( [ H 3 Au O 3 ] ) =2.75
13. pH=−14.493+ log¿
14. pH=13.92+0.5 log ¿
15. Eth =1.629+ 0.0591∗log ¿
16. Eth =−1.50−0.02∗log ¿
17. Eth =2.06−0.02∗log ( [ H 2 Au O 3 ] ) −0.0591∗pH
18. Eth =1.797−0.02∗log ¿
19. Eth =2.06−0.02∗log ¿
20. Eth =2.50−0.06∗log ¿
21. Eth =2.03−0.06∗Ph−0.06∗log ¿
22. Eth =−1.61+0.06∗log¿
23. Eth =0.82−0.06∗log ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Se procede a graficar el diagrama de Pourbaix del oro, en la abscisa se posiciona el pH y
en la ordenada el Potencial eléctrico.
Figura 1 Ecuaciones para el oro según pH y potencial
Lo primero fue graficar las rectas que no dependían de la concentración (1 al 8) y luego se
borró las secciones de las rectas para que coincidieran entre sí, de tal forma que quede
clara las zonas de dominancia de estos.
A continuación, se graficaron el resto de las ecuaciones y se recortaron para que
concordara con las especies existentes. Además, en las zonas de corrosión se graficaron
las rectas a distintas concentraciones. Obteniéndose lo siguiente:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Diagrama de Pourbaix para Oro (Au).
3
2.8
2.6
2.4
2.2
2
1.8
1.6
1.4
1.2
1
0.8
0.6
0.4
0.2
E [V]
0
-0.2
-0.4
-0.6
-0.8
-1
-1.2
-1.4
-1.6
-1.8
-2
-2.2
-2.4
-2.6
-2.8
-3
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
ecu 1 ecu 2 PH ecu 5 ecu 6
ecu 7 ecu 8 ecu 9 ecu 10
ecu 11 ecu 14 ecu 15 ecu 16
ecu 17 ecu 18 ecu 19 ecu 20
ecu 21 ecu 22 ecu 23 ecu 3
ecu 20' ecu 11' ecu 16' ecu 16''
ecu 19' ecu 14' ecu 23' Agua a
agua b
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Figura 2 Diagrama de Pourbaix para el Oro
Primero hay que mencionar que el diagrama fue construido con la energía libre de Gibbs
del Óxido Aurico Anhidro Au2O3 que corresponde a la especie b de los parámetros
termodinámicos entregado, además hubo una ecuación que fue graficada en el diagrama
ya que estaban fuera del rango de 0 a 14 pH, la cual fue:
4. pH=16.00+ log¿
Por otra parte, hubo 2 casos importantes en que la recta que representa una reacción
pasa por sobre el área de predominio de otra especie, esto no significa que reacción no
ocurra, sólo que presenta un porcentaje de especie menor al 40%. Esta es una de las
desventajas que tiene este tipo de diagramas ya que no puede representar las especies
con porcentaje de existencia menor al 40%.
El primer caso que se encontró fue el del Au con su ion Au + y Au3+ ya que no hay una
clara división entre estos debido a que las ecuaciones que los involucran (5, 15 y 16)
quedan superpuestas en el diagrama, y en consecuencia el porcentaje de ocurrencia de
estos depende exclusivamente de la concentración de dicho compuesto ya que de esta
forma hace que la recta se desplace hacia arriba o hacia abajo. Lo anterior se presenta en
la siguiente figura:
Figura 3 Caso Au+ y Au3+
Y el segundo caso sucede con las ecuaciones 9, 10, 17 y 21, provocando que la especie
AuO2 ocurra solamente en un pequeño sector en vez de toda la zona:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Figura 4 Sector AuO2
Al analizar el diagrama se observa que la zona de corrosión es bastante estrecha y se
encuentra a valores de potencial muy altos, por el contrario, la zona de pasividad es
bastante ancha, la cual impide que el metal se disuelva.
Lo que implica que el oro es un elemento mucho más difícil de tratar en la hidrometalurgia
ya que indica una falta de reactividad, solo reacciona a potenciales altos en donde el agua
este oxidada.
Diagrama del aluminio
Al igual que en el caso del oro, las especies iónicas y neutras estables, están a una
temperatura ambiente de 25 °C.
Tabla 3 Parámetros termodinámicos del Aluminio
Energía Libre de
Especie n° de oxidación Estado
Gibbs [kcal/mol]
Al 0 Sólido 0
Al2 O 3 3 Sólido -384.53
Al2 O 3 3 Sólido -382.4
Al2 O 3 3 Sólido -378.31
Al2 O 3 3 Sólido -376.77
Al2 O 3 3 Sólido -373.73
Al3 +¿¿ 3 Acuoso -115
AlO−¿¿
2 3 Acuoso -200.71
H2O - Líquido -56.7
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
H +¿¿ - Acuoso -
Las reacciones en estado de reducción y las especies involucradas, son las siguientes:
Tabla 4 Reacciones en el sistema Aluminio-Agua
N° reacción Especies involucradas Reacción
3+ ¿+2 H O¿
3 +¿¿ 2
−¿/ Al ¿ H +¿↔ Al ¿
1 AlO 2 AlO−¿+4
2
¿
−¿↔ Al+ 3 H2 O ¿
2 Al2 O3 / Al Al2 O 3+ 6 H +¿+ 6 e ¿
3 Al2 O3 / Al 3+¿ ¿ Al2 O3+ 6 H +¿↔¿ 2 Al 3+¿+3 H O ¿ 2
+¿ ↔Al 2 O3 + H 2 O ¿
Al H
4 AlO−¿/
¿ O3 ¿ 2 AlO−¿+2
2
¿
−¿↔ Al¿
5 Al3 +¿/ Al ¿ Al3 +¿+3 e ¿
−¿ ↔ Al+2H O ¿
2
Al¿ H +¿+ 3e ¿
6 AlO−¿/
2 AlO−¿+4
2
¿
Para realizar la construcción del diagrama de Pourbaix, se calcula las ecuaciones para pH
y potencial de las 6 reacciones presentadas en la tabla XX.
3+ ¿+2 H O ¿
2
H +¿=Al ¿
Ecuación 1 AlO−¿+4
2
¿
+¿¿ −¿¿
La reacción química involucra H y no e , por lo que en el grafico será una línea
vertical.
Se calcula la energía libre de Gibbs de la siguiente manera:
0 0 0
∆ G =∑ ∆ G ( Productos )−∑ ∆ G ( Reactantes)
Kcal Kcal Kcal
∆ G 0 =−115 [ ] (
mol
+2 −56.7 )
mol
−(−200.71 )
mol [ ] [ ]
Kcal
∆ G0 =−27.69 [ ] mol
Se pasa las Kcal a KJ:
KJ
∆ G0 =−115.85 [ ]
mol
Se procede a calcular la fórmula de pH:
log ( k )=log ¿ ¿
log ( k )=log ¿ ¿
Ya que la concentración de [ H 2 O ] es 1, se puede eliminar de la ecuación:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
−∆ G 0
=log ¿ ¿
2.303 RT
Se acomoda la ecuación y se remplaza el ∆ G 0 :
log ¿ ¿
log ¿ ¿
log ¿ ¿
Remplazando los valores de concentración, se obtiene el valor de pH
pH=5.08
Ecuación 2
−¿= Al+ 3H 2 O ¿
Al2 O 3+ 6 H +¿+ 6 e ¿
+¿¿ −¿¿
La reacción química involucra H ye , por lo que en el grafico será una diagonal.
El cálculo de la energía libre de Gibbs se realiza de la siguiente manera:
∆ G 0 =∑ ∆ G 0 ( Productos )−∑ ∆ G 0 ( Reactantes )
Kcal Kcal
∆ G0 =3(−56.7) [ ] mol
−(−384.53 )
mol [ ]
Kcal
∆ G 0 =214.43 [ ]
mol
KJ
∆ G0 =897.175 [ ] mol
Se calcula el potencial estándar, de acuerdo con la siguiente formula:
0 −a∙ ∆G0
E=
nF
Remplazando cada uno de los valores:
KJ
E0 =
−897.175
mol [ ]
C
6 ∙96485
mol [ ]
J
E0 =1.550 [ ]
C
Para el cálculo del potencial estándar en equilibrio, se utiliza la siguiente formula:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
a
RT [A] 2.3 RTm
Eth =E + 0
nF
ln
[ B] ( )
b
−
nF
pH
Remplazando cada uno de los valores:
KJ KJ
J
2.4789
mol [ ][ Al2 O3 ] −
2.868468
mol [ ]
Eth =1.550
C
+[ ]
6 ∙ 96.485
KC
ln
[ ]
([ Al ] )6 ∙ 96485
pH
mol
Ya que la concentración de [ Al2 O 3 ] y de [ Al ] son 1 y el ln de ese numero es cero, esa
parte de la ecuación se elimina, quedando lo siguiente:
Eth =−1.550−0.0591 ∙ pH
Ecuación 3
Al2 O3+ 6 H +¿=¿¿ 2 Al 3+¿+3 H O ¿
2
+¿¿ −¿¿
La reacción química involucra H y no e , por lo que en el grafico será una línea
vertical.
Primero, se calcula la energía libre de Gibbs:
∆ G 0 =∑ ∆ G 0 ( Productos )−∑ ∆ G 0 ( Reactantes )
Kcal Kcal Kcal
∆ G 0 =2(−115) [ ] mol
+3 (−56.7 )[ ]
mol
−(−384.53)
mol [ ]
Kcal
∆ G0 =−15.57 [ ] mol
KJ
∆ G 0 =−65.1149 [ ]mol
Se procede a realizar la fórmula de pH de acuerdo con la siguiente formula:
log ( k )=log ¿ ¿
log ( k )=log ¿ ¿
Ya que la concentración de [ H 2 O ] y del [ Al2 O 3 ] es 1, se puede eliminar de la ecuación:
−∆ G 0
=log ¿ ¿
2.303 RT
Remplazando la energía libre de Gibbs:
log ¿ ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Realizando el arreglo del exponente del elemento:
2 log ( [ Al2 O3 ] )=0.0114 −6 pH
log ( [ Al 2 O 3 ] ) =5.70−3 pH
Remplazando el valor de la concentración de [ Al2 O 3 ], se puede obtener el pH
pH=2.23
Ecuación 4
+¿¿ −¿¿
La reacción química involucra H y no e , por lo que en el grafico será una línea
vertical.
+¿=Al 2 O3 + H 2 O ¿
H
2 AlO−¿+2
2
¿
Se calcula la energía libre de Gibbs que posee esta ecuación:
∆ G 0 =∑ ∆ G 0 ( Productos )−∑ ∆ G 0 ( Reactantes )
Kcal Kcal Kcal
∆ G0 =−384.53 [ ] mol
+(−56.7)[ ]
mol
−2 (−200.71 )
mol [ ]
Kcal
∆ G 0 =−39.81 [ ]mol
KJ
∆ G0 =−166.565 [ ] mol
Se procede a realizar la fórmula de pH de acuerdo con la siguiente formula:
log ( k )=log ¿ ¿
log ( k )=log ¿ ¿
−∆ G 0
=log ¿ ¿
2.303 RT
Ya que la concentración de [ H 2 O ] y del [ Al2 O3 ] es 1, se puede eliminar de la ecuación,
como también pudiendo remplazar el ∆ G 0 :
log ¿ ¿
Realizando los acomodos necesarios, se obtiene:
−log ¿ ¿
log ¿ ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Remplazando el valor de la concentración de ¿, se puede obtener el pH
pH=13.6
Ecuación 5
−¿¿ +¿¿
La reacción química involucra e y no H , por lo que en el grafico será una línea
Horizontal.
−¿= Al¿
Al3 +¿+3 e ¿
Se realiza el cálculo de la energía libre de Gibbs de la ecuación:
∆ G 0 =∑ ∆ G 0 ( Productos )−∑ ∆ G 0 ( Reactantes )
Kcal
∆ G0 =−(−115 ) [ ] mol
Kcal
∆ G 0 =115 [ ] mol
KJ
∆ G0 =481.16 [ ] mol
Para plantear el potencial estándar de equilibrio en este caso, se tiene la siguiente
formula:
−∆ G 0 2.3 RT
Eth = + ∙ log¿ ¿
nF nF
Remplazando los valores de cada elemento de la ecuación:
KJ KJ
Eth =
−481.16
mol
+
5708 [ ]
mol
∙ log¿ ¿
[ ]
C KC
3 ∙ 96485
mol
3 ∙96.485[ ]
mol [ ]
Eth =1.663+ 0.0197∙ log ¿
Ecuación 6
−¿=Al +2H O ¿
2
+¿+ 3e
H ¿
AlO−¿+4 ¿
2
+¿¿ −¿¿
La reacción química involucra H ye , por lo que en el grafico será una diagonal.
Se calcula la energía libre de Gibbs con la diferencia entre las energías de los productos y
los reactantes:
∆ G 0 =∑ ∆ G 0 ( Productos )−∑ ∆ G 0 ( Reactantes )
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Kcal Kcal
∆ G 0 =2(−56.7) [ ] mol
−(−200.71 )
mol [ ]
Kcal
∆ G0 =87.31 [ ]mol
KJ
∆ G 0 =365.305 [ ] mol
Se calcula el potencial estándar, de acuerdo con la siguiente formula:
0 −a∙ ∆G0
E=
nF
Remplazando los valores:
KJ
E0 =
−365.305
mol [ ]
C
3∙ 96485
mol[ ]
J
E0 =−1.262 [ ]
C
Para el cálculo del potencial estándar en equilibrio, se utiliza la siguiente formula:
a
RT [A] 2.3 RTm
Eth =E +0
nF
ln
[ B] b ( )
−
nF
pH
Remplazando cada uno de los valores, se obtiene lo siguiente:
KJ
J mol
2.4789 [ ]
Eth =−1.262
C
+ [ ] KC
ln ¿ ¿
3 ∙96.485
mol [ ]
Eth =−1.262+0.0197 ∙ log ¿
Para graficar el diagram de Pourbaix del aluminio se utilizarán las siguientes ecuaciones
encontradas anteriormente:
3+ ¿→ pH =5.07 ¿
1. AlO2−¿/ Al ¿
2. Al2 O 3 / Al → Eth =−1.55−0.06∗pH
3. Al2 O 3 / Al 3+¿ ¿
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
pH=1.9 con log ¿
pH=2.6 con log¿
pH=3.2 con log ¿
pH=3.9 con log ¿
−¿/ Al 2 O3 ¿
4. Al O 2
pH=14.60 con log ¿
pH=12.60 con log ¿
pH=10.60 con log ¿
pH=8.60 con log ¿
5. Al3 +¿/ Al ¿
E=−1.66 con log ¿
E=−1.70 con log ¿
E=−1.74 con log ¿
E=−1.78 con log ¿
−¿/ Al ¿
6. AlO2
E=−1.26−0.08∗pH con log ¿
E=−1.30−0.08∗pH con log ¿
E=−1.34−0.08∗pH con log ¿
E=−1.38−0.08∗pH con log ¿
7. Limite superior del agua
E=1.23−0.06∗pH
8. Limite inferior del agua E=−0.06∗pH
Luego, el eje X corresponde al pH y el eje Y será el potencia E.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Figura 5 Ecuaciones para el Aluminio
Como las ecuaciones se obtuvieron de reacciones de reducción, el reactante va sobre las
curvas hozirontales/inclinadas mientras que para las curvas verticales, se encuentra a la
derecha.
Para visualizar de mejor manera el diagrama se limitó el rango del potencial desde -2.6
hasta 1.4 [V] ya que se presentan todas las especies posibles.
Para ordenar el diagrama, se eliminarán las curvas que no sean comunes en la zona
como se observa en el siguiente ejemplo:
Figura 6 Ejemplo eliminación de curvas 1 para el Al3+
En la zona se observa que se presenta el mismo elemento Al 3+ (elemento que es común
en la zona) por lo tanto las curvas resultantes en el medio serán eliminadas.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Quedando la zona de la siguiente manera:
Figura 7 Curvas eliminadas para Al3+
Dentro del Diagrama se observa otra zona con presencia de Al con múltiples curvas como
se observa a continuación:
Figura 8 Eliminación de rectas verticales en el Al
En este caso, el Al se encuentro delimitado por rectas verticales que serán eliminadas de
igual forma:
Figura 9 Rectas eliminadas para Al
Finalmente, el diagrama de Pourbaix del Aluminio se presenta en la siguiente figura:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Figura 10 Diagrama de Pourbaix del Aluminio
Dentro del diagrama existen 3 zonas de estabilidad para el aluminio:
Imunidad en la zona Al, comprende la forma elemental del metal y no se produce
corrosión ya que el elemento no se puede reducir.
-
Corrosión en la zona Al3+ y AlO2, bajo esas condiciones (fase termodinámica)
estos iones son estables y cada uno atrae átomos de oxígeno para entrar en la
etapa de pasividad lo que provoca la corrosión. En este caso se observa que el
metal es sensible al pH tanto para ambientes ácidos y básicos (extremos).
Pasividad en la zona del Al2 O 3, se forman precipitados sólidos sobre el metal
como una capa estable libre de porosidad que lo protege en la superficie. En esta
zona se originan compuestos sólidos insolubles y dificultan la disolución posterior.
Las ecuaciones del agua que se representan por las dos líneas punteadas en el
diagrama, indican los limites de oxidación y reducción del agua o disolvente que se esté
utilizando. Las reacciones que se produzcan en el aluminio sobre este límite (recta
punteada azul) serán en condiciones oxidantes produciendo una capa de oxígeno sobre el
metal. El límite el diagrama corresponde a un potencial 1.2 [V].
En el limite inferior ocurre la reducción del agua, produciendo hidrógeno molecular sobre
el metal lo que se traduce en una severa corrosión, siendo éste el caso más probable
para el aluminio.
La zona entre ambas rectas delimitantes no se produce oxidación ni reducción del agua.
Finalmente, las regiones se pueden mejor en el siguente diagrama:
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Figura 11 Zonas en el Diagrama de Pourbaix del Aluminio
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
De acuerdo a los gráficos construidos y a la información proporcionada
anteriormente, responda: ¿Qué condiciones debe cumplir una especie para que
pueda ser tratada a través de procesos hidrometalúrgicos?
El metal de interés debe ser soluble en el disolvente o agente oxidante que se utilizará
para minimizar precipitaciones y posible pasivación (caso de los sulfuros). Además, las
reacciones deben ser termodinámicamente posibles y desde la cinética de la reacción
ésta debe producirse en tiempos prácticos.
El agua disuelve muchas especies, pero sólo oxidadas para el caso de los sulfuros se
adicionan sustancias para ser afines al proceso.
¿Qué sucede con aquellas especies iónicas de un metal ( 𝑀+ o 𝑀2+ ) cuya
estabilidad termodinámica se encuentra por sobre la del agua? ¿Es posible obtener
por medios hidrometalúrgicos las especies metálicas sólidas (𝑀0 (𝑠) o 𝑀(𝑠))?
Las especies metálicas al hidratarse pierden H+ quedando de la forma M + o M2+, bajando
el pH de la solución por lo que su disolución se realizará en en ambientes ácidos. Sin
embargo para que esto se produzca su estabilidad termodinámica debe encontrarse entre
los límites del agua, de lo contrario comienzan las reacciones de reducción/oxidación del
agua. En el caso de encontrarse sobre el límite superior provocará la oxidación del agua a
oxígeno por lo que no se disolverá, así mismo, si se encontrase bajo el límite inferior
serían especies inestables en soluciones acuosas reduciendo el agua a hidrógeno
gaseoso.
Es posible obtener por medios hidrometalúrgicos las especies metálicas sólidas
elementales independiente que termodinámicamente son resistentes a formar
compuestos como las demás especies (como el caso del oro). Mediante el proceso de
molienda las partículas son separadas y recuperadas mediante procesos de separación
gravitacional, principalmente. Luego, se hidratan con compuestos afines para la formación
de complejos y seguir el proceso similar a las demás especies.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Conclusión
Mediante el diagrama de Pourbaix de un sistema Metal-Agua resume las reacciones que
son teóricamente posibles y representa las especies con concentraciones mayor al 50%,
sin embargo la cinética de las reacciones determinan que es lo prácticamente posible. En
el caso del Oro la especie Au2O3 es descartada del diagrama por tener una concentración
menor a la expuesta.
Para el Aluminio se observó un fácil tratamiento desde el punto de vista de la
hidrometalurgia ya que su zona de disolución tiene un rango de potencial más amplio que
el agua, en cuanto al ambiente de la solución debe ser ácido. La zona de corrosión
comienza a manifestarse en el límite inferior del agua (potencial cercano a 0) y es el lugar
donde es más probable que produzcan las reacciones.
En el caso del oro, la zona de corrosión es bastante estrecha tanto de potencial como de
pH, se encuentra a valores de potencial muy altos, por el contrario, la zona de pasividad
es bastante ancha, la cual impide que el metal se disuelva. La corrosión ocurre sobre el
límite superior de agua donde ésta se oxida y pasa a reducir cada de las formas oxidadas
de oro a oro metálico, es decir, si no se adicionan químicos correctos el oro no será
oxidado por el oxígeno disuelto en agua, por lo tanto necesitará de un agente oxidante
potente para que se produzca la disolución.
Por lo tanto, el oro es un elemento mucho más difícil de tratar en la hidrometalurgia ya
que indica una falta de reactividad, solo reacciona a potenciales altos en donde el agua
esté oxidada.
Debido a lo anterior, las reacciones que incluyen el oro Au 0 (reacciones que forman Au+ y
Au3+) no existen en la práctica en la solución acuosa planteada. Sin embargo, mediante el
cianuro es posible procesar la especie por métodos hidrometalúrgicos. Al igual que los
demás metales nobles mediante agentes oxidantes potentes.
El caso del cobre resulta interesante pues hay una extensa zona de disolución al variar el
pH (desde 0 a 16) lo cual se entiende por las variadas formas que se presenta en la
naturaleza las que irán lixiviando en diferentes condiciones de pH y potencial. Además,
una estrecha zona de pasividad
Finalmente, el Aluminio, Cobre y Oro representan 3 posibles formas de sistemas
termodinámicos. Siendo el más complejo de estudiar el oro por ser un metal con una
estabilidad superior a la del agua dificultando la disolución. En cuanto a las otras dos
especies, el aluminio se encuentra dentro del límites del agua con un pH muy ácido o
básico (encontrándose en los extremos de pH) siendo de fácil tratamiento al igual que el
cobre.
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Martes, 19 de mayo de 2020
Universidad de Santiago de Chile
Facultad de Ingeniería
Departamento de Ingeniería en Minas
Laboratorio de Procesos Metalúrgicos
Bibliografía
Domic Mihovilovic, E. M. (2001). Hidrometalurgia: fundamentos, procesos y
aplicaciones. Recuperado desde: https://es.scribd.com/doc/300542083/m-LIBRO-
Hidrometalurgia-Fundamentos-Procesos-y-Aplicaciones-Esteban-Domic
Martes, 19 de mayo de 2020
S-ar putea să vă placă și
- Diagrama de PourbaixDocument46 paginiDiagrama de PourbaixIgnacio Esteban100% (1)
- Diagramas de PourbaixDocument11 paginiDiagramas de PourbaixDavid AguilarÎncă nu există evaluări
- Construcción de Diagramas de Pourbaix 1Document14 paginiConstrucción de Diagramas de Pourbaix 1Victor LaosÎncă nu există evaluări
- EllinghamDocument7 paginiEllinghamTeresa MataÎncă nu există evaluări
- Diagramas de PourbaixDocument7 paginiDiagramas de PourbaixLizbeth Nallely Jimenez MartinezÎncă nu există evaluări
- Cinética de Lixiviacion-2019Document15 paginiCinética de Lixiviacion-2019Marcos Orlando Calla CondoriÎncă nu există evaluări
- Separata Nâ 06 Diagrama EllinghamDocument16 paginiSeparata Nâ 06 Diagrama EllinghamRenatoAlonsoAbarcaAranaÎncă nu există evaluări
- Diagramas de PourbaixDocument19 paginiDiagramas de PourbaixCAROLINA RUIZ DAZAÎncă nu există evaluări
- Laboratorio 8 Flotacion MarmatitaDocument13 paginiLaboratorio 8 Flotacion MarmatitaJona Luis AmézagaÎncă nu există evaluări
- Fusión CuDocument32 paginiFusión CuamilcarÎncă nu există evaluări
- Fundamentos de La CorrosionDocument55 paginiFundamentos de La Corrosioncristian omanaÎncă nu există evaluări
- Diagrama de PourbaixDocument13 paginiDiagrama de PourbaixJhanÎncă nu există evaluări
- Diagramas de Pourbaix - Documento FinalDocument14 paginiDiagramas de Pourbaix - Documento FinalAndresÎncă nu există evaluări
- Cap 4 Cianuracion de Au-AgDocument27 paginiCap 4 Cianuracion de Au-AgDavid Jose Martinez BarronÎncă nu există evaluări
- Leyes de Oxidacion de MetalesDocument9 paginiLeyes de Oxidacion de MetalesJeyson GrandaÎncă nu există evaluări
- Guia de Ejercicios PDFDocument72 paginiGuia de Ejercicios PDFYanina FerreiraÎncă nu există evaluări
- Diagramas Eh - PHDocument20 paginiDiagramas Eh - PHrogerlucano4646Încă nu există evaluări
- Diagrama Poubaix Ag A 298KDocument14 paginiDiagrama Poubaix Ag A 298KLS Emanuel DiegoÎncă nu există evaluări
- Tostación de CalcopiritaDocument20 paginiTostación de CalcopiritaJohn Reyes100% (2)
- Laboratorio Nº5Document18 paginiLaboratorio Nº5lopezfloreslaÎncă nu există evaluări
- 1 Tecsup Termodinamica de La Cianuracion 777777Document36 pagini1 Tecsup Termodinamica de La Cianuracion 777777Gianfranco Ampuero VillavicencioÎncă nu există evaluări
- Diagrama Eh - PHDocument11 paginiDiagrama Eh - PHYvan Cesar Guzman JacoboÎncă nu există evaluări
- Manual de Practicas Electrometalurgía2019-1Document22 paginiManual de Practicas Electrometalurgía2019-1Eder RysÎncă nu există evaluări
- Tema 10 Diagrama de EllinghamDocument23 paginiTema 10 Diagrama de EllinghamLourdes100% (1)
- Curvas de PolarizacionDocument8 paginiCurvas de PolarizacionRichard Gonzalo YtoÎncă nu există evaluări
- Diagrama de PourbaixDocument4 paginiDiagrama de PourbaixFelipe EstañaÎncă nu există evaluări
- Diagramas de EllinghamDocument4 paginiDiagramas de EllinghamDarilJohannesDeLaCruzCalderonÎncă nu există evaluări
- Ejercicios PrácticosDocument5 paginiEjercicios PrácticosRobinsonÎncă nu există evaluări
- Limpieza Hombre MuertoDocument21 paginiLimpieza Hombre MuertochristianÎncă nu există evaluări
- 3.0. Diagrama PourbaixDocument40 pagini3.0. Diagrama PourbaixJair Jhosue Zavala Rojas100% (1)
- Laboratorio de Lixivicion DinamicaDocument21 paginiLaboratorio de Lixivicion DinamicaAlguienÎncă nu există evaluări
- Química de La Fundición Del OroDocument2 paginiQuímica de La Fundición Del OroLuis Angel Palomino100% (1)
- Clase 16-Refinación A FuegoDocument13 paginiClase 16-Refinación A FuegoJosé Daniel Canales Pallarés100% (3)
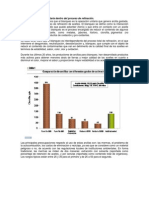
- Fundamentos Termodinamicos de La Fusion A MataDocument27 paginiFundamentos Termodinamicos de La Fusion A MataJoaquin LagosÎncă nu există evaluări
- Proceso de Cementación o PrecipitaciónDocument14 paginiProceso de Cementación o PrecipitaciónManuel HTÎncă nu există evaluări
- Obtención de Plomo Metálico A Partir de Concentrados Sulfurosos Mediante El Proceso de Lixiviación ElectrolíticaDocument11 paginiObtención de Plomo Metálico A Partir de Concentrados Sulfurosos Mediante El Proceso de Lixiviación ElectrolíticaCM AntoniÎncă nu există evaluări
- Tostación de SulfurosDocument16 paginiTostación de SulfurosBRENDA EMELYC FLORES MUÑOZÎncă nu există evaluări
- Guias de Laboratorio de PirometalurgiaDocument49 paginiGuias de Laboratorio de PirometalurgiaLuis C. Chambi V.Încă nu există evaluări
- Laboratorio 3 PrirometalurgiaDocument13 paginiLaboratorio 3 PrirometalurgiaeduardoÎncă nu există evaluări
- Auxiliar No 6Document6 paginiAuxiliar No 6Cristian AlvayaiÎncă nu există evaluări
- Informe Final ArenasDocument13 paginiInforme Final ArenasrosarioÎncă nu există evaluări
- Lab 2 PirometalurgiaDocument13 paginiLab 2 PirometalurgiaeduardoÎncă nu există evaluări
- Concentración MagnéticaDocument8 paginiConcentración MagnéticaDanny joaquin100% (1)
- Examen Resuelto de Pirometalurgia 2016Document4 paginiExamen Resuelto de Pirometalurgia 2016Luis C. Chambi V.Încă nu există evaluări
- Interpretación de Los Diagramas de Ellingham en Los Monóxidos 1Document13 paginiInterpretación de Los Diagramas de Ellingham en Los Monóxidos 1BryanHinojosaAnchaya100% (3)
- Termodinamica en La LixiviaciónDocument38 paginiTermodinamica en La LixiviaciónFelipe Riquelme OlavarriaÎncă nu există evaluări
- Cinetica ElectroquimicaDocument66 paginiCinetica ElectroquimicaIsaac Israel Talavera BlandonÎncă nu există evaluări
- Pirometalurgia Aspectos AmbientalesDocument17 paginiPirometalurgia Aspectos AmbientalesFernando Nicolas Ureta GodoyÎncă nu există evaluări
- Diagrama de PourbaixDocument2 paginiDiagrama de PourbaixUbaldo Fragoso PalafoxÎncă nu există evaluări
- Electrodeposicion Del OroDocument6 paginiElectrodeposicion Del OroElvis BoNiÎncă nu există evaluări
- Diagrama de PourbaixDocument1 paginăDiagrama de PourbaixLuis RomeroÎncă nu există evaluări
- DIAGRAMA DE POURBAIX DEL H2O CuDocument9 paginiDIAGRAMA DE POURBAIX DEL H2O CuJhuan Uchasara SihuayroÎncă nu există evaluări
- Diagramas de PourbaixDocument5 paginiDiagramas de PourbaixDaniel Alonso Luna MermaÎncă nu există evaluări
- Manual Ejercicios Quimica Analitica InstrumentalDocument63 paginiManual Ejercicios Quimica Analitica InstrumentalAADIL BAJOUBÎncă nu există evaluări
- Guia 3 Reacciones y EcuacionesDocument15 paginiGuia 3 Reacciones y Ecuacionesdavid santiago baez barretoÎncă nu există evaluări
- Sep 11 BalanceDocument12 paginiSep 11 Balanceluis de la cruzÎncă nu există evaluări
- REPORTE PRACTICA No 5Document6 paginiREPORTE PRACTICA No 5won choiÎncă nu există evaluări
- Balanceo de ReaccionesDocument16 paginiBalanceo de ReaccionesJohan Gregorio BautistaÎncă nu există evaluări
- Practica 4Document6 paginiPractica 4willhurtado1205Încă nu există evaluări
- Caracterización química, morfológica y estructural de materialesDe la EverandCaracterización química, morfológica y estructural de materialesÎncă nu există evaluări
- FULLTEXT03 en EsDocument96 paginiFULLTEXT03 en EsMaria JoseÎncă nu există evaluări
- Clase 4Document40 paginiClase 4Maria JoseÎncă nu există evaluări
- FULLTEXT09 (001-070) en EsDocument70 paginiFULLTEXT09 (001-070) en EsMaria JoseÎncă nu există evaluări
- Resumen Del Libro Del Nuevo Conductor Clase BDocument33 paginiResumen Del Libro Del Nuevo Conductor Clase BMaria Jose100% (1)
- Clase 5Document27 paginiClase 5Maria JoseÎncă nu există evaluări
- Papeo Mejorado Pep 2 Evalpro2.0Document57 paginiPapeo Mejorado Pep 2 Evalpro2.0Maria JoseÎncă nu există evaluări
- Desarrollo y Evaluación de Algoritmos de Optimización Que Permitan Definir Envolventes Económicas para Métodos de Hundimiento MasivoDocument112 paginiDesarrollo y Evaluación de Algoritmos de Optimización Que Permitan Definir Envolventes Económicas para Métodos de Hundimiento MasivoMaria JoseÎncă nu există evaluări
- Carguio y PapeoDocument33 paginiCarguio y PapeoMaria JoseÎncă nu există evaluări
- Ayudantía 10 - Extracción VerticalDocument38 paginiAyudantía 10 - Extracción VerticalMaria JoseÎncă nu există evaluări
- Control de TirajeDocument1 paginăControl de TirajeMaria JoseÎncă nu există evaluări
- Ayudant A N 7 - Panel CavingDocument25 paginiAyudant A N 7 - Panel CavingMaria JoseÎncă nu există evaluări
- Resources, Conservation Y Recycling ESPAÑOLDocument9 paginiResources, Conservation Y Recycling ESPAÑOLMaria JoseÎncă nu există evaluări
- TorresAndrewESM T3Document12 paginiTorresAndrewESM T3ANTONIO ROLDAN MENDOZAÎncă nu există evaluări
- Cuadro Comparativo Resumen Ensayo ComentarioDocument3 paginiCuadro Comparativo Resumen Ensayo ComentarioCesarSalamanca100% (1)
- Cuadro de Estadisticas SST - TCC - 5 AñosDocument17 paginiCuadro de Estadisticas SST - TCC - 5 AñosCesar Harrison Prado AyquipaÎncă nu există evaluări
- Especificaciones Tecnicas DrywallDocument16 paginiEspecificaciones Tecnicas DrywallNilocasas83% (35)
- György LukácsDocument15 paginiGyörgy LukácsValeria MontañoÎncă nu există evaluări
- La Cultura Desde El Paradigma Del Conflicto SocialDocument3 paginiLa Cultura Desde El Paradigma Del Conflicto SocialYorca Vargas LopezÎncă nu există evaluări
- Gthy Gestion PDFDocument5 paginiGthy Gestion PDFAlbert MateoÎncă nu există evaluări
- Catálogo Gyol 2013Document22 paginiCatálogo Gyol 2013Greg Anthony ReaÎncă nu există evaluări
- Transformación de Laguna Anaerobia en Biodigestor PDFDocument13 paginiTransformación de Laguna Anaerobia en Biodigestor PDFAngelly Perez FernandezÎncă nu există evaluări
- Argumentacion JuridicaDocument2 paginiArgumentacion JuridicaPaulaA.DiazÎncă nu există evaluări
- Educacion Sexual para NinosDocument48 paginiEducacion Sexual para NinosHilda MartínezÎncă nu există evaluări
- Costos 7.21 - 7.27Document5 paginiCostos 7.21 - 7.27ÁNGELO MOISÉS OBREGÓN GUILLERMOÎncă nu există evaluări
- Check List MaquinasDocument4 paginiCheck List MaquinasFERNANDAÎncă nu există evaluări
- 20.fin de Los Tiempos y Apariciones MarianasDocument4 pagini20.fin de Los Tiempos y Apariciones MarianasLuz Katerine Maya MÎncă nu există evaluări
- Ensayo Estudios CulturalesDocument6 paginiEnsayo Estudios CulturalesMagdalenaFuenzalidaRey0% (1)
- Locomoción AnimalDocument1 paginăLocomoción AnimalJDCLÎncă nu există evaluări
- Tarea 2 - Cristian - de - Jesus - Mercado - Gomez - 205Document12 paginiTarea 2 - Cristian - de - Jesus - Mercado - Gomez - 205Christiam J. MerkdoÎncă nu există evaluări
- Trabajo Final - Carolina HerreraDocument40 paginiTrabajo Final - Carolina HerreratomascrespolobilloÎncă nu există evaluări
- BhvyvyDocument8 paginiBhvyvyyulaiÎncă nu există evaluări
- 01 Grupos de DiscusiónDocument16 pagini01 Grupos de DiscusiónJr Valencia100% (1)
- Tarea 4 EntregaDocument34 paginiTarea 4 EntregaManzanog IngrisÎncă nu există evaluări
- Plan de Trabajo Inmunizaciones Huayllasp 2022Document7 paginiPlan de Trabajo Inmunizaciones Huayllasp 2022P.S Huayllaspanca67% (6)
- 2º Practica PecuariaDocument9 pagini2º Practica PecuariaHeber Quispe HuyhuaÎncă nu există evaluări
- BIOMICROSDocument15 paginiBIOMICROSJhoanna Acuña Botiquin100% (1)
- E973 Turbina de Vapor - Ignacio MoralesDocument28 paginiE973 Turbina de Vapor - Ignacio MoralesDiego Nicolas Figueroa QuirozÎncă nu există evaluări
- Teoria 10-Fenómenos Térmicos y TermodinámicaDocument23 paginiTeoria 10-Fenómenos Térmicos y Termodinámicaxa asadÎncă nu există evaluări
- 16 Nuevas Tecnologias en Puertos ProsertekDocument21 pagini16 Nuevas Tecnologias en Puertos ProsertekAbd El Latif ALFAYEDÎncă nu există evaluări
- Parcial Micro Op2Document3 paginiParcial Micro Op2JHON EDWIN SOTO COLORADOÎncă nu există evaluări
- BLANQUEODocument3 paginiBLANQUEOjotachuquiÎncă nu există evaluări
- Guía 4 Español SéptimoDocument2 paginiGuía 4 Español Séptimoalexnei12Încă nu există evaluări